Презентация_Лекция_12_Мышцы.ppt
- Количество слайдов: 20

Лекция 12 Биохимия мышечной ткани

Лекция 12 Биохимия мышечной ткани

Лекция 12 Биохимия мышечной ткани Мышцы составляют у взрослого человека 40 % от массы тела. • Функция мышц: напряжение и укорочение с последующим расслаблением. • Значение мышц: обеспечение подвижности организма и сопротивление механической силе, в том числе и статические нагрузки. • Механизм работы мышц: превращение химической энергии в механическую.

Лекция 12 Биохимия мышечной ткани К мышечным тканям относятся: • скелетная мускулатура • сердечная мышца • гладкая мускулатура Скелетная и сердечная мышцы – это поперечно-полосатые мышцы. Мышечные клетки состоят из миофибрилл. Функциональной единицей миофибрилл является саркомер.
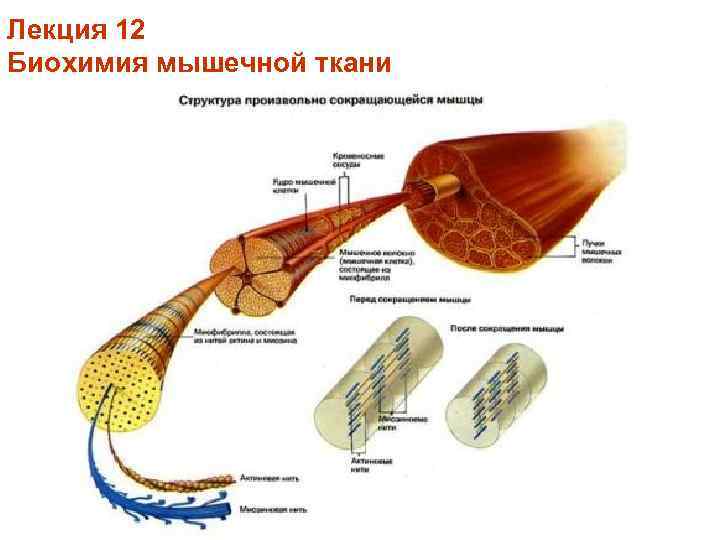
Лекция 12 Биохимия мышечной ткани
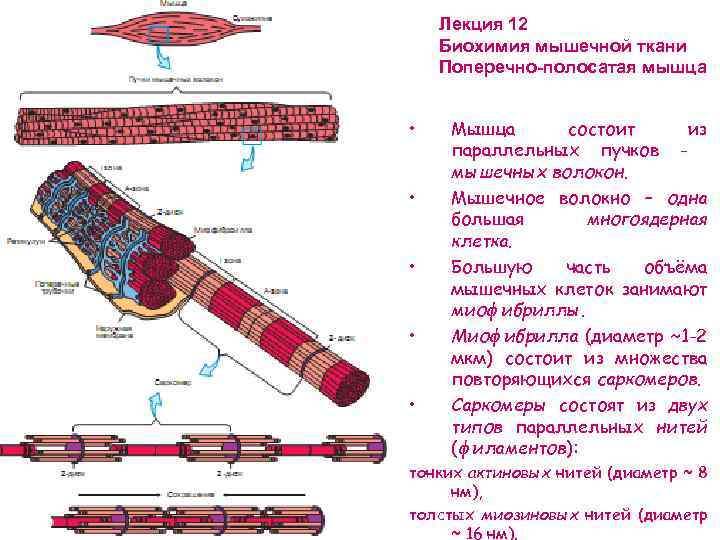
Лекция 12 Биохимия мышечной ткани Поперечно-полосатая мышца • • • Мышца состоит из параллельных пучков мышечных волокон. Мышечное волокно – одна большая многоядерная клетка. Большую часть объёма мышечных клеток занимают миофибриллы. Миофибрилла (диаметр ~1 -2 мкм) состоит из множества повторяющихся саркомеров. Саркомеры состоят из двух типов параллельных нитей (филаментов): тонких актиновых нитей (диаметр ~ 8 нм), толстых миозиновых нитей (диаметр ~ 16 нм).

Лекция 12 Биохимия мышечной ткани Структура поперечно-полосатых мышц Электронная фотография продольного участка мышечного волокна.
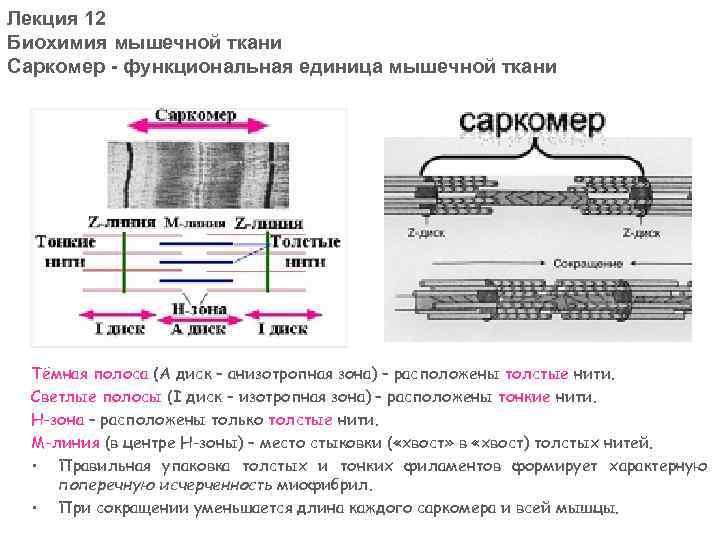
Лекция 12 Биохимия мышечной ткани Саркомер - функциональная единица мышечной ткани Тёмная полоса (А диск – анизотропная зона) – расположены толстые нити. Светлые полосы (I диск – изотропная зона) – расположены тонкие нити. Н-зона – расположены только толстые нити. М-линия (в центре Н-зоны) – место стыковки ( «хвост» в «хвост) толстых нитей. • Правильная упаковка толстых и тонких филаментов формирует характерную поперечную исчерченность миофибрил. • При сокращении уменьшается длина каждого саркомера и всей мышцы.
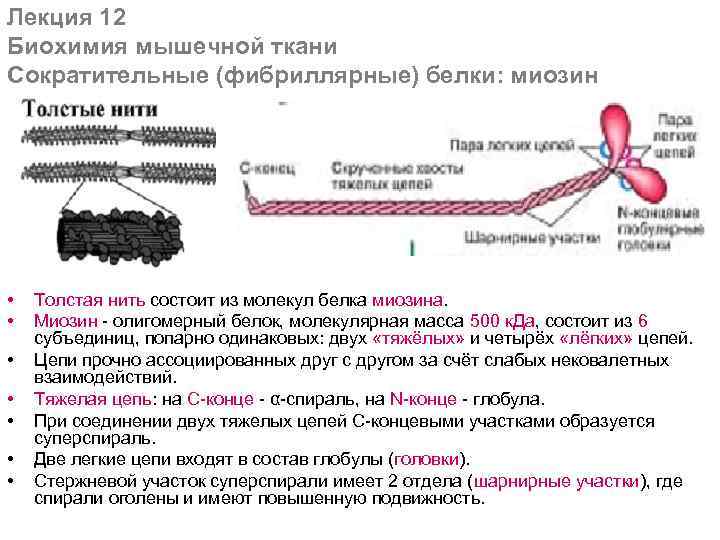
Лекция 12 Биохимия мышечной ткани Сократительные (фибриллярные) белки: миозин • • Толстая нить cостоит из молекул белка миозина. Миозин - олигомерный белок, молекулярная масса 500 к. Да, состоит из 6 субъединиц, попарно одинаковых: двух «тяжёлых» и четырёх «лёгких» цепей. Цепи прочно ассоциированных друг с другом за счёт слабых нековалетных взаимодействий. Тяжелая цепь: на С-конце - α-спираль, на N-конце - глобула. При соединении двух тяжелых цепей С-концевыми участками образуется суперспираль. Две легкие цепи входят в состав глобулы (головки). Стержневой участок суперспирали имеет 2 отдела (шарнирные участки), где спирали оголены и имеют повышенную подвижность.
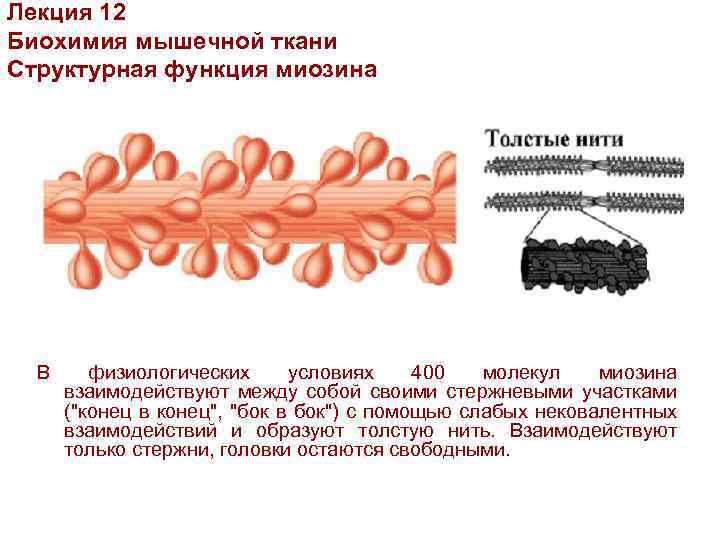
Лекция 12 Биохимия мышечной ткани Структурная функция миозина В физиологических условиях 400 молекул миозина взаимодействуют между собой своими стержневыми участками ("конец в конец", "бок в бок") с помощью слабых нековалентных взаимодействий и образуют толстую нить. Взаимодействуют только стержни, головки остаются свободными.
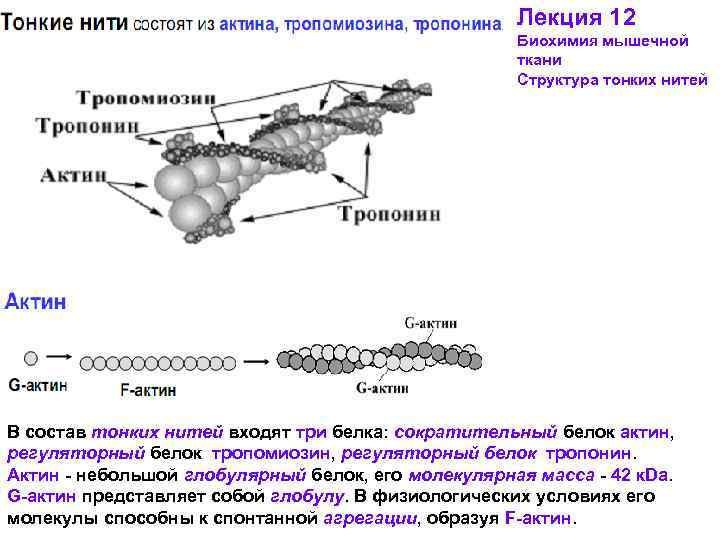
Лекция 12 Биохимия мышечной ткани Структура тонких нитей В состав тонких нитей входят три белка: сократительный белок актин, регуляторный белок тропомиозин, регуляторный белок тропонин. Актин - небольшой глобулярный белок, его молекулярная масса - 42 к. Dа. G-актин представляет собой глобулу. В физиологических условиях его молекулы способны к спонтанной агрегации, образуя F-актин.
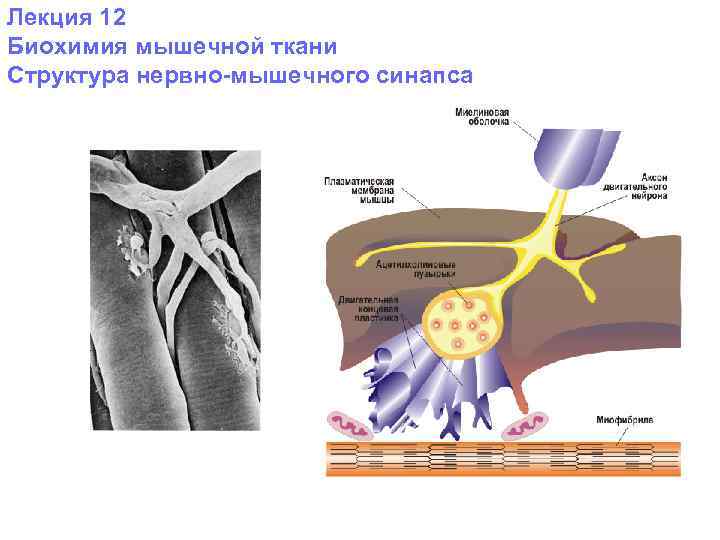
Лекция 12 Биохимия мышечной ткани Структура нервно-мышечного синапса
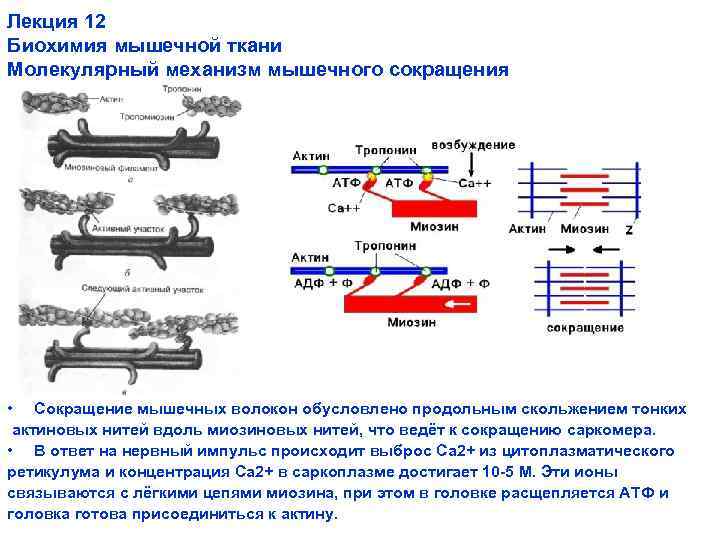
Лекция 12 Биохимия мышечной ткани Молекулярный механизм мышечного сокращения • Сокращение мышечных волокон обусловлено продольным скольжением тонких актиновых нитей вдоль миозиновых нитей, что ведёт к сокращению саркомера. • В ответ на нервный импульс происходит выброс Ca 2+ из цитоплазматического ретикулума и концентрация Ca 2+ в саркоплазме достигает 10 -5 М. Эти ионы связываются с лёгкими цепями миозина, при этом в головке расщепляется АТФ и головка готова присоединиться к актину.
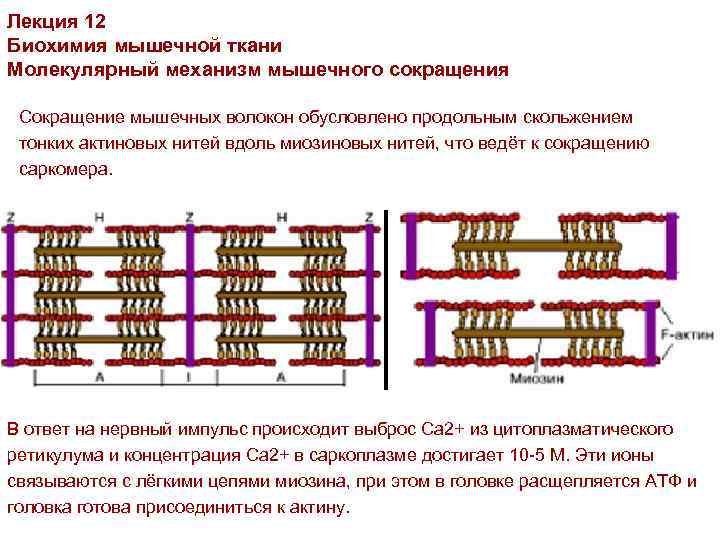
Лекция 12 Биохимия мышечной ткани Молекулярный механизм мышечного сокращения Сокращение мышечных волокон обусловлено продольным скольжением тонких актиновых нитей вдоль миозиновых нитей, что ведёт к сокращению саркомера. В ответ на нервный импульс происходит выброс Ca 2+ из цитоплазматического ретикулума и концентрация Ca 2+ в саркоплазме достигает 10 -5 М. Эти ионы связываются с лёгкими цепями миозина, при этом в головке расщепляется АТФ и головка готова присоединиться к актину.
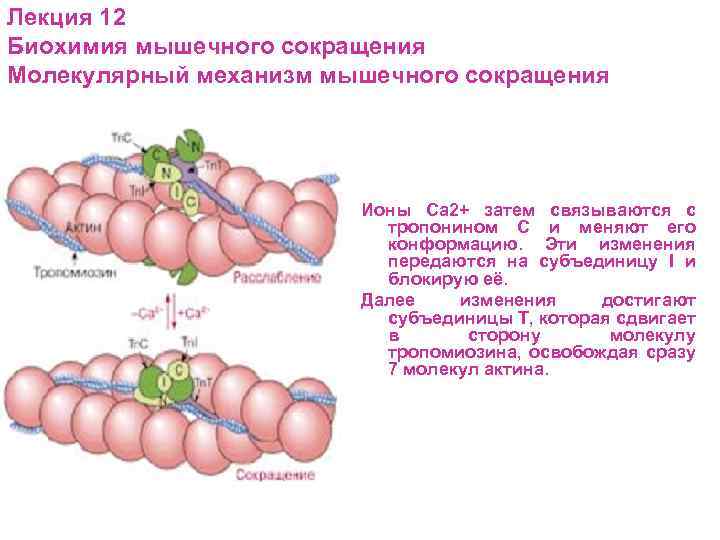
Лекция 12 Биохимия мышечного сокращения Молекулярный механизм мышечного сокращения Ионы Са 2+ затем связываются с тропонином С и меняют его конформацию. Эти изменения передаются на субъединицу I и блокирую её. Далее изменения достигают субъединицы Т, которая сдвигает в сторону молекулу тропомиозина, освобождая сразу 7 молекул актина.
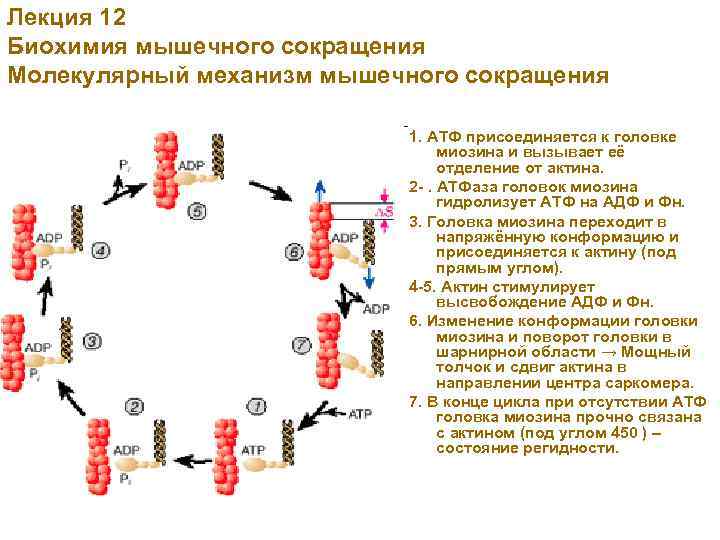
Лекция 12 Биохимия мышечного сокращения Молекулярный механизм мышечного сокращения 1. АТФ присоединяется к головке миозина и вызывает её отделение от актина. 2 -. АТФаза головок миозина гидролизует АТФ на АДФ и Фн. 3. Головка миозина переходит в напряжённую конформацию и присоединяется к актину (под прямым углом). 4 -5. Актин стимулирует высвобождение АДФ и Фн. 6. Изменение конформации головки миозина и поворот головки в шарнирной области → Мощный толчок и сдвиг актина в направлении центра саркомера. 7. В конце цикла при отсутствии АТФ головка миозина прочно связана с актином (под углом 450 ) – состояние регидности.

Лекция 12 Обмен углеводов Гидролиз гликогена
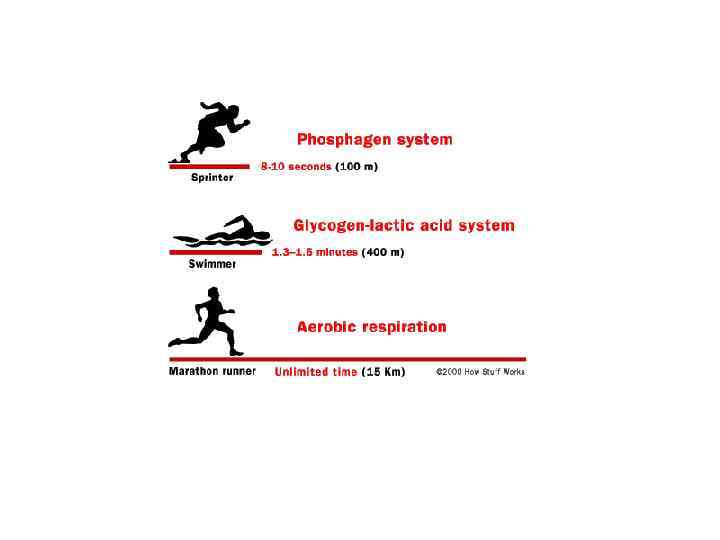
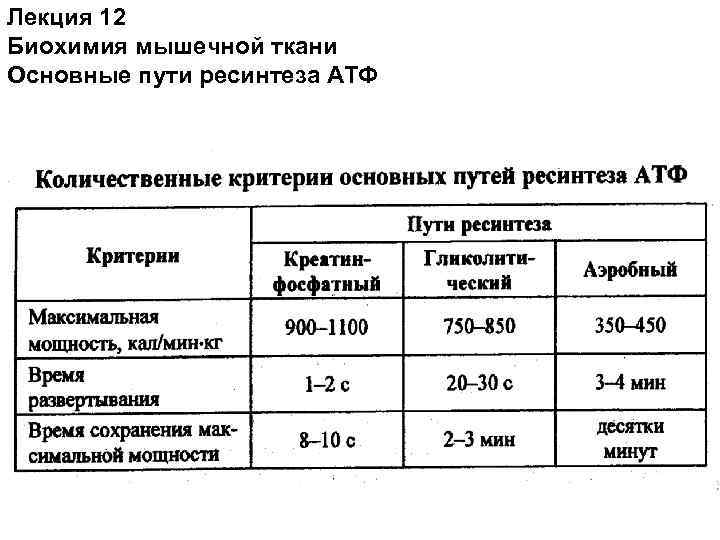
Лекция 12 Биохимия мышечной ткани Основные пути ресинтеза АТФ
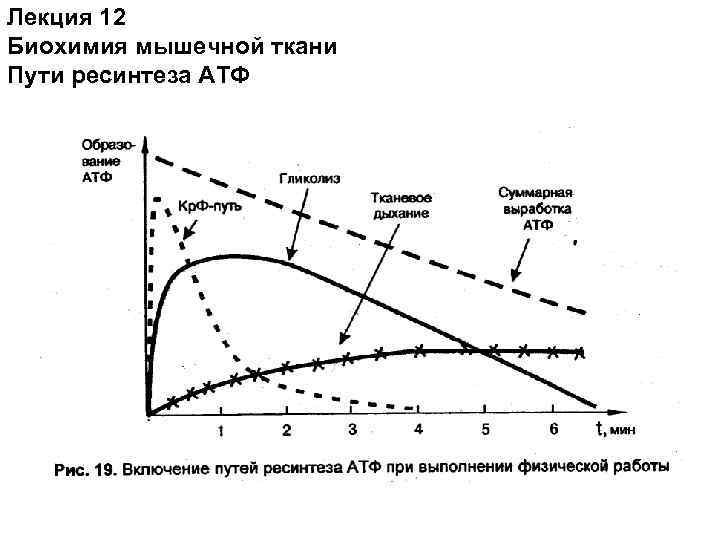
Лекция 12 Биохимия мышечной ткани Пути ресинтеза АТФ
Презентация_Лекция_12_Мышцы.ppt