Л_12-SPA-Термическая обработка кат.ppt
- Количество слайдов: 23

Лекция 12 10. Термическая обработка предшественника катализатора 10. 1. Термическое разложение солей и гидроксидов: закономерности формирования фазового состава и текстуры 10. 1. 1. Формирование фазового состава 10. 1. 2. Формирование текстуры 10. 1. 3. Термохимическая активация гиббсита 10. 2. Спекание пористых тел

Природа процессов, протекающих при термической обработке предшественников катализаторов Термическое разложение компонентов Спекание пористых тел Полиморфные превращения Твердофазные взаимодействия (в многокомпонентных системах) Окислительно-восстановительные и другие химические процессы в присутствии химически активных газов Факторы, затрагивающие интенсивность и глубину этих процессов температура, продолжительность термообработки, состав газовой среды, компонентный состав предшественника, предыстория формирования предшественника
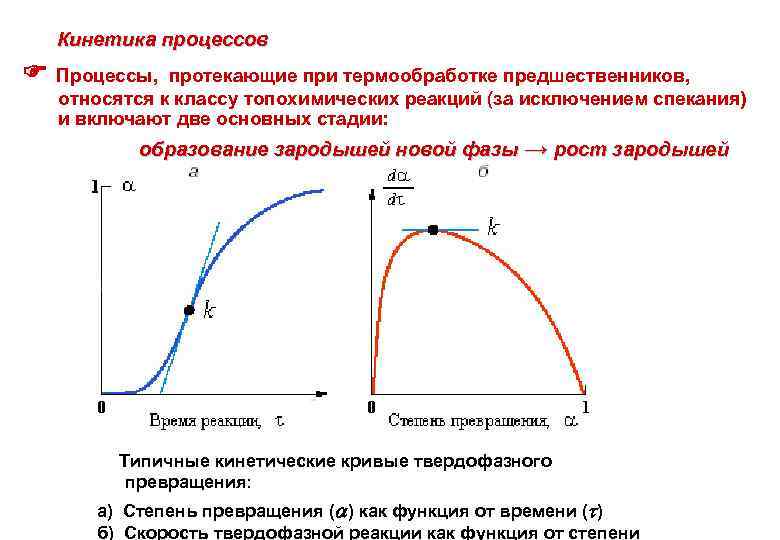
Кинетика процессов Процессы, протекающие при термообработке предшественников, относятся к классу топохимических реакций (за исключением спекания) и включают две основных стадии: образование зародышей новой фазы → рост зародышей Типичные кинетические кривые твердофазного превращения: а) Степень превращения ( ) как функция от времени ( ) б) Скорость твердофазной реакции как функция от степени

10. 1. Термическое разложение солей и гидроксидов: закономерности формирования фазового состава и текстуры Термическое разложение топохимическая реакция, когда одним из продуктов реакции является газообразное вещество Атв. → Втв. + Сгаз Для управления процессом формирования фазового состава катализатора необходимо знать температуру начала и завершения процессов разложения компонентов; количество и физико-химическую природу стадий каждого процесса; характер зависимости этих стадий от природы твердого тела и его взаимодействия с другими компонентами системы; влияние условий осуществления процесса на протекание этих стадий: скорости нагрева,
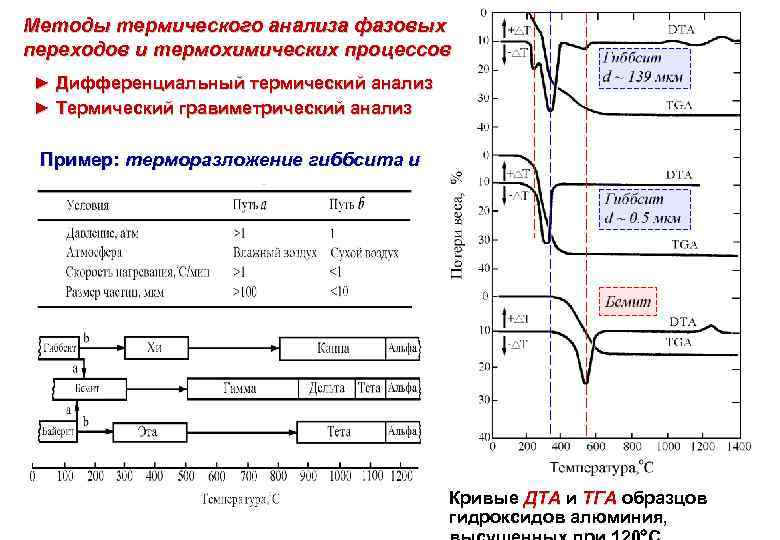
Методы термического анализа фазовых переходов и термохимических процессов ► Дифференциальный термический анализ ► Термический гравиметрический анализ Пример: терморазложение гиббсита и бемита Кривые ДТА и ТГА образцов гидроксидов алюминия,
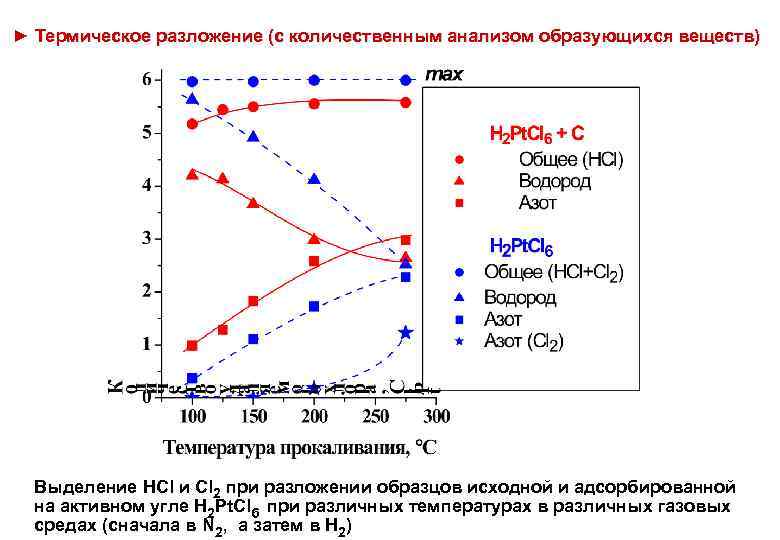
► Термическое разложение (с количественным анализом образующихся веществ) Выделение HCl и Cl 2 при разложении образцов исходной и адсорбированной на активном угле H 2 Pt. Cl 6 при различных температурах в различных газовых средах (сначала в N 2, а затем в H 2)
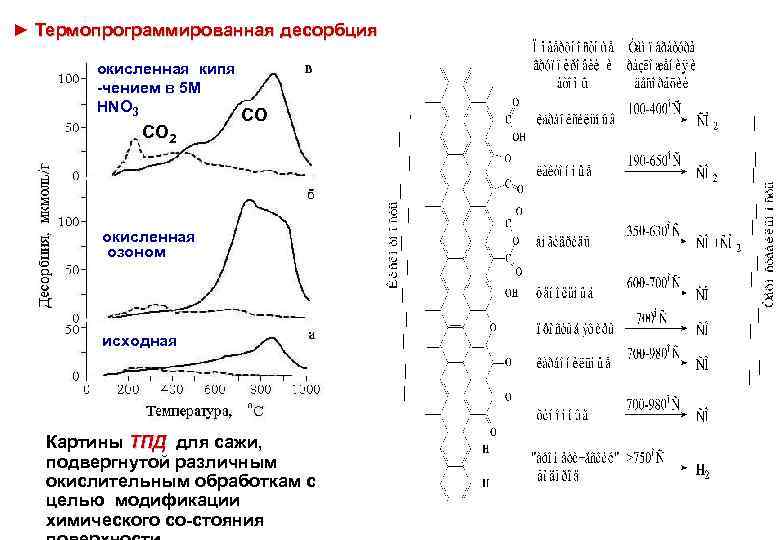
► Термопрограммированная десорбция окисленная кипя -чением в 5 М HNO 3 СО 2 СО окисленная озоном исходная Картины ТПД для сажи, подвергнутой различным окислительным обработкам с целью модификации химического со-стояния
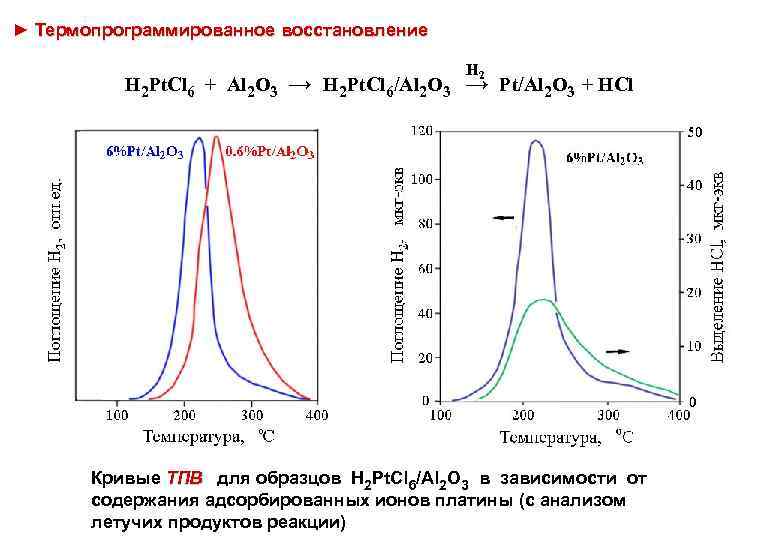
► Термопрограммированное восстановление H 2 Pt. Cl 6 + Al 2 O 3 H 2 → H 2 Pt. Cl 6/Al 2 O 3 → Pt/Al 2 O 3 + HCl Кривые ТПВ для образцов H 2 Pt. Cl 6/Al 2 O 3 в зависимости от содержания адсорбированных ионов платины (с анализом летучих продуктов реакции)

10. 1. 1. Формирование фазового состава при термическом разложении I. Разложение индивидуальных соединений ► прямое: Mg(OH)2 Mg. O + H 2 O ► через промежуточные стадии: 200 C 1) La(OH)3 La. O(OH) 2) (NH 4)6 Mo 7 O 24 4 H 2 O 115 -130 C {(NH 4)2 Mo 4 O 13} 320 -355 C Mo. O 3 3) NH 4 VO 3 418 -435 C (NH 4)2 V 4 O 11 300 C La 2 O 3 {(NH 4)4 O 5 Mo 5 O 17} 533 -551 C 225 -245 C V 2 O 5 ► с изменением валентности: 1) Sb 2 O 5 n. H 2 O 2) 4 Cr. O 3 >250 C 100 -200 C Sb 2 O 5 2 Cr 2 O 3 + 3 O 2↑ 225 -245 C (Sb 23+Sb 45+)O 13 320 -355 C Sb 2 O 3 Направление и глубина редокс процессов зависят от состава газовой

II. Разложение бинарных соединений ► разложение соединений переменного состава а) на индивидуальные оксиды x. Cu. O y. Si. O 2 n. H 2 O x. Cu. O + y. Si. O 2 + n. H 2 O x. Cu(OH)2 y. Ti(OH)4 x. Cu. O + y. Ti. O 2 + (x+2 y) H 2 O б) на оксид одного из компонентов и твёрдый раствор Mg(OH)2 Cu(OH)2 (1 2 x) Cu. O 500 C Mg. O Cu. O n. H 2 O 800 C Mg 1 -x. Cux. O + в) на оксид одного из компонентов и стехиометрическое соединение Zn 2 Al (OH)7 x(NO 3)x Zn. Al 2 O 4 + Zn. O Zn. Al 2 O 4 n. H 2 O + Zn 2 Al (OH)9 NO 3 ► разложение стехиометрических соединений с образованием другого соединения:

Протекание процессов разложения веществ зависит от парциального давления газообразных продуктов реакции: с его реакции уменьшением уменьшается энергия активации процесса разложения, снижается температура начала кристаллизации образующихся фаз от дисперсности и дефектности исходных веществ: с их ростом растут константы равновесия химических реакций где G 0 д приращение хим. потенциала, обусловленного дисперсностью и/или дефектностью; Kд и K константы равновесия реакции для дисперсных (и/или дефектных) и массивных тел. снижаются температуры фазовых переходов на величину Т = Т Тд где T и Tд температуры фазового перехода для массивного и диспергированного вещества, соответственно; поверхностное натяжение; Vм мольный объем вещества; Hф. п энтальпия фазового перехода; S поверхность, а V объем от характера. взаимодействия частиц компонентов в частицы вещества многокомпонентных системах
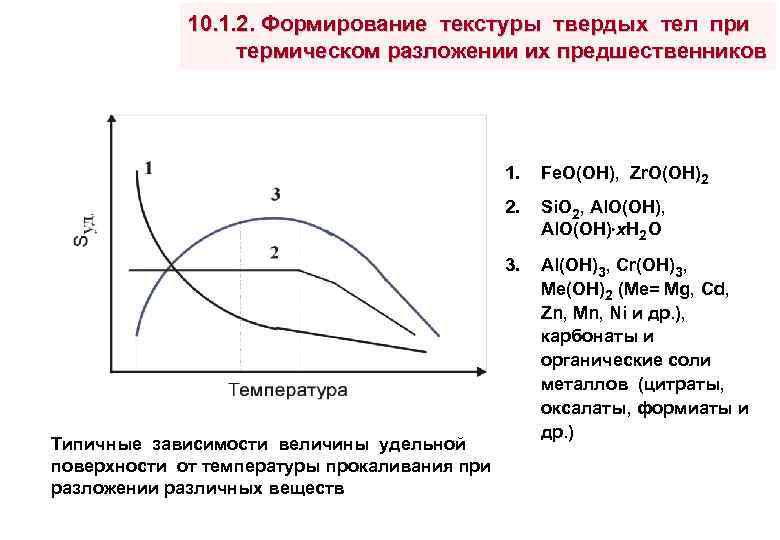
10. 1. 2. Формирование текстуры твердых тел при термическом разложении их предшественников 1. 2. Si. O 2, Al. O(OH) x. H 2 O 3. Типичные зависимости величины удельной поверхности от температуры прокаливания при разложении различных веществ Fe. O(OH), Zr. O(OH)2 Al(OH)3, Cr(OH)3, Me(OH)2 (Me= Mg, Cd, Zn, Mn, Ni и др. ), карбонаты и органические соли металлов (цитраты, оксалаты, формиаты и др. )

Факторы, затрагивающие формирование поверхности твердых тел при термическом разложении их предшественников 1. Химическая природа исходных веществ: При отсутствии фазовых превращений Sуд. не меняется вплоть до начала спекания (Si. O 2) При наличии фазовых превращений величина Sуд. определяется а) природой исходных и конечных продуктов: продуктов – аморфные или кристаллические исходные вещества; – гидроксиды, кристаллогидраты, безводные соли; б) различиями в плотности исходных веществ и продуктов их разложения; в) наложением областей термического разложения на фазовые переходы продуктов; г) наличием /концентрацией/ инородных включений (затрудняют срастание кристаллитов) Пористая структура предшественника (микропористые тела быстрее уплотняются) Наличие примесей щелочных металлов, анионов, флюсов и др. (например, примеси NH 4 NO 3 снижают температуру образования кристаллического Fe 2 O 3 на 100 С) 2. Условия термообработки: Состав атмосферы (исходные компоненты газовой среды + газообразные
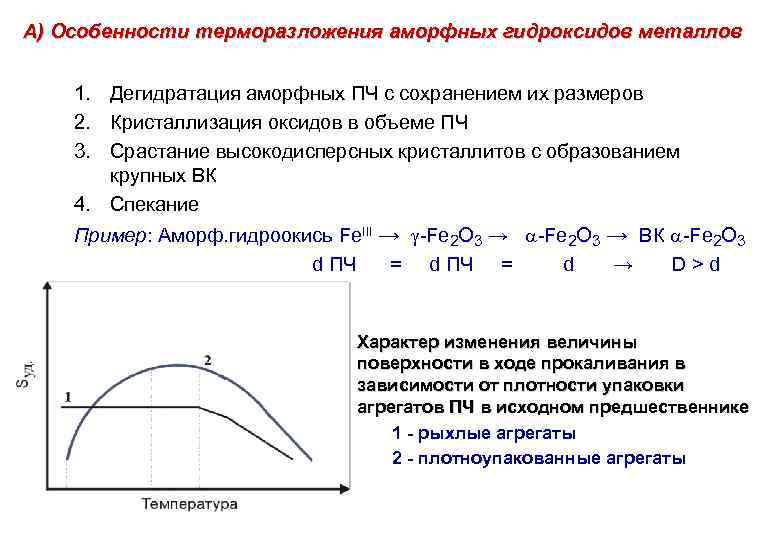
А) Особенности терморазложения аморфных гидроксидов металлов 1. Дегидратация аморфных ПЧ с сохранением их размеров 2. Кристаллизация оксидов в объеме ПЧ 3. Срастание высокодисперсных кристаллитов с образованием крупных ВК 4. Спекание Пример: Аморф. гидроокись Fe. III → -Fe 2 O 3 → ВК -Fe 2 O 3 d ПЧ = d → D>d Характер изменения величины поверхности в ходе прокаливания в зависимости от плотности упаковки агрегатов ПЧ в исходном предшественнике 1 - рыхлые агрегаты 2 - плотноупакованные агрегаты
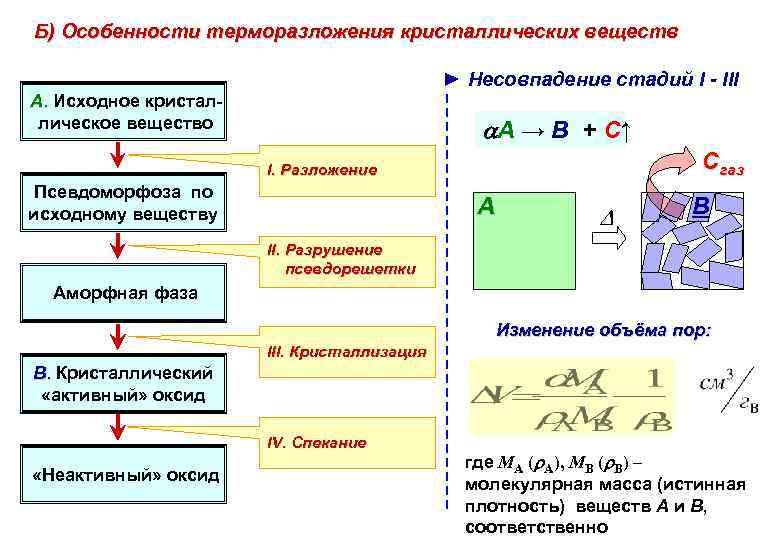
Б) Особенности терморазложения кристаллических веществ ► Несовпадение стадий I - III А. Исходное кристаллическое вещество А → В + С↑ Сгаз I. Разложение Псевдоморфоза по исходному веществу А В II. Разрушение псевдорешетки Аморфная фаза Изменение объёма пор: III. Кристаллизация В. Кристаллический «активный» оксид IV. Спекание «Неактивный» оксид где МА ( А), МВ ( В) – молекулярная масса (истинная плотность) веществ А и В, соответственно
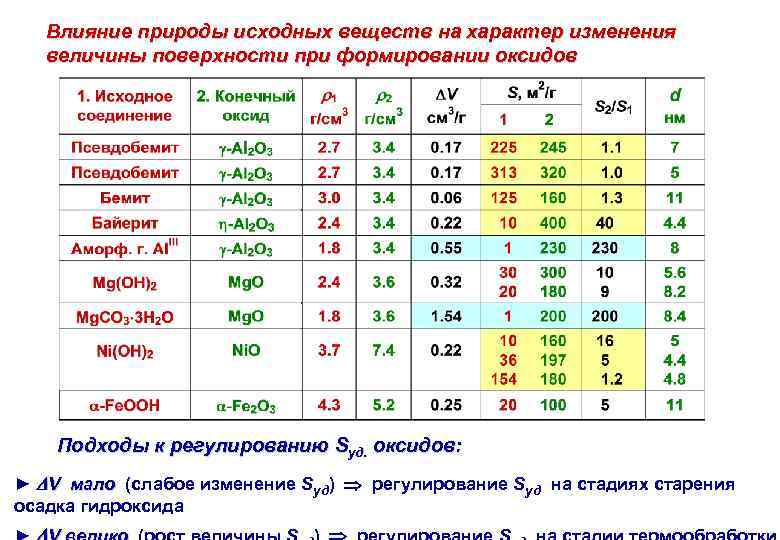
Влияние природы исходных веществ на характер изменения величины поверхности при формировании оксидов Подходы к регулированию Sуд. оксидов: ► V мало (слабое изменение Sуд) регулирование Sуд на стадиях старения осадка гидроксида
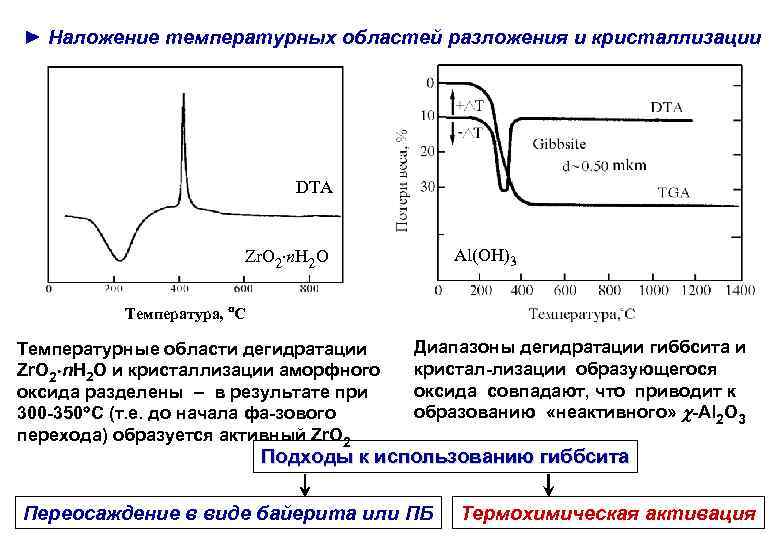
► Наложение температурных областей разложения и кристаллизации DTA Zr. O 2 n. H 2 O Al(OH)3 Температура, С Температурные области дегидратации Zr. O 2 n. H 2 O и кристаллизации аморфного оксида разделены – в результате при 300 -350 С (т. е. до начала фа-зового перехода) образуется активный Zr. O 2 Диапазоны дегидратации гиббсита и кристал-лизации образующегося оксида совпадают, что приводит к образованию «неактивного» -Al 2 O 3 Подходы к использованию гиббсита Переосаждение в виде байерита или ПБ Термохимическая активация

10. 1. 3. Термохимическая активация гиббсита Режимы дегидратации гиббсита Термохимическая активация твердых веществ это процесс извлечения скорость нагрева < 100 С/мин некоторых элементов из Al(OH)3 → -Al 2 O 3 + H 2 O устойчивой ЯМР: 4 -x и 6 -ти координированные кристаллической структуры 3+ ионы Al при её нагревании в не 2. Импульсный нагрев равновесных условиях с скорость нагрева >> 100 С/мин ( 1000 ), образо-ванием мягкие температурные условия метастабильных структур с в зоне реакции ( Тдегидратац), повышенной избыточной оптимальное парциальное давление энер-гией, которые обладают высокой паров воды, быстрое охлаждение (“закаливание”) реакционной способностью продукта. Продукт ТХА – аморфный, состав – Продукт ТХА гиббсита – не просто промежуточное Al 2 O 3 0. 63 H 2 O соединение его дегидратации, а качественно новое ЯМР: 4 -x , 5 -ти и 6 -ти координированные состояние вещества 1. Стандартный (традиционный)

Использование продукта ТХА гиббсита для синтеза гидроксидов алюминия ► Экструзия (закатывание) + гидратация в жидкой среде Продукт ТХА → Псевдобемит (р. Н 7, 80 С, 4 ч) Продукт ТХА → Байерит (р. Н 9, 80 С, 4 ч) ► Окатывание на грануляторе + гидратация в парах воды Псевдобемит, байерит (Т, Р, ) Достоинства метода ТХА: получение реакционного продукта, из которого удается синтезировать полный набор «активных» оксидов алюминия, технологическая простота получения продукта, экологическая чистота (отсутствие или минимальное количество «жидких» стадий и агрессивных реагентов) Недостатки метода ТХА: трудность в получении фазово чистого продукта ТХА (наличие примесей гиббсита или кристаллической фазы оксида, определяемых режимом процесса)

10. 2. Спекание пористых тел – совокупность термически активированных процессов переноса массы, приводящих к снижению площади поверхности и уплотнению Классификация процессов спекания пористых тел Жидкофазное спекание. Механизмы: спекание вязкое течение жидкости (смачивание и стягивание частиц вещества под действием сил поверхностного натяжения жидкой фазы), перенос вещества через жидкую фазу (растворение+кристаллизация) Твердофазное спекание. Механизмы: спекание диффузия (поверхностная, объёмная; атомов, вакансий и др. ), пластическая деформация, перенос вещества через газовую фазу (сублимация+конденсация) Реакционное спекание. Механизм: спекание
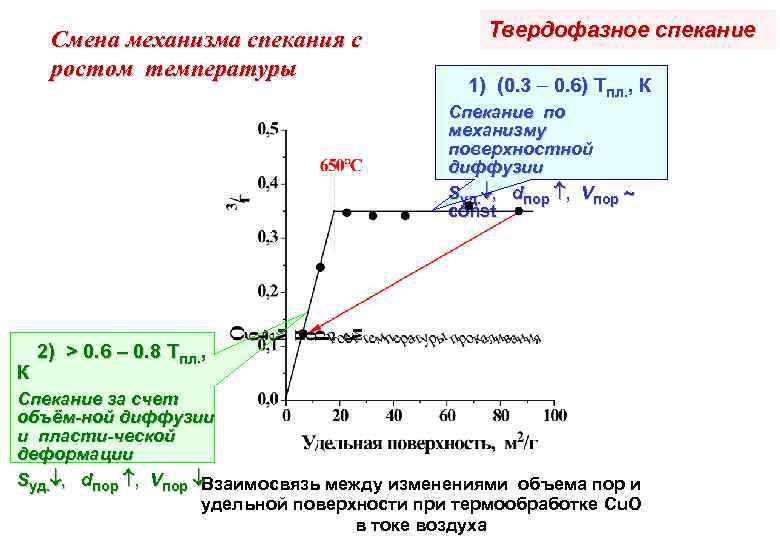
Смена механизма спекания с ростом температуры Твердофазное спекание 1) (0. 3 0. 6) Tпл. , К Спекание по механизму поверхностной диффузии Sуд. , dпор , Vпор const К 2) > 0. 6 – 0. 8 Tпл. , Спекание за счет объём-ной диффузии и пласти-ческой деформации Sуд. , dпор , Vпор Взаимосвязь между изменениями объема пор и удельной поверхности при термообработке Cu. O в токе воздуха
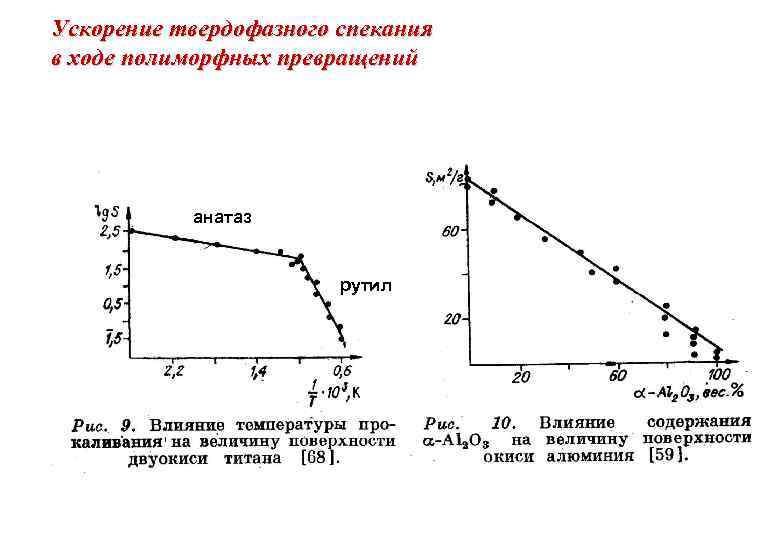
Ускорение твердофазного спекания в ходе полиморфных превращений анатаз рутил

Влияние химических примесей на интенсивность твердофазного спекания Эффект действия микродобавки определяется её природой, концентрацией и характером её распределения в матрице Типы добавок в зависимости от характера взаимодействия с матрицей Нерастворимые, а образующие жидкую фазу при плавлении или взаимодействии с основным веществом с образованием эвтектического расплава (ускоряют спекание за счет интенсификации массопереноса через жидкую среду) Полностью растворимые в кристаллической решетке основного вещества (ускоряют спекание за счет изменения концентраций вакансий в анионной либо катионной подрешетках кристаллов), Вступающие в химическое взаимодействие с основным веществом с образовани-ем нового соединения (замедляют или ускоряют спекание в зависимости от вида образующегося соединения) Нужно обращать внимание на побочное влияние Инертные, не растворимые в микродобавок на свойстваи не основном веществе катализаторов
Л_12-SPA-Термическая обработка кат.ppt