Лекция_11(Уравнение состояния и МКТ) 2сем.pptx
- Количество слайдов: 20
 Лекция 11 Уравнение состояния идеального газа. Элементы молекулярно-кинетической теории газов 1
Лекция 11 Уравнение состояния идеального газа. Элементы молекулярно-кинетической теории газов 1
 Вопросы: • Уравнения состояния термодинамических систем • Уравнение Клапейрона – Менделеева • Основное уравнение молекулярно-кинетической теории • Равномерное распределение энергии по степеням свободы молекул • Внутренняя энергия идеального газа • Эффективный диаметр и средняя длина свободного пробега молекул газа • Экспериментальные подтверждения молекулярно-кинетической теории 2
Вопросы: • Уравнения состояния термодинамических систем • Уравнение Клапейрона – Менделеева • Основное уравнение молекулярно-кинетической теории • Равномерное распределение энергии по степеням свободы молекул • Внутренняя энергия идеального газа • Эффективный диаметр и средняя длина свободного пробега молекул газа • Экспериментальные подтверждения молекулярно-кинетической теории 2
 Уравнения состояния термодинамических систем Состояния макросистем описываются тем или иным набором термодинамических параметров. Количество параметров может быть избыточным. В этом случае одни параметры полностью определяют другие, а, следовательно, в ходе описания системы последние можно смело исключить. Зависимость между параметрами состояния термодинамической системы (ТС) выражается соответствующим уравнением состояния. В простейшем случае равновесное состояние ТС можно аналитически записать некоторой функциональной зависимостью трех основных параметров – давления р, объема V и температуры Т: F(р, V, T) = 0 (1) Конкретный вид формулы (1) зависит от физических свойств ТС. Уравнения состояния в термодинамике позволяют дополнительно классифицировать системы. Существуют и используются при описании систем следующие модели: идеальный газ, газ Ван-дер. Ваальса, фотонный газ; причем каждой из моделей соответствует свое уравнение состояния. 3
Уравнения состояния термодинамических систем Состояния макросистем описываются тем или иным набором термодинамических параметров. Количество параметров может быть избыточным. В этом случае одни параметры полностью определяют другие, а, следовательно, в ходе описания системы последние можно смело исключить. Зависимость между параметрами состояния термодинамической системы (ТС) выражается соответствующим уравнением состояния. В простейшем случае равновесное состояние ТС можно аналитически записать некоторой функциональной зависимостью трех основных параметров – давления р, объема V и температуры Т: F(р, V, T) = 0 (1) Конкретный вид формулы (1) зависит от физических свойств ТС. Уравнения состояния в термодинамике позволяют дополнительно классифицировать системы. Существуют и используются при описании систем следующие модели: идеальный газ, газ Ван-дер. Ваальса, фотонный газ; причем каждой из моделей соответствует свое уравнение состояния. 3
 Уравнение Клапейрона – Менделеева Опытным путем было установлено, что при обычных условиях (при комнатной температуре и атмосферном давлении) для таких газов, как кислород и азот, достаточно выполняется соотношение: (2) где b – постоянная, пропорциональная массе газа (или количеству вещества). Причем, чем разреженней газ, тем точнее выполняется соотношение (2). У разреженных газов молекулы практически не взаимодействуют между собой, они лишь изредка сталкиваются друг с другом. Газ, взаимодействием между молекулами которого можно пренебречь, называется идеальным газом. Такой газ подчиняется уравнению (2), которое можно рассматривать как уравнение состояния идеального газа. Если воспользоваться законом Авогадро (объем 1 моля любого газа при нормальных условиях Т = 273 К и р = 105 Па составляет 22, 4 л), то для 1 моля идеального газа можно записать выражение (2) в виде: р. Vμ = R. T (3) 4 где Vμ – молярный объем, R = 8, 31 Дж/моль. К – газовая постоянная.
Уравнение Клапейрона – Менделеева Опытным путем было установлено, что при обычных условиях (при комнатной температуре и атмосферном давлении) для таких газов, как кислород и азот, достаточно выполняется соотношение: (2) где b – постоянная, пропорциональная массе газа (или количеству вещества). Причем, чем разреженней газ, тем точнее выполняется соотношение (2). У разреженных газов молекулы практически не взаимодействуют между собой, они лишь изредка сталкиваются друг с другом. Газ, взаимодействием между молекулами которого можно пренебречь, называется идеальным газом. Такой газ подчиняется уравнению (2), которое можно рассматривать как уравнение состояния идеального газа. Если воспользоваться законом Авогадро (объем 1 моля любого газа при нормальных условиях Т = 273 К и р = 105 Па составляет 22, 4 л), то для 1 моля идеального газа можно записать выражение (2) в виде: р. Vμ = R. T (3) 4 где Vμ – молярный объем, R = 8, 31 Дж/моль. К – газовая постоянная.
 Уравнение Клапейрона – Менделеева Чтобы получить уравнение состояния для произвольной массы М идеального газа, умножим обе части уравнения (3) на М /μ (μ – молярная масса газа): р(М /μ)Vμ = (М /μ)R. T. Так как (М /μ)Vμ = V – объем, занимаемый газом массой М, получаем классическое уравнение Клапейрона – Менделеева: p. V = (M /μ)R. T (4) С учетом, что ν = М /μ определяет число молей газа, уравнение (4) можно также записать в виде: p. V = ν. R. T (5) Если умножить и разделить правую часть уравнения (4) на число Авогадро NA= 6, 02. 1023 моль– 1, то получим выражение p. V = (M /μ)NA. . R/N. T = N. k. T, где N = (M /μ)N – общее число молекул в газе массой A A. 10– 23 Дж/К – постоянная Больцмана. Разделив обе М, а k = R / NA = 1, 38 части последнего выражения на объем газа V получим уравнение состояния идеального газа (в форме Больцмана): p = n. k. T (6) где n = N / V – концентрация молекул в газе. 5
Уравнение Клапейрона – Менделеева Чтобы получить уравнение состояния для произвольной массы М идеального газа, умножим обе части уравнения (3) на М /μ (μ – молярная масса газа): р(М /μ)Vμ = (М /μ)R. T. Так как (М /μ)Vμ = V – объем, занимаемый газом массой М, получаем классическое уравнение Клапейрона – Менделеева: p. V = (M /μ)R. T (4) С учетом, что ν = М /μ определяет число молей газа, уравнение (4) можно также записать в виде: p. V = ν. R. T (5) Если умножить и разделить правую часть уравнения (4) на число Авогадро NA= 6, 02. 1023 моль– 1, то получим выражение p. V = (M /μ)NA. . R/N. T = N. k. T, где N = (M /μ)N – общее число молекул в газе массой A A. 10– 23 Дж/К – постоянная Больцмана. Разделив обе М, а k = R / NA = 1, 38 части последнего выражения на объем газа V получим уравнение состояния идеального газа (в форме Больцмана): p = n. k. T (6) где n = N / V – концентрация молекул в газе. 5
 Основное уравнение молекулярнокинетической теории (МКТ) Будем рассматривать находящийся в сосуде равновесный газ, движение молекул которого полностью хаотично. Это позволяет в первом приближении считать, что все молекулы движутся только в 3 -х взаимно перпендикулярных направлениях x, y, z, т. е. если в единице объема газа имеется п молекул, то в каждом направлении движутся ( «туда – обратно» ) по 1/3. п молекул или 1/6. п молекул в одну сторону ( «туда» или «обратно» ). Разобьем молекулы в каждом единичном объеме на группы (фракции) ∆пi, в каждой из которых скорости молекул можно считать практически одинаковыми и равными υi, так, чтобы выполнялось условие ∑i ∆пi = п. Число νi молекул i-ой группы, которые ежесекундно достигают единицы поверхности стенки сосуда, двигаясь нормально к ней (допущение прямого «лобового» удара), равно числу таких молекул в цилиндре длиной (υi. 1 с) и сечением S = 1 м 2 (см. рис. ), т. е. νi = 1/6. ∆ni. υi (7) S (υi. 1 с) 6
Основное уравнение молекулярнокинетической теории (МКТ) Будем рассматривать находящийся в сосуде равновесный газ, движение молекул которого полностью хаотично. Это позволяет в первом приближении считать, что все молекулы движутся только в 3 -х взаимно перпендикулярных направлениях x, y, z, т. е. если в единице объема газа имеется п молекул, то в каждом направлении движутся ( «туда – обратно» ) по 1/3. п молекул или 1/6. п молекул в одну сторону ( «туда» или «обратно» ). Разобьем молекулы в каждом единичном объеме на группы (фракции) ∆пi, в каждой из которых скорости молекул можно считать практически одинаковыми и равными υi, так, чтобы выполнялось условие ∑i ∆пi = п. Число νi молекул i-ой группы, которые ежесекундно достигают единицы поверхности стенки сосуда, двигаясь нормально к ней (допущение прямого «лобового» удара), равно числу таких молекул в цилиндре длиной (υi. 1 с) и сечением S = 1 м 2 (см. рис. ), т. е. νi = 1/6. ∆ni. υi (7) S (υi. 1 с) 6
 Основное уравнение молекулярнокинетической теории (МКТ) Суммируя по всем фракциям молекул, определяем ν = ∑iνi = 1/6∑i∆ni. υi, а разделив и умножив последнюю сумму на п, получаем: ν = 1/6. п. <υ> (8) где принято <υ> = ∑i∆ni. υi /п – среднее значение скорости молекул. Величина, определяемая по формуле (8), называется частотой соударения молекул газа о стенку. Примечание. Более строгий расчет ν, учитывающий движение молекул не вдоль 3 -х выбранных направлений, а с равной вероятностью вдоль любого направления в пространстве, приводит к формуле: ν = 1/4. п. <υ> (9) Природа давления газа на стенку (которое измеряется в эксперименте) заключается в совокупном действии множества молекул. При оценочном подходе будем считать, что каждая молекула, налетая на стенку нормально, в результате упругого столкновения с ней отлетает строго в противоположном направлении. При этом приращение импульса молекулы в процессе удара (см. рис. ): ∆р = р2 – р1 = mυ – (– mυ) = 2 mυ (10) p 1= mυ p 2= mυ x 7
Основное уравнение молекулярнокинетической теории (МКТ) Суммируя по всем фракциям молекул, определяем ν = ∑iνi = 1/6∑i∆ni. υi, а разделив и умножив последнюю сумму на п, получаем: ν = 1/6. п. <υ> (8) где принято <υ> = ∑i∆ni. υi /п – среднее значение скорости молекул. Величина, определяемая по формуле (8), называется частотой соударения молекул газа о стенку. Примечание. Более строгий расчет ν, учитывающий движение молекул не вдоль 3 -х выбранных направлений, а с равной вероятностью вдоль любого направления в пространстве, приводит к формуле: ν = 1/4. п. <υ> (9) Природа давления газа на стенку (которое измеряется в эксперименте) заключается в совокупном действии множества молекул. При оценочном подходе будем считать, что каждая молекула, налетая на стенку нормально, в результате упругого столкновения с ней отлетает строго в противоположном направлении. При этом приращение импульса молекулы в процессе удара (см. рис. ): ∆р = р2 – р1 = mυ – (– mυ) = 2 mυ (10) p 1= mυ p 2= mυ x 7
 Основное уравнение молекулярнокинетической теории (МКТ) В соответствии с уравнением изменения импульса имеем ∆р = F. ∆t, где импульс силы F. ∆t, передаваемый молекулам от стенки, а молекулы в свою очередь передают стенке импульс силы (– F. ∆t), который и определяет интересующее нас давление (по определению р = Fn /S, Н/м 2). Поэтому с учетом выражения частоты соударения i-ых молекул о стенку получаем импульс (он же парциальное давление), который передают стенке молекулы i-ой группы: pi = 2 mi. υi. νi = 1/3. m. υi 2. ∆ni (11) где для случая однородного газа принято m = mi. Полное давление газа на стенку найдем, просуммировав формулу (11) по всем группам ∆пi молекул: p = ∑i pi = 1/3 m. ∑iυi 2. ∆ni (12) Примечание. Выражение p = ∑i pi отражает закон Дальтона. Разделив и умножив выражение (12) на п, получим одну из форм записи основного уравнения МКТ: р = 1/3. п. m. <υ2> (13) где <υ2> = ∑iυi 2. ∆ni/п – среднее значение квадрата скорости молекул. 8
Основное уравнение молекулярнокинетической теории (МКТ) В соответствии с уравнением изменения импульса имеем ∆р = F. ∆t, где импульс силы F. ∆t, передаваемый молекулам от стенки, а молекулы в свою очередь передают стенке импульс силы (– F. ∆t), который и определяет интересующее нас давление (по определению р = Fn /S, Н/м 2). Поэтому с учетом выражения частоты соударения i-ых молекул о стенку получаем импульс (он же парциальное давление), который передают стенке молекулы i-ой группы: pi = 2 mi. υi. νi = 1/3. m. υi 2. ∆ni (11) где для случая однородного газа принято m = mi. Полное давление газа на стенку найдем, просуммировав формулу (11) по всем группам ∆пi молекул: p = ∑i pi = 1/3 m. ∑iυi 2. ∆ni (12) Примечание. Выражение p = ∑i pi отражает закон Дальтона. Разделив и умножив выражение (12) на п, получим одну из форм записи основного уравнения МКТ: р = 1/3. п. m. <υ2> (13) где <υ2> = ∑iυi 2. ∆ni/п – среднее значение квадрата скорости молекул. 8
 Основное уравнение молекулярнокинетической теории (МКТ) Так как мы предположили массу всех молекул одинаковой, то m в (13) можно внести под знак среднего < > и переписать (13) в виде: p = 2/3. п.
Основное уравнение молекулярнокинетической теории (МКТ) Так как мы предположили массу всех молекул одинаковой, то m в (13) можно внести под знак среднего < > и переписать (13) в виде: p = 2/3. п.
 Равномерное распределение энергии по степеням свободы молекул Понятие степени свободы – это число независимых координат, полностью определяющих положение рассматриваемой системы (в нашем случае – молекулы) в пространстве. 1. Для определения положения центра масс молекулы необходимо задать три координаты (например, x, y, z). Это значит, что любая одноатомная молекула (как материальная точка) имеет три поступательных степени свободы, т. е. число степеней свободы такой молекулы i = 3. Примечание. Система, состоящая из N материальных точек, между которыми нет жестких связей, имеет i = 3. N степеней свободы. Каждая жесткая связь, обусловливающая неизменное расстояние между двумя точками, уменьшает число i ровно на 1. 2. Если молекула двухатомная и жесткая, то к трем поступательным степеням добавляются две вращательные степени свободы, связанные с возможными углами поворота вокруг двух взаимно перпендикулярных осей: (1 – 1') и (2 – 2'). Таким образом такая молекула имеет i= 3 + 2 = 5 (степеней свободы), т. е. 1 2 работает формула i = 3. N – 1, где N – А 1 А 2 10 число атомов. 2' 1'
Равномерное распределение энергии по степеням свободы молекул Понятие степени свободы – это число независимых координат, полностью определяющих положение рассматриваемой системы (в нашем случае – молекулы) в пространстве. 1. Для определения положения центра масс молекулы необходимо задать три координаты (например, x, y, z). Это значит, что любая одноатомная молекула (как материальная точка) имеет три поступательных степени свободы, т. е. число степеней свободы такой молекулы i = 3. Примечание. Система, состоящая из N материальных точек, между которыми нет жестких связей, имеет i = 3. N степеней свободы. Каждая жесткая связь, обусловливающая неизменное расстояние между двумя точками, уменьшает число i ровно на 1. 2. Если молекула двухатомная и жесткая, то к трем поступательным степеням добавляются две вращательные степени свободы, связанные с возможными углами поворота вокруг двух взаимно перпендикулярных осей: (1 – 1') и (2 – 2'). Таким образом такая молекула имеет i= 3 + 2 = 5 (степеней свободы), т. е. 1 2 работает формула i = 3. N – 1, где N – А 1 А 2 10 число атомов. 2' 1'
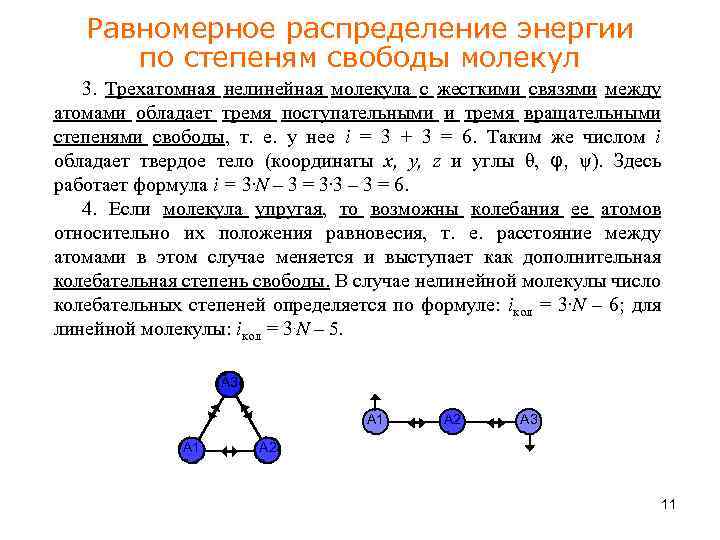 Равномерное распределение энергии по степеням свободы молекул 3. Трехатомная нелинейная молекула с жесткими связями между атомами обладает тремя поступательными и тремя вращательными степенями свободы, т. е. у нее i = 3 + 3 = 6. Таким же числом i обладает твердое тело (координаты x, y, z и углы θ, φ, ψ). Здесь работает формула i = 3. N – 3 = 3. 3 – 3 = 6. 4. Если молекула упругая, то возможны колебания ее атомов относительно их положения равновесия, т. е. расстояние между атомами в этом случае меняется и выступает как дополнительная колебательная степень свободы. В случае нелинейной молекулы число колебательных степеней определяется по формуле: iкол = 3. N – 6; для линейной молекулы: iкол = 3. N – 5. A 3 А 1 А 2 А 3 А 2 11
Равномерное распределение энергии по степеням свободы молекул 3. Трехатомная нелинейная молекула с жесткими связями между атомами обладает тремя поступательными и тремя вращательными степенями свободы, т. е. у нее i = 3 + 3 = 6. Таким же числом i обладает твердое тело (координаты x, y, z и углы θ, φ, ψ). Здесь работает формула i = 3. N – 3 = 3. 3 – 3 = 6. 4. Если молекула упругая, то возможны колебания ее атомов относительно их положения равновесия, т. е. расстояние между атомами в этом случае меняется и выступает как дополнительная колебательная степень свободы. В случае нелинейной молекулы число колебательных степеней определяется по формуле: iкол = 3. N – 6; для линейной молекулы: iкол = 3. N – 5. A 3 А 1 А 2 А 3 А 2 11
 Равномерное распределение энергии по степеням свободы молекул Гипотеза Больцмана о равномерном распределении энергии по степеням свободы Тот факт, что средняя кинетическая энергия поступательного движения молекулы согласно (15) <Епост> = 3/2. k. T, означает, что на каждую поступательную степень свободы приходится 1/2. k. T энергии. Л. Больцман обобщил этот вывод в виде гипотезы (закона) о равном распределении средней кинетической энергии молекул по всем ее степеням свободы, т. е. он записал: <Е> = i/2. k. T (17) где i = iпос+ iвр+ 2. iкол – полное число поступательных, вращательных и колебательных степеней свободы. В последнем выражении учтено, что на каждую колебательную степень приходится в среднем по две 1/2. k. T энергии: одна половинка в виде кинетической энергии и одна – в виде потенциальной энергии (известно, что для гармонического осциллятора средние значения этих энергий одинаковы). 12
Равномерное распределение энергии по степеням свободы молекул Гипотеза Больцмана о равномерном распределении энергии по степеням свободы Тот факт, что средняя кинетическая энергия поступательного движения молекулы согласно (15) <Епост> = 3/2. k. T, означает, что на каждую поступательную степень свободы приходится 1/2. k. T энергии. Л. Больцман обобщил этот вывод в виде гипотезы (закона) о равном распределении средней кинетической энергии молекул по всем ее степеням свободы, т. е. он записал: <Е> = i/2. k. T (17) где i = iпос+ iвр+ 2. iкол – полное число поступательных, вращательных и колебательных степеней свободы. В последнем выражении учтено, что на каждую колебательную степень приходится в среднем по две 1/2. k. T энергии: одна половинка в виде кинетической энергии и одна – в виде потенциальной энергии (известно, что для гармонического осциллятора средние значения этих энергий одинаковы). 12
 Внутренняя энергия идеального газа Следует напомнить, что внутренней энергией U макросистемы называют энергетическую величину, состоящую из § суммарной кинетической энергии хаотического движения всех молекул в Ц-системе отсчета, где макросистема как целое покоится; § собственной потенциальной энергии взаимодействия всех молекул макросистемы; § внутримолекулярной энергии (энергии электронных оболочек атомов, энергии ядер и т. п. ). Свойства внутренней энергии. 1. Внутренняя энергия является функцией состояния и, следовательно, приращение внутренней энергии определяется только ее значениями в конечном и начальном состояниях и не зависит от вида процесса (его направления), который перевел систему из одного состояния в другое, т. е. ∆U = U 2 – U 1 (18) 2. Внутренняя энергия является аддитивной величиной. Так как молекулы идеального газа практически не взаимодействуют между собой, то внутреннюю энергию 1 моля идеального газа можно определить, умножив среднюю энергию одной молекулы <Е> = i/2. k. T на число Авогадро NA= 6, 02. 1023 моль-1: 13 Uμ= i/2. R. T , где учтено, что R = k. NA (19)
Внутренняя энергия идеального газа Следует напомнить, что внутренней энергией U макросистемы называют энергетическую величину, состоящую из § суммарной кинетической энергии хаотического движения всех молекул в Ц-системе отсчета, где макросистема как целое покоится; § собственной потенциальной энергии взаимодействия всех молекул макросистемы; § внутримолекулярной энергии (энергии электронных оболочек атомов, энергии ядер и т. п. ). Свойства внутренней энергии. 1. Внутренняя энергия является функцией состояния и, следовательно, приращение внутренней энергии определяется только ее значениями в конечном и начальном состояниях и не зависит от вида процесса (его направления), который перевел систему из одного состояния в другое, т. е. ∆U = U 2 – U 1 (18) 2. Внутренняя энергия является аддитивной величиной. Так как молекулы идеального газа практически не взаимодействуют между собой, то внутреннюю энергию 1 моля идеального газа можно определить, умножив среднюю энергию одной молекулы <Е> = i/2. k. T на число Авогадро NA= 6, 02. 1023 моль-1: 13 Uμ= i/2. R. T , где учтено, что R = k. NA (19)
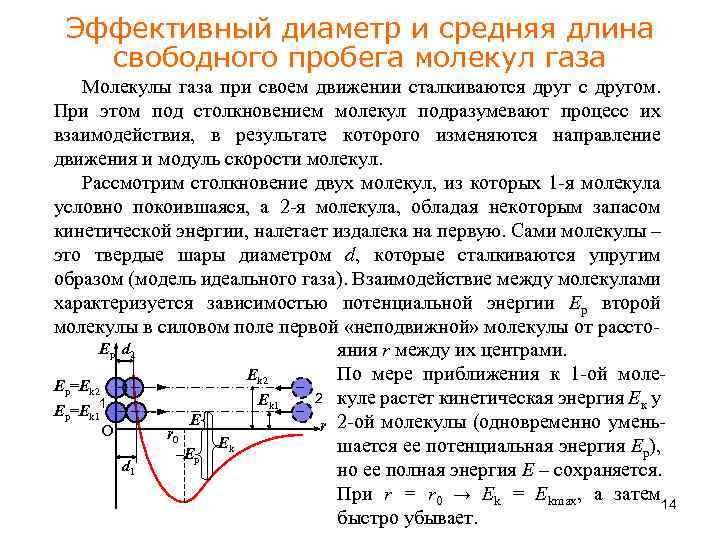 Эффективный диаметр и средняя длина свободного пробега молекул газа Молекулы газа при своем движении сталкиваются друг с другом. При этом под столкновением молекул подразумевают процесс их взаимодействия, в результате которого изменяются направление движения и модуль скорости молекул. Рассмотрим столкновение двух молекул, из которых 1 -я молекула условно покоившаяся, а 2 -я молекула, обладая некоторым запасом кинетической энергии, налетает издалека на первую. Сами молекулы – это твердые шары диаметром d, которые сталкиваются упругим образом (модель идеального газа). Взаимодействие между молекулами характеризуется зависимостью потенциальной энергии Ер второй молекулы в силовом поле первой «неподвижной» молекулы от рассто. Ep d 2 яния r между их центрами. Ek 2 По мере приближения к 1 -ой моле. Ep=Ek 2 2 куле растет кинетическая энергия Ек у Ek 1 Ep=Ek 11 E r 2 -ой молекулы (одновременно умень. О r 0 Ek шается ее потенциальная энергия Ер), –Ep d 1 но ее полная энергия Е – сохраняется. При r = r 0 → Ek = Ekmax, а затем 14 быстро убывает.
Эффективный диаметр и средняя длина свободного пробега молекул газа Молекулы газа при своем движении сталкиваются друг с другом. При этом под столкновением молекул подразумевают процесс их взаимодействия, в результате которого изменяются направление движения и модуль скорости молекул. Рассмотрим столкновение двух молекул, из которых 1 -я молекула условно покоившаяся, а 2 -я молекула, обладая некоторым запасом кинетической энергии, налетает издалека на первую. Сами молекулы – это твердые шары диаметром d, которые сталкиваются упругим образом (модель идеального газа). Взаимодействие между молекулами характеризуется зависимостью потенциальной энергии Ер второй молекулы в силовом поле первой «неподвижной» молекулы от рассто. Ep d 2 яния r между их центрами. Ek 2 По мере приближения к 1 -ой моле. Ep=Ek 2 2 куле растет кинетическая энергия Ек у Ek 1 Ep=Ek 11 E r 2 -ой молекулы (одновременно умень. О r 0 Ek шается ее потенциальная энергия Ер), –Ep d 1 но ее полная энергия Е – сохраняется. При r = r 0 → Ek = Ekmax, а затем 14 быстро убывает.
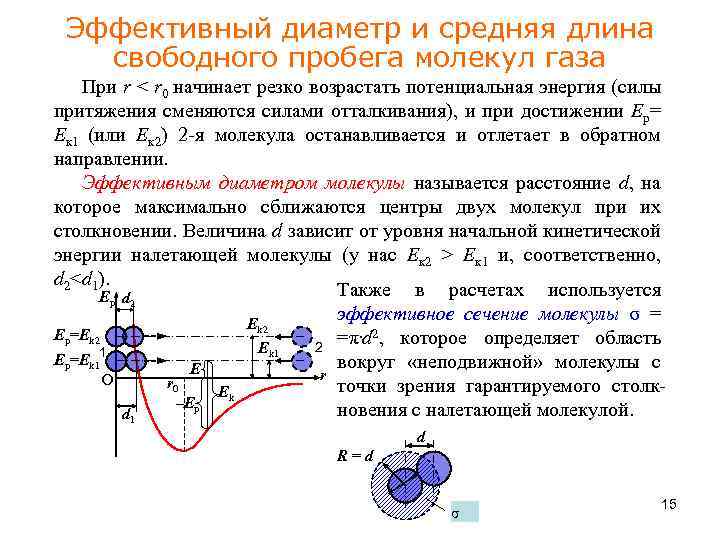 Эффективный диаметр и средняя длина свободного пробега молекул газа При r < r 0 начинает резко возрастать потенциальная энергия (силы притяжения сменяются силами отталкивания), и при достижении Ер= Ек 1 (или Ек 2) 2 -я молекула останавливается и отлетает в обратном направлении. Эффективным диаметром молекулы называется расстояние d, на которое максимально сближаются центры двух молекул при их столкновении. Величина d зависит от уровня начальной кинетической энергии налетающей молекулы (у нас Ек 2 > Ек 1 и, соответственно, d 2
Эффективный диаметр и средняя длина свободного пробега молекул газа При r < r 0 начинает резко возрастать потенциальная энергия (силы притяжения сменяются силами отталкивания), и при достижении Ер= Ек 1 (или Ек 2) 2 -я молекула останавливается и отлетает в обратном направлении. Эффективным диаметром молекулы называется расстояние d, на которое максимально сближаются центры двух молекул при их столкновении. Величина d зависит от уровня начальной кинетической энергии налетающей молекулы (у нас Ек 2 > Ек 1 и, соответственно, d 2
 Эффективный диаметр и средняя длина свободного пробега молекул газа Средняя длина свободного пробега молекулы – это расстояние, которое проходит молекула между двумя последовательными столкновениями, которое определяется по формуле: λ = 1/ν. <υ> (20) где ν – среднее число столкновений молекулы в 1 времени, <υ> средняя скорость молекулы. Чтобы определить частоту столкновений ν, проследим за поведением некоторой движущейся молекулы. Нетрудно сообразить, что она испытает за 1 единицу времени столько столкновений, сколько встретится на ее пути «неподвижных» молекул, центры которых окажутся в пределах объема цилиндра радиуса R = d. Ясно, что при каждом столкновении этот цилиндр будет испытывать «излом» . Объем этого «ломаного» цилиндра практически равен V = 1 c. <υ>. πd 2 = <υ>. σ, причем в виду того, что расстояние между изломами гораздо больше d, можно пренебречь частями объема, приходящимися на изломы. С учетом последнего можно определить: ν = n. <υ>. σ (21) где п – концентрация молекул. 16
Эффективный диаметр и средняя длина свободного пробега молекул газа Средняя длина свободного пробега молекулы – это расстояние, которое проходит молекула между двумя последовательными столкновениями, которое определяется по формуле: λ = 1/ν. <υ> (20) где ν – среднее число столкновений молекулы в 1 времени, <υ> средняя скорость молекулы. Чтобы определить частоту столкновений ν, проследим за поведением некоторой движущейся молекулы. Нетрудно сообразить, что она испытает за 1 единицу времени столько столкновений, сколько встретится на ее пути «неподвижных» молекул, центры которых окажутся в пределах объема цилиндра радиуса R = d. Ясно, что при каждом столкновении этот цилиндр будет испытывать «излом» . Объем этого «ломаного» цилиндра практически равен V = 1 c. <υ>. πd 2 = <υ>. σ, причем в виду того, что расстояние между изломами гораздо больше d, можно пренебречь частями объема, приходящимися на изломы. С учетом последнего можно определить: ν = n. <υ>. σ (21) где п – концентрация молекул. 16
 Эффективный диаметр и средняя длина свободного пробега молекул газа А средняя длина свободного пробега в соответствии с (20) равна: λ = 1/(σ. п). (22) На самом деле все молекулы движутся, вследствие чего число столкновений определяется не средней скоростью <υ> движения молекул относительно стенок сосуда, а средней относительной скоростью <υотн> молекул (скоростью молекул относительно друга), которая в √ 2 раз больше <υ>. В этом случае получаем: ν = √ 2. n. <υ>. σ , а λ = 1/(√ 2. п. σ) (23) Свободный пробег молекулы тем меньше, чем больше концентрация молекул п в сосуде и чем больше эффективное сечение взаимодействия молекул σ. При Т= const и р = п. k. Т получаем λ ~ 1/p. 17
Эффективный диаметр и средняя длина свободного пробега молекул газа А средняя длина свободного пробега в соответствии с (20) равна: λ = 1/(σ. п). (22) На самом деле все молекулы движутся, вследствие чего число столкновений определяется не средней скоростью <υ> движения молекул относительно стенок сосуда, а средней относительной скоростью <υотн> молекул (скоростью молекул относительно друга), которая в √ 2 раз больше <υ>. В этом случае получаем: ν = √ 2. n. <υ>. σ , а λ = 1/(√ 2. п. σ) (23) Свободный пробег молекулы тем меньше, чем больше концентрация молекул п в сосуде и чем больше эффективное сечение взаимодействия молекул σ. При Т= const и р = п. k. Т получаем λ ~ 1/p. 17
 Экспериментальные подтверждения молекулярно-кинетической теории Наиболее известными экспериментами, демонстрирующими молекулярную структуру вещества и подтверждающими положения МКТ, являются опыты Дюнуайе и Штерна, выполненные соответственно в 1911 г. и 1920 г. В этих опытах молекулярные пучки создавались путем испарения различных металлов (Na, Ag и др. ) и поэтому молекулы исследуемых газов представляли собой атомы этих металлов. Это позволяло проверить положения МКТ для газов, молекулы которых можно рассматривать как материальные точки (модель идеального газа). Схема эксперимента Дюнуайе Стеклянный сосуд (8), материал которого обеспечивает создание вы сокого вакуума в отделениях (3, 4), был разделен диафрагмами (2) на три отделения (1, 3, 4). Отделение (1) ΔΩ заполнено парами натрия. Молекулы (атомы) этого газа могли свободно проле 8 тать через отверстия в диафрагмах. 18
Экспериментальные подтверждения молекулярно-кинетической теории Наиболее известными экспериментами, демонстрирующими молекулярную структуру вещества и подтверждающими положения МКТ, являются опыты Дюнуайе и Штерна, выполненные соответственно в 1911 г. и 1920 г. В этих опытах молекулярные пучки создавались путем испарения различных металлов (Na, Ag и др. ) и поэтому молекулы исследуемых газов представляли собой атомы этих металлов. Это позволяло проверить положения МКТ для газов, молекулы которых можно рассматривать как материальные точки (модель идеального газа). Схема эксперимента Дюнуайе Стеклянный сосуд (8), материал которого обеспечивает создание вы сокого вакуума в отделениях (3, 4), был разделен диафрагмами (2) на три отделения (1, 3, 4). Отделение (1) ΔΩ заполнено парами натрия. Молекулы (атомы) этого газа могли свободно проле 8 тать через отверстия в диафрагмах. 18
 Экспериментальные подтверждения молекулярно-кинетической теории Диафрагмы коллимировали молекулярный пучок (7), т. е. позволяли ему проходить только в пределах малого телесного угла (ΔΩ). В отделениях (3 и 4) был сверхвысокий вакуум, при котором атомы натрия могли пролетать эти области без столкновений с молекулами воздуха. Нерассеянный пучок оставлял на торцевой стенке сосуда «жирный» след (6). Но даже в случае сверхвысокого вакуума имело место рассеяние пучка на краях диафрагм. Поэтому на стенке сосуда получалась также область «полутени» (5), в которой оставляли следы рассеянные частицы. Причем, по мере «ухудшения» вакуума в области (4) область (5) – росла. По величине следа рассеянных атомов можно было оценить длину их свободного пробега λ. ΔΩ 8 19
Экспериментальные подтверждения молекулярно-кинетической теории Диафрагмы коллимировали молекулярный пучок (7), т. е. позволяли ему проходить только в пределах малого телесного угла (ΔΩ). В отделениях (3 и 4) был сверхвысокий вакуум, при котором атомы натрия могли пролетать эти области без столкновений с молекулами воздуха. Нерассеянный пучок оставлял на торцевой стенке сосуда «жирный» след (6). Но даже в случае сверхвысокого вакуума имело место рассеяние пучка на краях диафрагм. Поэтому на стенке сосуда получалась также область «полутени» (5), в которой оставляли следы рассеянные частицы. Причем, по мере «ухудшения» вакуума в области (4) область (5) – росла. По величине следа рассеянных атомов можно было оценить длину их свободного пробега λ. ΔΩ 8 19
 Экспериментальные подтверждения молекулярно-кинетической теории 20
Экспериментальные подтверждения молекулярно-кинетической теории 20


