11 Лек Магния, цинка сульфат.PPT
- Количество слайдов: 17
 ЛЕКЦИЯ № 11 ТЕМА: «II ГРУППА ПЕРИОДИЧЕСКОЙ СИСТЕМЫ Д. И. МЕНДЕЛЕЕВА. МАГНИЯ СУЛЬФАТ. КАЛЬЦИЯ ХЛОРИД» .
ЛЕКЦИЯ № 11 ТЕМА: «II ГРУППА ПЕРИОДИЧЕСКОЙ СИСТЕМЫ Д. И. МЕНДЕЛЕЕВА. МАГНИЯ СУЛЬФАТ. КАЛЬЦИЯ ХЛОРИД» .
 МАГНИЯ СУЛЬФАТ. MAGNESII SULFAS. Mg. SO 4 • 7 H 2 O
МАГНИЯ СУЛЬФАТ. MAGNESII SULFAS. Mg. SO 4 • 7 H 2 O
 Магния сульфат впервые был получен в 1695 году. Как лечебное средство его начали применять в конце XVIII в в Англии (отсюда его первоначальное название – горькая или английская соль). В природе встречается в виде различных минералов, магнезит Mg. СO 3 , доломит Mg. СO 3 • Ca. CO 3 , кизерит Mg. SO 4 • 7 H 2 O или эмпосит, залежи которых встречаются в Сибири, на Кавказе, Кубани. Богаты сульфатом магния воды Каспийского моря. В промышленности получают из магнезита: Mg. СO 3 + H 2 SO 4 Mg. SO 4 + H 2 O + CO 2 ↑ Добавляют избыток серной кислоты во избежание гидролиза магния сульфата и образования основных солей. Свойства: Бесцветные призматические кристаллы или белый кристаллический порошок выветривающийся на воздухе, без запаха, горько – соленого вкуса. Хорошо растворяется в воде, практически не растворим в спирте 950. р. Н нейтральная.
Магния сульфат впервые был получен в 1695 году. Как лечебное средство его начали применять в конце XVIII в в Англии (отсюда его первоначальное название – горькая или английская соль). В природе встречается в виде различных минералов, магнезит Mg. СO 3 , доломит Mg. СO 3 • Ca. CO 3 , кизерит Mg. SO 4 • 7 H 2 O или эмпосит, залежи которых встречаются в Сибири, на Кавказе, Кубани. Богаты сульфатом магния воды Каспийского моря. В промышленности получают из магнезита: Mg. СO 3 + H 2 SO 4 Mg. SO 4 + H 2 O + CO 2 ↑ Добавляют избыток серной кислоты во избежание гидролиза магния сульфата и образования основных солей. Свойства: Бесцветные призматические кристаллы или белый кристаллический порошок выветривающийся на воздухе, без запаха, горько – соленого вкуса. Хорошо растворяется в воде, практически не растворим в спирте 950. р. Н нейтральная.
 Подлинность: Определяется по катиону Mg 2+ и аниону SO 42 -. HCl 1. Mg. SO 4 + Ba. Cl 2 Ba. SO 4 ↓ + Mg. Cl 2 белый осадок, не растворим в кислотах и щелочах 2. К раствору препарата прибавляют раствор хлорид аммония, раствор гидрофосфат натрия, раствор гидроксида аммония, образуется белый кристаллический осадок, растворимый в уксусной кислоте. NH 4 Cl Mg. SO 4 + NH 4 OH + Na 2 HPO 4 Mg. NH 4 PO 4 ↓ + Na 2 SO 4 + H 2 O белый осадок Чистота: Не должно быть посторонних примесей. Определяется кислотность или щелочность. Хлориды, тяжелые металлы, железо, мышьяк в пределе эталона. Потеря в весе при прокаливании не более 52% (не менее 48%).
Подлинность: Определяется по катиону Mg 2+ и аниону SO 42 -. HCl 1. Mg. SO 4 + Ba. Cl 2 Ba. SO 4 ↓ + Mg. Cl 2 белый осадок, не растворим в кислотах и щелочах 2. К раствору препарата прибавляют раствор хлорид аммония, раствор гидрофосфат натрия, раствор гидроксида аммония, образуется белый кристаллический осадок, растворимый в уксусной кислоте. NH 4 Cl Mg. SO 4 + NH 4 OH + Na 2 HPO 4 Mg. NH 4 PO 4 ↓ + Na 2 SO 4 + H 2 O белый осадок Чистота: Не должно быть посторонних примесей. Определяется кислотность или щелочность. Хлориды, тяжелые металлы, железо, мышьяк в пределе эталона. Потеря в весе при прокаливании не более 52% (не менее 48%).
 Количественное определение: 1) Комплексонометрический метод. Этим методом определяются препараты, содержащие в своем составе катионы двух, трех- валентных элементов, с которыми трилон Б (рабочий раствор) образует комплексы устойчивые, не окрашенные и растворимые в воде. Титрование проводят в среде аммиачного буфера (гидроксид аммония и хлорид аммония). Индикаторы, применяющиеся при комплексонометрическом титровании называются металл – индикаторами. К ним относятся: кислотный хром темно – синий, кислотный хром черный специальный (эриохром черный Т), мурексид и т. д. Эти вещества обладают способностью образовывать с определенными металлами окрашенные комплексные соединения, неустойчивые, растворимые в воде. Методика: Навеску препарата растворяют в воде, прибавляют аммиачный буфер, затем несколько кристалликов кислотного хром черного – образуется хорошо растворимое в воде, окрашенное в красный цвет комплексное соединение. В точке эквивалентности комплекс катиона с индикатором, как менее стойкий, полностью распадается и раствор приобретает окраску свободного индикатора – синий цвет.
Количественное определение: 1) Комплексонометрический метод. Этим методом определяются препараты, содержащие в своем составе катионы двух, трех- валентных элементов, с которыми трилон Б (рабочий раствор) образует комплексы устойчивые, не окрашенные и растворимые в воде. Титрование проводят в среде аммиачного буфера (гидроксид аммония и хлорид аммония). Индикаторы, применяющиеся при комплексонометрическом титровании называются металл – индикаторами. К ним относятся: кислотный хром темно – синий, кислотный хром черный специальный (эриохром черный Т), мурексид и т. д. Эти вещества обладают способностью образовывать с определенными металлами окрашенные комплексные соединения, неустойчивые, растворимые в воде. Методика: Навеску препарата растворяют в воде, прибавляют аммиачный буфер, затем несколько кристалликов кислотного хром черного – образуется хорошо растворимое в воде, окрашенное в красный цвет комплексное соединение. В точке эквивалентности комплекс катиона с индикатором, как менее стойкий, полностью распадается и раствор приобретает окраску свободного индикатора – синий цвет.
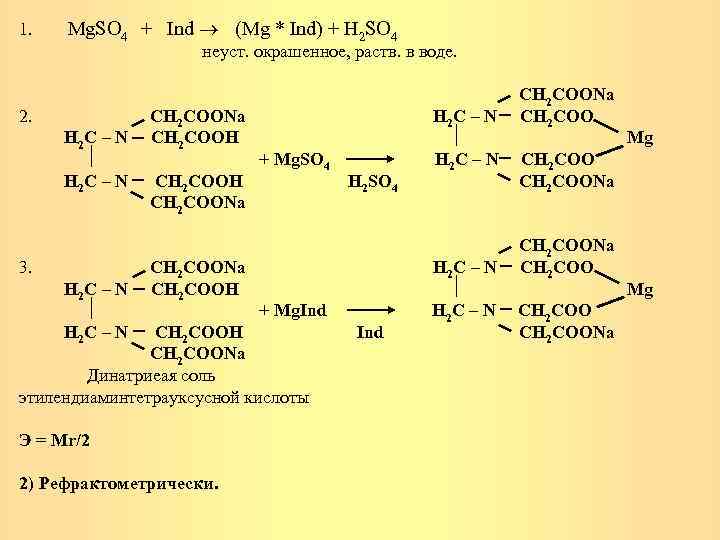 1. Mg. SO 4 + Ind (Mg * Ind) + H 2 SO 4 неуст. окрашенное, раств. в воде. CH 2 COONa 2. CH 2 COONa H 2 C – N CH 2 COOH Mg + Mg. SO 4 H 2 C – N CH 2 COOH H 2 SO 4 CH 2 COONa CH 2 COONa 3. CH 2 COONa H 2 C – N CH 2 COOH Mg + Mg. Ind H 2 C – N CH 2 COOH Ind CH 2 COONa Динатриеая соль этилендиаминтетрауксусной кислоты Э = Мr/2 2) Рефрактометрически.
1. Mg. SO 4 + Ind (Mg * Ind) + H 2 SO 4 неуст. окрашенное, раств. в воде. CH 2 COONa 2. CH 2 COONa H 2 C – N CH 2 COOH Mg + Mg. SO 4 H 2 C – N CH 2 COOH H 2 SO 4 CH 2 COONa CH 2 COONa 3. CH 2 COONa H 2 C – N CH 2 COOH Mg + Mg. Ind H 2 C – N CH 2 COOH Ind CH 2 COONa Динатриеая соль этилендиаминтетрауксусной кислоты Э = Мr/2 2) Рефрактометрически.
 Применение: 1. Слабительное – внутрь 15, 0 - 30, 0 на прием. 2. При парентеральном введении оказывает успокаивающее действие на ЦНС, при увеличении концентрации в крови оказывает снотворное действие. Большие концентрации могут вызвать угнетение дыхания. Принимают также как спазмолитическое средство при гипертонической болезни подкожно – 5% раствор. 3. Как желчегонное внутрь 20 -25% раствор. Хранение: в хорошо укупоренной таре.
Применение: 1. Слабительное – внутрь 15, 0 - 30, 0 на прием. 2. При парентеральном введении оказывает успокаивающее действие на ЦНС, при увеличении концентрации в крови оказывает снотворное действие. Большие концентрации могут вызвать угнетение дыхания. Принимают также как спазмолитическое средство при гипертонической болезни подкожно – 5% раствор. 3. Как желчегонное внутрь 20 -25% раствор. Хранение: в хорошо укупоренной таре.
 КАЛЬЦИЯ ХЛОРИД CALCII CHLORIDUM Ca. Cl 2 • 6 H 2 O
КАЛЬЦИЯ ХЛОРИД CALCII CHLORIDUM Ca. Cl 2 • 6 H 2 O
 Получение: Получают в результате обработки карбоната кальция (мрамора) соляной кислотой. Ca. CO 3 + 2 HCl Ca. Cl 2 + CO 2↑ + H 2 O Очищают путем перекристаллизации из водного раствора. Свойства: Бесцветные призматические кристаллы без запаха, горько – соленого вкуса. Очень гигроскопичен, на воздухе расплывается. Очень легко растворим в воде, вызывая при этом сильное охлаждение раствора, легко растворим в 95% спирте. р. Н – нейтральная. Крайняя гигроскопичность препарата, способность его расплываться под влиянием влаги делают состав соли непостоянным, что может привести к неточной дозировке при изготовлении лекарств с хлоридом кальция. Учитывая это в аптеке готовят 50% концентрат.
Получение: Получают в результате обработки карбоната кальция (мрамора) соляной кислотой. Ca. CO 3 + 2 HCl Ca. Cl 2 + CO 2↑ + H 2 O Очищают путем перекристаллизации из водного раствора. Свойства: Бесцветные призматические кристаллы без запаха, горько – соленого вкуса. Очень гигроскопичен, на воздухе расплывается. Очень легко растворим в воде, вызывая при этом сильное охлаждение раствора, легко растворим в 95% спирте. р. Н – нейтральная. Крайняя гигроскопичность препарата, способность его расплываться под влиянием влаги делают состав соли непостоянным, что может привести к неточной дозировке при изготовлении лекарств с хлоридом кальция. Учитывая это в аптеке готовят 50% концентрат.
 Подлинность: 1. Соли кальция окрашивают бесцветное пламя горелки в кирпично- красный цвет. 2. С оксалатом аммония. NH 4 OH Ca. Cl 2 + (NH 4)2 C 2 O 4 Ca. C 2 O 4↓ + 2 NH 4 Cl белый осадок, растворим в минеральных кислотах, не растворим в уксусной кислоте • На Cl 1. HNO 3 2. Ca. Cl 2 + 2 Ag. NO 3 2 Ag. Cl↓ + Ca(NO 3)2 белый осадок, 3. 4. растворим в растворе 5. аммиака
Подлинность: 1. Соли кальция окрашивают бесцветное пламя горелки в кирпично- красный цвет. 2. С оксалатом аммония. NH 4 OH Ca. Cl 2 + (NH 4)2 C 2 O 4 Ca. C 2 O 4↓ + 2 NH 4 Cl белый осадок, растворим в минеральных кислотах, не растворим в уксусной кислоте • На Cl 1. HNO 3 2. Ca. Cl 2 + 2 Ag. NO 3 2 Ag. Cl↓ + Ca(NO 3)2 белый осадок, 3. 4. растворим в растворе 5. аммиака
 Количественное определение: 1. Комплексонометрический метод. Точную навеску препарата растворяют в воде прибавляют аммиачно – буферную смесь. Индикатор – кислотный хром темно – синий и титруют 0, 05 М раствором трилона Б до синего окрашивания. Ca. Cl 2 + Ind (Ca * Ind) + HCl неуст. окрашенное, раств. в воде. CH 2 COONa 2. CH 2 COONa H 2 C – N CH 2 COOH Ca + Ca. Cl 2 H 2 C – N CH 2 COO 1. H 2 C – N CH 2 COOH HCl CH 2 COONa 2. CH 2 COONa 3. CH 2 COONa 4. 3. CH 2 COONa H 2 C – N CH 2 COO 5. H 2 C – N CH 2 COOH Ca 6. + Ca. Ind H 2 C – N CH 2 COO 7. H 2 C – N CH 2 COOH H 2 Ind CH 2 COONa 8. CH 2 COONa 9. Динатриеая соль 10. этилендиаминтетрауксусной кислоты 11. Э = Мr/2
Количественное определение: 1. Комплексонометрический метод. Точную навеску препарата растворяют в воде прибавляют аммиачно – буферную смесь. Индикатор – кислотный хром темно – синий и титруют 0, 05 М раствором трилона Б до синего окрашивания. Ca. Cl 2 + Ind (Ca * Ind) + HCl неуст. окрашенное, раств. в воде. CH 2 COONa 2. CH 2 COONa H 2 C – N CH 2 COOH Ca + Ca. Cl 2 H 2 C – N CH 2 COO 1. H 2 C – N CH 2 COOH HCl CH 2 COONa 2. CH 2 COONa 3. CH 2 COONa 4. 3. CH 2 COONa H 2 C – N CH 2 COO 5. H 2 C – N CH 2 COOH Ca 6. + Ca. Ind H 2 C – N CH 2 COO 7. H 2 C – N CH 2 COOH H 2 Ind CH 2 COONa 8. CH 2 COONa 9. Динатриеая соль 10. этилендиаминтетрауксусной кислоты 11. Э = Мr/2
 Возможные методы: 2. Метод Мора 3. Метод Фаянса 4. Меркуриметрический метод 5. Метод Фольгарда 6. Рефрактометрический метод Применение: Источник ионов кальция, антиаллергическое средство. Проивовоспалительное средство, кровоостанавливающее, угнетает процесс свертывания крови. Внутрь 5 -10% раствор, в/в 10% Хранение: В хорошо укупоренных стеклянных банках, с пробками, залитыми парафином, с сухом месте. Срок годности: 5 лет.
Возможные методы: 2. Метод Мора 3. Метод Фаянса 4. Меркуриметрический метод 5. Метод Фольгарда 6. Рефрактометрический метод Применение: Источник ионов кальция, антиаллергическое средство. Проивовоспалительное средство, кровоостанавливающее, угнетает процесс свертывания крови. Внутрь 5 -10% раствор, в/в 10% Хранение: В хорошо укупоренных стеклянных банках, с пробками, залитыми парафином, с сухом месте. Срок годности: 5 лет.
 ЦИНКА СУЛЬФАТ. ZINCI SULFAS. Zn. SO 4 • 7 H 2 O
ЦИНКА СУЛЬФАТ. ZINCI SULFAS. Zn. SO 4 • 7 H 2 O
 Получение: Получают путем растворения цинка или его оксида в разбавленной серной кислоте. Затем производят соответствующую очистку. Zn + H 2 SO 4 Zn. SO 4 + H 2 Zn. О + H 2 SO 4 Zn. SO 4 + H 2 О Свойства: Бесцветные, прозрачные кристаллы или мелкокристаллический порошок, вяжущего вкуса, без запаха, при нагревании плавится, при дальнейшем нагревании переходит в твердую массу. Очень легко растворимый в воде, медленно в глицерине, нерастворим в спирте. Водный раствор имеет слабокислую реакцию. На воздухе выветривается.
Получение: Получают путем растворения цинка или его оксида в разбавленной серной кислоте. Затем производят соответствующую очистку. Zn + H 2 SO 4 Zn. SO 4 + H 2 Zn. О + H 2 SO 4 Zn. SO 4 + H 2 О Свойства: Бесцветные, прозрачные кристаллы или мелкокристаллический порошок, вяжущего вкуса, без запаха, при нагревании плавится, при дальнейшем нагревании переходит в твердую массу. Очень легко растворимый в воде, медленно в глицерине, нерастворим в спирте. Водный раствор имеет слабокислую реакцию. На воздухе выветривается.
 Подлинность: 1. С ферроцианидом калия образует белый студенистый осадок, не растворяется в разведенной хлороводородной кислоте. 3 Zn. SO 4 + 2 K 4[Fe(CN)6] K 2 Zn 3[Fe(CN)6]2 + 3 K 2 SO 4 желтая кровяная соль 2. С сульфидом натрия образует белый осадок, нерастворимый в уксусной кислоте, легко растворим в разведенной хлороводородной кислоте. Zn. SO 4 + Na 2 S Zn. S + Na 2 SO 4 3. С хлоридом бария образует белый осадок, нерастворимый в разведенных кислотах и щелочах. Zn. SO 4 + Ba. CI 2 Ba. SO 4 + Zn. CI 2 Чистота: Не должно быть нитратов, солей алюминия, железа, меди, кальция, хлориды и мышьяк в пределе эталона.
Подлинность: 1. С ферроцианидом калия образует белый студенистый осадок, не растворяется в разведенной хлороводородной кислоте. 3 Zn. SO 4 + 2 K 4[Fe(CN)6] K 2 Zn 3[Fe(CN)6]2 + 3 K 2 SO 4 желтая кровяная соль 2. С сульфидом натрия образует белый осадок, нерастворимый в уксусной кислоте, легко растворим в разведенной хлороводородной кислоте. Zn. SO 4 + Na 2 S Zn. S + Na 2 SO 4 3. С хлоридом бария образует белый осадок, нерастворимый в разведенных кислотах и щелочах. Zn. SO 4 + Ba. CI 2 Ba. SO 4 + Zn. CI 2 Чистота: Не должно быть нитратов, солей алюминия, железа, меди, кальция, хлориды и мышьяк в пределе эталона.
 Количественное определение: Комплексонометрический метод. Точную навеску препарата растворяют в воде, прибавляют аммиачно – буферную смесь, индикатор – кислотный хром темно – синий и титруют 0, 05 М раствором трилона Б до синего окрашивания. 1. Zn. SO 4 + Ind (Zn * Ind) + H 2 SO 4 Комплексное соединение неустойчивое, растворимое в воде, вишнево – красного цвета. CH 2 COONa 2. CH 2 COONa H 2 C – N CH 2 COOH Zn + Zn. SO 4 H 2 C – N CH 2 COOH H 2 SO 4 CH 2 COONa CH 2 COONa 3. CH 2 COONa H 2 C – N CH 2 COOH Zn + Zn. Ind H 2 C – N CH 2 COOH H 2 Ind CH 2 COONa Динатриеая соль этилендиаминтетрауксусной кислоты Э = Мr/2
Количественное определение: Комплексонометрический метод. Точную навеску препарата растворяют в воде, прибавляют аммиачно – буферную смесь, индикатор – кислотный хром темно – синий и титруют 0, 05 М раствором трилона Б до синего окрашивания. 1. Zn. SO 4 + Ind (Zn * Ind) + H 2 SO 4 Комплексное соединение неустойчивое, растворимое в воде, вишнево – красного цвета. CH 2 COONa 2. CH 2 COONa H 2 C – N CH 2 COOH Zn + Zn. SO 4 H 2 C – N CH 2 COOH H 2 SO 4 CH 2 COONa CH 2 COONa 3. CH 2 COONa H 2 C – N CH 2 COOH Zn + Zn. Ind H 2 C – N CH 2 COOH H 2 Ind CH 2 COONa Динатриеая соль этилендиаминтетрауксусной кислоты Э = Мr/2
 Применение: В глазных каплях 0, 25% и 0, 5% растворы, как антисептическое и вяжущее средство применяется вместе с борной кислотой. В гинекологической практике 0, 1% и 0, 5% растворы для спринцеваний. Хранение: Сп. Б. В хорошо укупоренной таре, предохраняющей от выветривания.
Применение: В глазных каплях 0, 25% и 0, 5% растворы, как антисептическое и вяжущее средство применяется вместе с борной кислотой. В гинекологической практике 0, 1% и 0, 5% растворы для спринцеваний. Хранение: Сп. Б. В хорошо укупоренной таре, предохраняющей от выветривания.


