lec11-IN-ВПТ-ХТТ.ppt
- Количество слайдов: 27
 Лекция 11. СИНТЕЗ НАНОСЛОЕВ НЕОРГАНИЧЕСКИХ СОЕДИНЕНИЙ МЕТОДАМИ ИОННОГО И ИОННОМОЛЕКУЛЯРНОГО НАСЛАИВАНИЯ
Лекция 11. СИНТЕЗ НАНОСЛОЕВ НЕОРГАНИЧЕСКИХ СОЕДИНЕНИЙ МЕТОДАМИ ИОННОГО И ИОННОМОЛЕКУЛЯРНОГО НАСЛАИВАНИЯ
 Синтезы нанослоев методом ионного наслаивания (ИН) с участием растворов реагентов были независимо описаны на примере слоев Zn. S и Mn. O 2 соответственно в патентах Y. F. Nicolau и В. П. Толстого и др. , выполненных в середине 80 -х годов. Ими были найдены условия проведения реакций алсорбции, при которых на поверхности подложки на каждой стадии синтеза происходит последовательная адсорбция катионов и анионов, образующих при взаимодействии вещество синтезируемого слоя. Англоязычным вариантом названия данного метода синтеза являются - Successive Ionic Layer Deposition (SILD) или Successive Ionic Layer Adsorption and Reaction (SILAR), а также Layer-by-Layer (Lb. L) synthesis. Кроме стадий адсорбции непременным условием синтеза слоев этим методом является проведение после каждой стадии адсорбции реагентов стадии удаления их избытка и продуктов реакций, например промывкой образца растворителем. Действительно, если не проводить стадию удаления избытка реагентов, то синтез слоя будет проходить в условиях, аналогичных условиям смесевого режима и толщину растущего слоя не удастся прецизионно контролировать.
Синтезы нанослоев методом ионного наслаивания (ИН) с участием растворов реагентов были независимо описаны на примере слоев Zn. S и Mn. O 2 соответственно в патентах Y. F. Nicolau и В. П. Толстого и др. , выполненных в середине 80 -х годов. Ими были найдены условия проведения реакций алсорбции, при которых на поверхности подложки на каждой стадии синтеза происходит последовательная адсорбция катионов и анионов, образующих при взаимодействии вещество синтезируемого слоя. Англоязычным вариантом названия данного метода синтеза являются - Successive Ionic Layer Deposition (SILD) или Successive Ionic Layer Adsorption and Reaction (SILAR), а также Layer-by-Layer (Lb. L) synthesis. Кроме стадий адсорбции непременным условием синтеза слоев этим методом является проведение после каждой стадии адсорбции реагентов стадии удаления их избытка и продуктов реакций, например промывкой образца растворителем. Действительно, если не проводить стадию удаления избытка реагентов, то синтез слоя будет проходить в условиях, аналогичных условиям смесевого режима и толщину растущего слоя не удастся прецизионно контролировать.
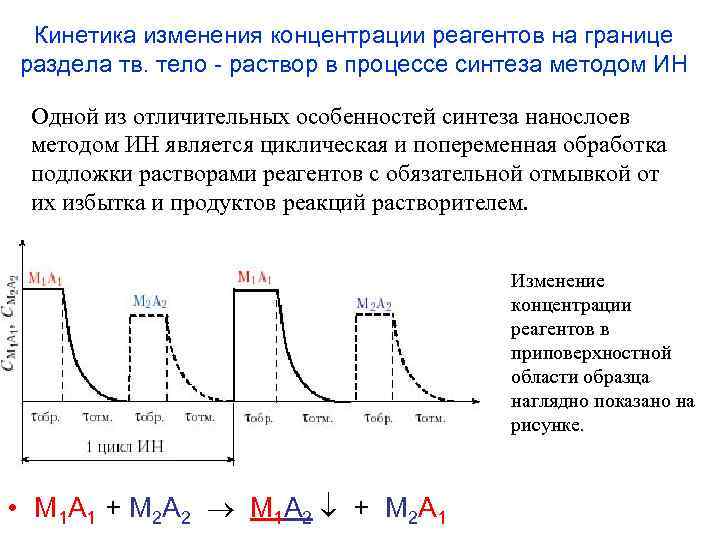 Кинетика изменения концентрации реагентов на границе раздела тв. тело - раствор в процессе синтеза методом ИН Одной из отличительных особенностей синтеза нанослоев методом ИН является циклическая и попеременная обработка подложки растворами реагентов с обязательной отмывкой от их избытка и продуктов реакций растворителем. Изменение концентрации реагентов в приповерхностной области образца наглядно показано на рисунке. • M 1 A 1 + M 2 A 2 M 1 A 2 + M 2 A 1
Кинетика изменения концентрации реагентов на границе раздела тв. тело - раствор в процессе синтеза методом ИН Одной из отличительных особенностей синтеза нанослоев методом ИН является циклическая и попеременная обработка подложки растворами реагентов с обязательной отмывкой от их избытка и продуктов реакций растворителем. Изменение концентрации реагентов в приповерхностной области образца наглядно показано на рисунке. • M 1 A 1 + M 2 A 2 M 1 A 2 + M 2 A 1
 Адсорбция ионов на поверхности подложки и синтез первого нанослоя При синтезе методом ИН в результате первого цикла обработки реагентами на поверхности должно происходить образования внутри- или внешнесферного комплекса, который при удалении избытка реагентов промывкой не разрушается. Если при выбранных для синтеза значениях р. Н растворов подложка имеет отрицательный заряд, то в качестве первого реагента при синтезе используют раствор соли, катион которой входит в состав синтезируемого слоя, а если заряд положительный, то раствор соли с анионом, входящим в состав слоя. Внутри-сферные компл Внешне-сферные компл 4
Адсорбция ионов на поверхности подложки и синтез первого нанослоя При синтезе методом ИН в результате первого цикла обработки реагентами на поверхности должно происходить образования внутри- или внешнесферного комплекса, который при удалении избытка реагентов промывкой не разрушается. Если при выбранных для синтеза значениях р. Н растворов подложка имеет отрицательный заряд, то в качестве первого реагента при синтезе используют раствор соли, катион которой входит в состав синтезируемого слоя, а если заряд положительный, то раствор соли с анионом, входящим в состав слоя. Внутри-сферные компл Внешне-сферные компл 4
 Схемы реакций, протекающих на поверхности на каждой стадии обработки подложки в растворах при синтезе нанослоев методом ИН I. [M]OH + M 1 A 1 [M]OM 1 aq+n-1. (M 1 A 1)ads + H+ II. [M]OM 1 aq+n-1. (M 1 A 1)ads + пром. (H 2 O) [M]OM 1 aq(OH)n-1 III. [M]OM 1(OH)n-1 + M 2 A 2 [M]OM 1 A 2(n-1)/k (M 2 A 2)ads IV. [M]OM 1 A 2(n-1)/k (M 2 A 2)ads+ пром. (H 2 O) [M]OM 1 A 2(n-1)/k [M]OH + {M 1 A 1(I) + H 2 O(II) + M 2 A 2(III) + H 2 O(IV)}N [M]O(M 1 A 2(n-1)/k)N N -число циклов ИН M 1 - Ag+, Zn 2+, Cd 2+, Cu 2+, Hg 2+, In 3+, Bi 3+ и др. , A 1 - NO 3 -, Cl- и др. A 2 - F-, S 2 -, Se 2 - и др. , M 2 - Na+, K+, NH 4+ и др. I. - обработка в растворе катион-содержащего реагента, II. - обработка в растворителе, III. - обработка в растворе анион-содержащего реагента, IV. - … вновь в растворителе. 5
Схемы реакций, протекающих на поверхности на каждой стадии обработки подложки в растворах при синтезе нанослоев методом ИН I. [M]OH + M 1 A 1 [M]OM 1 aq+n-1. (M 1 A 1)ads + H+ II. [M]OM 1 aq+n-1. (M 1 A 1)ads + пром. (H 2 O) [M]OM 1 aq(OH)n-1 III. [M]OM 1(OH)n-1 + M 2 A 2 [M]OM 1 A 2(n-1)/k (M 2 A 2)ads IV. [M]OM 1 A 2(n-1)/k (M 2 A 2)ads+ пром. (H 2 O) [M]OM 1 A 2(n-1)/k [M]OH + {M 1 A 1(I) + H 2 O(II) + M 2 A 2(III) + H 2 O(IV)}N [M]O(M 1 A 2(n-1)/k)N N -число циклов ИН M 1 - Ag+, Zn 2+, Cd 2+, Cu 2+, Hg 2+, In 3+, Bi 3+ и др. , A 1 - NO 3 -, Cl- и др. A 2 - F-, S 2 -, Se 2 - и др. , M 2 - Na+, K+, NH 4+ и др. I. - обработка в растворе катион-содержащего реагента, II. - обработка в растворителе, III. - обработка в растворе анион-содержащего реагента, IV. - … вновь в растворителе. 5
 Выбор оптим. условий синтеза нанослоев методом ИН Первые эксперименты показали, что для большинства составов после адсорбции реагента на стадии промывки образца растворителем наблюдается удаление с поверхности не только избытка реагента и продуктов реакций, но части или всего исходного адсорбированного слоя. Определение условий синтеза методом ИН, таким образом, представляет сравнительно сложную задачу, поскольку, несмотря на простоту операций с учетом многостадийности процесса приходится контролировать 10 и более условий синтеза, включая концентрацию и р. Н нескольких растворов реагентов, р. Н промывных жидкостей, время обработки ими и т. д. (I) (III) (IV) 6
Выбор оптим. условий синтеза нанослоев методом ИН Первые эксперименты показали, что для большинства составов после адсорбции реагента на стадии промывки образца растворителем наблюдается удаление с поверхности не только избытка реагента и продуктов реакций, но части или всего исходного адсорбированного слоя. Определение условий синтеза методом ИН, таким образом, представляет сравнительно сложную задачу, поскольку, несмотря на простоту операций с учетом многостадийности процесса приходится контролировать 10 и более условий синтеза, включая концентрацию и р. Н нескольких растворов реагентов, р. Н промывных жидкостей, время обработки ими и т. д. (I) (III) (IV) 6
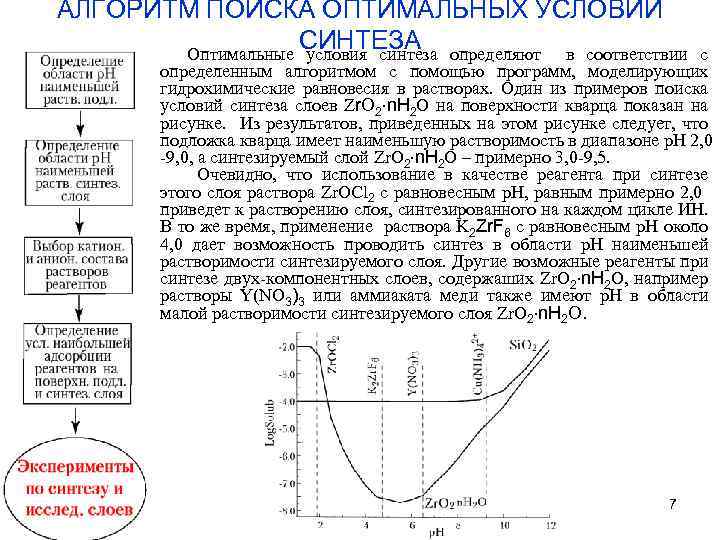 АЛГОРИТМ ПОИСКА ОПТИМАЛЬНЫХ УСЛОВИЙ СИНТЕЗА Оптимальные условия синтеза определяют в соответствии с определенным алгоритмом с помощью программ, моделирующих гидрохимические равновесия в растворах. Один из примеров поиска условий синтеза слоев Zr. O 2 n. H 2 O на поверхности кварца показан на рисунке. Из результатов, приведенных на этом рисунке следует, что подложка кварца имеет наименьшую растворимость в диапазоне р. Н 2, 0 -9, 0, а синтезируемый слой Zr. O 2 n. H 2 O – примерно 3, 0 -9, 5. Очевидно, что использование в качестве реагента при синтезе этого слоя раствора Zr. OCl 2 с равновесным р. Н, равным примерно 2, 0 приведет к растворению слоя, синтезированного на каждом цикле ИН. В то же время, применение раствора K 2 Zr. F 6 с равновесным р. Н около 4, 0 дает возможность проводить синтез в области р. Н наименьшей растворимости синтезируемого слоя. Другие возможные реагенты при синтезе двух-компонентных слоев, содержаших Zr. O 2 n. H 2 O, например растворы Y(NO 3)3 или аммиаката меди также имеют р. Н в области малой растворимости синтезируемого слоя Zr. O 2 n. H 2 O. 7
АЛГОРИТМ ПОИСКА ОПТИМАЛЬНЫХ УСЛОВИЙ СИНТЕЗА Оптимальные условия синтеза определяют в соответствии с определенным алгоритмом с помощью программ, моделирующих гидрохимические равновесия в растворах. Один из примеров поиска условий синтеза слоев Zr. O 2 n. H 2 O на поверхности кварца показан на рисунке. Из результатов, приведенных на этом рисунке следует, что подложка кварца имеет наименьшую растворимость в диапазоне р. Н 2, 0 -9, 0, а синтезируемый слой Zr. O 2 n. H 2 O – примерно 3, 0 -9, 5. Очевидно, что использование в качестве реагента при синтезе этого слоя раствора Zr. OCl 2 с равновесным р. Н, равным примерно 2, 0 приведет к растворению слоя, синтезированного на каждом цикле ИН. В то же время, применение раствора K 2 Zr. F 6 с равновесным р. Н около 4, 0 дает возможность проводить синтез в области р. Н наименьшей растворимости синтезируемого слоя. Другие возможные реагенты при синтезе двух-компонентных слоев, содержаших Zr. O 2 n. H 2 O, например растворы Y(NO 3)3 или аммиаката меди также имеют р. Н в области малой растворимости синтезируемого слоя Zr. O 2 n. H 2 O. 7
 Многообразные реакции синтеза методом ИН могут быть разделены на различные группы в соответствии с основными типами реакций катионов и анионов в растворах. Изложим с этой точки зрения полученный к настоящему времени экспериментальный материал более детально. Прежде всего, отметим, что среди возможных реакций ИН основную группу составляют реакции, которые протекают на поверхности при взаимодействии адсорбированного катиона (аниона) с анионом (катионом), находящимся в растворе. При этом степень окисления катионов и анионов не изменяется. Если в результате такой реакции образуется труднорастворимое соединение, то на поверхности возникает его нанослой. К числу таких реакций относится, например, реакция взаимодействия адсорбированных аква-комплексов Zn 2+ с анионами HS-. В результате взаимодействия возникает прочная связь Zn. S и молекулы воды “выдавливаются” из координационной сферы катионов цинка. После высушивания с поверхности удаляются молекулы воды и несмотря на то, что синтез проходил в водном растворе, образуется слой безводного Zn. S. Наряду с реакциями, протекающих без изменения степени окисления взаимодействующих ионов можно выделить реакции ИН, в которых наблюдаются окислительно-восстановительные процессы и среди них выделить несколько групп, в частности, реакции, в которых адсорбированный катион окисляется (Sn 2+ Sn 4+), адсорбированный катион восстанавливается (Ag+ Ag 0), адсорбированный анион восстанавливается (Cr 2 O 72 - Cr 3+) и т. д. . При этом участвующие в реакции и находящиеся в растворе молекулы или ионы окислителя и восстановителя не входят в состав образующегося слоя. Другую группу составляют окислительно-восстановительные реакции в результате которых окислитель или восстановитель из раствора, а возможно и продукт его химического превращения включается в состав слоя и на поверхности образуется многокомпонентный нанослой (Sn 2+ + Mo. O 42 - Snx. Mo. Oy). Многочисленную группу составляют также своеобразные “сопряженные” реакции ИН, при проведении которых на поверхности происходит окислительно-восстановительная реакция одного из отмеченного типов и реакция адсорбции других катионов или анионов с образованием труднорастворимого соединения, например при обработке адсорбированного слоя Ce 3+ раствором, содержащим H 2 O 2 и OH- реакции Ce 3+ Ce 4+ и адсорбции H 2 O 2 и OH-8 с образованием нанослоя -Ce(OH)2 OOH
Многообразные реакции синтеза методом ИН могут быть разделены на различные группы в соответствии с основными типами реакций катионов и анионов в растворах. Изложим с этой точки зрения полученный к настоящему времени экспериментальный материал более детально. Прежде всего, отметим, что среди возможных реакций ИН основную группу составляют реакции, которые протекают на поверхности при взаимодействии адсорбированного катиона (аниона) с анионом (катионом), находящимся в растворе. При этом степень окисления катионов и анионов не изменяется. Если в результате такой реакции образуется труднорастворимое соединение, то на поверхности возникает его нанослой. К числу таких реакций относится, например, реакция взаимодействия адсорбированных аква-комплексов Zn 2+ с анионами HS-. В результате взаимодействия возникает прочная связь Zn. S и молекулы воды “выдавливаются” из координационной сферы катионов цинка. После высушивания с поверхности удаляются молекулы воды и несмотря на то, что синтез проходил в водном растворе, образуется слой безводного Zn. S. Наряду с реакциями, протекающих без изменения степени окисления взаимодействующих ионов можно выделить реакции ИН, в которых наблюдаются окислительно-восстановительные процессы и среди них выделить несколько групп, в частности, реакции, в которых адсорбированный катион окисляется (Sn 2+ Sn 4+), адсорбированный катион восстанавливается (Ag+ Ag 0), адсорбированный анион восстанавливается (Cr 2 O 72 - Cr 3+) и т. д. . При этом участвующие в реакции и находящиеся в растворе молекулы или ионы окислителя и восстановителя не входят в состав образующегося слоя. Другую группу составляют окислительно-восстановительные реакции в результате которых окислитель или восстановитель из раствора, а возможно и продукт его химического превращения включается в состав слоя и на поверхности образуется многокомпонентный нанослой (Sn 2+ + Mo. O 42 - Snx. Mo. Oy). Многочисленную группу составляют также своеобразные “сопряженные” реакции ИН, при проведении которых на поверхности происходит окислительно-восстановительная реакция одного из отмеченного типов и реакция адсорбции других катионов или анионов с образованием труднорастворимого соединения, например при обработке адсорбированного слоя Ce 3+ раствором, содержащим H 2 O 2 и OH- реакции Ce 3+ Ce 4+ и адсорбции H 2 O 2 и OH-8 с образованием нанослоя -Ce(OH)2 OOH
 Классификация реакций на поверхности в процессе синтеза методом ИН • Реакции без изменения степени окисления адсорбированных ионов (In 3+ + H 2 S In 2 S 3). • Реакции с изменением степени окисления адсорбир. катионов или анионов: - окисления адсорб. катионов (Fe 2+ + H 2 O 2 Fe. OOH), - восстановления адсорб. катионов (Ag+ + red Ag 0), - последоват. ок. и восст. адсорб. кат. (Fe 2+ +Cu 2+ Fex. Cu(OH)y, ) - восстановления адсорб. анионов (Cr. O 42 - + red Cr(OH)3), • Сопряженные реакции, включающие стадии ок. или восст. ионов и реакц. адсорб. (Ce 3++ H 2 O 2 Ce(OH)4 -x(OOH)x)
Классификация реакций на поверхности в процессе синтеза методом ИН • Реакции без изменения степени окисления адсорбированных ионов (In 3+ + H 2 S In 2 S 3). • Реакции с изменением степени окисления адсорбир. катионов или анионов: - окисления адсорб. катионов (Fe 2+ + H 2 O 2 Fe. OOH), - восстановления адсорб. катионов (Ag+ + red Ag 0), - последоват. ок. и восст. адсорб. кат. (Fe 2+ +Cu 2+ Fex. Cu(OH)y, ) - восстановления адсорб. анионов (Cr. O 42 - + red Cr(OH)3), • Сопряженные реакции, включающие стадии ок. или восст. ионов и реакц. адсорб. (Ce 3++ H 2 O 2 Ce(OH)4 -x(OOH)x)
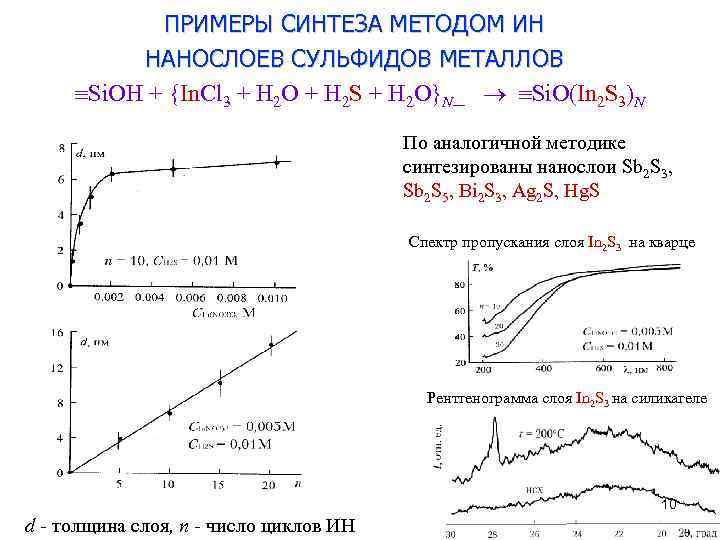 ПРИМЕРЫ СИНТЕЗА МЕТОДОМ ИН НАНОСЛОЕВ СУЛЬФИДОВ МЕТАЛЛОВ Si. OH + {In. Cl 3 + H 2 O + H 2 S + H 2 O}N_ Si. O(In 2 S 3)N По аналогичной методике синтезированы нанослои Sb 2 S 3, Sb 2 S 5, Bi 2 S 3, Ag 2 S, Hg. S Спектр пропускания слоя In 2 S 3 на кварце Рентгенограмма слоя In 2 S 3 на силикагеле 10 d - толщина слоя, n - число циклов ИН
ПРИМЕРЫ СИНТЕЗА МЕТОДОМ ИН НАНОСЛОЕВ СУЛЬФИДОВ МЕТАЛЛОВ Si. OH + {In. Cl 3 + H 2 O + H 2 S + H 2 O}N_ Si. O(In 2 S 3)N По аналогичной методике синтезированы нанослои Sb 2 S 3, Sb 2 S 5, Bi 2 S 3, Ag 2 S, Hg. S Спектр пропускания слоя In 2 S 3 на кварце Рентгенограмма слоя In 2 S 3 на силикагеле 10 d - толщина слоя, n - число циклов ИН
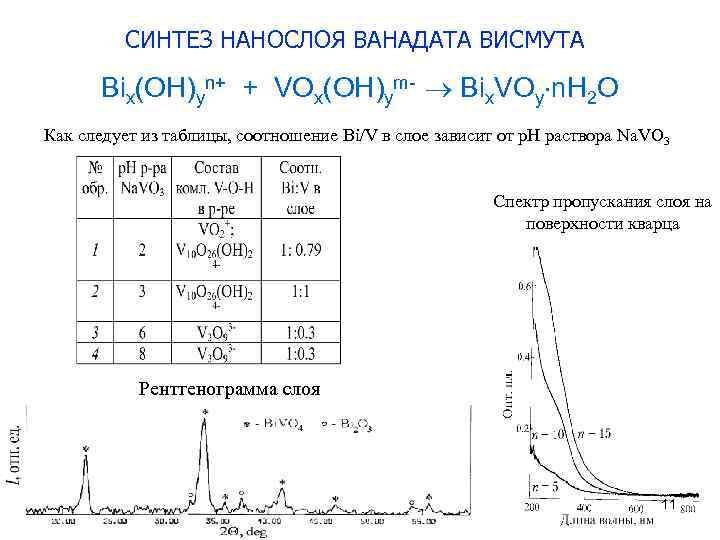 СИНТЕЗ НАНОСЛОЯ ВАНАДАТА ВИСМУТА Bix(OH)yn+ + VOx(OH)ym- Bix. VOy n. H 2 O Как следует из таблицы, соотношение Bi/V в слое зависит от р. Н раствора Na. VO 3 Спектр пропускания слоя на поверхности кварца Рентгенограмма слоя 11
СИНТЕЗ НАНОСЛОЯ ВАНАДАТА ВИСМУТА Bix(OH)yn+ + VOx(OH)ym- Bix. VOy n. H 2 O Как следует из таблицы, соотношение Bi/V в слое зависит от р. Н раствора Na. VO 3 Спектр пропускания слоя на поверхности кварца Рентгенограмма слоя 11
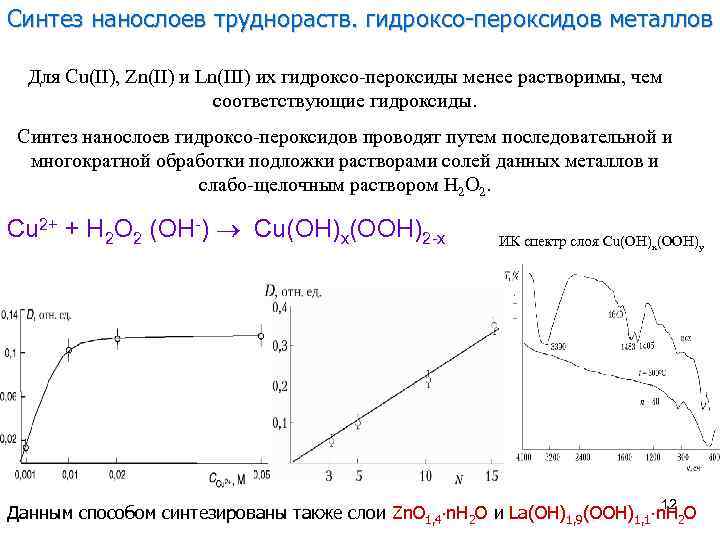 Синтез нанослоев труднораств. гидроксо-пероксидов металлов Для Cu(II), Zn(II) и Ln(III) их гидроксо-пероксиды менее растворимы, чем соответствующие гидроксиды. Синтез нанослоев гидроксо-пероксидов проводят путем последовательной и многократной обработки подложки растворами солей данных металлов и слабо-щелочным раствором H 2 O 2. Cu 2+ + H 2 O 2 (OH-) Cu(OH)x(OOH)2 -x ИК спектр слоя Cu(OH)x(OOH)y 12 Данным способом синтезированы также слои Zn. O 1, 4 n. H 2 O и La(OH)1, 9(OOH)1, 1 n. H 2 O
Синтез нанослоев труднораств. гидроксо-пероксидов металлов Для Cu(II), Zn(II) и Ln(III) их гидроксо-пероксиды менее растворимы, чем соответствующие гидроксиды. Синтез нанослоев гидроксо-пероксидов проводят путем последовательной и многократной обработки подложки растворами солей данных металлов и слабо-щелочным раствором H 2 O 2. Cu 2+ + H 2 O 2 (OH-) Cu(OH)x(OOH)2 -x ИК спектр слоя Cu(OH)x(OOH)y 12 Данным способом синтезированы также слои Zn. O 1, 4 n. H 2 O и La(OH)1, 9(OOH)1, 1 n. H 2 O
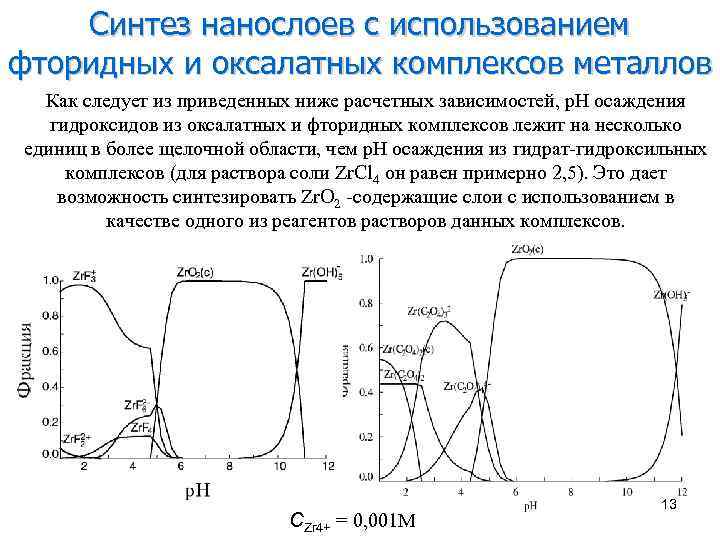 Синтез нанослоев с использованием фторидных и оксалатных комплексов металлов Как следует из приведенных ниже расчетных зависимостей, р. Н осаждения гидроксидов из оксалатных и фторидных комплексов лежит на несколько единиц в более щелочной области, чем р. Н осаждения из гидрат-гидроксильных комплексов (для раствора соли Zr. Cl 4 он равен примерно 2, 5). Это дает возможность синтезировать Zr. O 2 -содержащие слои с использованием в качестве одного из реагентов растворов данных комплексов. CZr 4+ = 0, 001 М 13
Синтез нанослоев с использованием фторидных и оксалатных комплексов металлов Как следует из приведенных ниже расчетных зависимостей, р. Н осаждения гидроксидов из оксалатных и фторидных комплексов лежит на несколько единиц в более щелочной области, чем р. Н осаждения из гидрат-гидроксильных комплексов (для раствора соли Zr. Cl 4 он равен примерно 2, 5). Это дает возможность синтезировать Zr. O 2 -содержащие слои с использованием в качестве одного из реагентов растворов данных комплексов. CZr 4+ = 0, 001 М 13
 СХЕМЫ РЕАКЦИЙ ПРИ СИНТЕЗЕ СЛОЯ Znx. Zr. Fy(OH)z. n. H 2 O 1. Si. O- + [Zn(NH 3)4]2+ Si. O[Zn(NH 3)4]+ [Zn(NH 3)4]2+изб 2. Si. O[Zn(NH 3)4]+ [Zn(NH 3)4]2+изб + промывка H 2 O Si. OZn. OH 3. Si. OZn. OH+ Zr. F 62 - Si. OZn. OH (Zr. F 62 -)адс (Zr. F 62 -)изб 4. Si. OZn. OH (Zr. F 62 -)адс (Zr. F 62 -)изб + промывка H 2 O Si. OZn. OH Zrx. Fy(OH)z 5. Si. OZn. OH Zrx. Fy(OH)z + [Zn(NH 3)4]2+ Si. OZn. OH Zrx 1 Fy 1(OH)z 1 [Zn(NH 3)4]2+адс [Zn(NH 3)4]2+изб и т. д. В результате проведения данных реакций на поверхности происходит образование слоя Znx. Zr. Fy(OH)z. n. H 2 O 14
СХЕМЫ РЕАКЦИЙ ПРИ СИНТЕЗЕ СЛОЯ Znx. Zr. Fy(OH)z. n. H 2 O 1. Si. O- + [Zn(NH 3)4]2+ Si. O[Zn(NH 3)4]+ [Zn(NH 3)4]2+изб 2. Si. O[Zn(NH 3)4]+ [Zn(NH 3)4]2+изб + промывка H 2 O Si. OZn. OH 3. Si. OZn. OH+ Zr. F 62 - Si. OZn. OH (Zr. F 62 -)адс (Zr. F 62 -)изб 4. Si. OZn. OH (Zr. F 62 -)адс (Zr. F 62 -)изб + промывка H 2 O Si. OZn. OH Zrx. Fy(OH)z 5. Si. OZn. OH Zrx. Fy(OH)z + [Zn(NH 3)4]2+ Si. OZn. OH Zrx 1 Fy 1(OH)z 1 [Zn(NH 3)4]2+адс [Zn(NH 3)4]2+изб и т. д. В результате проведения данных реакций на поверхности происходит образование слоя Znx. Zr. Fy(OH)z. n. H 2 O 14
 По аналогии были синтезированы и Cu- Zr(OH)x. Fy-содержащие слои NCu 0, 04 Zr(OH)y. F 0, 63 = 30 NZn 0, 08 Zr(OH)y. F 0, 32 = 3015
По аналогии были синтезированы и Cu- Zr(OH)x. Fy-содержащие слои NCu 0, 04 Zr(OH)y. F 0, 63 = 30 NZn 0, 08 Zr(OH)y. F 0, 32 = 3015
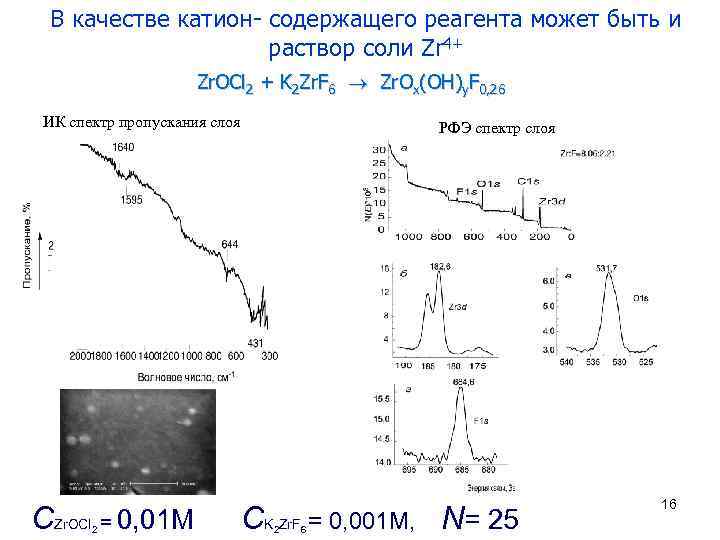 В качестве катион- содержащего реагента может быть и раствор соли Zr 4+ Zr. OCl 2 + K 2 Zr. F 6 Zr. Ox(OH)y. F 0, 26 ИК спектр пропускания слоя CZr. OCl = 0, 01 M 2 РФЭ спектр слоя CK Zr. F = 0, 001 M, N= 25 2 6 16
В качестве катион- содержащего реагента может быть и раствор соли Zr 4+ Zr. OCl 2 + K 2 Zr. F 6 Zr. Ox(OH)y. F 0, 26 ИК спектр пропускания слоя CZr. OCl = 0, 01 M 2 РФЭ спектр слоя CK Zr. F = 0, 001 M, N= 25 2 6 16
 РЕАГЕНТЫ И СОСТАВ СЛОЕВ, СИНТЕЗИРОВАННЫХ С ИСПОЛЬЗОВАНИЕМ ОКСАЛАТНЫХ КОМПЛЕКСОВ МЕТАЛЛОВ NZn 0, 13 Zr(OH)x(C 2 O 4)y = 25 NMg 1, 6 Al(OH)x(CO 3)y = 35 17
РЕАГЕНТЫ И СОСТАВ СЛОЕВ, СИНТЕЗИРОВАННЫХ С ИСПОЛЬЗОВАНИЕМ ОКСАЛАТНЫХ КОМПЛЕКСОВ МЕТАЛЛОВ NZn 0, 13 Zr(OH)x(C 2 O 4)y = 25 NMg 1, 6 Al(OH)x(CO 3)y = 35 17
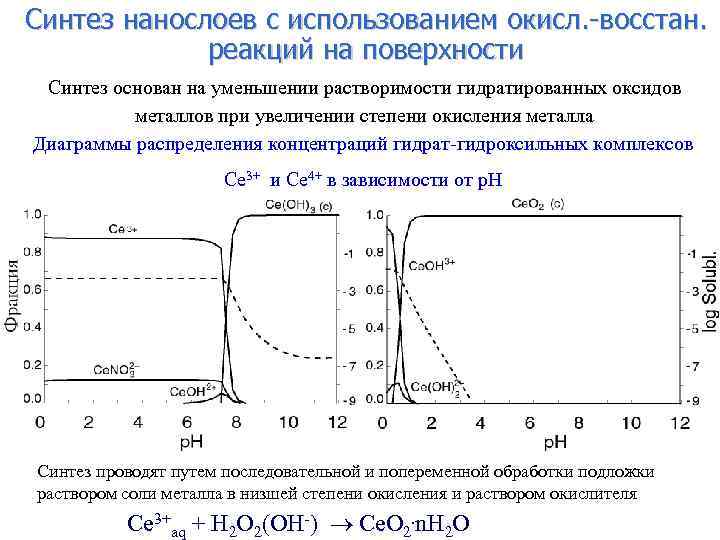 Синтез нанослоев с использованием окисл. -восстан. реакций на поверхности Синтез основан на уменьшении растворимости гидратированных оксидов металлов при увеличении степени окисления металла Диаграммы распределения концентраций гидрат-гидроксильных комплексов Ce 3+ и Ce 4+ в зависимости от р. Н Синтез проводят путем последовательной и попеременной обработки подложки раствором соли металла в низшей степени окисления и раствором окислителя Ce 3+aq + H 2 O 2(OH-) Ce. O 2. n. H 2 O
Синтез нанослоев с использованием окисл. -восстан. реакций на поверхности Синтез основан на уменьшении растворимости гидратированных оксидов металлов при увеличении степени окисления металла Диаграммы распределения концентраций гидрат-гидроксильных комплексов Ce 3+ и Ce 4+ в зависимости от р. Н Синтез проводят путем последовательной и попеременной обработки подложки раствором соли металла в низшей степени окисления и раствором окислителя Ce 3+aq + H 2 O 2(OH-) Ce. O 2. n. H 2 O
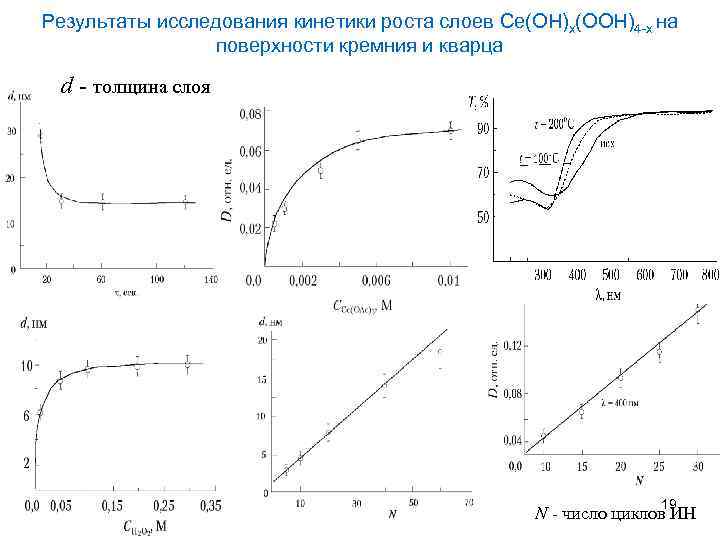 Результаты исследования кинетики роста слоев Ce(OH)x(OOH)4 -x на поверхности кремния и кварца d - толщина слоя 19 N - число циклов ИН
Результаты исследования кинетики роста слоев Ce(OH)x(OOH)4 -x на поверхности кремния и кварца d - толщина слоя 19 N - число циклов ИН
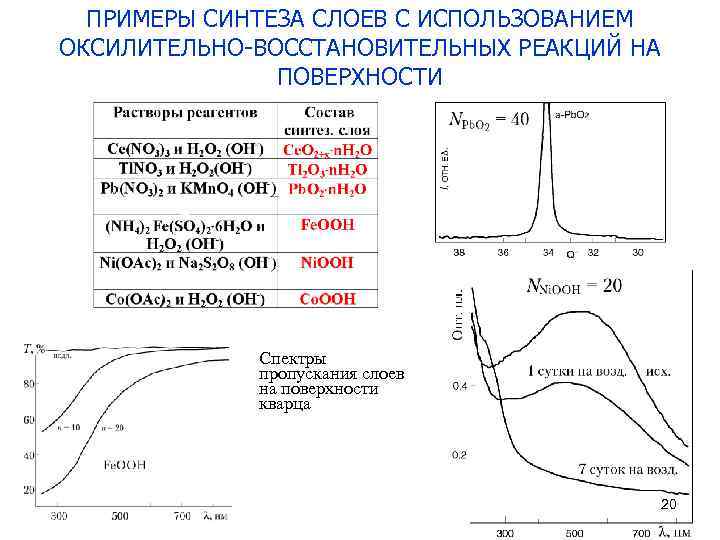 ПРИМЕРЫ СИНТЕЗА СЛОЕВ С ИСПОЛЬЗОВАНИЕМ ОКСИЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫХ РЕАКЦИЙ НА ПОВЕРХНОСТИ Спектры пропускания слоев на поверхности кварца 20
ПРИМЕРЫ СИНТЕЗА СЛОЕВ С ИСПОЛЬЗОВАНИЕМ ОКСИЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫХ РЕАКЦИЙ НА ПОВЕРХНОСТИ Спектры пропускания слоев на поверхности кварца 20
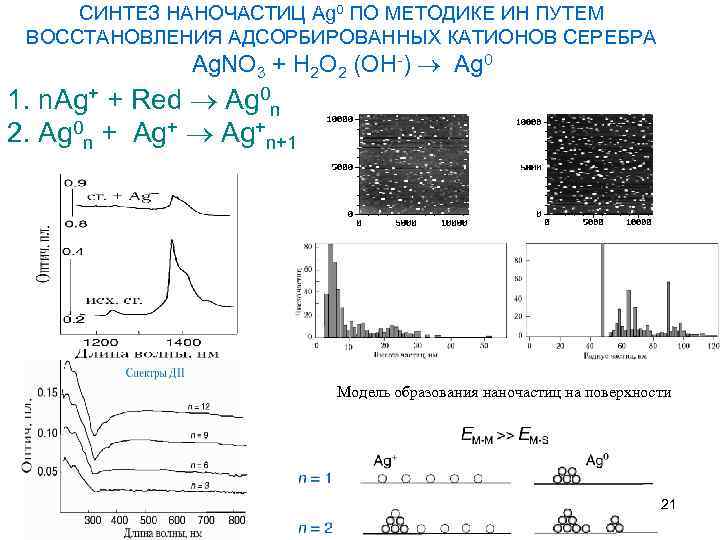 СИНТЕЗ НАНОЧАСТИЦ Ag 0 ПО МЕТОДИКЕ ИН ПУТЕМ ВОССТАНОВЛЕНИЯ АДСОРБИРОВАННЫХ КАТИОНОВ СЕРЕБРА Ag. NO 3 + H 2 O 2 (OH-) Ag 0 1. n. Ag+ + Red Ag 0 n 2. Ag 0 n + Ag+n+1 АСМ n=1 n=3 Модель образования наночастиц на поверхности 21
СИНТЕЗ НАНОЧАСТИЦ Ag 0 ПО МЕТОДИКЕ ИН ПУТЕМ ВОССТАНОВЛЕНИЯ АДСОРБИРОВАННЫХ КАТИОНОВ СЕРЕБРА Ag. NO 3 + H 2 O 2 (OH-) Ag 0 1. n. Ag+ + Red Ag 0 n 2. Ag 0 n + Ag+n+1 АСМ n=1 n=3 Модель образования наночастиц на поверхности 21
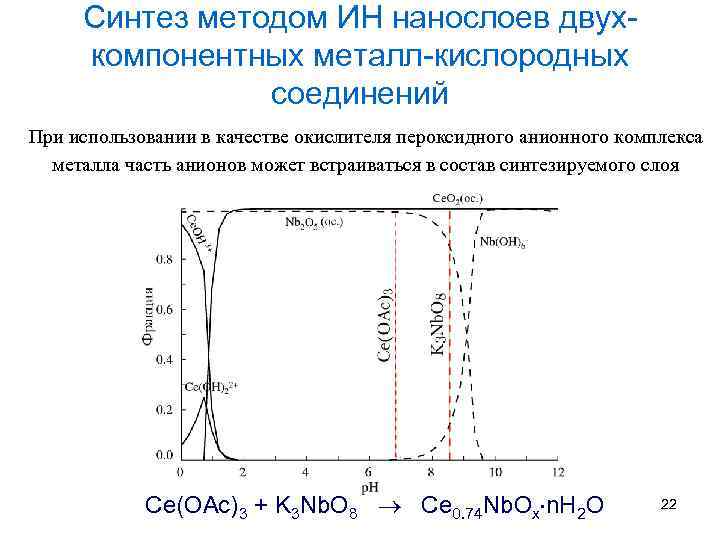 Синтез методом ИН нанослоев двухкомпонентных металл-кислородных соединений При использовании в качестве окислителя пероксидного анионного комплекса металла часть анионов может встраиваться в состав синтезируемого слоя Ce(OAc)3 + K 3 Nb. O 8 Ce 0. 74 Nb. Ox n. H 2 O 22
Синтез методом ИН нанослоев двухкомпонентных металл-кислородных соединений При использовании в качестве окислителя пероксидного анионного комплекса металла часть анионов может встраиваться в состав синтезируемого слоя Ce(OAc)3 + K 3 Nb. O 8 Ce 0. 74 Nb. Ox n. H 2 O 22
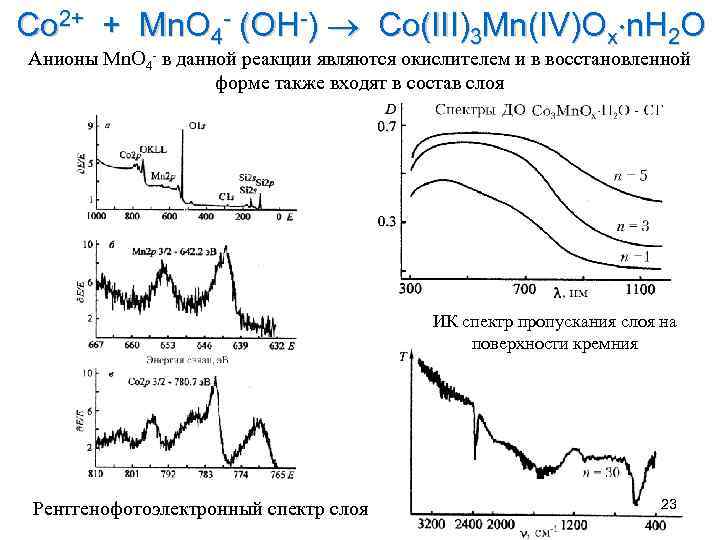 Co 2+ + Mn. O 4 - (OH-) Co(III)3 Mn(IV)Ox n. H 2 O Анионы Mn. O 4 - в данной реакции являются окислителем и в восстановленной форме также входят в состав слоя ИК спектр пропускания слоя на поверхности кремния Рентгенофотоэлектронный спектр слоя 23
Co 2+ + Mn. O 4 - (OH-) Co(III)3 Mn(IV)Ox n. H 2 O Анионы Mn. O 4 - в данной реакции являются окислителем и в восстановленной форме также входят в состав слоя ИК спектр пропускания слоя на поверхности кремния Рентгенофотоэлектронный спектр слоя 23
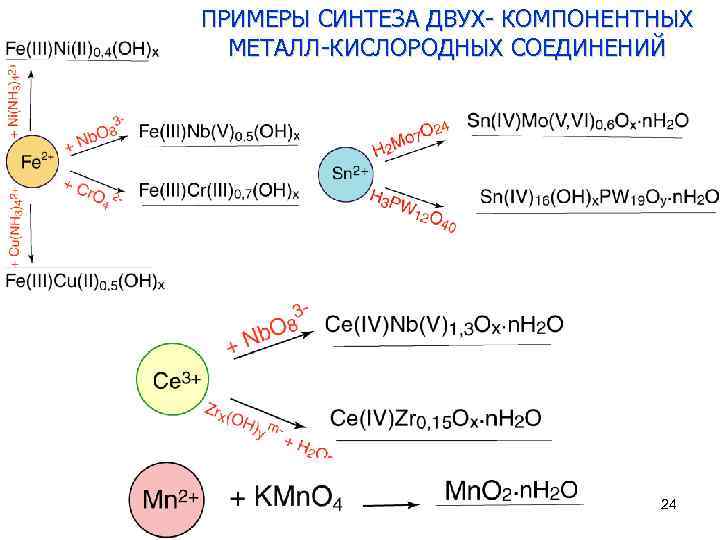 ПРИМЕРЫ СИНТЕЗА ДВУХ- КОМПОНЕНТНЫХ МЕТАЛЛ-КИСЛОРОДНЫХ СОЕДИНЕНИЙ 24
ПРИМЕРЫ СИНТЕЗА ДВУХ- КОМПОНЕНТНЫХ МЕТАЛЛ-КИСЛОРОДНЫХ СОЕДИНЕНИЙ 24
![Синтез методом ИН гибридных слоев металла и оксида [Si. O 2]OH + (Mn 2+ Синтез методом ИН гибридных слоев металла и оксида [Si. O 2]OH + (Mn 2+](https://present5.com/presentation/-101369386_437489810/image-25.jpg) Синтез методом ИН гибридных слоев металла и оксида [Si. O 2]OH + (Mn 2+ + Ag+)n [Si. O 2](Mn. O 2 x. Ag 0)n РФЭ спектр слоя на поверхности кремния n = 25 ИК спектр пропускания слоя на поверхности кремния
Синтез методом ИН гибридных слоев металла и оксида [Si. O 2]OH + (Mn 2+ + Ag+)n [Si. O 2](Mn. O 2 x. Ag 0)n РФЭ спектр слоя на поверхности кремния n = 25 ИК спектр пропускания слоя на поверхности кремния
Mb. OH+ n[HFгаз + удал. изб. + La(NO 3)3 ПРИМЕРЫ РЕАКЦИЙ ИМН 1. [Si](Si. Oa)Mb. OH+ n[HFгаз + удал. изб. + La(NO 3)3](https://present5.com/presentation/-101369386_437489810/image-26.jpg) ПРИМЕРЫ РЕАКЦИЙ ИМН 1. [Si](Si. Oa)Mb. OH+ n[HFгаз + удал. изб. + La(NO 3)3 (р-р) + удал. изб. ]n + HFгаз + удал. изб. [Si](Mc. Si. Fd)(La. F 3)n(HF)e а = 0, 712, с = 0, 732 нм [Fe]Fe-OH + {P 4 O 10 (газ) + Ba(NO 3)2(р-р)}n [Fe](Fe. PO 4)(Ba. HPO 4 n. H 2 O)n 2. 26
ПРИМЕРЫ РЕАКЦИЙ ИМН 1. [Si](Si. Oa)Mb. OH+ n[HFгаз + удал. изб. + La(NO 3)3 (р-р) + удал. изб. ]n + HFгаз + удал. изб. [Si](Mc. Si. Fd)(La. F 3)n(HF)e а = 0, 712, с = 0, 732 нм [Fe]Fe-OH + {P 4 O 10 (газ) + Ba(NO 3)2(р-р)}n [Fe](Fe. PO 4)(Ba. HPO 4 n. H 2 O)n 2. 26
 Полученный экспериментальный материал, таким образом, указывает на следующие особенности синтеза слоев методами ИН и ИМН: - возможность прецизионного регулирования толщины слоев и их синтеза на поверхности подложек сколь угодно сложной формы, - возможность синтеза методом ИН слоев практически всех трудно растворимых веществ, а методом ИМН - тех трудно растворимых, анионы которых существуют при низких температурах в газообразном виде. 27
Полученный экспериментальный материал, таким образом, указывает на следующие особенности синтеза слоев методами ИН и ИМН: - возможность прецизионного регулирования толщины слоев и их синтеза на поверхности подложек сколь угодно сложной формы, - возможность синтеза методом ИН слоев практически всех трудно растворимых веществ, а методом ИМН - тех трудно растворимых, анионы которых существуют при низких температурах в газообразном виде. 27


