Лекция 11 Полифенкц. соединения.pptx
- Количество слайдов: 32
 Лекция № 11 Полифункциональные соединения Многоатомные спирты и фенолы, полиамины, двухосновные карбоновые кислоты
Лекция № 11 Полифункциональные соединения Многоатомные спирты и фенолы, полиамины, двухосновные карбоновые кислоты
 • Биоорганическая химия – раздел биохимии, который изучает физико-химические основы и механизмы функционирования важнейших систем живой клетки. • Биоорганическая химия использует достижения классической химии. Дисциплина устанавливает взаимосвязь между возможностью повреждения структуры биологически активных молекул и возникновением заболевания. • Методами биоорганической химии осуществляется синтез природных веществ, изучаются способы их химической модификации с целью применения нативных и частично измененных соединений в качестве лекарственных препаратов.
• Биоорганическая химия – раздел биохимии, который изучает физико-химические основы и механизмы функционирования важнейших систем живой клетки. • Биоорганическая химия использует достижения классической химии. Дисциплина устанавливает взаимосвязь между возможностью повреждения структуры биологически активных молекул и возникновением заболевания. • Методами биоорганической химии осуществляется синтез природных веществ, изучаются способы их химической модификации с целью применения нативных и частично измененных соединений в качестве лекарственных препаратов.
 Полифункциональность и гетерофункциональность – важнейшая особенность строения биоорганических соединений • Человек представляет собой химическую машину. В 1 мл плазмы крови находится 40 миллионов молекул биоорганических соединений
Полифункциональность и гетерофункциональность – важнейшая особенность строения биоорганических соединений • Человек представляет собой химическую машину. В 1 мл плазмы крови находится 40 миллионов молекул биоорганических соединений
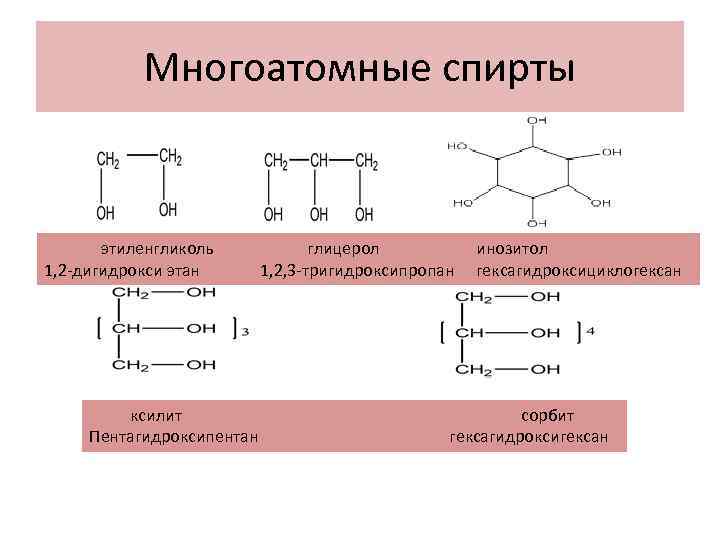 Многоатомные спирты этиленгликоль 1, 2 -дигидрокси этан ксилит Пентагидроксипентан глицерол 1, 2, 3 -тригидроксипропан инозитол гексагидроксициклогексан сорбит гексагидроксигексан
Многоатомные спирты этиленгликоль 1, 2 -дигидрокси этан ксилит Пентагидроксипентан глицерол 1, 2, 3 -тригидроксипропан инозитол гексагидроксициклогексан сорбит гексагидроксигексан
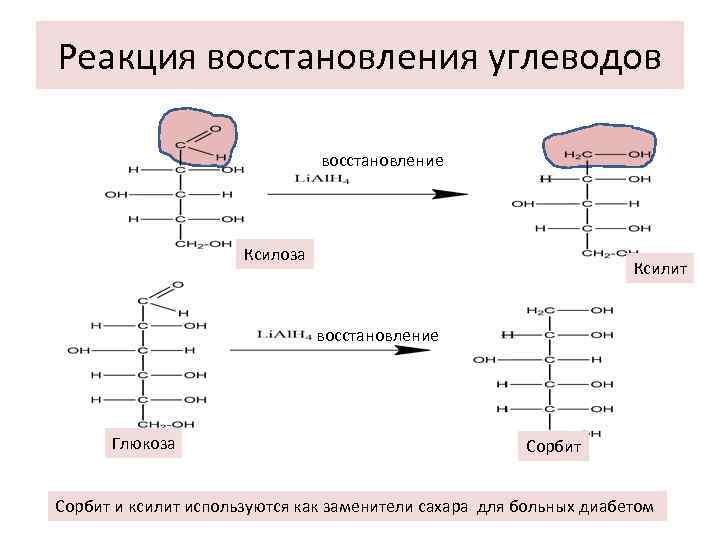 Реакция восстановления углеводов восстановление Ксилоза Ксилит восстановление Глюкоза Сорбит и ксилит используются как заменители сахара для больных диабетом
Реакция восстановления углеводов восстановление Ксилоза Ксилит восстановление Глюкоза Сорбит и ксилит используются как заменители сахара для больных диабетом
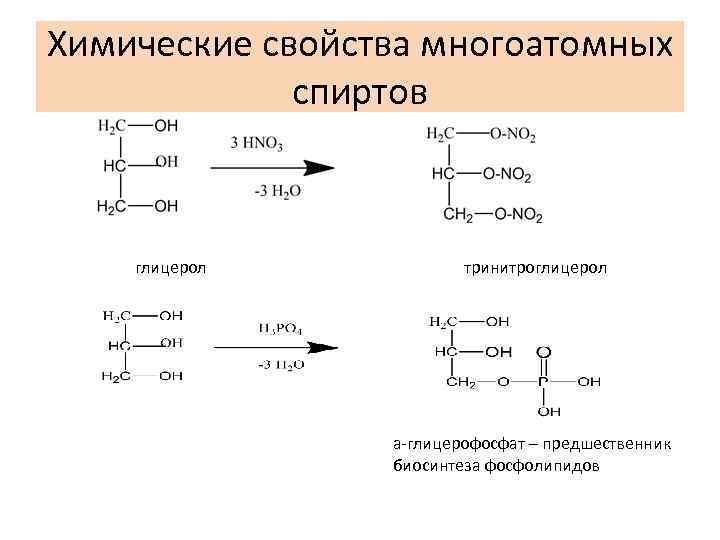 Химические свойства многоатомных спиртов глицерол тринитроглицерол а-глицерофосфат – предшественник биосинтеза фосфолипидов
Химические свойства многоатомных спиртов глицерол тринитроглицерол а-глицерофосфат – предшественник биосинтеза фосфолипидов
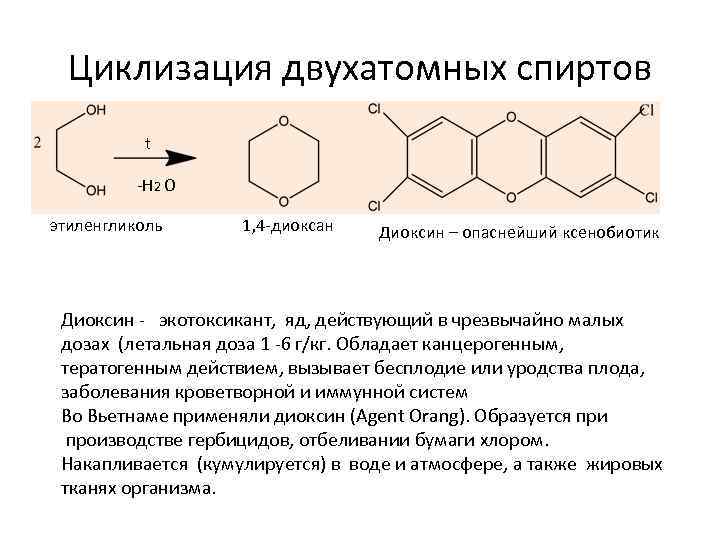 Циклизация двухатомных спиртов t -Н 2 О этиленгликоль 1, 4 -диоксан Диоксин – опаснейший ксенобиотик Диоксин - экотоксикант, яд, действующий в чрезвычайно малых дозах (летальная доза 1 -6 г/кг. Обладает канцерогенным, тератогенным действием, вызывает бесплодие или уродства плода, заболевания кроветворной и иммунной систем Во Вьетнаме применяли диоксин (Agent Orang). Образуется при производстве гербицидов, отбеливании бумаги хлором. Накапливается (кумулируется) в воде и атмосфере, а также жировых тканях организма.
Циклизация двухатомных спиртов t -Н 2 О этиленгликоль 1, 4 -диоксан Диоксин – опаснейший ксенобиотик Диоксин - экотоксикант, яд, действующий в чрезвычайно малых дозах (летальная доза 1 -6 г/кг. Обладает канцерогенным, тератогенным действием, вызывает бесплодие или уродства плода, заболевания кроветворной и иммунной систем Во Вьетнаме применяли диоксин (Agent Orang). Образуется при производстве гербицидов, отбеливании бумаги хлором. Накапливается (кумулируется) в воде и атмосфере, а также жировых тканях организма.
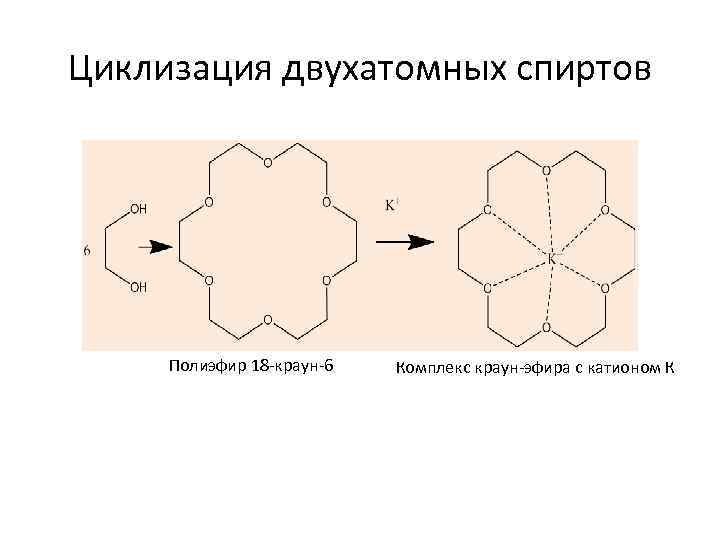 Циклизация двухатомных спиртов Полиэфир 18 -краун-6 Комплекс краун-эфира с катионом К
Циклизация двухатомных спиртов Полиэфир 18 -краун-6 Комплекс краун-эфира с катионом К
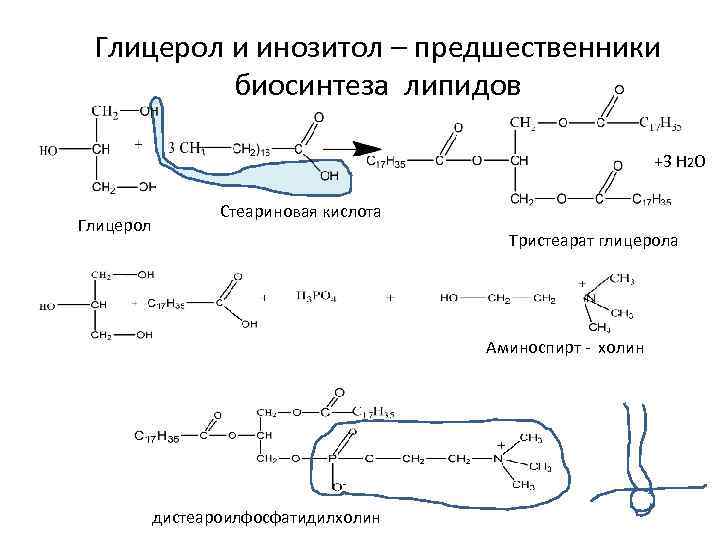 Глицерол и инозитол – предшественники биосинтеза липидов +3 Н 2 О Глицерол Стеариновая кислота Тристеарат глицерола Аминоспирт - холин дистеароилфосфатидилхолин
Глицерол и инозитол – предшественники биосинтеза липидов +3 Н 2 О Глицерол Стеариновая кислота Тристеарат глицерола Аминоспирт - холин дистеароилфосфатидилхолин
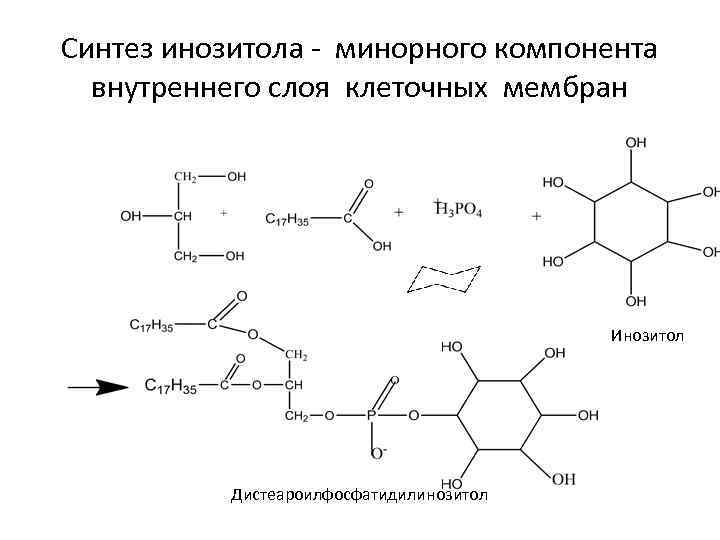 Синтез инозитола - минорного компонента внутреннего слоя клеточных мембран Инозитол Дистеароилфосфатидилинозитол
Синтез инозитола - минорного компонента внутреннего слоя клеточных мембран Инозитол Дистеароилфосфатидилинозитол
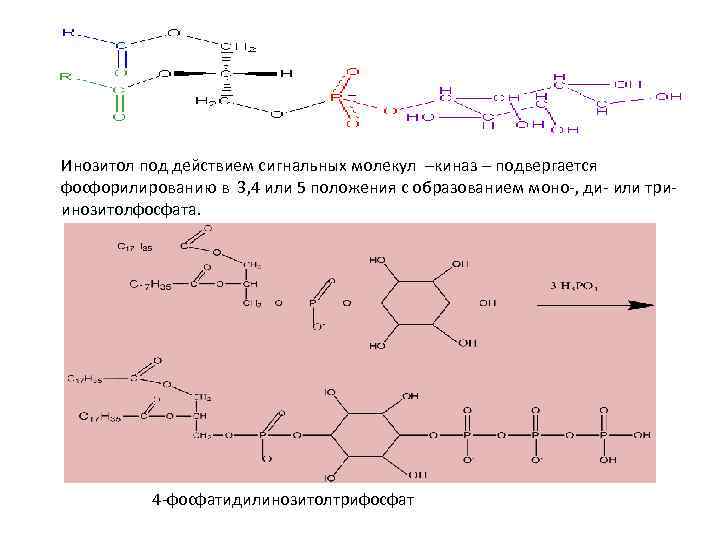 Инозитол под действием сигнальных молекул –киназ – подвергается фосфорилированию в 3, 4 или 5 положения с образованием моно-, ди- или триинозитолфосфата. 4 -фосфатидилинозитолтрифосфат
Инозитол под действием сигнальных молекул –киназ – подвергается фосфорилированию в 3, 4 или 5 положения с образованием моно-, ди- или триинозитолфосфата. 4 -фосфатидилинозитолтрифосфат
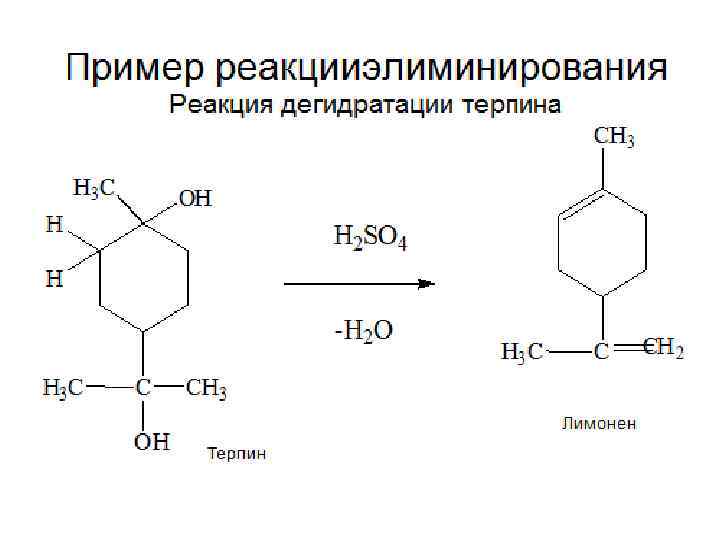
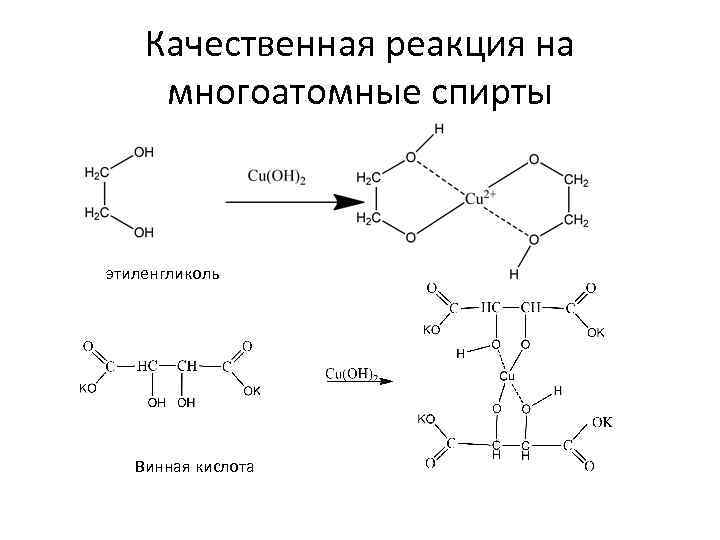 Качественная реакция на многоатомные спирты этиленгликоль Винная кислота
Качественная реакция на многоатомные спирты этиленгликоль Винная кислота
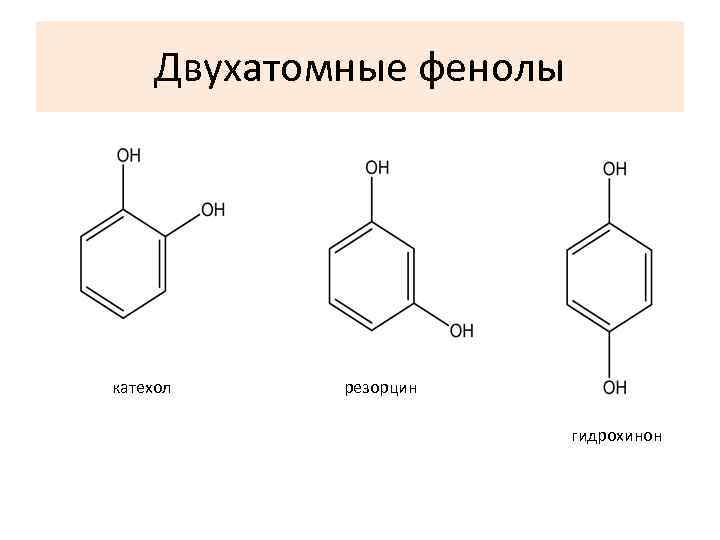 Двухатомные фенолы катехол резорцин гидрохинон
Двухатомные фенолы катехол резорцин гидрохинон
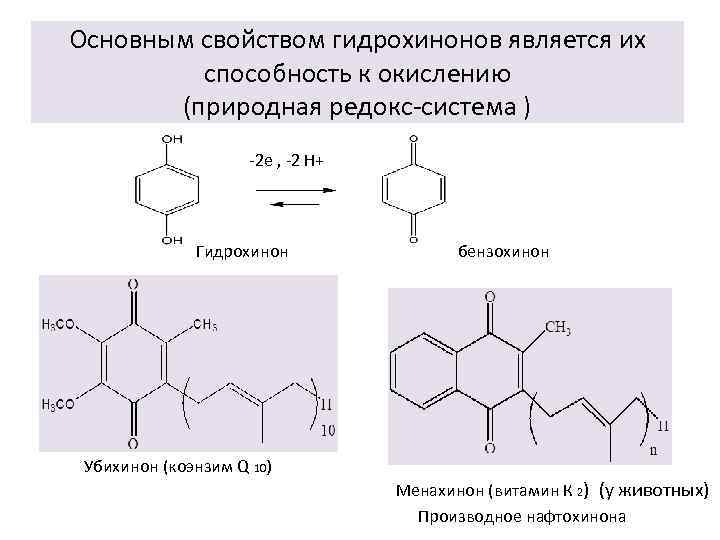 Основным свойством гидрохинонов является их способность к окислению (природная редокс-система ) -2 е , -2 Н+ Гидрохинон бензохинон Убихинон (коэнзим Q 10) Менахинон (витамин К 2) (у животных) Производное нафтохинона
Основным свойством гидрохинонов является их способность к окислению (природная редокс-система ) -2 е , -2 Н+ Гидрохинон бензохинон Убихинон (коэнзим Q 10) Менахинон (витамин К 2) (у животных) Производное нафтохинона
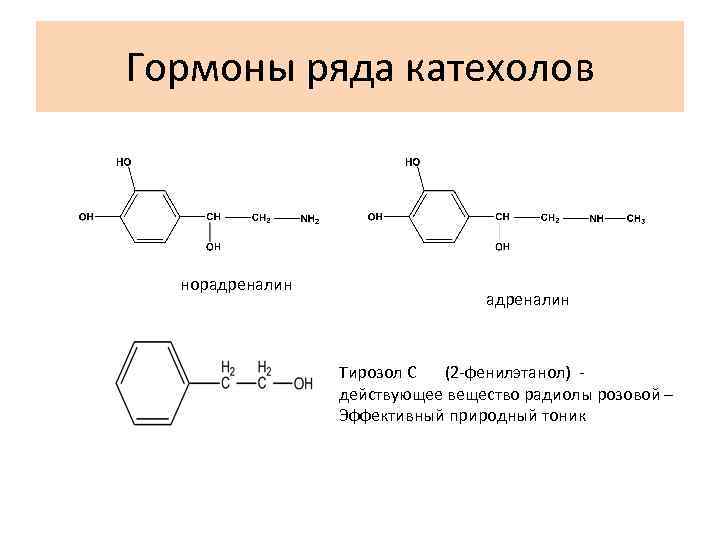 Гормоны ряда катехолов норадреналин Тирозол С (2 -фенилэтанол) действующее вещество радиолы розовой – Эффективный природный тоник
Гормоны ряда катехолов норадреналин Тирозол С (2 -фенилэтанол) действующее вещество радиолы розовой – Эффективный природный тоник
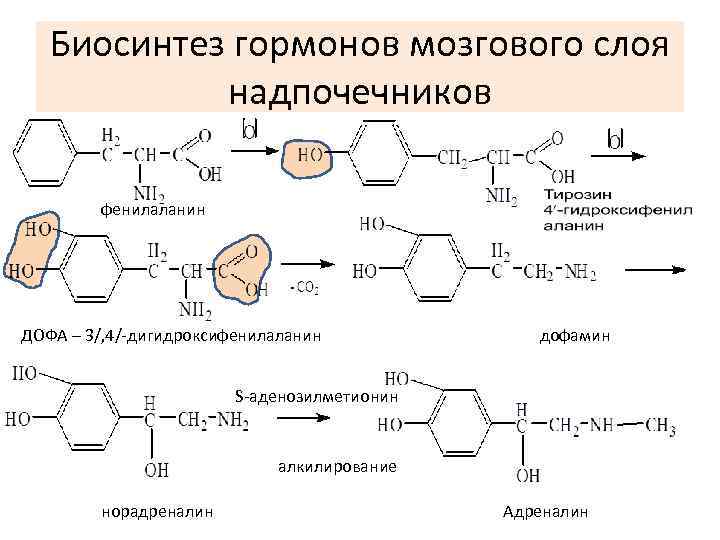 Биосинтез гормонов мозгового слоя надпочечников фенилаланин ДОФА – 3/, 4/-дигидроксифенилаланин дофамин S-аденозилметионин алкилирование норадреналин Адреналин
Биосинтез гормонов мозгового слоя надпочечников фенилаланин ДОФА – 3/, 4/-дигидроксифенилаланин дофамин S-аденозилметионин алкилирование норадреналин Адреналин
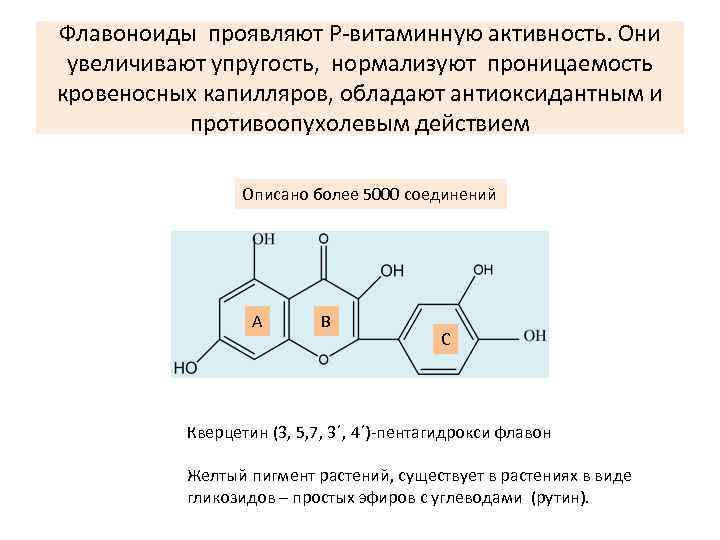 Флавоноиды проявляют Р-витаминную активность. Они увеличивают упругость, нормализуют проницаемость кровеносных капилляров, обладают антиоксидантным и противоопухолевым действием Описано более 5000 соединений А В С Кверцетин (3, 5, 7, 3´, 4´)-пентагидрокси флавон Желтый пигмент растений, существует в растениях в виде гликозидов – простых эфиров с углеводами (рутин).
Флавоноиды проявляют Р-витаминную активность. Они увеличивают упругость, нормализуют проницаемость кровеносных капилляров, обладают антиоксидантным и противоопухолевым действием Описано более 5000 соединений А В С Кверцетин (3, 5, 7, 3´, 4´)-пентагидрокси флавон Желтый пигмент растений, существует в растениях в виде гликозидов – простых эфиров с углеводами (рутин).
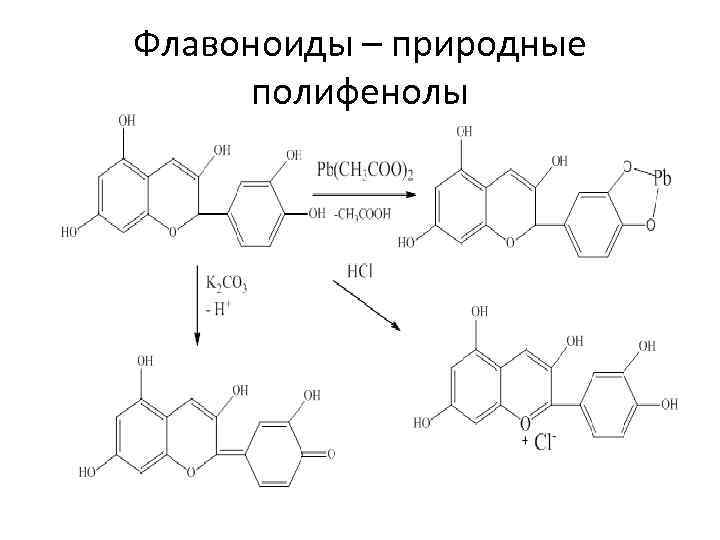 Флавоноиды – природные полифенолы
Флавоноиды – природные полифенолы
 Окраска цветочного ковра, цветов, плодов и ягод определяется 3 соединениями класса флавоноидов (цианидин, пеларгонидин, дельфинидин)
Окраска цветочного ковра, цветов, плодов и ягод определяется 3 соединениями класса флавоноидов (цианидин, пеларгонидин, дельфинидин)


 • Флавоноиды, способны уничтожать свободные радикалы, поэтому являются ингибиторами процессов свободнорадикального окисления (антиоксидантами). • Обозначаем ингибитор как In-H. • • Радикальные продукты ингибитора In • не активны и не участвуют в дальнейшем в реакциях с субстратом (RH) , поскольку электронная плотность равномерно перераспределяется (делокализуется) по всей ароматической системе флавоноидов.
• Флавоноиды, способны уничтожать свободные радикалы, поэтому являются ингибиторами процессов свободнорадикального окисления (антиоксидантами). • Обозначаем ингибитор как In-H. • • Радикальные продукты ингибитора In • не активны и не участвуют в дальнейшем в реакциях с субстратом (RH) , поскольку электронная плотность равномерно перераспределяется (делокализуется) по всей ароматической системе флавоноидов.
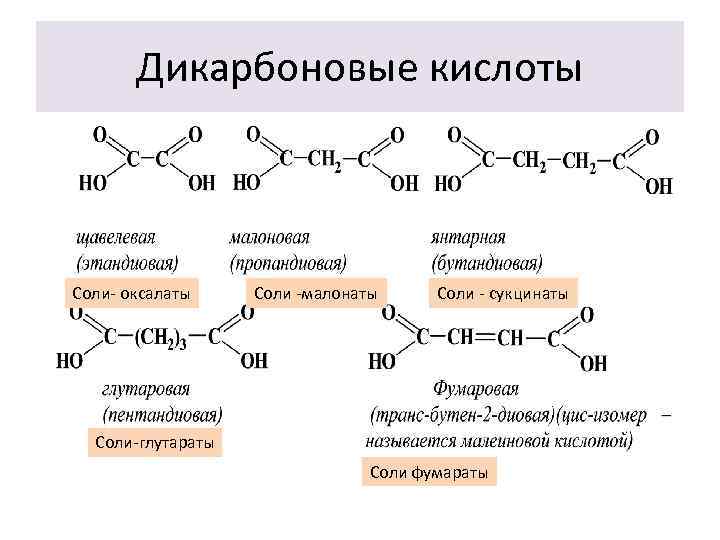 Дикарбоновые кислоты Соли- оксалаты Соли -малонаты Соли - сукцинаты Соли-глутараты Соли фумараты
Дикарбоновые кислоты Соли- оксалаты Соли -малонаты Соли - сукцинаты Соли-глутараты Соли фумараты
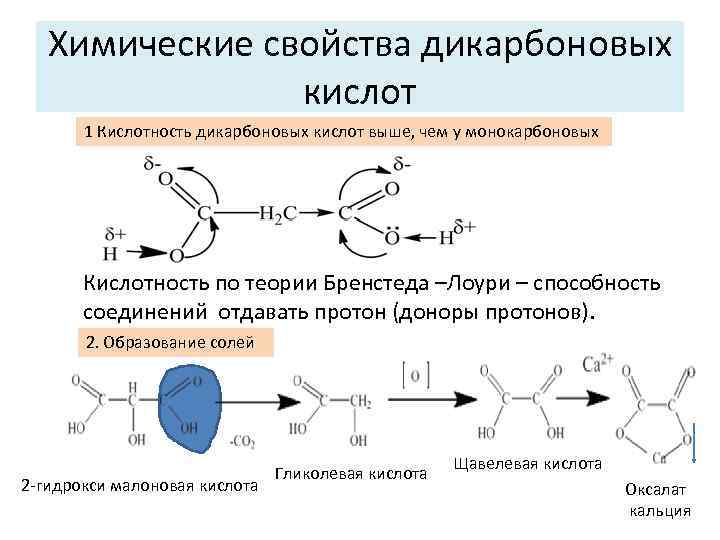 Химические свойства дикарбоновых кислот 1 Кислотность дикарбоновых кислот выше, чем у монокарбоновых Кислотность по теории Бренстеда –Лоури – способность соединений отдавать протон (доноры протонов). 2. Образование солей 2 -гидрокси малоновая кислота Гликолевая кислота Щавелевая кислота Оксалат кальция
Химические свойства дикарбоновых кислот 1 Кислотность дикарбоновых кислот выше, чем у монокарбоновых Кислотность по теории Бренстеда –Лоури – способность соединений отдавать протон (доноры протонов). 2. Образование солей 2 -гидрокси малоновая кислота Гликолевая кислота Щавелевая кислота Оксалат кальция
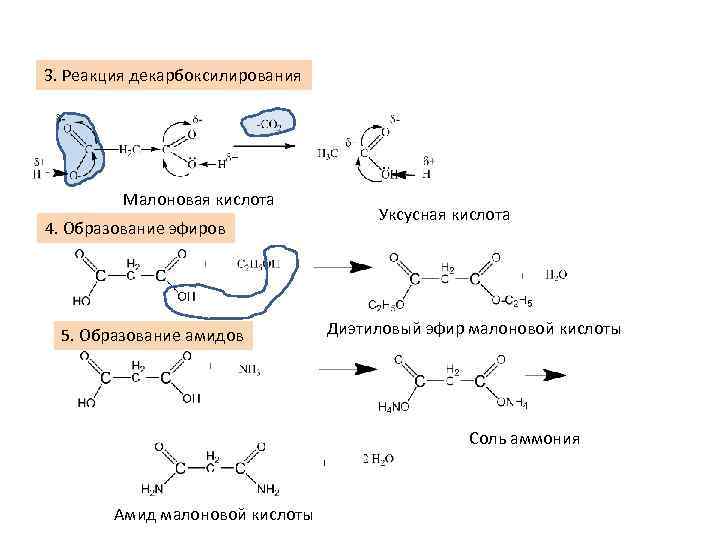 3. Реакция декарбоксилирования Малоновая кислота 4. Образование эфиров 5. Образование амидов Уксусная кислота Диэтиловый эфир малоновой кислоты Соль аммония Амид малоновой кислоты
3. Реакция декарбоксилирования Малоновая кислота 4. Образование эфиров 5. Образование амидов Уксусная кислота Диэтиловый эфир малоновой кислоты Соль аммония Амид малоновой кислоты
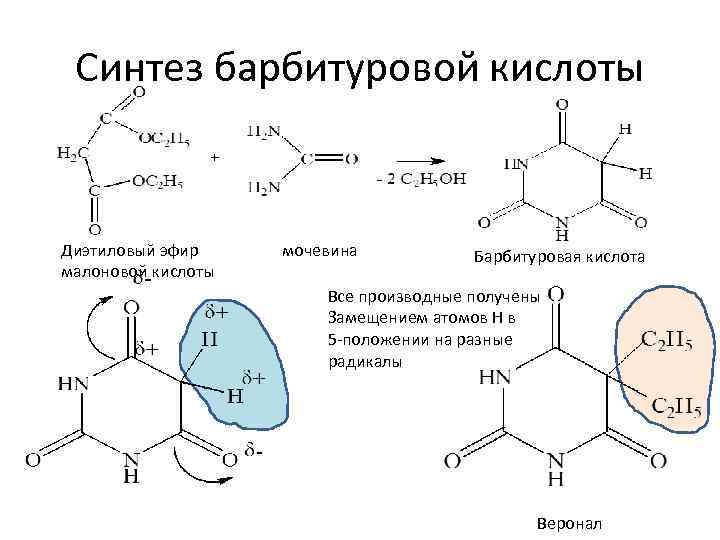 Синтез барбитуровой кислоты Диэтиловый эфир малоновой кислоты мочевина Барбитуровая кислота Все производные получены Замещением атомов Н в 5 -положении на разные радикалы Веронал
Синтез барбитуровой кислоты Диэтиловый эфир малоновой кислоты мочевина Барбитуровая кислота Все производные получены Замещением атомов Н в 5 -положении на разные радикалы Веронал
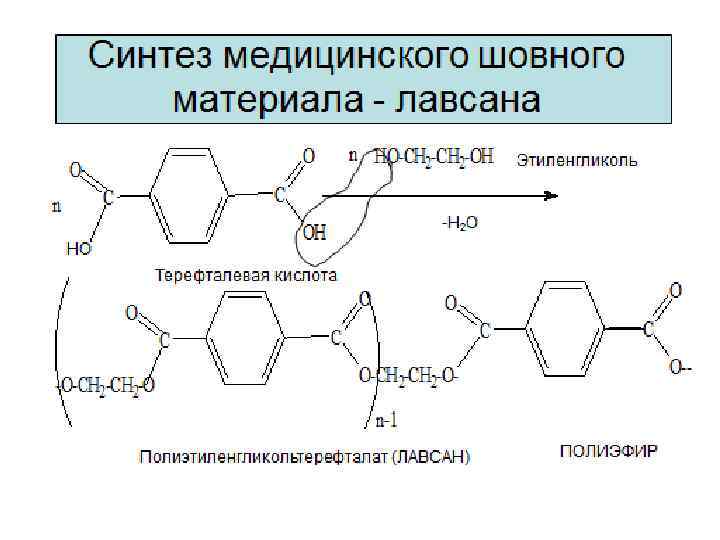
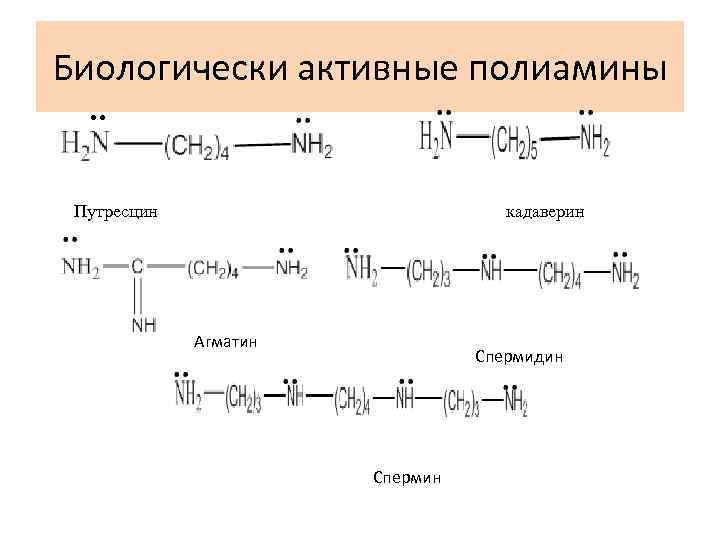 Биологически активные полиамины. . Путресцин кадаверин Агматин Спермидин Спермин
Биологически активные полиамины. . Путресцин кадаверин Агматин Спермидин Спермин
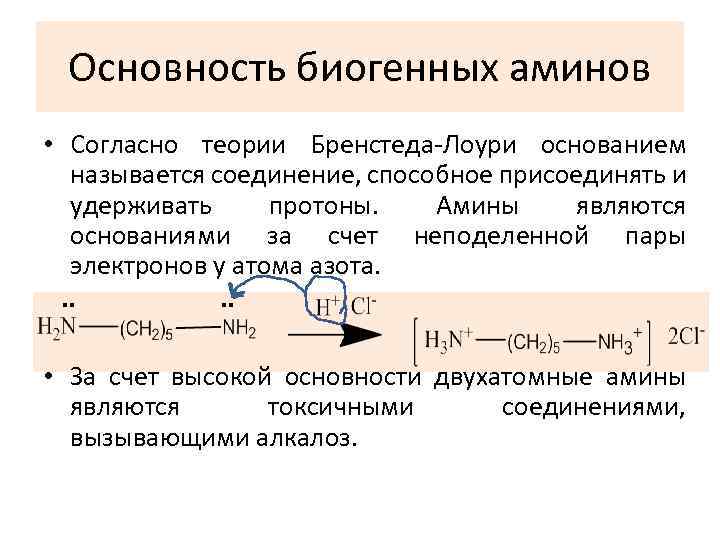 Основность биогенных аминов • Согласно теории Бренстеда-Лоури основанием называется соединение, способное присоединять и удерживать протоны. Амины являются основаниями за счет неподеленной пары электронов у атома азота. . . • За счет высокой основности двухатомные амины являются токсичными соединениями, вызывающими алкалоз.
Основность биогенных аминов • Согласно теории Бренстеда-Лоури основанием называется соединение, способное присоединять и удерживать протоны. Амины являются основаниями за счет неподеленной пары электронов у атома азота. . . • За счет высокой основности двухатомные амины являются токсичными соединениями, вызывающими алкалоз.
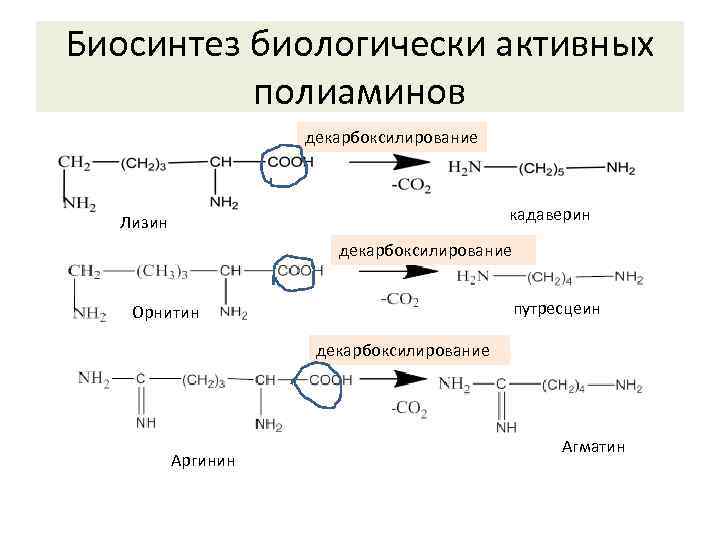 Биосинтез биологически активных полиаминов декарбоксилирование кадаверин Лизин декарбоксилирование путресцеин Орнитин декарбоксилирование Аргинин Агматин
Биосинтез биологически активных полиаминов декарбоксилирование кадаверин Лизин декарбоксилирование путресцеин Орнитин декарбоксилирование Аргинин Агматин
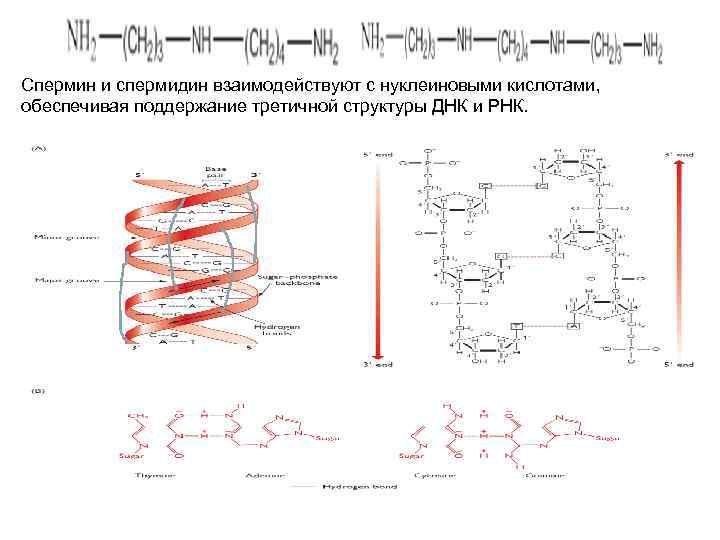 Спермин и спермидин взаимодействуют с нуклеиновыми кислотами, обеспечивая поддержание третичной структуры ДНК и РНК.
Спермин и спермидин взаимодействуют с нуклеиновыми кислотами, обеспечивая поддержание третичной структуры ДНК и РНК.


