Lektsia_11.ppt
- Количество слайдов: 69
 Лекция 11 Органическая химия.
Лекция 11 Органическая химия.
 План лекции 1. Особенности органических соединений. 2. Теория химического строения органических веществ. 3. Классификация органических соединений. 4. Основные классы органических соединений 5. Жиры. Белки. Углеводы. 2
План лекции 1. Особенности органических соединений. 2. Теория химического строения органических веществ. 3. Классификация органических соединений. 4. Основные классы органических соединений 5. Жиры. Белки. Углеводы. 2
 Отличительные особенности органических соединений 1) Кроме углерода в их состав почти всегда входит водород, часто кислород, азот, иногда сера и фосфор. 2) Соединения с одинаковым качественным и количественным составом могут обладать разными физическими и химическими свойствами (изомерия). 3) Температура плавления не превышает 350 -400°С. При нагревании без доступа воздуха органические вещества подвергаются глубоким изменениям с образованием новых веществ. 4) Связь между атомами в органических соединениях – ковалентная, поэтому они неэлектролиты, не диссоциируют в растворах, медленно взаимодействуют друг с другом. 3
Отличительные особенности органических соединений 1) Кроме углерода в их состав почти всегда входит водород, часто кислород, азот, иногда сера и фосфор. 2) Соединения с одинаковым качественным и количественным составом могут обладать разными физическими и химическими свойствами (изомерия). 3) Температура плавления не превышает 350 -400°С. При нагревании без доступа воздуха органические вещества подвергаются глубоким изменениям с образованием новых веществ. 4) Связь между атомами в органических соединениях – ковалентная, поэтому они неэлектролиты, не диссоциируют в растворах, медленно взаимодействуют друг с другом. 3
 Теория химического строения органических соединений А. М. Бутлерова 4
Теория химического строения органических соединений А. М. Бутлерова 4
 Углерод в органических соединениях четырехвалентен Гибридизация алкины алкены, алкадиены, арены алканы, циклоалканы 5
Углерод в органических соединениях четырехвалентен Гибридизация алкины алкены, алкадиены, арены алканы, циклоалканы 5
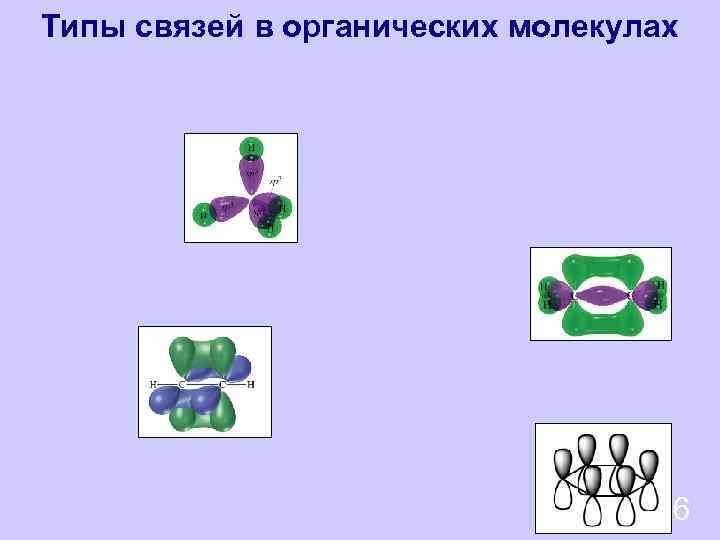 Типы связей в органических молекулах 6
Типы связей в органических молекулах 6
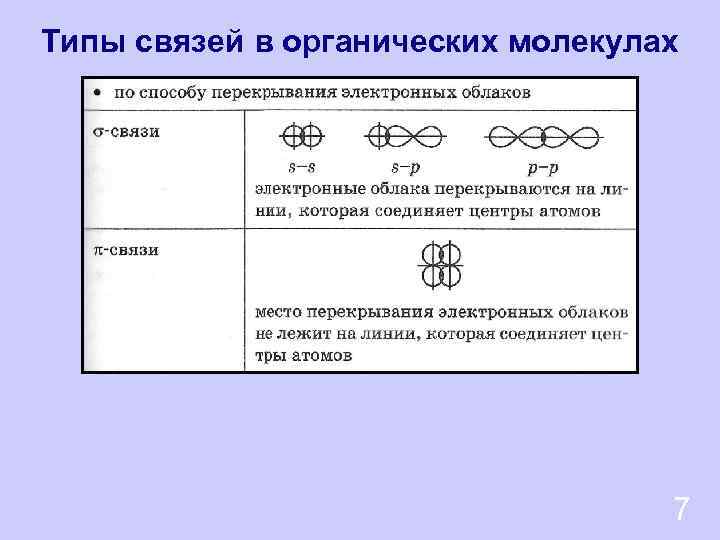 Типы связей в органических молекулах 7
Типы связей в органических молекулах 7
 Гомологический ряд – ряд соединений, близких по химическим свойствам, с характерными закономерностями изменения физических свойств, имеют однотипную структуру и отличаются друг от друга одной или несколькими –СН 2 - группами. Гомологи – отдельные члены гомологического ряда. 8
Гомологический ряд – ряд соединений, близких по химическим свойствам, с характерными закономерностями изменения физических свойств, имеют однотипную структуру и отличаются друг от друга одной или несколькими –СН 2 - группами. Гомологи – отдельные члены гомологического ряда. 8
 Виды изомерии Изомеры – вещества с одинаковым качественным и количественным составом, но с разным строением и следовательно с разными свойствами. 8
Виды изомерии Изомеры – вещества с одинаковым качественным и количественным составом, но с разным строением и следовательно с разными свойствами. 8
 Виды изомерии 10
Виды изомерии 10
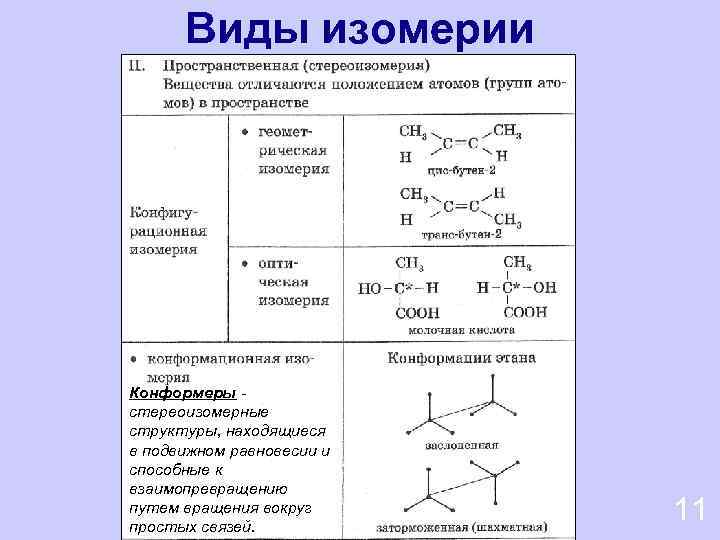 Виды изомерии Конформеры стереоизомерные структуры, находящиеся в подвижном равновесии и способные к взаимопревращению путем вращения вокруг простых связей. 11
Виды изомерии Конформеры стереоизомерные структуры, находящиеся в подвижном равновесии и способные к взаимопревращению путем вращения вокруг простых связей. 11
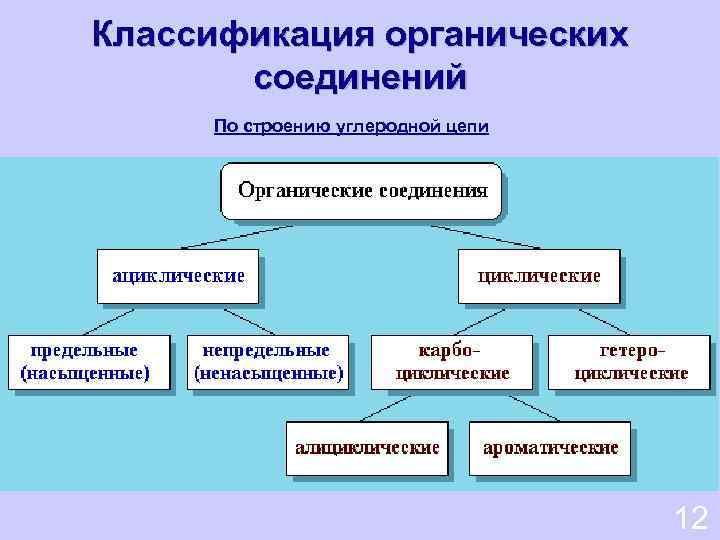 Классификация органических соединений По строению углеродной цепи 12
Классификация органических соединений По строению углеродной цепи 12
 По типу химических связей 13
По типу химических связей 13
 Функциональная группа постоянная группа атомов, которая определяет характерные свойства вещества: –ОН, –СООН и т. д. Н Н С О Н Н В СН 3 ОН высокая подвижность Н и Н 13
Функциональная группа постоянная группа атомов, которая определяет характерные свойства вещества: –ОН, –СООН и т. д. Н Н С О Н Н В СН 3 ОН высокая подвижность Н и Н 13
 Природные источники углеводородов 15
Природные источники углеводородов 15
 Переработка нефти 16
Переработка нефти 16
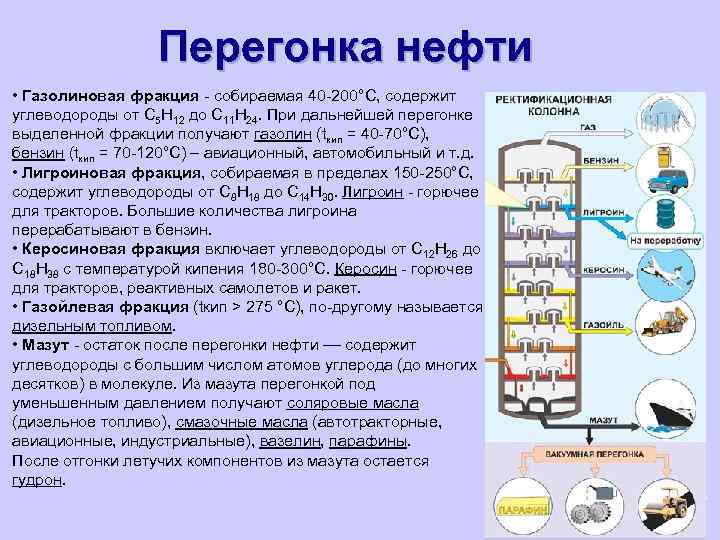 Перегонка нефти • Газолиновая фракция - собираемая 40 -200°С, содержит углеводороды от С 5 Н 12 до С 11 Н 24. При дальнейшей перегонке выделенной фракции получают газолин (tкип = 40 -70°С), бензин (tкип = 70 -120°С) – авиационный, автомобильный и т. д. • Лигроиновая фракция, собираемая в пределах 150 -250°С, содержит углеводороды от С 8 Н 18 до С 14 Н 30. Лигроин - горючее для тракторов. Большие количества лигроина перерабатывают в бензин. • Керосиновая фракция включает углеводороды от С 12 Н 26 до С 18 Н 38 с температурой кипения 180 -300°С. Керосин - горючее для тракторов, реактивных самолетов и ракет. • Газойлевая фракция (tкип > 275 °С), по-другому называется дизельным топливом. • Мазут - остаток после перегонки нефти –– содержит углеводороды с большим числом атомов углерода (до многих десятков) в молекуле. Из мазута перегонкой под уменьшенным давлением получают соляровые масла (дизельное топливо), смазочные масла (автотракторные, авиационные, индустриальные), вазелин, парафины. После отгонки летучих компонентов из мазута остается гудрон. 17
Перегонка нефти • Газолиновая фракция - собираемая 40 -200°С, содержит углеводороды от С 5 Н 12 до С 11 Н 24. При дальнейшей перегонке выделенной фракции получают газолин (tкип = 40 -70°С), бензин (tкип = 70 -120°С) – авиационный, автомобильный и т. д. • Лигроиновая фракция, собираемая в пределах 150 -250°С, содержит углеводороды от С 8 Н 18 до С 14 Н 30. Лигроин - горючее для тракторов. Большие количества лигроина перерабатывают в бензин. • Керосиновая фракция включает углеводороды от С 12 Н 26 до С 18 Н 38 с температурой кипения 180 -300°С. Керосин - горючее для тракторов, реактивных самолетов и ракет. • Газойлевая фракция (tкип > 275 °С), по-другому называется дизельным топливом. • Мазут - остаток после перегонки нефти –– содержит углеводороды с большим числом атомов углерода (до многих десятков) в молекуле. Из мазута перегонкой под уменьшенным давлением получают соляровые масла (дизельное топливо), смазочные масла (автотракторные, авиационные, индустриальные), вазелин, парафины. После отгонки летучих компонентов из мазута остается гудрон. 17
 Типы органических реакций 18
Типы органических реакций 18
 Алканы 19
Алканы 19
 Получение 20
Получение 20
 Химические свойства 21
Химические свойства 21
 22
22
 Применение Изооктан обуславливает антидетонационные свойства бензина. Октановое число — показатель, характеризующий детонационную стойкость топлива, равно содержанию (%) изооктана (2, 2, 4 триметилпентана) в его смеси с н-гептаном. 23
Применение Изооктан обуславливает антидетонационные свойства бензина. Октановое число — показатель, характеризующий детонационную стойкость топлива, равно содержанию (%) изооктана (2, 2, 4 триметилпентана) в его смеси с н-гептаном. 23
 Алкены 24
Алкены 24
 Получение 25
Получение 25
 Химические свойства 26
Химические свойства 26
 27
27
 Диены 28
Диены 28
 Получение 29
Получение 29
 Химические свойства 30
Химические свойства 30
 Алкины 31
Алкины 31
 Получение 32
Получение 32
 Химические свойства 33
Химические свойства 33
 34
34
 Ароматические углеводороды 35
Ароматические углеводороды 35
 Бензол Особенности строения молекулы С 6 Н 6 36
Бензол Особенности строения молекулы С 6 Н 6 36
 Получение 37
Получение 37
 Химические свойства 31
Химические свойства 31
 При введении в молекулу бензола любого заместителя происходит перераспределение электронной плотности. Заместители по оказываемому влиянию делятся на: Ориентанты 1 рода – доноры электронной плотности, повышают эл. плотность в орто- и пара-положении, именно туда будет направлена электрофильная атака. ОН-, ОR-, SH-, NH 2 - , NH-, NHR-, CH 3 Ориентанты 2 рода – акцепторы электронной плотности, понижают эл. плотность в орто- и пара-положении, именно туда будет направлена нуклефильная атака. Электрофильная атака протекает с трудом в мета-положении CN+ , NO 2+ , COH+ , COOH+ , SO 3 H+ , NH 3+ COOH
При введении в молекулу бензола любого заместителя происходит перераспределение электронной плотности. Заместители по оказываемому влиянию делятся на: Ориентанты 1 рода – доноры электронной плотности, повышают эл. плотность в орто- и пара-положении, именно туда будет направлена электрофильная атака. ОН-, ОR-, SH-, NH 2 - , NH-, NHR-, CH 3 Ориентанты 2 рода – акцепторы электронной плотности, понижают эл. плотность в орто- и пара-положении, именно туда будет направлена нуклефильная атака. Электрофильная атака протекает с трудом в мета-положении CN+ , NO 2+ , COH+ , COOH+ , SO 3 H+ , NH 3+ COOH
 Толуол Химические свойства 31
Толуол Химические свойства 31
 41
41
 Спирты 42
Спирты 42
 Получение 43
Получение 43
 Химические свойства 44
Химические свойства 44
 45
45
 46
46
 Фенолы Физические свойства фенола С 6 Н 5 ОН 47
Фенолы Физические свойства фенола С 6 Н 5 ОН 47
 Получение Применение 48
Получение Применение 48
 Химические свойства 31
Химические свойства 31
 Альдегиды 50
Альдегиды 50
 Физические свойства Получение 51
Физические свойства Получение 51
 Химические свойства 31
Химические свойства 31
 Химические свойства 53
Химические свойства 53
 Карбоновые кислоты 54
Карбоновые кислоты 54
 Химические свойства 55
Химические свойства 55
 Муравьиная кислота Получение 56
Муравьиная кислота Получение 56
 Уксусная кислота Получение 57
Уксусная кислота Получение 57
 Высшие кислоты 58
Высшие кислоты 58
 Сложные эфиры Физические свойства 59
Сложные эфиры Физические свойства 59
 Азотосодержащие органические соединений Амины Аминокислоты 59
Азотосодержащие органические соединений Амины Аминокислоты 59
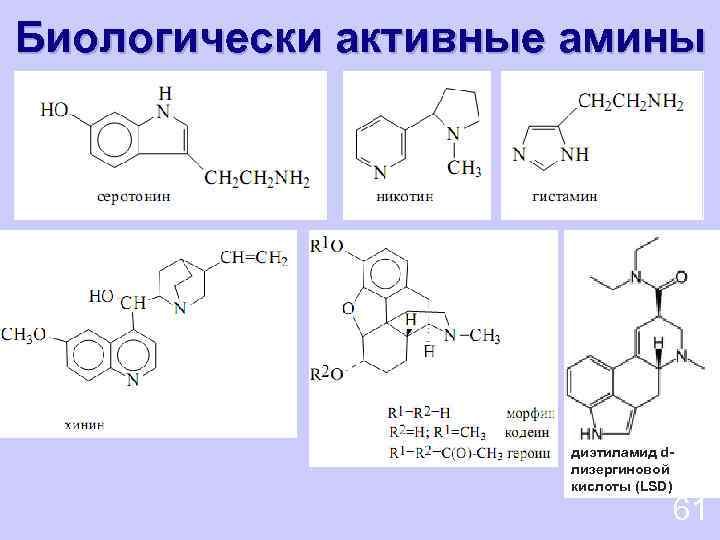 Биологически активные амины диэтиламид dлизергиновой кислоты (LSD) 61
Биологически активные амины диэтиламид dлизергиновой кислоты (LSD) 61
 Биологически важные вещества Жиры 31
Биологически важные вещества Жиры 31
 Углеводы 63
Углеводы 63
 64
64
 31
31
 Белки 66
Белки 66
 Взаимосвязь различных классов органических соединений 67
Взаимосвязь различных классов органических соединений 67
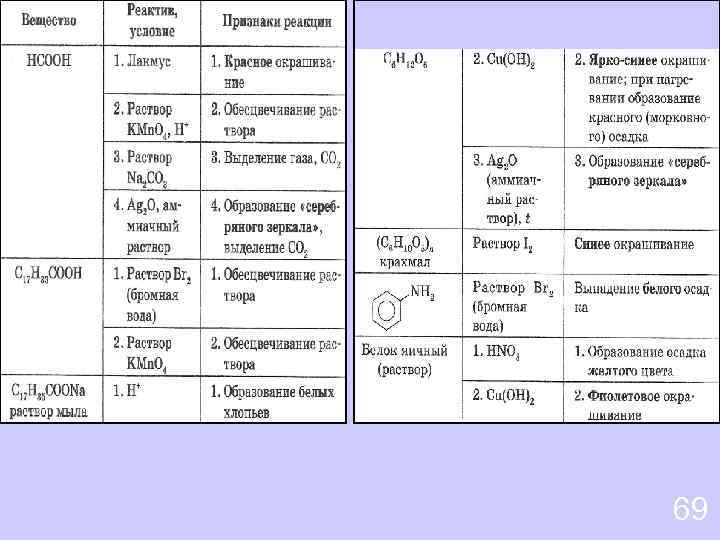
 Качественные реакции на органические вещества 68
Качественные реакции на органические вещества 68
 69
69


