LecSS-11(2012).ppt
- Количество слайдов: 11
 Лекция-11 Окисление металлов
Лекция-11 Окисление металлов
 Лекция-11 Металлы в природе Свободная энергия металлов при взаимодействии с кислородом уменьшается Металлы за геологическое время жизни Земли превратились в соответствующие оксиды и соли. Окисление металлов Сухое травление – взаимодействие металла с газом, приводящее к образованию газообразного продукта. Оксидирование, нитридизация, сульфидирование и т. д. – взаимодействие металла с газом, приводящее к образованию твердого продукта в виде тонкого слоя на поверхности металла. 2 Al + 3 Cl 2 Al 2 Cl 6 Si + O 2 Si. O 2 Si + 1/2 O 2 Si. O 3 Si + NH 3 Si 3 N 4 + 6 H 2
Лекция-11 Металлы в природе Свободная энергия металлов при взаимодействии с кислородом уменьшается Металлы за геологическое время жизни Земли превратились в соответствующие оксиды и соли. Окисление металлов Сухое травление – взаимодействие металла с газом, приводящее к образованию газообразного продукта. Оксидирование, нитридизация, сульфидирование и т. д. – взаимодействие металла с газом, приводящее к образованию твердого продукта в виде тонкого слоя на поверхности металла. 2 Al + 3 Cl 2 Al 2 Cl 6 Si + O 2 Si. O 2 Si + 1/2 O 2 Si. O 3 Si + NH 3 Si 3 N 4 + 6 H 2
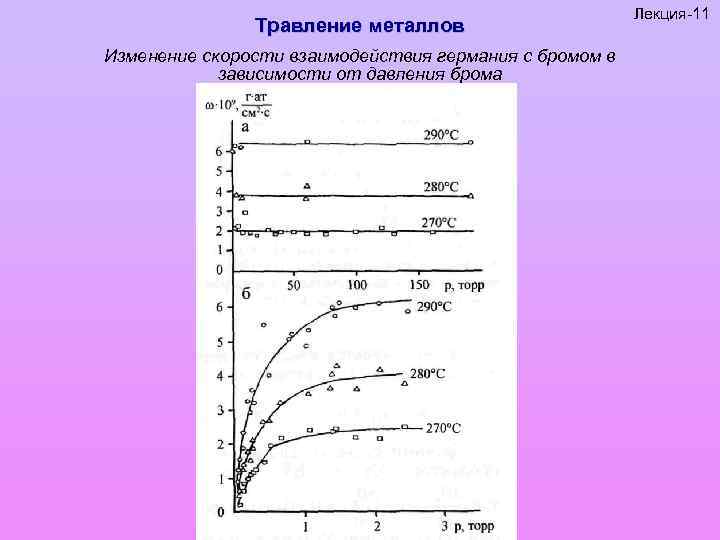 Травление металлов Изменение скорости взаимодействия германия с бромом в зависимости от давления брома Лекция-11
Травление металлов Изменение скорости взаимодействия германия с бромом в зависимости от давления брома Лекция-11
 Лекция-11 Травление металлов k 1 А + S AS 1. Адсорбция реагента k-1 2. Превращение в 3. адсорбционном слое k 2 АS BS 4. 3. Десорбция продукта. BS k-2 А – частица газа; S – адсорбционный центр на поверхности; В – продукт. k 3 B+S k-3 Стационарный режим: w = w 1 – w-1 = w 2 – w-2 = w 3 – w-3 d AS/dt = 0, d BS/dt = 0. 0 + AS + BS = 1 Условия проточного реактора или вакуумной камеры p. B << p. A:
Лекция-11 Травление металлов k 1 А + S AS 1. Адсорбция реагента k-1 2. Превращение в 3. адсорбционном слое k 2 АS BS 4. 3. Десорбция продукта. BS k-2 А – частица газа; S – адсорбционный центр на поверхности; В – продукт. k 3 B+S k-3 Стационарный режим: w = w 1 – w-1 = w 2 – w-2 = w 3 – w-3 d AS/dt = 0, d BS/dt = 0. 0 + AS + BS = 1 Условия проточного реактора или вакуумной камеры p. B << p. A:
 Лекция-11 Травление металлов 1 Лимитирующая стадия – превращение в адсорбционном слое: w = k 2(bp. A/(1+bp. A)), где b = k 1/k-1 = b 0 exp(q/RT). 2 Реакция в реакционном слое протекает быстро: Условия проточного реактора или вакуумной камеры p. B << p. A или необратимая хемосорбция А (k-1 = 0): Энергии активации стадии адсорбции и десорбции.
Лекция-11 Травление металлов 1 Лимитирующая стадия – превращение в адсорбционном слое: w = k 2(bp. A/(1+bp. A)), где b = k 1/k-1 = b 0 exp(q/RT). 2 Реакция в реакционном слое протекает быстро: Условия проточного реактора или вакуумной камеры p. B << p. A или необратимая хемосорбция А (k-1 = 0): Энергии активации стадии адсорбции и десорбции.
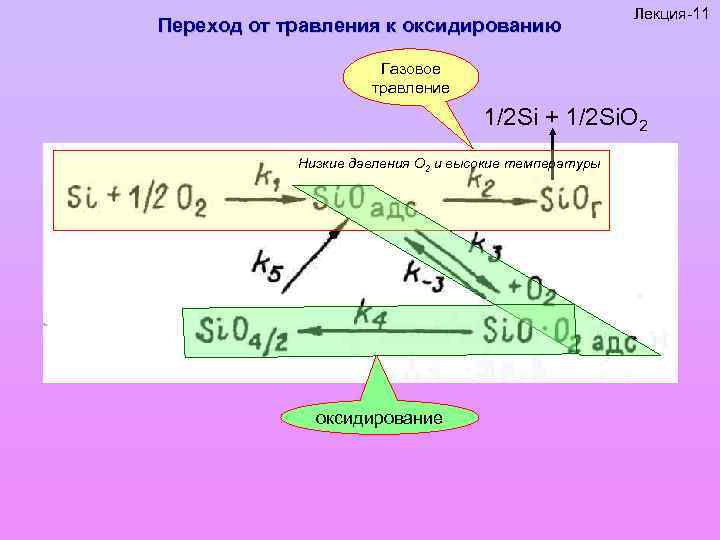 Переход от травления к оксидированию Лекция-11 Газовое травление 1/2 Si + 1/2 Si. O 2 Низкие давления О 2 и высокие температуры оксидирование
Переход от травления к оксидированию Лекция-11 Газовое травление 1/2 Si + 1/2 Si. O 2 Низкие давления О 2 и высокие температуры оксидирование
 Переход от травления к оксидированию Лекция-11 Обозначим степени заполнения поверхности: Si. Oадс - 1, Si. O∙Oадс. - 2, Si. O 4/2 - 3. Вблизи критических Т и р воспользуемся квазистационарным приближением: В критических условиях: w 2 = k 2 1 = w 4 = k 4 2. k 3 k-3>k 4 k 02 k 04 Е 2, Е 4 – энергии активации соответствующих стадий, q 3 – теплота адсорбции окислителя.
Переход от травления к оксидированию Лекция-11 Обозначим степени заполнения поверхности: Si. Oадс - 1, Si. O∙Oадс. - 2, Si. O 4/2 - 3. Вблизи критических Т и р воспользуемся квазистационарным приближением: В критических условиях: w 2 = k 2 1 = w 4 = k 4 2. k 3 k-3>k 4 k 02 k 04 Е 2, Е 4 – энергии активации соответствующих стадий, q 3 – теплота адсорбции окислителя.
 Оксидирование металлов Лекция-11 Обобщение экспериментальных данных по исследованию закономерностей роста оксидного слоя на поверхности металлов или полупроводников позволило вывести ряд простых зависимостей, связывающих толщину оксида h со временем t: Vox/Vmet < 1 или Vox/Vmet > 2. 5. Не происходит формирования сплошной пленки оксида. Процесс лимитируется диффузионным массопереносом реагентов через слой оксида.
Оксидирование металлов Лекция-11 Обобщение экспериментальных данных по исследованию закономерностей роста оксидного слоя на поверхности металлов или полупроводников позволило вывести ряд простых зависимостей, связывающих толщину оксида h со временем t: Vox/Vmet < 1 или Vox/Vmet > 2. 5. Не происходит формирования сплошной пленки оксида. Процесс лимитируется диффузионным массопереносом реагентов через слой оксида.
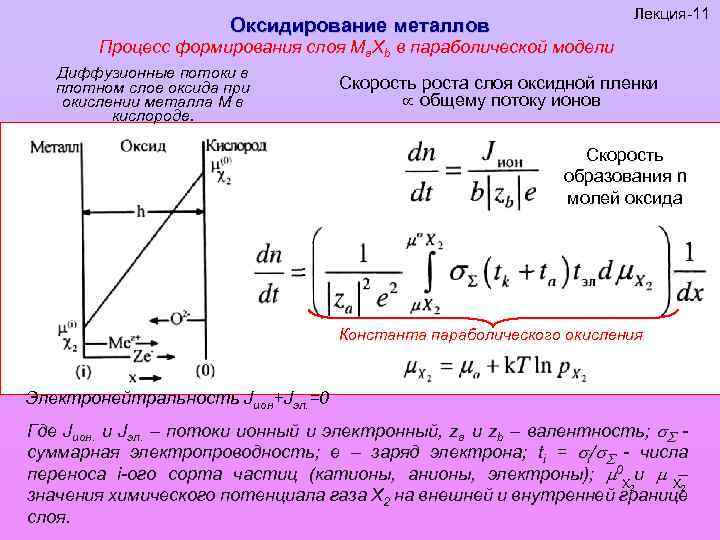 Оксидирование металлов Лекция-11 Процесс формирования слоя Ма. Хb в параболической модели Диффузионные потоки в плотном слое оксида при окислении металла М в кислороде. Скорость роста слоя оксидной пленки общему потоку ионов Скорость образования n молей оксида Константа параболического окисления Электронейтральность Jион+Jэл. =0 Где Jион. и Jэл. – потоки ионный и электронный, za и zb – валентность; суммарная электропроводность; e – заряд электрона; ti = i/ - числа переноса i-ого сорта частиц (катионы, анионы, электроны); 0 Х и Х– 2 2 значения химического потенциала газа Х 2 на внешней и внутренней границе слоя.
Оксидирование металлов Лекция-11 Процесс формирования слоя Ма. Хb в параболической модели Диффузионные потоки в плотном слое оксида при окислении металла М в кислороде. Скорость роста слоя оксидной пленки общему потоку ионов Скорость образования n молей оксида Константа параболического окисления Электронейтральность Jион+Jэл. =0 Где Jион. и Jэл. – потоки ионный и электронный, za и zb – валентность; суммарная электропроводность; e – заряд электрона; ti = i/ - числа переноса i-ого сорта частиц (катионы, анионы, электроны); 0 Х и Х– 2 2 значения химического потенциала газа Х 2 на внешней и внутренней границе слоя.
 Лекция-11 Оксидирование металлов Зависимость параболической константы от давления окислителя Рост слоя оксида МО, в котором доминируют кислородные вакансии и проводимость слоя n-типа: -типа Соотношение Нернста-Эйнштейна для константы : М + b/2 O 2 = MOb DO>>DM Оксид – проводник n – типа: o и i O Где DO и DM – коэффициенты диффузии ионов кислорода и металла в оксиде, 0 Vo. . – двухзарядные кислородные вакансии; р. О - внешнее давление кислорода; 2 i р. О - давление диссоциации оксида; сi – концентрации i сорта частиц. 2
Лекция-11 Оксидирование металлов Зависимость параболической константы от давления окислителя Рост слоя оксида МО, в котором доминируют кислородные вакансии и проводимость слоя n-типа: -типа Соотношение Нернста-Эйнштейна для константы : М + b/2 O 2 = MOb DO>>DM Оксид – проводник n – типа: o и i O Где DO и DM – коэффициенты диффузии ионов кислорода и металла в оксиде, 0 Vo. . – двухзарядные кислородные вакансии; р. О - внешнее давление кислорода; 2 i р. О - давление диссоциации оксида; сi – концентрации i сорта частиц. 2
 Оксидирование металлов Лекция-11 Зависимость параболической константы от давления окислителя Рост слоя оксида МО, в котором доминируют катионные вакансии и проводимость слоя р-типа: р-типа Соотношение Нернста-Эйнштейна для константы : М + b/2 O 2 = MOb DO<
Оксидирование металлов Лекция-11 Зависимость параболической константы от давления окислителя Рост слоя оксида МО, в котором доминируют катионные вакансии и проводимость слоя р-типа: р-типа Соотношение Нернста-Эйнштейна для константы : М + b/2 O 2 = MOb DO<


