Лекция_11_многокомп_среды.ppt
- Количество слайдов: 34
 Лекция 11 Многокомпонентные среды 1. Химические реакции в гомогенной среде. Переопределение стехиометрических коэффициентов. Время релаксации реакции. 2. Особенности реакций в твердых средах. Пример термодинамического описания реакции в твердой деформируемой среде 3. Простейшие модели многокомпонентных сред. Изотермические условия: «бездиффузионные» модели для газа и твердого тела. 4. Общий вид уравнения энергии в форме уравнения теплопроводности для среды с химическими реакциями. Частные варианты уравнения энергии. Переопределение потоков и сил 5. Простейшие неизотермические модели: газ с единственной химической реакцией; низкие и высокие скорости течения. Вязкая ньютоновкая жидкость с единственной химической реакцией. Многокомпонентная деформируемая среда: варианты уравнения энергии и обобщенных УРС. Простейшие варианты изотропной деформируемой среды
Лекция 11 Многокомпонентные среды 1. Химические реакции в гомогенной среде. Переопределение стехиометрических коэффициентов. Время релаксации реакции. 2. Особенности реакций в твердых средах. Пример термодинамического описания реакции в твердой деформируемой среде 3. Простейшие модели многокомпонентных сред. Изотермические условия: «бездиффузионные» модели для газа и твердого тела. 4. Общий вид уравнения энергии в форме уравнения теплопроводности для среды с химическими реакциями. Частные варианты уравнения энергии. Переопределение потоков и сил 5. Простейшие неизотермические модели: газ с единственной химической реакцией; низкие и высокие скорости течения. Вязкая ньютоновкая жидкость с единственной химической реакцией. Многокомпонентная деформируемая среда: варианты уравнения энергии и обобщенных УРС. Простейшие варианты изотропной деформируемой среды
 1. Химические реакции в гомогенной среде Мольные или молярные (объемные) концентрации Л. 2: ввели концентрации и установили соотношения между ними: МАСА ЧАСТИЦЫ СУММА ВСЕХ МАСС Массовые концентрации число частиц в единице объема МОЛЯРНАЯ МАСА Определение относительных концентраций остается тем же самым
1. Химические реакции в гомогенной среде Мольные или молярные (объемные) концентрации Л. 2: ввели концентрации и установили соотношения между ними: МАСА ЧАСТИЦЫ СУММА ВСЕХ МАСС Массовые концентрации число частиц в единице объема МОЛЯРНАЯ МАСА Определение относительных концентраций остается тем же самым
 Л. 2: Ввели определение координаты реакции и нашли производство энтропии, связанное с реакциями: - скорость реакции j Изменение числа частиц сорта i в реакции j координата или путь реакции; одинакова для всех веществ Изменение числа частиц сорта i во всех реакциях в единице объема закрытой системы В закрытой системе (1) для любого i
Л. 2: Ввели определение координаты реакции и нашли производство энтропии, связанное с реакциями: - скорость реакции j Изменение числа частиц сорта i в реакции j координата или путь реакции; одинакова для всех веществ Изменение числа частиц сорта i во всех реакциях в единице объема закрытой системы В закрытой системе (1) для любого i
 Однородные системы Переопределение стехиометрических коэффициентов Уравнение баланса для компонента i (2) Кг/(м 3 с) Моль /(м 3 с) Дж/кг Уравнение реакции: Дж/моль Дж /(К м 3 с) При совместном протекании r химических реакций аналогичные соотношения имеют вид Л 2 Перейдем в уравнениях баланса (2) к мольным концентрациям, используя связь: Это возможно, если Моль/(м 3 с) Т. е. , получим (1)
Однородные системы Переопределение стехиометрических коэффициентов Уравнение баланса для компонента i (2) Кг/(м 3 с) Моль /(м 3 с) Дж/кг Уравнение реакции: Дж/моль Дж /(К м 3 с) При совместном протекании r химических реакций аналогичные соотношения имеют вид Л 2 Перейдем в уравнениях баланса (2) к мольным концентрациям, используя связь: Это возможно, если Моль/(м 3 с) Т. е. , получим (1)
 Для произвольной ситуации сделаем некоторые преобразования: В соответствии с общей термодинамической теорией можем записать Потоком для химической реакции является ее скорость Матрица феноменологических коэффициентов (в соответствии с общей теории) является симметричной и положительно определенной. Это означает, что Переопределим стехиометрические коэффициенты так, чтобы выполнялись соотношения число реагентов, участвующих в реакции i число продуктов этой реакции
Для произвольной ситуации сделаем некоторые преобразования: В соответствии с общей термодинамической теорией можем записать Потоком для химической реакции является ее скорость Матрица феноменологических коэффициентов (в соответствии с общей теории) является симметричной и положительно определенной. Это означает, что Переопределим стехиометрические коэффициенты так, чтобы выполнялись соотношения число реагентов, участвующих в реакции i число продуктов этой реакции
 Новые стехиометрические коэффициенты связаны со старыми коэффициентами равенством Тогда для одной реакции имеем число реагентов, участвующих в реакции i где В результате для одной реакции имеем Введем величину Интегрируя уравнения по времени, находим Следовательно, задание ξ в некоторый момент времени эквивалентно заданию в этот момент всех массовых концентраций (или мольных при мольном описании). Производство энтропии и другие выводы не изменяются.
Новые стехиометрические коэффициенты связаны со старыми коэффициентами равенством Тогда для одной реакции имеем число реагентов, участвующих в реакции i где В результате для одной реакции имеем Введем величину Интегрируя уравнения по времени, находим Следовательно, задание ξ в некоторый момент времени эквивалентно заданию в этот момент всех массовых концентраций (или мольных при мольном описании). Производство энтропии и другие выводы не изменяются.
 Время релаксации реакции Пусть протекает единственная реакция Осуществимость реакции зависит от условий, в которых она протекает. Так, из уравнения Гиббса для многокомпонентной системы найдем Для единственной реакции Тогда сродство химической реакции можно определить следующим образом (1) Используя другие потенциалы сможем записать: Для каждой реакции: (2)
Время релаксации реакции Пусть протекает единственная реакция Осуществимость реакции зависит от условий, в которых она протекает. Так, из уравнения Гиббса для многокомпонентной системы найдем Для единственной реакции Тогда сродство химической реакции можно определить следующим образом (1) Используя другие потенциалы сможем записать: Для каждой реакции: (2)
 (3) или Так как, по определению, сродство реакции A зависит от координаты реакции ξ и двух других переменных состояния, соответствующих условиям протекания реакции: или , а в условиях равновесия то равновесное значение химического сродства Разложим химическое сродство в ряд Тейлора вблизи равновесного значения, ограничиваясь первым членом разложения (4) Феноменологический коэффициент l для всех четырех уравнений одинаков, но производные - различны Соответственно четырем условиям протекания реакции, имеем четыре уравнения. Например, в условиях постоянства температуры и объема:
(3) или Так как, по определению, сродство реакции A зависит от координаты реакции ξ и двух других переменных состояния, соответствующих условиям протекания реакции: или , а в условиях равновесия то равновесное значение химического сродства Разложим химическое сродство в ряд Тейлора вблизи равновесного значения, ограничиваясь первым членом разложения (4) Феноменологический коэффициент l для всех четырех уравнений одинаков, но производные - различны Соответственно четырем условиям протекания реакции, имеем четыре уравнения. Например, в условиях постоянства температуры и объема:
 Проинтегрировав (4) по времени, найдем где время релаксации химической реакции к равновесным условиям ее протекания Соответственно четырем типам условий протекания химических реакций в простой гомогенной среде имеем четыре различных времени релаксации Все эти величины положительны, так как термодинамические потенциалы в условиях равновесия имеют минимум. Различные времена релаксации химической реакции связаны между собой термодинамическими соотношениями, которые легко получить, используя термодинамические соотношения Максвелла. На основе этого подхода строится общая теория термодинамической релаксации
Проинтегрировав (4) по времени, найдем где время релаксации химической реакции к равновесным условиям ее протекания Соответственно четырем типам условий протекания химических реакций в простой гомогенной среде имеем четыре различных времени релаксации Все эти величины положительны, так как термодинамические потенциалы в условиях равновесия имеют минимум. Различные времена релаксации химической реакции связаны между собой термодинамическими соотношениями, которые легко получить, используя термодинамические соотношения Максвелла. На основе этого подхода строится общая теория термодинамической релаксации
 2. Особенности химических реакций в твердой фазе 1. Браун Р. , Доллимор Д. , Галвей А. Реакции твердых тел / М. : Мир, 1983. – 360 С. 2. Вест. А Химия твердого тела. Теория м приложения, в 2 -х частях, М. : Мир, 1988 Долгое время считалось, что реакции (химические и фазовые превращения) в твердой фазе вообще не идут или идут чрезвычайно медленно, что делает их бесполезными для практического использования. Систематическое исследование в этой области началось лишь в 30 -е годы, что связано непосредственно с развитием новых технологий. Под твердофазными превращениями часто понимают те, которые идут с участием твердых веществ, т. е. хоть одно из веществ является твердым (реагент, промежуточный продукт, катализатор). Примеры: Полимеризация в твердой фазе СВ-синтез в твердой фазе Твердофазная детонация Дегидратация (сушка) Реакции на пористых катализаторах Окисление металлов Образование и распад твердых растворов Полиморфные превращения, связанные с изменением состава Разложение в твердой фазе (ВВ, ПХА…)
2. Особенности химических реакций в твердой фазе 1. Браун Р. , Доллимор Д. , Галвей А. Реакции твердых тел / М. : Мир, 1983. – 360 С. 2. Вест. А Химия твердого тела. Теория м приложения, в 2 -х частях, М. : Мир, 1988 Долгое время считалось, что реакции (химические и фазовые превращения) в твердой фазе вообще не идут или идут чрезвычайно медленно, что делает их бесполезными для практического использования. Систематическое исследование в этой области началось лишь в 30 -е годы, что связано непосредственно с развитием новых технологий. Под твердофазными превращениями часто понимают те, которые идут с участием твердых веществ, т. е. хоть одно из веществ является твердым (реагент, промежуточный продукт, катализатор). Примеры: Полимеризация в твердой фазе СВ-синтез в твердой фазе Твердофазная детонация Дегидратация (сушка) Реакции на пористых катализаторах Окисление металлов Образование и распад твердых растворов Полиморфные превращения, связанные с изменением состава Разложение в твердой фазе (ВВ, ПХА…)
 Особенности реакций с участием твердых веществ: 1. Пространственная разделенность реагентов, а также реагентов и продуктов реакции, наличие границы раздела, локализация реакции на границе раздела фаз. Процесс формирования реакционной границы раздела состоит из целого ряда событий: образование зародышей, их рост, слияние 2. Важная роль процессов переноса. Массоперенос имеет место в большинстве реакций. Имеются аналоги диффузионных процессов – перенос дислокаций, вакансий, пор 3. Наличие и определяющая роль обратных связей между разными физическими процессами. Простые типы обратных связей, известные из макрокинетики, довольно редкое явлений
Особенности реакций с участием твердых веществ: 1. Пространственная разделенность реагентов, а также реагентов и продуктов реакции, наличие границы раздела, локализация реакции на границе раздела фаз. Процесс формирования реакционной границы раздела состоит из целого ряда событий: образование зародышей, их рост, слияние 2. Важная роль процессов переноса. Массоперенос имеет место в большинстве реакций. Имеются аналоги диффузионных процессов – перенос дислокаций, вакансий, пор 3. Наличие и определяющая роль обратных связей между разными физическими процессами. Простые типы обратных связей, известные из макрокинетики, довольно редкое явлений
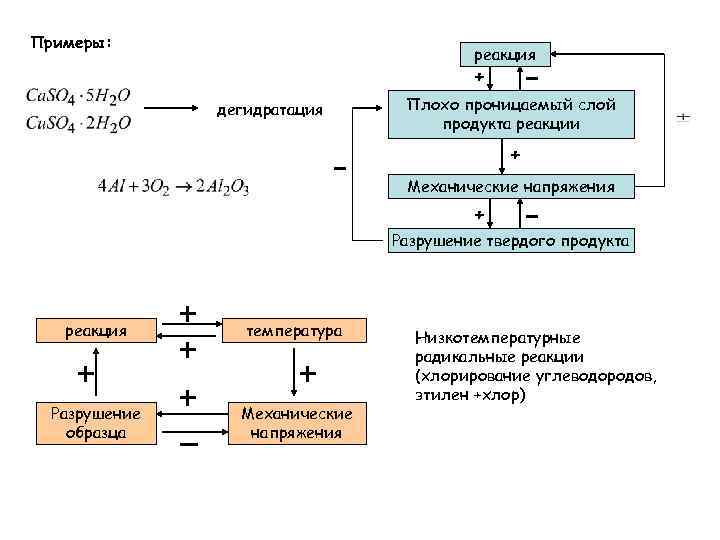 Примеры: реакция + дегидратация Плохо проницаемый слой продукта реакции + Механические напряжения + Разрушение твердого продукта реакция температура Разрушение образца Механические напряжения Низкотемпературные радикальные реакции (хлорирование углеводородов, этилен +хлор)
Примеры: реакция + дегидратация Плохо проницаемый слой продукта реакции + Механические напряжения + Разрушение твердого продукта реакция температура Разрушение образца Механические напряжения Низкотемпературные радикальные реакции (хлорирование углеводородов, этилен +хлор)
 Вариант термодинамического описания реакции в однородной деформируемой среде Если в однородной деформируемой среде протекают химические реакции, то уравнение Гиббса можно представить в виде (1) или (2) сродство химической реакции с номером Для единственной реакции Выделенные слагаемые дают нам УРС для термоупругой среды Появились новые перекрестные эффекты , - координата этой реакции (3) (4) (5) (6)
Вариант термодинамического описания реакции в однородной деформируемой среде Если в однородной деформируемой среде протекают химические реакции, то уравнение Гиббса можно представить в виде (1) или (2) сродство химической реакции с номером Для единственной реакции Выделенные слагаемые дают нам УРС для термоупругой среды Появились новые перекрестные эффекты , - координата этой реакции (3) (4) (5) (6)
 Аналогично газам и жидкостям -энтропия реакции В изотропной среде -деформация превращения или химическая деформация УРС: (7) Определяем иным способом Например, для шаровой части тензора неупругие напряжения Аналогично (8) газам и жидкостям
Аналогично газам и жидкостям -энтропия реакции В изотропной среде -деформация превращения или химическая деформация УРС: (7) Определяем иным способом Например, для шаровой части тензора неупругие напряжения Аналогично (8) газам и жидкостям
 Полный тензор деформаций (9) Это деление весьма условно!!! Аналогично предыдущему определим время релаксации реакции: (10) (11) В неоднородных средах появляются дополнительные особенности (12) Вязкие напряжения, девиатор (формальная теория) градиент вектора скорости
Полный тензор деформаций (9) Это деление весьма условно!!! Аналогично предыдущему определим время релаксации реакции: (10) (11) В неоднородных средах появляются дополнительные особенности (12) Вязкие напряжения, девиатор (формальная теория) градиент вектора скорости
 3. Простейшие модели многокомпонентных сред, Т=const Допустим, реакция протекает в изотермических условиях, но сопровождается диффузий или конвекцией. В таких условиях могут протекать, например, реакции ионизации и рекомбинации. В этом случае нам требуются уравнения баланса для компонентов, уравнение неразрывности и уравнение движения (13) 1. Пусть скорость v настолько велика, что различием скоростей компонентов можно пренебречь Т. е. , диффузией Это возможно, если принять или можно пренебречь Домножим уравнение неразрывности на и просуммируем с или (14)
3. Простейшие модели многокомпонентных сред, Т=const Допустим, реакция протекает в изотермических условиях, но сопровождается диффузий или конвекцией. В таких условиях могут протекать, например, реакции ионизации и рекомбинации. В этом случае нам требуются уравнения баланса для компонентов, уравнение неразрывности и уравнение движения (13) 1. Пусть скорость v настолько велика, что различием скоростей компонентов можно пренебречь Т. е. , диффузией Это возможно, если принять или можно пренебречь Домножим уравнение неразрывности на и просуммируем с или (14)
 Пусть тензор напряжений – шаровой, т. е. уравнение движения примет вид Поступим с ним аналогично уравнениям для компонентов (для каждой компоненты вектора скорости), т. е. складываем с уравнением неразрывности, домноженным на компоненту вектора скорости: или (15) Т. е. , все уравнения (14) (15) имеют единый вид, что удобно для численного решения. Осталось добавить УРС Идеальный баротропный газ или Неидеальный газ
Пусть тензор напряжений – шаровой, т. е. уравнение движения примет вид Поступим с ним аналогично уравнениям для компонентов (для каждой компоненты вектора скорости), т. е. складываем с уравнением неразрывности, домноженным на компоненту вектора скорости: или (15) Т. е. , все уравнения (14) (15) имеют единый вид, что удобно для численного решения. Осталось добавить УРС Идеальный баротропный газ или Неидеальный газ
 2. Пусть единственная изотермическая химическая реакция протекает в деформируемой ( «упругой» ) среде (1) В случае малых упругих деформаций Вследствие различных масштабов разных физических процессов можно принять, что диффузионные процессы влияют на кинетическую функцию (т. е. «пренебрегаем» диффузией по другой причине) вследствие «тонких» процессов на микроуровне А - зависит от условий осуществления реакции Закон действующих масс: (2) (3) или иные модели
2. Пусть единственная изотермическая химическая реакция протекает в деформируемой ( «упругой» ) среде (1) В случае малых упругих деформаций Вследствие различных масштабов разных физических процессов можно принять, что диффузионные процессы влияют на кинетическую функцию (т. е. «пренебрегаем» диффузией по другой причине) вследствие «тонких» процессов на микроуровне А - зависит от условий осуществления реакции Закон действующих масс: (2) (3) или иные модели
 3. Среда с объемной вязкостью (формальная теория) (1) Преобразование уравнения движения Поступаем аналогично предыдущему: (2) (3) +УРС для и Не изменяется
3. Среда с объемной вязкостью (формальная теория) (1) Преобразование уравнения движения Поступаем аналогично предыдущему: (2) (3) +УРС для и Не изменяется
 4. Общий вид уравнения энергии в форме уравнения теплопроводности для среды с химическими реакциями Для вывода уравнения энергии в форме уравнения теплопроводности для многокомпонентных сред, как и для простых, воспользуемся уравнением Гиббса и уравнением баланса внутренней энергии (т. е. , совершенно аналогично простым средам) В общем случае (16) Подчеркнутые слагаемые взаимно уничтожаются (в приближении малых деформаций)
4. Общий вид уравнения энергии в форме уравнения теплопроводности для среды с химическими реакциями Для вывода уравнения энергии в форме уравнения теплопроводности для многокомпонентных сред, как и для простых, воспользуемся уравнением Гиббса и уравнением баланса внутренней энергии (т. е. , совершенно аналогично простым средам) В общем случае (16) Подчеркнутые слагаемые взаимно уничтожаются (в приближении малых деформаций)
 остается Частные варианты уравнения энергии (17) 1. Идеальная простая среда, 2. Многокомпонентная идеальная среда (18) Дальнейшая конкретизация зависит от того, что «удобно» принять постоянным или (19) Подставим (19) в (18):
остается Частные варианты уравнения энергии (17) 1. Идеальная простая среда, 2. Многокомпонентная идеальная среда (18) Дальнейшая конкретизация зависит от того, что «удобно» принять постоянным или (19) Подставим (19) в (18):
 Подставим (19) в (18): или (20) Аналогично можем найти (если в качестве основного потенциала выбрать свободную энергию Гельмгольца): (21) Воспользуемся теперь уравнениями баланса для компонентов Подставим их в (20) Тепловыделение в реакции i (22) суммарный поток тепла Поток тепла можем переопределить, при этом производство энтропии не изменяется
Подставим (19) в (18): или (20) Аналогично можем найти (если в качестве основного потенциала выбрать свободную энергию Гельмгольца): (21) Воспользуемся теперь уравнениями баланса для компонентов Подставим их в (20) Тепловыделение в реакции i (22) суммарный поток тепла Поток тепла можем переопределить, при этом производство энтропии не изменяется
 Действительно: Производство энтропии, связанное процессами теплопроводности, диффузии и химическими реакциями: Для диффузии подробно все выведем позже Поток энтропии Введем новое определение для потока тепла Тогда найдем новое определение потока энтропии Тождественные преобразования: Сумма в третьем слагаемом (23)
Действительно: Производство энтропии, связанное процессами теплопроводности, диффузии и химическими реакциями: Для диффузии подробно все выведем позже Поток энтропии Введем новое определение для потока тепла Тогда найдем новое определение потока энтропии Тождественные преобразования: Сумма в третьем слагаемом (23)
 Все подставляем в уравнение баланса энтропии Подставим в это уравнение: Результат не изменился. Если имеется внешняя массовая сила, то производство энтропии, связанное с диффузионными процессами, принимает вид
Все подставляем в уравнение баланса энтропии Подставим в это уравнение: Результат не изменился. Если имеется внешняя массовая сила, то производство энтропии, связанное с диффузионными процессами, принимает вид
 Простейшие неизотермические модели многокомпонентных сред 1. Газ с единственной химической реакцией в неизотермических условиях Протекает единственная реакция реагент продукт (1) (2) (3) Из (21): (4) Неизвестные: 6+ Уравнений – 6 Требуется добавить уравнение состояния. Например, газ - идеальный: (5, а) Газ – неидеальный: (5, б; Л. 7)
Простейшие неизотермические модели многокомпонентных сред 1. Газ с единственной химической реакцией в неизотермических условиях Протекает единственная реакция реагент продукт (1) (2) (3) Из (21): (4) Неизвестные: 6+ Уравнений – 6 Требуется добавить уравнение состояния. Например, газ - идеальный: (5, а) Газ – неидеальный: (5, б; Л. 7)
 Частный вариант 1. 1: Среда несжимаемая: Скорость мала и постоянна газ – идеальный: (6) (7) Нет перекрестных потоков Подобие полей температуры и концентраций в газах: Базовые уравнения теории горения газов (самый простой вариант) (8) Введем новые стехиометрические коэффициенты, функцию скорости и тепловыделение (9) Дж/кг
Частный вариант 1. 1: Среда несжимаемая: Скорость мала и постоянна газ – идеальный: (6) (7) Нет перекрестных потоков Подобие полей температуры и концентраций в газах: Базовые уравнения теории горения газов (самый простой вариант) (8) Введем новые стехиометрические коэффициенты, функцию скорости и тепловыделение (9) Дж/кг
 Домножим уравнение для компонента на и вычтем одно из другого , а уравнение теплопроводности – на (10) Т. е. , при условии подобия полей теплодиффузионная задача сводится к уравнению для энтальпии
Домножим уравнение для компонента на и вычтем одно из другого , а уравнение теплопроводности – на (10) Т. е. , при условии подобия полей теплодиффузионная задача сводится к уравнению для энтальпии
 Частный вариант 1. 2. Для высокой скорости течения пренебрегаем диффузией и теплопроводностью по сравнению с конвективным переносом – все аналогично изотермической модели: или Домножаем уравнение неразрывности на (1) или и складываем с уравнением теплопроводности: (11) или Аналогично поступаем с уравнением для компонента: (12) или и с уравнением движения (для каждой компоненты вектора скорости) из которых получаем (13) Т. е. , все уравнения имеют единый вид, что удобно для численного решения
Частный вариант 1. 2. Для высокой скорости течения пренебрегаем диффузией и теплопроводностью по сравнению с конвективным переносом – все аналогично изотермической модели: или Домножаем уравнение неразрывности на (1) или и складываем с уравнением теплопроводности: (11) или Аналогично поступаем с уравнением для компонента: (12) или и с уравнением движения (для каждой компоненты вектора скорости) из которых получаем (13) Т. е. , все уравнения имеют единый вид, что удобно для численного решения
 2. Вязкая (ньютоновская) жидкость с единственной химической реакцией в неизотермических условиях В общем случае жидкость (газ) сжимаемая Остается работа вязких напряжений Перекрестные эффекты между х. р. и давлением! - в качестве УРС Если жидкость – несжимаемая, выделенные слагаемые 0 Но в уравнении движения останется градиент вязкого давления!
2. Вязкая (ньютоновская) жидкость с единственной химической реакцией в неизотермических условиях В общем случае жидкость (газ) сжимаемая Остается работа вязких напряжений Перекрестные эффекты между х. р. и давлением! - в качестве УРС Если жидкость – несжимаемая, выделенные слагаемые 0 Но в уравнении движения останется градиент вязкого давления!
 3. Многокомпонентная деформируемая (твердая) среда если вязких сил и внешних массовых сил нет и тензор напряжений – симметричен (14) А) или Уравнение теплопроводности (15) для упругой среды с химическими реакциями, а) - тензор коэффициентов термоупругости
3. Многокомпонентная деформируемая (твердая) среда если вязких сил и внешних массовых сил нет и тензор напряжений – симметричен (14) А) или Уравнение теплопроводности (15) для упругой среды с химическими реакциями, а) - тензор коэффициентов термоупругости
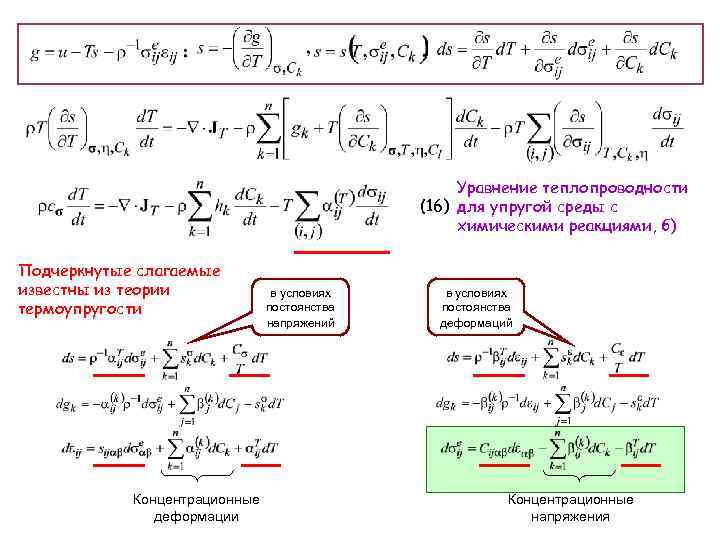 Уравнение теплопроводности (16) для упругой среды с химическими реакциями, б) Подчеркнутые слагаемые известны из теории термоупругости Концентрационные деформации в условиях постоянства напряжений в условиях постоянства деформаций Концентрационные напряжения
Уравнение теплопроводности (16) для упругой среды с химическими реакциями, б) Подчеркнутые слагаемые известны из теории термоупругости Концентрационные деформации в условиях постоянства напряжений в условиях постоянства деформаций Концентрационные напряжения
 Изотропная среда Выделенные УРС принимают вид Малые деформации (плотность перестает быть искомой величиной) Thermal elastic diffusion with reaction Система уравнений термоупругой диффузии с реакцией В этом случае от приращений можем перейти к абсолютным величинам
Изотропная среда Выделенные УРС принимают вид Малые деформации (плотность перестает быть искомой величиной) Thermal elastic diffusion with reaction Система уравнений термоупругой диффузии с реакцией В этом случае от приращений можем перейти к абсолютным величинам
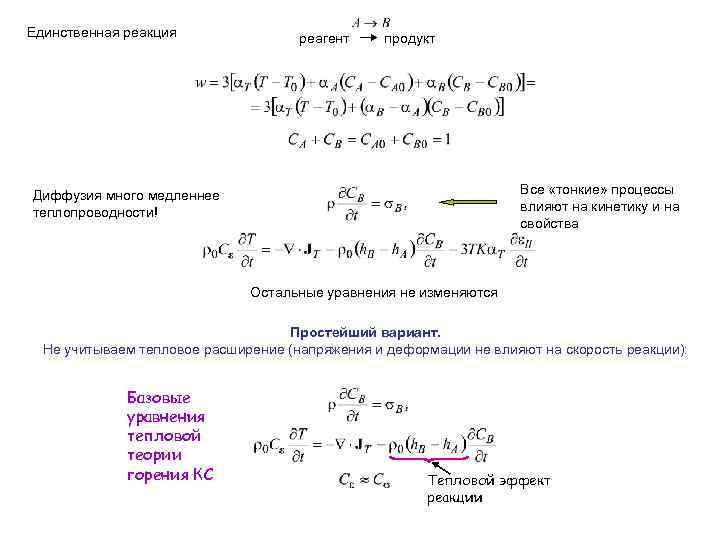 Единственная реакция реагент продукт Все «тонкие» процессы влияют на кинетику и на свойства Диффузия много медленнее теплопроводности! Остальные уравнения не изменяются Простейший вариант. Не учитываем тепловое расширение (напряжения и деформации не влияют на скорость реакции): Базовые уравнения тепловой теории горения КС Тепловой эффект реакции
Единственная реакция реагент продукт Все «тонкие» процессы влияют на кинетику и на свойства Диффузия много медленнее теплопроводности! Остальные уравнения не изменяются Простейший вариант. Не учитываем тепловое расширение (напряжения и деформации не влияют на скорость реакции): Базовые уравнения тепловой теории горения КС Тепловой эффект реакции
 Требуются определить потоки тепла и массы, скорости реакций, коэффициенты концентрационного расширения, свойства материалов, смесей и т. п.
Требуются определить потоки тепла и массы, скорости реакций, коэффициенты концентрационного расширения, свойства материалов, смесей и т. п.


