Coll_Chem_L9.ppt
- Количество слайдов: 22

Лекция 11 Механизм коагуляции Механизм образования почв Влияние расклинивающего давления на прочность материалов Пептизация Эмульсии
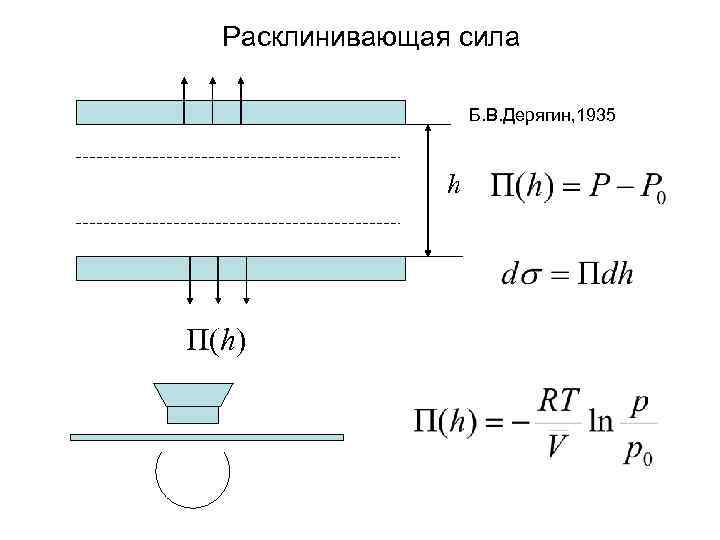
Расклинивающая сила Б. В. Дерягин, 1935 h П(h)

Теория Смолуховского Все соударения эффективны R – диаметр частиц быстрая коагуляция период коагуляции при τ’ = 2 τ t =τ v = v 0/2

Медленная коагуляция Теория Дерягина, Ландау, Фейрвея, Овербека (ДЛФО) • Дерягин: Если два двойных слоя перекрываются => возникает осмотическое давление => появляется расклинивающая сила • Есть притяжение обусловленное силами Лондона • На малых расстояниях преобладает притяжение

Теория Дерягина, Ландау, Фейрвея, Овербека (ДЛФО) A ≈ 10 -12 эрг – константа Гамакера γ = f (ψ1, z, T), ψ1 z =const U периодические коллоидные структуры: глубина минимума > k. T h

Механизм коагуляции Гетерокоагуляция взаимная коагуляция адгезионная коагуляция Адсорбционно-сольватный = структурно-механический барьер стабилизаторы Денатурация белков в адсорбционном слое в/м, в/т защитное действие Образование почв

Механизм коагуляции Гетерокоагуляция взаимная коагуляция адгезионная коагуляция Адсорбционно-сольватный = структурно-механический барьер стабилизаторы Денатурация белков в адсорбционном слое в/м, в/т защитное действие Образование почв
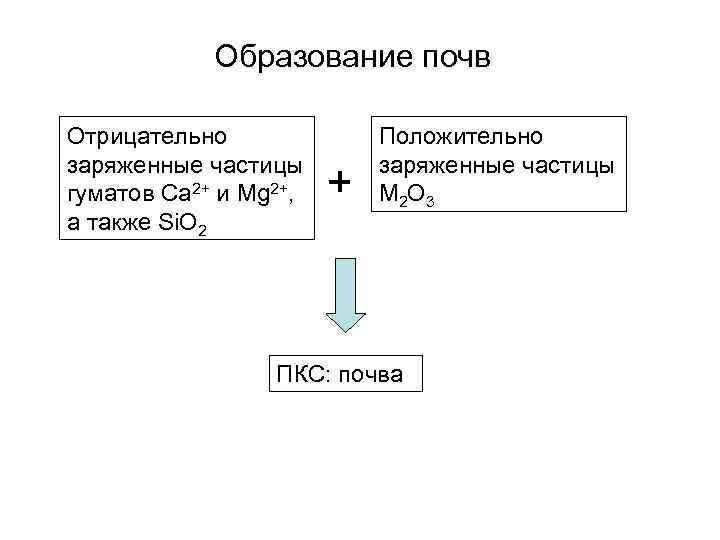
Образование почв Отрицательно заряженные частицы гуматов Ca 2+ и Mg 2+, а также Si. O 2 + Положительно заряженные частицы M 2 O 3 ПКС: почва
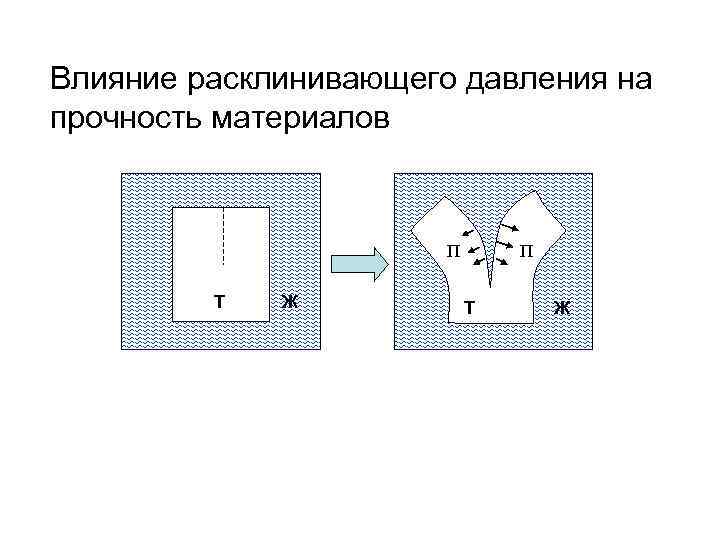
Влияние расклинивающего давления на прочность материалов П Т Ж
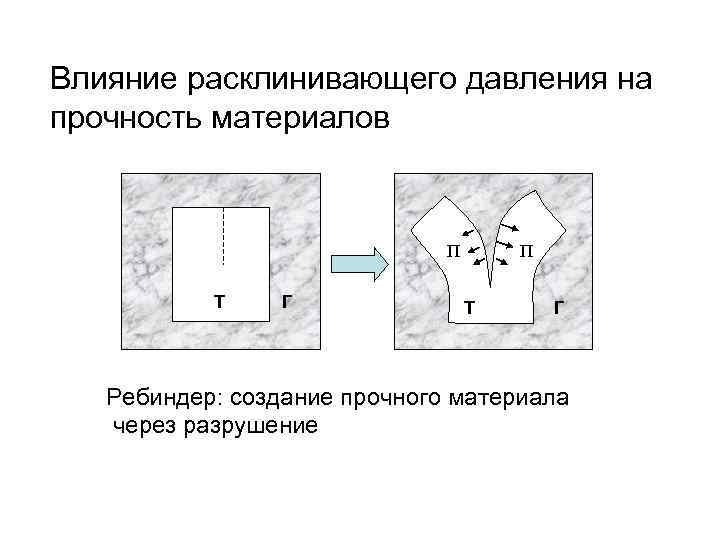
Влияние расклинивающего давления на прочность материалов П Т Г Ребиндер: создание прочного материала через разрушение
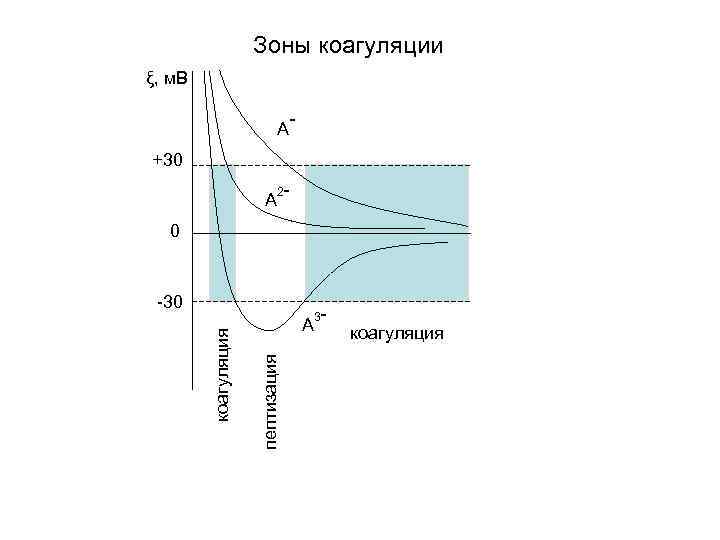
Зоны коагуляции ξ, м. В A - +30 A 2 - 0 A пептизация коагуляция -30 3 - коагуляция

Пептизация Процесс, обратный коагуляции Причины: удаление электролита, повышение поверхностного заряда Отличается от диспергирования твердой фазы Агрегативно-равновесные системы
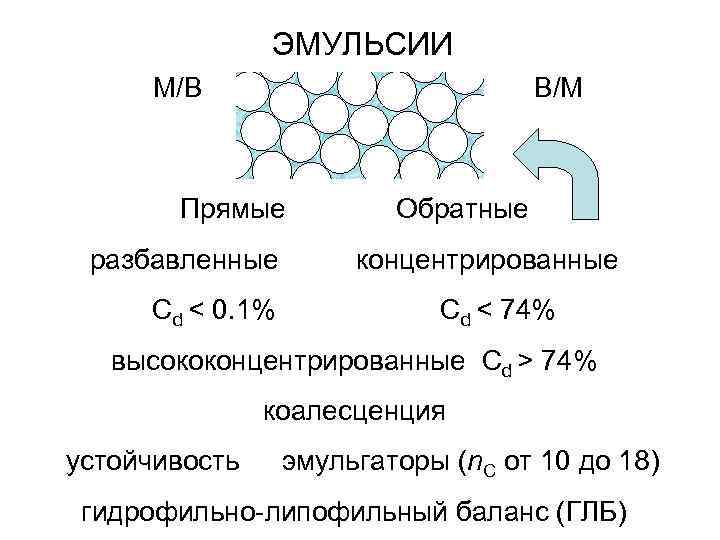
ЭМУЛЬСИИ М/В В/М Прямые разбавленные Cd < 0. 1% Обратные концентрированные Cd < 74% высококонцентрированные Cd > 74% коалесценция устойчивость эмульгаторы (n. C от 10 до 18) гидрофильно-липофильный баланс (ГЛБ)
ЭМУЛЬСИИ Порошковые эмульгаторы тип эмульсии в концентрированных системах Обращение фаз Критические эмульсии Деэмульгаторы: электролиты и со. ПАВ

Пены Аэрозоли
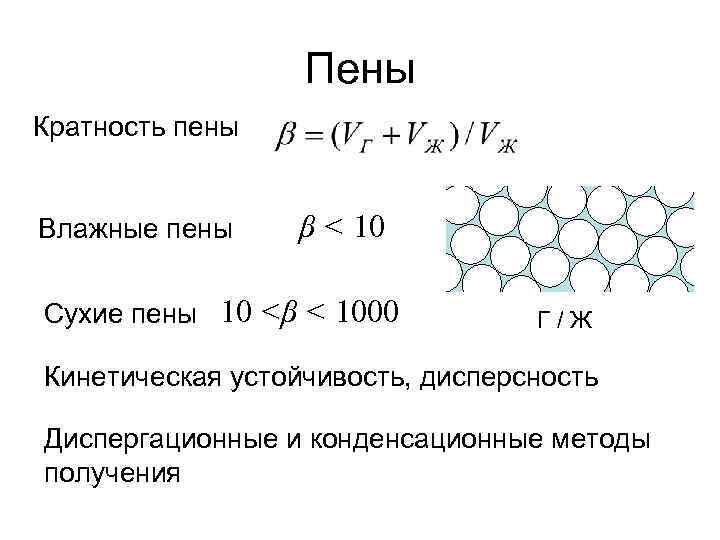
Пены Кратность пены Влажные пены β < 10 Сухие пены 10 <β < 1000 Г/Ж Кинетическая устойчивость, дисперсность Диспергационные и конденсационные методы получения

Свободные пленки толстые тонкие черные пленки от 4 до 10 нм сильные пенообразователи Устойчивость пен: Теория Гиббса Эффект Марагони

Аэрозоли туманы пыль дым (Ж/Г) (Т/Г) диспергационные аэрозоли (Т/Г) конденсационные аэрозоли системы смешанного типа Размер частиц, см Вода туман слоистые облака кучевые облака Дым окиси цинка табачный пятиокиси фосфора Пыль природная Споры и пыльца растений 5 • 10 -5 10 -4 - 10 -3 - 10 -2 5 • 10 -6 10 -5 -10 -4 -10 -3 10 -4 -10 -2 10 -4 -10 -3

Аэрозоли Длина свободного пробега, λ при, r >> λ при, r << λ закон Стокса Формула Кеннингема Заряд частицы при r = 10 -4 см, Т = 300 К qср= 4 e r = 10 -5 см qср= e Электрофорез, термофорез (фотофорез), термопреципитация

Коагуляционные структуры структурированные жидкости (ПКС) → структуры с фазовыми контактами → монолитные тела Синерезис Золь Si. O 2 → силикагель → опал → халцедон → кварц коагуляционные и конденсационные структуры (с фазовыми контактами) Число адгезии (оседания) γ 90 и γ 180
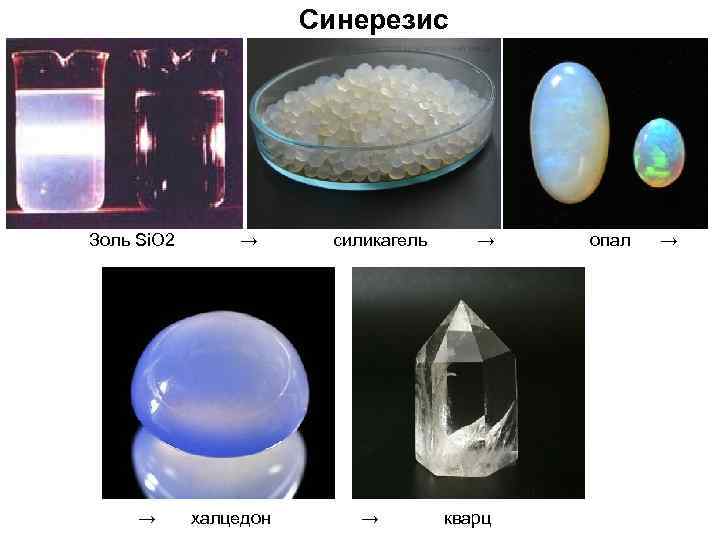
Синерезис Золь Si. O 2 → → халцедон силикагель → → кварц опал →

Энергия взаимодействия дисперсных частиц Сила отрыва стеклянных сферических частиц Удельная свободная энергия взаимодействия Fa Fa /2, эрг/см 2 Среда: воздух гептан вода Стекло >40 ~20 <0, 01 Стекло метилированное 22 <0, 01 40 величины fa и Fa возрастают с увеличением времени контакта
Coll_Chem_L9.ppt