Лекция 11 карбоновые кислоты и производные.ppt
- Количество слайдов: 34

Лекция 11. Карбоновые кислоты и их производные.

Номенклатура. В системе IUPAC карбоксильная группа является одной из самых старших, поэтому в названиях органических соединений эта группа упоминается в конце названия (в окончании) –овая кислота. В редких случаях, когда необходимо упомянуть карбоксильную группу на фоне других старших групп в приставке карбокси-. Многие карбоновые кислоты имеют часто используемые тривиальные названия.
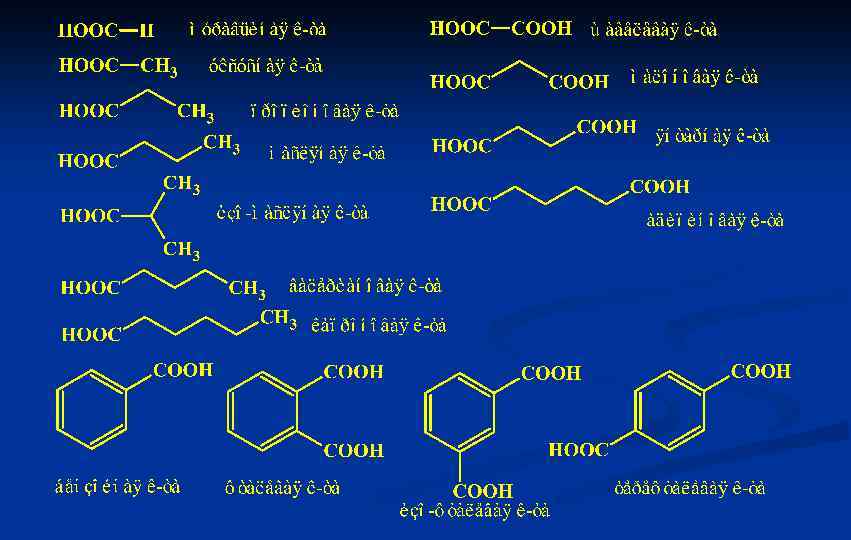

Методы получения карбоновых кислот §Окисление первичных спиртов и альдегидов под действием K 2 Cr 2 O 7, KMn. O 4 (см. лекции 7, 8, 10). §Окисление линейных и циклических алкенов под действием KMn. O 4 или озона с последующим окислительным гидролизом озонидов (см. лекцию 2).
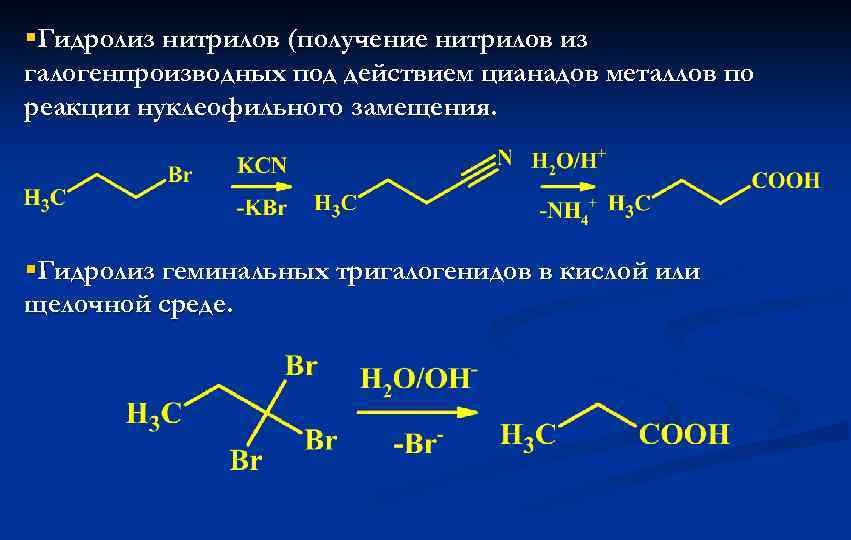
§Гидролиз нитрилов (получение нитрилов из галогенпроизводных под действием цианадов металлов по реакции нуклеофильного замещения. §Гидролиз геминальных тригалогенидов в кислой или щелочной среде.
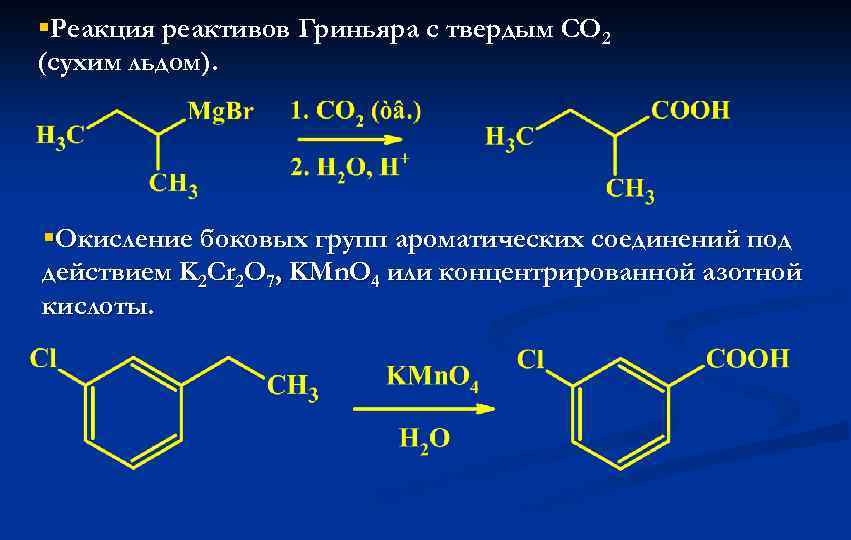
§Реакция реактивов Гриньяра с твердым СО 2 (сухим льдом). §Окисление боковых групп ароматических соединений под действием K 2 Cr 2 O 7, KMn. O 4 или концентрированной азотной кислоты.

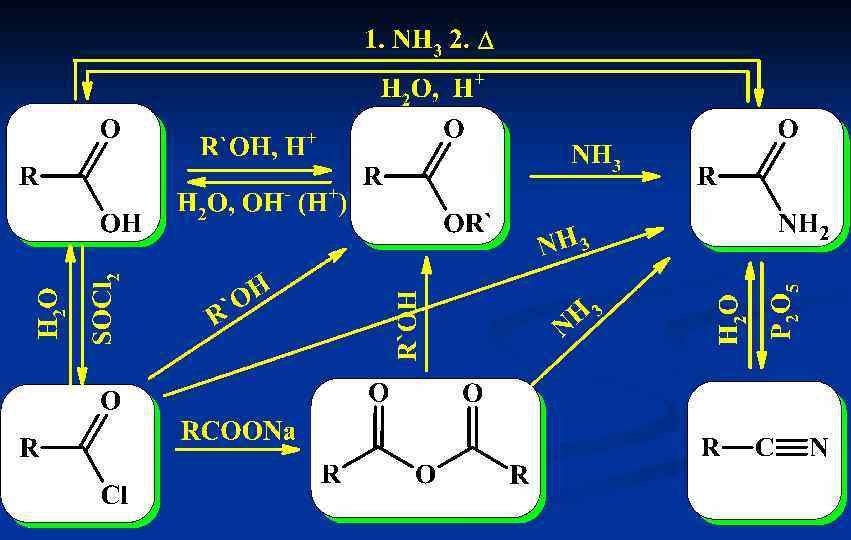
Химические свойства карбоновых кислот и их производных. Благодаря влиянию гидроксильного атома кислорода карбонильная активность центрального атома углерода и, следовательно, склонность к реакциям нуклеофильного присоединения сильно понижается. Наоборот, акцепторное влияние карбонильной группы в целом увеличивает поляризацию связи О-Н в гидроксильной группе, что приводит к облегчению диссоциации этой связи по кислотному типу по сравнению со спиртами. р. Ка карбоновых кислот близко к 5 и степень диссоциации в 0, 1 молярном растворе около 1%.
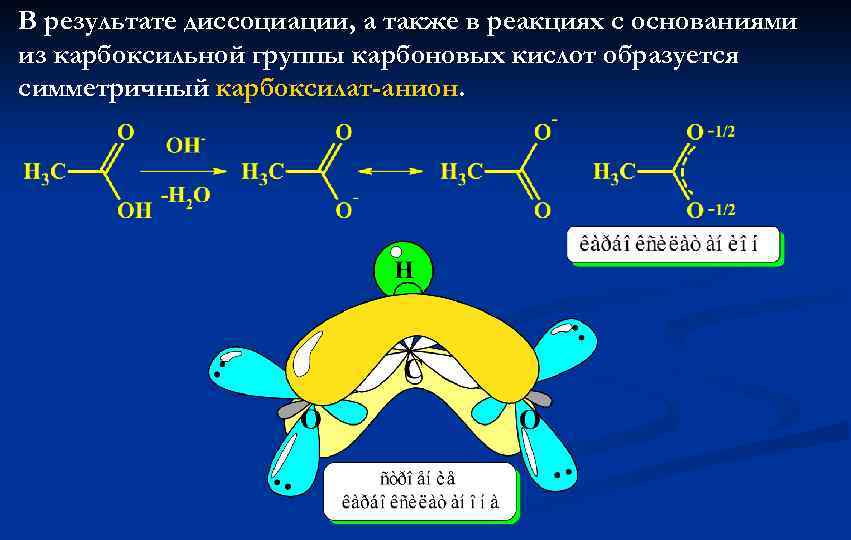
В результате диссоциации, а также в реакциях с основаниями из карбоксильной группы карбоновых кислот образуется симметричный карбоксилат-анион.
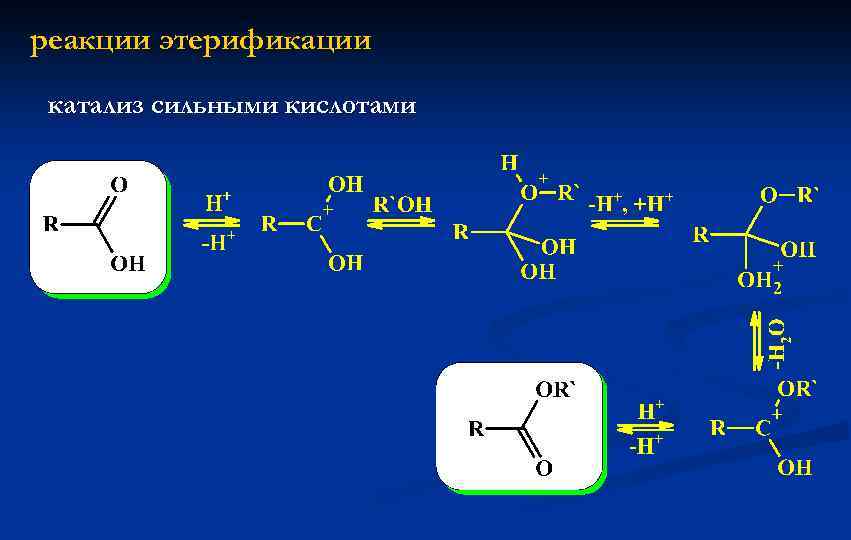
реакции этерификации катализ сильными кислотами
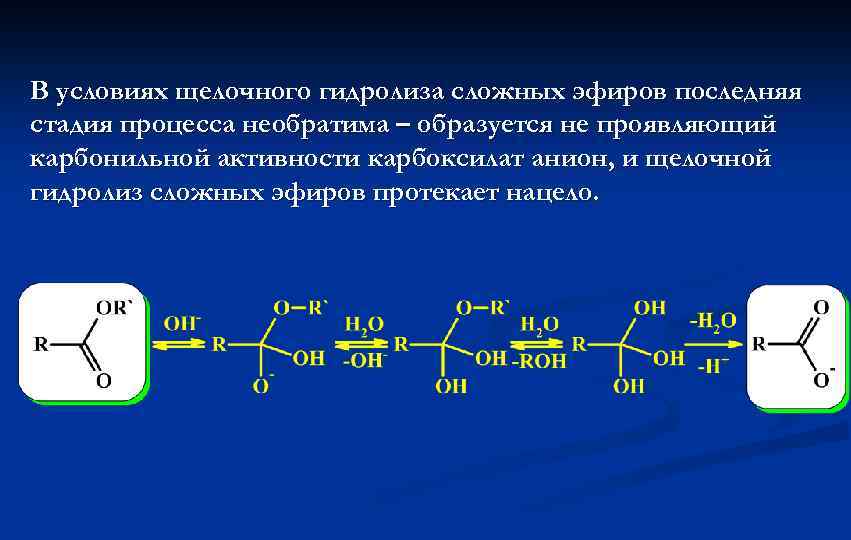
В условиях щелочного гидролиза сложных эфиров последняя стадия процесса необратима – образуется не проявляющий карбонильной активности карбоксилат анион, и щелочной гидролиз сложных эфиров протекает нацело.
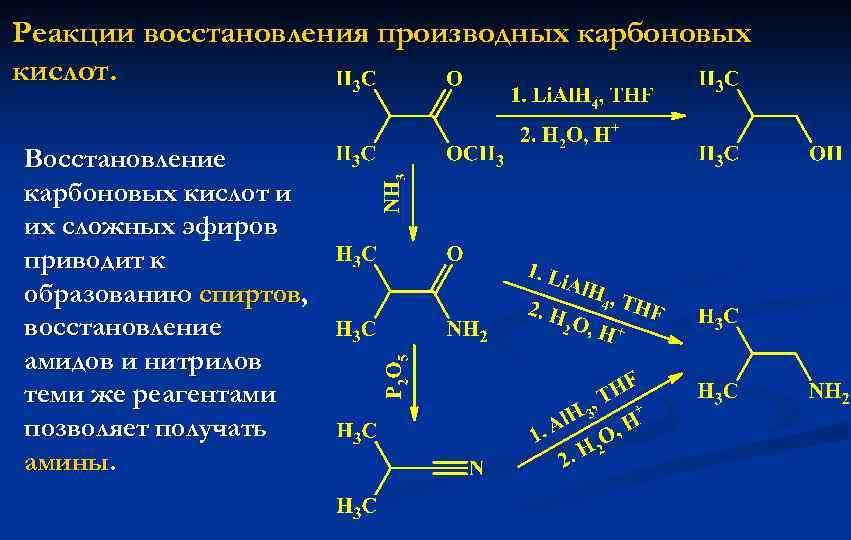
Реакции восстановления производных карбоновых кислот. Восстановление карбоновых кислот и их сложных эфиров приводит к образованию спиртов, восстановление амидов и нитрилов теми же реагентами позволяет получать амины.
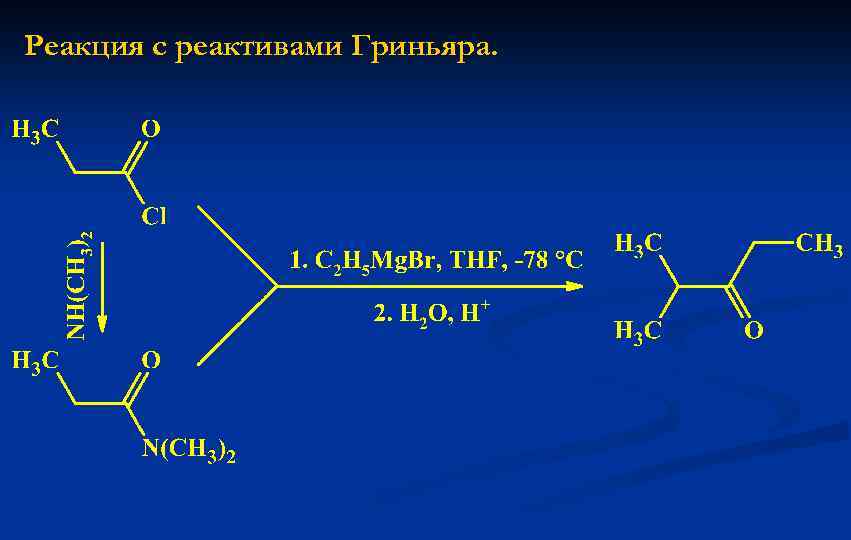
Реакция с реактивами Гриньяра.
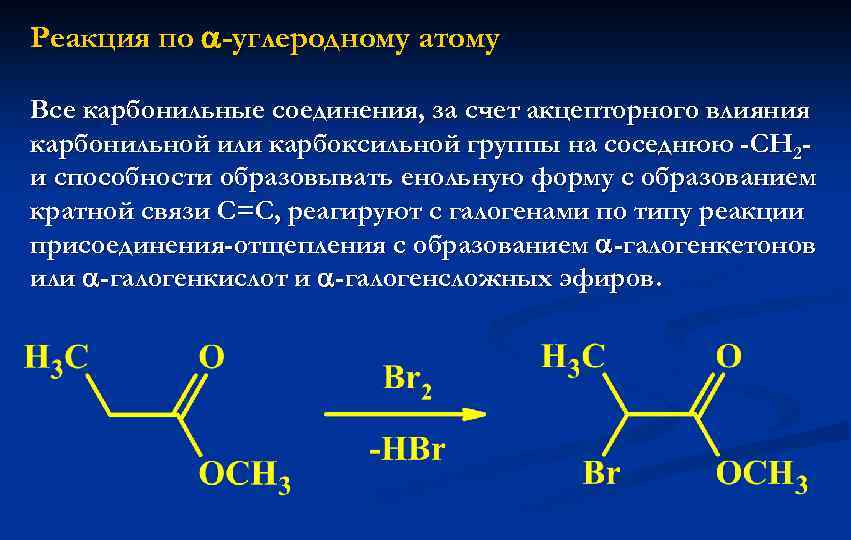
Реакция по -углеродному атому Все карбонильные соединения, за счет акцепторного влияния карбонильной или карбоксильной группы на соседнюю -СН 2 и способности образовывать енольную форму с образованием кратной связи С=С, реагируют с галогенами по типу реакции присоединения-отщепления с образованием -галогенкетонов или -галогенкислот и -галогенсложных эфиров.
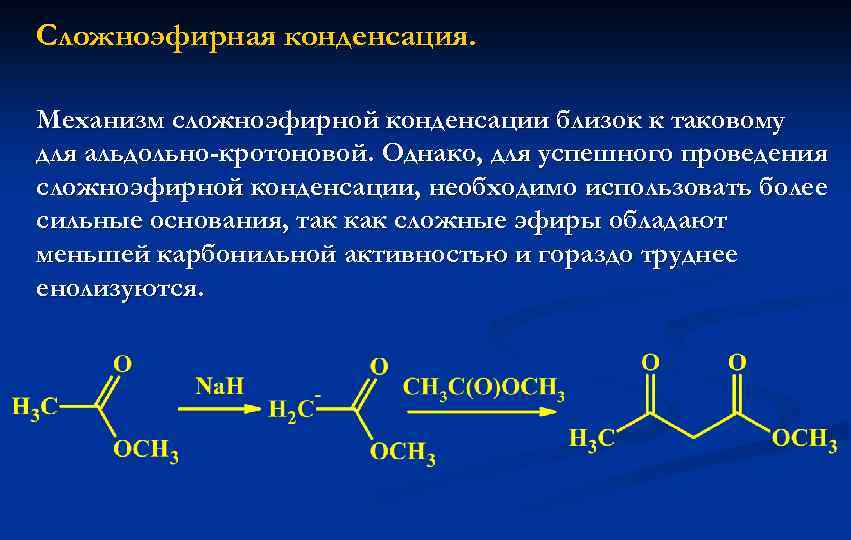
Сложноэфирная конденсация. Механизм сложноэфирной конденсации близок к таковому для альдольно-кротоновой. Однако, для успешного проведения сложноэфирной конденсации, необходимо использовать более сильные основания, так как сложные эфиры обладают меньшей карбонильной активностью и гораздо труднее енолизуются.

Реакции декарбоксилирования. При высокой температуре большинство карбоновых кислот подвергается декарбоксилированию с выбросом СО 2. Ароматические карбоновые кислоты отщепляют углекислый газ гораздо легче и при более низких температурах. Особенно легко отщепляют карбоксильную группу арилдикарбоновые и поликарбоновые кислоты. Также легко (ниже 100˚С) декарбоксилируется малоновая кислота.

Реакции дикарбоновых кислот Щавелевая, малоновая и отчасти янтарная кислоты обладают сильно отличающимися от обычных карбоновых кислот свойствами. Более протяженные дикарбоновые кислоты близки по свойствам к соответствующим монокарбоновым с той только разницей, что в молекуле присутствуют два реакционных центра. Последние способны к внутримолекулярным реакциям между концевыми карбоксильными группами. В частности, янтарная (С 4), глутаровая (С 5) и адипиновая (С 6) кислоты способны образовывать циклические ангидриды и амиды, а адипиновая и пимелиновая (С 7) кислоты легко вступают в реакцию образования циклических кетонов по реакции разложения соответствующих кальциевых, бариевых, железных или ториевых солей соответствующих. Этот способ широко используется для синтеза циклических кетонов с размером цикла от 4 до 7.
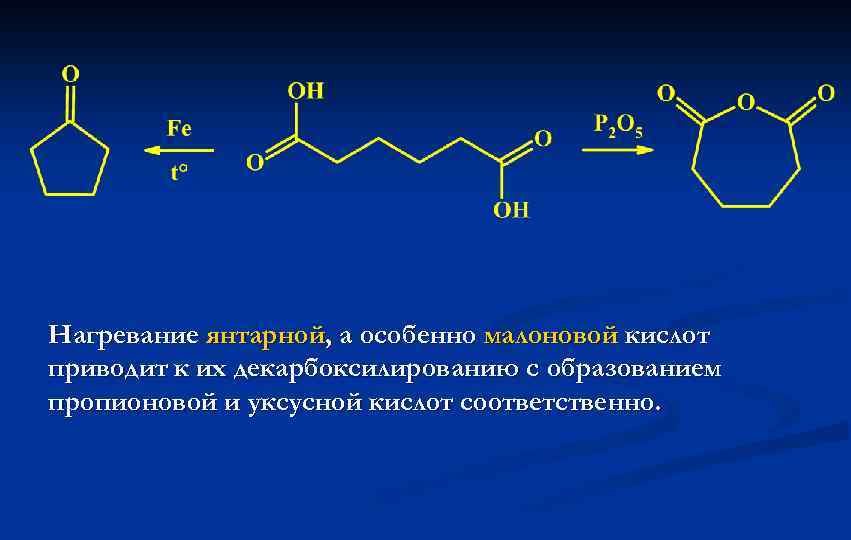
Нагревание янтарной, а особенно малоновой кислот приводит к их декарбоксилированию с образованием пропионовой и уксусной кислот соответственно.
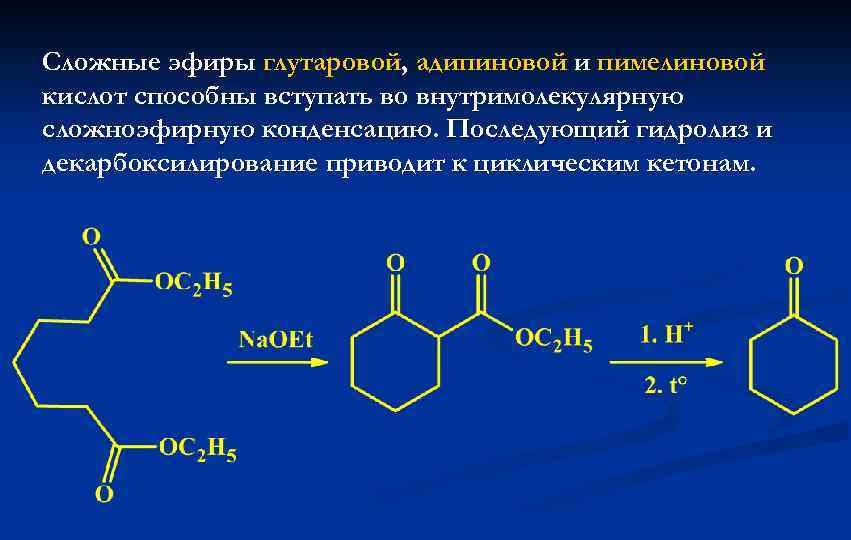
Сложные эфиры глутаровой, адипиновой и пимелиновой кислот способны вступать во внутримолекулярную сложноэфирную конденсацию. Последующий гидролиз и декарбоксилирование приводит к циклическим кетонам.

Дикарбонильные соединения. Свойства 1, 3 -дикетонов, ацетоуксусного и малонового эфиров. С-Н кислотность некоторых дикарбонильных соединений в сравнении с их моно-аналогами. Карбонильное соединение ацетилацетон ацетоуксусный эфир р. Ка 9, 0 10, 7 диэтиловый эфир малоновой кислоты ацетальдегид ацетон этиловый эфир уксусной кислоты 13, 0 ~18 ~20 ~25
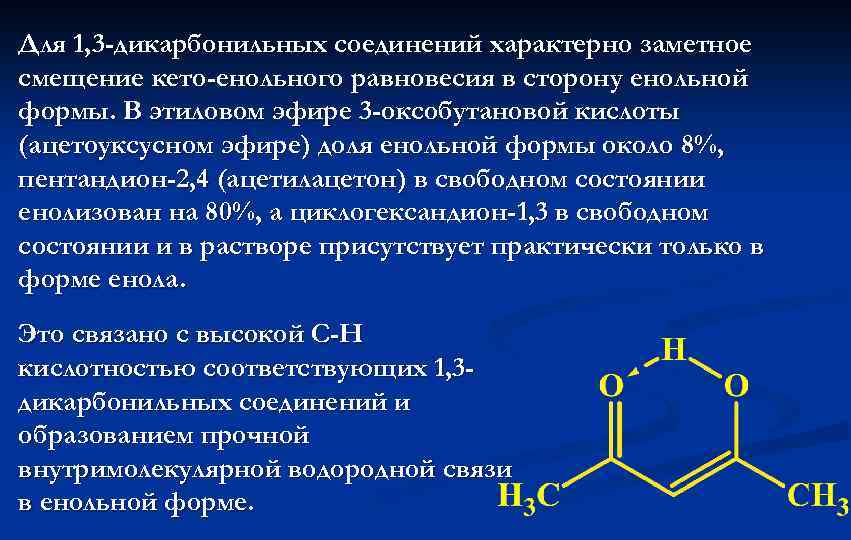
Для 1, 3 -дикарбонильных соединений характерно заметное смещение кето-енольного равновесия в сторону енольной формы. В этиловом эфире 3 -оксобутановой кислоты (ацетоуксусном эфире) доля енольной формы около 8%, пентандион-2, 4 (ацетилацетон) в свободном состоянии енолизован на 80%, а циклогександион-1, 3 в свободном состоянии и в растворе присутствует практически только в форме енола. Это связано с высокой С-Н кислотностью соответствующих 1, 3 дикарбонильных соединений и образованием прочной внутримолекулярной водородной связи в енольной форме.
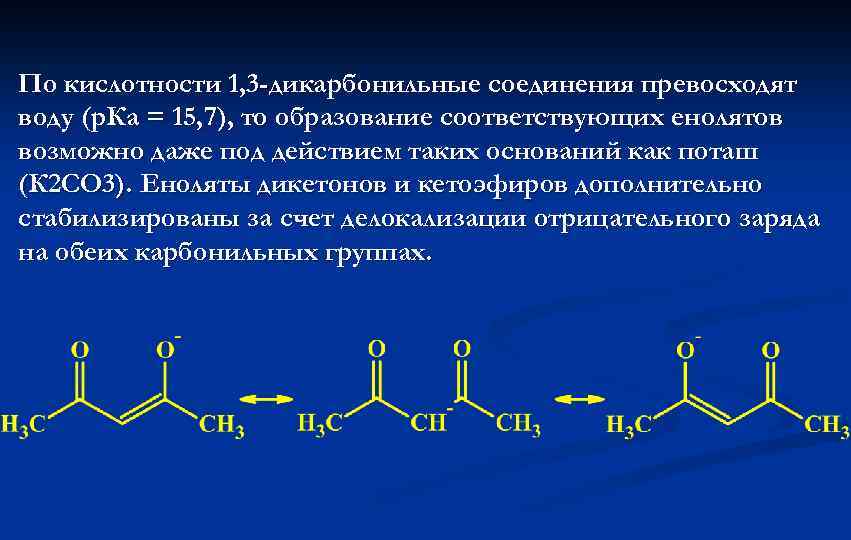
По кислотности 1, 3 -дикарбонильные соединения превосходят воду (р. Ка = 15, 7), то образование соответствующих енолятов возможно даже под действием таких оснований как поташ (К 2 СО 3). Еноляты дикетонов и кетоэфиров дополнительно стабилизированы за счет делокализации отрицательного заряда на обеих карбонильных группах.

Образовавшийся анион проявляет нуклеофильные свойства по отношению к галоидным алкилам, карбонильным соединениям. В результате протекает алкилирование или ацилирование енолята. В связи с тем, что енолят анион проявляет амбидентный характер, то в зависимости от противоиона образуются продукты С- или О- алкилирования и ацилирования. Магниевые и отчасти натриевые и калиевые еноляты предпочтительно атакуются по атому углерода. Литиевые еноляты, наоборот склонны к взаимодействиям по кислородному атому. Дополнительные возможности в данной синтетической области открывает тот факт, что возможно двукратное селективное алкилирование или ацилирование разными реагентами.
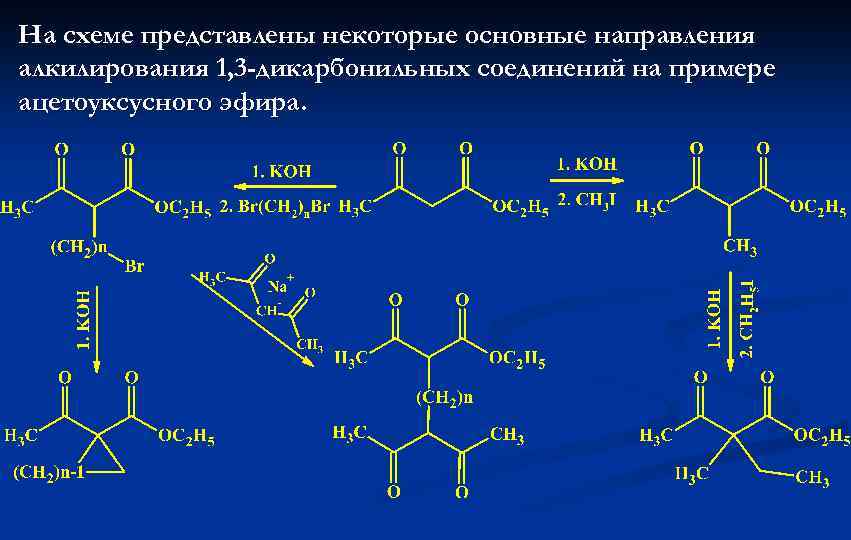
На схеме представлены некоторые основные направления алкилирования 1, 3 -дикарбонильных соединений на примере ацетоуксусного эфира.
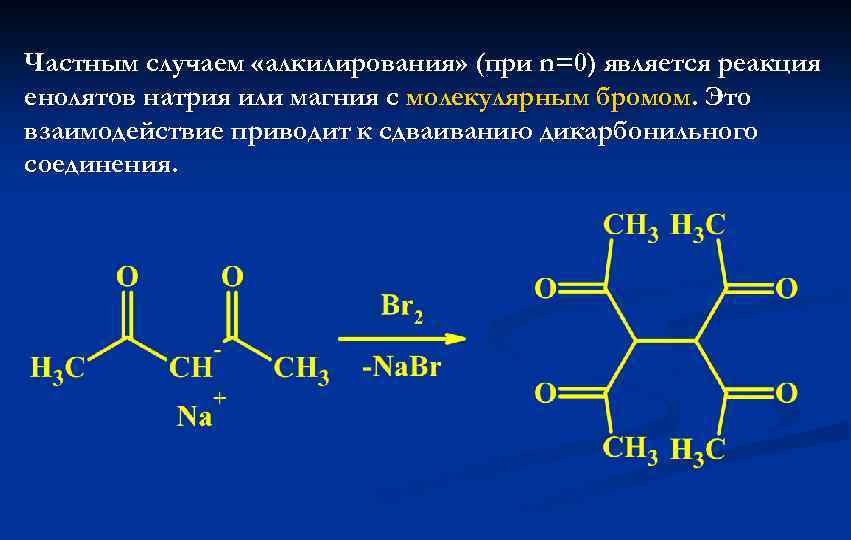
Частным случаем «алкилирования» (при n=0) является реакция енолятов натрия или магния с молекулярным бромом. Это взаимодействие приводит к сдваиванию дикарбонильного соединения.
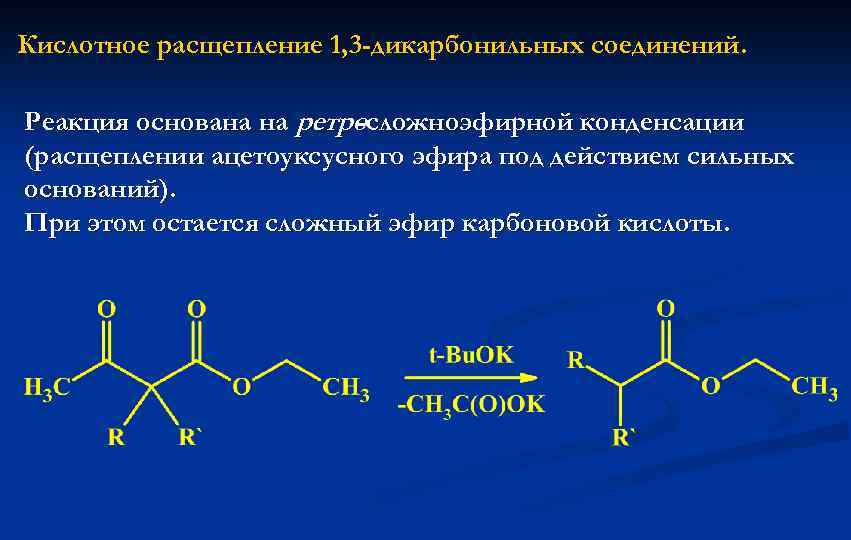
Кислотное расщепление 1, 3 -дикарбонильных соединений. Реакция основана на ретро -сложноэфирной конденсации (расщеплении ацетоуксусного эфира под действием сильных оснований). При этом остается сложный эфир карбоновой кислоты.
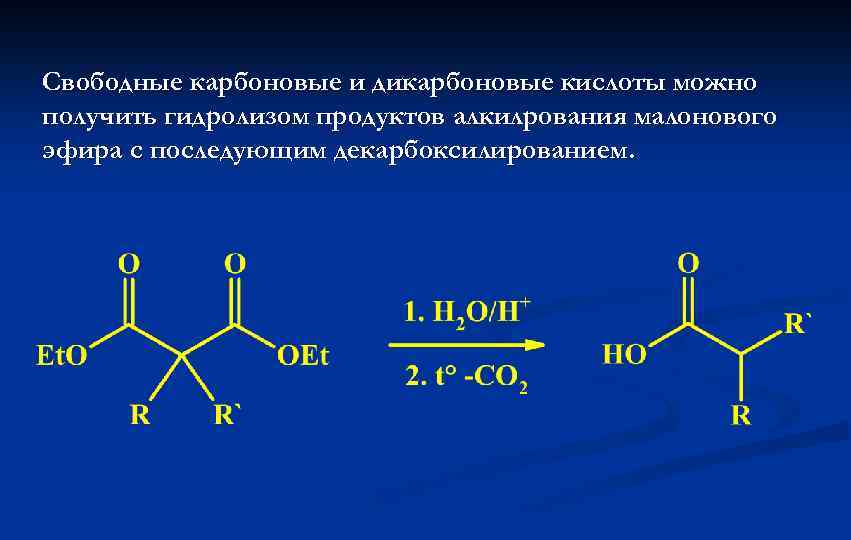
Свободные карбоновые и дикарбоновые кислоты можно получить гидролизом продуктов алкилрования малонового эфира с последующим декарбоксилированием.
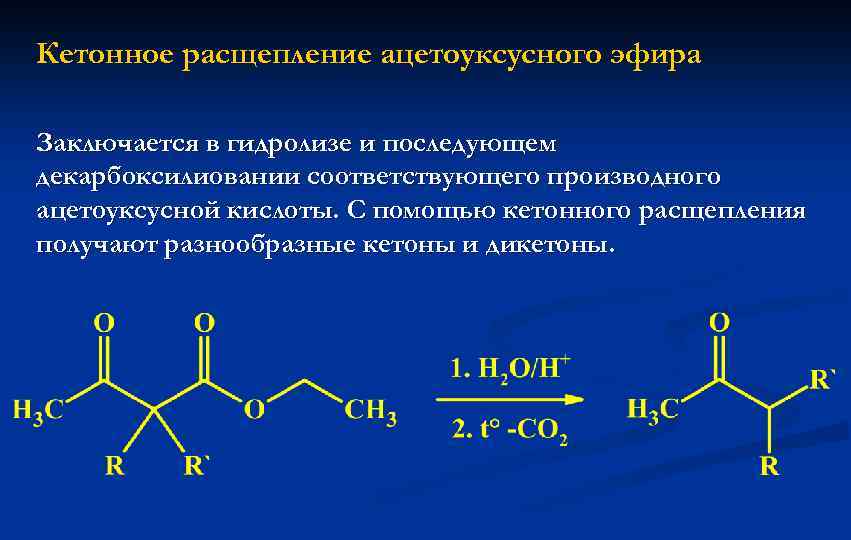
Кетонное расщепление ацетоуксусного эфира Заключается в гидролизе и последующем декарбоксилиовании соответствующего производного ацетоуксусной кислоты. С помощью кетонного расщепления получают разнообразные кетоны и дикетоны.

Аминокислоты Номенклатура аминокислот. Аминокислоты подразделяют по положению аминогруппы в цепи относительно карбоксила. Это удобно, так как химические свойства аминокислот зависят от взаимного расположения этих функциональных групп. Принято указывать положения аминогруппы буквой греческого алфавита. Соседнее положение (2 -е положение) называют α-положение, через один (3 -е положение) – β-положение, и т. д. Последнее положение в углеродной цепи, вне зависимости от ее длины (но не менее 6 -и атомов углерода) называют ω-положение. Многие как природные, так и синтетические α-аминокислоты носят тривиальные названия.
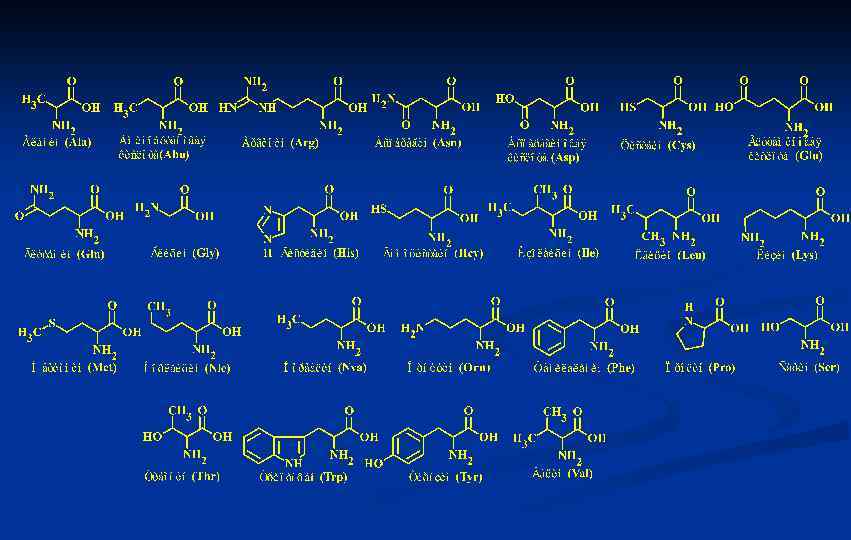
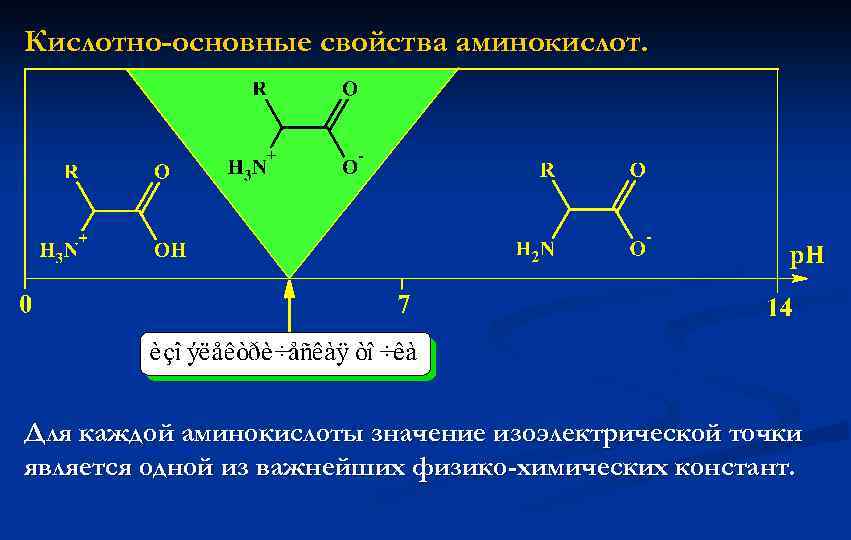
Кислотно-основные свойства аминокислот. Для каждой аминокислоты значение изоэлектрической точки является одной из важнейших физико-химических констант.
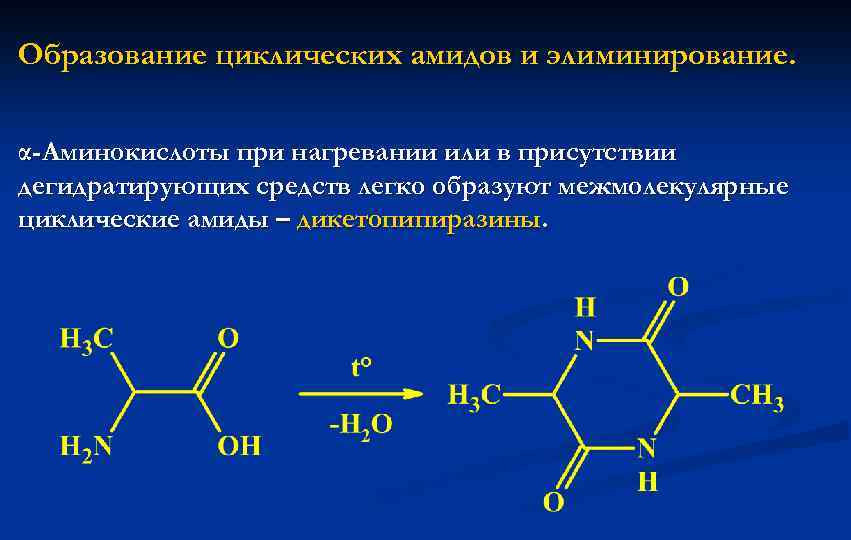
Образование циклических амидов и элиминирование. α-Аминокислоты при нагревании или в присутствии дегидратирующих средств легко образуют межмолекулярные циклические амиды – дикетопипиразины.
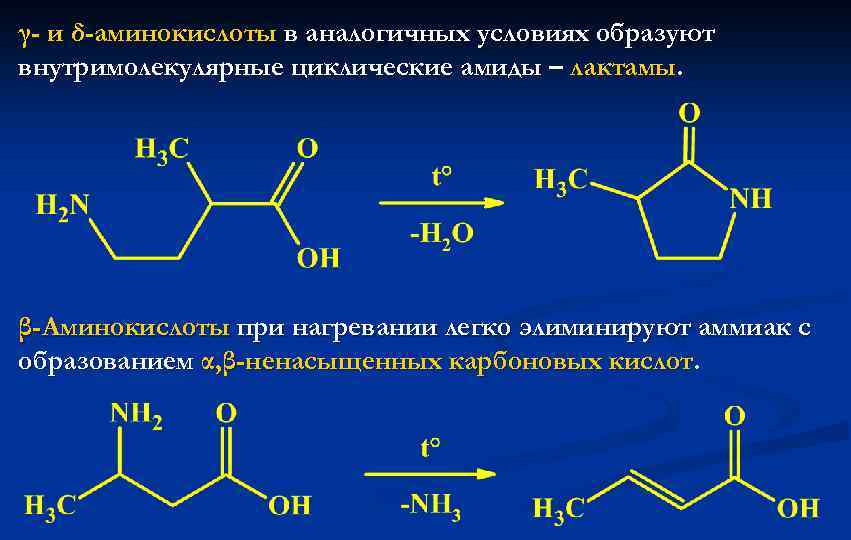
γ- и δ-аминокислоты в аналогичных условиях образуют внутримолекулярные циклические амиды – лактамы. β-Аминокислоты при нагревании легко элиминируют аммиак с образованием α, β-ненасыщенных карбоновых кислот.
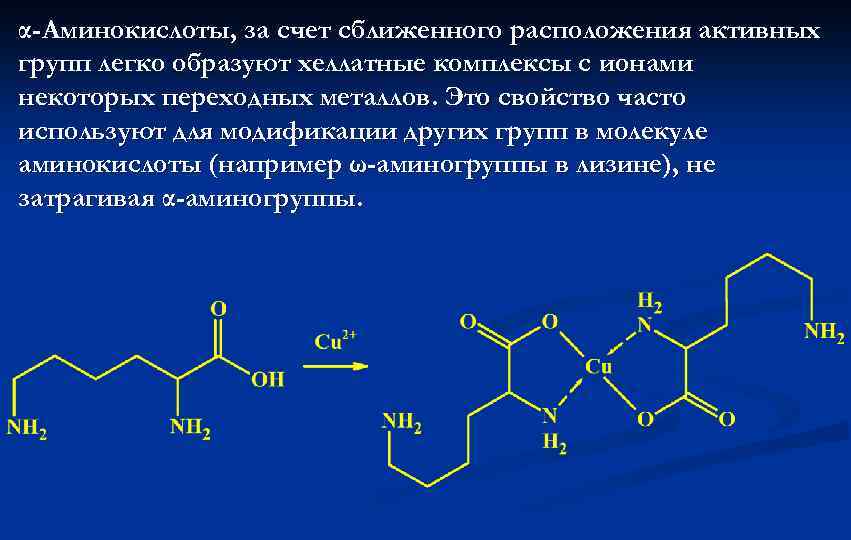
α-Аминокислоты, за счет сближенного расположения активных групп легко образуют хеллатные комплексы с ионами некоторых переходных металлов. Это свойство часто используют для модификации других групп в молекуле аминокислоты (например ω-аминогруппы в лизине), не затрагивая α-аминогруппы.
Лекция 11 карбоновые кислоты и производные.ppt