
Лекция № 11 Элементы VIIB подгруппы Mn, Tc, Re
H Li He Be B C N O F Ne Na Mg Al Si P S Cl Ar K Ca Sc Ti Cu Zn Ga Ge Rb Sr Y Ag Cd In Cs Ba La Au Hg Tl Fr Ra V Cr As Se Mn Br Zr Nb Mo Sn Sb Hf Ta Pb Bi Te W Po Tc I Re At Fe Co Ni Kr Ru Rh Pd Xe Os Rn Ir Pt
![Общая характеристика элементов VIIB подгруппы Эл. cтроение устойчивость в. СО СО Mn [Ar] 3 Общая характеристика элементов VIIB подгруппы Эл. cтроение устойчивость в. СО СО Mn [Ar] 3](https://present5.com/presentation/3/26150394_165585911.pdf-img/26150394_165585911.pdf-3.jpg)
Общая характеристика элементов VIIB подгруппы Эл. cтроение устойчивость в. СО СО Mn [Ar] 3 d 54 s 2 II, IV, (V), VII Tc [Kr] 4 d 55 s 2 IV, VII Re [Xe] 4 f 145 d 56 s 2 IV, VII О высшей степени окисления Не склонны к комплексообразованию

Нахождение в природе Э Cодержание в Место по распростземной коре, раненности % (мас. ) Важнейшие природные соединения Mn. O 2 (пиролюзит) Mn 2 O 3 (браунит) Mn. O(OH) (манганит) Mn 3 O 4 (гаусманит) Mn. CO 3 (родохрозит) Mn 0, 085 15 Tc - Не обнаружен - Re 10 -7 81 Cu. Re. S 4 (джезказганит), примесь сульфида к молибдениту (Mo. S 2)

Пиролюзит Mn. O 2

Свойства Mn, Tc, Re Тяжёлые, тугоплавкие металлы Re: ρ = 20, 5 г/см 3, т. пл. 3190 °С Mn: = 7, 44 ; t пл. 1244 ºC ; ЭО = 1, 5 О химической активности Mn, Tc, Re Mn реагирует с O 2, S, галогенами при 200 °С, при более высокой т-ре с N и С Mn как раскислитель (ферромарганец Fe–Mn)
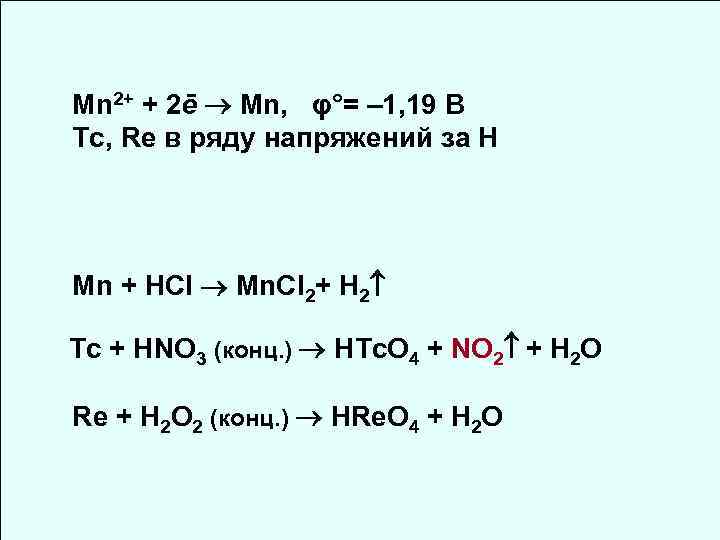
Mn 2+ + 2ē Mn, φ°= – 1, 19 B Tc, Re в ряду напряжений за Н Mn + HCl Mn. Cl 2+ H 2 Tc + HNO 3 (конц. ) HTc. O 4 + NO 2 + Н 2 О Re + H 2 O 2 (конц. ) HRe. O 4 + Н 2 О
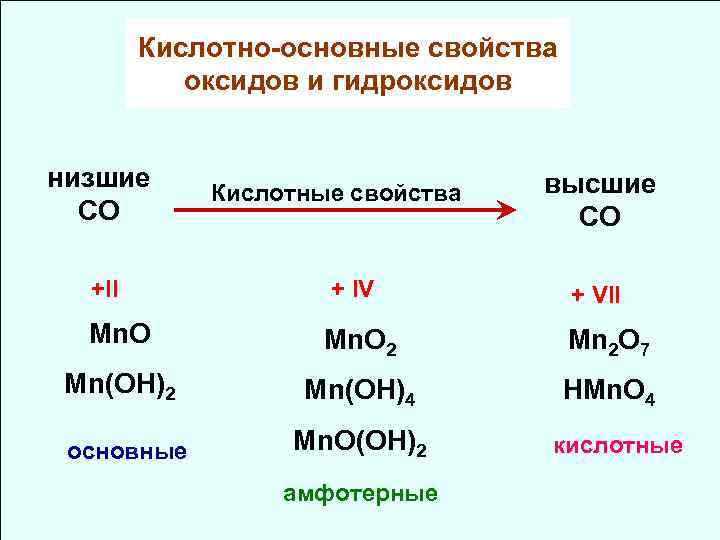
Кислотно-основные свойcтва оксидов и гидроксидов низшие СО +II Кислотные свойства + IV высшие СО + VII Mn. O 2 Mn 2 O 7 Mn(OH)2 Mn(OH)4 HMn. O 4 основные Mn. O(OH)2 амфотерные кислотные
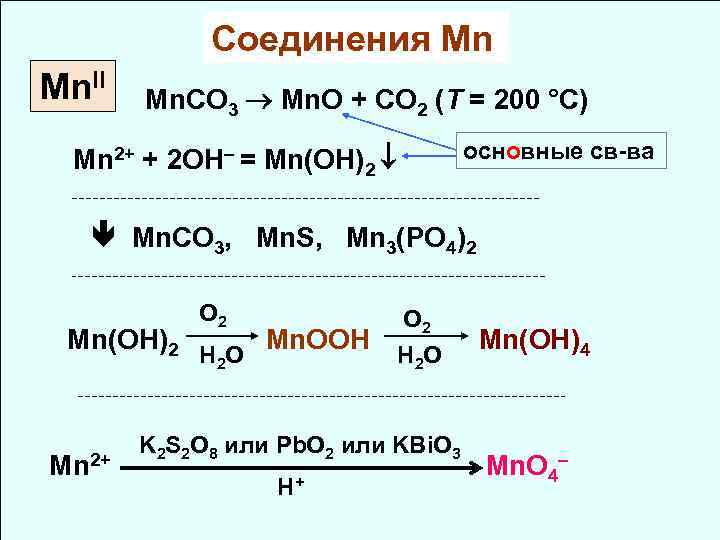
Соединения Mn Mn. II Mn. CO 3 Mn. O + CO 2 (T = 200 °C) oснoвные св-ва Mn 2+ + 2 OH– = Mn(OH)2 Mn. CO 3, Mn. S, Mn 3(PO 4)2 Mn(OH)2 Mn 2+ O 2 H 2 O Mn. OOH O 2 H 2 O K 2 S 2 O 8 или Pb. O 2 или KBi. O 3 H+ Mn(OH)4 Mn. O 4–
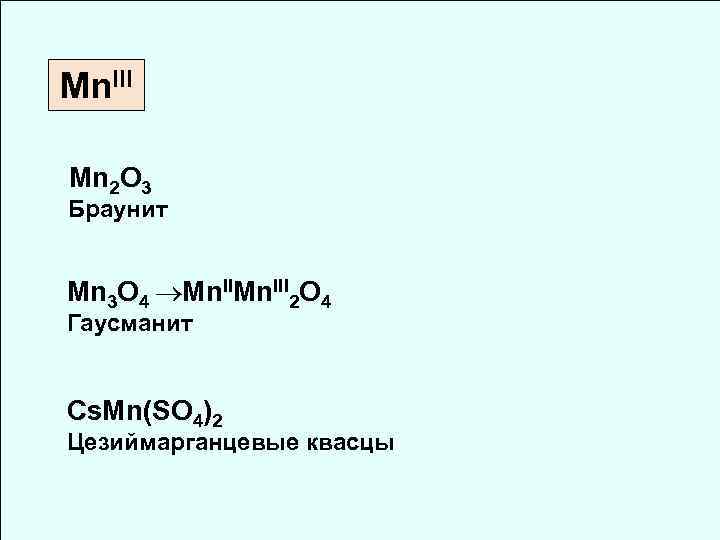
Mn. III Mn 2 O 3 Браунит Mn 3 O 4 Mn. III 2 O 4 Гаусманит Cs. Mn(SO 4)2 Цезиймарганцевые квасцы
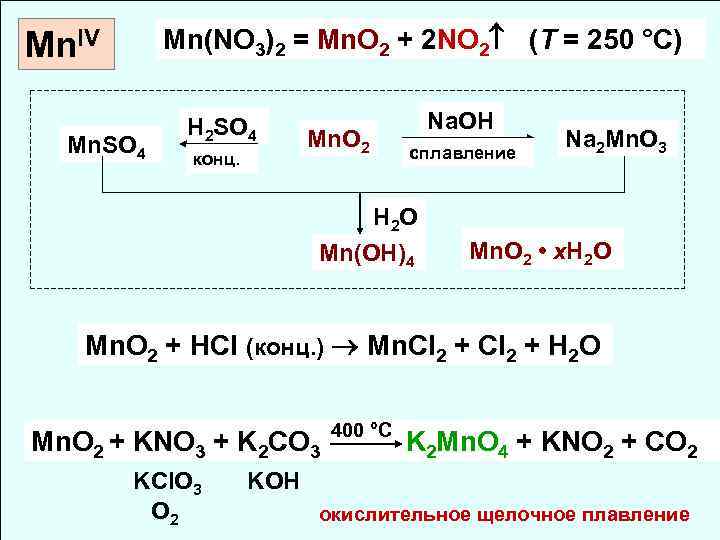
Mn(NO 3)2 = Mn. O 2 + 2 NO 2 (T = 250 °C) Mn. IV Mn. SO 4 H 2 SO 4 конц. Mn. O 2 Na. OH сплавление H 2 O Mn(OH)4 Na 2 Mn. O 3 Mn. O 2 • x. H 2 O Mn. O 2 + HCl (конц. ) Mn. Cl 2 + H 2 O Mn. O 2 + KNO 3 + K 2 CO 3 KCl. O 3 O 2 400 °C K 2 Mn. O 4 + KNO 2 + CO 2 KOH oкислительное щелочное плавление
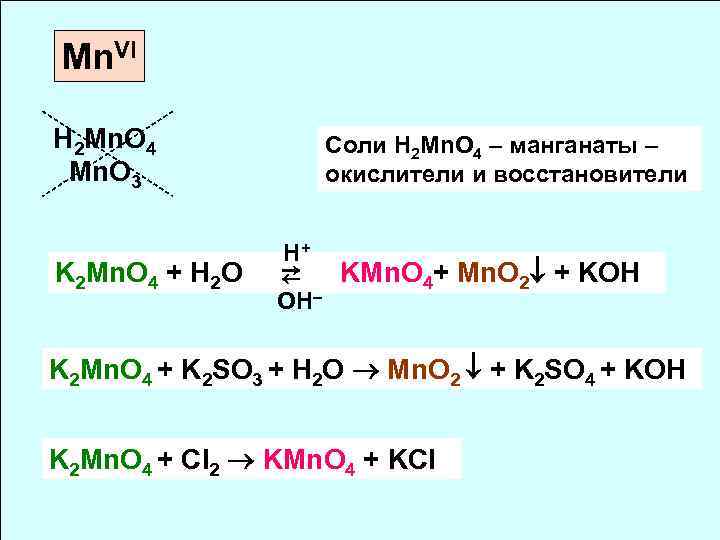
Mn. VI H 2 Mn. O 4 Mn. O 3 K 2 Mn. O 4 + H 2 O Соли H 2 Mn. O 4 – манганаты – окислители и восстановители H+ ⇄ OH– KMn. O 4+ Mn. O 2 + KOH K 2 Mn. O 4 + K 2 SO 3 + H 2 O Mn. O 2 + K 2 SO 4 + KOH K 2 Mn. O 4 + Cl 2 KMn. O 4 + KCl

Mn. VII 0 ºC KMn. O 4(k) + H 2 SO 4 (конц. ) Mn 2 O 7 + KHSO 4 + H 2 O Mn 2 O 7 Mn. O 2 + O 2 Mn 2 O 7 — чрезвычайно сильный окислитель Mn 2 O 7 + H 2 O HMn. O 4 cильная к-та, устойчива только в р-ре при С < 20 % Соли HMn. O 4 — перманганаты
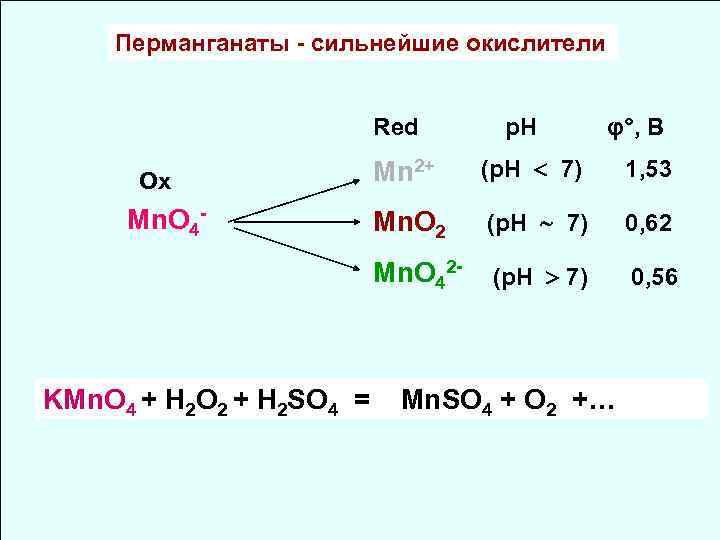
Перманганаты - сильнейшие окислители Red p. H φ°, В Mn. O 4 - KMn. O 4 + H 2 O 2 + H 2 SO 4 = (p. H 7) 1, 53 Mn. O 2 (p. H 7) 0, 62 Mn. O 42 - Oх Mn 2+ (p. H 7) 0, 56 Mn. SO 4 + O 2 +…

Дополнительный материал по производству ферромарганца и марганца смотрите на сайте кафедры Лекция № 11 Mn, Tc, Re

Cайт кафедры Лекция № 11 МАРГАНЕЦ, ТЕХНЕЦИЙ, РЕНИЙ

ПОЛУЧЕНИЕ ФЕРРОСПЛАВОВ Ферросплавы широко применяются в сталеплавильной промышленности для раскисления и легирования стали. Ферросплавами называют сплавы железа с легирующими элементами (V, W, Ti, Zr, Nb, Cr и др. ) или с элементами-раскислителями (Mn, Si и др. ). Применение их в технологическом процессе производства стали более выгодно, чем чистых элементов: ферросплавы имеют более низкую температуру плавления ; ферросплавы значительно дешевле, чем чистые металлы, так как получаются непосредственно из руд. Исходным сырьем для получения ферросплавов являются руды или концентраты. Поскольку легирующий металл находится в руде или концентрате в виде оксида, то процесс получения ферросплавов сводится к восстановлению данного элемента и его растворению в расплавленном железе.

Если исходная руда не содержит железа, то его вводят в шихту в виде лома или железной руды. Восстановителем чаще всего является углерод, в этом случае получаются ферросплавы с большим содержанием углерода. Для выплавления безуглеродистых ферросплавов в качестве восстановителя используют кремний, алюминий или другой элемент, обладающий большим сродством к кислороду. ПРОИЗВОДСТВО ФЕРРОМАРГАНЦА Шихта при производстве ферромарганца состоит из марганцевой руды, восстановителя, флюса, железного скрапа (или стальной стружки). Ферромарганец можно выплавлять в доменных или в электрических печах. В доменных печах получается ферромарганец с высоким содержанием углерода 6, 5 -7, 0 % , Mn ~ 75 – 78 %, поскольку восстановление ведется в условиях избытка углерода. Малоуглеродистый ферромарганец (c содержанием углерода до 1, 5 %) выплавляют в электрических печах.

Основные химические реакции получения ферромарганца В основе плавки ферромарганца лежат реакции восстановления оксидов марганца и железа. В общем виде реакция выглядет следующим образом. t Mn. O 2 + Fe 2 O 3 + 5 C Mn + 2 Fe + 5 CO Однако, механизм восстановления оксидов марганца более сложен и многостадиен. Высшие оксиды марганца восстанавливаются до закиси марганца при умеренных температурах (200 -500 ºC). Причем реакции экзотермические. 2 Mn. O 2 + CO= Mn 2 O 3 + CO 2 + Q 3 Mn 2 O 3+ CO= 2 Mn 3 O 4+ CO 2 + Q Mn 3 O 4+ CO= 3 Mn. O+ CO 2 + Q Восстановление марганца из закиси – процесс эндотермический, идет с образованием не только марганца, но и карбида марганца. Температура начала реакции составляет 1420 ºС. Mn. O + C = Mn + CO - Q 3 Mn. O +4 C = Mn 3 C + 3 CO - Q

Поскольку в марганцевых рудах содержится кремний, то в результате плавки образуются силикаты марганца. Восстановление марганца из силикатов облегчается наличием извести. Mn. Si. O 3 + Ca. O + C = Mn + Ca. Si. O 3 + CO -Q При необходимости получения безуглеродистых ферросплавов используют металлотермический способ восстановления. В этом случае в качестве восстановителей используют кремний, алюминий или их смеси. Mn. O 2 + Si + Ca. O = Mn + Ca. Si. O 3 + Q Mn. O 2 + Al = Mn + Al 2 O 3 + Q Mn Металлический марганец высокой чистоты, без примеси железа, значительно дороже, его получают методом алюмотермии. Для этого пиролюзит предварительно прокаливают (понижается содержание кислорода), а затем Mn 3 O 4 восстанавливают алюминием. t 3 Mn. O 2 Mn 3 O 4 + O 2 3 Mn 3 O 4 + 8 Al = 9 Mn + 4 Al 2 O 3

Общий вид ферросплавной печи (с водоохлаждаемым сводом и вращающейся ванной) 1 печь; 2 – зубчатый венец; 3 – ходовые колеса (30 шт. ); 4 –пята; 5 - железобетонная плита; 6 – кольцевой рельс Стр424 рис191 восокбойников Восстановительные ферросплавные печи работают непрерывно. В работающей печи электроды погружены в твердую шихту, которую пополняют по мере ее проплавления; сплав и шлак выпускают периодически. Печи оснащены мощными трансформаторами. Кожух печи выполнен из листового железа. Для выплавки ферромарганца печи футеруют угольными блоками.

Области применения марганца 1. Некоторое количество марганца в виде химических соединений используют в качестве катализаторов химических процессов, в производстве стекла. 2. Основная доля марганца идет на выплавку легированных сталей. Стали, содержащие марганец: - «сталь Гадфильда» (с содержанием Mn ~ 10%) – обладает очень высоким сопротивлением ударно-истирающим нагрузкам (применяют для изготовления рельсов, тракторных траков, ковшей экскаваторов, деталей дробилок, мельниц и др. ) - сплав манганин (Mn-Cu-Ni). Он сильно меняет свое электрическое сопротивление в зависимости от давления на него. Используют для изготовления монометров, измеряющих давление в десятки тысяч атмосфер (тысячи МПа).

Области применения рения 1. Химическая и нефтяная промышленность - в качестве катализатора химических процессов (при крекинге нефти). 2. Рений в чистом виде и в сплавах с вольфрамом применяется для производства изделий в электротехнике. 3. Получение жаропрочных сталей (совместно с W, Mo, Ta).