Лекция 10 Полициклические ароматические соединения с конденсированными ядрами1.ppt
- Количество слайдов: 16

ЛЕКЦИЯ 10. ПОЛИЦИКЛИЧЕСКИЕ АРОМАТИЧЕСКИЕ УГЛЕВОДОРОДЫ С КОНДЕНСИРОВАННЫМИ БЕНЗОЛЬНЫМИ ЯДРАМИ n n n Номенклатура Нафталин Антрацен Фенантрен Спектроскопические характеристики бензоидных ароматических соединений 1
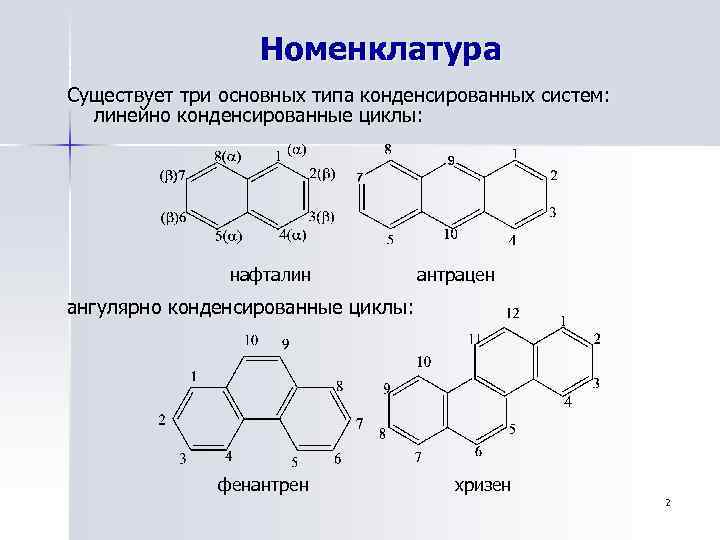
Номенклатура Существует три основных типа конденсированных систем: линейно конденсированные циклы: нафталин антрацен ангулярно конденсированные циклы: фенантрен хризен 2
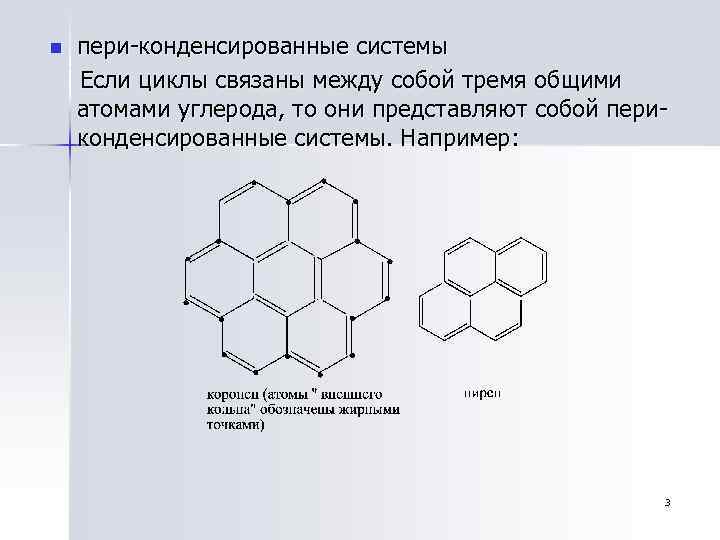
n пери-конденсированные системы Если циклы связаны между собой тремя общими атомами углерода, то они представляют собой периконденсированные системы. Например: 3
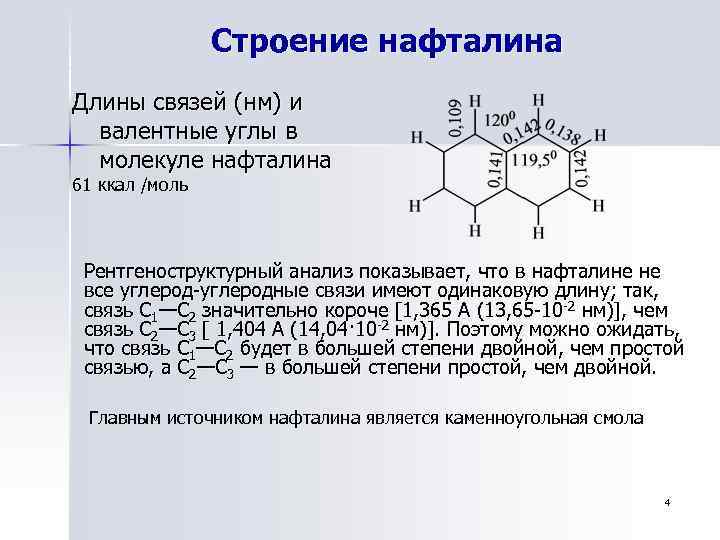
Строение нафталина Длины связей (нм) и валентные углы в молекуле нафталина 61 ккал /моль Рентгеноструктурный анализ показывает, что в нафталине не все углерод-углеродные связи имеют одинаковую длину; так, связь С 1—С 2 значительно короче [1, 365 А (13, 65 -10 -2 нм)], чем связь С 2—С 3 [ 1, 404 А (14, 04· 10 -2 нм)]. Поэтому можно ожидать, что связь С 1—С 2 будет в большей степени двойной, чем простой связью, a С 2—С 3 — в большей степени простой, чем двойной. Главным источником нафталина является каменноугольная смола 4
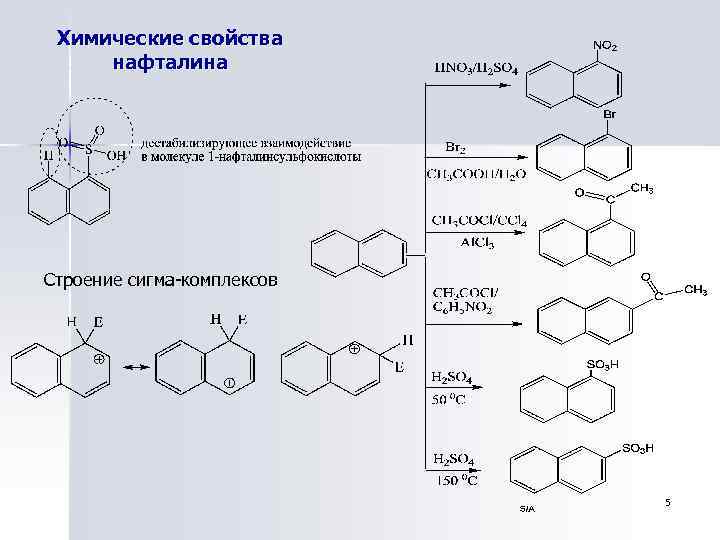
Химические свойства нафталина Строение сигма-комплексов 5
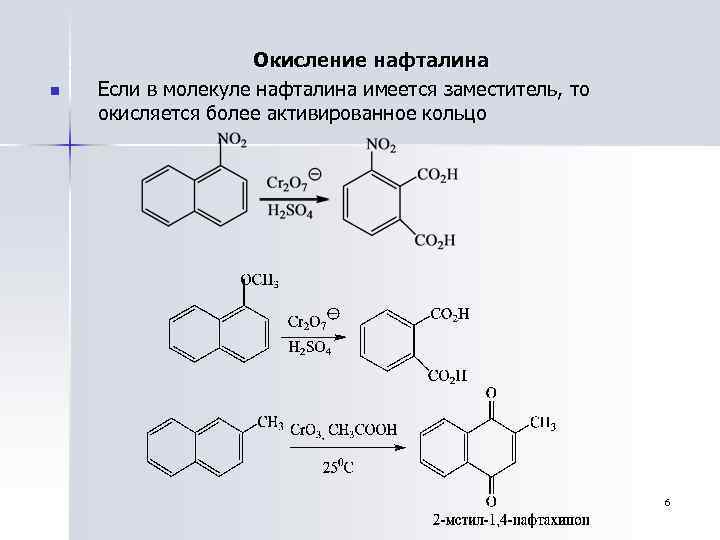
n Окисление нафталина Если в молекуле нафталина имеется заместитель, то окисляется более активированное кольцо 6
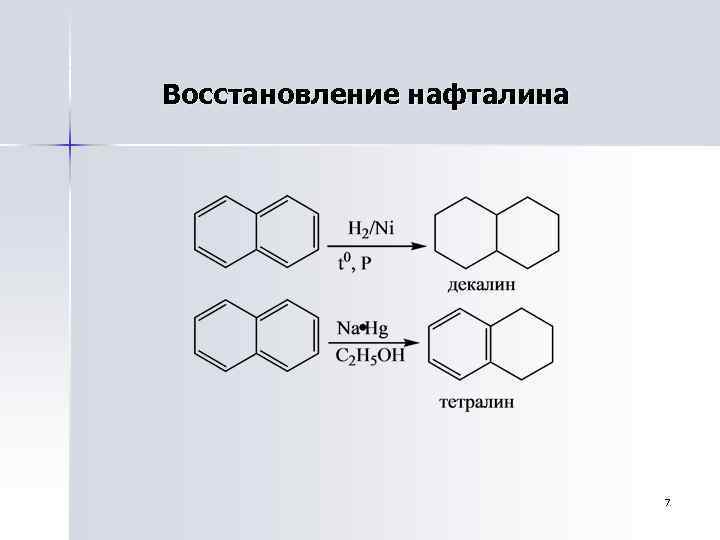
Восстановление нафталина 7

Антрацен n n n Антрацен имеет ярко выраженные электронодонорные свойства (ЭИ=7, 4 э. В). Длины связей в молекулах антрацена и нафталина близки. Углы между связями 119— 121°. Квантово-химические расчеты показывают, что наибольшая свободная валентность наблюдается в положениях 9 и 10. Там и ожидается наибольшая реакционная способность. Величины теплоты сгорания показывает, что резонансная энергия составляет 84 ккал/моль (351, 69· 103 Дж/моль для антрацена) ароматический характер выражен в меньшей степени, чем у нафталина а реакционная способность соответственно выше. В высших аценах эта тенденция продолжает развиваться 8
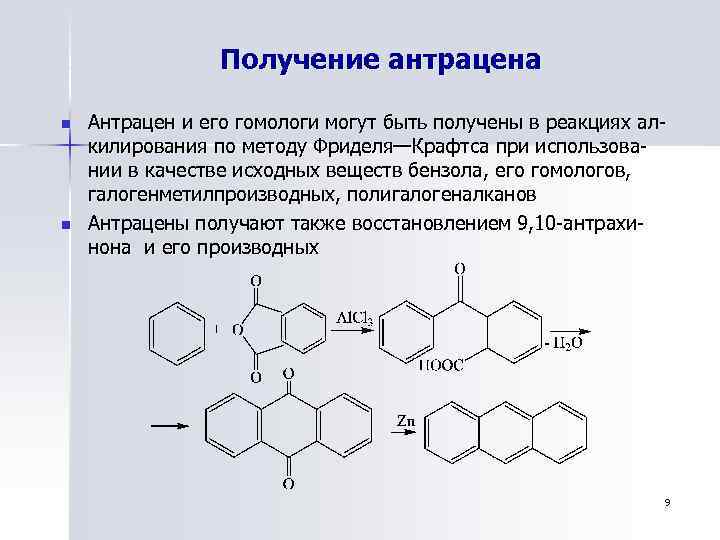
Получение антрацена n n Антрацен и его гомологи могут быть получены в реакциях алкилирования по методу Фриделя—Крафтса при использовании в качестве исходных веществ бензола, его гомологов, галогенметилпроизводных, полигалогеналканов Антрацены получают также восстановлением 9, 10 -антрахинона и его производных 9
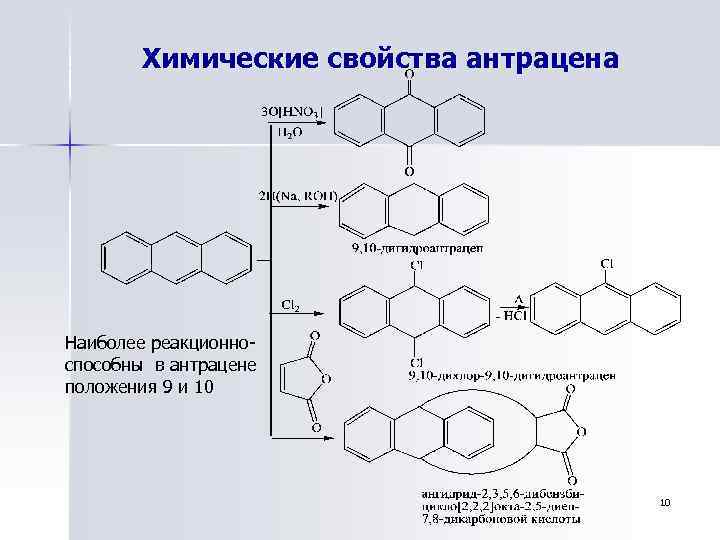
Химические свойства антрацена Наиболее реакционноспособны в антрацене положения 9 и 10 10
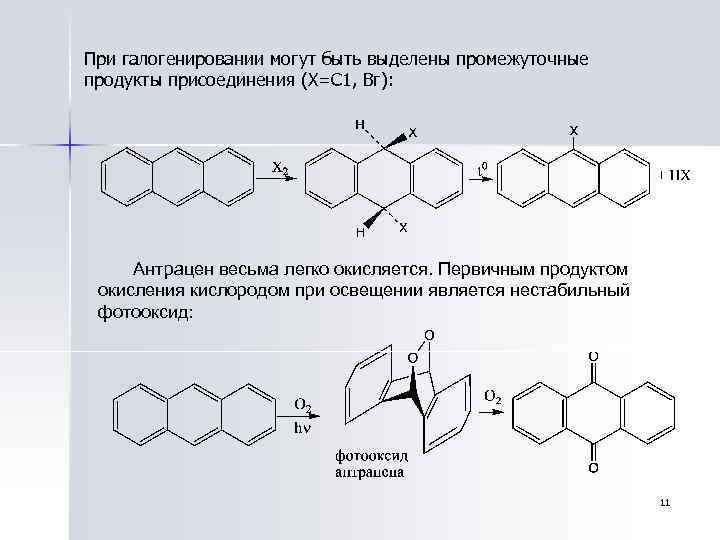
При галогенировании могут быть выделены промежуточные продукты присоединения (Х=С 1, Вг): Антрацен весьма легко окисляется. Первичным продуктом окисления кислородом при освещении является нестабильный фотооксид: 11

Фенантрен n n Молекула фенантрена является более стабильной, чем молекула антрацена, разница составляет около 33 к. Дж/моль. Величина теплоты сгорания показывает, что резонансная энергия составляет 92 ккал/моль (385, 10· 10 3 Дж/моль). Донорные свойства у фенантрена выражены слабее, чем у антрацена (ЭИ=7, 9 э. В). Это свидетельствует о том, что в молекуле фенантрена осуществляется более значительное взаимодействие p-электронов (делокализация), чем в молекуле антрацена Ароматический характер в этом случае выражен сильнее, что в частности, сказывается и на энергии делокализации. Связь между атомами 9 и 10 имеет характер почти чистой двойной связи С—С. Для фенантрена наряду с реакциями электрофильного замещения, характерны процессы присоединения 12
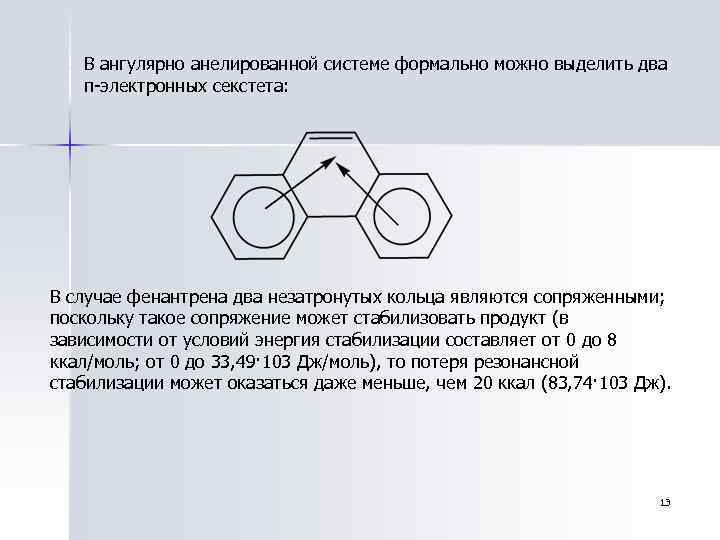
В ангулярно анелированной системе формально можно выделить два π-электронных секстета: В случае фенантрена два незатронутых кольца являются сопряженными; поскольку такое сопряжение может стабилизовать продукт (в зависимости от условий энергия стабилизации составляет от 0 до 8 ккал/моль; от 0 до 33, 49· 103 Дж/моль), то потеря резонансной стабилизации может оказаться даже меньше, чем 20 ккал (83, 74· 103 Дж). 13

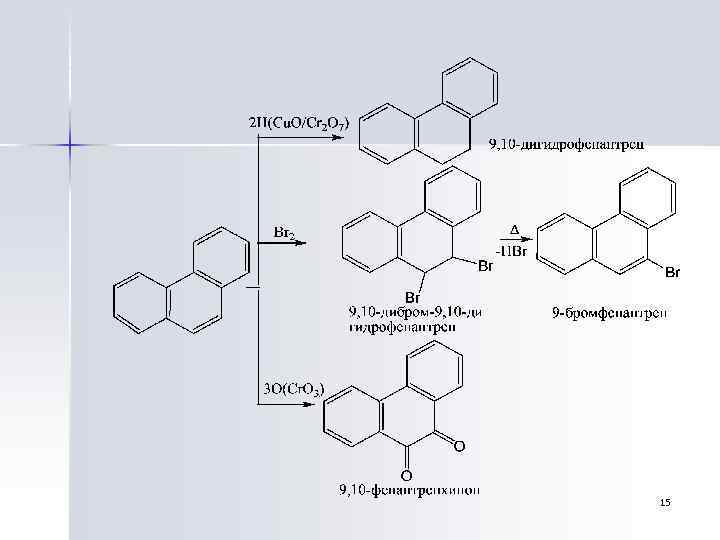
Химические свойства фенантрена • • Фенантрен легко вступает в реакции с электрофильными реагентами. Реакционная способность у фенантрена ниже, чем у антрацена. Наиболее активными являются положения 9 и 10, при этом в отдельных случаях можно выделить промежуточные продукты присоединения При каталитическом гидрировании фенантрена получается 9, 10 -дигидрофенантрен. В более жестких условиях может быть получен тетрадекагидрофенантрен (пергидрофенантрен). Окисление фенантрена различными окислителями приводит к фенантренхинону 14
15

Спектроскопические характеристики бензоидных ароматических соединений В ИК-спектрах бензол и его гомологи поглощают в областях 3000— 3050 см-1 (валентные колебания С—Н), 1500— 1600 см-1 (валентные колебания С=С) и 700— 900 см-1 (деформационные колебания С—Н). n В спектрах ЯМР протоны бензольного кольца характеризуются сдвигом в слабые магнитные поля (d=6, 4 – 8, 2) n 16
Лекция 10 Полициклические ароматические соединения с конденсированными ядрами1.ppt