2010 Лекция 10 Кислород, сера.ppt
- Количество слайдов: 25

Лекция 10 Подгруппа кислорода

КИСЛОРОД Общее содержание кислорода в земной коре, океане и воздухе оценивается примерно в 50%. Содержание кислорода в сухом воздухе составляет 20, 9 об. % или 23, 0 вес. %. 16 О - 99, 76 %, 17 О - 0, 04 %, 18 О - 0, 20 %. - радиоактивен
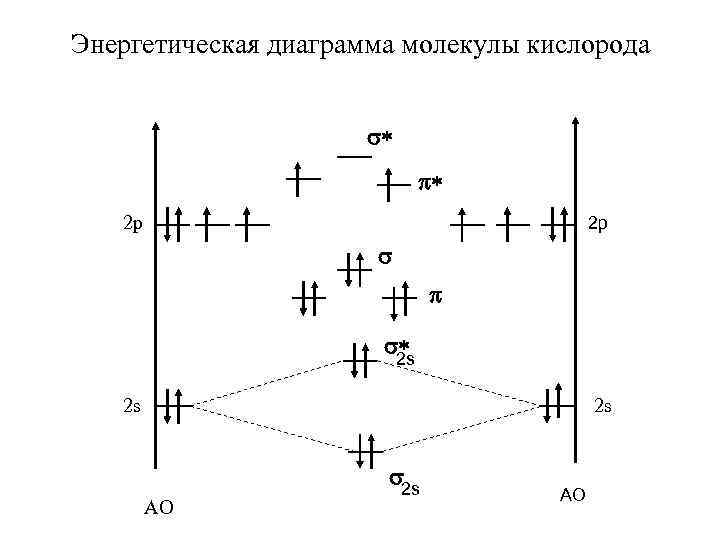
Энергетическая диаграмма молекулы кислорода s* p* 2 p 2 p s p s* 2 s 2 s 2 s АО

ПОЛУЧЕНИЕ КИСЛОРОДА. Сжижение и фракционированная перегонка жидкого воздуха. В лаборатории: а) 2 Н 2 О 2 2 Н 2 О(ж) + О 2(г) б) 2 KCl. O 3(тв) 2 KCl(тв) + 3 O 2(г) 2 Pb 3 O 4(тв) 6 Pb. O(тв) + O 2(г) в) 2 Na 2 O 2 + 2 H 2 O(ж) 4 Na. OH(водн) + O 2(г) г) Электролиз водных растворов, кислот и щелочей 4 ОН-(водн) 2 Н 2 О(ж) + О 2(г) + 4ē - анодный процесс

Физические свойства кислорода. Жидкий кислород светло-голубого цвета, сильно парамагнитен. Ткип. = -1830 С, Тпл. = -218, 80 С

Химические свойства кислорода. S 8 + 8 O 2 = 8 SO 2 P 4 + 5 O 2 = P 4 O 10 C + O 2 = CO 2 3 Fe + 2 O 2 = Fe 3 O 4 2 Na + O 2 = Na 2 O 2 H 2 + 1/2 O 2 = H 2 O SO 2 + H 2 O 2 H+ +SO 32 кислотный окисел Ba. O + H 2 O Ba 2+ + 2 OHосновный окисел NO, N 2 O, CO – инертные окислы H 2 O, Al 2 O 3, Ti. O 2, Zn. O, Cr 2 O 3 амфотерные окислы
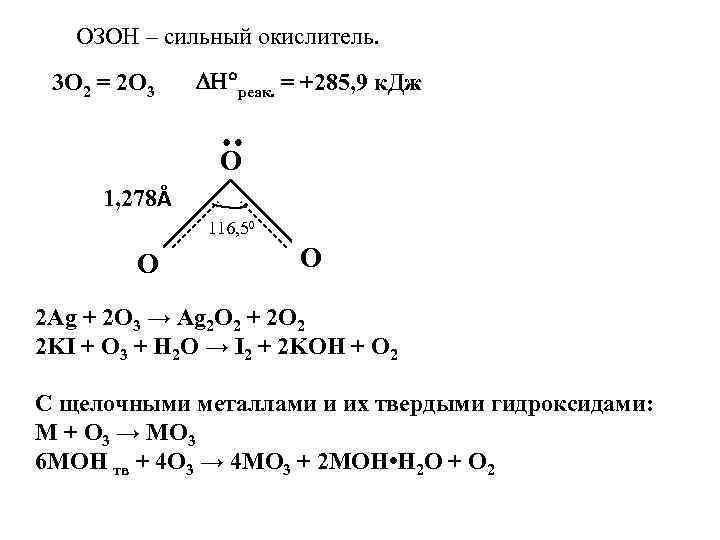
ОЗОН – сильный окислитель. 3 O 2 = 2 O 3 реак. = +285, 9 к. Дж О 1, 278Å 116, 50 О О 2 Ag + 2 O 3 → Ag 2 O 2 + 2 O 2 2 KI + O 3 + H 2 O → I 2 + 2 KOH + O 2 С щелочными металлами и их твердыми гидроксидами: M + O 3 → MO 3 6 MOH тв + 4 О 3 → 4 МО 3 + 2 МОН • Н 2 О + О 2

СЕРА S - 1 s 22 p 63 s 23 p 43 d 0 16 S 8 - самородная сера Fe. S 2 - железный колчедан (пирит) Cu. Fe. S 2 - медный колчедан Pb. S - свинцовый блеск Zn. S - цинковая обманка Mg. SO 4 - кизерит, горькая соль Ca. SO 4 - ангидрит, гипс Na 2 SO 4 10 Н 2 О - глауберова соль

ПОЛУЧЕНИЕ а) Ca. SO 4 + 2 C = Ca. S + 2 CO 2 б) Ca. S + CO 2 + H 2 O = Ca. CO 3 + H 2 S в) H 2 S + 1/2 O 2 S + H 2 O Выплавляется из руд. Используется в с/х, медицине. 2 KNO 3 + 3 C + S = N 2 + 3 CO 2 + K 2 S черный порох

Полиморфизм серы: - S 8 - ромбическая; b- S 8 – моноклинная; Sn - пластическая. Na 2 S 2 O 3 + 2 H 2 SO 4 = [H 2 S 2 O 3] + 2 Na. HSO 4 [H 2 S 2 O 3] = S + SO 2 + H 2 O S 2 O 32 - + 6 H+ + 4ē = 2 S + 3 H 2 O S 2 O 32 - + H 2 O - 4ē = 2 SO 2 + 2 H+ 2 S 2 O 32 - + 4 H+ = 2 S + 2 SO 2 + 2 H 2 O S - в аморфном состоянии.
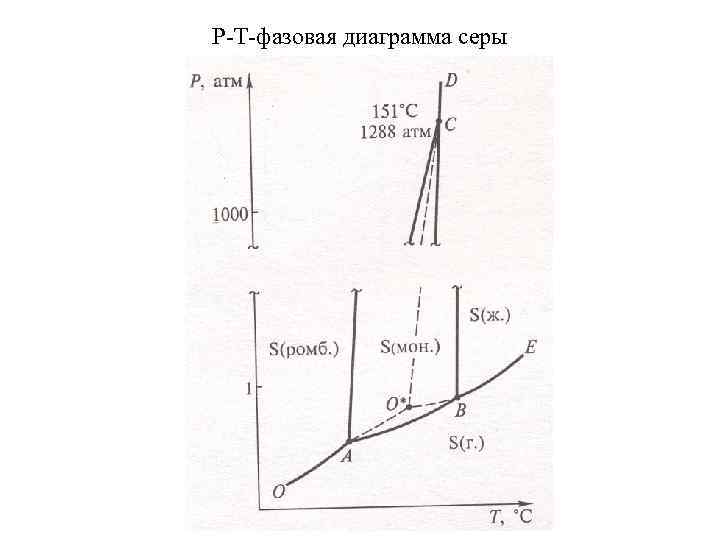
P-T-фазовая диаграмма серы

S + 3 F 2 = SF 6 S + Cl 2 = S 2 Cl 2 S + Cl 2 = SCl 2 S + 2 HNO 3 = H 2 SO 4 + 2 NO

Сера в степени окисления -2. -2 H 2 + S H 2 S Fe. Sтв + 2 HCl = Fe. Cl 2 + H 2 S H+ + HS , HS H+ + S 2 - HSH = 92 K 1 = 10 -7 K 2 = H 2 Sn - сульфаны H-S-S-H - дисероводород, дисульфан H-S-S-S-H - трисероводород, трисульфан H-S-S-H - тетрасероводород, тетрасульфан
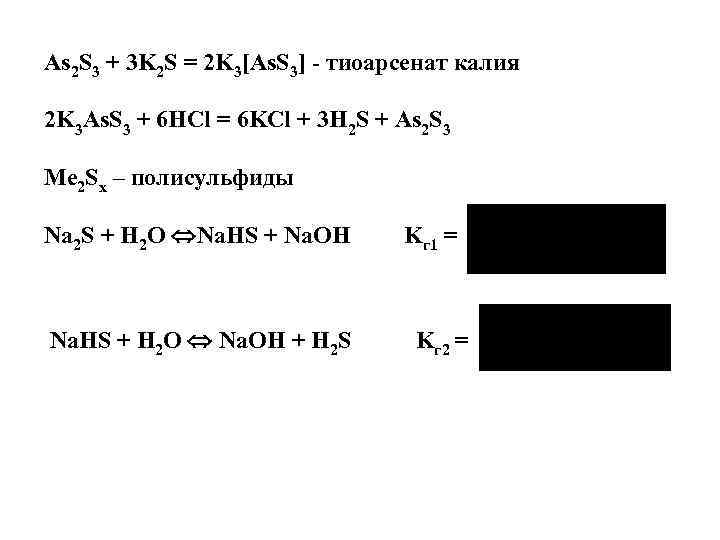
As 2 S 3 + 3 K 2 S = 2 K 3[As. S 3] - тиоарсенат калия 2 K 3 As. S 3 + 6 HCl = 6 KCl + 3 H 2 S + As 2 S 3 Me 2 Sx – полисульфиды Na 2 S + H 2 O Na. HS + Na. OH Na. HS + H 2 O Na. OH + H 2 S Kг 1 = Kг 2 =
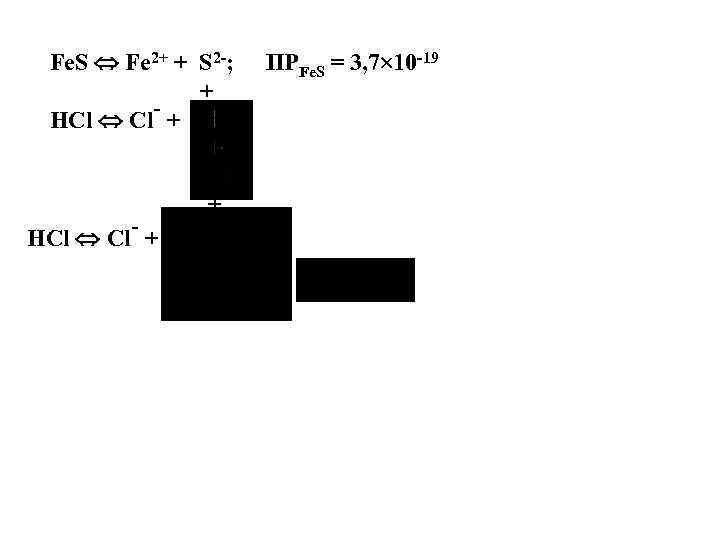
Fe. S Fe 2+ + S 2 -; + HCl Cl + + ПРFe. S = 3, 7 10 -19

Сu. S + HCl реакция не идет, ПРCu. S = 8, 5 10 -45 Hg. S + HCl реакция не идет, ПРHg. S = 4 10 -53 S-2 в растворе меньше, чем S-2 в насыщенном растворе H 2 S. Cu. S + 8 HNO 3 конц. = Cu. SO 4 + 8 NO 2 + 4 H 2 O 3 Pb. O 2 + 4 H 2 S = 3 Pb. S + SO 2 + 4 H 2 O
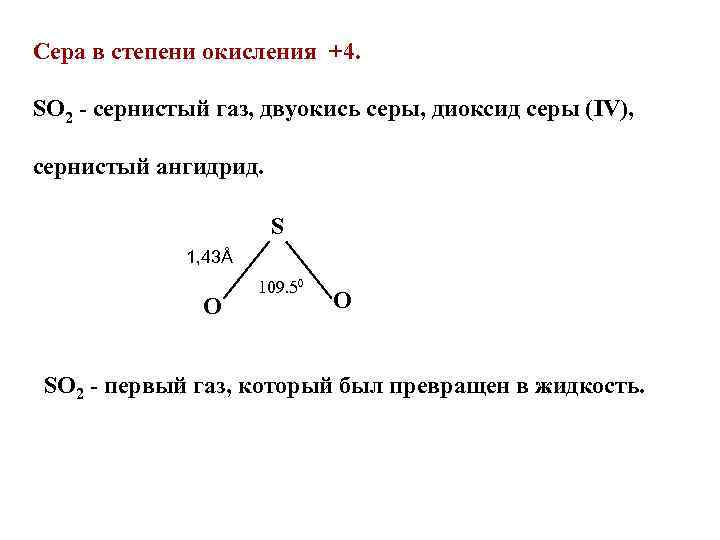
Сера в степени окисления +4. SO 2 - сернистый газ, двуокись серы, диоксид серы (IV), сернистый ангидрид. S 1, 43Å O 109. 50 O SO 2 - первый газ, который был превращен в жидкость.

ПОЛУЧЕНИЕ S + O 2 = SO 2 реак. = -296 к. Дж/моль 2 Fe. S 2 + 11/2 O 2 Fe 2 O 3 + 4 SO 2 пирит Cu + 2 H 2 SO 4 = Cu. SO 4 + SO 2 + 2 H 2 O

Химические свойства. SO 2 + Cl 2 + 2 H 2 O = H 2 SO 4 + 2 HCl SO 2 + H 2 O 2 = H 2 SO 4 Na 2 SO 3 + 1/2 O 2 = Na 2 SO 4 SO 2 + 2 CO = S + 2 CO 2 SO 2 + 2 H 2 S = 3 S + 2 H 2 O SO 2 + 4 HI = 2 I 2 + S + 2 H 2 O
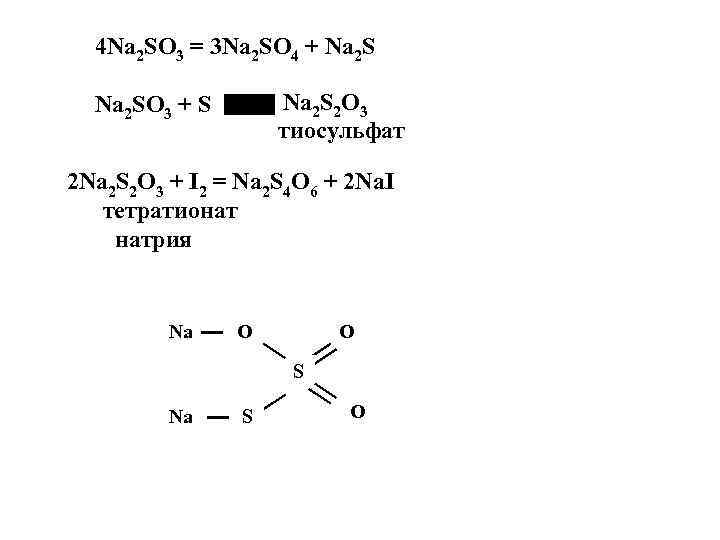
4 Na 2 SO 3 = 3 Na 2 SO 4 + Na 2 S 2 O 3 тиосульфат Na 2 SO 3 + S 2 Na 2 S 2 O 3 + I 2 = Na 2 S 4 O 6 + 2 Na. I тетратионат натрия Na O O S Na S O
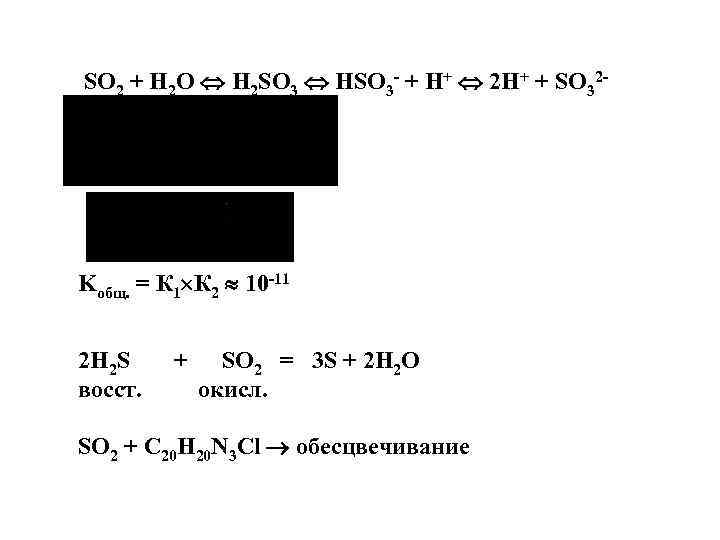
SO 2 + H 2 O H 2 SO 3 HSO 3 - + H+ 2 H+ + SO 32 - Kобщ. = К 1 К 2 10 -11 2 H 2 S восст. + SO 2 = 3 S + 2 H 2 O окисл. SO 2 + C 20 H 20 N 3 Cl обесцвечивание
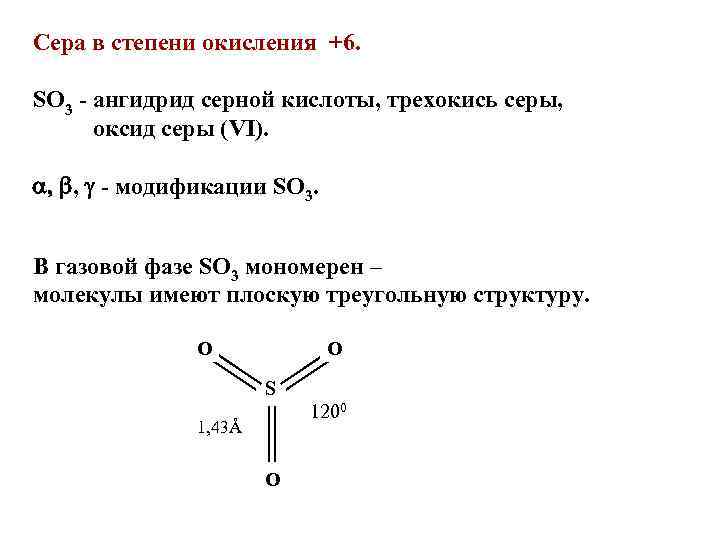
Сера в степени окисления +6. SO 3 - ангидрид серной кислоты, трехокись серы, оксид серы (VI). , - модификации SO 3. В газовой фазе SO 3 мономерен – молекулы имеют плоскую треугольную структуру. О О S 1200 1, 43Å О
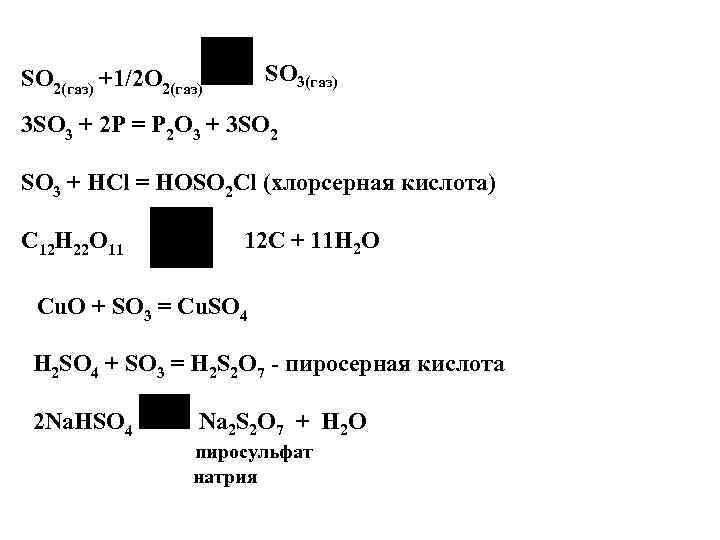
SO 3(газ) SO 2(газ) +1/2 O 2(газ) 3 SO 3 + 2 P = P 2 O 3 + 3 SO 2 SO 3 + HCl = HOSO 2 Cl (хлорсерная кислота) C 12 H 22 O 11 12 C + 11 H 2 O Cu. O + SO 3 = Cu. SO 4 H 2 SO 4 + SO 3 = H 2 S 2 O 7 - пиросерная кислота 2 Na. HSO 4 Na 2 S 2 O 7 + H 2 O пиросульфат натрия

3 Zn + 4 H 2 SO 4(конц. ) = 3 Zn. SO 4 + S + 4 H 2 O 2 H 2 SO 4(конц. ) + Cu = Cu. SO 4 + SO 2 + 2 H 2 O H 2 SO 4(конц. ) + HCl H 2 SO 4(конц. ) + 2 HBr = SO 2 + Br 2 + 2 H 2 O H 2 SO 4(конц. ) + 8 HI H 2 S + 4 I 2 + 4 H 2 O 2 H 2 SO 4(конц. ) + S = 3 SO 2 + 2 H 2 O
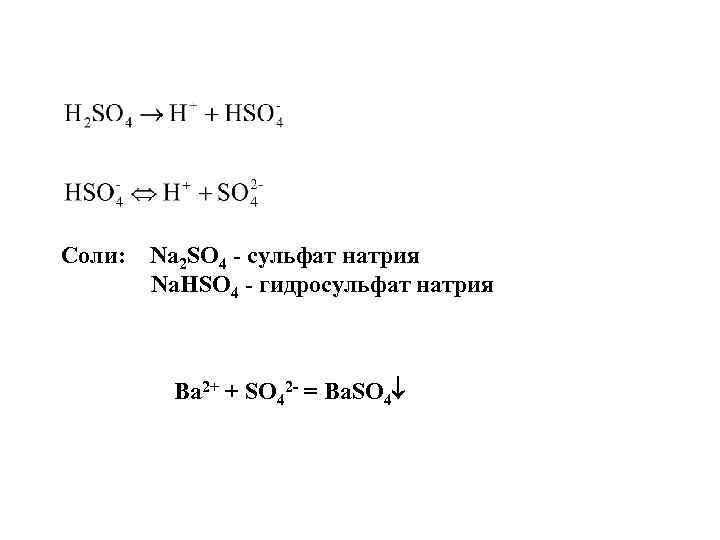
Соли: Na 2 SO 4 - сульфат натрия Na. HSO 4 - гидросульфат натрия Ba 2+ + SO 42 - = Ba. SO 4
2010 Лекция 10 Кислород, сера.ppt