Лекция_10(1 Начало термодинамики) 2сем.pptx
- Количество слайдов: 24
 Лекция 10. Первое начало термодинамики 1
Лекция 10. Первое начало термодинамики 1
 Вопросы: • Статистический и термодинамический методы описания макросистем • Термодинамическая система и ее виды. Термодинамические состояния • Обратимые и необратимые термодинамические процессы • Температура как характеристика термодинамического равновесия • Методы измерения температуры • Внутренняя энергия системы. Теплота и работа • Первое начало термодинамики 2
Вопросы: • Статистический и термодинамический методы описания макросистем • Термодинамическая система и ее виды. Термодинамические состояния • Обратимые и необратимые термодинамические процессы • Температура как характеристика термодинамического равновесия • Методы измерения температуры • Внутренняя энергия системы. Теплота и работа • Первое начало термодинамики 2
 Статистический и термодинамический методы описания макросистем Мы приступаем к изучению систем, состоящих из очень большого числа частиц (молекул, атомов, электронов, фотонов и др. ), т. е. макросистем (или макротел). Примером может служить газ. Казалось бы, поведение таких систем можно рассматривать с позиций законов классической механики. Однако для этого пришлось бы составить огромное число уравнений для всех частиц, а, следовательно, потребовалось бы колоссальное количество времени. Так, если рассмотреть 1 см 3 воздуха при комнатной температуре (20 ºС) и нормальном давлении (760 мм рт. ст. ), то в нем будет находиться ~3. 1019 молекул. Если даже затрачивать только на запись уравнения движения каждой молекулы по 1 с, то на всю систему уравнений потребовалось бы времени в 300 раз больше возраста Вселенной (которой по современным оценкам ~1010 лет). Но именно огромное число частиц в системе позволило в свое время разработать два различных метода изучения макросистем − статистический и термодинамический методы. 3
Статистический и термодинамический методы описания макросистем Мы приступаем к изучению систем, состоящих из очень большого числа частиц (молекул, атомов, электронов, фотонов и др. ), т. е. макросистем (или макротел). Примером может служить газ. Казалось бы, поведение таких систем можно рассматривать с позиций законов классической механики. Однако для этого пришлось бы составить огромное число уравнений для всех частиц, а, следовательно, потребовалось бы колоссальное количество времени. Так, если рассмотреть 1 см 3 воздуха при комнатной температуре (20 ºС) и нормальном давлении (760 мм рт. ст. ), то в нем будет находиться ~3. 1019 молекул. Если даже затрачивать только на запись уравнения движения каждой молекулы по 1 с, то на всю систему уравнений потребовалось бы времени в 300 раз больше возраста Вселенной (которой по современным оценкам ~1010 лет). Но именно огромное число частиц в системе позволило в свое время разработать два различных метода изучения макросистем − статистический и термодинамический методы. 3
 Статистический и термодинамический методы описания макросистем Суть дела в том, что в большой совокупности микрочастиц возникают качественно новые закономерности, имеющие статистический характер. Причем при переходе к системам с малым числом частиц эти закономерности утрачивают свой смысл. Молекулярная (статистическая) физика исходит из представлений о молекулярном строении вещества. При этом она пользуется вероятностными подходами и истолковывает наблюдаемые в опыте свойства макросистем как суммарный, усредненный результат действия отдельных молекул, базируясь на определенных моделях (например, модель идеального газа). Таким образом, статистический метод описания макросистем оперирует средними значениями характеристических величин и через них объясняет изменение наблюдаемых величин. Термодинамика (феноменологическая термодинамика) является постулативной наукой: в ее основе лежат фундаментальные законы − начала термодинамики, установленные путем обобщения большого экспериментального материала. Термодинамика изучает свойства макросистем и протекающие в них процессы, не вдаваясь в микроскопическую природу вещества. В термодинамическом методе используются понятия и величины (V, p, T), относящиеся к системе в целом. 4
Статистический и термодинамический методы описания макросистем Суть дела в том, что в большой совокупности микрочастиц возникают качественно новые закономерности, имеющие статистический характер. Причем при переходе к системам с малым числом частиц эти закономерности утрачивают свой смысл. Молекулярная (статистическая) физика исходит из представлений о молекулярном строении вещества. При этом она пользуется вероятностными подходами и истолковывает наблюдаемые в опыте свойства макросистем как суммарный, усредненный результат действия отдельных молекул, базируясь на определенных моделях (например, модель идеального газа). Таким образом, статистический метод описания макросистем оперирует средними значениями характеристических величин и через них объясняет изменение наблюдаемых величин. Термодинамика (феноменологическая термодинамика) является постулативной наукой: в ее основе лежат фундаментальные законы − начала термодинамики, установленные путем обобщения большого экспериментального материала. Термодинамика изучает свойства макросистем и протекающие в них процессы, не вдаваясь в микроскопическую природу вещества. В термодинамическом методе используются понятия и величины (V, p, T), относящиеся к системе в целом. 4
 Термодинамическая система и ее виды. Термодинамические состояния Термодинамическая система (ТС) − это совокупность макротел, выделенных из окружающей среды с помощью оболочки, которые в общем случае могут обмениваться энергией и веществом между собой и с внешней средой (т. е. с другими телами). Примеры ТС: «твердое тело» , «жидкость» , «газ» , «жидкость + пар» . Каждая из этих ТС состоит из большого количества микрочастиц и поэтому относится к макросистемам. Виды термодинамических систем: § ТС, не обменивающаяся с внешней средой ни энергией, ни веществом, называется изолированной. § ТС, обменивающаяся с внешней средой только энергией, называется закрытой. § ТС, обменивающаяся с внешней средой как энергией, так и веществом, называется открытой. 5
Термодинамическая система и ее виды. Термодинамические состояния Термодинамическая система (ТС) − это совокупность макротел, выделенных из окружающей среды с помощью оболочки, которые в общем случае могут обмениваться энергией и веществом между собой и с внешней средой (т. е. с другими телами). Примеры ТС: «твердое тело» , «жидкость» , «газ» , «жидкость + пар» . Каждая из этих ТС состоит из большого количества микрочастиц и поэтому относится к макросистемам. Виды термодинамических систем: § ТС, не обменивающаяся с внешней средой ни энергией, ни веществом, называется изолированной. § ТС, обменивающаяся с внешней средой только энергией, называется закрытой. § ТС, обменивающаяся с внешней средой как энергией, так и веществом, называется открытой. 5
 Термодинамическая система и ее виды. Термодинамические состояния Часто имеют дело с адиабатически изолированной системой, т. е. ТС, в которой изменения ее состояния могут происходить только благодаря механическим перемещениям частей системы и ее оболочки причем без теплообмена с окружающей средой. В качестве примера такой системы рассмотрим жидкий азот, заключенный в сосуд Дьюара. Этот сосуд имеет внутреннюю 1 и внешнюю 2 жесткие оболочки, зазор между которыми тщательно отвакуумирован (5) и играет роль надежной теплоизоляции 3. Через малое входное отверстие (горловина) 4, которое выполнено с тонкими стенками для обеспечения низкой теплопроводности, заливается азот N 2. После этого горловина накрывается небольшим колпачком, и сосуд готов к транспортировке. N 2 6
Термодинамическая система и ее виды. Термодинамические состояния Часто имеют дело с адиабатически изолированной системой, т. е. ТС, в которой изменения ее состояния могут происходить только благодаря механическим перемещениям частей системы и ее оболочки причем без теплообмена с окружающей средой. В качестве примера такой системы рассмотрим жидкий азот, заключенный в сосуд Дьюара. Этот сосуд имеет внутреннюю 1 и внешнюю 2 жесткие оболочки, зазор между которыми тщательно отвакуумирован (5) и играет роль надежной теплоизоляции 3. Через малое входное отверстие (горловина) 4, которое выполнено с тонкими стенками для обеспечения низкой теплопроводности, заливается азот N 2. После этого горловина накрывается небольшим колпачком, и сосуд готов к транспортировке. N 2 6
 Термодинамическая система и ее виды. Термодинамические состояния Макросистемы могут находиться в различных состояниях, отличающихся, например, температурой Т, давлением р, объемом V, плотностью ρ и др. Подобные величины, характеризующие состояние системы, называются параметрами состояния (для ТС – термодинамическими параметрами). Если эти параметры имеют вполне определенные и постоянные значения для любой части системы, то такое состояние системы называют равновесным. Сами ТС, у которых параметры (Т, р, V, ρ) имеют определенные и не изменяющиеся с течением времени значения, называются равновесными ТС. Если система выведена тем или иным внешним образом из состояния равновесия, то она становится неравновесной ТС. Параметры состояния могут быть внутренними и внешними. Рис. 1. Сосуд с поршнем р перемещение поршня V – внешний параметр внутренний параметр р – внешний параметр Рис. 2. Шар– внутренний монгольфьер параметр поступление горячего воздуха пламя горелки V 7
Термодинамическая система и ее виды. Термодинамические состояния Макросистемы могут находиться в различных состояниях, отличающихся, например, температурой Т, давлением р, объемом V, плотностью ρ и др. Подобные величины, характеризующие состояние системы, называются параметрами состояния (для ТС – термодинамическими параметрами). Если эти параметры имеют вполне определенные и постоянные значения для любой части системы, то такое состояние системы называют равновесным. Сами ТС, у которых параметры (Т, р, V, ρ) имеют определенные и не изменяющиеся с течением времени значения, называются равновесными ТС. Если система выведена тем или иным внешним образом из состояния равновесия, то она становится неравновесной ТС. Параметры состояния могут быть внутренними и внешними. Рис. 1. Сосуд с поршнем р перемещение поршня V – внешний параметр внутренний параметр р – внешний параметр Рис. 2. Шар– внутренний монгольфьер параметр поступление горячего воздуха пламя горелки V 7
 Обратимые и необратимые процессы Термодинамическим процессом называется переход системы из одного состояния в другое. Обычно такой переход связан с нарушением равновесия системы. Бесконечно медленный процесс, состоящий из последовательности равновесных состояний, называется равновесным (или квазистатическим). Равновесные термодинамические процессы, протекающие в изотропных системах, являются обратимыми, т. е. при изменении направления процессов с прямого хода на обратный (например см. рис. , при замене расширения газа 1– 2 его сжатием 2– 1) системы будут проходить через те же равновесные состояния, но в обратной последовательности. Процесс, при котором система после ряда изменений возвращается в исходное состояние, называется круговым процессом (или циклом 1– 2– 1). p 2 1 V 8
Обратимые и необратимые процессы Термодинамическим процессом называется переход системы из одного состояния в другое. Обычно такой переход связан с нарушением равновесия системы. Бесконечно медленный процесс, состоящий из последовательности равновесных состояний, называется равновесным (или квазистатическим). Равновесные термодинамические процессы, протекающие в изотропных системах, являются обратимыми, т. е. при изменении направления процессов с прямого хода на обратный (например см. рис. , при замене расширения газа 1– 2 его сжатием 2– 1) системы будут проходить через те же равновесные состояния, но в обратной последовательности. Процесс, при котором система после ряда изменений возвращается в исходное состояние, называется круговым процессом (или циклом 1– 2– 1). p 2 1 V 8
 Обратимые и необратимые процессы У тела, подогреваемого с одной стороны (+ Q 1) и охлаждаемого с другой (– Q 2), температура в разных точках будет различной, и телу, как целому, нельзя приписать определенное значение температуры Тf. Состояние системы, в котором хотя бы один из параметров (например Т) не имеет определенного значения, называется неравновесным. Нулевое начало термодинамики: Если систему (тело), находящуюся в неравновесном состоянии, изолировать от внешней среды, т. е. предоставить самой себе, то она перейдет в равновесное состояние. Так в неравномерно нагретом теле, помещенном в адиабатически изолированную оболочку, сразу начинается необратимый процесс теплопередачи между сторонами (гранями) тела qc, а также идет процесс теплообмена излучением qr между телом и замкнутым пространством. Эти процессы завершаются установлением термодинамического равновесия с общей для всей изолированной системы температурой Тр. +Q 1 Тр. Тело = const qr Т 1 q –Q 2 c Т Т Т = fconst р qr Оболочка 2 Тело 9
Обратимые и необратимые процессы У тела, подогреваемого с одной стороны (+ Q 1) и охлаждаемого с другой (– Q 2), температура в разных точках будет различной, и телу, как целому, нельзя приписать определенное значение температуры Тf. Состояние системы, в котором хотя бы один из параметров (например Т) не имеет определенного значения, называется неравновесным. Нулевое начало термодинамики: Если систему (тело), находящуюся в неравновесном состоянии, изолировать от внешней среды, т. е. предоставить самой себе, то она перейдет в равновесное состояние. Так в неравномерно нагретом теле, помещенном в адиабатически изолированную оболочку, сразу начинается необратимый процесс теплопередачи между сторонами (гранями) тела qc, а также идет процесс теплообмена излучением qr между телом и замкнутым пространством. Эти процессы завершаются установлением термодинамического равновесия с общей для всей изолированной системы температурой Тр. +Q 1 Тр. Тело = const qr Т 1 q –Q 2 c Т Т Т = fconst р qr Оболочка 2 Тело 9
 Температура как характеристика термодинамического равновесия Понятие температуры можно считать следствием из нулевого начала термодинамики. Температура – это величина, характеризующая состояние термодинамического равновесия макросистемы. Если после установления теплового контакта между телами одно из тел передает энергию другому (посредством теплопередачи Q 12), то считают, что первое тело имеет бóльшую температуру Т 1, чем второе – Т 2. T 1 > T 2 Q 12 Т 1 Т 2 Для данной изолированной системы из двух тел процесс теплопередачи закончится установлением термодинамического равновесия с определенной температурой Тр. 10
Температура как характеристика термодинамического равновесия Понятие температуры можно считать следствием из нулевого начала термодинамики. Температура – это величина, характеризующая состояние термодинамического равновесия макросистемы. Если после установления теплового контакта между телами одно из тел передает энергию другому (посредством теплопередачи Q 12), то считают, что первое тело имеет бóльшую температуру Т 1, чем второе – Т 2. T 1 > T 2 Q 12 Т 1 Т 2 Для данной изолированной системы из двух тел процесс теплопередачи закончится установлением термодинамического равновесия с определенной температурой Тр. 10
 Температура как характеристика термодинамического равновесия Равновесные термодинамические системы обладают следующими свойствами: § если две равновесные ТС, имеющие одинаковую температуру, приводятся в тепловой контакт, то образующаяся совокупная система также находится в равновесии и имеет ту же температуру; § если некоторая равновесная ТС имеет одну и ту же температуру с двумя другими системами, то все три системы находятся в состоянии равновесия при одной и той же температуре. Каждому равновесному состоянию системы можно поставить в соответствие некоторый параметр (физическую величину), характеризующий температуру системы, причем, чем выше температура, тем больше значение этого параметра. Таким образом, температура является мерой термодинамически равновесного состояния, и для изучения поведения макросистем крайне важным является умение определять (измерять) температуру системы (тела). 11
Температура как характеристика термодинамического равновесия Равновесные термодинамические системы обладают следующими свойствами: § если две равновесные ТС, имеющие одинаковую температуру, приводятся в тепловой контакт, то образующаяся совокупная система также находится в равновесии и имеет ту же температуру; § если некоторая равновесная ТС имеет одну и ту же температуру с двумя другими системами, то все три системы находятся в состоянии равновесия при одной и той же температуре. Каждому равновесному состоянию системы можно поставить в соответствие некоторый параметр (физическую величину), характеризующий температуру системы, причем, чем выше температура, тем больше значение этого параметра. Таким образом, температура является мерой термодинамически равновесного состояния, и для изучения поведения макросистем крайне важным является умение определять (измерять) температуру системы (тела). 11
 Методы измерения температуры Любой метод измерения температуры требует установления температурной шкалы, т. е. упорядоченной последовательности значений температуры. По международному соглашению температурную шкалу строят на основе реперных точек. Наиболее часто в качестве реперов используют характерные температуры фазовых переходов воды: точка плавления льда, точка кипения воды (при нормальном атмосферном давлении). Такие реперы выбраны в температурных шкалах, предложенных А. Цельсием, Р. Реомюром, Г. Фаренгейтом. Шкалы Реомюра (°R) и Фаренгейта (°F) в настоящее время применяют в США, Великобритании и ряде других стран. А. Цельсий в 1742 г. предложил температурный интервал между точками плавления льда и кипения воды разбить на 100 равных частей (градусов). Шкалу Цельсия (°С) широко используют и сегодня с учетом уточнения: один градус Цельсия равен одному градусу Кельвина. При этом принимают: tпл= 0 °С, а tкип= 100 °С при р = 105 Па. 12
Методы измерения температуры Любой метод измерения температуры требует установления температурной шкалы, т. е. упорядоченной последовательности значений температуры. По международному соглашению температурную шкалу строят на основе реперных точек. Наиболее часто в качестве реперов используют характерные температуры фазовых переходов воды: точка плавления льда, точка кипения воды (при нормальном атмосферном давлении). Такие реперы выбраны в температурных шкалах, предложенных А. Цельсием, Р. Реомюром, Г. Фаренгейтом. Шкалы Реомюра (°R) и Фаренгейта (°F) в настоящее время применяют в США, Великобритании и ряде других стран. А. Цельсий в 1742 г. предложил температурный интервал между точками плавления льда и кипения воды разбить на 100 равных частей (градусов). Шкалу Цельсия (°С) широко используют и сегодня с учетом уточнения: один градус Цельсия равен одному градусу Кельвина. При этом принимают: tпл= 0 °С, а tкип= 100 °С при р = 105 Па. 12
 Методы измерения температуры После введения Международной системы единиц (СИ) были рекомендованы к применению две температурные шкалы. Одна из них – термодинамическая шкала, она не зависит от свойств рабочего тела термометра и вводится с помощью цикла Карно. Единицей измерения температуры в этой шкале является 1 К – одна из семи основных единиц в СИ; названа в честь англ. физика У. Томсона (лорд Кельвин), разработчика шкалы. Другая шкала – международная практическая шкала – имеет 11 реперных точек; единицей измерения температуры в ней также является 1 К. Основной реперной точкой для этих двух шкал является тройная точка воды, которая соответствует строго определенным значениям Т = 273, 16 К и р = 609 Па, когда вода может одновременно находиться в твердом, жидком и газообразном состояниях. 13
Методы измерения температуры После введения Международной системы единиц (СИ) были рекомендованы к применению две температурные шкалы. Одна из них – термодинамическая шкала, она не зависит от свойств рабочего тела термометра и вводится с помощью цикла Карно. Единицей измерения температуры в этой шкале является 1 К – одна из семи основных единиц в СИ; названа в честь англ. физика У. Томсона (лорд Кельвин), разработчика шкалы. Другая шкала – международная практическая шкала – имеет 11 реперных точек; единицей измерения температуры в ней также является 1 К. Основной реперной точкой для этих двух шкал является тройная точка воды, которая соответствует строго определенным значениям Т = 273, 16 К и р = 609 Па, когда вода может одновременно находиться в твердом, жидком и газообразном состояниях. 13
 Методы измерения температуры Кроме задания реперов необходимо также выбрать термодинамическое свойство тела (т. е. некоторую физическую величину), изменение которого является признаком изменения температуры ( так называемым термометрическим признаком). Тело, с привлечением термометрического признака которого осуществляется измерение (определение) температуры, называется термометрическим телом. Термометрическими признаками могут быть: § изменение давления газа (∆р); § изменение объема газа или жидкости (∆V); § изменение электрического сопротивления тела (∆R); § изменение разности электрических потенциалов на границе раздела двух разнородных проводящих тел (∆φ) и др. Соответствующие этим признакам приборы для измерения температуры: § газовый термометр; § спиртовой и ртутный термометры; § термометр с датчиком термосопротивления; § термометр с датчиком – термопарой. 14
Методы измерения температуры Кроме задания реперов необходимо также выбрать термодинамическое свойство тела (т. е. некоторую физическую величину), изменение которого является признаком изменения температуры ( так называемым термометрическим признаком). Тело, с привлечением термометрического признака которого осуществляется измерение (определение) температуры, называется термометрическим телом. Термометрическими признаками могут быть: § изменение давления газа (∆р); § изменение объема газа или жидкости (∆V); § изменение электрического сопротивления тела (∆R); § изменение разности электрических потенциалов на границе раздела двух разнородных проводящих тел (∆φ) и др. Соответствующие этим признакам приборы для измерения температуры: § газовый термометр; § спиртовой и ртутный термометры; § термометр с датчиком термосопротивления; § термометр с датчиком – термопарой. 14
 Методы измерения температуры Кроме перечисленных средств измерения температуры существует еще отдельный класс оптических термометрических приборов – пирометры – для измерения температуры нагретых веществ по интенсивности их теплового излучения. Все термометрические средства предполагают выполнение (и использование) нулевого начала термодинамики. Т. е. приводя термометрическое тело (датчик) в тепловой контакт с измеряемым телом (объектом), по прошествии времени, достаточного для установления термодинамического равновесия в системе «датчик – объект» , их температуры сравняются. С этого момента можно считать температуру, которую показывает термометр, равной температуре объекта. Далее рассмотрим принцип действия газового термометра. 15
Методы измерения температуры Кроме перечисленных средств измерения температуры существует еще отдельный класс оптических термометрических приборов – пирометры – для измерения температуры нагретых веществ по интенсивности их теплового излучения. Все термометрические средства предполагают выполнение (и использование) нулевого начала термодинамики. Т. е. приводя термометрическое тело (датчик) в тепловой контакт с измеряемым телом (объектом), по прошествии времени, достаточного для установления термодинамического равновесия в системе «датчик – объект» , их температуры сравняются. С этого момента можно считать температуру, которую показывает термометр, равной температуре объекта. Далее рассмотрим принцип действия газового термометра. 15
 Методы измерения температуры Газовый термометр постоянного объема Данный термометр был изобретен Г. Галилеем и состоит (см. рис. ) из сосуда с газом 1 (последний играет роль термометрического тела), U-образного подвижного жидкостного манометра 3 и гибких соединительных трубок 4. В этом приборе термометрическим V = const признаком является давление газа в сосуде при некотором фиксированном объеме V = ∆s const. Так, например, при увеличении ↑∆p ↑∆T температуры окружающей атмосферы на ∆Т ∆h градусов давление в сосуде увеличивается соответственно на ∆р, что приводит к расширению газа и вытеснению рабочей жидкости из правой трубки манометра 3 в левую. Для восстановления исходного объема газа V вертикальным перемещением ∆s левой трубки доводят уровень жидкости в правой трубке до реперной метки 2 и измеряют разность высот уровней ∆h, которая соответствует увеличениям ∆р в давлении газа и ∆Т 16 в температуре.
Методы измерения температуры Газовый термометр постоянного объема Данный термометр был изобретен Г. Галилеем и состоит (см. рис. ) из сосуда с газом 1 (последний играет роль термометрического тела), U-образного подвижного жидкостного манометра 3 и гибких соединительных трубок 4. В этом приборе термометрическим V = const признаком является давление газа в сосуде при некотором фиксированном объеме V = ∆s const. Так, например, при увеличении ↑∆p ↑∆T температуры окружающей атмосферы на ∆Т ∆h градусов давление в сосуде увеличивается соответственно на ∆р, что приводит к расширению газа и вытеснению рабочей жидкости из правой трубки манометра 3 в левую. Для восстановления исходного объема газа V вертикальным перемещением ∆s левой трубки доводят уровень жидкости в правой трубке до реперной метки 2 и измеряют разность высот уровней ∆h, которая соответствует увеличениям ∆р в давлении газа и ∆Т 16 в температуре.
 Внутренняя энергия системы. Теплота и работа Первое начало термодинамики относится к одному из фундаментальных законов физики макросистем, оно является обобщением большого экспериментального материала и представляет собой по сути обобщенный закон сохранения энергии, отнесенный к тепловым процессам. Этот закон содержит три величины: внутреннюю энергию U, работу А и теплоту Q. Определим физический смысл этих величин. Внутренняя энергия U макросистемы состоит из: § суммарной кинетической энергии хаотического движения молекул в Ц-системе отсчета, связанной с самой макросистемой (в эту сумму входят кинетические энергии поступательного, вращательного и колебательного движений молекул рассматриваемой системы); § собственной потенциальной энергии взаимодействия всех молекул данной макросистемы (здесь не учитывается потенциальная энергия всей системы во внешнем силовом поле); § внутримолекулярной энергии, т. е. энергии электронных оболочек атомов и внутриядерной энергии ( часто вклад этой энергии во внутреннюю энергию постоянен и не зависит от вида процесса). 17
Внутренняя энергия системы. Теплота и работа Первое начало термодинамики относится к одному из фундаментальных законов физики макросистем, оно является обобщением большого экспериментального материала и представляет собой по сути обобщенный закон сохранения энергии, отнесенный к тепловым процессам. Этот закон содержит три величины: внутреннюю энергию U, работу А и теплоту Q. Определим физический смысл этих величин. Внутренняя энергия U макросистемы состоит из: § суммарной кинетической энергии хаотического движения молекул в Ц-системе отсчета, связанной с самой макросистемой (в эту сумму входят кинетические энергии поступательного, вращательного и колебательного движений молекул рассматриваемой системы); § собственной потенциальной энергии взаимодействия всех молекул данной макросистемы (здесь не учитывается потенциальная энергия всей системы во внешнем силовом поле); § внутримолекулярной энергии, т. е. энергии электронных оболочек атомов и внутриядерной энергии ( часто вклад этой энергии во внутреннюю энергию постоянен и не зависит от вида процесса). 17
 Внутренняя энергия системы. Теплота и работа Свойства внутренней энергии: § внутренняя энергия является функцией состояния и не зависит от того, каким путем система пришла в данное состояние (при переходе системы из состояния 1 в состояние 2 приращение внутренней энергии ∆U определяется только конечным U 2 и начальным U 1 ее значениями и не зависит от вида процесса [1– 2], т. е. всегда ∆U = U 2 – U 1); 2 1 § внутренняя энергия является величиной аддитивной, т. е. для большой системы, состоящей из нескольких подсистем (частей), полная внутренняя энергия равна сумме энергий отдельных подсистем 18
Внутренняя энергия системы. Теплота и работа Свойства внутренней энергии: § внутренняя энергия является функцией состояния и не зависит от того, каким путем система пришла в данное состояние (при переходе системы из состояния 1 в состояние 2 приращение внутренней энергии ∆U определяется только конечным U 2 и начальным U 1 ее значениями и не зависит от вида процесса [1– 2], т. е. всегда ∆U = U 2 – U 1); 2 1 § внутренняя энергия является величиной аддитивной, т. е. для большой системы, состоящей из нескольких подсистем (частей), полная внутренняя энергия равна сумме энергий отдельных подсистем 18
 Внутренняя энергия системы. Теплота и работа Работа А макросистемы сопровождается тем или иным механическим перемещением внешних тел, действующих на систему (так, например, ведет себя поршень в цилиндре с газом). Если объем макросистемы (газ) получает элементарное приращение d. V, а давление, оказываемое газом на стенки цилиндра и поршень, равно р, то элементарная работа δА сил, действующих со стороны газа на поршень: δА = р. d. V (1) Последнее легко доказывается из определения механической работы: δА = F. dh, где F – сила (нормальная), с которой газ действует на поршень, dh – элементарное перемещение поршня. Выразив силу как F = p. S (S – площадь поршня), получаем для δА = p. S. dh = p. d. V. Работа, совершаемая газом при конечном увеличении объема системы от V 1 до V 2, S dh определяется интегралом: F и является положительной. p Работа по сжатию газа (уменьшению объема системы) считается отрицательной. 19
Внутренняя энергия системы. Теплота и работа Работа А макросистемы сопровождается тем или иным механическим перемещением внешних тел, действующих на систему (так, например, ведет себя поршень в цилиндре с газом). Если объем макросистемы (газ) получает элементарное приращение d. V, а давление, оказываемое газом на стенки цилиндра и поршень, равно р, то элементарная работа δА сил, действующих со стороны газа на поршень: δА = р. d. V (1) Последнее легко доказывается из определения механической работы: δА = F. dh, где F – сила (нормальная), с которой газ действует на поршень, dh – элементарное перемещение поршня. Выразив силу как F = p. S (S – площадь поршня), получаем для δА = p. S. dh = p. d. V. Работа, совершаемая газом при конечном увеличении объема системы от V 1 до V 2, S dh определяется интегралом: F и является положительной. p Работа по сжатию газа (уменьшению объема системы) считается отрицательной. 19
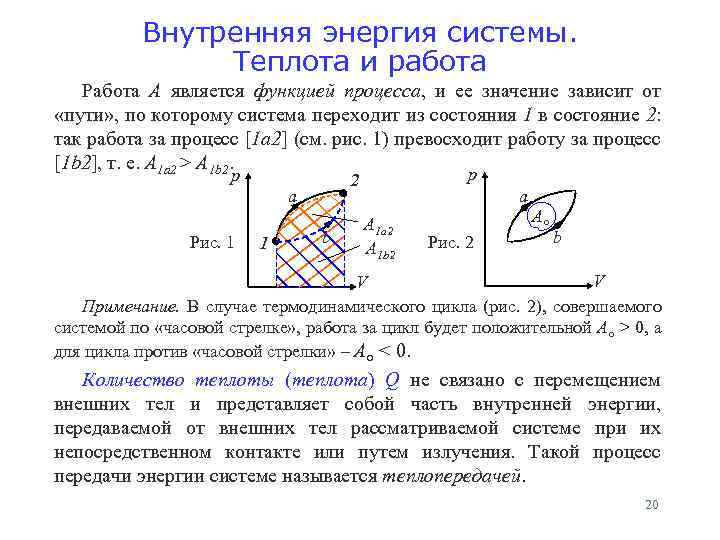 Внутренняя энергия системы. Теплота и работа Работа А является функцией процесса, и ее значение зависит от «пути» , по которому система переходит из состояния 1 в состояние 2: так работа за процесс [1 a 2] (см. рис. 1) превосходит работу за процесс [1 b 2], т. е. А 1 а 2 > А 1 b 2. р a Рис. 1 1 р 2 b a А 1 а 2 А 1 b 2 Рис. 2 А○ b V V Примечание. В случае термодинамического цикла (рис. 2), совершаемого системой по «часовой стрелке» , работа за цикл будет положительной А○ > 0, а для цикла против «часовой стрелки» – А○ < 0. Количество теплоты (теплота) Q не связано с перемещением внешних тел и представляет собой часть внутренней энергии, передаваемой от внешних тел рассматриваемой системе при их непосредственном контакте или путем излучения. Такой процесс передачи энергии системе называется теплопередачей. 20
Внутренняя энергия системы. Теплота и работа Работа А является функцией процесса, и ее значение зависит от «пути» , по которому система переходит из состояния 1 в состояние 2: так работа за процесс [1 a 2] (см. рис. 1) превосходит работу за процесс [1 b 2], т. е. А 1 а 2 > А 1 b 2. р a Рис. 1 1 р 2 b a А 1 а 2 А 1 b 2 Рис. 2 А○ b V V Примечание. В случае термодинамического цикла (рис. 2), совершаемого системой по «часовой стрелке» , работа за цикл будет положительной А○ > 0, а для цикла против «часовой стрелки» – А○ < 0. Количество теплоты (теплота) Q не связано с перемещением внешних тел и представляет собой часть внутренней энергии, передаваемой от внешних тел рассматриваемой системе при их непосредственном контакте или путем излучения. Такой процесс передачи энергии системе называется теплопередачей. 20
 Внутренняя энергия системы. Теплота и работа В 1840 -х годах английский физик Дж. Джоуль провел серию экспериментов по выяснению соотношения между теплотой и механической работой. Им был опубликован очень важный результат по установлению механического эквивалента теплоты, который составлял величину в современных единицах измерения 4, 185 Дж/кал. В установке Джоуля (см. рис. ) воду 7, находящуюся в калориметре 6 (сосуд с теплоизолированными стенками), перемешивали лопатками 5, насаженными на деревянный нетеплопроводный стержень-шкив 4. Дополнительно в сосуде были установлены перегородки с прорезями 8, которые 8 ограничивали скорость воды при вращении. Вследствие действия сил внутреннего трения между слоями жидкости по окончании вращения лопаток циркулирующие потоки быстро затухали, и вода приходила в термодинамическое равновесие. Вода в калориметре рассматривалась как адиабатически изолированная система, т. е. изменения ее состояния могли происходить только в результате механических 21 перемещений ее частей (областей).
Внутренняя энергия системы. Теплота и работа В 1840 -х годах английский физик Дж. Джоуль провел серию экспериментов по выяснению соотношения между теплотой и механической работой. Им был опубликован очень важный результат по установлению механического эквивалента теплоты, который составлял величину в современных единицах измерения 4, 185 Дж/кал. В установке Джоуля (см. рис. ) воду 7, находящуюся в калориметре 6 (сосуд с теплоизолированными стенками), перемешивали лопатками 5, насаженными на деревянный нетеплопроводный стержень-шкив 4. Дополнительно в сосуде были установлены перегородки с прорезями 8, которые 8 ограничивали скорость воды при вращении. Вследствие действия сил внутреннего трения между слоями жидкости по окончании вращения лопаток циркулирующие потоки быстро затухали, и вода приходила в термодинамическое равновесие. Вода в калориметре рассматривалась как адиабатически изолированная система, т. е. изменения ее состояния могли происходить только в результате механических 21 перемещений ее частей (областей).
 Внутренняя энергия системы. Теплота и работа В опыте Джоуля механическая работа, состоящая в перемешивании воды в калориметре, определялась по изменению механической энергии двух гирь 1, опускавшихся на тросах 2 под действием своего веса и создававших с помощью шкива вращение стержня с лопатками. Зная высоту, на которую переместились гири, и их скорости в нижней точке, вычисляли изменение механической энергии системы. Переход воды из одного состояния в другое определялся по измерениям ее температуры в начальном и конечном состояниях. При заданных объеме воды и внешнем давлении (они считались постоянными) температура полностью определяла состояние равновесия системы. Джоуль установил, что при различных массах грузов, скоростях вращения лопаток работа Á12, произведенная над водой при адиабатическом переходе из состояния 1 с температурой Т 1 в состояние 2 с температурой Т 2, остается неизменной при одинаковом количестве воды. Эта работа равна изменению функции состояния системы, которой является внутренняя энергия, т. е. имеем равенство: U 2 – U 1 = Á12 (3) 22
Внутренняя энергия системы. Теплота и работа В опыте Джоуля механическая работа, состоящая в перемешивании воды в калориметре, определялась по изменению механической энергии двух гирь 1, опускавшихся на тросах 2 под действием своего веса и создававших с помощью шкива вращение стержня с лопатками. Зная высоту, на которую переместились гири, и их скорости в нижней точке, вычисляли изменение механической энергии системы. Переход воды из одного состояния в другое определялся по измерениям ее температуры в начальном и конечном состояниях. При заданных объеме воды и внешнем давлении (они считались постоянными) температура полностью определяла состояние равновесия системы. Джоуль установил, что при различных массах грузов, скоростях вращения лопаток работа Á12, произведенная над водой при адиабатическом переходе из состояния 1 с температурой Т 1 в состояние 2 с температурой Т 2, остается неизменной при одинаковом количестве воды. Эта работа равна изменению функции состояния системы, которой является внутренняя энергия, т. е. имеем равенство: U 2 – U 1 = Á12 (3) 22
 Первое начало термодинамики В опыте Джоуля рассматривалась термодинамическая система (ТС), заключенная в адиабатическую оболочку. Однако большинство ТС такой оболочки не имеют и находятся в состоянии постоянного теплообмена с окружающими телами. Первое начало термодинамики утверждает, что приращение внутренней энергии ∆U у ТС может быть обусловлено как совершением механической работы, так и теплопередачей. Поэтому можно записать: ∆U = U 2 – U 1 = Á + Q (4) где Á – работа, совершенная над системой, Q – количество теплоты, переданной системе от окружающих тел. Так как Á = – А, где А – работа, совершенная самой системой над внешними телами, то первое начало термодинамики в форме (4) может быть сформулировано следующим образом: количество теплоты Q, переданное макросистеме, идет на приращение ее внутренней энергии ∆U и на совершение системой работы А над внешними телами, т. е. Q = ∆U + A (5) 23
Первое начало термодинамики В опыте Джоуля рассматривалась термодинамическая система (ТС), заключенная в адиабатическую оболочку. Однако большинство ТС такой оболочки не имеют и находятся в состоянии постоянного теплообмена с окружающими телами. Первое начало термодинамики утверждает, что приращение внутренней энергии ∆U у ТС может быть обусловлено как совершением механической работы, так и теплопередачей. Поэтому можно записать: ∆U = U 2 – U 1 = Á + Q (4) где Á – работа, совершенная над системой, Q – количество теплоты, переданной системе от окружающих тел. Так как Á = – А, где А – работа, совершенная самой системой над внешними телами, то первое начало термодинамики в форме (4) может быть сформулировано следующим образом: количество теплоты Q, переданное макросистеме, идет на приращение ее внутренней энергии ∆U и на совершение системой работы А над внешними телами, т. е. Q = ∆U + A (5) 23
 Первое начало термодинамики Дифференциальная форма первого начала термодинамики утверждает, что элементарное количество теплоты δQ, переданное системе, идет на элементарное приращение ее внутренней энергии d. U и на совершение системой элементарной механической работы δА над внешними телами, т. е. δQ = d. U + δА (6) Согласно первому началу термодинамики невозможен «перпетуум мобиле» 1 рода, т. е. невозможен такой периодически действующий двигатель, который совершал бы полезную работу без подвода внешней энергии к нему. Действительно, если к системе не подводится теплота, то в соответствии с (5) работа может быть совершена только за счет убыли внутренней энергии системы. Но внутренняя энергия любой системы ограничена, а, следовательно, и полезная работа будет ограниченной величиной. После исчерпания внутренней энергии такой «двигатель» остановится. 24
Первое начало термодинамики Дифференциальная форма первого начала термодинамики утверждает, что элементарное количество теплоты δQ, переданное системе, идет на элементарное приращение ее внутренней энергии d. U и на совершение системой элементарной механической работы δА над внешними телами, т. е. δQ = d. U + δА (6) Согласно первому началу термодинамики невозможен «перпетуум мобиле» 1 рода, т. е. невозможен такой периодически действующий двигатель, который совершал бы полезную работу без подвода внешней энергии к нему. Действительно, если к системе не подводится теплота, то в соответствии с (5) работа может быть совершена только за счет убыли внутренней энергии системы. Но внутренняя энергия любой системы ограничена, а, следовательно, и полезная работа будет ограниченной величиной. После исчерпания внутренней энергии такой «двигатель» остановится. 24


