LecSS-10(2012).ppt
- Количество слайдов: 42
 Лекция-10 Кинетика гетерогенных реакций
Лекция-10 Кинетика гетерогенных реакций
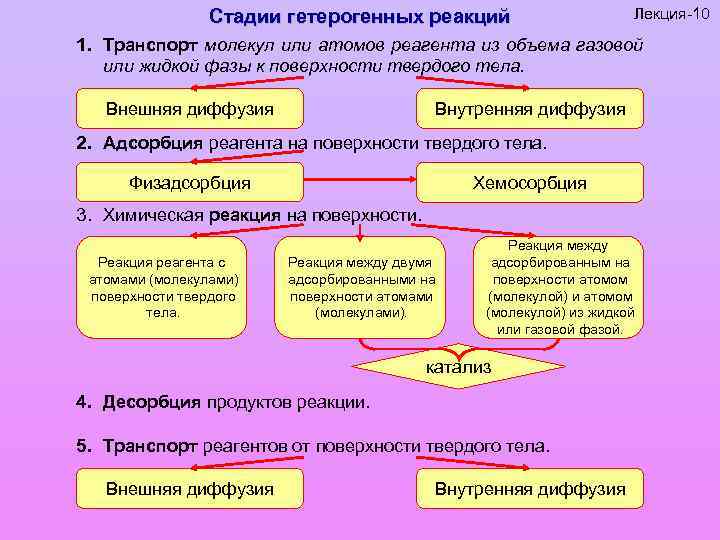 Стадии гетерогенных реакций Лекция-10 1. Транспорт молекул или атомов реагента из объема газовой или жидкой фазы к поверхности твердого тела. Внешняя диффузия Внутренняя диффузия 2. Адсорбция реагента на поверхности твердого тела. Физадсорбция Хемосорбция 3. Химическая реакция на поверхности. Реакция реагента с атомами (молекулами) поверхности твердого тела. Реакция между двумя адсорбированными на поверхности атомами (молекулами). Реакция между адсорбированным на поверхности атомом (молекулой) из жидкой или газовой фазой. катализ 4. Десорбция продуктов реакции. 5. Транспорт реагентов от поверхности твердого тела. Внешняя диффузия Внутренняя диффузия
Стадии гетерогенных реакций Лекция-10 1. Транспорт молекул или атомов реагента из объема газовой или жидкой фазы к поверхности твердого тела. Внешняя диффузия Внутренняя диффузия 2. Адсорбция реагента на поверхности твердого тела. Физадсорбция Хемосорбция 3. Химическая реакция на поверхности. Реакция реагента с атомами (молекулами) поверхности твердого тела. Реакция между двумя адсорбированными на поверхности атомами (молекулами). Реакция между адсорбированным на поверхности атомом (молекулой) из жидкой или газовой фазой. катализ 4. Десорбция продуктов реакции. 5. Транспорт реагентов от поверхности твердого тела. Внешняя диффузия Внутренняя диффузия
 Основы кинетики Лекция-10 Закон действующих масс – применим для элементарных реакций. ν 1 А + ν 2 В + … = ν 3 С + ν 4 D + … или ν 1 А + ν 2 В + … = продукты Скорость реакции: ν ν r = kp 1 p 2 Кинетический порядок реакции – показатель в уравнении для скорости (по выбранному компоненту). Молекулярность – число частиц, реально участвующих в элементарной реакции: мономолекулярные, бимолекулярные, тримолекулярные.
Основы кинетики Лекция-10 Закон действующих масс – применим для элементарных реакций. ν 1 А + ν 2 В + … = ν 3 С + ν 4 D + … или ν 1 А + ν 2 В + … = продукты Скорость реакции: ν ν r = kp 1 p 2 Кинетический порядок реакции – показатель в уравнении для скорости (по выбранному компоненту). Молекулярность – число частиц, реально участвующих в элементарной реакции: мономолекулярные, бимолекулярные, тримолекулярные.
 Кинетика сложных реакций Скорость элементарной стадии (r) равна разнице скоростей прямой (ri) и обратной (r-i) реакции: r = ri - r-i Если ri r-i, стадия обратима: Реагент Продукт Если ri > r-I стадия кинетически необратима: Реагент Продукт Многостадийный процесс: A B C D E Лимитирующая стадия Скорость процесса = скорость стадии С D. Лекция-10
Кинетика сложных реакций Скорость элементарной стадии (r) равна разнице скоростей прямой (ri) и обратной (r-i) реакции: r = ri - r-i Если ri r-i, стадия обратима: Реагент Продукт Если ri > r-I стадия кинетически необратима: Реагент Продукт Многостадийный процесс: A B C D E Лимитирующая стадия Скорость процесса = скорость стадии С D. Лекция-10
![Лекция-10 Кинетика сложных реакций Мономолекулярная реакция на поверхности: А + [s] быстро [Аадс] k Лекция-10 Кинетика сложных реакций Мономолекулярная реакция на поверхности: А + [s] быстро [Аадс] k](https://present5.com/presentation/3/-42749098_138471399.pdf-img/-42749098_138471399.pdf-5.jpg) Лекция-10 Кинетика сложных реакций Мономолекулярная реакция на поверхности: А + [s] быстро [Аадс] k [Радс] медленно быстро Р + [s] Бимолекулярная реакция в адсорбционном слое: А + [s] быстро [Аадс] В + [s] быстро [Вадс] [Аадс] + [Вадс] медленно [Радс] быстро Р + [s] Скорость процесса лимитируется химической реакцией на поверхности.
Лекция-10 Кинетика сложных реакций Мономолекулярная реакция на поверхности: А + [s] быстро [Аадс] k [Радс] медленно быстро Р + [s] Бимолекулярная реакция в адсорбционном слое: А + [s] быстро [Аадс] В + [s] быстро [Вадс] [Аадс] + [Вадс] медленно [Радс] быстро Р + [s] Скорость процесса лимитируется химической реакцией на поверхности.
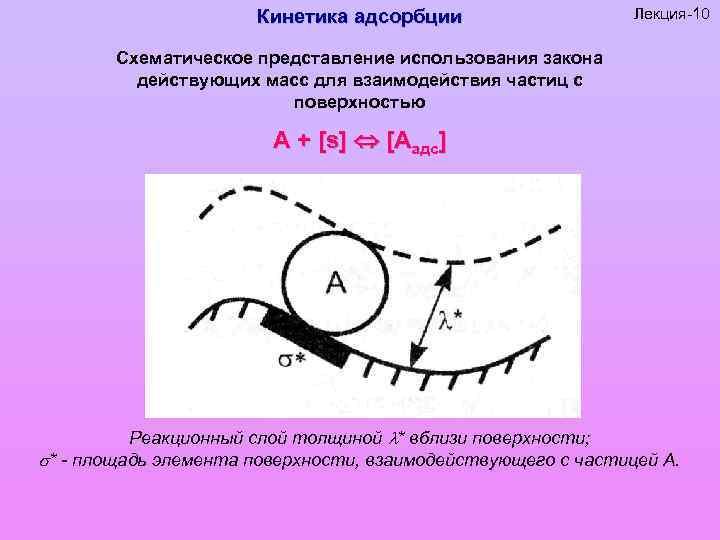 Кинетика адсорбции Лекция-10 Схематическое представление использования закона действующих масс для взаимодействия частиц с поверхностью А + [s] [Аадс] Реакционный слой толщиной * вблизи поверхности; * - площадь элемента поверхности, взаимодействующего с частицей А.
Кинетика адсорбции Лекция-10 Схематическое представление использования закона действующих масс для взаимодействия частиц с поверхностью А + [s] [Аадс] Реакционный слой толщиной * вблизи поверхности; * - площадь элемента поверхности, взаимодействующего с частицей А.
![Кинетика адсорбции Лекция-10 Закон действующих масс для взаимодействия частицы с поверхностью: А + [s] Кинетика адсорбции Лекция-10 Закон действующих масс для взаимодействия частицы с поверхностью: А + [s]](https://present5.com/presentation/3/-42749098_138471399.pdf-img/-42749098_138471399.pdf-7.jpg) Кинетика адсорбции Лекция-10 Закон действующих масс для взаимодействия частицы с поверхностью: А + [s] [Аадс] А [Аадс] Скорость реакции: d. СА/dt = - ks(S/V)CA, Где S – площадь поверхности, не занятой реагентами, V – объем системы, ks = k 1 [t-1 l] = [см/с], где k 1 – константа скорости мономолекулярной реакции между А и s в реакционном слое толщиной * вблизи поверхности. Скорость адсорбции: Wадс = -(d. СА/dt )= ks(S/V)CA = kадс(S/V)CA, Число частиц А в газовой или жидкой фазе NA = CAV: -(d. NА/dt )адс= kадс. SCA
Кинетика адсорбции Лекция-10 Закон действующих масс для взаимодействия частицы с поверхностью: А + [s] [Аадс] А [Аадс] Скорость реакции: d. СА/dt = - ks(S/V)CA, Где S – площадь поверхности, не занятой реагентами, V – объем системы, ks = k 1 [t-1 l] = [см/с], где k 1 – константа скорости мономолекулярной реакции между А и s в реакционном слое толщиной * вблизи поверхности. Скорость адсорбции: Wадс = -(d. СА/dt )= ks(S/V)CA = kадс(S/V)CA, Число частиц А в газовой или жидкой фазе NA = CAV: -(d. NА/dt )адс= kадс. SCA
 Кинетика адсорбции Введем обозначения: *А – площадь поверхности, занимаемая одной адсорбированной частицей; Sадс. – площадь поверхности, занятая адсорбированными частицами; S 0 – полная площадь поверхности; N 0 – полное число центров адсорбции; NA – число адсорбированных частиц; N – число свободных центров адсорбции; А – доля активной поверхности, занятой частицами А. Лекция-10
Кинетика адсорбции Введем обозначения: *А – площадь поверхности, занимаемая одной адсорбированной частицей; Sадс. – площадь поверхности, занятая адсорбированными частицами; S 0 – полная площадь поверхности; N 0 – полное число центров адсорбции; NA – число адсорбированных частиц; N – число свободных центров адсорбции; А – доля активной поверхности, занятой частицами А. Лекция-10
 Кинетика адсорбции Лекция-10
Кинетика адсорбции Лекция-10
 Кинетика адсорбции Константа скорости мономолекулярной реакции между частицей А и центром адсорбции с площадью *А. V* = * *А – элементарный реакционный объем для процесса адсорбции. Изменение покрытия только за счет процесса адсорбции. Константа скорости бимолекулярного процесса взаимодействия частиц А с поверхностью, приводящего к адсорбции. Лекция-10
Кинетика адсорбции Константа скорости мономолекулярной реакции между частицей А и центром адсорбции с площадью *А. V* = * *А – элементарный реакционный объем для процесса адсорбции. Изменение покрытия только за счет процесса адсорбции. Константа скорости бимолекулярного процесса взаимодействия частиц А с поверхностью, приводящего к адсорбции. Лекция-10
![Лекция-10 Кинетика десорбции Мономолекулярная реакция: [Аадс] А + [s] V V /N 0 Изменение Лекция-10 Кинетика десорбции Мономолекулярная реакция: [Аадс] А + [s] V V /N 0 Изменение](https://present5.com/presentation/3/-42749098_138471399.pdf-img/-42749098_138471399.pdf-11.jpg) Лекция-10 Кинетика десорбции Мономолекулярная реакция: [Аадс] А + [s] V V /N 0 Изменение покрытия только за счет процесса десорбции. /N 0
Лекция-10 Кинетика десорбции Мономолекулярная реакция: [Аадс] А + [s] V V /N 0 Изменение покрытия только за счет процесса десорбции. /N 0
 Химическая реакция на поверхности Лекция-10 Закон действующих поверхностей (И. Ленгмюр, 1918 г) – описание кинетики процессов на поверхности твердых тел, а именно, применительно к реакциям частиц (молекул или атомов) на поверхности твердого тела: üповерхность состоит из определенного числа адсорбционных центров; ü каждый из которых удерживает в адсорбированном состоянии одну частицу; üчастицы на соседних центрах не взаимодействуют, если не вступают в реакцию друг с другом; üреакция протекает в мономолекулярном слое ( А+ В+ Z+…=1) Реакция с участием адсорбированных молекул А, В и т. д. и свободных центров: ν 1 А + ν 2 В + ν 3 Z + … = продукты Скорость реакции на адсорбционных центрах: ν 1 ν 2 ν 3 rk = k S z θ A θ B θ Z… Где Z – общее число адсорбционных центров на единице поверхности; А и В – доля центров, заполненных адсорбированными веществами А и В; Z – доля свободных центров.
Химическая реакция на поверхности Лекция-10 Закон действующих поверхностей (И. Ленгмюр, 1918 г) – описание кинетики процессов на поверхности твердых тел, а именно, применительно к реакциям частиц (молекул или атомов) на поверхности твердого тела: üповерхность состоит из определенного числа адсорбционных центров; ü каждый из которых удерживает в адсорбированном состоянии одну частицу; üчастицы на соседних центрах не взаимодействуют, если не вступают в реакцию друг с другом; üреакция протекает в мономолекулярном слое ( А+ В+ Z+…=1) Реакция с участием адсорбированных молекул А, В и т. д. и свободных центров: ν 1 А + ν 2 В + ν 3 Z + … = продукты Скорость реакции на адсорбционных центрах: ν 1 ν 2 ν 3 rk = k S z θ A θ B θ Z… Где Z – общее число адсорбционных центров на единице поверхности; А и В – доля центров, заполненных адсорбированными веществами А и В; Z – доля свободных центров.
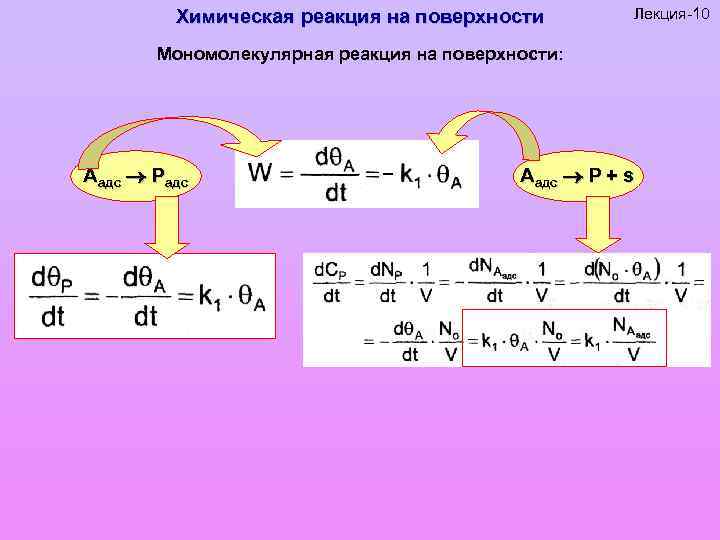 Химическая реакция на поверхности Лекция-10 Мономолекулярная реакция на поверхности: Аадс Радс _ Аадс Р + s
Химическая реакция на поверхности Лекция-10 Мономолекулярная реакция на поверхности: Аадс Радс _ Аадс Р + s
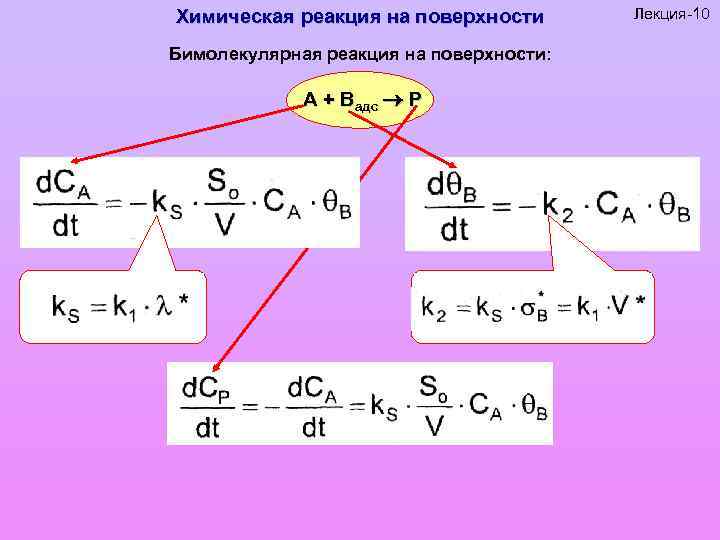 Химическая реакция на поверхности Бимолекулярная реакция на поверхности: А + Вадс Р Лекция-10
Химическая реакция на поверхности Бимолекулярная реакция на поверхности: А + Вадс Р Лекция-10
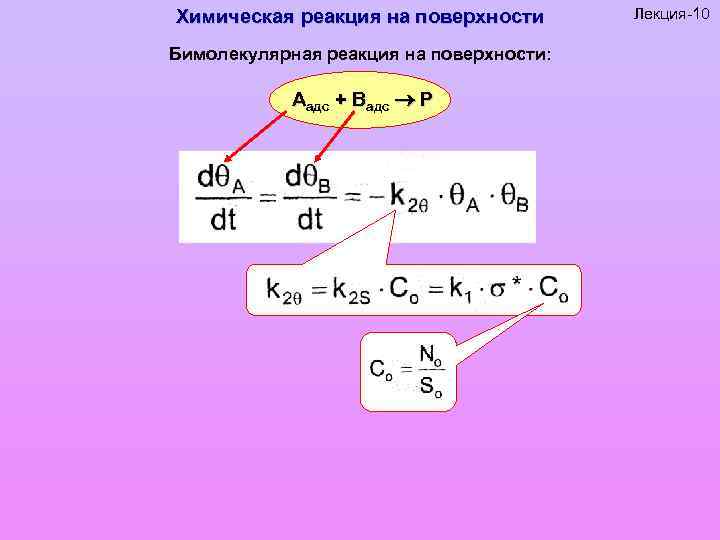 Химическая реакция на поверхности Бимолекулярная реакция на поверхности: Аадс + Вадс Р Лекция-10
Химическая реакция на поверхности Бимолекулярная реакция на поверхности: Аадс + Вадс Р Лекция-10
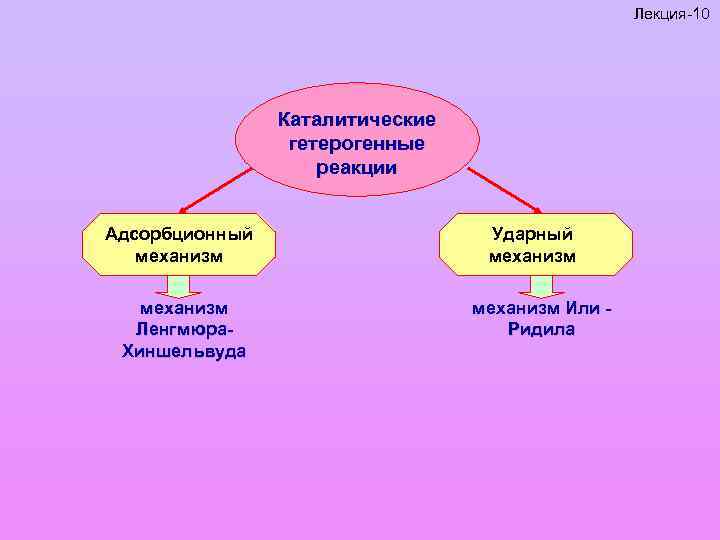 Лекция-10 Каталитические гетерогенные реакции Адсорбционный механизм Ленгмюра. Хиншельвуда Ударный механизм Или Ридила
Лекция-10 Каталитические гетерогенные реакции Адсорбционный механизм Ленгмюра. Хиншельвуда Ударный механизм Или Ридила
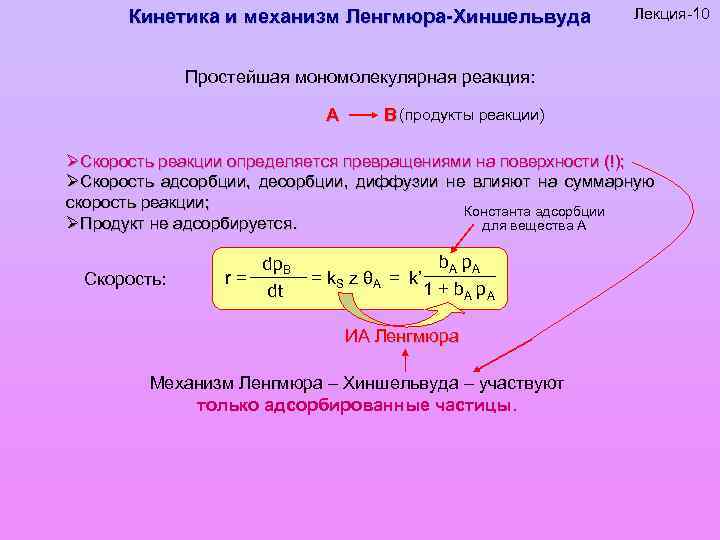 Кинетика и механизм Ленгмюра-Хиншельвуда Лекция-10 Простейшая мономолекулярная реакция: A B (продукты реакции) ØСкорость реакции определяется превращениями на поверхности (!); ØСкорость адсорбции, десорбции, диффузии не влияют на суммарную скорость реакции; Константа адсорбции ØПродукт не адсорбируется. для вещества А Скорость: r= dp. B dt = k. S z θA = k’ b. A p A 1 + b A p. A ИА Ленгмюра Механизм Ленгмюра – Хиншельвуда – участвуют только адсорбированные частицы.
Кинетика и механизм Ленгмюра-Хиншельвуда Лекция-10 Простейшая мономолекулярная реакция: A B (продукты реакции) ØСкорость реакции определяется превращениями на поверхности (!); ØСкорость адсорбции, десорбции, диффузии не влияют на суммарную скорость реакции; Константа адсорбции ØПродукт не адсорбируется. для вещества А Скорость: r= dp. B dt = k. S z θA = k’ b. A p A 1 + b A p. A ИА Ленгмюра Механизм Ленгмюра – Хиншельвуда – участвуют только адсорбированные частицы.
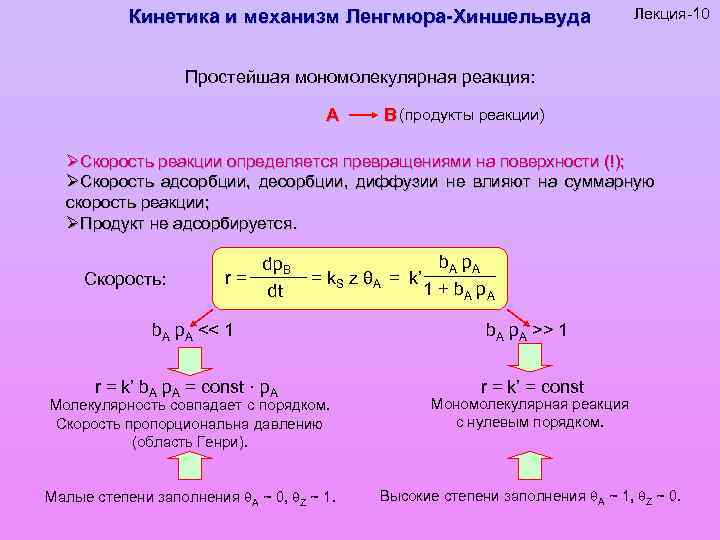 Кинетика и механизм Ленгмюра-Хиншельвуда Лекция-10 Простейшая мономолекулярная реакция: A B (продукты реакции) ØСкорость реакции определяется превращениями на поверхности (!); ØСкорость адсорбции, десорбции, диффузии не влияют на суммарную скорость реакции; ØПродукт не адсорбируется. Скорость: r= dp. B dt = k. S z θA = k’ b. A p. A << 1 r = k’ b. A p. A = const · p. A b. A p A 1 + b A p. A b. A p. A >> 1 r = k’ = const Молекулярность совпадает с порядком. Скорость пропорциональна давлению (область Генри). Мономолекулярная реакция с нулевым порядком. Малые степени заполнения А ~ 0, Z ~ 1. Высокие степени заполнения А ~ 1, Z ~ 0.
Кинетика и механизм Ленгмюра-Хиншельвуда Лекция-10 Простейшая мономолекулярная реакция: A B (продукты реакции) ØСкорость реакции определяется превращениями на поверхности (!); ØСкорость адсорбции, десорбции, диффузии не влияют на суммарную скорость реакции; ØПродукт не адсорбируется. Скорость: r= dp. B dt = k. S z θA = k’ b. A p. A << 1 r = k’ b. A p. A = const · p. A b. A p A 1 + b A p. A b. A p. A >> 1 r = k’ = const Молекулярность совпадает с порядком. Скорость пропорциональна давлению (область Генри). Мономолекулярная реакция с нулевым порядком. Малые степени заполнения А ~ 0, Z ~ 1. Высокие степени заполнения А ~ 1, Z ~ 0.
 Кинетика и механизм Ленгмюра-Хиншельвуда Лекция-10 Бимолекулярная реакция: A+B C ØСкорость реакции определяется превращениями на поверхности (!); ØА и В адсорбируются на разных центрах (!) ØСкорость адсорбции, десорбции, диффузии не влияют на суммарную скорость реакции; ØПродукт не адсорбируется. Скорость: r= dp. C dt = k. S z θA θB = k’’ Малые степени заполнения А ~ 0, В ~ 0, Z ~ 1. r = k. S z θA θB = k’’ b. A p. A b. B p. B Бимолекулярная реакция с первым порядком по каждому веществу, а суммарно со вторым порядком. b. B p B b. A p A · 1 + b A p. A 1 + b B p. B b. A p. A >> 1 и b. В p. В >> 1 r = k’’ = const Бимолекулярная реакция с нулевым порядком.
Кинетика и механизм Ленгмюра-Хиншельвуда Лекция-10 Бимолекулярная реакция: A+B C ØСкорость реакции определяется превращениями на поверхности (!); ØА и В адсорбируются на разных центрах (!) ØСкорость адсорбции, десорбции, диффузии не влияют на суммарную скорость реакции; ØПродукт не адсорбируется. Скорость: r= dp. C dt = k. S z θA θB = k’’ Малые степени заполнения А ~ 0, В ~ 0, Z ~ 1. r = k. S z θA θB = k’’ b. A p. A b. B p. B Бимолекулярная реакция с первым порядком по каждому веществу, а суммарно со вторым порядком. b. B p B b. A p A · 1 + b A p. A 1 + b B p. B b. A p. A >> 1 и b. В p. В >> 1 r = k’’ = const Бимолекулярная реакция с нулевым порядком.
 Кинетика и механизм Ленгмюра-Хиншельвуда Лекция-10 Бимолекулярная реакция: A+B C ØСкорость реакции определяется превращениями на поверхности (!); ØСкорость адсорбции, десорбции, диффузии не влияют на суммарную скорость реакции; ØПродукт адсорбируется. r = k’’ θA θB = k’’ b. Ap. A 1 + b. Ap. A + b. Bp. B + b. Cp. C · b. Bp. B 1 + b. Ap. A + b. Bp. B + b. Cp. C Сильная адсорбция С b. Cp. C >> (1 + b. Ap. A + b. Bp. B) r = k’’ b. Ap. Ab. Bp. B (b. Cp. C)2 Бимолекулярная реакция с отрицательным порядком по продукту.
Кинетика и механизм Ленгмюра-Хиншельвуда Лекция-10 Бимолекулярная реакция: A+B C ØСкорость реакции определяется превращениями на поверхности (!); ØСкорость адсорбции, десорбции, диффузии не влияют на суммарную скорость реакции; ØПродукт адсорбируется. r = k’’ θA θB = k’’ b. Ap. A 1 + b. Ap. A + b. Bp. B + b. Cp. C · b. Bp. B 1 + b. Ap. A + b. Bp. B + b. Cp. C Сильная адсорбция С b. Cp. C >> (1 + b. Ap. A + b. Bp. B) r = k’’ b. Ap. Ab. Bp. B (b. Cp. C)2 Бимолекулярная реакция с отрицательным порядком по продукту.
 Кинетика и механизм Ленгмюра-Хиншельвуда При наличии диссоциативной адсорбции: O 2 + 2 Z ↔ 2 OZ О 2 + СО 2 O O+C Pt Pt CO 2 + Pt Pt СО и O адсорбируются на одних и тех же центрах Pt r=k b. Op 1/2 b. COp. CO O 1 + b. COp. CO + b. Op 1/2 O 2 2 · 1 + b. COp. CO+ b. Op 1/2 O 2 b. COp. CO >> 1+ b. Op 1/2 O 2 r = const · p 1/2 /p. CO O 2 Дробный порядок по кислороду. Лекция-10
Кинетика и механизм Ленгмюра-Хиншельвуда При наличии диссоциативной адсорбции: O 2 + 2 Z ↔ 2 OZ О 2 + СО 2 O O+C Pt Pt CO 2 + Pt Pt СО и O адсорбируются на одних и тех же центрах Pt r=k b. Op 1/2 b. COp. CO O 1 + b. COp. CO + b. Op 1/2 O 2 2 · 1 + b. COp. CO+ b. Op 1/2 O 2 b. COp. CO >> 1+ b. Op 1/2 O 2 r = const · p 1/2 /p. CO O 2 Дробный порядок по кислороду. Лекция-10
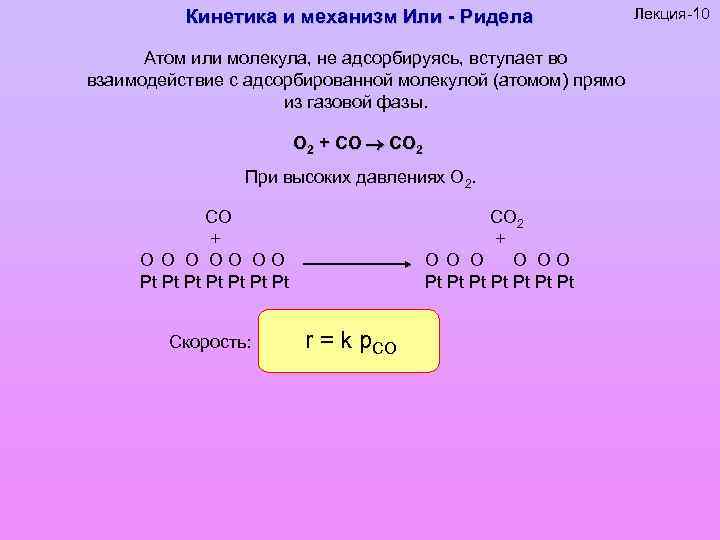 Кинетика и механизм Или - Ридела Атом или молекула, не адсорбируясь, вступает во взаимодействие с адсорбированной молекулой (атомом) прямо из газовой фазы. О 2 + СО 2 При высоких давлениях О 2. СО + О ОО ОО Pt Pt Скорость: СО 2 + ОО О О ОО Pt Pt r = k p. CO Лекция-10
Кинетика и механизм Или - Ридела Атом или молекула, не адсорбируясь, вступает во взаимодействие с адсорбированной молекулой (атомом) прямо из газовой фазы. О 2 + СО 2 При высоких давлениях О 2. СО + О ОО ОО Pt Pt Скорость: СО 2 + ОО О О ОО Pt Pt r = k p. CO Лекция-10
 Кинетика сложных реакций по М. И. Темкину Окисление SO 2 на Pt – катализаторе: 2 Z + O 2 2 ZO SO 2 + ZO SO 3 + Z 1 2 2 SO 2 + O 2 = 2 SO 3 Стехиометрические числа выбираются целыми 1/2 1 SO 2 + 1/2 O 2 = SO 3 Маршрут реакции – набор стехиометрических чисел стадий, приводящий к суммарному уравнению брутто-процесса (Ю. Хориути) Лекция-10
Кинетика сложных реакций по М. И. Темкину Окисление SO 2 на Pt – катализаторе: 2 Z + O 2 2 ZO SO 2 + ZO SO 3 + Z 1 2 2 SO 2 + O 2 = 2 SO 3 Стехиометрические числа выбираются целыми 1/2 1 SO 2 + 1/2 O 2 = SO 3 Маршрут реакции – набор стехиометрических чисел стадий, приводящий к суммарному уравнению брутто-процесса (Ю. Хориути) Лекция-10
 Маршруты У Ударный механизм И л и -Р и д и л а Адсорбционный механизм Ленгмюра Баланс по числу активных поверхностных центров: Лекция-10 Кинетика сложных реакций по М. И. Темкину
Маршруты У Ударный механизм И л и -Р и д и л а Адсорбционный механизм Ленгмюра Баланс по числу активных поверхностных центров: Лекция-10 Кинетика сложных реакций по М. И. Темкину
 Кинетика сложных реакций по М. И. Темкину Лекция-10 В стационарном режиме (например, проточном реакторе) – концентрация всех реагентов и промежуточных веществ постоянна во времени и в любом объеме реакционного пространства. Скорость реакции по i-ой стадии: ir = ri - r-i Скорость реакции по j-ой стадии: jr = rj - r-j Скорость одномаршрутной реакции = скорость любой из стадий, деленная на стехиометрическое число: r = (ri - r-i )/ i = (rj - r-j)/ j = (rk - r-k)/ k = … Скорость стадии протекании реакции по нескольким независимым маршрутам получается суммированием по р-основным маршрутам (r(p) – скорость реакции по р-ому маршруту):
Кинетика сложных реакций по М. И. Темкину Лекция-10 В стационарном режиме (например, проточном реакторе) – концентрация всех реагентов и промежуточных веществ постоянна во времени и в любом объеме реакционного пространства. Скорость реакции по i-ой стадии: ir = ri - r-i Скорость реакции по j-ой стадии: jr = rj - r-j Скорость одномаршрутной реакции = скорость любой из стадий, деленная на стехиометрическое число: r = (ri - r-i )/ i = (rj - r-j)/ j = (rk - r-k)/ k = … Скорость стадии протекании реакции по нескольким независимым маршрутам получается суммированием по р-основным маршрутам (r(p) – скорость реакции по р-ому маршруту):
 Кинетика сложных реакций по М. И. Темкину Скорости элементарных стадий: Баланс по активным центрам на поверхности: В стационарной реакции: Выражение для скорости: Лекция-10
Кинетика сложных реакций по М. И. Темкину Скорости элементарных стадий: Баланс по активным центрам на поверхности: В стационарной реакции: Выражение для скорости: Лекция-10
 Кинетика сложных реакций по М. И. Темкину Лекция-10 Каталитическая конверсия СО водяным паром (Т=4000 С, Кт- Fe 3 O 4). Активные центры – вакансии кислорода. При этом ZO >> Z: Константа равновесия реакции конверсии СО: Где k = k 1 k 2/k-2 и a = k 1/k-2:
Кинетика сложных реакций по М. И. Темкину Лекция-10 Каталитическая конверсия СО водяным паром (Т=4000 С, Кт- Fe 3 O 4). Активные центры – вакансии кислорода. При этом ZO >> Z: Константа равновесия реакции конверсии СО: Где k = k 1 k 2/k-2 и a = k 1/k-2:
 Лекция-10 Кинетика топохимических реакций
Лекция-10 Кинетика топохимических реакций
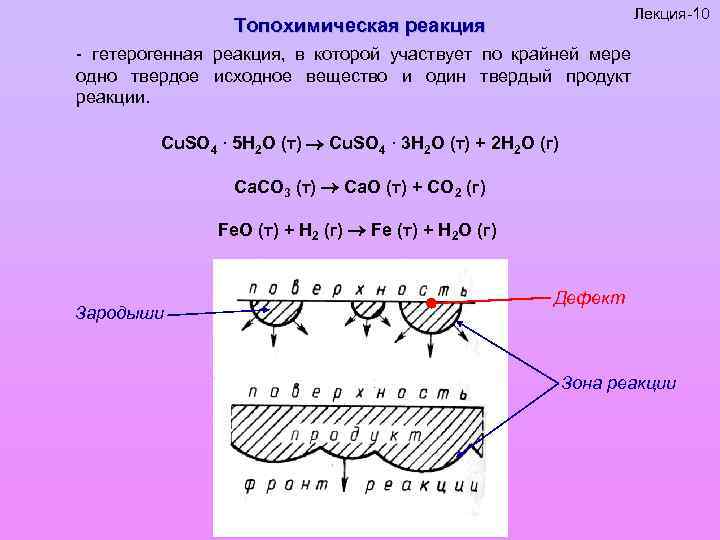 Лекция-10 Топохимическая реакция - гетерогенная реакция, в которой участвует по крайней мере одно твердое исходное вещество и один твердый продукт реакции. Cu. SO 4 ∙ 5 H 2 O (т) Cu. SO 4 ∙ 3 H 2 O (т) + 2 H 2 O (г) Ca. CO 3 (т) Ca. O (т) + CO 2 (г) Fe. O (т) + H 2 (г) Fe (т) + Н 2 О (г) Зародыши Дефект Зона реакции
Лекция-10 Топохимическая реакция - гетерогенная реакция, в которой участвует по крайней мере одно твердое исходное вещество и один твердый продукт реакции. Cu. SO 4 ∙ 5 H 2 O (т) Cu. SO 4 ∙ 3 H 2 O (т) + 2 H 2 O (г) Ca. CO 3 (т) Ca. O (т) + CO 2 (г) Fe. O (т) + H 2 (г) Fe (т) + Н 2 О (г) Зародыши Дефект Зона реакции
 Кинетика топохимической реакции Лекция-10 Скорость топохимической реакции: w = - dm/dt, Изменение массы одного из исходных веществ (взятого в недостатке). Степень превращения исходного вещества: = (m 0 – m)/m 0 = 1 – m/m 0, Где m 0 – начальная масса исходного вещества. m = m 0(1 - ) dm = m 0 d w = m 0 d /dt w = d /dt = -(1/m 0)dm/dt = (1/m 0)w
Кинетика топохимической реакции Лекция-10 Скорость топохимической реакции: w = - dm/dt, Изменение массы одного из исходных веществ (взятого в недостатке). Степень превращения исходного вещества: = (m 0 – m)/m 0 = 1 – m/m 0, Где m 0 – начальная масса исходного вещества. m = m 0(1 - ) dm = m 0 d w = m 0 d /dt w = d /dt = -(1/m 0)dm/dt = (1/m 0)w
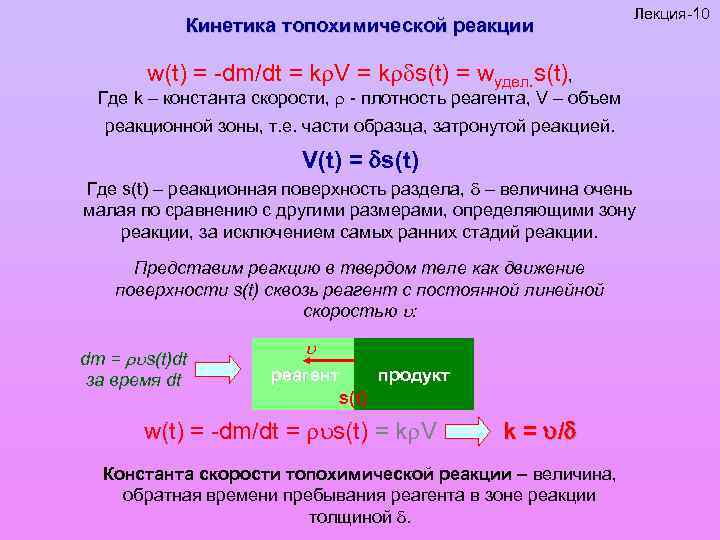 Кинетика топохимической реакции Лекция-10 w(t) = -dm/dt = k V = k s(t) = wудел. s(t), Где k – константа скорости, - плотность реагента, V – объем реакционной зоны, т. е. части образца, затронутой реакцией. V(t) = s(t) Где s(t) – реакционная поверхность раздела, – величина очень малая по сравнению с другими размерами, определяющими зону реакции, за исключением самых ранних стадий реакции. Представим реакцию в твердом теле как движение поверхности s(t) сквозь реагент с постоянной линейной скоростью : dm = s(t)dt за время dt реагент продукт s(t) w(t) = -dm/dt = s(t) = k V k = / Константа скорости топохимической реакции – величина, обратная времени пребывания реагента в зоне реакции толщиной .
Кинетика топохимической реакции Лекция-10 w(t) = -dm/dt = k V = k s(t) = wудел. s(t), Где k – константа скорости, - плотность реагента, V – объем реакционной зоны, т. е. части образца, затронутой реакцией. V(t) = s(t) Где s(t) – реакционная поверхность раздела, – величина очень малая по сравнению с другими размерами, определяющими зону реакции, за исключением самых ранних стадий реакции. Представим реакцию в твердом теле как движение поверхности s(t) сквозь реагент с постоянной линейной скоростью : dm = s(t)dt за время dt реагент продукт s(t) w(t) = -dm/dt = s(t) = k V k = / Константа скорости топохимической реакции – величина, обратная времени пребывания реагента в зоне реакции толщиной .
 Лекция-10 Морфологические модели реакции для определения s(t) Модели, включающие представления об образовании и росте зародышей фазы твердого продукта, сохраняющих свою форму (т. е. соотношение размеров) на протяжении всей реакции. Полусферические зародыши с плотностью N 0 м-2: все зародыши образуются в начальный момент и не перекрываются Радиус r = t, Полубесконечный образец Поверхность (t)=2 r 2 = 2 2 t 2 s(t) = N 0 (t)
Лекция-10 Морфологические модели реакции для определения s(t) Модели, включающие представления об образовании и росте зародышей фазы твердого продукта, сохраняющих свою форму (т. е. соотношение размеров) на протяжении всей реакции. Полусферические зародыши с плотностью N 0 м-2: все зародыши образуются в начальный момент и не перекрываются Радиус r = t, Полубесконечный образец Поверхность (t)=2 r 2 = 2 2 t 2 s(t) = N 0 (t)
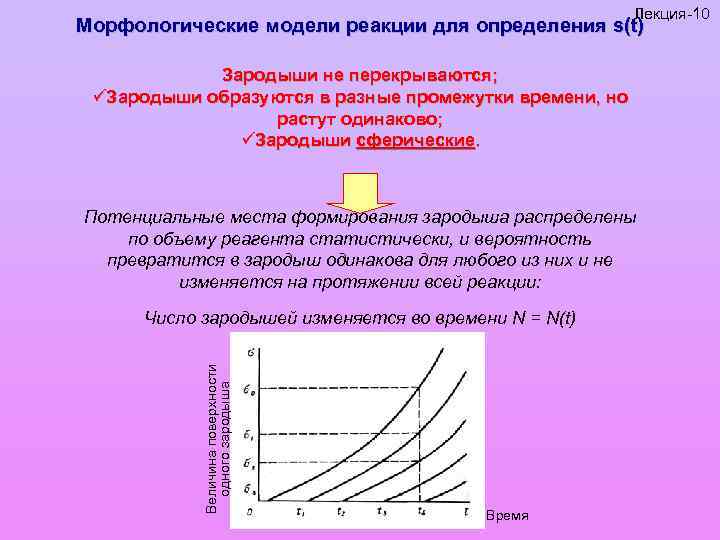 Лекция-10 Морфологические модели реакции для определения s(t) Зародыши не перекрываются; üЗародыши образуются в разные промежутки времени, но растут одинаково; üЗародыши сферические. Потенциальные места формирования зародыша распределены по объему реагента статистически, и вероятность превратится в зародыш одинакова для любого из них и не изменяется на протяжении всей реакции: Величина поверхности одного зародыша Число зародышей изменяется во времени N = N(t) Время
Лекция-10 Морфологические модели реакции для определения s(t) Зародыши не перекрываются; üЗародыши образуются в разные промежутки времени, но растут одинаково; üЗародыши сферические. Потенциальные места формирования зародыша распределены по объему реагента статистически, и вероятность превратится в зародыш одинакова для любого из них и не изменяется на протяжении всей реакции: Величина поверхности одного зародыша Число зародышей изменяется во времени N = N(t) Время
 Лекция-10 Морфологические модели реакции для определения s(t) Суммарная поверхность всех зародышей: = (t-ti) Если в выбранный интервал времени образуется много зародышей, и в интервале ti в окрестности ti образуется в среднем d. N/dt |t=ti ti зародышей: Время появления данного зародыша
Лекция-10 Морфологические модели реакции для определения s(t) Суммарная поверхность всех зародышей: = (t-ti) Если в выбранный интервал времени образуется много зародышей, и в интервале ti в окрестности ti образуется в среднем d. N/dt |t=ti ti зародышей: Время появления данного зародыша
 Формальная топокинетика Лекция-10 Необходим явный вид зависимостей В рамках предположения о постоянстве линейной скорости продвижения границы раздела и о сферической форме зародыша: r = (t- ) (t) = 4 r 2 = 4 2(t- )2 N(t) 1) эксперимент; 2) теоретические предпосылки. Экспоненциальный закон зародышеобразования Степенной закон зародышеобразования
Формальная топокинетика Лекция-10 Необходим явный вид зависимостей В рамках предположения о постоянстве линейной скорости продвижения границы раздела и о сферической форме зародыша: r = (t- ) (t) = 4 r 2 = 4 2(t- )2 N(t) 1) эксперимент; 2) теоретические предпосылки. Экспоненциальный закон зародышеобразования Степенной закон зародышеобразования
 Формальная топокинетика Кинетическое уравнение на основе Экспоненциального закона зародышеобразования (опущены математические выкладки) Лекция-10
Формальная топокинетика Кинетическое уравнение на основе Экспоненциального закона зародышеобразования (опущены математические выкладки) Лекция-10
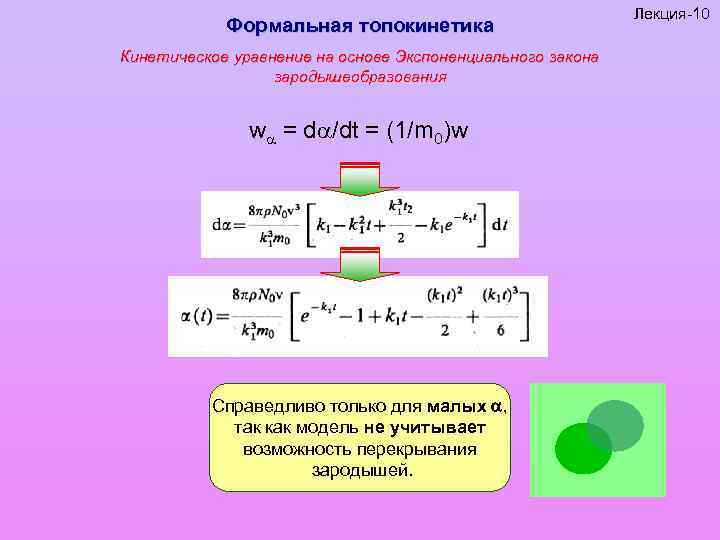 Формальная топокинетика Кинетическое уравнение на основе Экспоненциального закона зародышеобразования w = d /dt = (1/m 0)w Справедливо только для малых , так как модель не учитывает возможность перекрывания зародышей. Лекция-10
Формальная топокинетика Кинетическое уравнение на основе Экспоненциального закона зародышеобразования w = d /dt = (1/m 0)w Справедливо только для малых , так как модель не учитывает возможность перекрывания зародышей. Лекция-10
 Формальная топокинетика Кинетическое уравнение на основе Экспоненциального закона зародышеобразования Без учета перекрывания зародышей Реальная < расчетная (фиктивная - f) Учет перекрывания зародышей Отношение приращений за один и тот же промежуток времени пропорционально количеству непрореагировавшего вещества: d /d f = 1 - f = -ln(1 - ) Для более высоких степеней превращения: Лекция-10
Формальная топокинетика Кинетическое уравнение на основе Экспоненциального закона зародышеобразования Без учета перекрывания зародышей Реальная < расчетная (фиктивная - f) Учет перекрывания зародышей Отношение приращений за один и тот же промежуток времени пропорционально количеству непрореагировавшего вещества: d /d f = 1 - f = -ln(1 - ) Для более высоких степеней превращения: Лекция-10
 Формальная топокинетика Лекция-10 Кинетическое уравнение на основе Степенного закона зародышеобразования (опущены математические выкладки) Справедливо только для малых .
Формальная топокинетика Лекция-10 Кинетическое уравнение на основе Степенного закона зародышеобразования (опущены математические выкладки) Справедливо только для малых .
 Формальная топокинетика Кинетическое уравнение на основе Степенного закона зародышеобразования Для больших r Лекция-10
Формальная топокинетика Кинетическое уравнение на основе Степенного закона зародышеобразования Для больших r Лекция-10
 Формальная топокинетика. Частные случаи Лекция-10 Зародыши возникают сразу по всей поверхности и в большом количестве. Поверхность быстро покрывается слоем продукта, и реакция распространяется вглубь за счет продвижения границы раздела. продукт реагент R r Реакционная поверхность: s(t) = 4 r 2, R – радиус зерна, r(t=0)=R; r(t) = R - t. (1 - )1/3 = 1 - t/R или 1 – (1 - )1/3 = t/R
Формальная топокинетика. Частные случаи Лекция-10 Зародыши возникают сразу по всей поверхности и в большом количестве. Поверхность быстро покрывается слоем продукта, и реакция распространяется вглубь за счет продвижения границы раздела. продукт реагент R r Реакционная поверхность: s(t) = 4 r 2, R – радиус зерна, r(t=0)=R; r(t) = R - t. (1 - )1/3 = 1 - t/R или 1 – (1 - )1/3 = t/R
 Формальная топокинетика. Частные случаи Лекция-10 Зародыши образуются: ü из потенциальных центров (первичные зародыши); ü в результате «ответвлений» от уже существующих (вторичные или индуцированные зародыши). Рост зародышей прекращается: при пересечении зародыша с любым другим растущим зародышем. Предположение: Вероятность ветвления и гибели зародышей пропорциональна их числу в данный момент времени. Уравнение Праута – Томпкинса для скорости топохимической реакции: max= 0. 5 ln( /(1 - )) = k 1 t = 1/(1+exp(-k 1 t)) Вероятность Степень превращения при максимальной «ветвления» скорости реакции зародышей
Формальная топокинетика. Частные случаи Лекция-10 Зародыши образуются: ü из потенциальных центров (первичные зародыши); ü в результате «ответвлений» от уже существующих (вторичные или индуцированные зародыши). Рост зародышей прекращается: при пересечении зародыша с любым другим растущим зародышем. Предположение: Вероятность ветвления и гибели зародышей пропорциональна их числу в данный момент времени. Уравнение Праута – Томпкинса для скорости топохимической реакции: max= 0. 5 ln( /(1 - )) = k 1 t = 1/(1+exp(-k 1 t)) Вероятность Степень превращения при максимальной «ветвления» скорости реакции зародышей


