лекция 10 карбонильные соединения.ppt
- Количество слайдов: 24

Лекция 10. Карбонильные соединения.

Номенклатура основных типов карбонильных соединений. Х Карбонильное соединение альдегид H Alk (Ar) кетон OH O-Alk карбоновая кислота сложный эфир карбоновой кислоты OC(O)R ангидрид кислоты амид кислоты NH 2 Cl (Br) хлорангидрид (бромангидрид) кислоты
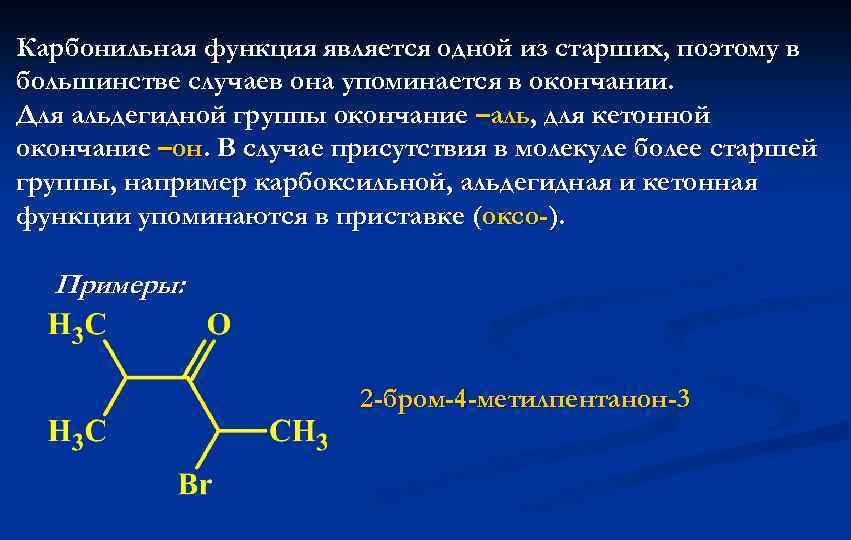
Карбонильная функция является одной из старших, поэтому в большинстве случаев она упоминается в окончании. Для альдегидной группы окончание –аль, для кетонной окончание –он. В случае присутствия в молекуле более старшей группы, например карбоксильной, альдегидная и кетонная функции упоминаются в приставке (оксо-). Примеры: 2 -бром-4 -метилпентанон-3
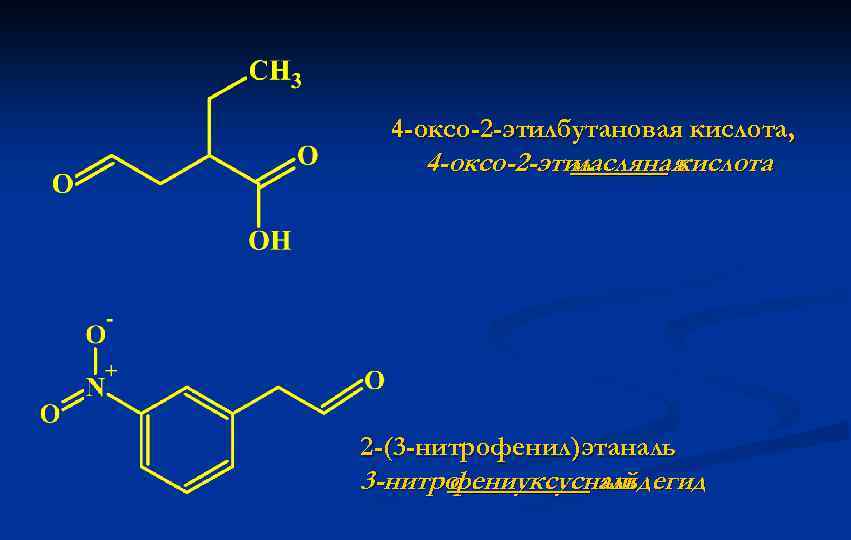
4 -оксо-2 -этилбутановая кислота, 4 -оксо-2 -этил масляная кислота 2 -(3 -нитрофенил)этаналь 3 -нитро фениуксусный альдегид

Методы получения альдегидов и кетонов. §Окисление первичных спиртов до альдегидов и вторичных спиртов до кетонов под действием K 2 Cr 2 O 7, KMn. O 4 и др. (см. лекцию 9). §Озонолиз алкенов и полиенов с последующим восстановительным или нейтральным расщеплением озонидов. Те же продукты получают деструкцией алкенов под действием тетроксида осмия (Os. O 4) с последующей обработкой периодатом натрия (Na. IO 4). (см. лекцию 2, 3) §Получение кетонов гидратацией ацетиленов в присутствии солей ртути – реакция Кучерова (см. лекцию 3) Продукт образуется в соответствии с правилом Марковникова.
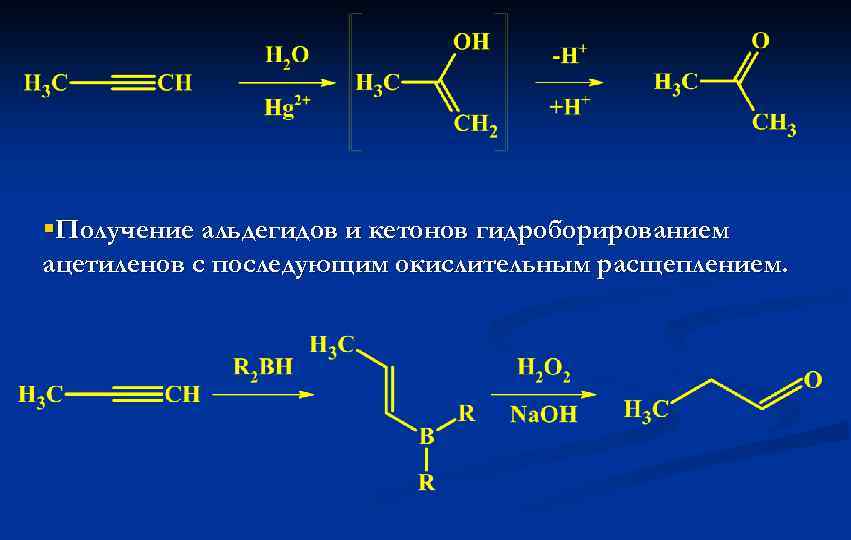
§Получение альдегидов и кетонов гидроборированием ацетиленов с последующим окислительным расщеплением.
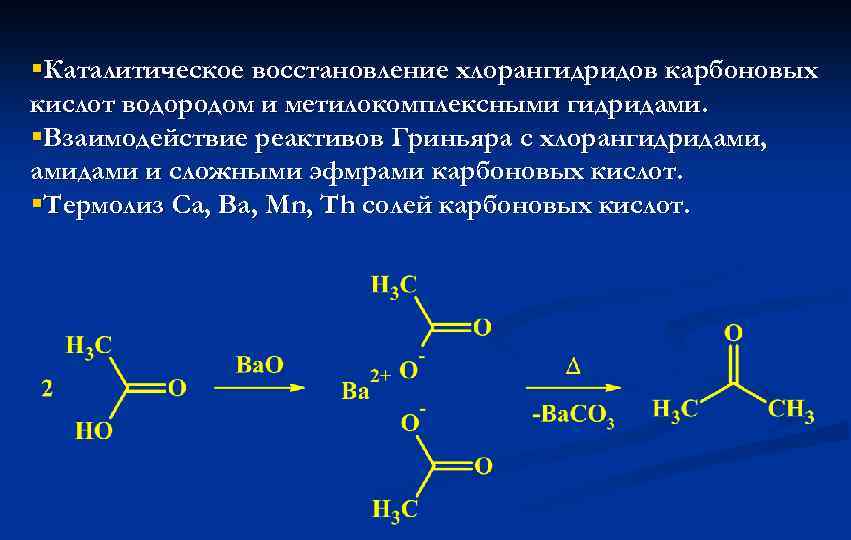
§Каталитическое восстановление хлорангидридов карбоновых кислот водородом и метилокомплексными гидридами. §Взаимодействие реактивов Гриньяра с хлорангидридами, амидами и сложными эфмрами карбоновых кислот. §Термолиз Ca, Ba, Mn, Th солей карбоновых кислот.
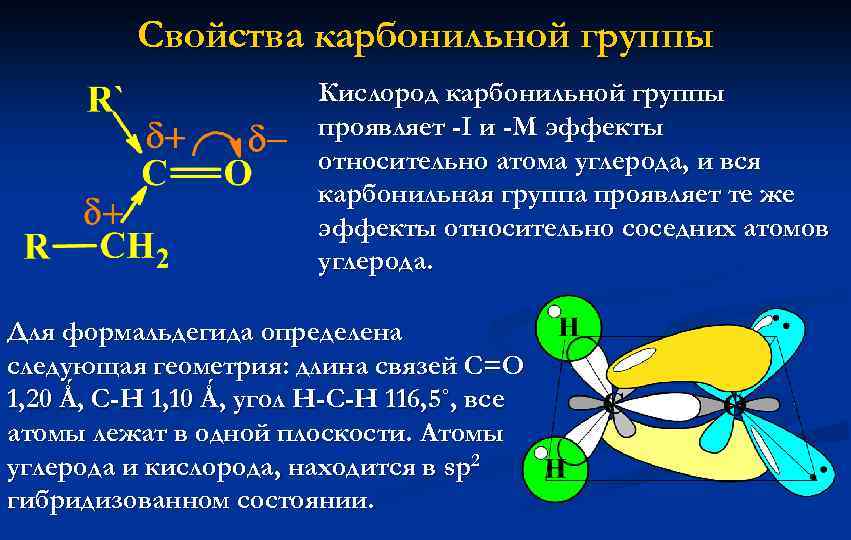
Свойства карбонильной группы Кислород карбонильной группы проявляет -I и -M эффекты относительно атома углерода, и вся карбонильная группа проявляет те же эффекты относительно соседних атомов углерода. Для формальдегида определена следующая геометрия: длина связей С=О 1, 20 Ǻ, С-Н 1, 10 Ǻ, угол Н-С-Н 116, 5˚, все атомы лежат в одной плоскости. Атомы углерода и кислорода, находится в sp 2 гибридизованном состоянии.

Реакционная способность карбонильной группы связана с присутствием элемента ненасыщенности, и поэтому, как и кратные С=С связи, она вступает в реакции присоединения, разница заключается в том, что карбонильная группа изначально поляризована (μ=2, 7 -3, 05 D) и направление присоединения диполя однозначно. Причем, первичная атака осуществляется нуклеофильной частицей Ad. N. Вклад в дипольный момент вносит наличие двух неподеленных пар электронов кислорода. Так как данные пары лежат в плоскости карбонильной группы, они не могут перекрываться с π-электронными облаками кратной связи С=О. Поэтому, в отличие от гидроксильной группы в спиртах и фенолах кислород карбонильной группы не может проявлять +М эффект

В связи с наличием свободных электронных пар кислорода альдегиды и кетоны проявляют свойства слабых оснований. Протонирование карбонильного кислорода наблюдается только в концентрированных растворах сильных минеральных кислот. За счет электроноакцепторных свойств карбонильной группы в целом, она облегчает нуклеофильное замещение у атома углерода соседнего с группой С=О.

Химические свойства альдегидов и кетонов. Присоединение и замещение по кратной связи С=О Механизм реакций присоединения по карбонильной группе близок к механизму присоединения по связи С=С, но начинается с атаки нуклеофильной частицы по атому углерода карбонильной группы (Ad. N). Атака нуклеофила направлена перпендикулярно плоскости карбонильной группы и на первой стадии образуется тетраэдрический интермедиат. По большей части данная стадия носит обратимый характер.
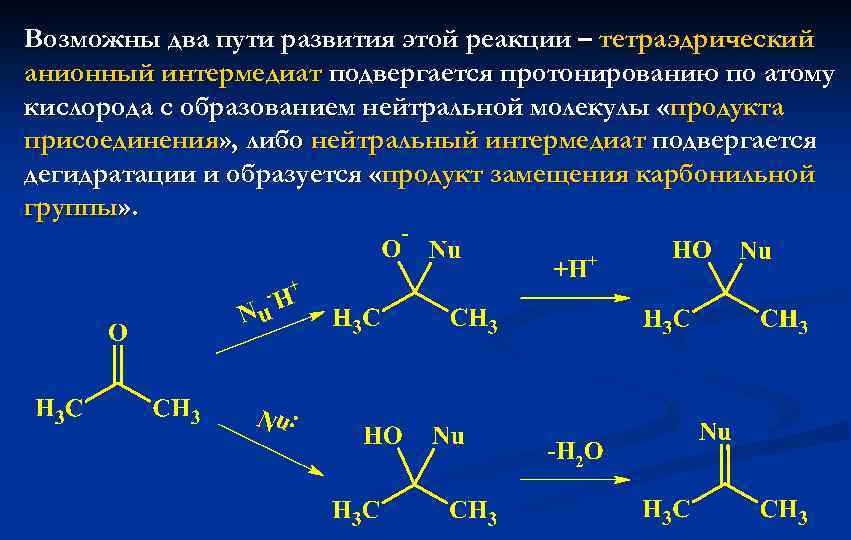
Возможны два пути развития этой реакции – тетраэдрический анионный интермедиат подвергается протонированию по атому кислорода с образованием нейтральной молекулы «продукта присоединения» , либо нейтральный интермедиат подвергается дегидратации и образуется «продукт замещения карбонильной группы» .
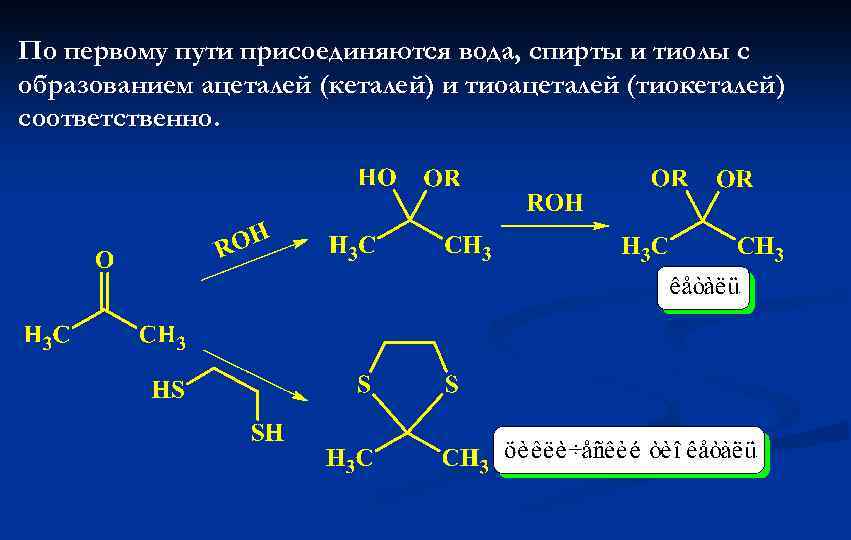
По первому пути присоединяются вода, спирты и тиолы с образованием ацеталей (кеталей) и тиоацеталей (тиокеталей) соответственно.
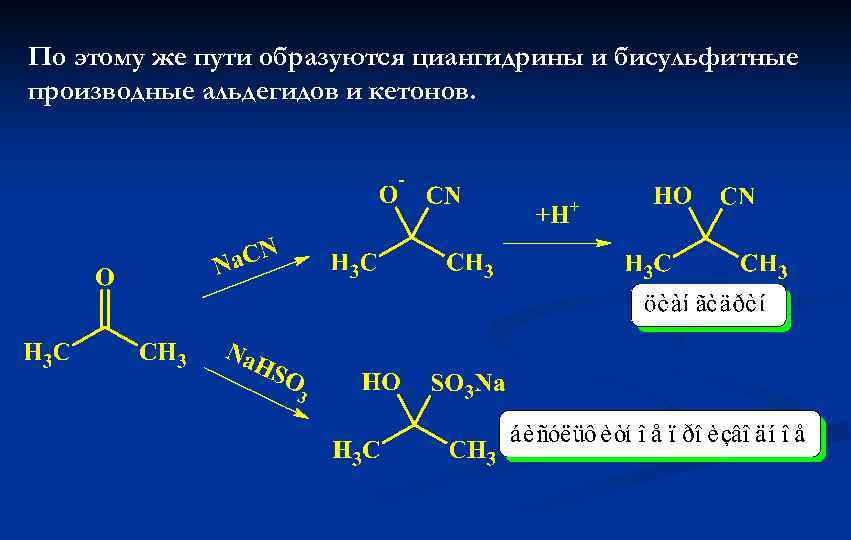
По этому же пути образуются циангидрины и бисульфитные производные альдегидов и кетонов.

Альдегиды, как правило, более реакционноспособны в реакциях нуклеофильного присоединения и замещения чем кетоны. Это объясняется меньшими стерическими препятствиями у альдегидов для атаки. Следует отметить, что в реакцию с бисульфитом натрия вступают только альдегиды и кетоны, в которых хотя бы один из заместителей - метил. Взаимодействие карбонильных соединений с бисульфитом натрия – процесс обратимый, для получения препаративных выходов используют большой избыток бисульфита натрия. Обратимость этой реакции используют для выделения некоторых карбонильных соединений из реакционных смесей.
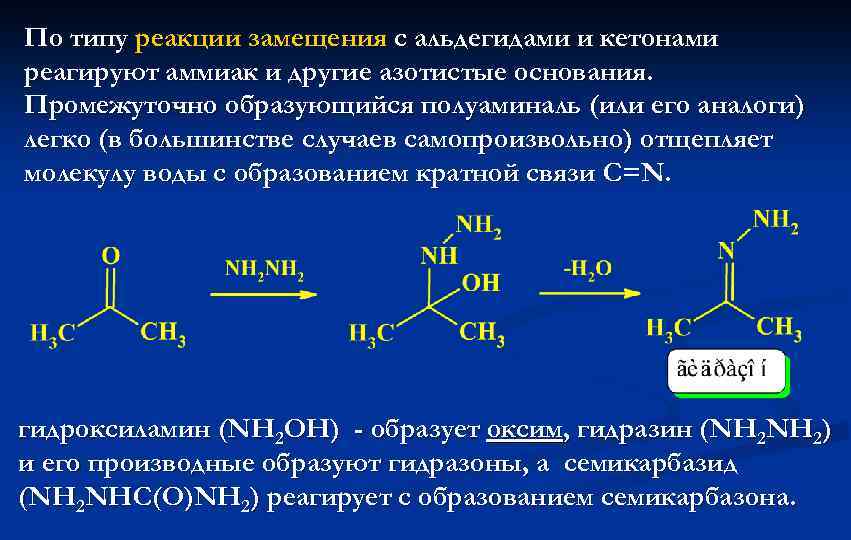
По типу реакции замещения с альдегидами и кетонами реагируют аммиак и другие азотистые основания. Промежуточно образующийся полуаминаль (или его аналоги) легко (в большинстве случаев самопроизвольно) отщепляет молекулу воды с образованием кратной связи C=N. гидроксиламин (NH 2 OH) - образует оксим, гидразин (NH 2) и его производные образуют гидразоны, а семикарбазид (NH 2 NHC(O)NH 2) реагирует с образованием семикарбазона.
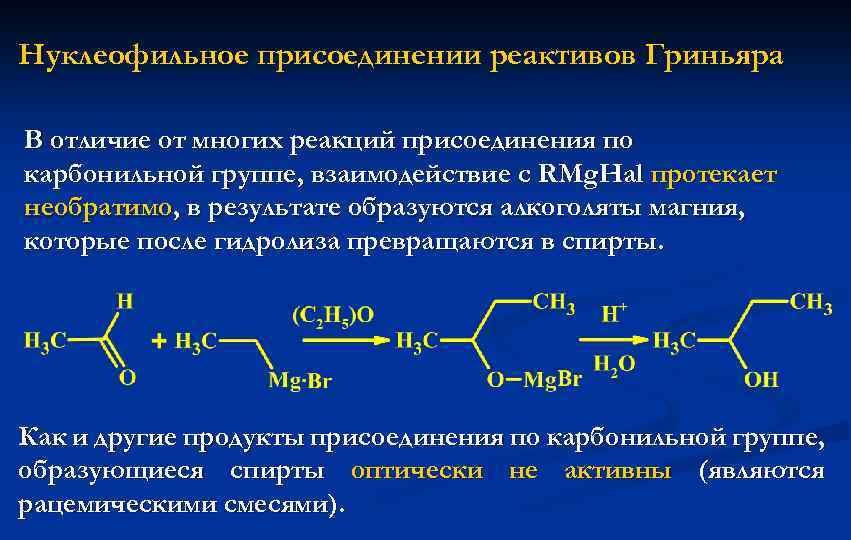
Нуклеофильное присоединении реактивов Гриньяра В отличие от многих реакций присоединения по карбонильной группе, взаимодействие с RMg. Hal протекает необратимо, в результате образуются алкоголяты магния, которые после гидролиза превращаются в спирты. Как и другие продукты присоединения по карбонильной группе, образующиеся спирты оптически не активны (являются рацемическими смесями).
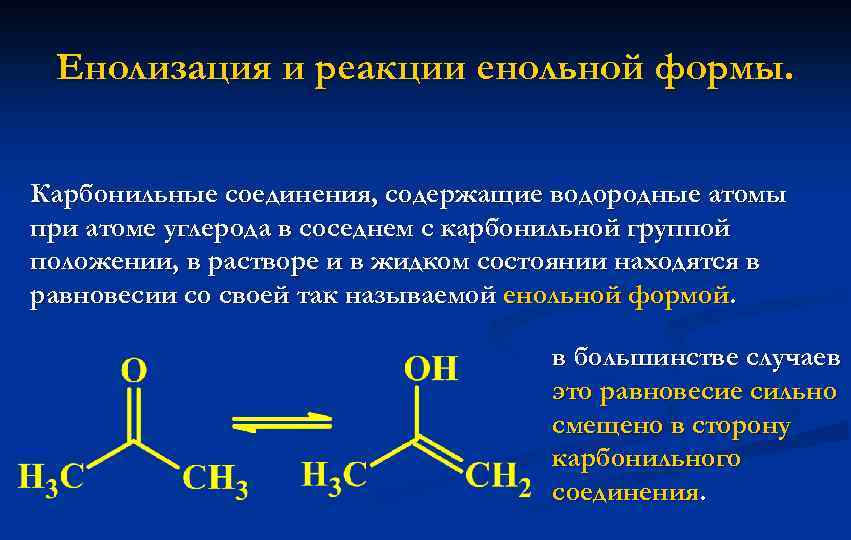
Енолизация и реакции енольной формы. Карбонильные соединения, содержащие водородные атомы при атоме углерода в соседнем с карбонильной группой положении, в растворе и в жидком состоянии находятся в равновесии со своей так называемой енольной формой. в большинстве случаев это равновесие сильно смещено в сторону карбонильного соединения.
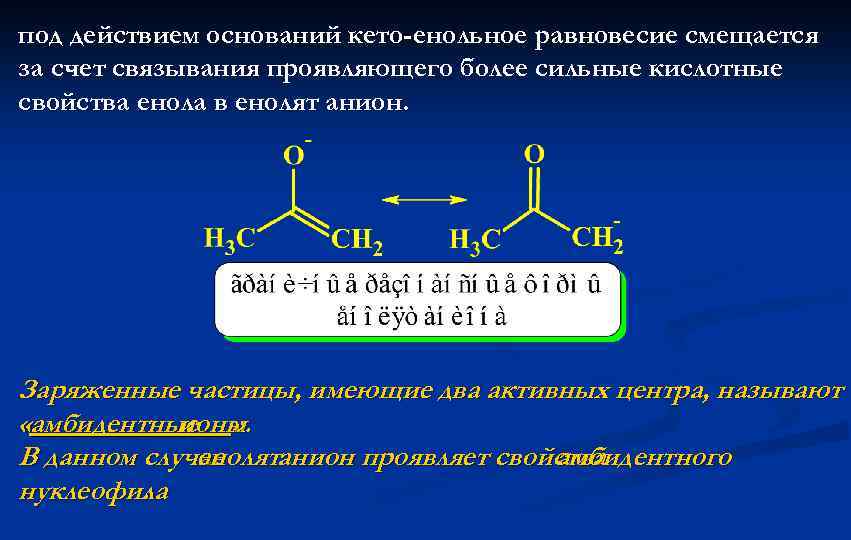
под действием оснований кето-енольное равновесие смещается за счет связывания проявляющего более сильные кислотные свойства енола в енолят анион. Заряженные частицы, имеющие два активных центра, называют «амбидентные » . ионы В данном случае енолятанион проявляет свойства амбидентного нуклеофила.

Альдольно-кротоновая конденсация Под действием основания часть молекул карбонильного соединения переходят в форму енолята, который нуклеофильно атакует неенолизованную молекулу по карбонильной группе. В результате реакции, на первой стадии образуется продукт альдольной конденсации – кетоспирт (в данном примере 4 -гидрокси-4 -метилпентанон-2), а после элиминирования воды образуется α, β-непредельное карбонильное соединение – продукт кротоновой конденсации (в случае ацетона образуется 4 -метилпентен-3 -он-2 «окись мезитила» ).
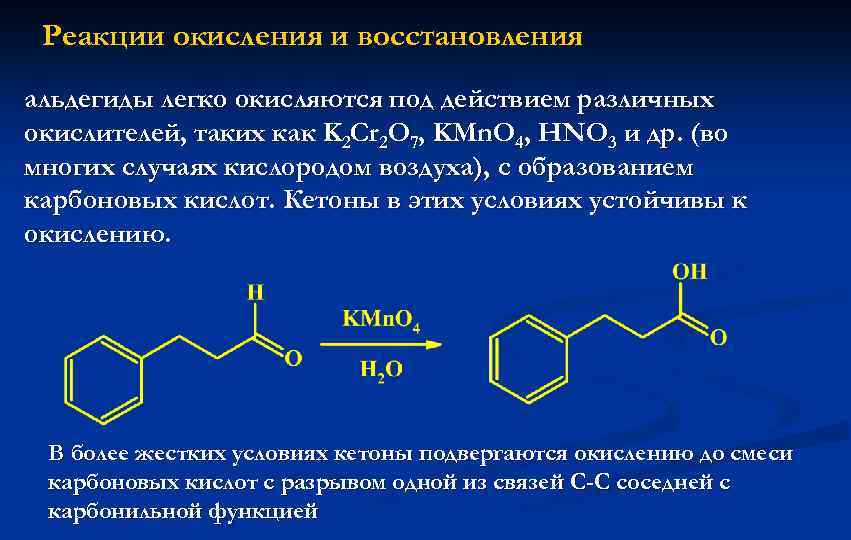
Реакции окисления и восстановления альдегиды легко окисляются под действием различных окислителей, таких как K 2 Cr 2 O 7, KMn. O 4, HNO 3 и др. (во многих случаях кислородом воздуха), с образованием карбоновых кислот. Кетоны в этих условиях устойчивы к окислению. В более жестких условиях кетоны подвергаются окислению до смеси карбоновых кислот с разрывом одной из связей С-С соседней с карбонильной функцией
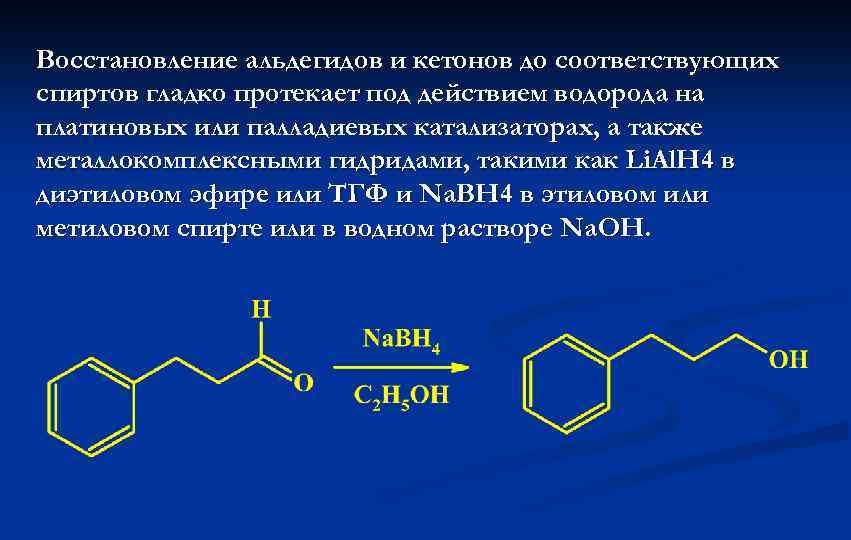
Восстановление альдегидов и кетонов до соответствующих спиртов гладко протекает под действием водорода на платиновых или палладиевых катализаторах, а также металлокомплексными гидридами, такими как Li. Al. H 4 в диэтиловом эфире или ТГФ и Na. BH 4 в этиловом или метиловом спирте или в водном растворе Na. OH.
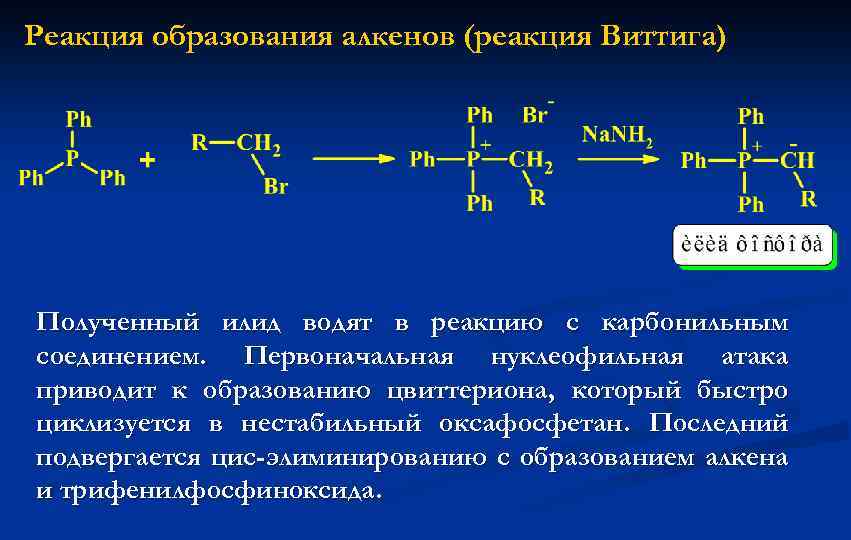
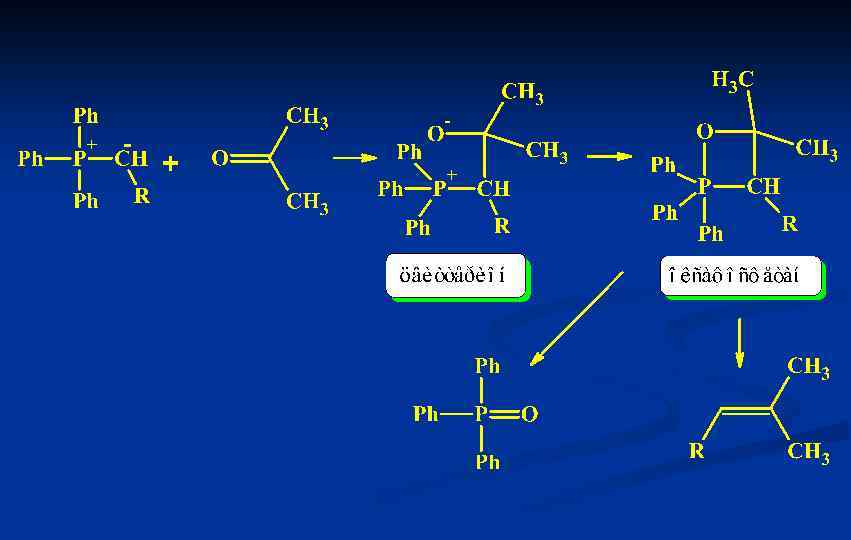
Реакция образования алкенов (реакция Виттига) Полученный илид водят в реакцию с карбонильным соединением. Первоначальная нуклеофильная атака приводит к образованию цвиттериона, который быстро циклизуется в нестабильный оксафосфетан. Последний подвергается цис-элиминированию с образованием алкена и трифенилфосфиноксида.
лекция 10 карбонильные соединения.ppt