111 II-е начало термодинамики.ppt
- Количество слайдов: 31
 Лекция 10
Лекция 10
 §§ Циклы Круговым процессом (циклом) называется процесс, при котором система, пройдя ряд состояний, возвращается в начальное состояние A > 0 – прямой цикл Работа совершается системой за счет подводимого тепла Q (тепловой двигатель) 02
§§ Циклы Круговым процессом (циклом) называется процесс, при котором система, пройдя ряд состояний, возвращается в начальное состояние A > 0 – прямой цикл Работа совершается системой за счет подводимого тепла Q (тепловой двигатель) 02
 A < 0 – обратный цикл Работа совершается над системой (холодильная машина) Происходит превращение работы в теплоту, т. к. выходит энергии больше, чем входит. ∫ (L) (в каждой точке цикла выполняется УС) 03
A < 0 – обратный цикл Работа совершается над системой (холодильная машина) Происходит превращение работы в теплоту, т. к. выходит энергии больше, чем входит. ∫ (L) (в каждой точке цикла выполняется УС) 03
 §§ КПД цикла Тепловая машина термодинамически действующее устройство, совершающее работу за счет подводимого из вне тепла Элементы тепловой машины 1) нагреватель тела с очень большой 2) рабочее тело теплоемкостью 3) холодильник 04
§§ КПД цикла Тепловая машина термодинамически действующее устройство, совершающее работу за счет подводимого из вне тепла Элементы тепловой машины 1) нагреватель тела с очень большой 2) рабочее тело теплоемкостью 3) холодильник 04
 Для кругового процесса ∫ ∫ т. е. работа совершается за счет поступающей энергии На участке цикла рабочее тело может получать энергию: и отдавать: 05
Для кругового процесса ∫ ∫ т. е. работа совершается за счет поступающей энергии На участке цикла рабочее тело может получать энергию: и отдавать: 05
 Пусть Q 1 – количество энергии, полученное системой от нагревателя Q 2 – количество энергии, отданное холодильнику Тогда эффективность машины (КПД): 06
Пусть Q 1 – количество энергии, полученное системой от нагревателя Q 2 – количество энергии, отданное холодильнику Тогда эффективность машины (КПД): 06
 Существует бесконечное множество циклов и у каждого свой КПД. В механике циклы используют для преобразования энергии (превращения теплоты в работу). На практике используется всего несколько десятков циклов. 07
Существует бесконечное множество циклов и у каждого свой КПД. В механике циклы используют для преобразования энергии (превращения теплоты в работу). На практике используется всего несколько десятков циклов. 07
 §§ Цикл Карно Рассмотрим наиболее эффективный цикл, состоящий из двух изотерм T 1 и T 2 и двух адиабат Вычислим работу тела за цикл: 08
§§ Цикл Карно Рассмотрим наиболее эффективный цикл, состоящий из двух изотерм T 1 и T 2 и двух адиабат Вычислим работу тела за цикл: 08
 1→ 2 – изотермическое расширение – за счет нагревателя 2→ 3 – адиабатическое расширение – за счет 09
1→ 2 – изотермическое расширение – за счет нагревателя 2→ 3 – адиабатическое расширение – за счет 09
 Аналогично следовательно 10
Аналогично следовательно 10
 Работа за цикл Вычислим КПД: 11
Работа за цикл Вычислим КПД: 11
 Теорема Карно–Клаузиуса КПД тепловой машины, работающей по циклу Карно, зависит только от температур T 1 и T 2 нагревателя и холодильника, но не зависит от устройства машины и вида рабочего тела Теорема Карно (2) КПД всякой ТМ не может превосходить КПД идеальной ТМ, работающей по циклу Карно, с теми же самыми температурами нагревателя и холодильника 12
Теорема Карно–Клаузиуса КПД тепловой машины, работающей по циклу Карно, зависит только от температур T 1 и T 2 нагревателя и холодильника, но не зависит от устройства машины и вида рабочего тела Теорема Карно (2) КПД всякой ТМ не может превосходить КПД идеальной ТМ, работающей по циклу Карно, с теми же самыми температурами нагревателя и холодильника 12
 §§ Обратимые процессы Обратимым называется процесс, для которого возможен обратный переход из конечного состояния в начальное через те же промежуточные состояния, что и в прямом процессе или если систему можно вернуть в исходное состояние хотя бы одним способом и притом так, чтобы состояние тел вне системы осталось неизменным. 13
§§ Обратимые процессы Обратимым называется процесс, для которого возможен обратный переход из конечного состояния в начальное через те же промежуточные состояния, что и в прямом процессе или если систему можно вернуть в исходное состояние хотя бы одним способом и притом так, чтобы состояние тел вне системы осталось неизменным. 13
 Процесс – равновесный, если система проходит ряд непрерывно следующих друг за другом равновесных состояний Условия равновесности: 1) непрерывность всех величин, характеризующих процесс 2) бесконечно малая скорость изменений в системе Необходимое и достаточное условие обратимости – равновесность. 14
Процесс – равновесный, если система проходит ряд непрерывно следующих друг за другом равновесных состояний Условия равновесности: 1) непрерывность всех величин, характеризующих процесс 2) бесконечно малая скорость изменений в системе Необходимое и достаточное условие обратимости – равновесность. 14
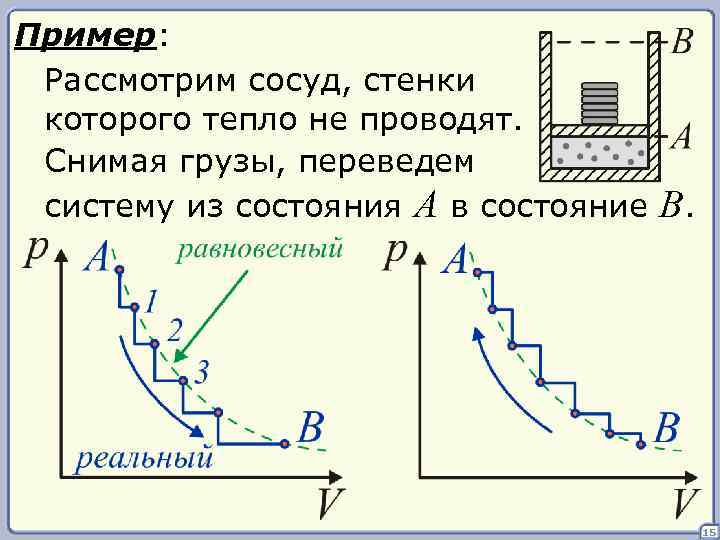 Пример: Рассмотрим сосуд, стенки которого тепло не проводят. Снимая грузы, переведем систему из состояния A в состояние B. 15
Пример: Рассмотрим сосуд, стенки которого тепло не проводят. Снимая грузы, переведем систему из состояния A в состояние B. 15
 Все реальные процессы протекают с конечной скоростью и являются необратимыми и неравновесными. При любом возмущении в системе требуется время для установления равновесия. Это приводит к тому, что в обратном процессе газ совершит большую работу, чем в прямом. 16
Все реальные процессы протекают с конечной скоростью и являются необратимыми и неравновесными. При любом возмущении в системе требуется время для установления равновесия. Это приводит к тому, что в обратном процессе газ совершит большую работу, чем в прямом. 16
 §§ Неравенство Клаузиуса Сравним КПД неравновесной и равновесной машины, работающей по циклу Карно: приведенная теплота ∫ – неравенство Клаузиуса 17
§§ Неравенство Клаузиуса Сравним КПД неравновесной и равновесной машины, работающей по циклу Карно: приведенная теплота ∫ – неравенство Клаузиуса 17
 §§ Энтропия идеального газа I-е начало в дифференциальной форме функция состояния полный дифференциал бесконечно малое приращение (Q – не функция состояния, как и Разделим на A) T левую и правую части: 18
§§ Энтропия идеального газа I-е начало в дифференциальной форме функция состояния полный дифференциал бесконечно малое приращение (Q – не функция состояния, как и Разделим на A) T левую и правую части: 18
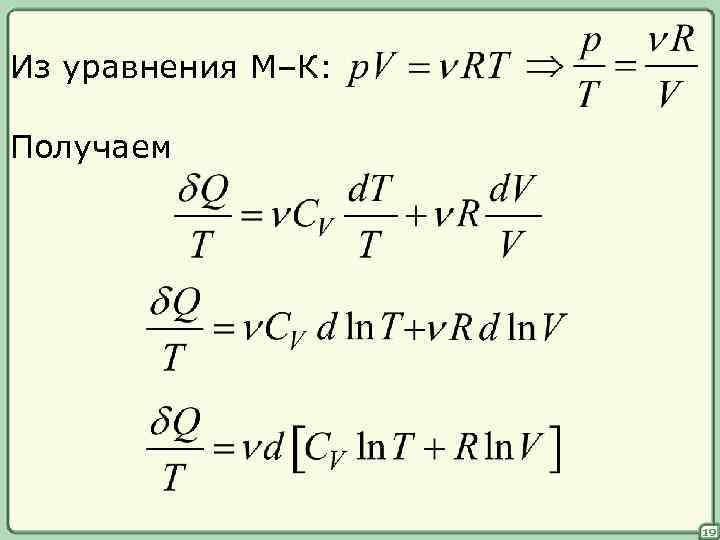 Из уравнения М–К: Получаем 19
Из уравнения М–К: Получаем 19
 Левая часть – полный дифференциал, тогда правая часть – дифференциал новой функции состояния S – энтропия Это выражение справедливо только для равновесных (обратимых) процессов. Оно позволяет вычислить разность S, но не абсолютное значение. 20
Левая часть – полный дифференциал, тогда правая часть – дифференциал новой функции состояния S – энтропия Это выражение справедливо только для равновесных (обратимых) процессов. Оно позволяет вычислить разность S, но не абсолютное значение. 20
 §§ Основное уравнение ТД Согласно первому началу и для равновесного процесса получаем основное уравнение термодинамики Оно справедливо при химических реакциях и при фазовых переходах. В физике имеет множество следствий. 21
§§ Основное уравнение ТД Согласно первому началу и для равновесного процесса получаем основное уравнение термодинамики Оно справедливо при химических реакциях и при фазовых переходах. В физике имеет множество следствий. 21
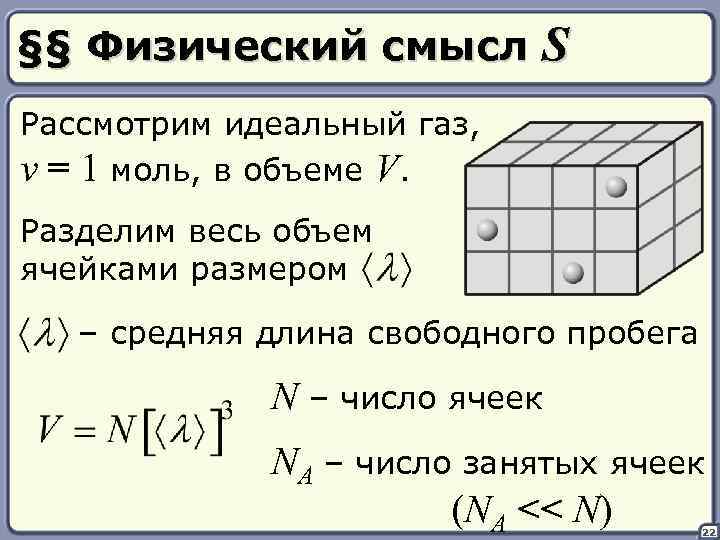 §§ Физический смысл S Рассмотрим идеальный газ, ν = 1 моль, в объеме V. Разделим весь объем ячейками размером – средняя длина свободного пробега N – число ячеек NA – число занятых ячеек (NA << N) 22
§§ Физический смысл S Рассмотрим идеальный газ, ν = 1 моль, в объеме V. Разделим весь объем ячейками размером – средняя длина свободного пробега N – число ячеек NA – число занятых ячеек (NA << N) 22
 Вычислим Г – число микросостояний, которое может реализоваться в системе Оно равно числу способов размещения NA молекул по N ячейкам: Формула Стирлинга: ≈ 23
Вычислим Г – число микросостояний, которое может реализоваться в системе Оно равно числу способов размещения NA молекул по N ячейкам: Формула Стирлинга: ≈ 23
 ≈ Следовательно, при T = const 24
≈ Следовательно, при T = const 24
 и const часто полагают равной нулю и считают, что энтропия пропорциональна логарифму числа пространственных микросостояний Энтропия является мерой беспорядка (разупорядочения) в системе. 25
и const часто полагают равной нулю и считают, что энтропия пропорциональна логарифму числа пространственных микросостояний Энтропия является мерой беспорядка (разупорядочения) в системе. 25
 §§ II-е начало термодинамики Система, предоставленная самой себе, приходит к равновесному состоянию, т. е. энтропия не уменьшается в предоставленной самой себе системе. I-е начало говорит о соотношении между величинами, характеризующими систему II-е начало указывает направление изменений в системе, если они должны произойти. 26
§§ II-е начало термодинамики Система, предоставленная самой себе, приходит к равновесному состоянию, т. е. энтропия не уменьшается в предоставленной самой себе системе. I-е начало говорит о соотношении между величинами, характеризующими систему II-е начало указывает направление изменений в системе, если они должны произойти. 26
 Пусть замкнутая система переходит из состояния 1 в состояние 2. Возвратим систему в состояние 1 с помощью обратимого процесса т. к. система изолирована 27
Пусть замкнутая система переходит из состояния 1 в состояние 2. Возвратим систему в состояние 1 с помощью обратимого процесса т. к. система изолирована 27
 Следовательно, При переходе замкнутой системы из состояния 1 (с S 1) в 2 (с S 2), энтропия либо увеличивается, либо не изменяется Замечание: о «тепловой смерти» Клаузиус, рассматривая Вселенную как замкнутую систему, утверждал: «энтропия Вселенной стремится к максимуму» 28
Следовательно, При переходе замкнутой системы из состояния 1 (с S 1) в 2 (с S 2), энтропия либо увеличивается, либо не изменяется Замечание: о «тепловой смерти» Клаузиус, рассматривая Вселенную как замкнутую систему, утверждал: «энтропия Вселенной стремится к максимуму» 28
 §§ Тепловая теорема Нернста Первое утверждение При приближении к абсолютному нулю энтропия стремится к определенному конечному пределу – т. е. этот интеграл сходится. 29
§§ Тепловая теорема Нернста Первое утверждение При приближении к абсолютному нулю энтропия стремится к определенному конечному пределу – т. е. этот интеграл сходится. 29
 Второе утверждение Все процессы при абсолютном нуле температур, переводящие систему из одного равновесного состояния в другое, происходят без изменения энтропии Классическое описание системы при абсолютном нуле неприменимо, т. к. оно допускает бесконечное множество состояний. Необходимо рассмотрение с квантовых позиций. 30
Второе утверждение Все процессы при абсолютном нуле температур, переводящие систему из одного равновесного состояния в другое, происходят без изменения энтропии Классическое описание системы при абсолютном нуле неприменимо, т. к. оно допускает бесконечное множество состояний. Необходимо рассмотрение с квантовых позиций. 30
 Список вопросов к экзамену по физике Семестр 1 « Механика. Молекулярная физика и термодинамика » §§ Кинематика материальной точки 1. Система отсчета. Радиус-вектор материальной точки, скорость и ускорение м. т. при криволинейном движении. 2. Движение материальной точки по окружности. 3. Нормальное и тангенциальное ускорение. Радиус кривизны траектории. §§ Динамика материальной точки 4. Первый закон Ньютона. Инерциальные системы отсчета. Закон сложения скоростей. 5. Второй закон Ньютона. Масса. Сила. Импульс материальной точки и системы м. т. Принцип суперпозиции сил. 6. Третий закон Ньютона. Внешние и внутренние силы. Закон сохранения импульса. 7. Центр масс. Теорема о движении центра масс. 8. Гравитационное и кулоновское взаимодействие. Сила упругости. Сила трения и сопротивления. 9. Реактивное движение. Уравнение Мещерского. Формула Циолковского. §§ Работа и энергия 10. Работа и мощность силы. 11. Кинетическая энергия. 12. Работа постоянной и центральной силы. Консервативные и неконсервативные силы. 13. Потенциальная энергия. 14. Закон сохранения энергии в механике и физике. 15. Силовое поле. §§ Механика абсолютно твердого тела 16. Виды движения абсолютно твердого тела. Мгновенная ось вращения. 17. Момент силы и момент импульса относительно неподвижного начала. 18. Момент силы и момент импульса относительно неподвижной оси. 19. Уравнение динамики вращательного движения системы материальных точек. 20. Момент инерции твердого тела. Моменты инерции простейших тел. Теорема Гюйгенса–Штейнера. 21. Работа внешних сил и кинетическая энергия при вращении твердого тела. §§ Колебания и волны 22. Уравнение гармонических колебаний и его решение.
Список вопросов к экзамену по физике Семестр 1 « Механика. Молекулярная физика и термодинамика » §§ Кинематика материальной точки 1. Система отсчета. Радиус-вектор материальной точки, скорость и ускорение м. т. при криволинейном движении. 2. Движение материальной точки по окружности. 3. Нормальное и тангенциальное ускорение. Радиус кривизны траектории. §§ Динамика материальной точки 4. Первый закон Ньютона. Инерциальные системы отсчета. Закон сложения скоростей. 5. Второй закон Ньютона. Масса. Сила. Импульс материальной точки и системы м. т. Принцип суперпозиции сил. 6. Третий закон Ньютона. Внешние и внутренние силы. Закон сохранения импульса. 7. Центр масс. Теорема о движении центра масс. 8. Гравитационное и кулоновское взаимодействие. Сила упругости. Сила трения и сопротивления. 9. Реактивное движение. Уравнение Мещерского. Формула Циолковского. §§ Работа и энергия 10. Работа и мощность силы. 11. Кинетическая энергия. 12. Работа постоянной и центральной силы. Консервативные и неконсервативные силы. 13. Потенциальная энергия. 14. Закон сохранения энергии в механике и физике. 15. Силовое поле. §§ Механика абсолютно твердого тела 16. Виды движения абсолютно твердого тела. Мгновенная ось вращения. 17. Момент силы и момент импульса относительно неподвижного начала. 18. Момент силы и момент импульса относительно неподвижной оси. 19. Уравнение динамики вращательного движения системы материальных точек. 20. Момент инерции твердого тела. Моменты инерции простейших тел. Теорема Гюйгенса–Штейнера. 21. Работа внешних сил и кинетическая энергия при вращении твердого тела. §§ Колебания и волны 22. Уравнение гармонических колебаний и его решение.


