Лекция 1_2016. Технология рекомбинантных ДНК.ppt
- Количество слайдов: 72

Лекция 1. Технология рекомбинантных ДНК.
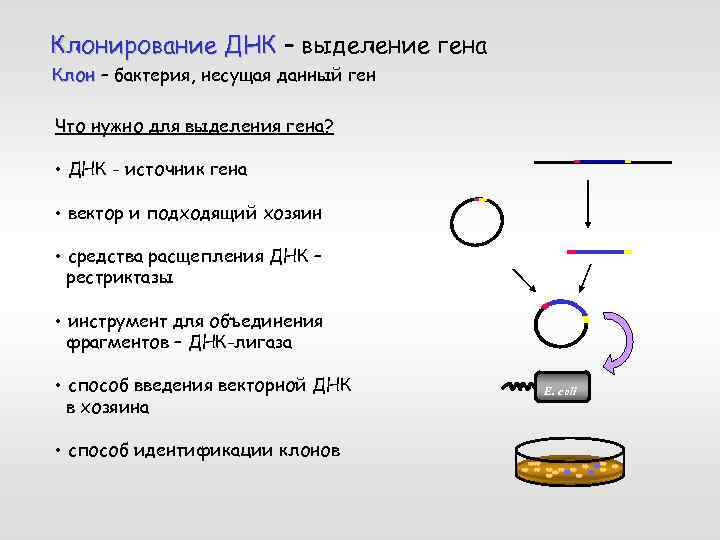
Клонирование ДНК – выделение гена Клон – бактерия, несущая данный ген Что нужно для выделения гена? • ДНК - источник гена • вектор и подходящий хозяин • средства расщепления ДНК – рестриктазы • инструмент для объединения фрагментов – ДНК-лигаза • способ введения векторной ДНК в хозяина • способ идентификации клонов E. coli
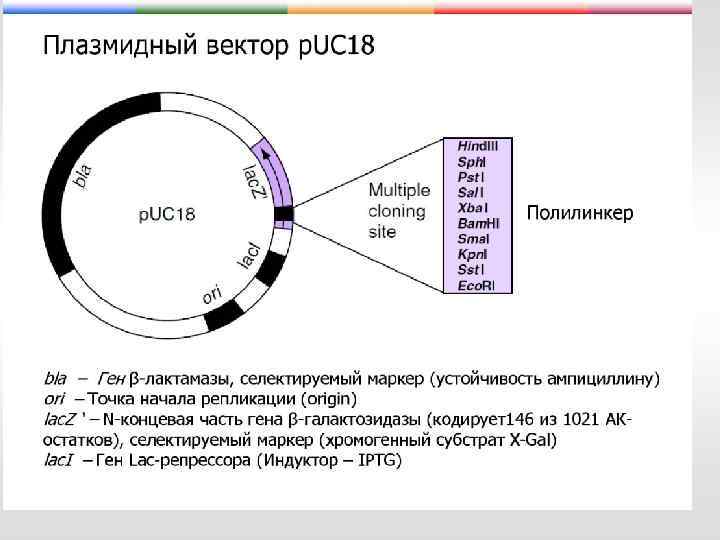
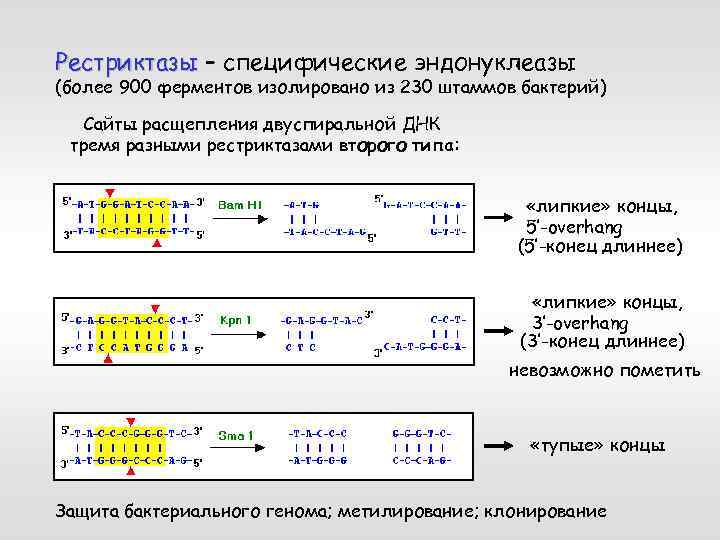
Рестриктазы – специфические эндонуклеазы (более 900 ферментов изолировано из 230 штаммов бактерий) Сайты расщепления двуспиральной ДНК тремя разными рестриктазами второго типа: «липкие» концы, 5’-overhang (5’-конец длиннее) «липкие» концы, 3’-overhang (3’-конец длиннее) невозможно пометить «тупые» концы Защита бактериального генома; метилирование; клонирование

Электрофорез ДНК: 1. разделение молекул по размеру ДНК подвижность молекул ДНК зависит от плотности агарозного геля концентрация агарозы В геле присутствует бромистый этидий, который интеркалирует в ДНК; комплекс флюоресцирует при 590 нм.
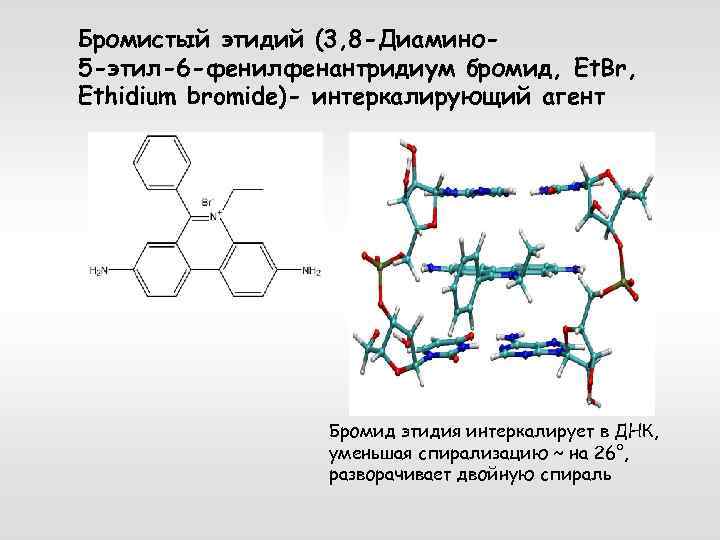
Бромистый этидий (3, 8 -Диамино 5 -этил-6 -фенилфенантридиум бромид, Et. Br, Ethidium bromide)- интеркалирующий агент Бромид этидия интеркалирует в ДНК, уменьшая спирализацию ~ на 26°, разворачивает двойную спираль
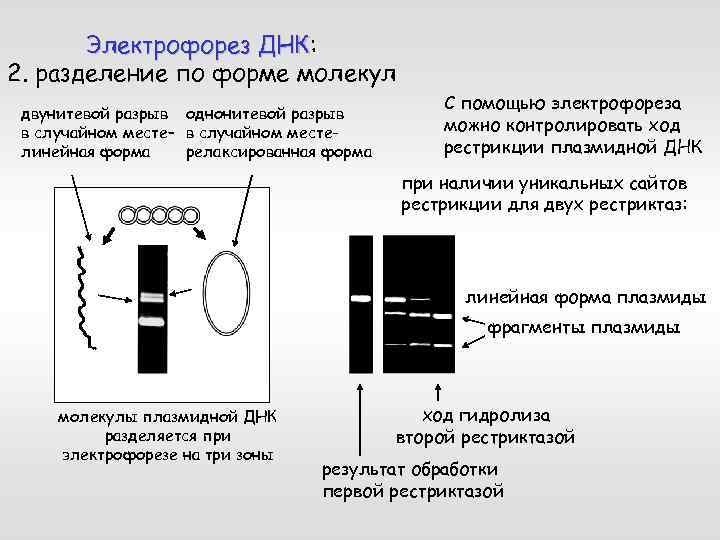
Электрофорез ДНК: ДНК 2. разделение по форме молекул двунитевой разрыв однонитевой разрыв в случайном месте– в случайном местелинейная форма релаксированная форма С помощью электрофореза можно контролировать ход рестрикции плазмидной ДНК при наличии уникальных сайтов рестрикции для двух рестриктаз: линейная форма плазмиды фрагменты плазмиды молекулы плазмидной ДНК разделяется при электрофорезе на три зоны ход гидролиза второй рестриктазой результат обработки первой рестриктазой
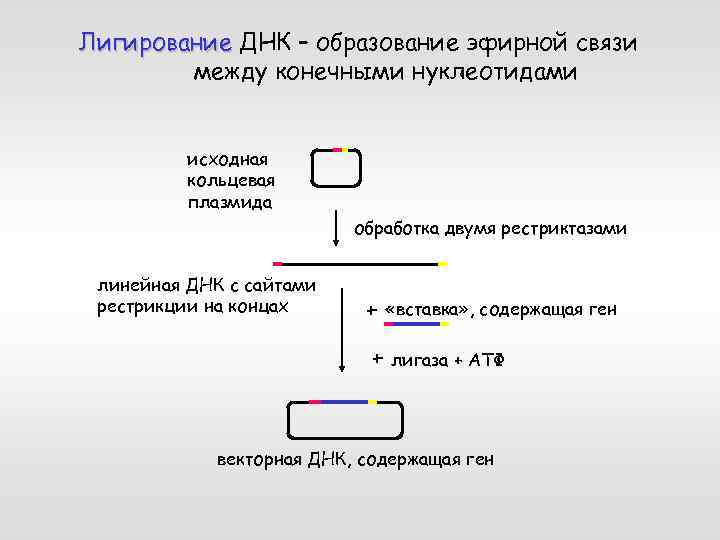
Лигирование ДНК – образование эфирной связи между конечными нуклеотидами исходная кольцевая плазмида обработка двумя рестриктазами линейная ДНК с сайтами рестрикции на концах + «вставка» , содержащая ген + лигаза + АТФ векторная ДНК, содержащая ген
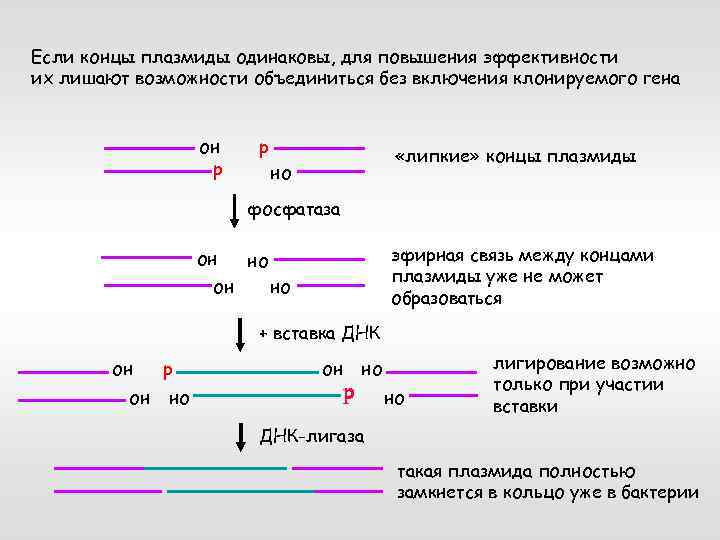
Если концы плазмиды одинаковы, для повышения эффективности их лишают возможности объединиться без включения клонируемого гена он р р «липкие» концы плазмиды но фосфатаза он он эфирная связь между концами плазмиды уже не может образоваться но но + вставка ДНК он он р но но лигирование возможно только при участии вставки ДНК-лигаза такая плазмида полностью замкнется в кольцо уже в бактерии
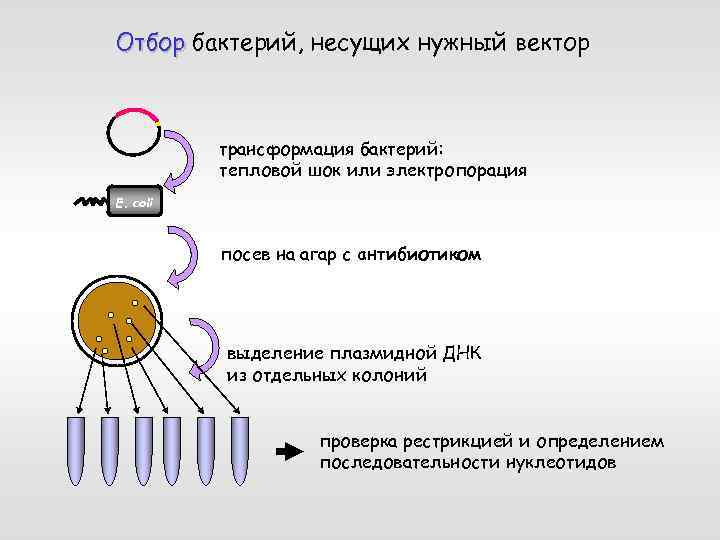
Отбор бактерий, несущих нужный вектор трансформация бактерий: тепловой шок или электропорация E. coli посев на агар с антибиотиком выделение плазмидной ДНК из отдельных колоний проверка рестрикцией и определением последовательности нуклеотидов

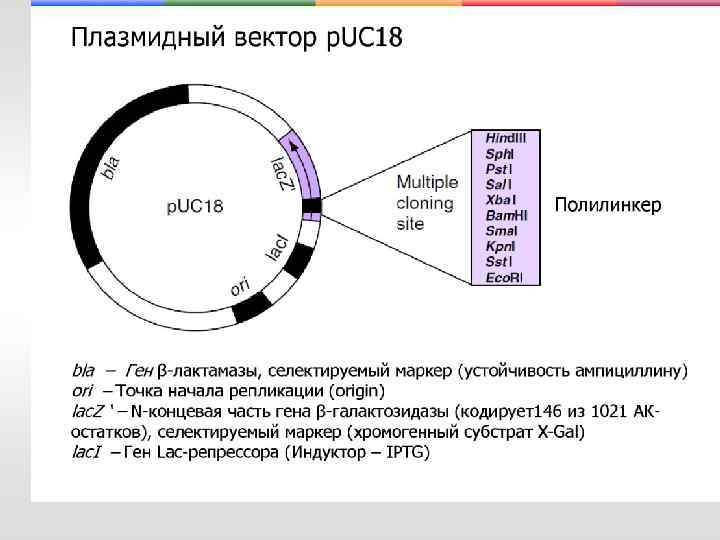
Отбор бактерий: ферментная система (бело-голубая селекция) • MCS плазмиды находится внутри последовательности lac. Z’, кодирующей N-концевой пептид β-галактозидазы, но не мешает образованию фермента после объединения с С-концевым пептидом. Растут голубые колонии. Однако клонирование в MCS нарушает рамку считывания N-концевого пептида, βгалактозидаза не образуется, растут белые колонии. • Индукцию lac-оперона осуществляют с помощью ИПТГ (изопропил-β-D-1 тиогалактопиранозид), аналога аллолактозы, метаболита лактозы.
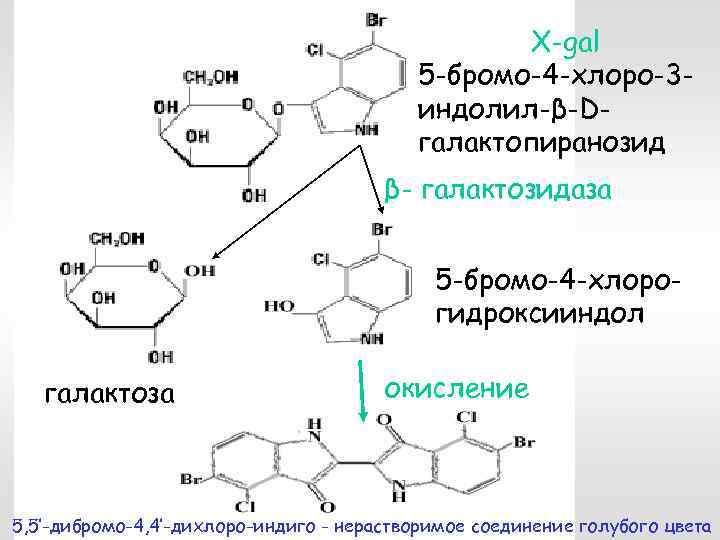
X-gal 5 -бромо-4 -хлоро-3 индолил-β-Dгалактопиранозид β- галактозидаза 5 -бромо-4 -хлорогидроксииндол галактоза окисление 5, 5’-дибромо-4, 4’-дихлоро-индиго - нерастворимое соединение голубого цвета
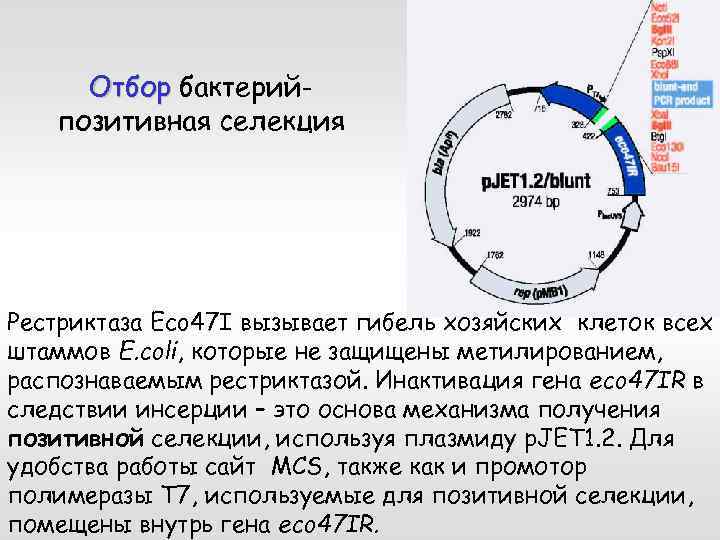
Отбор бактерийпозитивная селекция Рестриктаза Eco 47 I вызывает гибель хозяйских клеток всех штаммов E. coli, которые не защищены метилированием, распознаваемым рестриктазой. Инактивация гена еco 47 IR в следствии инсерции – это основа механизма получения позитивной селекции, используя плазмиду p. JET 1. 2. Для удобства работы сайт MCS, также как и промотор полимеразы Т 7, используемые для позитивной селекции, помещены внутрь гена еco 47 IR.

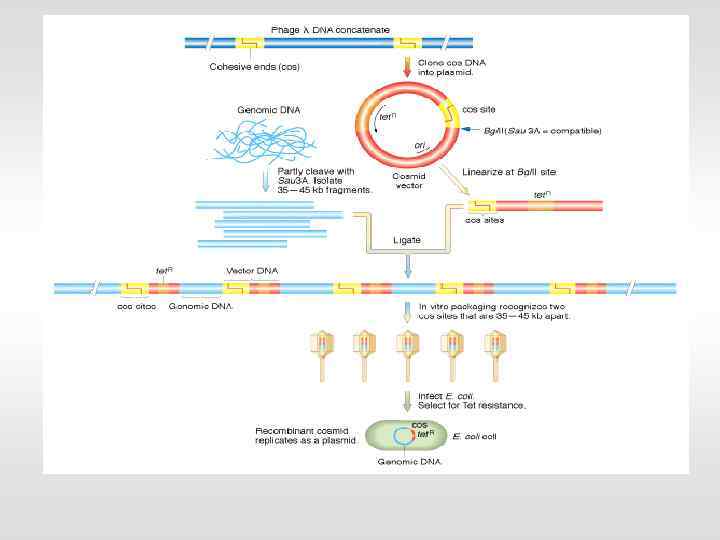
Векторная ДНК: • автономная репликация в бактериях или дрожжах • устойчивость к антибиотику • удобные сайты рестрикции (MCS) Размер вставки, которую могут переносить: - плазмиды - до 10 тыс. пар оснований (п. о. ) - вирусы (фаги) - до 25 тыс. п. о. - космиды - в среднем 45 тыс. п. о. - бактериальные искусственные хромосомы – до 300 тыс. п. о. - дрожжевые искусственные хромосомы - до 1 млн. п. о.
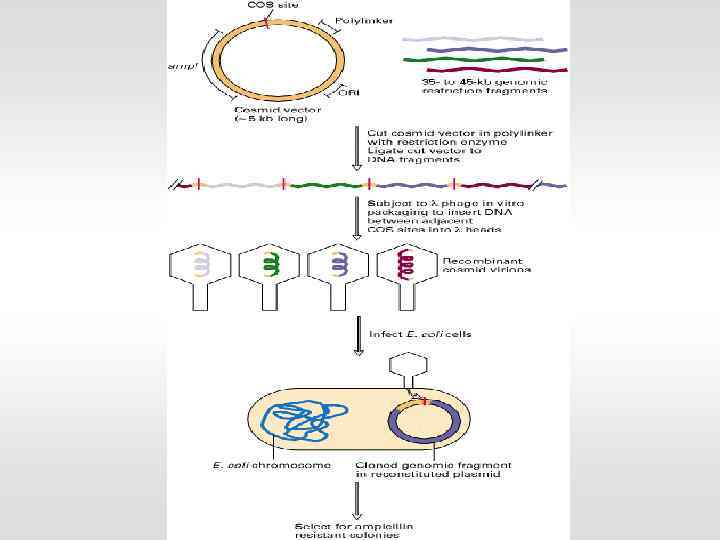
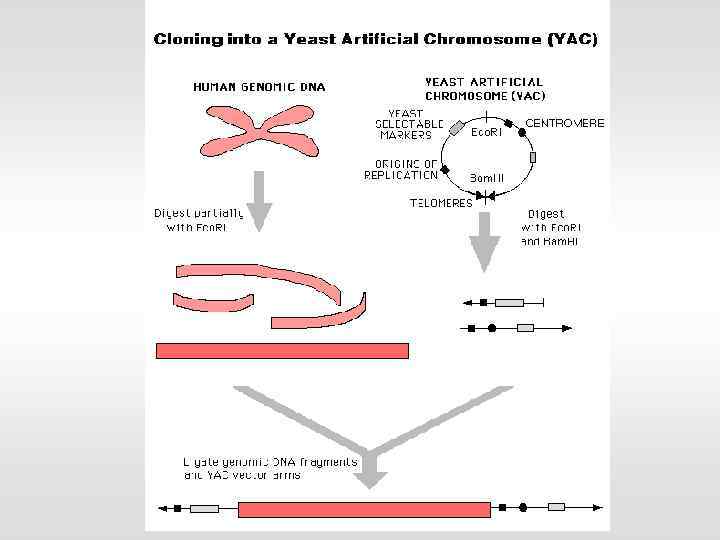
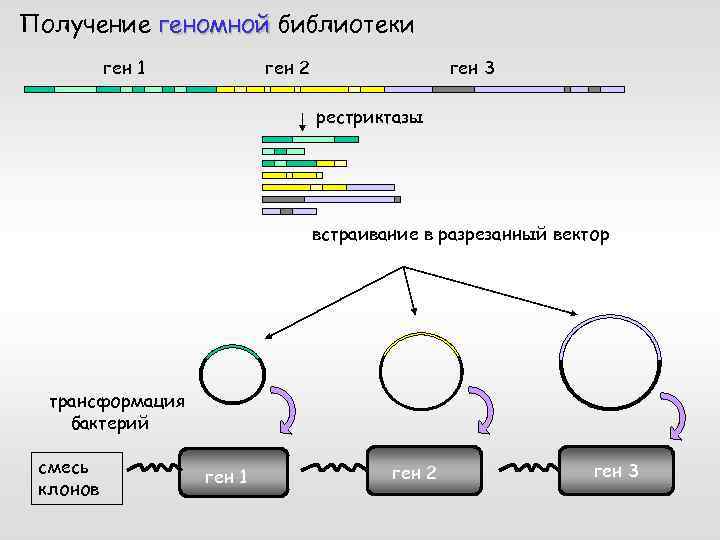
Получение геномной библиотеки ген 1 ген 3 ген 2 рестриктазы встраивание в разрезанный вектор трансформация бактерий смесь клонов ген 1 ген 2 ген 3
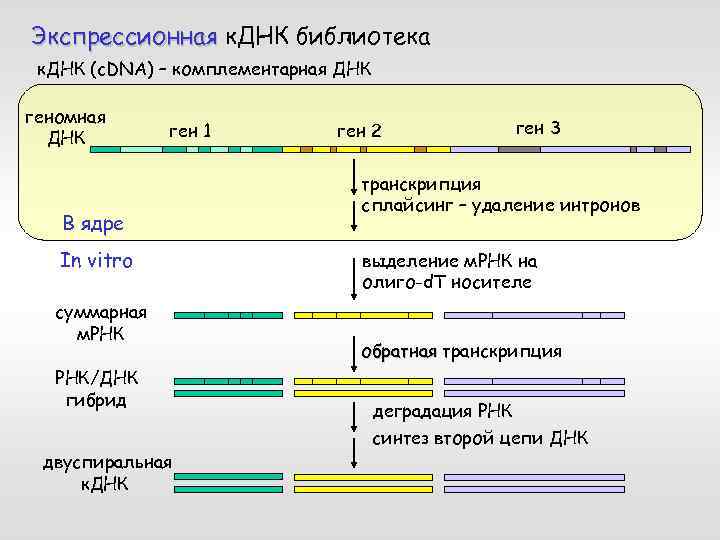
Экспрессионная к. ДНК библиотека к. ДНК (c. DNA) – комплементарная ДНК геномная ДНК ген 1 В ядре In vitro суммарная м. РНК/ДНК гибрид двуспиральная к. ДНК ген 2 ген 3 транскрипция сплайсинг – удаление интронов выделение м. РНК на олиго-d. T носителе обратная транскрипция деградация РНК синтез второй цепи ДНК
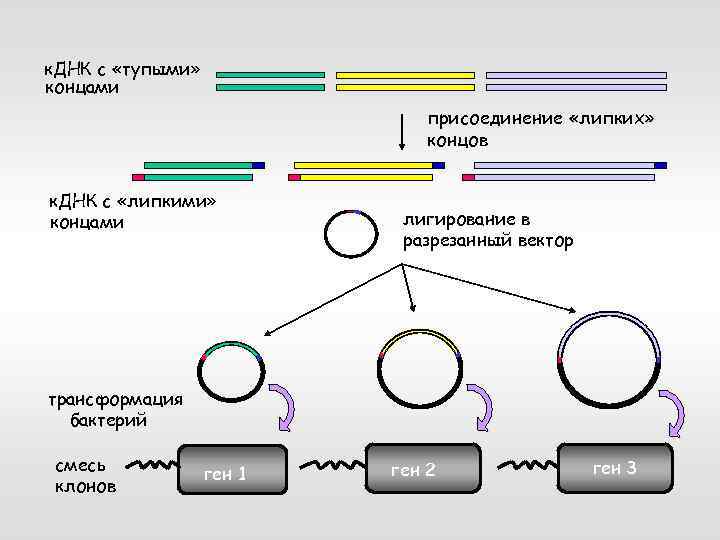
к. ДНК с «тупыми» концами присоединение «липких» « концов к. ДНК с «липкими» концами лигирование в разрезанный вектор трансформация бактерий смесь клонов ген 1 ген 2 ген 3
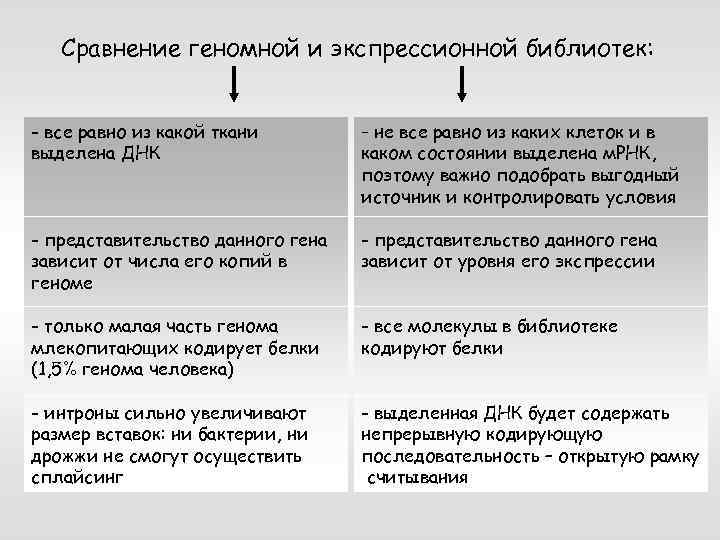
Сравнение геномной и экспрессионной библиотек: - все равно из какой ткани выделена ДНК - не все равно из каких клеток и в каком состоянии выделена м. РНК, поэтому важно подобрать выгодный источник и контролировать условия - представительство данного гена зависит от числа его копий в геноме - представительство данного гена зависит от уровня его экспрессии - только малая часть генома млекопитающих кодирует белки (1, 5% генома человека) - все молекулы в библиотеке кодируют белки - интроны сильно увеличивают размер вставок: ни бактерии, ни дрожжи не смогут осуществить сплайсинг - выделенная ДНК будет содержать непрерывную кодирующую последовательность – открытую рамку считывания
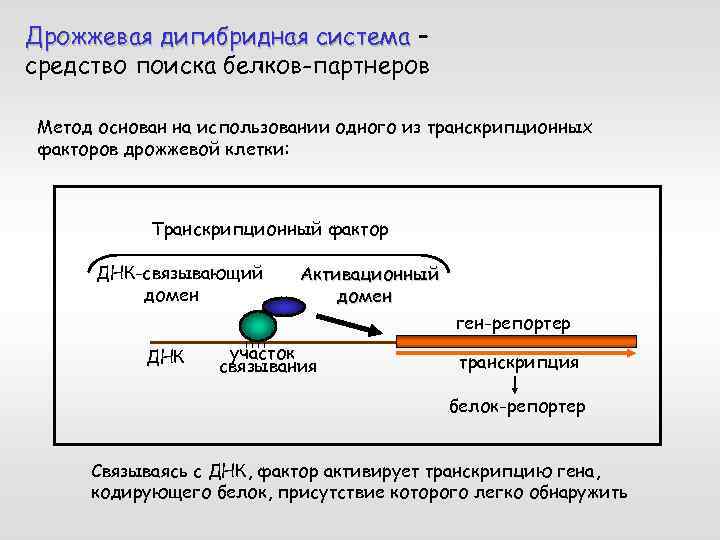
Дрожжевая дигибридная система – средство поиска белков-партнеров Метод основан на использовании одного из транскрипционных факторов дрожжевой клетки: Транскрипционный фактор ДНК-связывающий домен Активационный домен ген-репортер ДНК участок связывания транскрипция белок-репортер Связываясь с ДНК, фактор активирует транскрипцию гена, кодирующего белок, присутствие которого легко обнаружить
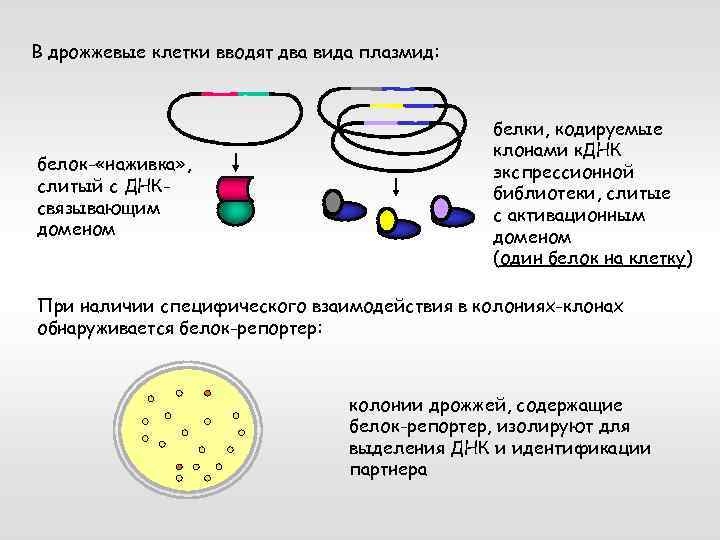
В дрожжевые клетки вводят два вида плазмид: белок- «наживка» , слитый с ДНКсвязывающим доменом белки, кодируемые клонами к. ДНК экспрессионной библиотеки, слитые с активационным доменом (один белок на клетку) При наличии специфического взаимодействия в колониях-клонах обнаруживается белок-репортер: колонии дрожжей, содержащие белок-репортер, изолируют для выделения ДНК и идентификации партнера
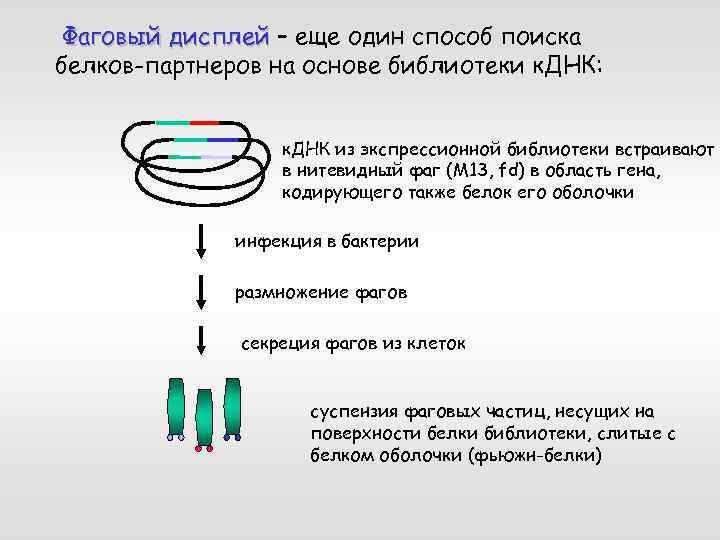
Фаговый дисплей – еще один способ поиска белков-партнеров на основе библиотеки к. ДНК: к. ДНК из экспрессионной библиотеки встраивают в нитевидный фаг (M 13, fd) в область гена, кодирующего также белок его оболочки инфекция в бактерии размножение фагов секреция фагов из клеток суспензия фаговых частиц, несущих на поверхности белки библиотеки, слитые с белком оболочки (фьюжн-белки)
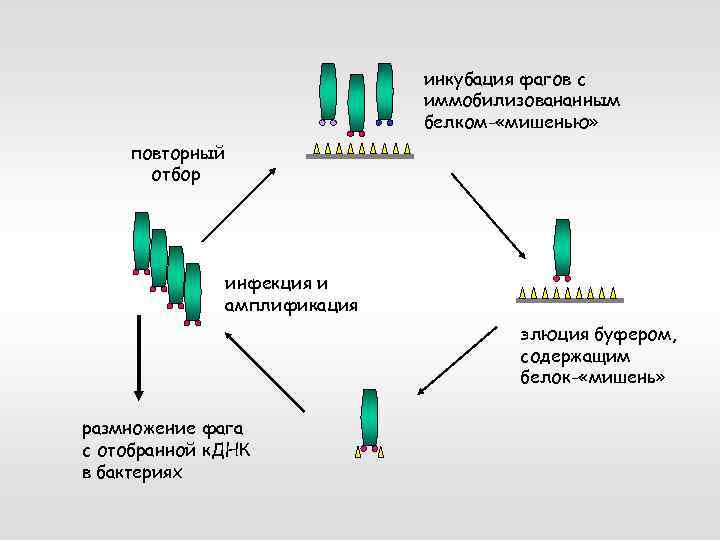
инкубация фагов с иммобилизовананным белком- «мишенью» повторный отбор инфекция и амплификация элюция буфером, содержащим белок- «мишень» размножение фага с отобранной к. ДНК в бактериях
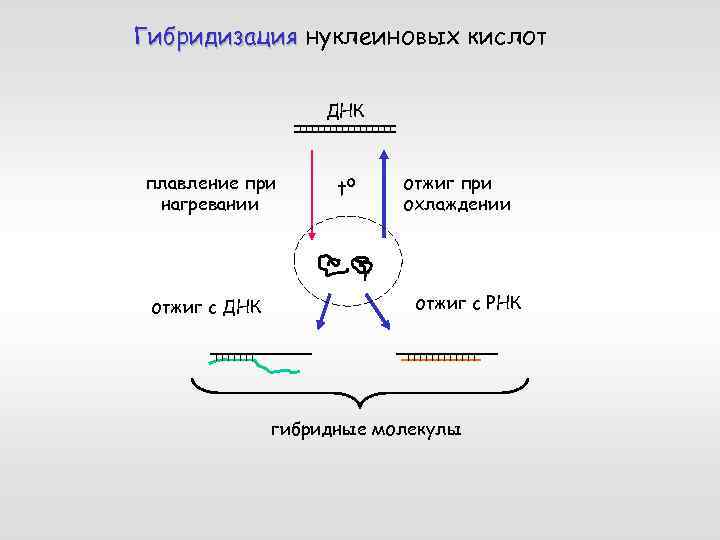
Гибридизация нуклеиновых кислот ДНК плавление при нагревании отжиг с ДНК tº отжиг при охлаждении отжиг с РНК гибридные молекулы
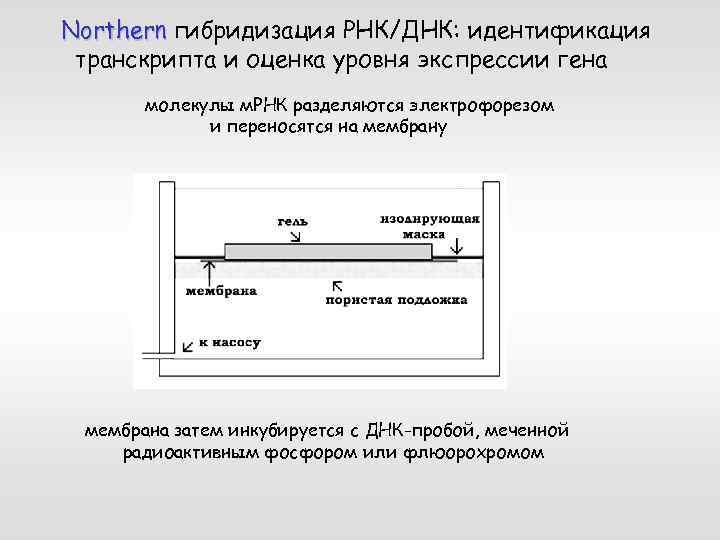
Northern гибридизация РНК/ДНК: идентификация транскрипта и оценка уровня экспрессии гена молекулы м. РНК разделяются электрофорезом и переносятся на мембрану мембрана затем инкубируется с ДНК-пробой, меченной радиоактивным фосфором или флюорохромом
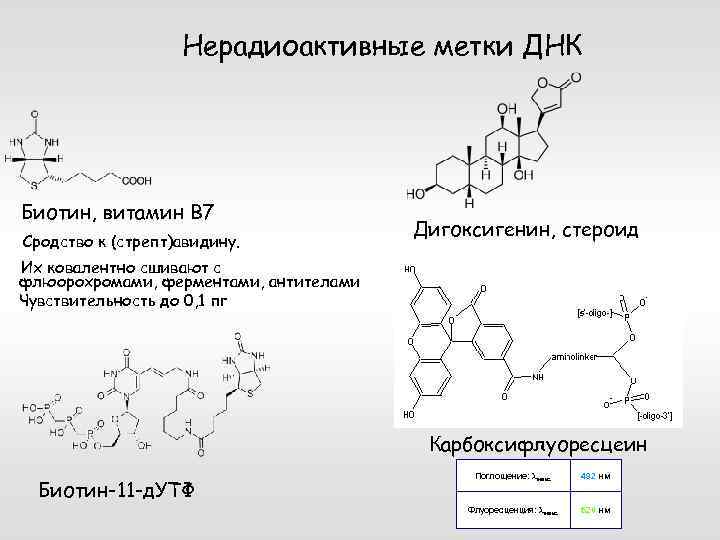
Нерадиоактивные метки ДНК Биотин, витамин В 7 Сродство к (стрепт)авидину. Дигоксигенин, стероид Их ковалентно сшивают с флюорохромами, ферментами, антителами Чувствительность до 0, 1 пг Карбоксифлуоресцеин Биотин-11 -д. УТФ Поглощение: lмакс. 492 нм Флуоресценция: lмакс. 520 нм
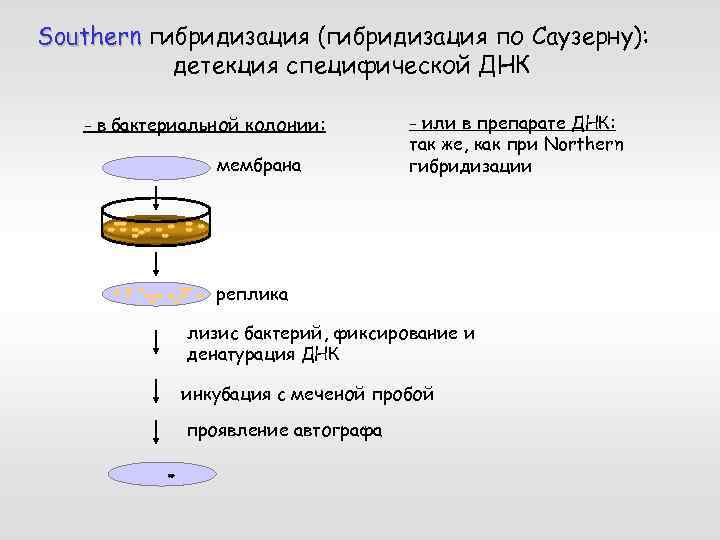
Southern гибридизация (гибридизация по Саузерну): детекция специфической ДНК - в бактериальной колонии: мембрана - или в препарате ДНК: так же, как при Northern гибридизации реплика лизис бактерий, фиксирование и денатурация ДНК инкубация с меченой пробой проявление автографа

Сравнительный анализ экспрессии генов норма опухоль суммарная м. РНК к. ДНК с флюоресцентной меткой смесь равных количеств двух препаратов “микрочип” с набором клонов к. ДНК, конкурентная гибридизация анализ флюоресценции отдельных пятен
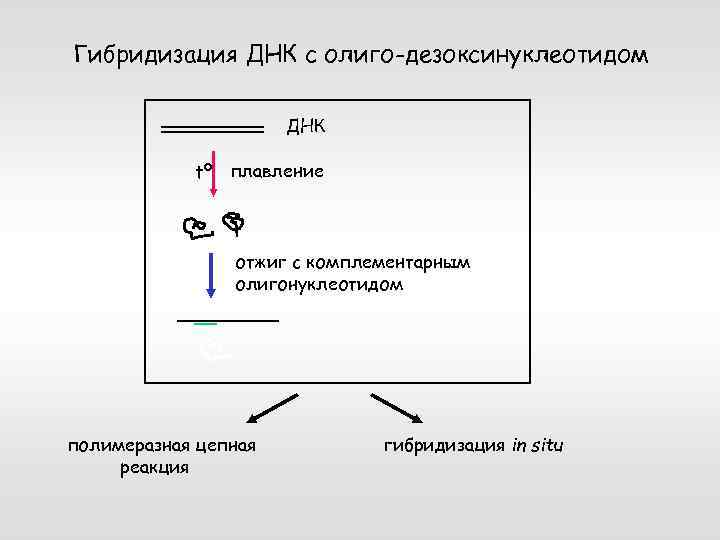
Гибридизация ДНК с олиго-дезоксинуклеотидом ДНК tº плавление отжиг с комплементарным олигонуклеотидом полимеразная цепная реакция гибридизация in situ
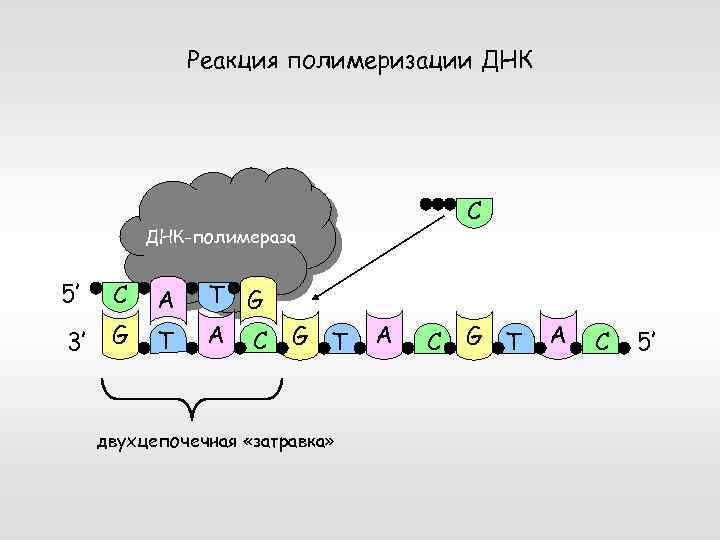
Реакция полимеризации ДНК C ДНК-полимераза 5’ C A 3’ G T T G A C G T двухцепочечная «затравка» A C G T A C 5’

Главный компонент PCR: ДНК-полимераза I из Escherichia coli – деградирует при 37º Taq-полимераза из Thermus aquaticus – термостабильна, работает быстро, но не исправляет ошибки при синтезе новой цепи (ок. 28 ошибок/10 6, скорость 1000 нуклеотидов/мин). Имеет 5’-3’-экзонуклеазную активность. Отсутствует 3’-5’-экзонуклеазная активность (редактирующая). Pfu-полимераза из Pyrococcus furiosus – термостабильна, работает медленнее, зато исправляет многие ошибки (имеет 3’-5’-экзонуклеазную активность, ок. 2 -4 ошибок/106, скорость 300 нукл. /мин)
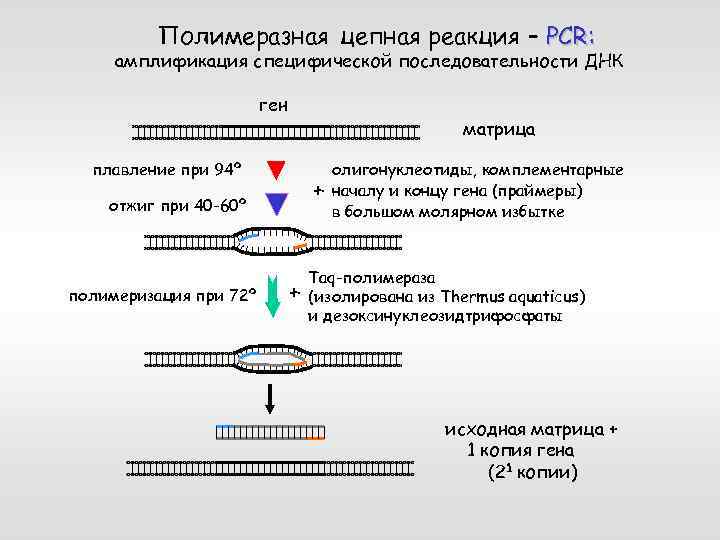
Полимеразная цепная реакция – PCR: амплификация специфической последовательности ДНК ген матрица плавление при 94º + отжиг при 40 -60º полимеризация при 72º + олигонуклеотиды, комплементарные началу и концу гена (праймеры) в большом молярном избытке Taq-полимераза (изолирована из Thermus aquaticus) и дезоксинуклеозидтрифосфаты исходная матрица + 1 копия гена (21 копии)
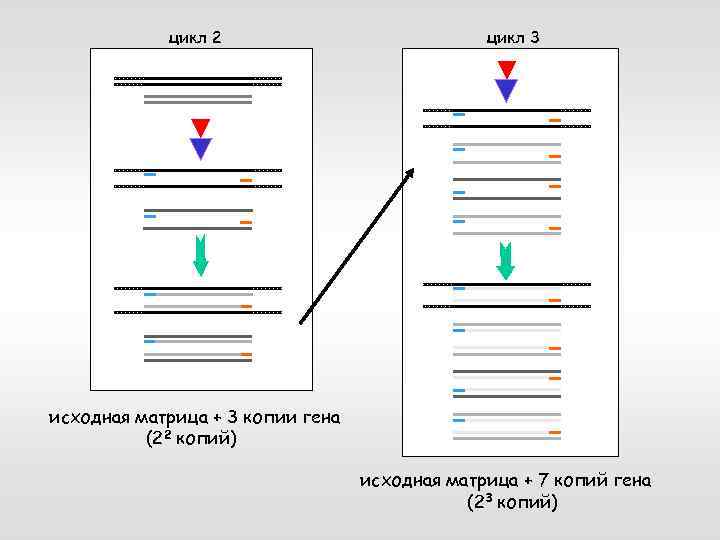
цикл 2 цикл 3 исходная матрица + 3 копии гена (22 копий) исходная матрица + 7 копий гена (23 копий)
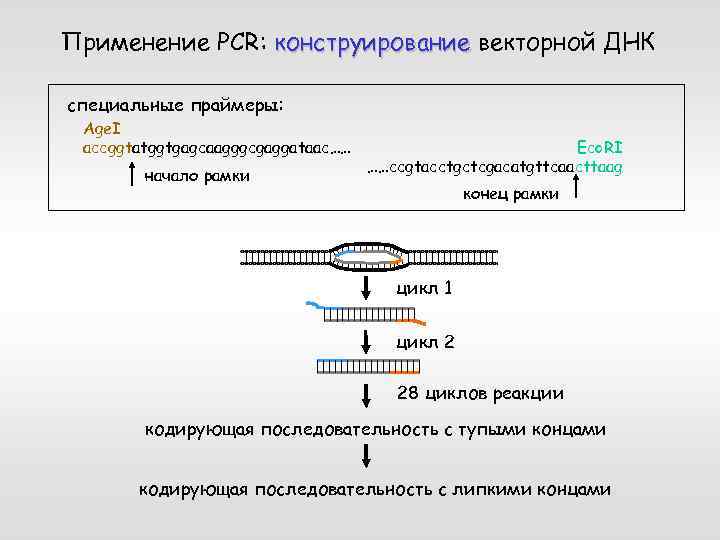
Применение PCR: конструирование векторной ДНК специальные праймеры: Age. I accggtatggtgagcaagggcgaggataac…… начало рамки Eco. RI ……ccgtacctgctcgacatgttcaacttaag конец рамки цикл 1 цикл 2 28 циклов реакции кодирующая последовательность с тупыми концами кодирующая последовательность с липкими концами
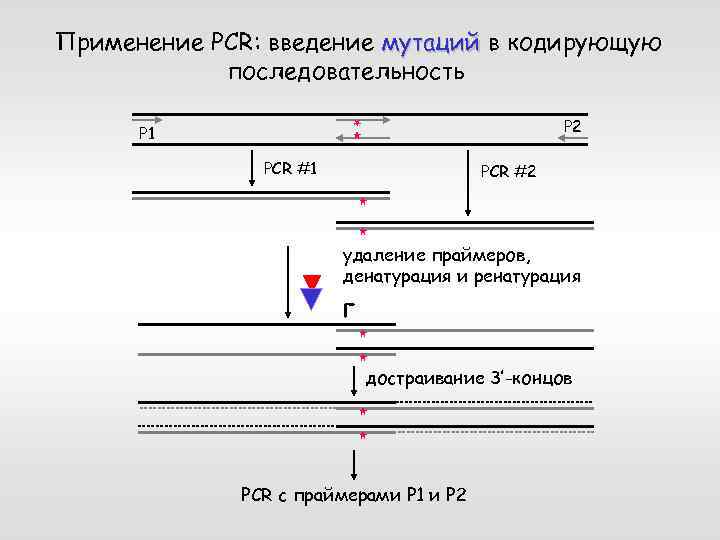
Применение PCR: введение мутаций в кодирующую последовательность P 2 P 1 PCR #2 удаление праймеров, денатурация и ренатурация г достраивание 3’-концов PCR с праймерами P 1 и P 2
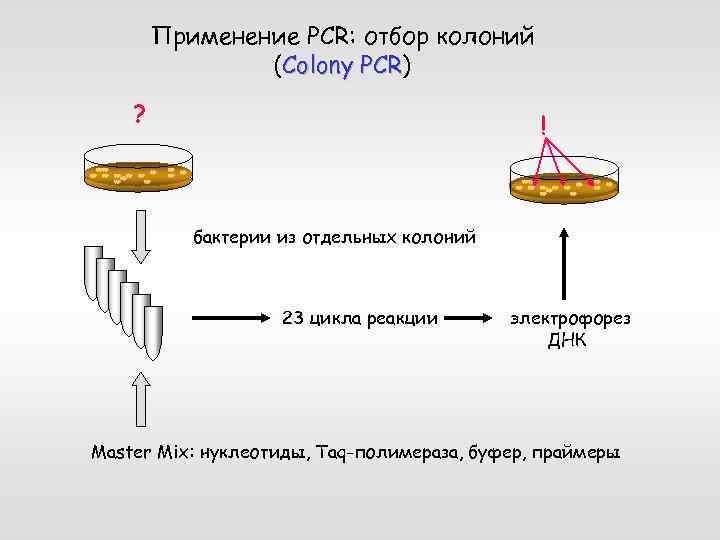
Применение PCR: отбор колоний (Colony PCR) PCR ? ! бактерии из отдельных колоний 23 цикла реакции электрофорез ДНК Master Mix: нуклеотиды, Taq-полимераза, буфер, праймеры
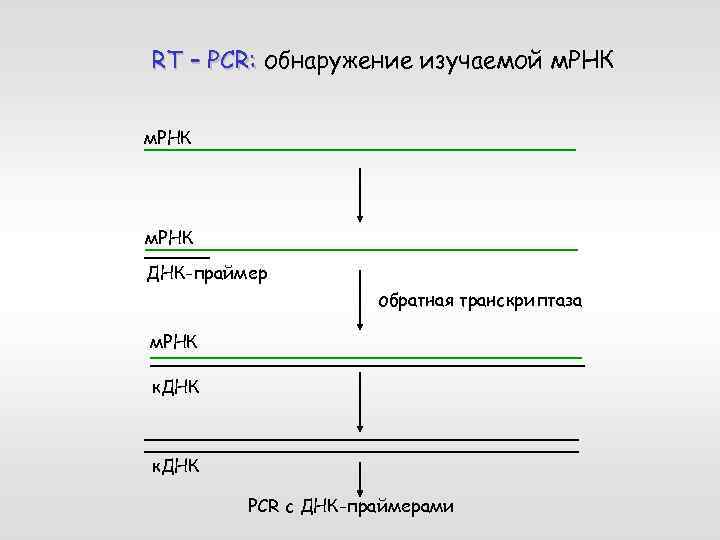
RT – PCR: обнаружение изучаемой м. РНК ДНК-праймер обратная транскриптаза м. РНК к. ДНК PCR с ДНК-праймерами
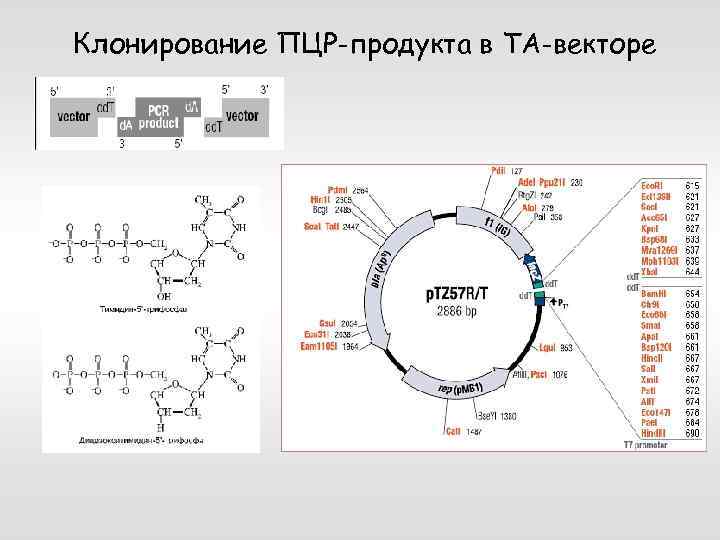
Клонирование ПЦР-продукта в ТА-векторе
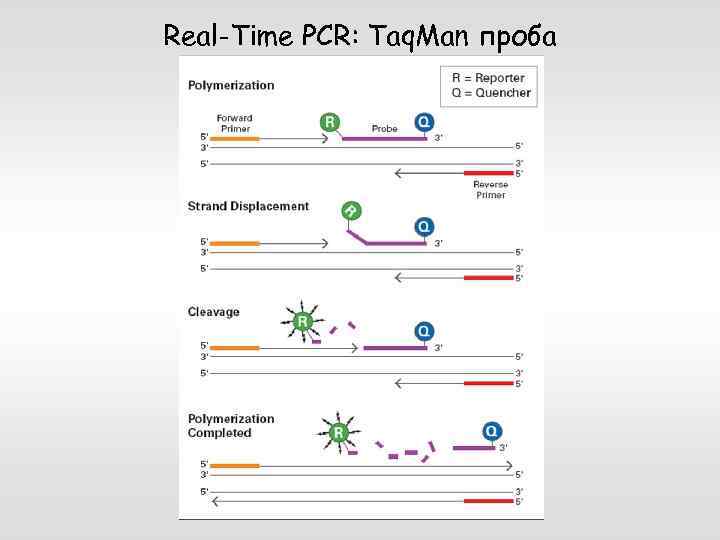
Real-Time PCR: Taq. Man проба
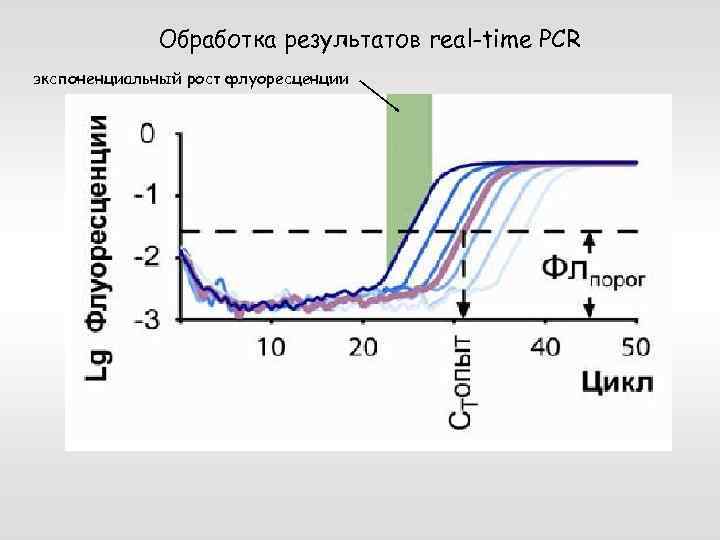
Обработка результатов real-time PCR экспоненциальный рост флуоресценции
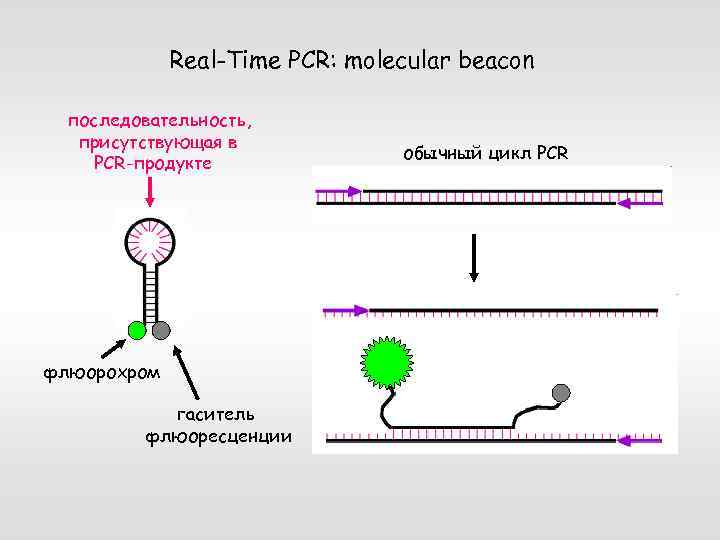
Real-Time PCR: molecular beacon последовательность, присутствующая в PCR-продукте флюорохром гаситель флюоресценции обычный цикл PCR

Real-Time PCR: with Sybr green I. Неспецифический интеркалирующий цианиновый краситель: поглощает синий свет(λ макс = 488 нм), излучает зеленый свет (λ макс = 522 нм).
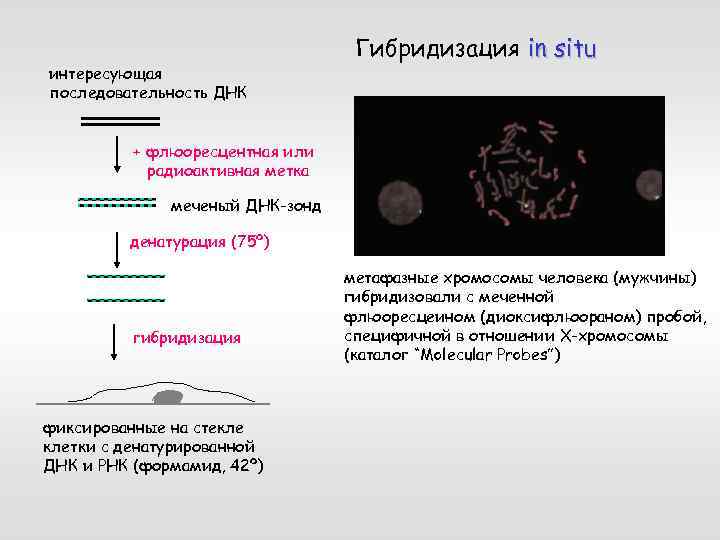
интересующая последовательность ДНК Гибридизация in situ + флюоресцентная или радиоактивная метка меченый ДНК-зонд денатурация (75º) гибридизация фиксированные на стекле клетки с денатурированной ДНК и РНК (формамид, 42º) метафазные хромосомы человека (мужчины) гибридизовали с меченной флюоресцеином (диоксифлюораном) пробой, специфичной в отношении Х-хромосомы (каталог “Molecular Probes”)
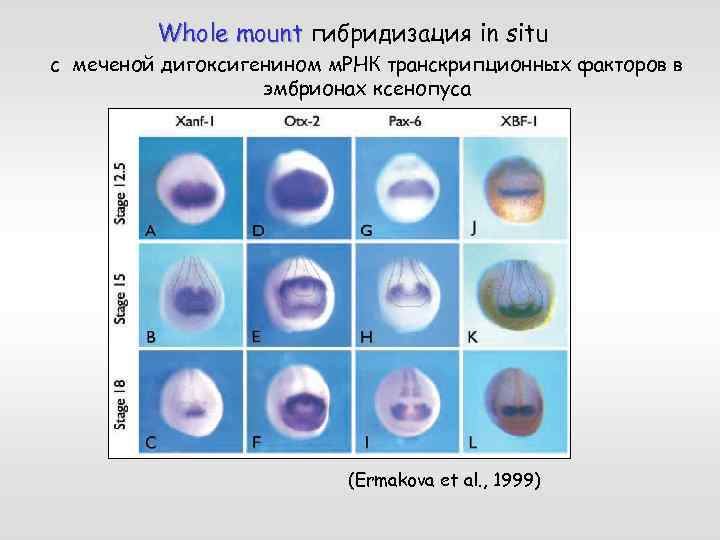
Whole mount гибридизация in situ с меченой дигоксигенином м. РНК транскрипционных факторов в эмбрионах ксенопуса (Ermakova et al. , 1999)
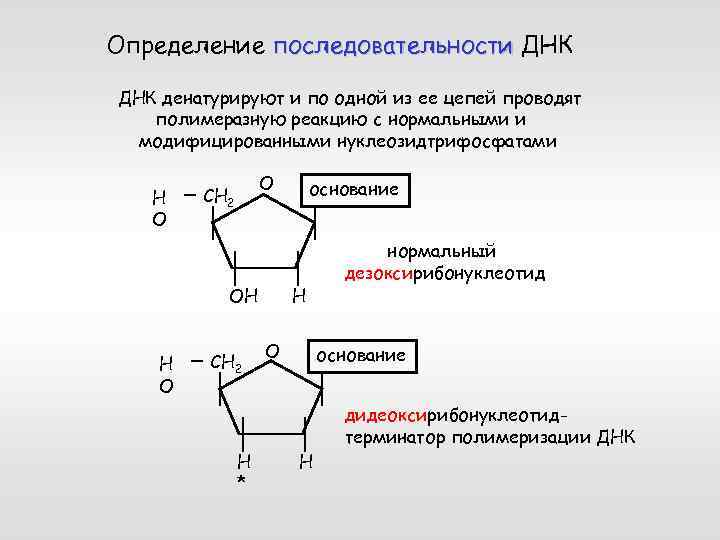
Определение последовательности ДНК денатурируют и по одной из ее цепей проводят полимеразную реакцию с нормальными и модифицированными нуклеозидтрифосфатами Н О О СН 2 ОН Н О СН 2 основание Н О нормальный дезоксирибонуклеотид основание дидеоксирибонуклеотидтерминатор полимеризации ДНК Н * Н
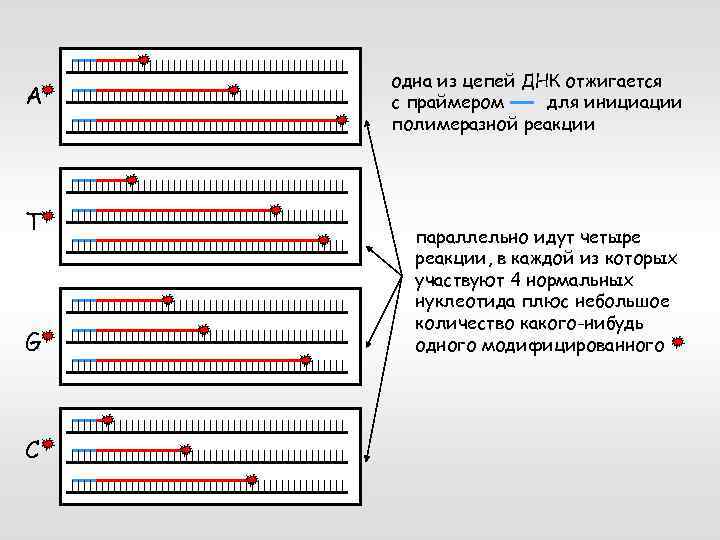
A T G C одна из цепей ДНК отжигается с праймером для инициации полимеразной реакции параллельно идут четыре реакции, в каждой из которых участвуют 4 нормальных нуклеотида плюс небольшое количество какого-нибудь одного модифицированного
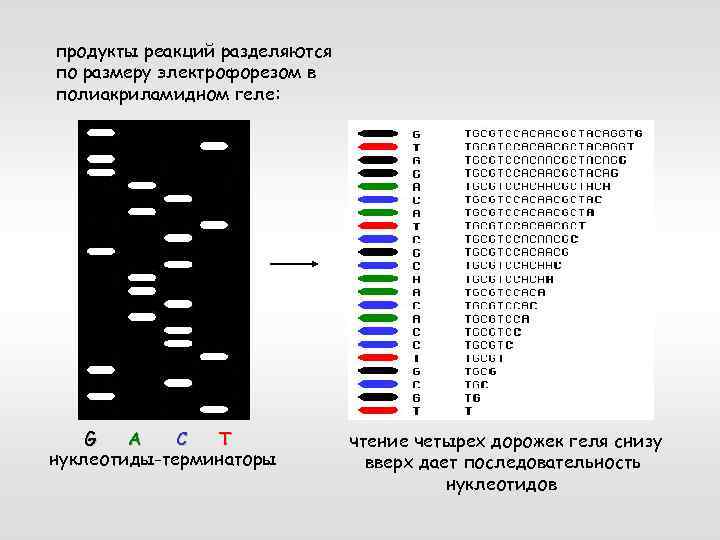
продукты реакций разделяются по размеру электрофорезом в полиакриламидном геле: G A C T нуклеотиды-терминаторы чтение четырех дорожек геля снизу вверх дает последовательность нуклеотидов

Определение последовательности ДНК Пиросеквенирование. 454 Life Science Одноцепочечную матрицу ДНК отжигают с праймером, затем инкубируют с ферментами ДНК-полимеразой, АТР-сульфурилазой, люциферазой и апиразой, а также с субстратами: аденозин-5’фосфосульфатом (APS) и люциферином. Каждый случай включения комплементарного нуклеотида сопровождается высвобождением пирофосфата (PPi) в эквимолярном количестве.
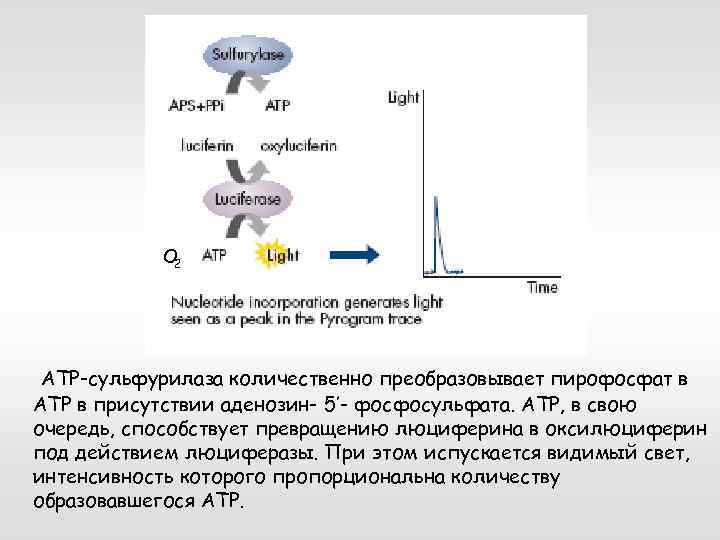
О 2 ATP-сульфурилаза количественно преобразовывает пирофосфат в ATP в присутствии аденозин- 5’- фосфосульфата. ATP, в свою очередь, способствует превращению люциферина в оксилюциферин под действием люциферазы. При этом испускается видимый свет, интенсивность которого пропорциональна количеству образовавшегося ATP.
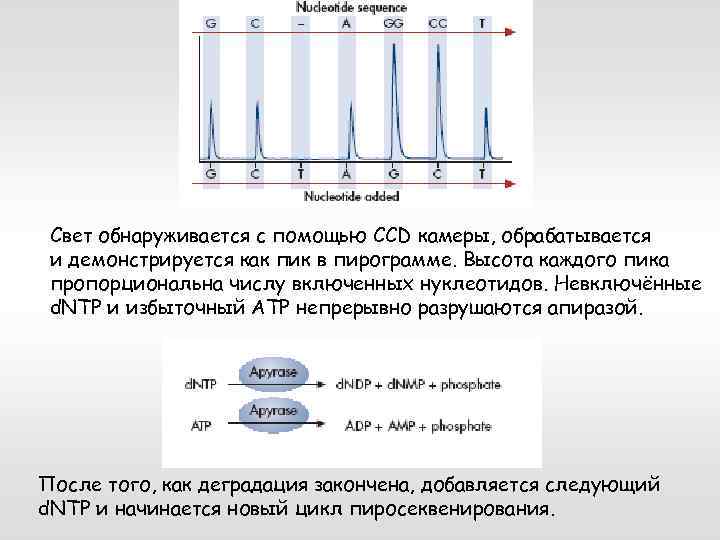
Свет обнаруживается с помощью CCD камеры, обрабатывается и демонстрируется как пик в пирограмме. Высота каждого пика пропорциональна числу включенных нуклеотидов. Невключённые d. NTP и избыточный ATP непрерывно разрушаются апиразой. После того, как деградация закончена, добавляется следующий d. NTP и начинается новый цикл пиросеквенирования.
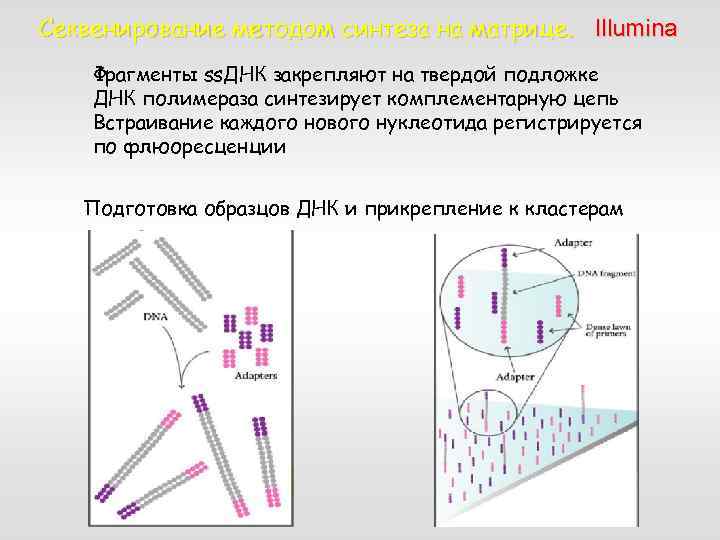
Секвенирование методом синтеза на матрице. Illumina Фрагменты ss. ДНК закрепляют на твердой подложке ДНК полимераза синтезирует комплементарную цепь Встраивание каждого нового нуклеотида регистрируется по флюоресценции Подготовка образцов ДНК и прикрепление к кластерам
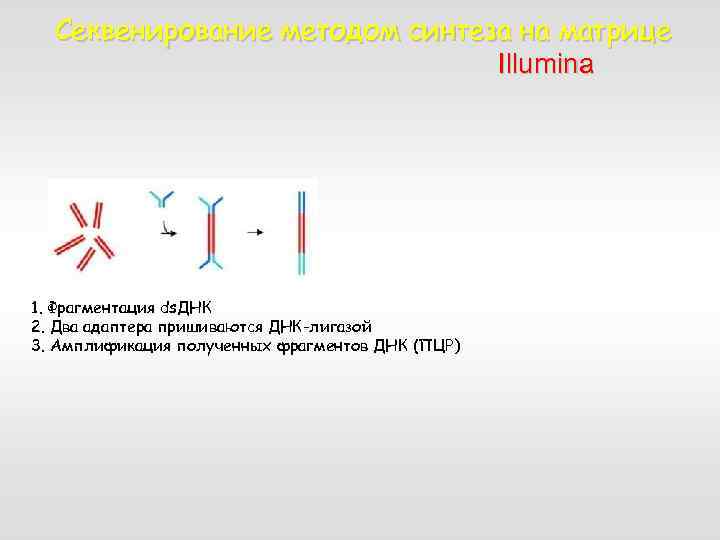
Секвенирование методом синтеза на матрице Illumina 1. Фрагментация ds. ДНК 2. Два адаптера пришиваются ДНК-лигазой 3. Амплификация полученных фрагментов ДНК (ПЦР)
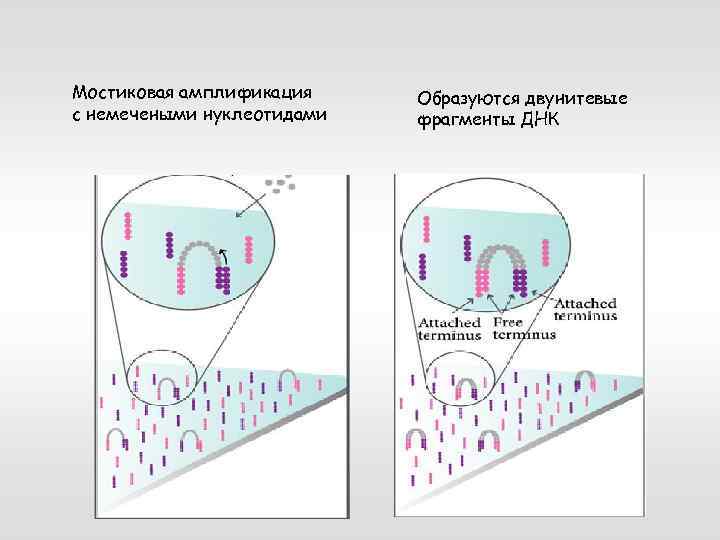
Мостиковая амплификация с немечеными нуклеотидами Образуются двунитевые фрагменты ДНК
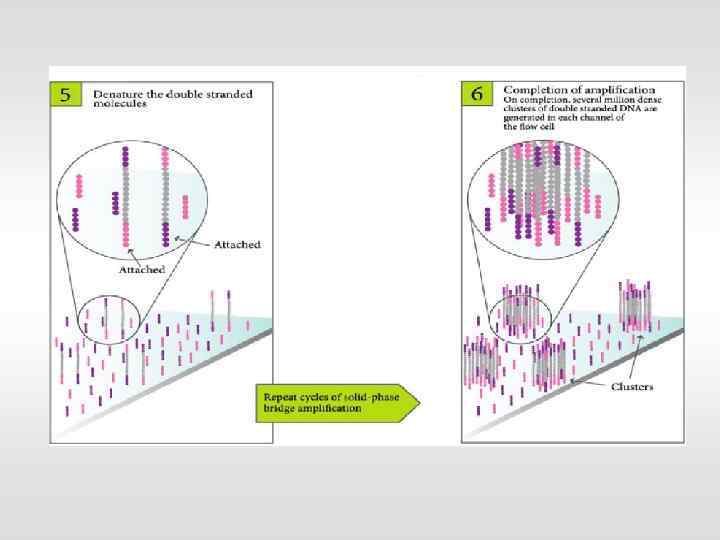
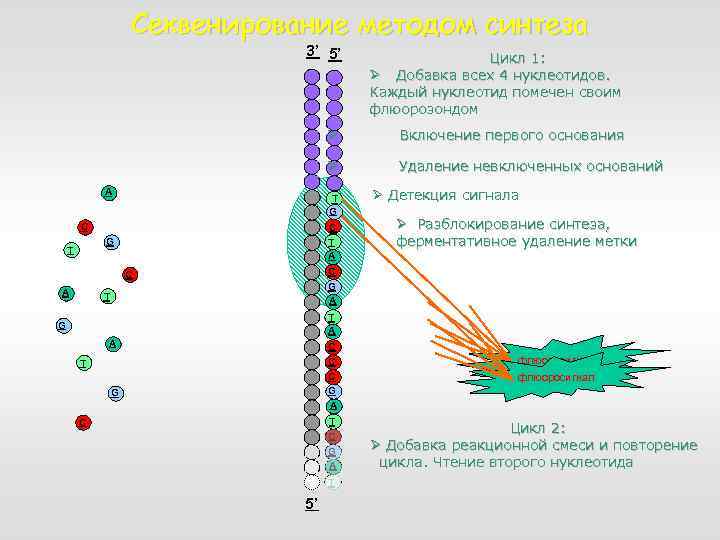
Секвенирование методом синтеза 3’ 5’ Цикл 1: Ø Добавка всех 4 нуклеотидов. Каждый нуклеотид помечен своим флюорозондом Ø Ø A C T A G Ø Детекция сигнала Ø Разблокирование синтеза, ферментативное удаление метки C C A Удаление невключенных оснований T G C T Включение первого основания G A T T A G A C C G флюоросигнал C G A T флюоросигнал T C C G A T 5’ Цикл 2: Ø Добавка реакционной смеси и повторение цикла. Чтение второго нуклеотида
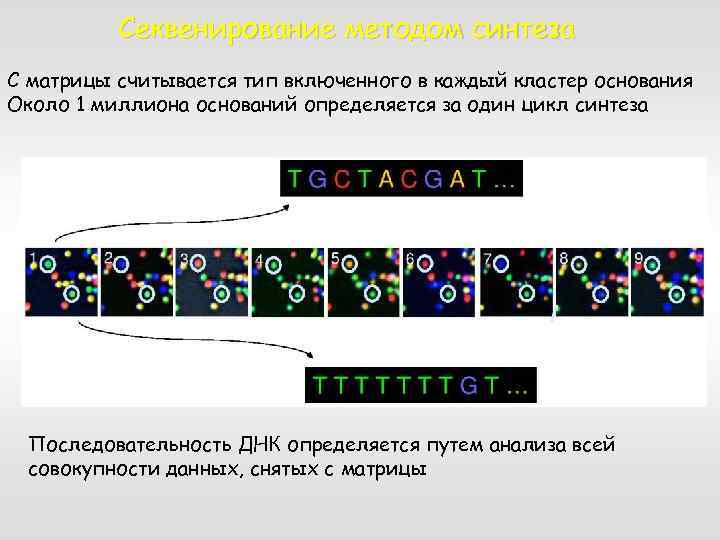
Секвенирование методом синтеза С матрицы считывается тип включенного в каждый кластер основания Около 1 миллиона оснований определяется за один цикл синтеза Последовательность ДНК определяется путем анализа всей совокупности данных, снятых с матрицы
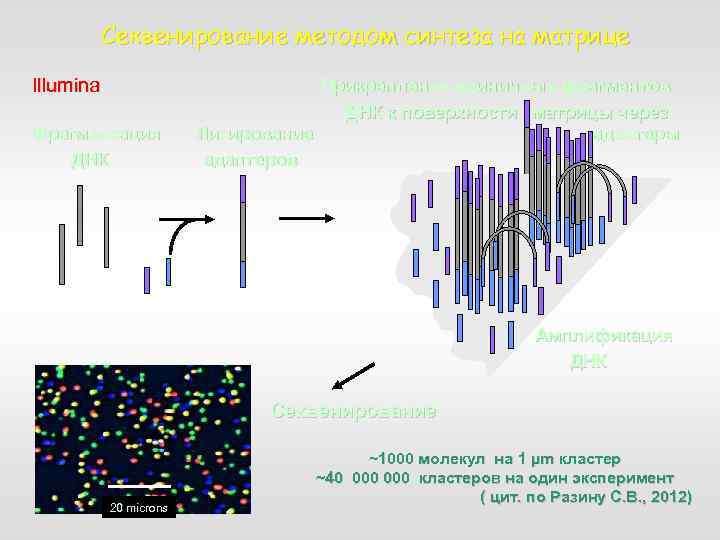
Секвенирование методом синтеза на матрице Illumina Фрагментация ДНК Прикрепление единичных фрагментов ДНК к поверхности матрицы через Лигирование адаптеры адаптеров Амплификация ДНК Секвенирование 20 microns ~1000 молекул на 1 µm кластер ~40 000 кластеров на один эксперимент ( цит. по Разину С. В. , 2012)

Секвенирование методом синтеза на матрице Illumina секвенировала индивидуальный геном африканского мужчины за несколько недель, достигнув скорости прочтения до 3 миллионов оснований за цикл (февраль 2008)

От последовательности нуклеотидов – к предполагаемой последовательности аминокислот Поиск открытой рамки считывания: считывания 5‘-atgcccaagctgaatagcgtagaggggttttcatcatttgaggacgatgtataa-3' 1 atg ccc aag ctg aat agc gta gag ggg ttt tca ttt gag gac gat gta taa M P K L N S V E G F S S F E D D V * 2 tgc cca agc tga ata gcg tag agg ggt ttt cat ttg agg acg atg tat C P S * I A * R G F H H L R T M Y 3 gcc caa gct gaa tag cgt aga ggg gtt ttc att tga gga cga tgt ata A Q A E * R R G V F I I * G R C I В неправильных рамках часто встречаются стоп-кодоны (отмечены красной звездочкой)

Конструирование к. ДНК клонотеки. Этап 1.
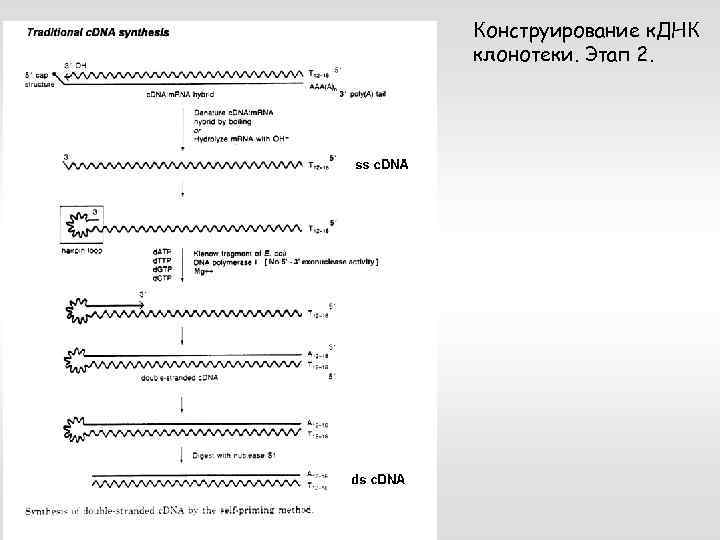
Конструирование к. ДНК клонотеки. Этап 2.
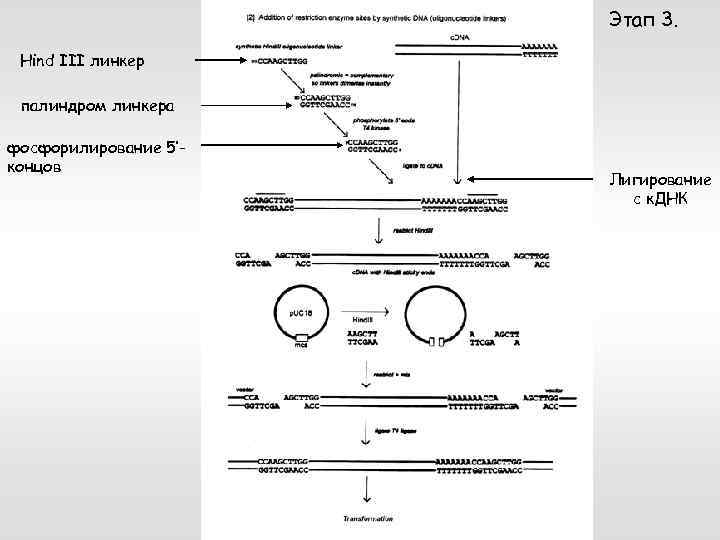
Этап 3. Hind III линкер палиндром линкера фосфорилирование 5’концов Лигирование с к. ДНК
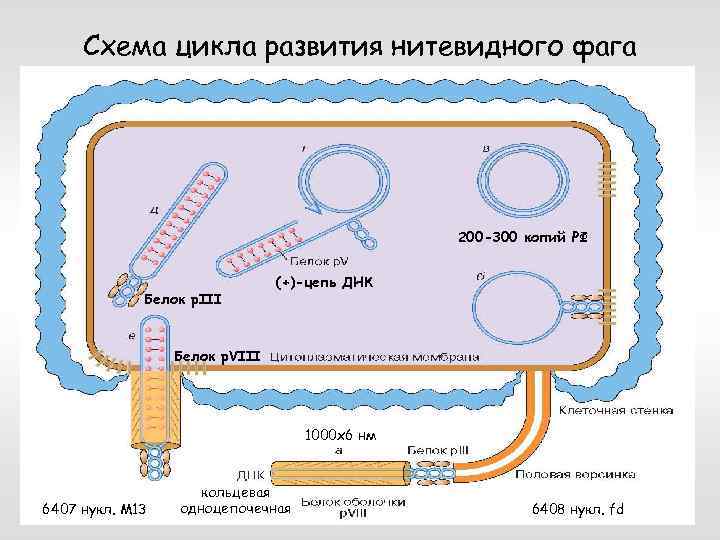
Схема цикла развития нитевидного фага 200 -300 копий РФ Белок р. III (+)-цепь ДНК Белок p. VIII 1000 х6 нм 6407 нукл. М 13 кольцевая одноцепочечная 6408 нукл. fd

Сколько копий плазмиды в клетке? • В зависимости от точки начала репликации (ori) в клетке может содержаться различное число копий плазмиды: • - Низкокопийные (1 -2 копии на клетку) • - Высококопийные (10 -100 копий на клетку)

Литература к курсу «Основы клеточной биологии» • Патрушев Л. И. Экспрессия генов. – М. : Наука, 2000. ил. ISBN 5 -02 -001890 -2 • Свердлов Е. Д. Взгляд на жизнь через окно генома. – М. : Наука, 2009. • А. Ройт, Дж. Бростофф, Д. Мейл. Иммунология. - М. : «Мир» , 2000. • И. Сердюк, Н. Заккаи, Дж. Заккаи. Методы в молекулярной биофизике. Учебное пособие. Том I. М. : КДУ (Книжный Дом Университет), 2009. • ПЦР «в реальном времени» . Под редакцией д. б. н. Д. В. Ребрикова. - М. : БИНОМ. Лаборатория знаний. 2009. • Оригинальные статьи.
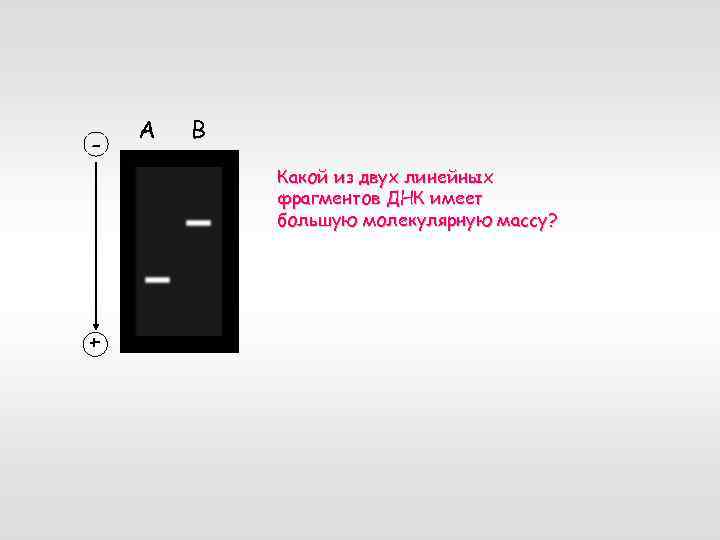
- А B Какой из двух линейных фрагментов ДНК имеет большую молекулярную массу? +
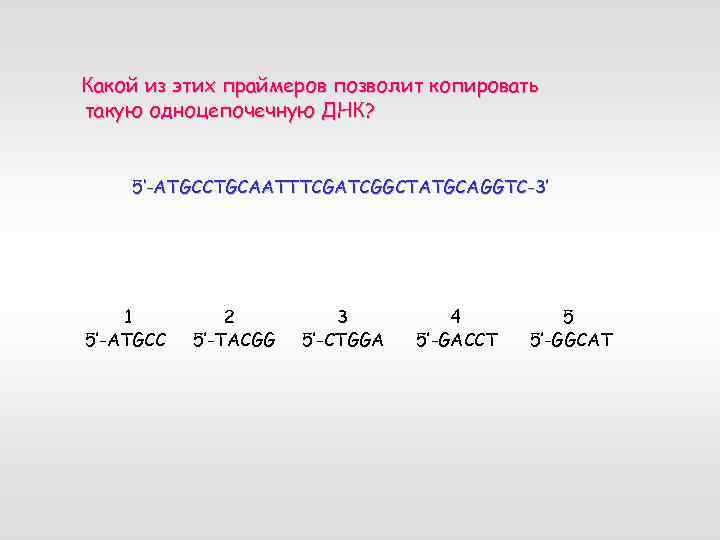
Какой из этих праймеров позволит копировать такую одноцепочечную ДНК? 5‘-ATGCCTGCAATTTCGATCGGCTATGCAGGTC-3’ 1 5’-ATGCC 2 5’-TACGG 3 5’-CTGGA 4 5’-GACCT 5 5’-GGCAT

Зачем и каким образом используют PCR в: - диагностике? - генетическом анализе в медицине? - криминалистике и судебной медицине? - палеонтологии?
Лекция 1_2016. Технология рекомбинантных ДНК.ppt