1.Комплексные соединения.pptx
- Количество слайдов: 17

Лекция 1 Тема Комплексные соединения Екатеринбург 2017

Составитель: К. т. н. , доцент Габдуллин Альфред Нафитович

Основные понятия • Комплексные (координационные) соединения (КС) состоят из центрального атома или иона металла (d- и f-металлы, щелочно-земельные металлы) ─ комплексообразователя (КО), • который окружают анионы и полярные или легко поляризующиеся нейтральные молекулы ─ лиганды (Л). • КО и Л образуют внутреннюю сферу и записываются в квадратных скобках. • Остальные ионы образуют внешнюю сферу. [Cu(H 2 O)5]SO 4

• Координационное число (К. Ч. ) ─ количество лигандов, связанных с центральным атомом во внутренней сфере (К. Ч. = 1─12). • Значение К. Ч. числа зависит: üОт химической природы КО; üОт заряда КО: чем выше его заряд, тем выше К. Ч. Например, [Pt 2+(NH 3)4]2+, [Pt 4+(NH 3)6]4+ üОт химической природы Л; üСоотношения радиусов КО и Л.

Природа связи в координационных соединениях • КС образуются благодаря донорно-акцепторным связям. • Лиганд ─ донор электронных пар. Это анионы (Cl─, S 2─, NO 2─ и т. д. ) и легко поляризующиеся (этилендиамин и др. ) или полярные молекулы (NH 3, CO, NO и др. ), имеющие электроны на внешней электронной оболочке. • Комплексообразователь ─ акцептор, должен иметь в своей электронной структуре свободные ячейки.
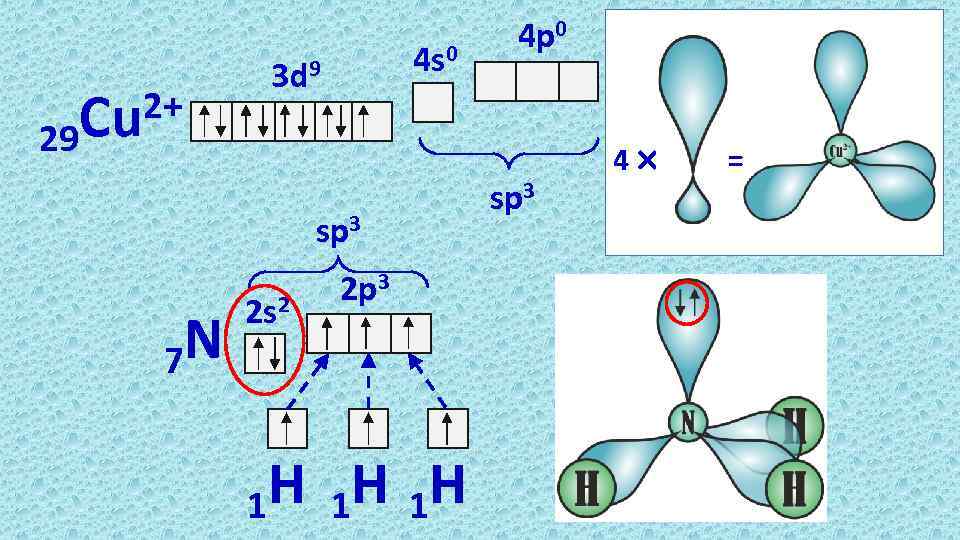
29 2+ Cu 4 s 0 3 d 9 sp 3 N 7 2 s 2 2 p 3 H 1 H 1 H 1 4 p 0 sp 3 4× =
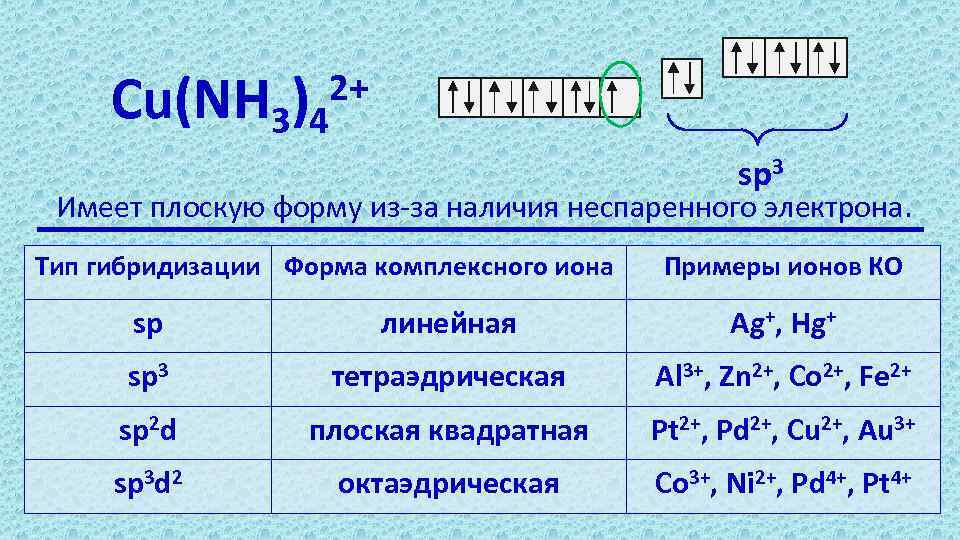
Cu(NH 3)4 2+ sp 3 Имеет плоскую форму из-за наличия неспаренного электрона. Тип гибридизации Форма комплексного иона Примеры ионов КО sp линейная Ag+, Hg+ sp 3 тетраэдрическая Al 3+, Zn 2+, Co 2+, Fe 2+ sp 2 d плоская квадратная Pt 2+, Pd 2+, Cu 2+, Au 3+ sp 3 d 2 октаэдрическая Co 3+, Ni 2+, Pd 4+, Pt 4+
![Номенклатура • Традиционные названия: ü [Pt(NH 3)4][Pt. Cl 4] – соль Магнуса ü K Номенклатура • Традиционные названия: ü [Pt(NH 3)4][Pt. Cl 4] – соль Магнуса ü K](https://present5.com/presentation/1/29580377_447005501.pdf-img/29580377_447005501.pdf-8.jpg)
Номенклатура • Традиционные названия: ü [Pt(NH 3)4][Pt. Cl 4] – соль Магнуса ü K 3[Fe(CN)6] – красная кровяная соль ü цис-[Pt(NH 3)2 Cl 2] – соль Пейроне • Название по ИЮПАК: Na[Ag(CN)2] – дицианоаргентат (I) натрия K 2[Pt. Cl 4] – тетрахлороплатинат (IV) калия K 3[Ga. F 6] – гексафторогаллат (III) калия [Cu(NH 3)4]SO 4 – сульфат тетрааминмеди (II) ИЮПАК — Международный союз теоретической и прикладной химии (ИЮПАК, англ. International Union of Pure and Applied Chemistry, IUPAC) международная неправительственная организация, способствующая прогрессу в области химии.

Правила записи формул комплексов • На первом месте записывается КО, затем Л • Если в комплексе несколько лигандов, то они записываются: ü По мере уменьшения заряда: [M(L+)X(L 0)Y(L─)Z]; ü При равенстве зарядов учитывается место элементов в Периодической системе; ü По мере усложнения лиганда В зависимости от природы лигандов различают: • Аквакомплексы: [Cu(H 2 O)5]SO 4, [Cr(H 2 O)6]Cl 3 и т. д. ; • Амминокомплексы: [Cu(NH 3)2]Cl, [Zn(NH 3)4]Cl 2 и т. д. ; • Гидроксокомплексы: K 2[Zn(OH)4], Na[Al(OH)4] и т. д. ; • Ацидокомплексы: K 4[Fe(CN)6], K 2[Hg. I 4] и т. д. ; • Комплексы смешанного типа: [Co(NH 3)4 Cl 2]Cl, [Pt(NH 3)4(H 2 O)2]Cl 4 и т. д.
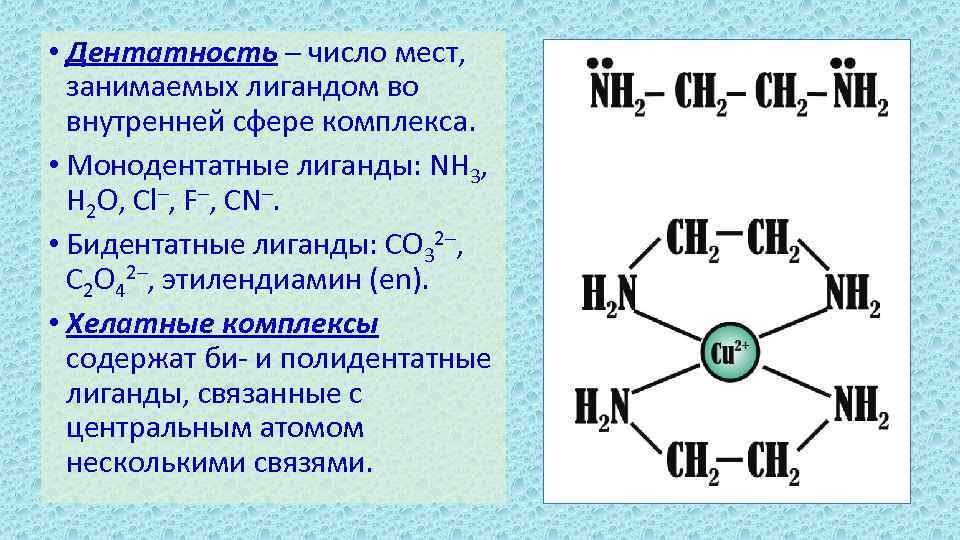
• Дентатность ─ число мест, занимаемых лигандом во внутренней сфере комплекса. • Монодентатные лиганды: NH 3, H 2 O, Cl─, F─, CN─. • Бидентатные лиганды: CO 32─, C 2 O 42─, этилендиамин (en). • Хелатные комплексы содержат би- и полидентатные лиганды, связанные с центральным атомом несколькими связями.
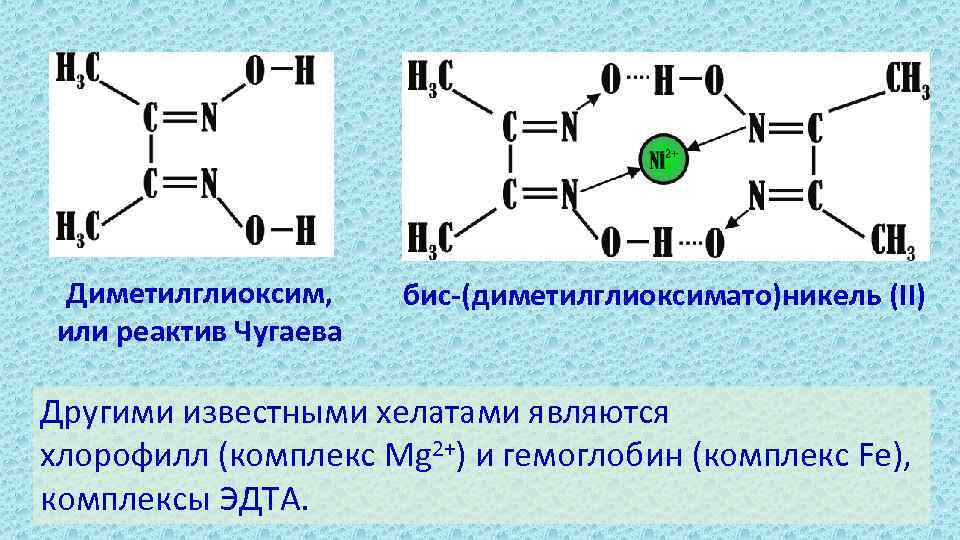
Диметилглиоксим, или реактив Чугаева бис-(диметилглиоксимато)никель (II) Другими известными хелатами являются хлорофилл (комплекс Mg 2+) и гемоглобин (комплекс Fe), комплексы ЭДТА.
![Диссоциация комплексов. Константа нестойкости Первичная диссоциация • [Co(NH 3)6]Cl 2 = [Co(NH 3)6]2+ + Диссоциация комплексов. Константа нестойкости Первичная диссоциация • [Co(NH 3)6]Cl 2 = [Co(NH 3)6]2+ +](https://present5.com/presentation/1/29580377_447005501.pdf-img/29580377_447005501.pdf-12.jpg)
Диссоциация комплексов. Константа нестойкости Первичная диссоциация • [Co(NH 3)6]Cl 2 = [Co(NH 3)6]2+ + 2 Cl─ Вторичная диссоциация • [Co(NH 3)6]2+ [Co(NH 3)5]2+ + NH 3 • [Co(NH 3)5]2+ [Co(NH 3)4]2+ + NH 3 • [Co(NH 3)4]2+ [Co(NH 3)3]2+ + NH 3 • [Co(NH 3)3]2+ [Co(NH 3)2]2+ + NH 3 • [Co(NH 3)2]2+ [Co(NH 3)]2+ + NH 3 • [Co(NH 3)]2+ Co 2+ + NH 3 Суммарное уравнение Σ [Co(NH 3)6]2+ Co 2+ + 6 NH 3

•

Реакции с участием комплексных соединений 1. Реакции ионного обмена +OH− − H 2 O [Cr(H 2 O)6]3+ [Cr(H 2 O)5(OH)]2+ +OH− 2 2 2 [Cr(H 2 O)4(OH)2]+− [Cr(H 2 O)3(OH)3] O −H O HO −H +OH− [Cr(H 2 O)2(OH)4 −H O 2 ─ ]
![Реакции с участием комплексных соединений • [Fe(H 2 O)6]3+ + 4 SCN─ ⇄ [Fe Реакции с участием комплексных соединений • [Fe(H 2 O)6]3+ + 4 SCN─ ⇄ [Fe](https://present5.com/presentation/1/29580377_447005501.pdf-img/29580377_447005501.pdf-15.jpg)
Реакции с участием комплексных соединений • [Fe(H 2 O)6]3+ + 4 SCN─ ⇄ [Fe (H 2 O)2(SCN)4]─ • Cu. O + 4 NH 4 OH(конц. ) = [Cu(NH 3)4](OH)2 Cu. O + 4 NH 4 OH(конц. ) ⟶ [Cu(NH 3)4] 2─ + 2 OH─ • Hg. I 2↓ + 2 KI = K 2[Hg. I 4] Hg. I 2 + 2 K+ + 2 I─ = 2 K+ + [Hg. I 4]2─ Hg. I 2 + 2 I─ = [Hg. I 4]2─ ПРHg. I 2 =4· 10─12 KH = 2, 48· 10─30

Реакции с участием комплексных соединений Co. Cl 2 + K 2[Hg(SCN)4 = Co[Hg(SCN)4↓ + 2 KCl Zn. Cl 2 + K 2[Hg(SCN)4 = Zn[Hg(SCN)4↓ + 2 KCl 3. Разрушение комплексов üСвязывание иона комплексообразователя K 2[Hg. I 4] + K 2 S = Hg. S + 4 KI KH = 2, 48· 10─30 ПРHg. S = 4· 10─53 üСвязывание лиганда [Zn(NH 3)2]Cl 2 + 2 HCl = Zn. Cl 2 + 2 NH 4 Cl Co[Hg(SCN)4] Zn[Hg(SCN)4]
![Реакции с участием комплексных соединений • 4. Гидролиз [Fe(H 2 O)6]3+ [Fe (H 2 Реакции с участием комплексных соединений • 4. Гидролиз [Fe(H 2 O)6]3+ [Fe (H 2](https://present5.com/presentation/1/29580377_447005501.pdf-img/29580377_447005501.pdf-17.jpg)
Реакции с участием комплексных соединений • 4. Гидролиз [Fe(H 2 O)6]3+ [Fe (H 2 O)5(OH─)]2+ + H+ (первая ступень) • 5. Окислительно-восстановительные реакции üЦианирование золота: 4 Au + 8 KCN + 2 H 2 O + O 2 = 4 K[Au(CN)4] + 4 KOH üЦементация: τ, кат. 2 K[Au(CN)4] + Zn = K 2[Zn(CN)4] + 2 Au 4[Co(NH 3)6]Cl 2 + 2 H 2 O + O 2 → 4[Co(NH 3)6]Cl 2(OH)2
1.Комплексные соединения.pptx