
Лекция 1. • • Предмет биохимии История развития науки Разделы биохимии Экологическая биохимия

Литература • • Литература основная Кольман Я. , Рем К. -Г. «Наглядная биохимия» . М. 2004. Харборн Дж. «Введение в экологическую биохимию» . М. 1985. Ленинджер А. «Основы биохимии» . 1, 2, 3 тт. М. 1985 Страйер Л. «Биохимия» . 1, 2, 3 тт. М. 1984 -1986 Литература дополнительная • Саловарова В. П. , Приставка А. А. , Берсенева О. А. Введение в биохимическую экологию. Иркутск. Изд-во ИГУ. 2007 • М. М. Телитченко, С. А. , Остроумов С. А. Введение в проблемы биохимической экологии. М. Наука. 1990.

Биохимия изучает химизм процессов, протекающих в живой природе. Предмет биохимии – живые системы – организмы: от бактерий до растений и животных, включая вирусы. Семейство биохимических наук По объекту: • Биохимия животных • Биохимия растений • Биохимия микроорганизмов • Биохимия насекомых, водорослей, грибов и т. д. Биохимия белков (протеомика) Биохимия целлюлозы Биохимия липидов (липидология) Биохимия нуклеиновых кислот и т. д. Аспект проблемы • Техническая биохимия, физическая биохимия • Биотехнология • Экологическая биохимия

Экологическая биохимия - новое междисциплинарное направление исследований (химическая экология, фитохимическая экология, биохимическая экология) – исследование основ взаимодействий (взаимоотношений) между живыми организмами, живыми организмами и окружающей средой, опосредованные химическими соединениями. Основные направления - изучение продуктов вторичного метаболизма (алкалоиды, флавоноиды, терпеноиды) животных, растений и микроорганизмов - участие вторичных метаболитов во взаимодействиях природных систем: животное – животное, растение – растение, животное – растение и т. д. и т. п. - биохимические адаптации живых организмов к окружающей среде(климат, почва, загрязнение и т. д. ) - биохимический ответ на стресс, окислительный стресс - разложение ксенобиотиков в окружающей среде, воздействие продуктов их деградации на живые организмы

Что такое любовь? Дофамин Исследование, поиск новизны, рискованное поведение, любопытство, спонтанность «Исследователь» Серотонин Социальность, спокойствие, лояльность, уважение традиций социума «Строитель» Тестостерон Прямота, решительность, состязательность, амбициозность, аналитичность «Начальник» Эстроген Вербальность, умение управлять людьми, общаться «Дипломат»

Принцип биохимического единства Все организмы состоят из одних и тех же соединений примерно в одинаковых пропорциях и эти соединения выполняют вполне определенные общие для всей живой природы функции. Биомолекулы: белки нуклеиновые кислоты углеводы липиды
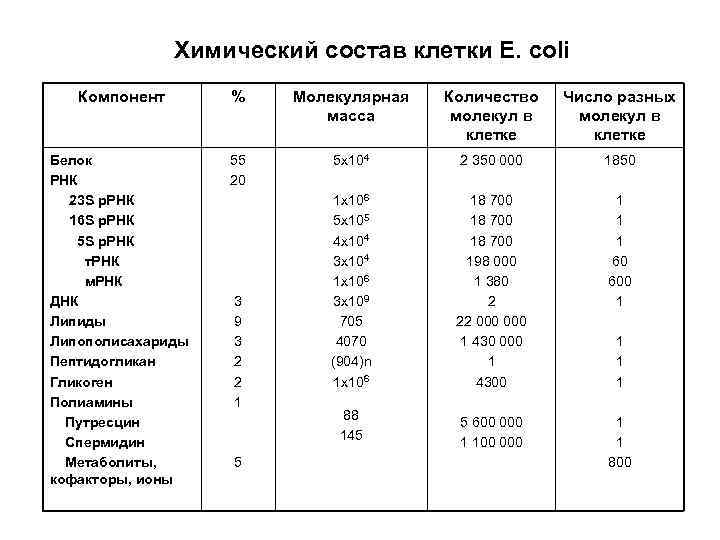
Химический состав клетки E. coli Компонент % Молекулярная масса Количество молекул в клетке Число разных молекул в клетке Белок РНК 23 S р. РНК 16 S р. РНК 5 S р. РНК т. РНК м. РНК ДНК Липиды Липополисахариды Пептидогликан Гликоген Полиамины Путресцин Спермидин Метаболиты, кофакторы, ионы 55 20 5 х104 2 350 000 1850 1 х106 5 х105 4 х104 3 х104 1 х106 3 х109 705 4070 (904)n 1 х106 18 700 198 000 1 380 2 22 000 1 4300 1 1 1 60 600 1 88 145 5 600 000 1 1 800 3 9 3 2 2 1 5 1 1 1

Химический состав клетки (усредненные данные) Состав живых клеток (% от сух. вещества) Углерод 50 -60 Водород 3 -4 Азот 8 -10 Кислород 25 -30 Биогенные элементы (биоэлементы) Макроэлементы ( более 0. 01%) Основные элементы, входящие в состав органического вещества (5 – 60%) Углерод C Азот N Водород H Фосфор P Кислород O Сера S Элементы, встречающиеся в виде ионов ( до 4 -5%) Натрий Na Кальций Ca Калий K Хлор Cl Магний Mg ( Железо Fe) Микроэлементы (0. 00001 – 0. 01%) Железо Fe Медь Cu Никель Ni Олово Sn Цинк Zn Йод J Хром Cr Бор B Марганец Mn Молибден Mo Фтор F Мышьяк As Кобальт Co Ванадий Va Селен Se Ультрамикроэлементы (менее 0. 00001%) Eu, Lu, Tb, Yb

Физиологическая роль некоторых элементов в организме человека • Эссенциальные (жизненно-необходимые): Ca, Co, Cr, Cu, Fe, K, Mg, Mn, Mo, Na, Se, Zn • Условно-эссенциальные (жизненно-важные, но вредные в определенных концентрациях): As, B, Li, Ni, Si, V • Потенциально-токсичные: Ag, Sn, Sc, Te, Ti • Токсичные: Al, Ba, Cd, Pb, Sb, Hg • Малоизученные или с неустановленной ролью – остальные элементы системы Менделеева

Роль некоторых элементов в клетке • • • Na, K – стабильность мембран Mg – хлорофилл Ca – амилазы, костные ткани Fe – гем, пероксидаза, каталаза Cu – цитохромы, оксигеназы Mn - аргиназа Co – витамин В 12 Mo, V – нитрогеназы Ni – фенолоксидаза

Вода – основная часть цитозоля (цитоплазмы) • • Вода свободная – среда, где протекают химические процессы, участие в окислительно-восстановительных реакциях (образование и потребление энергии) Вода связанная входит в состав биомолекул, образует коллоидные растворы, гидратирует ионы • Вода обладает уникальными свойствами: низкая температура замерзания и высокая температура кипения прекрасный биорастворитель – молекула воды – диполь, молекулы воды могут взаимодействовать за счет естественного притяжения одного конца диполя к другому – «кластерные структуры» лучший растворитель, чем большинство известных жидкостей – растворяет кристаллические вещества, растворяет вещества, содержащие полярные группы, растворяет вещества, содержащие гидрофобные и гидрофильные группы
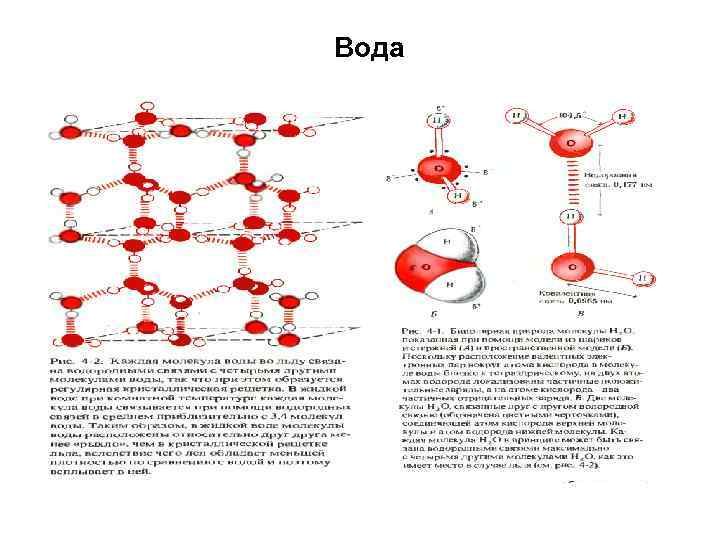
Вода

Лекция 2. Белки и аминокислоты - CO – NH C, O, N, H, P, S Качественные (цветные) реакции на белок • Биуретовая: Cu. SO 4 в щелочном растворе + белок → фиолетовожелтое окрашивание • Ксантопротеиновая: HNO 3(конц. ) + белок → желтое окрашивание (бензолные кольца: фенилаланин, тирозин) • Реакция Миллона: Hg. NO 3 ( в HNO 3) в присутствии HNO 2 + белок → красное окрашивание (тирозин) • Реакция Сакагучи: альфа-нафтол + гипохлорит + белок → красное окрашивание (аргинин) • Реакция Эрлиха: пара-диметиламинобензальдегид + белок → красное окрашивание (триптофан) • Реакция Паули: диазобензолсульфокислота + белок в щелочной среде → красное окрашивание (гистидин, тирозин)
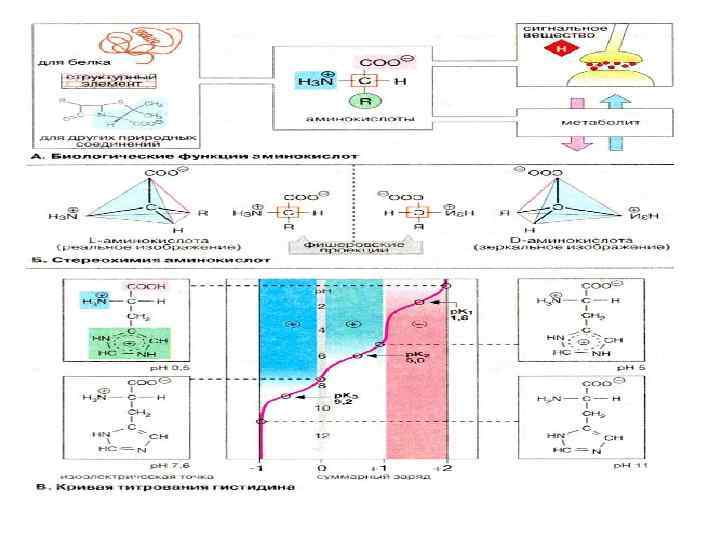
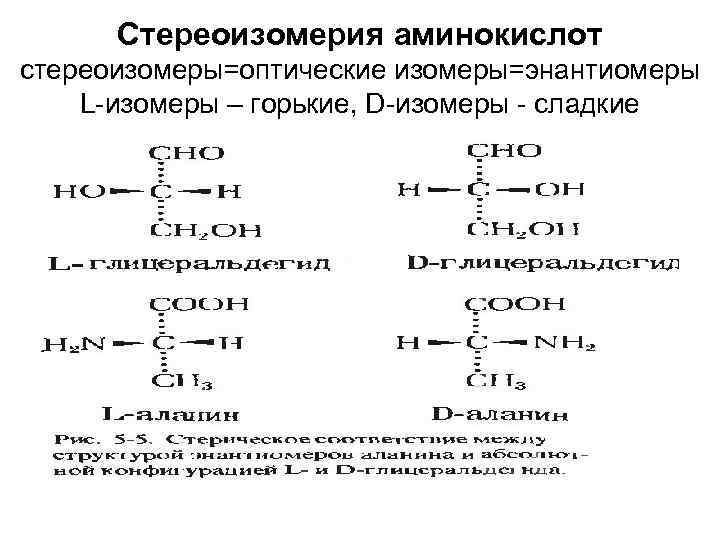
Стереоизомерия аминокислот стереоизомеры=оптические изомеры=энантиомеры L-изомеры – горькие, D-изомеры - сладкие
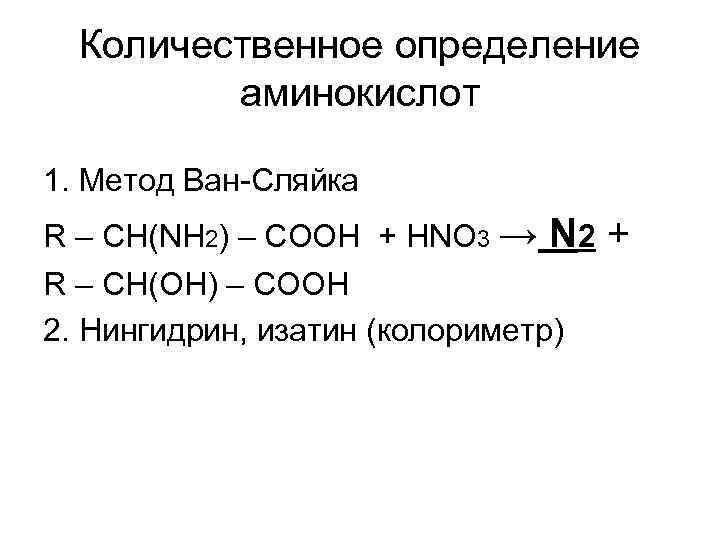
Количественное определение аминокислот 1. Метод Ван-Сляйка R – CH(NH 2) – COOH + HNO 3 → N 2 + R – CH(OH) – COOH 2. Нингидрин, изатин (колориметр)
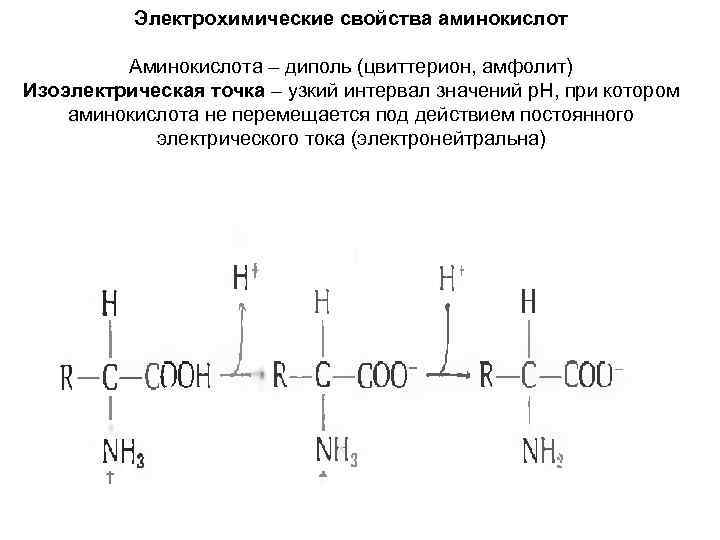
Электрохимические свойства аминокислот Аминокислота – диполь (цвиттерион, амфолит) Изоэлектрическая точка – узкий интервал значений р. Н, при котором аминокислота не перемещается под действием постоянного электрического тока (электронейтральна)

Классификация аминокислот в соответствии с полярностью R-группы при нейтральной реакции среды • • Неполярные R-группы: аланин, валин, изолейцин, метионин, пролин, триптофан, фенилаланин Полярные, но незаряженные R-группы: аспарагин, глицин, глутамин, серин, тирозин, треонин, цистеин. Отрицательно заряженные R-группы: аспарагиновая кислота, глутаминовая кислота. Положительно заряженные R-группы: аргинин (гуанидиновая группа), гистидин (имидазольное кольцо), лизин

Классификация аминокислот, основанная на присутствии и количестве функциональных групп (амино, амидо, карбокси, окси и некоторых других) Алифатические: моноаминомонокарбоновые: глицин, аланин, лейцин, изолейцин, валин, оксимоноаминомонокарбоновые: серин, треонин, моноаминодикарбоновые: аспарагиновая, глутаминовая, амиды моноаминодикарбоновых: аспарагин, глутамин диаминомонокарбоновые: гистидин, аргинин, лизин, cеросодержащие: цистеин, цистин, метионин. • • • Ароматические: фенилаланин, тирозин, триптофан Гетероциклические: триптофан, гистидин, пролин Иминокислоты: пролин
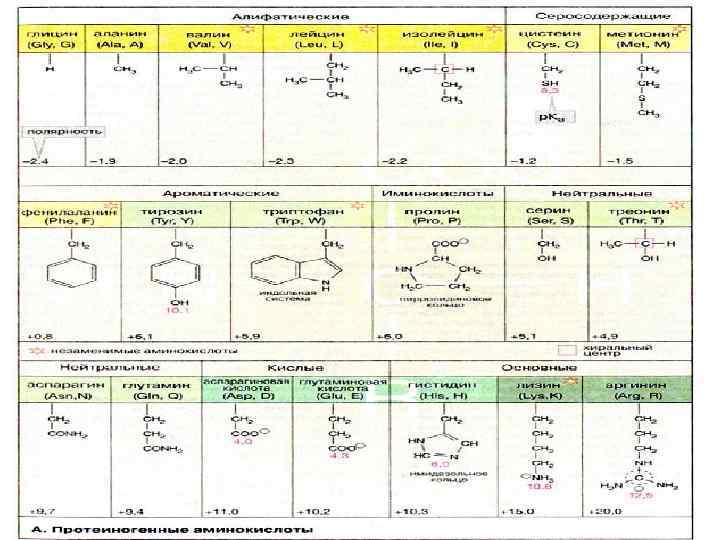

Лекция 2. Аминокислоты (продолжение) Классификация на основе питательной ценности (для человека) • Незаменимые: треонин, метионин, валин, лейцин, изолейцин, фенилаланин, триптофан, лизин, • Заменимые: глицин, аланин, серин, цистеин, аспарагиновая, глутаминовая, аспарагин, глутамин, тирозин, пролин. аргинин, гистидин 1. Природные (протеиногенные)- входят в состав белка 2. Неприродные (непротеиногенные) – не входят в состав белка
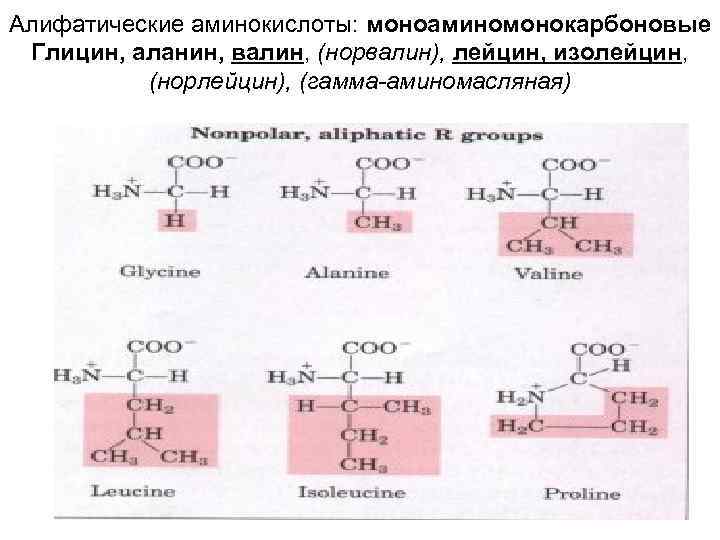
Алифатические аминокислоты: моноаминомонокарбоновые Глицин, аланин, валин, (норвалин), лейцин, изолейцин, (норлейцин), (гамма-аминомасляная)

Функции гидрофобных радикалов • Участие в формировании пространственной структуры белка – стабилизация глобулярной структуры белка: гидрофобная часть аминокислоты направлена внутрь глобулы, гидрофильная – наружу • При взаимодействии белков с липидами в мембранах гидрофобные радикалы аминокислот связаны с гидрофобной частью молекулы липида • Разобщение активных радикалов в полипептидной цепи

Алифатические аминокислоты • Оксиаминокислоты Серин, (серин-фосфорная кислота), (гомосерин), треонин
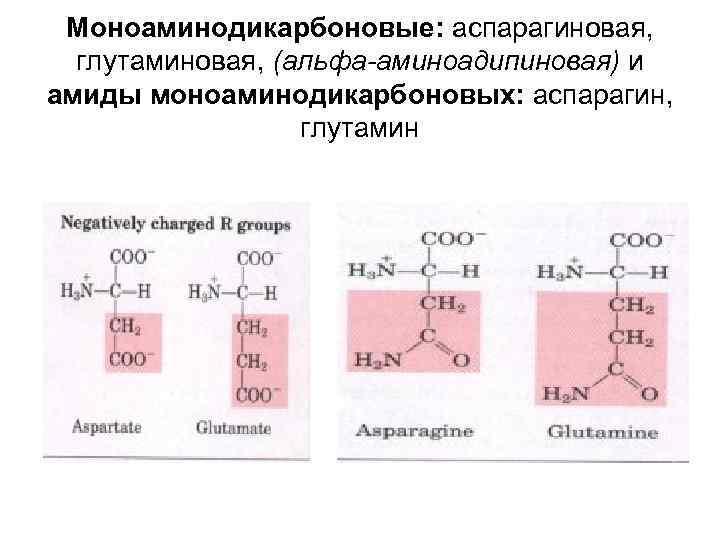
Моноаминодикарбоновые: аспарагиновая, глутаминовая, (альфа-аминоадипиновая) и амиды моноаминодикарбоновых: аспарагин, глутамин

Физиологическая роль дикарбоновых кислот в клетке 1. Участие в реакциях аминирования оксалоацетат+NH 3 →аспартат + (NH 3) →аспарагин 2. Участие в реакциях декарбоксилирования аспарагиновая → альфа-аланин, бета-аланин 3. Участие в реакциях переаминирования (трансаминирования): Глутаминовая +пировиноградная → аланин + альфа -кетоглутаровая

Алифатические Диаминомонокарбоновые: лизин, (диаминопимелиновая), аргинин, (орнитин), гистидин Реакция декарбоксилирования: амины, (полиамины) Серосодержащие: цистеин, (цистин), метионин (цистатионин) Ароматические: фенилаланин, тирозин, триптофан Гетероциклические: триптофан, гистидин, пролин Иминокислоты: пролин

Алифатические Диаминомонокарбоновые: лизин, (диаминопимелиновая), аргинин (гуанидиновая группировка), (орнитин), гистидин (имидазольное кольцо) Реакция декарбоксилирования: амины, (полиамины)

Лизин, аргинин, гистидин – незаменимые аминокислоты • Лизин → кадаверин →пиперидин →…→пиридин (никотинамид, НАД) • Аргинин → орнитин +CO(NH 2)2 → → путресцин Кадаверин, путресцин, спермидин – птомаины – продукты гниения белков Полиамины – галопротекторы (кадаверин, путресцин, спермин, спермидин) – у растений (хрустальная травка). • Диаминопимелиновая (LL-ДАПК и DL- ДАПК), гомолог лизина входит в состав КС пептидогликана бактерий При физиологических значениях р. Н (около 7) имеют положительный заряд, обладают высокой гидрофильностью, располагаются на внешней стороне глобулярных белков

Серосодержащие: цистеин, (цистин), метионин цистатионин – HOOC-CH(NH 2)(CH 2)2 -S-CH 2 CH(NH 2)-COOH
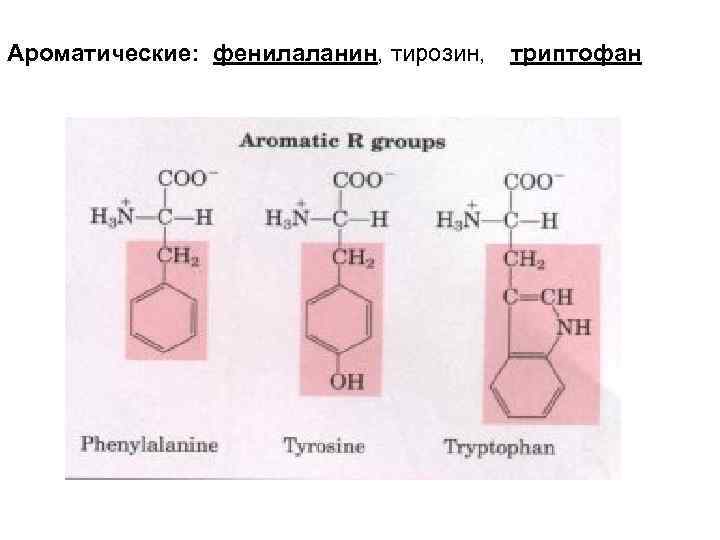
Ароматические: фенилаланин, тирозин, триптофан

Фениналанин →ДОФА →ДОФамин → → адренолин, норадренолин (нейромедиаторы, нейрогормоны) Тирозин + тирозиназа → меланоиды аминокислоты + сахара → меланоиды (реакция Майарда)
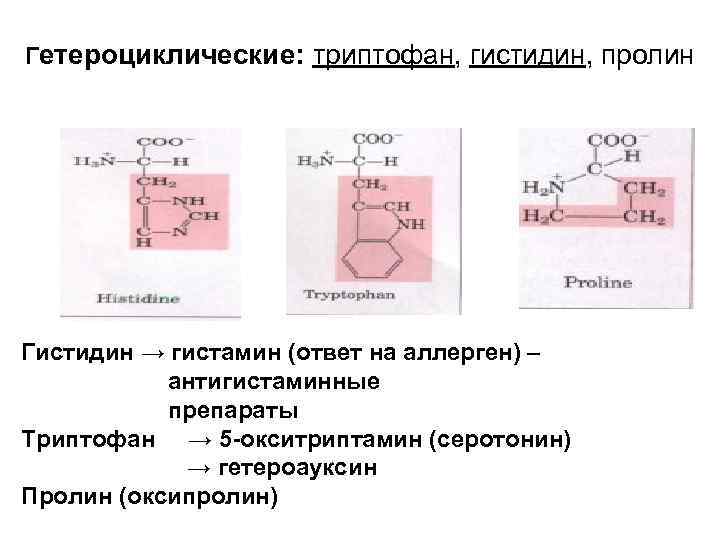
Гетероциклические: триптофан, гистидин, пролин Гистидин → гистамин (ответ на аллерген) – антигистаминные препараты Триптофан → 5 -окситриптамин (серотонин) → гетероауксин Пролин (оксипролин)

Нестандартные аминокислоты • Нестандартные аминокислоты – компоненты лишь некоторых белков и пептидов или находящиеся в значительных количествах в свободном состоянии. Это, как правило, производные 20 стандартных (природных) аминокислот: пролина, лизина, глицина, глутаминовой кислоты • 4 -гидроксипролин, 5 -гидроксилизин входят в состав коллагена (фибриллярный белок), карбоксиглутаминовая – протромбин.
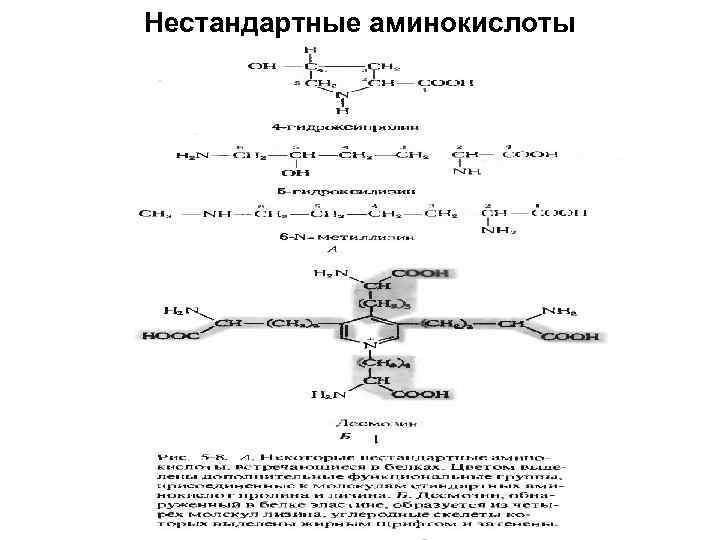
Нестандартные аминокислоты

Нестандартные аминокислоты (продолжение) Пирролизин — природная аминокислота, обнаруженная у некоторых метаногенных архей, входит в состав ферментов метаболизма метана. Пирролизин является производным аминокислоты лизина. Селеноцистеи н — нестандартная аминокиcлота, входящая в состав активного центра фермента глутатионпероксидазы, а также селенопротеинов. Гамма-карбоксиглутаминовая кислота – протромбина (кровь) N-метилглицин (саркозин) – (кератин – мышцы, антибиотики актиномицины) N, N, N- триметилглицин – бетаин – осмопротектор, защищает клетку в условиях повышенного осмотического давления

Классификация аминокислот в соответствии с их полярностью и расположением в молекулах глобулярных белков • • • Высокогидрофильные аминокислоты, расположенные на внешней поверхности молекулы глобулярного белков: аспарагиновая, глютаминовая, аспарагин, глютамин, лизин, аргинин, гистидин. Высокогидрофобные аминокислоты, расположенные внутри молекулы глобулярных белков: фенилаланин, лейцин, изолейцин, метионин, валин, триптофан. Аминокислоты, занимающие по степени полярности промежуточное положение, могут находиться как внутри, так и на поверхности глобулярных белков: пролин, треонин, серин, цистеин, аланин, глицин, тирозин.