Презентации 1 Еремин.pptx
- Количество слайдов: 192
 Лекция 1 Основные понятия и законы химии Еремин Вадим Владимирович, Химический факультет МГУ vadim@educ. chem. msu. ru Физтех, 1 курс. Осень 2015
Лекция 1 Основные понятия и законы химии Еремин Вадим Владимирович, Химический факультет МГУ vadim@educ. chem. msu. ru Физтех, 1 курс. Осень 2015
 1 семестр. Общая и неорганическая химия Всего – 16 лекций Введение – 1 лекция Строение вещества – 4 лекции Теоретическая неорганическая химия – 5 лекций Химия элементов – 5 лекций Химическая кинетика и катализ – 1 лекция Форма аттестации – экзамен Физтех, 1 курс. Осень 2015 2
1 семестр. Общая и неорганическая химия Всего – 16 лекций Введение – 1 лекция Строение вещества – 4 лекции Теоретическая неорганическая химия – 5 лекций Химия элементов – 5 лекций Химическая кинетика и катализ – 1 лекция Форма аттестации – экзамен Физтех, 1 курс. Осень 2015 2
 Литература В 2012 году вышел учебник «Общая и физическая химия» , по сути – Химия для физиков • Еремин В. В. , Борщевский А. Я. Основы общей и физической химии. – М. : Интеллект, 2012. • Глинка Н. Л. Общая химия. Изд. 28 -е. – М. : Интегралпресс, 2000. • Глинка Н. Л. Задачи и упражнения по общей химии. – М. : Интеграл-пресс, 2005. • Ахметов Н. С. Общая и неорганическая химия. Изд. 4 -е. – М. : Высшая школа, Академия, 2001. • Неорганическая химия. В 3 -х тт. / под ред. Третьякова Ю. Д. – М. : Академия, 2004 -2007. Физтех, 1 курс. Осень 2015 3
Литература В 2012 году вышел учебник «Общая и физическая химия» , по сути – Химия для физиков • Еремин В. В. , Борщевский А. Я. Основы общей и физической химии. – М. : Интеллект, 2012. • Глинка Н. Л. Общая химия. Изд. 28 -е. – М. : Интегралпресс, 2000. • Глинка Н. Л. Задачи и упражнения по общей химии. – М. : Интеграл-пресс, 2005. • Ахметов Н. С. Общая и неорганическая химия. Изд. 4 -е. – М. : Высшая школа, Академия, 2001. • Неорганическая химия. В 3 -х тт. / под ред. Третьякова Ю. Д. – М. : Академия, 2004 -2007. Физтех, 1 курс. Осень 2015 3
 Наука Современная наука – способ познания реального мира, включающего в себя как ощущаемую органами чувств человека реальность, так и реальность невидимую, способ познания, основанный на построении проверяемых моделей этой реальности. (Уильям Хетчер) Физтех, 1 курс. Осень 2015 4
Наука Современная наука – способ познания реального мира, включающего в себя как ощущаемую органами чувств человека реальность, так и реальность невидимую, способ познания, основанный на построении проверяемых моделей этой реальности. (Уильям Хетчер) Физтех, 1 курс. Осень 2015 4
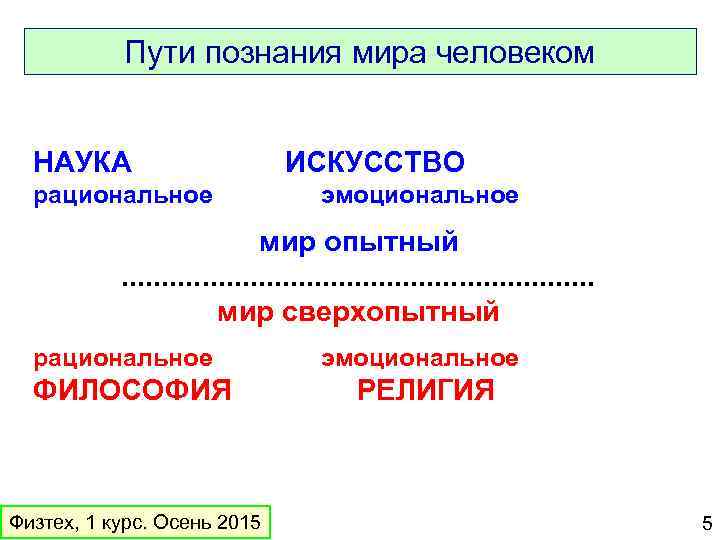 Пути познания мира человеком НАУКА рациональное ИСКУССТВО эмоциональное мир опытный. . . . мир сверхопытный рациональное ФИЛОСОФИЯ Физтех, 1 курс. Осень 2015 эмоциональное РЕЛИГИЯ 5
Пути познания мира человеком НАУКА рациональное ИСКУССТВО эмоциональное мир опытный. . . . мир сверхопытный рациональное ФИЛОСОФИЯ Физтех, 1 курс. Осень 2015 эмоциональное РЕЛИГИЯ 5
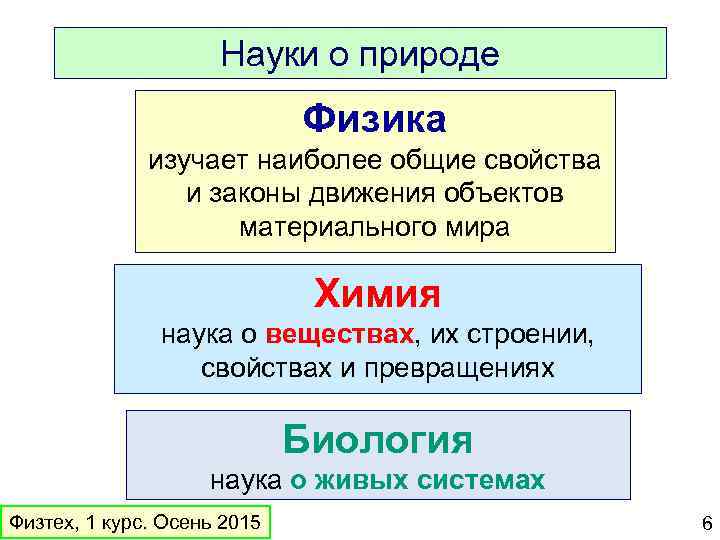 Науки о природе Физика изучает наиболее общие свойства и законы движения объектов материального мира Химия наука о веществах, их строении, свойствах и превращениях Биология наука о живых системах Физтех, 1 курс. Осень 2015 6
Науки о природе Физика изучает наиболее общие свойства и законы движения объектов материального мира Химия наука о веществах, их строении, свойствах и превращениях Биология наука о живых системах Физтех, 1 курс. Осень 2015 6
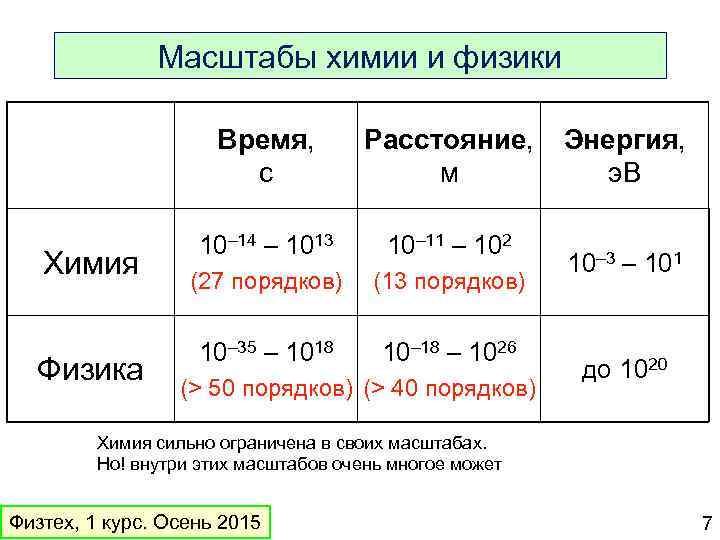 Масштабы химии и физики Время, с Химия Физика Расстояние, м 10– 14 – 1013 10– 11 – 102 (27 порядков) (13 порядков) 10– 35 – 1018 10– 18 – 1026 (> 50 порядков) (> 40 порядков) Энергия, э. В 10– 3 – 101 до 1020 Химия сильно ограничена в своих масштабах. Но! внутри этих масштабов очень многое может Физтех, 1 курс. Осень 2015 7
Масштабы химии и физики Время, с Химия Физика Расстояние, м 10– 14 – 1013 10– 11 – 102 (27 порядков) (13 порядков) 10– 35 – 1018 10– 18 – 1026 (> 50 порядков) (> 40 порядков) Энергия, э. В 10– 3 – 101 до 1020 Химия сильно ограничена в своих масштабах. Но! внутри этих масштабов очень многое может Физтех, 1 курс. Осень 2015 7
 В основе химического мышления – атомно-молекулярная картина мира Физтех, 1 курс. Осень 2015 8
В основе химического мышления – атомно-молекулярная картина мира Физтех, 1 курс. Осень 2015 8
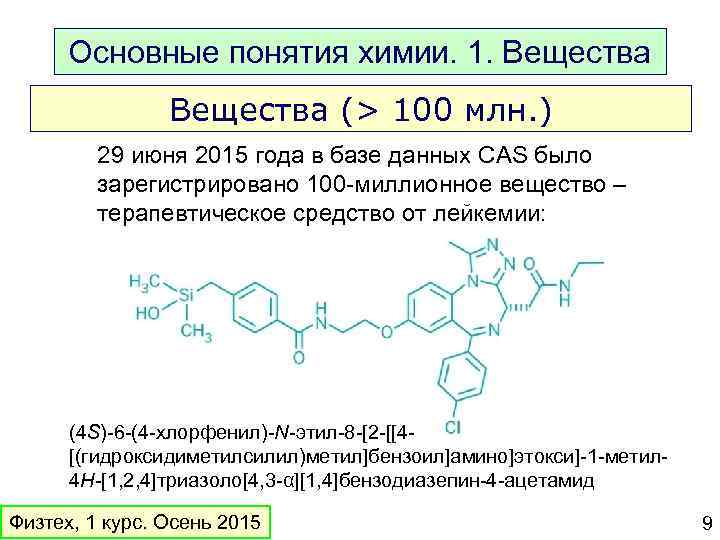 Основные понятия химии. 1. Вещества (> 100 млн. ) 29 июня 2015 года в базе данных CAS было зарегистрировано 100 -миллионное вещество – терапевтическое средство от лейкемии: (4 S)-6 -(4 -хлорфенил)-N-этил-8 -[2 -[[4[(гидроксидиметилсилил)метил]бензоил]амино]этокси]-1 -метил 4 H-[1, 2, 4]триазоло[4, 3 -α][1, 4]бензодиазепин-4 -ацетамид Физтех, 1 курс. Осень 2015 9
Основные понятия химии. 1. Вещества (> 100 млн. ) 29 июня 2015 года в базе данных CAS было зарегистрировано 100 -миллионное вещество – терапевтическое средство от лейкемии: (4 S)-6 -(4 -хлорфенил)-N-этил-8 -[2 -[[4[(гидроксидиметилсилил)метил]бензоил]амино]этокси]-1 -метил 4 H-[1, 2, 4]триазоло[4, 3 -α][1, 4]бензодиазепин-4 -ацетамид Физтех, 1 курс. Осень 2015 9
 Что надо знать о веществах? 1. 2. 3. 4. 5. Формула (из чего состоит) Структура (как устроено) Физические свойства Химические свойства Способы получения (лаб. и промышл. ) 6. Практическое применение Физтех, 1 курс. Осень 2015 10
Что надо знать о веществах? 1. 2. 3. 4. 5. Формула (из чего состоит) Структура (как устроено) Физические свойства Химические свойства Способы получения (лаб. и промышл. ) 6. Практическое применение Физтех, 1 курс. Осень 2015 10
 Основные понятия химии. 2. Реакции Химические реакции (> 80 млн. ) Что надо знать о химической реакции? 1. Условия проведения – температура, давление, агрегатное состояние веществ, растворитель, катализатор. 2. Кинетические и термодинамические функции – энергия активации, теплота, энтропия и энергия Гиббса 3. Механизм реакции – последовательность разрыва и образования химических связей Физтех, 1 курс. Осень 2015 11
Основные понятия химии. 2. Реакции Химические реакции (> 80 млн. ) Что надо знать о химической реакции? 1. Условия проведения – температура, давление, агрегатное состояние веществ, растворитель, катализатор. 2. Кинетические и термодинамические функции – энергия активации, теплота, энтропия и энергия Гиббса 3. Механизм реакции – последовательность разрыва и образования химических связей Физтех, 1 курс. Осень 2015 11
 Основные вопросы химии • Как устроены вещества? • Как связано строение веществ с их свойствами? Корреляция структура-свойство • Как создать вещество с заданной структурой и нужными свойствами? Молекулярный дизайн • Какие надо создать условия, чтобы реакция шла в нужном направлении? Физтех, 1 курс. Осень 2015 12
Основные вопросы химии • Как устроены вещества? • Как связано строение веществ с их свойствами? Корреляция структура-свойство • Как создать вещество с заданной структурой и нужными свойствами? Молекулярный дизайн • Какие надо создать условия, чтобы реакция шла в нужном направлении? Физтех, 1 курс. Осень 2015 12
 Особенности химии как науки • Отсутствие собственных законов • Многообразие объектов • Создание собственного предмета для изучения – большинство из 100 млн. веществ не существует в природе Никто не сделал так много для улучшения условий жизни людей, как химики. Г. Крото, Нобелевский лауреат по химии 1996 г. Основная задача химии – создание веществ с полезными свойствами Физтех, 1 курс. Осень 2015 13
Особенности химии как науки • Отсутствие собственных законов • Многообразие объектов • Создание собственного предмета для изучения – большинство из 100 млн. веществ не существует в природе Никто не сделал так много для улучшения условий жизни людей, как химики. Г. Крото, Нобелевский лауреат по химии 1996 г. Основная задача химии – создание веществ с полезными свойствами Физтех, 1 курс. Осень 2015 13
 Сотрудничество химии и физики • Физическая химия исследует вещества, состоящие из большого числа атомов и молекул, с помощью физических методов и на основе законов физики. • Химическая физика основной упор делает на физическое исследование элементарных химических процессов и строение молекул, ее предметом являются отдельные частицы вещества. Физико-химический факультет МГУ (2006 г. р. ) Физтех, 1 курс. Осень 2015 14
Сотрудничество химии и физики • Физическая химия исследует вещества, состоящие из большого числа атомов и молекул, с помощью физических методов и на основе законов физики. • Химическая физика основной упор делает на физическое исследование элементарных химических процессов и строение молекул, ее предметом являются отдельные частицы вещества. Физико-химический факультет МГУ (2006 г. р. ) Физтех, 1 курс. Осень 2015 14
 Междисциплинарные журналы • • Journal of Chemical Physics Journal of Physical Chemistry (серии A, B, C) Chemical Physics Letters Physical Chemistry Chemical Physics (PCCP) • Журнал физической химии • Химическая физика Физтех, 1 курс. Осень 2015 15
Междисциплинарные журналы • • Journal of Chemical Physics Journal of Physical Chemistry (серии A, B, C) Chemical Physics Letters Physical Chemistry Chemical Physics (PCCP) • Журнал физической химии • Химическая физика Физтех, 1 курс. Осень 2015 15
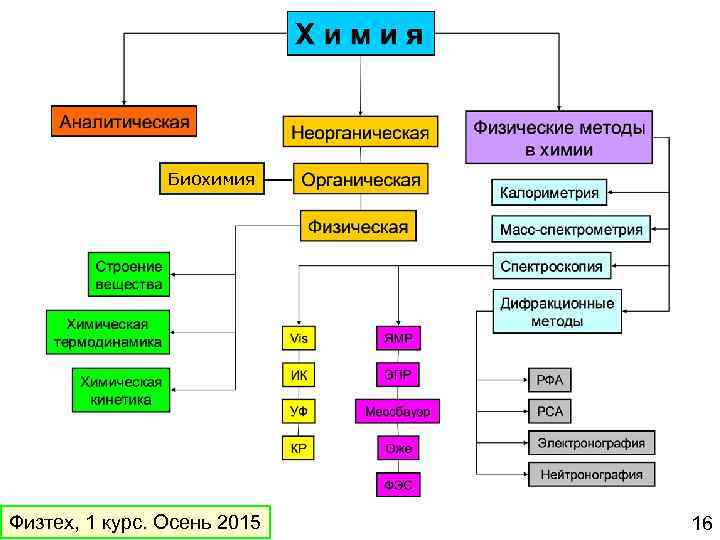 Биохимия Физтех, 1 курс. Осень 2015 16
Биохимия Физтех, 1 курс. Осень 2015 16
 Основные теории химии • Квантовая химия (квантовая механика в применении к атомам, молекулам и твердым телам) • Химическая термодинамика • Химическая кинетика • Структурная теория + стереохимия Физтех, 1 курс. Осень 2015 17
Основные теории химии • Квантовая химия (квантовая механика в применении к атомам, молекулам и твердым телам) • Химическая термодинамика • Химическая кинетика • Структурная теория + стереохимия Физтех, 1 курс. Осень 2015 17
 Язык химии. 1. Формулы • Химические формулы отражают состав и (или) строение молекул а) молекулярные – С 6 H 6 б) эмпирические (брутто) – CH в) структурные – • Названия веществ • Уравнения и схемы реакций Физтех, 1 курс. Осень 2015 18
Язык химии. 1. Формулы • Химические формулы отражают состав и (или) строение молекул а) молекулярные – С 6 H 6 б) эмпирические (брутто) – CH в) структурные – • Названия веществ • Уравнения и схемы реакций Физтех, 1 курс. Осень 2015 18
 Элементный анализ По массовым долям элементов можно определить брутто-формулу Ax. By. Cz Физтех, 1 курс. Осень 2015 19
Элементный анализ По массовым долям элементов можно определить брутто-формулу Ax. By. Cz Физтех, 1 курс. Осень 2015 19
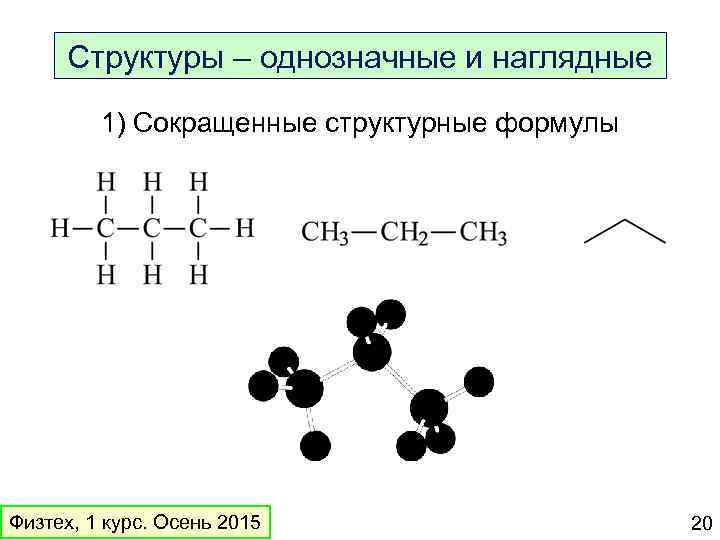 Структуры – однозначные и наглядные 1) Сокращенные структурные формулы Физтех, 1 курс. Осень 2015 20
Структуры – однозначные и наглядные 1) Сокращенные структурные формулы Физтех, 1 курс. Осень 2015 20
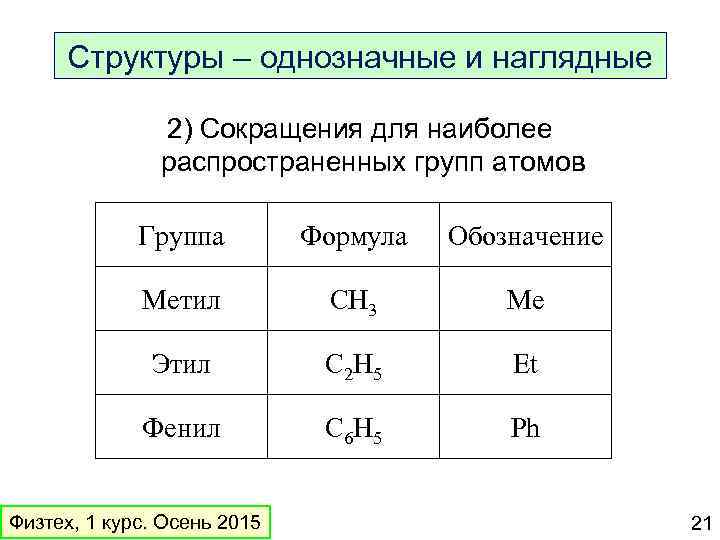 Структуры – однозначные и наглядные 2) Сокращения для наиболее распространенных групп атомов Группа Формула Обозначение Метил CH 3 Me Этил C 2 H 5 Et Фенил C 6 H 5 Ph Физтех, 1 курс. Осень 2015 21
Структуры – однозначные и наглядные 2) Сокращения для наиболее распространенных групп атомов Группа Формула Обозначение Метил CH 3 Me Этил C 2 H 5 Et Фенил C 6 H 5 Ph Физтех, 1 курс. Осень 2015 21
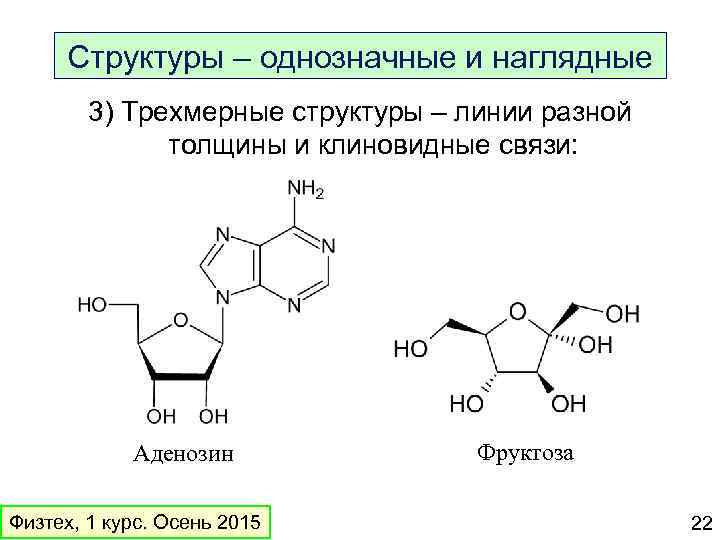 Структуры – однозначные и наглядные 3) Трехмерные структуры – линии разной толщины и клиновидные связи: Аденозин Физтех, 1 курс. Осень 2015 Фруктоза 22
Структуры – однозначные и наглядные 3) Трехмерные структуры – линии разной толщины и клиновидные связи: Аденозин Физтех, 1 курс. Осень 2015 Фруктоза 22
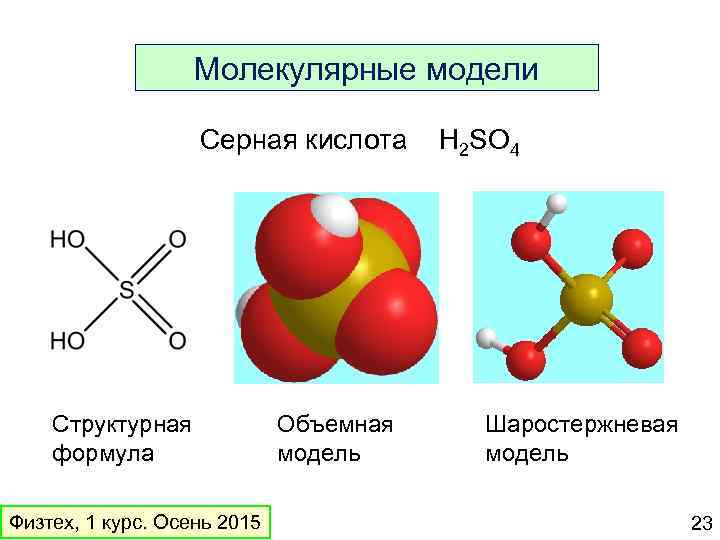 Молекулярные модели Серная кислота Структурная формула Физтех, 1 курс. Осень 2015 Объемная модель H 2 SO 4 Шаростержневая модель 23
Молекулярные модели Серная кислота Структурная формула Физтех, 1 курс. Осень 2015 Объемная модель H 2 SO 4 Шаростержневая модель 23
 Названия По номенклатуре – длинные, предпочитают использовать тривиальные 2 -Гидроксипропан-1, 2, 3 -трикарбоновая кислота (лимонная кислота) Физтех, 1 курс. Осень 2015 24
Названия По номенклатуре – длинные, предпочитают использовать тривиальные 2 -Гидроксипропан-1, 2, 3 -трикарбоновая кислота (лимонная кислота) Физтех, 1 курс. Осень 2015 24
 Вещества Вещество – любая совокупность атомов, молекул, ионов • Индивидуальные (чистые) • Смеси Физтех, 1 курс. Осень 2015 • Простые • Сложные (химические соединения) а) постоянного состава – CO 2 б) переменного состава – Ti. Ox (широкая область гомогенности, x = 0. 65 -1. 25) 25
Вещества Вещество – любая совокупность атомов, молекул, ионов • Индивидуальные (чистые) • Смеси Физтех, 1 курс. Осень 2015 • Простые • Сложные (химические соединения) а) постоянного состава – CO 2 б) переменного состава – Ti. Ox (широкая область гомогенности, x = 0. 65 -1. 25) 25
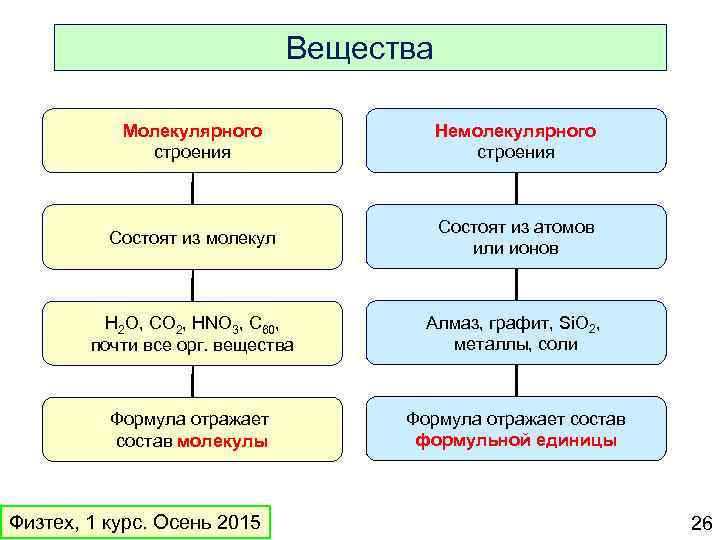 Вещества Молекулярного строения Немолекулярного строения Состоят из молекул Состоят из атомов или ионов H 2 O, CO 2, HNO 3, C 60, почти все орг. вещества Алмаз, графит, Si. O 2, металлы, соли Формула отражает состав молекулы Формула отражает состав формульной единицы Физтех, 1 курс. Осень 2015 26
Вещества Молекулярного строения Немолекулярного строения Состоят из молекул Состоят из атомов или ионов H 2 O, CO 2, HNO 3, C 60, почти все орг. вещества Алмаз, графит, Si. O 2, металлы, соли Формула отражает состав молекулы Формула отражает состав формульной единицы Физтех, 1 курс. Осень 2015 26
 Количество вещества 1 моль – 6. 0221 x 1023 частиц NA = 6. 0221 x 1023 моль– 1 – постоянная Авогадро F – любое аддитивное (экстенсивное) свойство: масса, объем, число частиц, заряд Физтех, 1 курс. Осень 2015 27
Количество вещества 1 моль – 6. 0221 x 1023 частиц NA = 6. 0221 x 1023 моль– 1 – постоянная Авогадро F – любое аддитивное (экстенсивное) свойство: масса, объем, число частиц, заряд Физтех, 1 курс. Осень 2015 27
![Молярные (мольные) величины – молярная масса. [M] = г/моль Численно равна массе молекулы в Молярные (мольные) величины – молярная масса. [M] = г/моль Численно равна массе молекулы в](https://present5.com/presentation/47475389_437174788/image-28.jpg) Молярные (мольные) величины – молярная масса. [M] = г/моль Численно равна массе молекулы в а. е. м. M(CO 2) = 44 г/моль, m(молек. CO 2) = 44 а. е. м. – молярный объем. [Vm] = л/моль Для твердых веществ и жидкостей – практически постоянный. Для газов – зависит от T и P: Vm = RT / P – постоянная Фарадея Равна заряду одного моля электронов Физтех, 1 курс. Осень 2015 28
Молярные (мольные) величины – молярная масса. [M] = г/моль Численно равна массе молекулы в а. е. м. M(CO 2) = 44 г/моль, m(молек. CO 2) = 44 а. е. м. – молярный объем. [Vm] = л/моль Для твердых веществ и жидкостей – практически постоянный. Для газов – зависит от T и P: Vm = RT / P – постоянная Фарадея Равна заряду одного моля электронов Физтех, 1 курс. Осень 2015 28
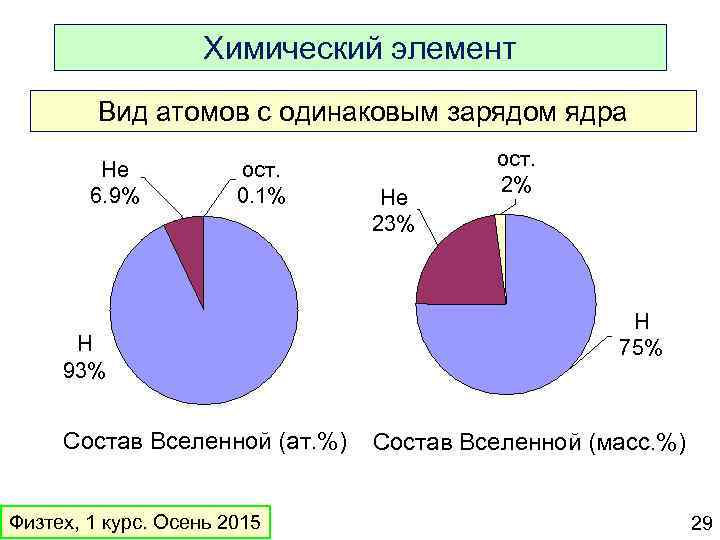 Химический элемент Вид атомов с одинаковым зарядом ядра He 6. 9% ост. 0. 1% H 93% Состав Вселенной (ат. %) Физтех, 1 курс. Осень 2015 He 23% ост. 2% H 75% Состав Вселенной (масс. %) 29
Химический элемент Вид атомов с одинаковым зарядом ядра He 6. 9% ост. 0. 1% H 93% Состав Вселенной (ат. %) Физтех, 1 курс. Осень 2015 He 23% ост. 2% H 75% Состав Вселенной (масс. %) 29
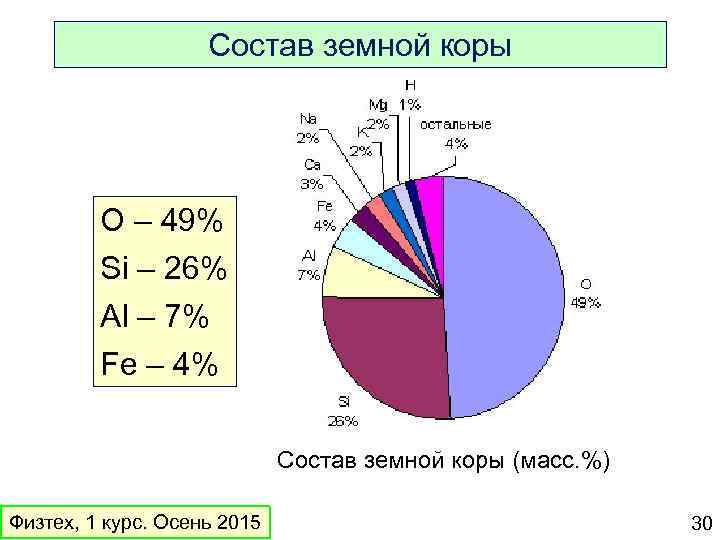 Состав земной коры O – 49% Si – 26% Al – 7% Fe – 4% Состав земной коры (масс. %) Физтех, 1 курс. Осень 2015 30
Состав земной коры O – 49% Si – 26% Al – 7% Fe – 4% Состав земной коры (масс. %) Физтех, 1 курс. Осень 2015 30
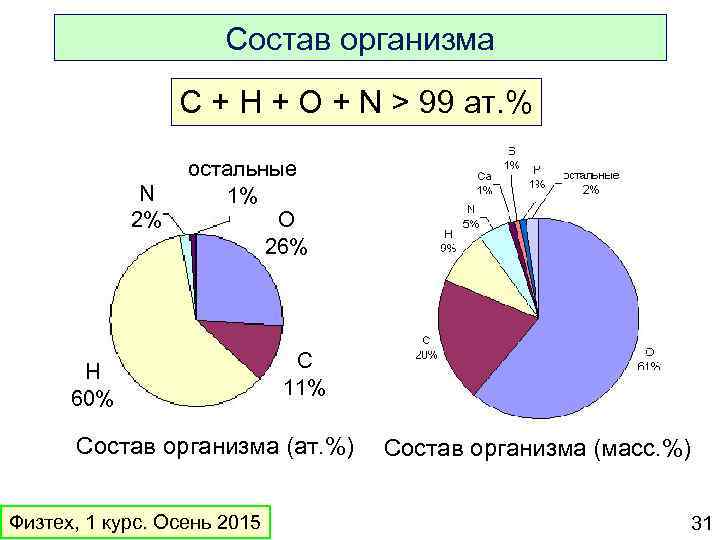 Состав организма C + H + O + N > 99 ат. % N 2% остальные 1% O 26% H 60% С 11% Состав организма (ат. %) Физтех, 1 курс. Осень 2015 Состав организма (масс. %) 31
Состав организма C + H + O + N > 99 ат. % N 2% остальные 1% O 26% H 60% С 11% Состав организма (ат. %) Физтех, 1 курс. Осень 2015 Состав организма (масс. %) 31
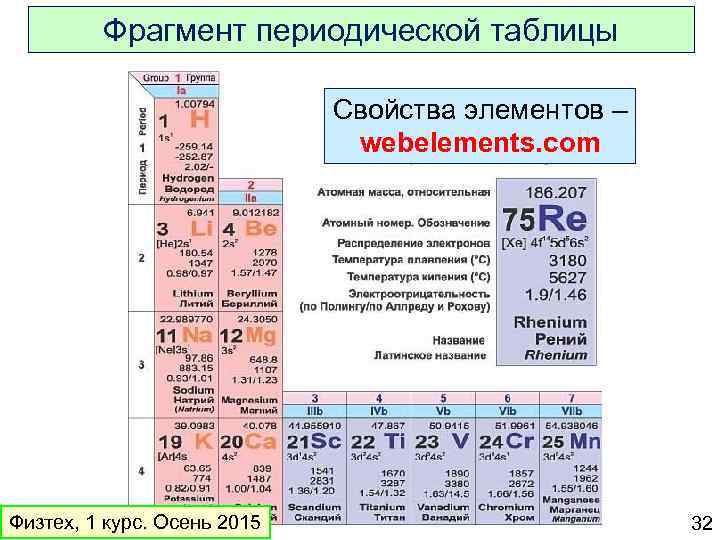 Фрагмент периодической таблицы Свойства элементов – webelements. com Физтех, 1 курс. Осень 2015 32
Фрагмент периодической таблицы Свойства элементов – webelements. com Физтех, 1 курс. Осень 2015 32
 Периодическая система. Длинный вариант Физтех, 1 курс. Осень 2015 33
Периодическая система. Длинный вариант Физтех, 1 курс. Осень 2015 33
 Атомная масса элемента Рассчитывается с учетом распространенности изотопов элемента (ат. %) в земной коре Физтех, 1 курс. Осень 2015 34
Атомная масса элемента Рассчитывается с учетом распространенности изотопов элемента (ат. %) в земной коре Физтех, 1 курс. Осень 2015 34
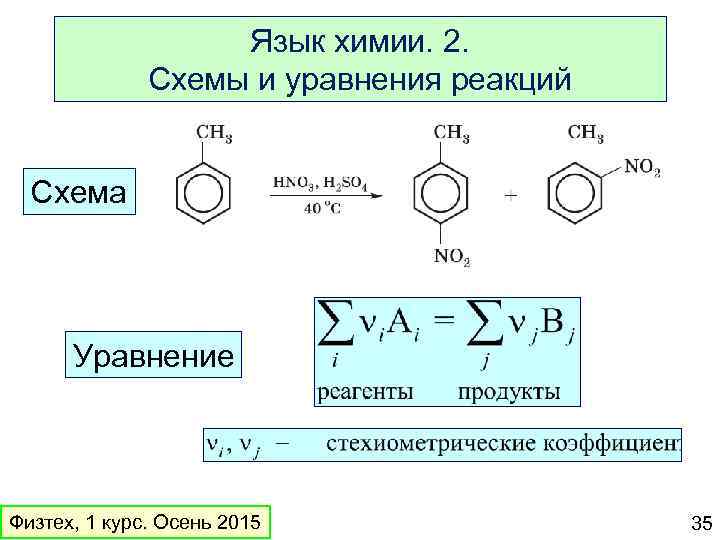 Язык химии. 2. Схемы и уравнения реакций Схема Уравнение Физтех, 1 курс. Осень 2015 35
Язык химии. 2. Схемы и уравнения реакций Схема Уравнение Физтех, 1 курс. Осень 2015 35
 Химическая переменная пропорция химическая переменная количества веществ Физтех, 1 курс. Осень 2015 36
Химическая переменная пропорция химическая переменная количества веществ Физтех, 1 курс. Осень 2015 36
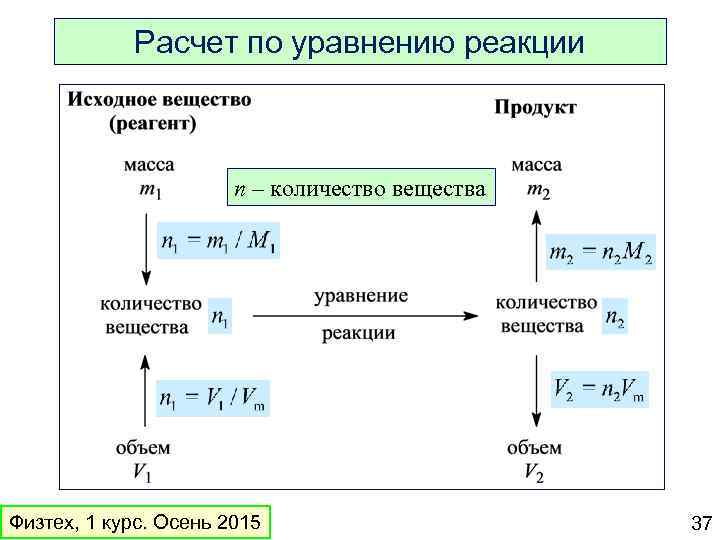 Расчет по уравнению реакции n – количество вещества Физтех, 1 курс. Осень 2015 37
Расчет по уравнению реакции n – количество вещества Физтех, 1 курс. Осень 2015 37
 Примеры задач на химическую стехиометрию 1. Определите простейшую формулу гексогена: 16. 2% С, 2. 7% H, 37. 8% N. (CH 2 N 2 O 2) 2. Определите молекулярную формулу гексогена, если при детонации 1 моля образуется 100 л газов (при 163 к. Па и 54 о. С). (C 3 H 6 N 6 O 6) 3. Определите формулу углеводорода, если при сгорании 10 л этого вещества образовалось 30 л углекислого газа и 40 л паров воды. (C 3 H 8) 4. Сколько азотной кислоты можно получить из 1 кубометра воздуха? Сколько для этого потребуется воды? (5 кг HNO 3, 750 г H 2 O) 5. При прокаливании 29 г гидроксида магния выделилось 7, 2 г воды. Какая часть гидроксида разложилась? (80%) Физтех, 1 курс. Осень 2015 38
Примеры задач на химическую стехиометрию 1. Определите простейшую формулу гексогена: 16. 2% С, 2. 7% H, 37. 8% N. (CH 2 N 2 O 2) 2. Определите молекулярную формулу гексогена, если при детонации 1 моля образуется 100 л газов (при 163 к. Па и 54 о. С). (C 3 H 6 N 6 O 6) 3. Определите формулу углеводорода, если при сгорании 10 л этого вещества образовалось 30 л углекислого газа и 40 л паров воды. (C 3 H 8) 4. Сколько азотной кислоты можно получить из 1 кубометра воздуха? Сколько для этого потребуется воды? (5 кг HNO 3, 750 г H 2 O) 5. При прокаливании 29 г гидроксида магния выделилось 7, 2 г воды. Какая часть гидроксида разложилась? (80%) Физтех, 1 курс. Осень 2015 38
 Важнейшие формулы Количество вещества Определение брутто-формулы Расчет по уравнению реакции Физтех, 1 курс. Осень 2015 39
Важнейшие формулы Количество вещества Определение брутто-формулы Расчет по уравнению реакции Физтех, 1 курс. Осень 2015 39
 Коротко о главном 1. Химия – часть естествознания. Это – наука о веществах, их строении, свойствах и превращениях. Главная задача химии – получение веществ с полезными свойствами. 2. Основные понятия химии – вещество и реакция. Вещества описываются химическими формулами, реакции – схемами и химическими уравнениями. Информация обо всех известных веществах и реакциях содержится в химических базах данных. 3. Расчеты по химическим формулам и уравнениями основаны на стехиометрических соотношениях (пропорциях) и использовании понятия «моль» . 4. Вещество – любая совокупность атомов, молекул или ионов. Химический элемент – вид атомов с одинаковым зарядом ядра. Свойства элементов периодически изменяются с увеличением заряда ядра. Физтех, 1 курс. Осень 2015 40
Коротко о главном 1. Химия – часть естествознания. Это – наука о веществах, их строении, свойствах и превращениях. Главная задача химии – получение веществ с полезными свойствами. 2. Основные понятия химии – вещество и реакция. Вещества описываются химическими формулами, реакции – схемами и химическими уравнениями. Информация обо всех известных веществах и реакциях содержится в химических базах данных. 3. Расчеты по химическим формулам и уравнениями основаны на стехиометрических соотношениях (пропорциях) и использовании понятия «моль» . 4. Вещество – любая совокупность атомов, молекул или ионов. Химический элемент – вид атомов с одинаковым зарядом ядра. Свойства элементов периодически изменяются с увеличением заряда ядра. Физтех, 1 курс. Осень 2015 40
 Основные понятия § § § § § Наука Вещество Химическая реакция Химический элемент Химическая формула - простейшая (брутто) - молекулярная - структурная Стехиометрия Схема реакции, уравнение реакции Стехиометрические коэффициенты Химическая переменная Моль, молярная масса, молярный объем Физтех, 1 курс. Осень 2015 41
Основные понятия § § § § § Наука Вещество Химическая реакция Химический элемент Химическая формула - простейшая (брутто) - молекулярная - структурная Стехиометрия Схема реакции, уравнение реакции Стехиометрические коэффициенты Химическая переменная Моль, молярная масса, молярный объем Физтех, 1 курс. Осень 2015 41
 Лекция 2 Электронное строение и периодические свойства атомов Физтех, 1 курс. Осень 2015
Лекция 2 Электронное строение и периодические свойства атомов Физтех, 1 курс. Осень 2015
 План лекции 1. Теория Бора атома водорода. 2. Основные понятия и принципы квантовой механики. 3. Водородоподобные атомы и ионы. Квантовые числа и волновые функции электрона. 4. Многоэлектронные атомы. Электронные конфигурации и атомные термы. 5. История открытия Периодического закона. 6. Периодические свойства элементов. Физтех, 1 курс. Осень 2015 43
План лекции 1. Теория Бора атома водорода. 2. Основные понятия и принципы квантовой механики. 3. Водородоподобные атомы и ионы. Квантовые числа и волновые функции электрона. 4. Многоэлектронные атомы. Электронные конфигурации и атомные термы. 5. История открытия Периодического закона. 6. Периодические свойства элементов. Физтех, 1 курс. Осень 2015 43
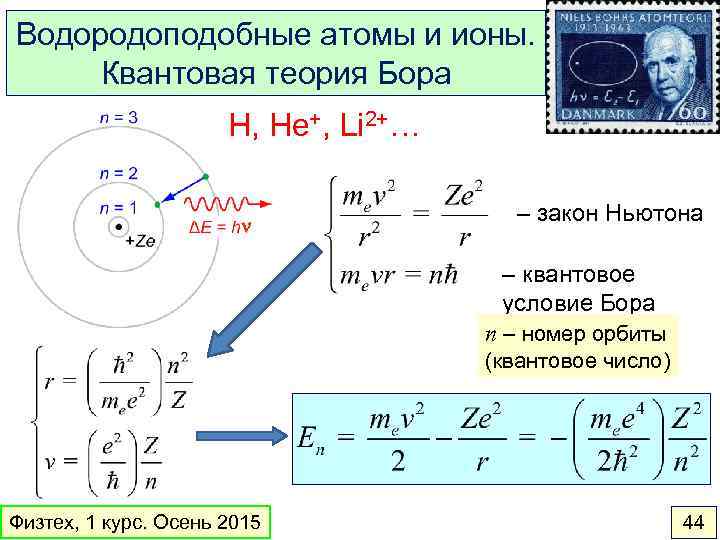 Водородоподобные атомы и ионы. Квантовая теория Бора H, He+, Li 2+… n – закон Ньютона – квантовое условие Бора n – номер орбиты (квантовое число) Физтех, 1 курс. Осень 2015 44
Водородоподобные атомы и ионы. Квантовая теория Бора H, He+, Li 2+… n – закон Ньютона – квантовое условие Бора n – номер орбиты (квантовое число) Физтех, 1 курс. Осень 2015 44
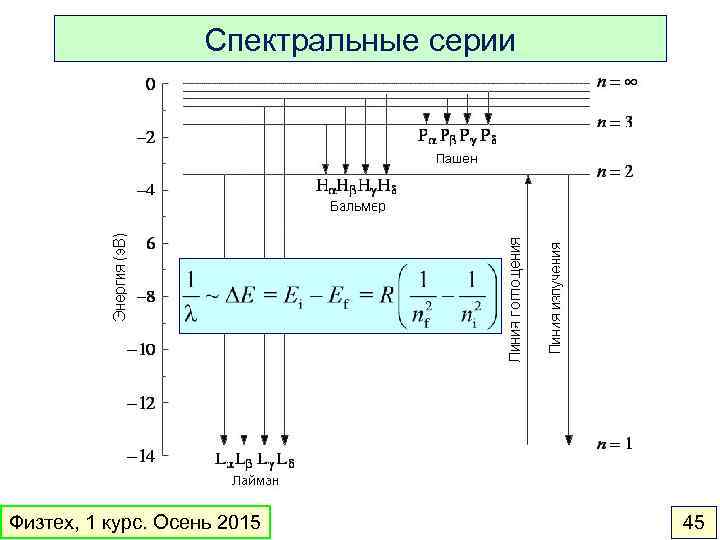 Спектральные серии Физтех, 1 курс. Осень 2015 45
Спектральные серии Физтех, 1 курс. Осень 2015 45
 Квантовая механика. Основные принципы «Квантовую механику не понимает никто. » Р. Фейнман «Если у человека при первом знакомстве с квантовой механикой голова не идет кругом, то он не понимает в ней ничего. » Н. Бор • Принцип неопределенности • Принцип суперпозиции Физтех, 1 курс. Осень 2015 46
Квантовая механика. Основные принципы «Квантовую механику не понимает никто. » Р. Фейнман «Если у человека при первом знакомстве с квантовой механикой голова не идет кругом, то он не понимает в ней ничего. » Н. Бор • Принцип неопределенности • Принцип суперпозиции Физтех, 1 курс. Осень 2015 46
 Принцип неопределенности q Наблюдаемые величины – результат процесса измерения – взаимодействия системы с телом ( «прибором» ), с достаточной точностью подчиняющимся классической механике. q Процесс измерения в общем случае изменяет состояние квантовой системы и этого влияния принципиально невозможно избежать. q Не все физические величины измеримы одновременно. Физтех, 1 курс. Осень 2015 47
Принцип неопределенности q Наблюдаемые величины – результат процесса измерения – взаимодействия системы с телом ( «прибором» ), с достаточной точностью подчиняющимся классической механике. q Процесс измерения в общем случае изменяет состояние квантовой системы и этого влияния принципиально невозможно избежать. q Не все физические величины измеримы одновременно. Физтех, 1 курс. Осень 2015 47
 Волновая функция ni - квантовые числа, нумерующие собственные значения физических величин из полного набора Волновая функция представляет состояние, описанное наиболее полным образом вероятность найти систему в заданном интервале координат нормировка Принцип суперпозиции состояний: 1(q, t) чистое состояние, в котором физическая величина f имеет определенное значение f 1 2(q, t) чистое состояние, в котором физическая величина f имеет определенное значение f 2 c 1 1(q, t) + c 2 2(q, t) смешанное состояние, в котором измерение величины f даст либо результат f 1, либо f 2. Вероятность того, что измерение даст значение fi, пропорциональна |ci|2 Физтех, 1 курс. Осень 2015 48
Волновая функция ni - квантовые числа, нумерующие собственные значения физических величин из полного набора Волновая функция представляет состояние, описанное наиболее полным образом вероятность найти систему в заданном интервале координат нормировка Принцип суперпозиции состояний: 1(q, t) чистое состояние, в котором физическая величина f имеет определенное значение f 1 2(q, t) чистое состояние, в котором физическая величина f имеет определенное значение f 2 c 1 1(q, t) + c 2 2(q, t) смешанное состояние, в котором измерение величины f даст либо результат f 1, либо f 2. Вероятность того, что измерение даст значение fi, пропорциональна |ci|2 Физтех, 1 курс. Осень 2015 48
 Операторы и средние значения q Каждой физической величине ставится в соответствие математический оператор. q Если в результате действия оператора функция не меняется с точностью до постоянного множителя, то говорят, что n собственная функция данного оператора, а fn – собственное значение величины f. q Необходимым и достаточным условием одновременной измеримости величин f и g является коммутативность соответствующих операторов: q Среднее значение физической величины за большое число измерений равно среднему значению соответствующего оператора. Оператор координаты компоненты импульса компоненты момента импульса Физтех, 1 курс. Осень 2015 Оператор энергии (гамильтониан) 49
Операторы и средние значения q Каждой физической величине ставится в соответствие математический оператор. q Если в результате действия оператора функция не меняется с точностью до постоянного множителя, то говорят, что n собственная функция данного оператора, а fn – собственное значение величины f. q Необходимым и достаточным условием одновременной измеримости величин f и g является коммутативность соответствующих операторов: q Среднее значение физической величины за большое число измерений равно среднему значению соответствующего оператора. Оператор координаты компоненты импульса компоненты момента импульса Физтех, 1 курс. Осень 2015 Оператор энергии (гамильтониан) 49
 Уравнение Шрёдингера Изменение квантового состояния во времени описывается уравнением Шрёдингера q У системы в стационарном состоянии энергия сохраняется. q Волновая функция стационарного состояния является собственной для оператора Гамильтона и разбивается на координатный и временной множители. q Возможные значения энергии системы (спектр энергий) определяются собственными значениями оператора Гамильтона q Одному и тому же значению (уровню) энергии может соответствовать несколько различных состояний (вырождение уровня). q Если оператор физической величины f коммутирует с гамильтонианом, то эта величина в данном стационарном состоянии сохраняется и измерима одновременно с энергией. Физтех, 1 курс. Осень 2015 50
Уравнение Шрёдингера Изменение квантового состояния во времени описывается уравнением Шрёдингера q У системы в стационарном состоянии энергия сохраняется. q Волновая функция стационарного состояния является собственной для оператора Гамильтона и разбивается на координатный и временной множители. q Возможные значения энергии системы (спектр энергий) определяются собственными значениями оператора Гамильтона q Одному и тому же значению (уровню) энергии может соответствовать несколько различных состояний (вырождение уровня). q Если оператор физической величины f коммутирует с гамильтонианом, то эта величина в данном стационарном состоянии сохраняется и измерима одновременно с энергией. Физтех, 1 курс. Осень 2015 50
 Водородоподобные атомы и ионы H, He+, Li 2+… В сферически симметричном поле ядра U(r) для электрона сохраняются следующие величины: Энергия n главное Момент импульса l орбитальное Проекция момента импульса на выделенную ось z ml магнитное Спин электрона s спиновое Проекция спина на ось z ms магнитное спиновое Физтех, 1 курс. Осень 2015 51
Водородоподобные атомы и ионы H, He+, Li 2+… В сферически симметричном поле ядра U(r) для электрона сохраняются следующие величины: Энергия n главное Момент импульса l орбитальное Проекция момента импульса на выделенную ось z ml магнитное Спин электрона s спиновое Проекция спина на ось z ms магнитное спиновое Физтех, 1 курс. Осень 2015 51
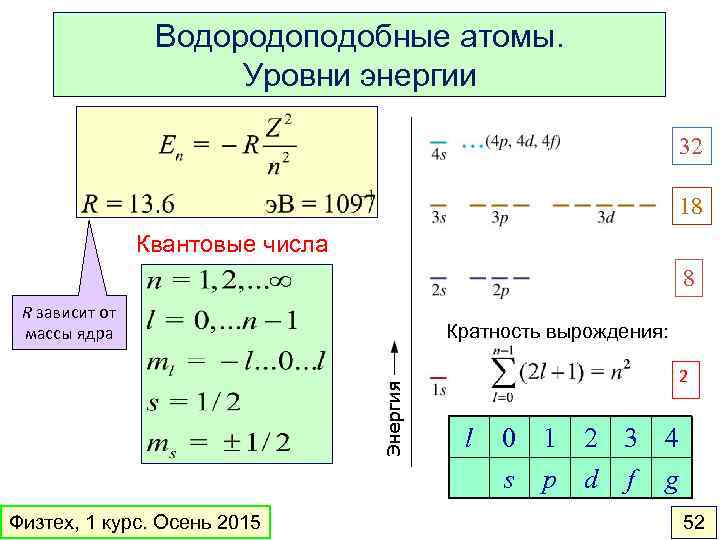 Водородоподобные атомы. Уровни энергии 32 18 Квантовые числа 8 R зависит от массы ядра Кратность вырождения: 2 l Физтех, 1 курс. Осень 2015 0 1 2 3 4 s p d f g 52
Водородоподобные атомы. Уровни энергии 32 18 Квантовые числа 8 R зависит от массы ядра Кратность вырождения: 2 l Физтех, 1 курс. Осень 2015 0 1 2 3 4 s p d f g 52
 Водородоподобные атомы. Волновые функции Физтех, 1 курс. Осень 2015 53
Водородоподобные атомы. Волновые функции Физтех, 1 курс. Осень 2015 53
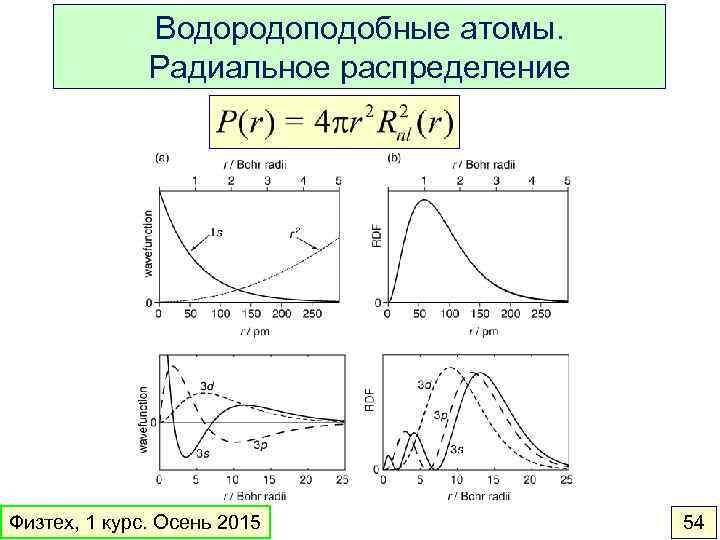 Водородоподобные атомы. Радиальное распределение Физтех, 1 курс. Осень 2015 54
Водородоподобные атомы. Радиальное распределение Физтех, 1 курс. Осень 2015 54
 Водородоподобные атомы. Угловые функции Физтех, 1 курс. Осень 2015 55
Водородоподобные атомы. Угловые функции Физтех, 1 курс. Осень 2015 55
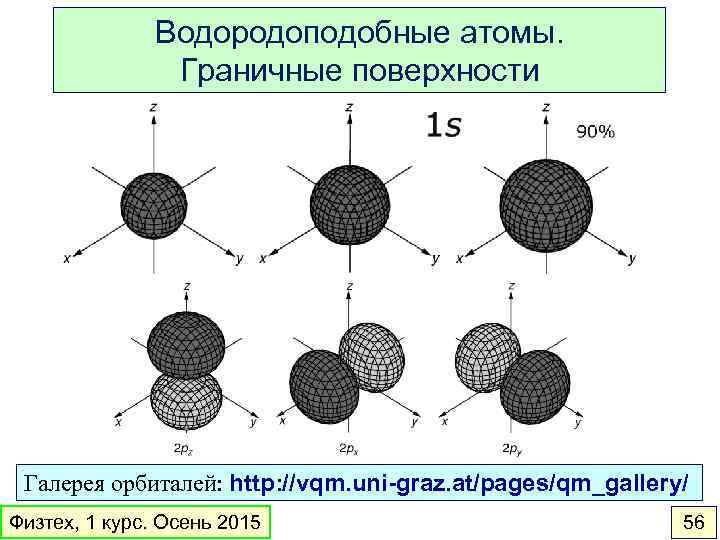 Водородоподобные атомы. Граничные поверхности Галерея орбиталей: http: //vqm. uni-graz. at/pages/qm_gallery/ Физтех, 1 курс. Осень 2015 56
Водородоподобные атомы. Граничные поверхности Галерея орбиталей: http: //vqm. uni-graz. at/pages/qm_gallery/ Физтех, 1 курс. Осень 2015 56
 Водородоподобные атомы. Граничные поверхности Физтех, 1 курс. Осень 2015 57
Водородоподобные атомы. Граничные поверхности Физтех, 1 курс. Осень 2015 57
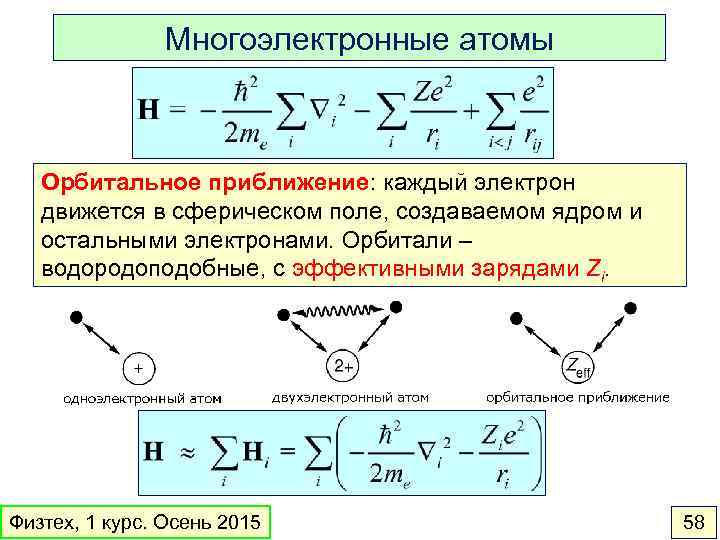 Многоэлектронные атомы Орбитальное приближение: каждый электрон движется в сферическом поле, создаваемом ядром и остальными электронами. Орбитали – водородоподобные, с эффективными зарядами Zi. Физтех, 1 курс. Осень 2015 58
Многоэлектронные атомы Орбитальное приближение: каждый электрон движется в сферическом поле, создаваемом ядром и остальными электронами. Орбитали – водородоподобные, с эффективными зарядами Zi. Физтех, 1 курс. Осень 2015 58
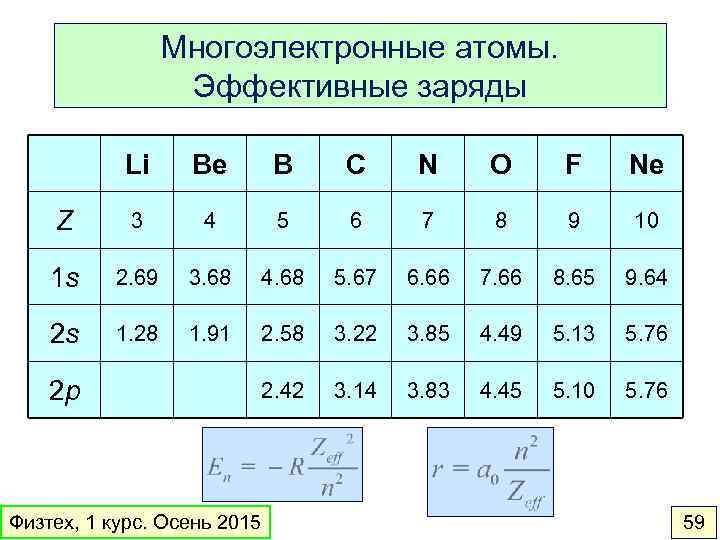 Многоэлектронные атомы. Эффективные заряды Li Be B C N O F Ne Z 3 4 5 6 7 8 9 10 1 s 2. 69 3. 68 4. 68 5. 67 6. 66 7. 66 8. 65 9. 64 2 s 1. 28 1. 91 2. 58 3. 22 3. 85 4. 49 5. 13 5. 76 2. 42 3. 14 3. 83 4. 45 5. 10 5. 76 2 p Физтех, 1 курс. Осень 2015 59
Многоэлектронные атомы. Эффективные заряды Li Be B C N O F Ne Z 3 4 5 6 7 8 9 10 1 s 2. 69 3. 68 4. 68 5. 67 6. 66 7. 66 8. 65 9. 64 2 s 1. 28 1. 91 2. 58 3. 22 3. 85 4. 49 5. 13 5. 76 2. 42 3. 14 3. 83 4. 45 5. 10 5. 76 2 p Физтех, 1 курс. Осень 2015 59
 Многоэлектронные атомы. Энергия орбиталей возрастает в ряду: 4 s 1 s < 2 p < 3 s < 3 p < 4 s < 3 d < 4 p … Порядок энергий орбиталей может быть разным для атомов и ионов Пример: Ti 4 s 23 d 2 Ti 3+ 3 d Оставшийся после ионизации валентный электрон занимает 3 dа не 4 s-орбиталь. Физтех, 1 курс. Осень 2015 3 p 4 d 3 d 4 f 3 s Энергия Обратный порядок энергий является причиной появления 1 -ого ряда переходных элементов 4 p 2 p 2 s Снятие вырождения по орбитальному моменту l 1 s 60
Многоэлектронные атомы. Энергия орбиталей возрастает в ряду: 4 s 1 s < 2 p < 3 s < 3 p < 4 s < 3 d < 4 p … Порядок энергий орбиталей может быть разным для атомов и ионов Пример: Ti 4 s 23 d 2 Ti 3+ 3 d Оставшийся после ионизации валентный электрон занимает 3 dа не 4 s-орбиталь. Физтех, 1 курс. Осень 2015 3 p 4 d 3 d 4 f 3 s Энергия Обратный порядок энергий является причиной появления 1 -ого ряда переходных элементов 4 p 2 p 2 s Снятие вырождения по орбитальному моменту l 1 s 60
 Многоэлектронные атомы. Принципы заполнения 1. Порядок заполнения орбиталей определяется главным квантовым числом и эффективным зарядом: 1 s < 2 p < 3 s < 3 p < 4 s < 3 d < 4 p < 5 s < 4 d < 5 p < 6 s < 4 f < 5 d < 6 p 2. На каждой орбитали – не более 2 электронов. 3. Правило Хунда: основное состояние имеет максимальную мультиплетность (максимальное число неспаренных электронов в пределах одного подуровня). Физтех, 1 курс. Осень 2015 61
Многоэлектронные атомы. Принципы заполнения 1. Порядок заполнения орбиталей определяется главным квантовым числом и эффективным зарядом: 1 s < 2 p < 3 s < 3 p < 4 s < 3 d < 4 p < 5 s < 4 d < 5 p < 6 s < 4 f < 5 d < 6 p 2. На каждой орбитали – не более 2 электронов. 3. Правило Хунда: основное состояние имеет максимальную мультиплетность (максимальное число неспаренных электронов в пределах одного подуровня). Физтех, 1 курс. Осень 2015 61
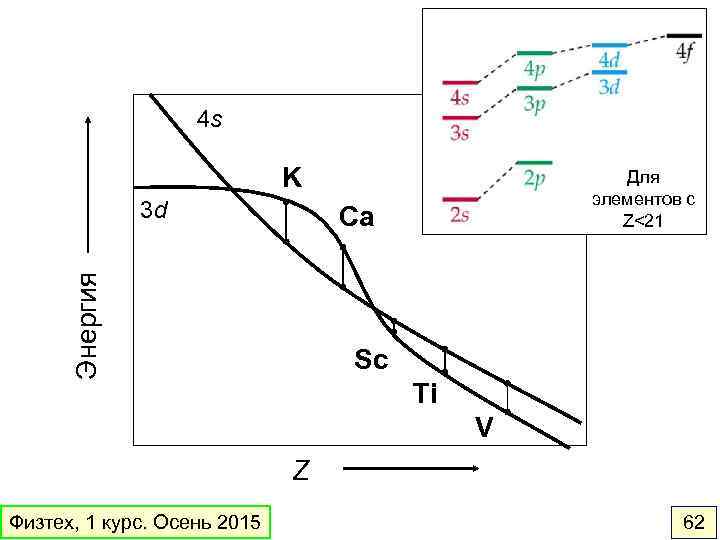 4 s K 3 d Для элементов с Z<21 Энергия Ca Sc Ti V Z Физтех, 1 курс. Осень 2015 62
4 s K 3 d Для элементов с Z<21 Энергия Ca Sc Ti V Z Физтех, 1 курс. Осень 2015 62
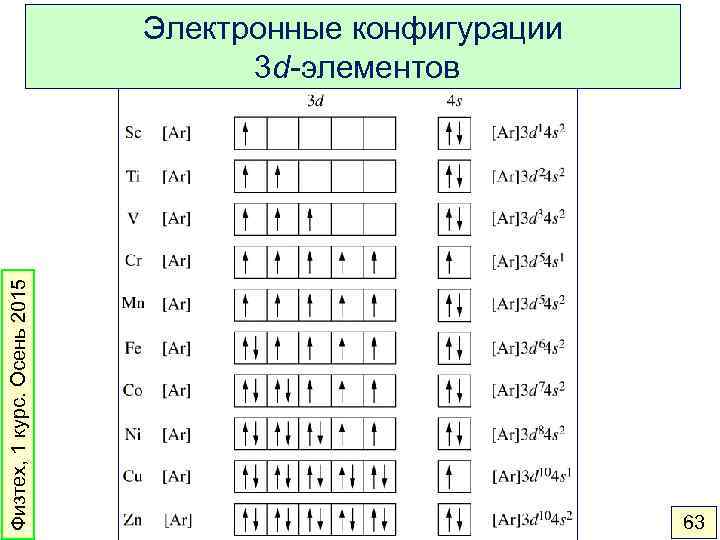 Физтех, 1 курс. Осень 2015 Электронные конфигурации 3 d-элементов 63
Физтех, 1 курс. Осень 2015 Электронные конфигурации 3 d-элементов 63
 Стационарные состояния атома как целого В центрально-симметричном поле ядра имеют место следующие точные законы сохранения: q Энергии E. q Полного момента импульса J. q Чётности состояния P. В нерелятивистском приближении отдельно сохраняются: q Полный орбитальный момент L. q Полный спин S. При заданных L и S число состояний с различными J равно: 2 S + 1 2 L + 1 при L > S при L < S Физтех, 1 курс. Осень 2015 Обозначения: L=0 S 1 2 3 4 P D F G • Без учета взаимодействия «спин-орбита» состояния с заданными L и S имеют одинаковую энергию: вырождение кратности (2 L + 1)(2 S + 1). • С учетом спин-орбитального взаимодействия (релятивистский эффект) уровни расщепляются (тонкая структура или мультиплетное расщепление) 64
Стационарные состояния атома как целого В центрально-симметричном поле ядра имеют место следующие точные законы сохранения: q Энергии E. q Полного момента импульса J. q Чётности состояния P. В нерелятивистском приближении отдельно сохраняются: q Полный орбитальный момент L. q Полный спин S. При заданных L и S число состояний с различными J равно: 2 S + 1 2 L + 1 при L > S при L < S Физтех, 1 курс. Осень 2015 Обозначения: L=0 S 1 2 3 4 P D F G • Без учета взаимодействия «спин-орбита» состояния с заданными L и S имеют одинаковую энергию: вырождение кратности (2 L + 1)(2 S + 1). • С учетом спин-орбитального взаимодействия (релятивистский эффект) уровни расщепляются (тонкая структура или мультиплетное расщепление) 64
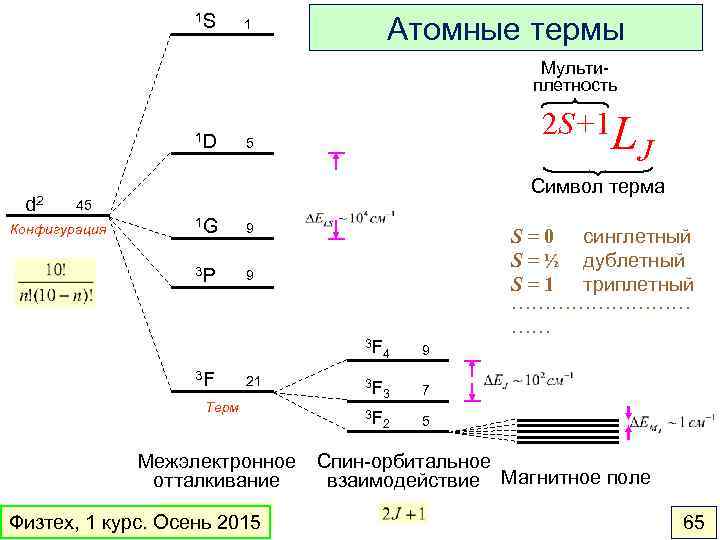 1 S Атомные термы 1 Мультиплетность 1 D d 2 2 S+1 L 5 J Символ терма 45 1 G 9 3 P Конфигурация 9 3 F 3 F 21 Терм Межэлектронное отталкивание Физтех, 1 курс. Осень 2015 4 9 3 F 3 7 3 F 2 S = 0 синглетный S = ½ дублетный S = 1 триплетный ·············· 5 Спин-орбитальное взаимодействие Магнитное поле 65
1 S Атомные термы 1 Мультиплетность 1 D d 2 2 S+1 L 5 J Символ терма 45 1 G 9 3 P Конфигурация 9 3 F 3 F 21 Терм Межэлектронное отталкивание Физтех, 1 курс. Осень 2015 4 9 3 F 3 7 3 F 2 S = 0 синглетный S = ½ дублетный S = 1 триплетный ·············· 5 Спин-орбитальное взаимодействие Магнитное поле 65
 Основное состояние атома Правила Хунда: q Из всех термов, отвечающих заданной электронной конфигурации наименьшей энергией обладает терм с максимальной мультиплетностью (спином S). q Для термов с одинаковой мультиплетностью наименьшей энергией обладает терм с наибольшим орбитальным моментом L. Cr 2+, Mn 3+: конфигурация валентных электронов d 4 S=0 Физтех, 1 курс. Осень 2015 S=1 S=2 66
Основное состояние атома Правила Хунда: q Из всех термов, отвечающих заданной электронной конфигурации наименьшей энергией обладает терм с максимальной мультиплетностью (спином S). q Для термов с одинаковой мультиплетностью наименьшей энергией обладает терм с наибольшим орбитальным моментом L. Cr 2+, Mn 3+: конфигурация валентных электронов d 4 S=0 Физтех, 1 курс. Осень 2015 S=1 S=2 66
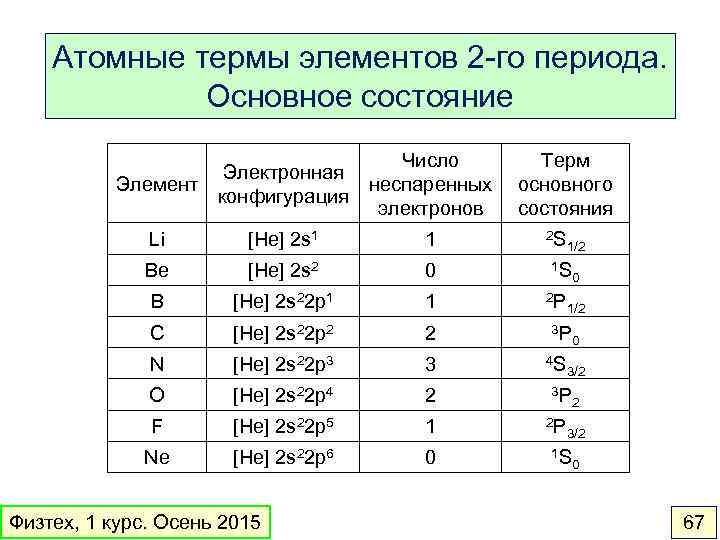 Атомные термы элементов 2 -го периода. Основное состояние Электронная Элемент конфигурация Число неспаренных электронов Li [He] 2 s 1 1 Be [He] 2 s 2 0 B [He] 2 s 22 p 1 1 C [He] 2 s 22 p 2 2 N [He] 2 s 22 p 3 3 O [He] 2 s 22 p 4 2 F [He] 2 s 22 p 5 1 Ne [He] 2 s 22 p 6 0 Физтех, 1 курс. Осень 2015 Терм основного состояния 2 S 1/2 1 S 2 P 1/2 3 P 4 S 0 3/2 3 P 2 P 0 2 3/2 1 S 0 67
Атомные термы элементов 2 -го периода. Основное состояние Электронная Элемент конфигурация Число неспаренных электронов Li [He] 2 s 1 1 Be [He] 2 s 2 0 B [He] 2 s 22 p 1 1 C [He] 2 s 22 p 2 2 N [He] 2 s 22 p 3 3 O [He] 2 s 22 p 4 2 F [He] 2 s 22 p 5 1 Ne [He] 2 s 22 p 6 0 Физтех, 1 курс. Осень 2015 Терм основного состояния 2 S 1/2 1 S 2 P 1/2 3 P 4 S 0 3/2 3 P 2 P 0 2 3/2 1 S 0 67
 Периодический закон. История открытия 1869 – Д. И. Менделеев (Россия). Периодический закон: 1. Элементы, расположенные по величине атомного веса, представляют явственную периодичность свойств. 2. Должно ожидать открытия еще многих неизвестных простых тел, например, сходных с Al и Si элементов с атомным весом 65– 75. 3. Величина атомного веса элемента иногда может быть исправлена, зная его аналогии. 4. Некоторые аналогии элементов открываются по величине веса их атомов. Физтех, 1 курс. Осень 2015 68
Периодический закон. История открытия 1869 – Д. И. Менделеев (Россия). Периодический закон: 1. Элементы, расположенные по величине атомного веса, представляют явственную периодичность свойств. 2. Должно ожидать открытия еще многих неизвестных простых тел, например, сходных с Al и Si элементов с атомным весом 65– 75. 3. Величина атомного веса элемента иногда может быть исправлена, зная его аналогии. 4. Некоторые аналогии элементов открываются по величине веса их атомов. Физтех, 1 курс. Осень 2015 68
 Как был открыт Периодический закон «Невольно зародилась мысль о том, что между массой и химическими свойствами необходимо должна быть связь. А так как масса вещества … выражается окончательно в виде весов атомов, то надо искать функциональное соответствие между индивидуальными свойствами элементов и их атомными весами. Искать же что-либо, хотя бы грибы или какую-нибудь зависимость, нельзя иначе, как смотря и пробуя. Вот я и стал подбирать, написав на отдельных карточках элементы с их атомными весами и коренными свойствами, сходные элементы и близкие атомные веса, что быстро и привело к тому заключению, что свойства элементов стоят в периодической зависимости от их атомного веса, причем, сомневаясь во многих неясностях, я ни минуты не сомневался в общности сделанного вывода, так как случайность допустить было невозможно» Физтех, 1 курс. Осень 2015 69
Как был открыт Периодический закон «Невольно зародилась мысль о том, что между массой и химическими свойствами необходимо должна быть связь. А так как масса вещества … выражается окончательно в виде весов атомов, то надо искать функциональное соответствие между индивидуальными свойствами элементов и их атомными весами. Искать же что-либо, хотя бы грибы или какую-нибудь зависимость, нельзя иначе, как смотря и пробуя. Вот я и стал подбирать, написав на отдельных карточках элементы с их атомными весами и коренными свойствами, сходные элементы и близкие атомные веса, что быстро и привело к тому заключению, что свойства элементов стоят в периодической зависимости от их атомного веса, причем, сомневаясь во многих неясностях, я ни минуты не сомневался в общности сделанного вывода, так как случайность допустить было невозможно» Физтех, 1 курс. Осень 2015 69
 Первые наброски. 17 февраля 1869 Физтех, 1 курс. Осень 2015 70
Первые наброски. 17 февраля 1869 Физтех, 1 курс. Осень 2015 70
 Физтех, 1 курс. Осень 2015 71
Физтех, 1 курс. Осень 2015 71
 Периодическая таблица. Самая первая (1869) Д. И. Менделеев, портрет 1869 г. Физтех, 1 курс. Осень 2015 72
Периодическая таблица. Самая первая (1869) Д. И. Менделеев, портрет 1869 г. Физтех, 1 курс. Осень 2015 72
 Предсказания на основе Периодического закона Предсказания Д. И. Менделеева: 1) Экабор (скандий, Sc) – открыт в 1879 г. 2) Экаалюминий (галлий, Ga) – открыт в 1875 г. 3) Экасилиций (германий, Ge) – открыт в 1886 г. 4) Экамарганец (Технеций, Tc) – синтезирован в 1937. Свойства 118 -го элемента: Открыт: в 2005 г. (Россия, США) в количестве 3 атомов Положение в Периодической системе: группа VIIIA (инертный газ) Электронная конфигурация: [Rn] 5 f 14 6 d 10 7 s 2 7 p 6. Температура плавления: – 10 о. С. Температура кипения: – 6 о. С Высший оксид: RO 4 Физтех, 1 курс. Осень 2015 73
Предсказания на основе Периодического закона Предсказания Д. И. Менделеева: 1) Экабор (скандий, Sc) – открыт в 1879 г. 2) Экаалюминий (галлий, Ga) – открыт в 1875 г. 3) Экасилиций (германий, Ge) – открыт в 1886 г. 4) Экамарганец (Технеций, Tc) – синтезирован в 1937. Свойства 118 -го элемента: Открыт: в 2005 г. (Россия, США) в количестве 3 атомов Положение в Периодической системе: группа VIIIA (инертный газ) Электронная конфигурация: [Rn] 5 f 14 6 d 10 7 s 2 7 p 6. Температура плавления: – 10 о. С. Температура кипения: – 6 о. С Высший оксид: RO 4 Физтех, 1 курс. Осень 2015 73
 Периодические свойства элементов • Радиус атома • Энергия ионизации • Сродство к электрону • Электроотрицательность www. webelements. com Физтех, 1 курс. Осень 2015 74
Периодические свойства элементов • Радиус атома • Энергия ионизации • Сродство к электрону • Электроотрицательность www. webelements. com Физтех, 1 курс. Осень 2015 74
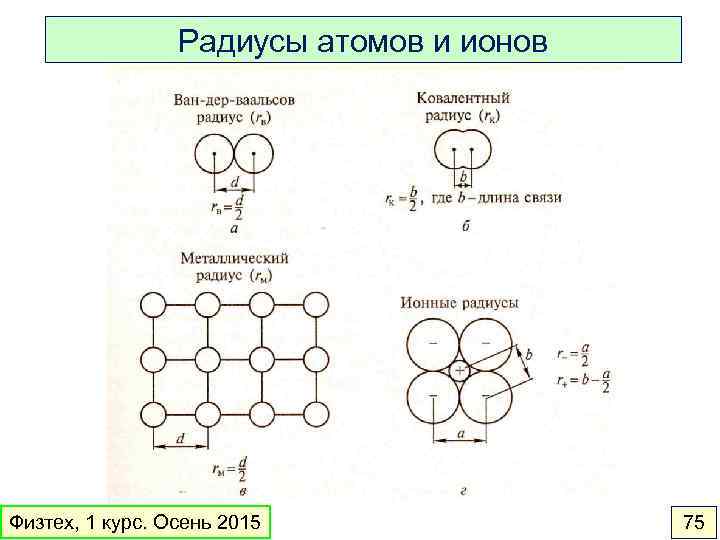 Радиусы атомов и ионов Физтех, 1 курс. Осень 2015 75
Радиусы атомов и ионов Физтех, 1 курс. Осень 2015 75
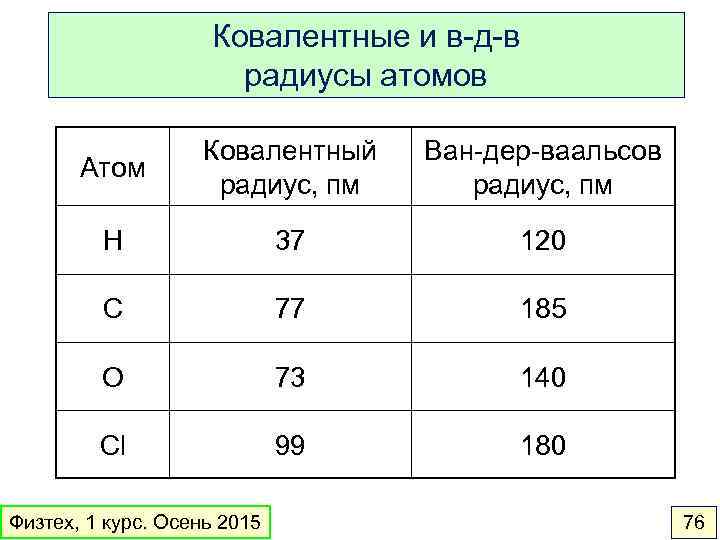 Ковалентные и в-д-в радиусы атомов Атом Ковалентный радиус, пм Ван-дер-ваальсов радиус, пм H 37 120 C 77 185 O 73 140 Cl 99 180 Физтех, 1 курс. Осень 2015 76
Ковалентные и в-д-в радиусы атомов Атом Ковалентный радиус, пм Ван-дер-ваальсов радиус, пм H 37 120 C 77 185 O 73 140 Cl 99 180 Физтех, 1 курс. Осень 2015 76
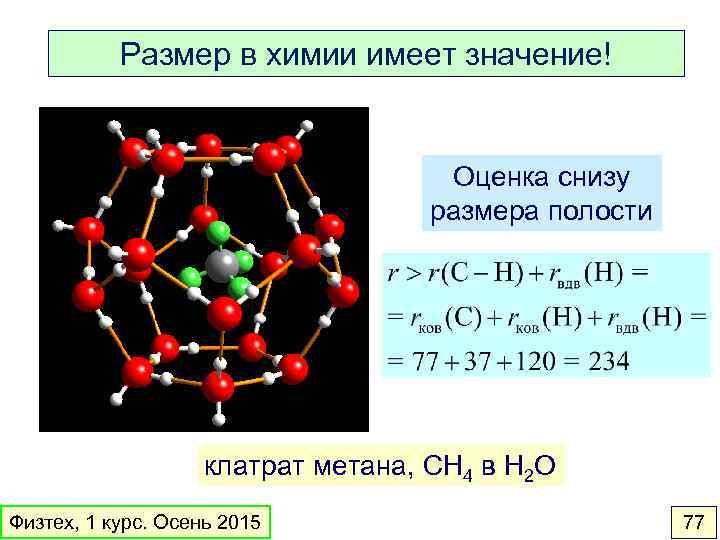 Размер в химии имеет значение! Оценка снизу размера полости клатрат метана, CH 4 в H 2 O Физтех, 1 курс. Осень 2015 77
Размер в химии имеет значение! Оценка снизу размера полости клатрат метана, CH 4 в H 2 O Физтех, 1 курс. Осень 2015 77
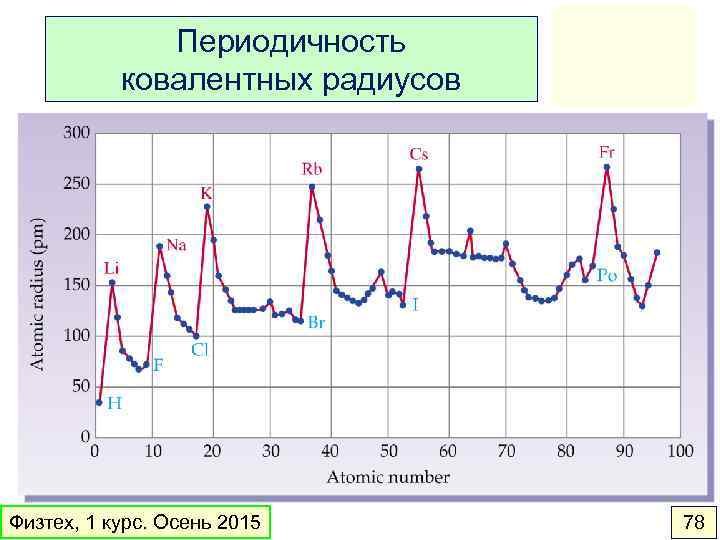 Периодичность ковалентных радиусов Физтех, 1 курс. Осень 2015 78
Периодичность ковалентных радиусов Физтех, 1 курс. Осень 2015 78
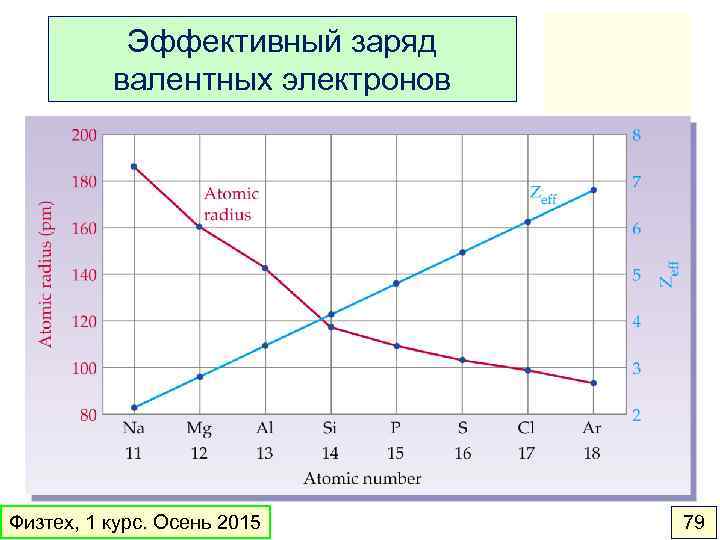 Эффективный заряд валентных электронов Физтех, 1 курс. Осень 2015 79
Эффективный заряд валентных электронов Физтех, 1 курс. Осень 2015 79
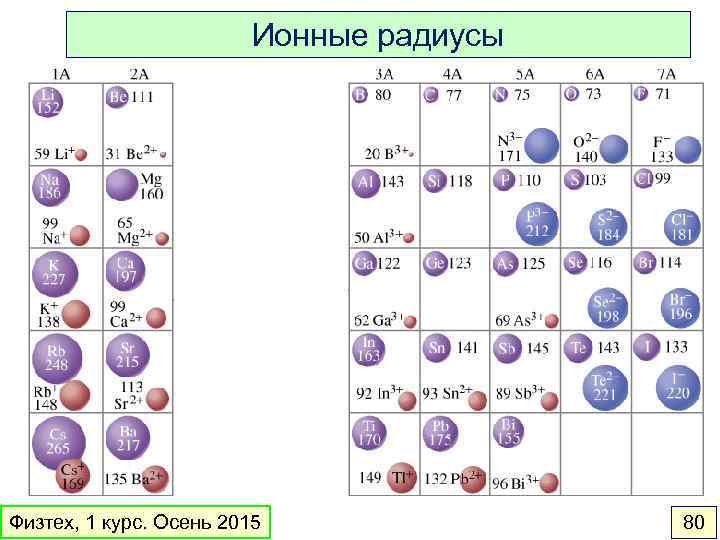 Ионные радиусы Физтех, 1 курс. Осень 2015 80
Ионные радиусы Физтех, 1 курс. Осень 2015 80
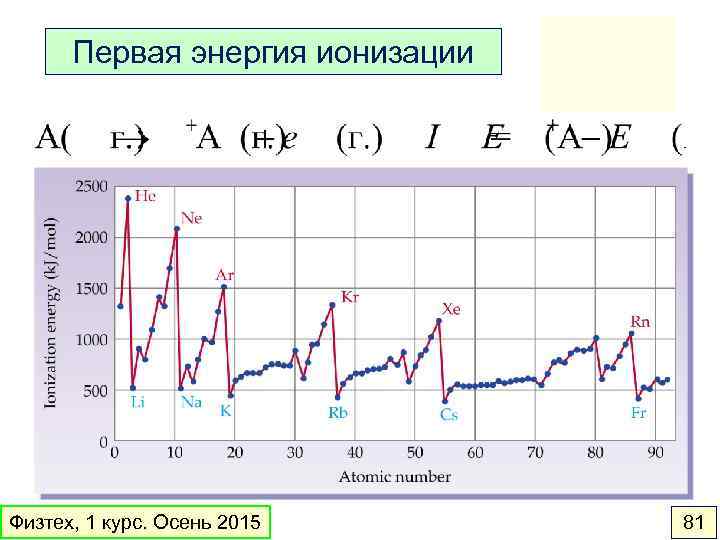 Первая энергия ионизации Физтех, 1 курс. Осень 2015 81
Первая энергия ионизации Физтех, 1 курс. Осень 2015 81
 Электроотрицательность Способность атома притягивать электроны химической связи в составе химического соединения Малликен Полинг Физтех, 1 курс. Осень 2015 82
Электроотрицательность Способность атома притягивать электроны химической связи в составе химического соединения Малликен Полинг Физтех, 1 курс. Осень 2015 82
 Электроотрицательность по Полингу Физтех, 1 курс. Осень 2015 83
Электроотрицательность по Полингу Физтех, 1 курс. Осень 2015 83
 Коротко о главном 1. Основные принципы квантовой механики – принцип неопределенности и принцип суперпозиции. Физические величины описываются операторами, а состояния систем – волновыми функциями. 2. Состояния электрона в водородоподобном атоме описываются орбиталями. Орбиталь характеризуется тремя квантовыми числами, а состояние электрона – пятью, из которых одно постоянное (спин s = ½), а четыре (n, l, ms) могут изменяться. 3. В многоэлектронных атомах электронная конфигурация характеризует распределение электронов по одноэлектронным орбиталям. 4. Орбитали заполняются электронами в порядке увеличения их энергии. На каждой орбитали может быть не больше 2 электронов. 5. Состояние атома как целого (терм) характеризуется полным орбитальным L и спиновым S моментами. 6. Периодические свойства элементов – радиус атома, энергия ионизации, электроотрицательность. Физтех, 1 курс. Осень 2015 84
Коротко о главном 1. Основные принципы квантовой механики – принцип неопределенности и принцип суперпозиции. Физические величины описываются операторами, а состояния систем – волновыми функциями. 2. Состояния электрона в водородоподобном атоме описываются орбиталями. Орбиталь характеризуется тремя квантовыми числами, а состояние электрона – пятью, из которых одно постоянное (спин s = ½), а четыре (n, l, ms) могут изменяться. 3. В многоэлектронных атомах электронная конфигурация характеризует распределение электронов по одноэлектронным орбиталям. 4. Орбитали заполняются электронами в порядке увеличения их энергии. На каждой орбитали может быть не больше 2 электронов. 5. Состояние атома как целого (терм) характеризуется полным орбитальным L и спиновым S моментами. 6. Периодические свойства элементов – радиус атома, энергия ионизации, электроотрицательность. Физтех, 1 курс. Осень 2015 84
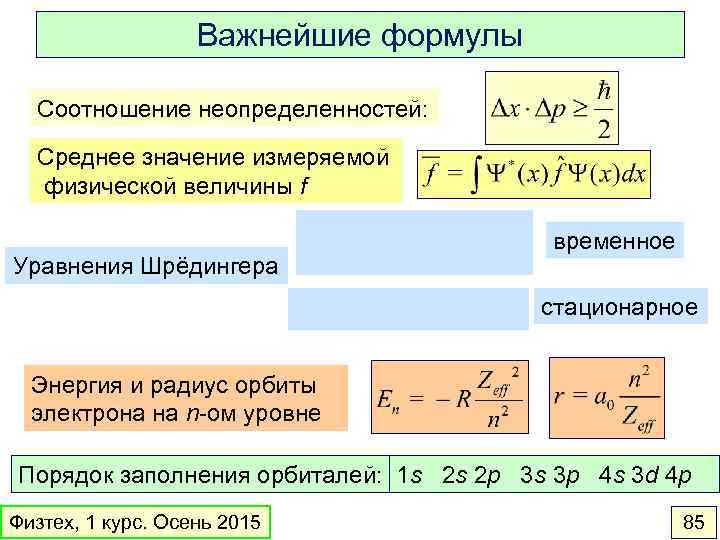 Важнейшие формулы Соотношение неопределенностей: Среднее значение измеряемой физической величины f Уравнения Шрёдингера временное стационарное Энергия и радиус орбиты электрона на n-ом уровне Порядок заполнения орбиталей: 1 s 2 s 2 p 3 s 3 p 4 s 3 d 4 p Физтех, 1 курс. Осень 2015 85
Важнейшие формулы Соотношение неопределенностей: Среднее значение измеряемой физической величины f Уравнения Шрёдингера временное стационарное Энергия и радиус орбиты электрона на n-ом уровне Порядок заполнения орбиталей: 1 s 2 s 2 p 3 s 3 p 4 s 3 d 4 p Физтех, 1 курс. Осень 2015 85
 Основные понятия § Оператор, волновая функция, уровень энергии § Водородоподобный атом (ион) § Квантовое число: главное, орбитальное, магнитное спиновое § Орбиталь § Радиальная и угловая часть волновой функции § Орбитальное приближение, эффективный заряд § Электронная конфигурация атома (иона) § Правило Хунда § Атомный терм, мультиплетность § Радиус атома (ковалентный, металлический) § Энергия ионизации § Электроотрицательность Физтех, 1 курс. Осень 2015 86
Основные понятия § Оператор, волновая функция, уровень энергии § Водородоподобный атом (ион) § Квантовое число: главное, орбитальное, магнитное спиновое § Орбиталь § Радиальная и угловая часть волновой функции § Орбитальное приближение, эффективный заряд § Электронная конфигурация атома (иона) § Правило Хунда § Атомный терм, мультиплетность § Радиус атома (ковалентный, металлический) § Энергия ионизации § Электроотрицательность Физтех, 1 курс. Осень 2015 86
 Литература 1. Еремин, Борщевский. Общая и неорганическая химия. – Гл. 12. (Очень подробно, подход физический, для углубленного уровня). 2. Глинка. Общая химия. – Глава 2, §§ 2. 2 -2. 6. (Химический подход, просто и понятно, но длинно). Глава 3, §§ 3. 1 -3. 4 – периодичность. 3. Шрайвер, Эткинс. Неорганическая химия. – Том 1, глава 1, §§ 1. 3 -1. 8. (Формул мало, изложение основано на качественном химическом подходе. Упражнения хорошие для углубленного уровня). 4. Ахметов. Общая и неорганическая химия. – Часть 1, раздел I, главы 2 -4. (Химический подход, физика упрощенная). Физтех, 1 курс. Осень 2015 87
Литература 1. Еремин, Борщевский. Общая и неорганическая химия. – Гл. 12. (Очень подробно, подход физический, для углубленного уровня). 2. Глинка. Общая химия. – Глава 2, §§ 2. 2 -2. 6. (Химический подход, просто и понятно, но длинно). Глава 3, §§ 3. 1 -3. 4 – периодичность. 3. Шрайвер, Эткинс. Неорганическая химия. – Том 1, глава 1, §§ 1. 3 -1. 8. (Формул мало, изложение основано на качественном химическом подходе. Упражнения хорошие для углубленного уровня). 4. Ахметов. Общая и неорганическая химия. – Часть 1, раздел I, главы 2 -4. (Химический подход, физика упрощенная). Физтех, 1 курс. Осень 2015 87
 Лекция 3 Химическая связь и строение молекул Физтех, 1 курс. Осень 2015
Лекция 3 Химическая связь и строение молекул Физтех, 1 курс. Осень 2015
 План лекции 1. Молекула. Образование химической связи между атомами 2. Типы химической связи 3. Ковалентная связь. Правило октета. Структуры Льюиса. Резонансные структуры 4. Характеристики химической связи – длина, энергия, полярность 5. Геометрия молекул. Модель ОЭПВО Физтех, 1 курс. Осень 2015 89
План лекции 1. Молекула. Образование химической связи между атомами 2. Типы химической связи 3. Ковалентная связь. Правило октета. Структуры Льюиса. Резонансные структуры 4. Характеристики химической связи – длина, энергия, полярность 5. Геометрия молекул. Модель ОЭПВО Физтех, 1 курс. Осень 2015 89
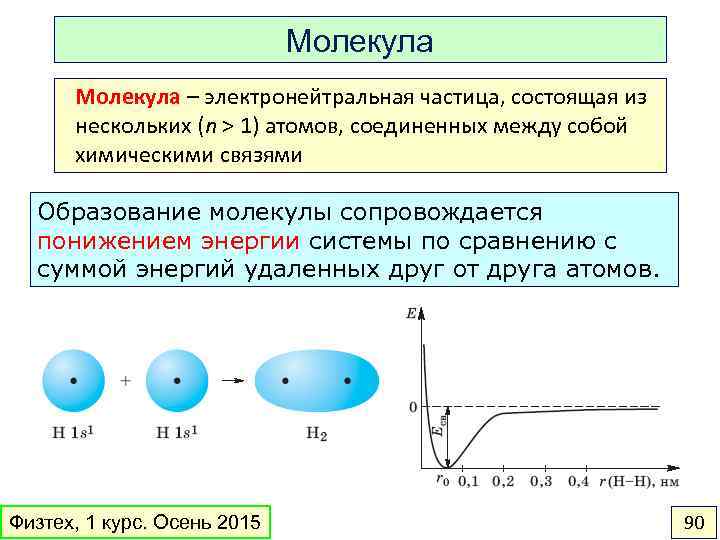 Молекула – электронейтральная частица, состоящая из нескольких (n > 1) атомов, соединенных между собой химическими связями Образование молекулы сопровождается понижением энергии системы по сравнению с суммой энергий удаленных друг от друга атомов. Физтех, 1 курс. Осень 2015 90
Молекула – электронейтральная частица, состоящая из нескольких (n > 1) атомов, соединенных между собой химическими связями Образование молекулы сопровождается понижением энергии системы по сравнению с суммой энергий удаленных друг от друга атомов. Физтех, 1 курс. Осень 2015 90
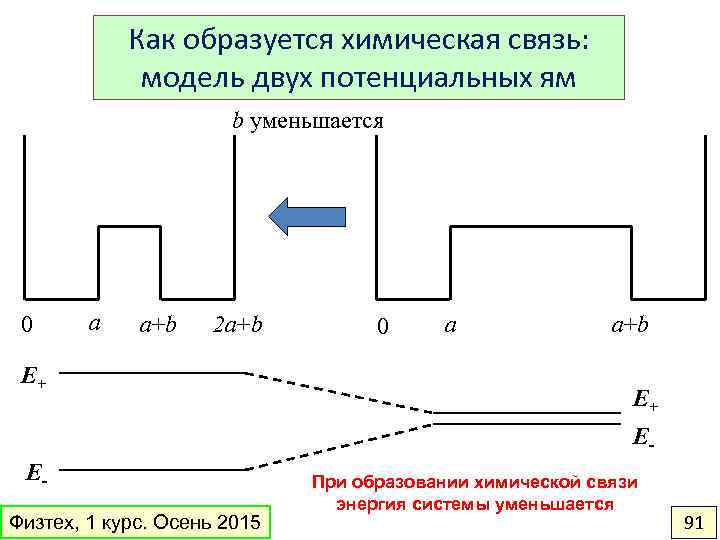 Как образуется химическая связь: модель двух потенциальных ям b уменьшается 0 a a+b 2 a+b E+ 0 a a+b E+ E- EФизтех, 1 курс. Осень 2015 При образовании химической связи энергия системы уменьшается 91
Как образуется химическая связь: модель двух потенциальных ям b уменьшается 0 a a+b 2 a+b E+ 0 a a+b E+ E- EФизтех, 1 курс. Осень 2015 При образовании химической связи энергия системы уменьшается 91
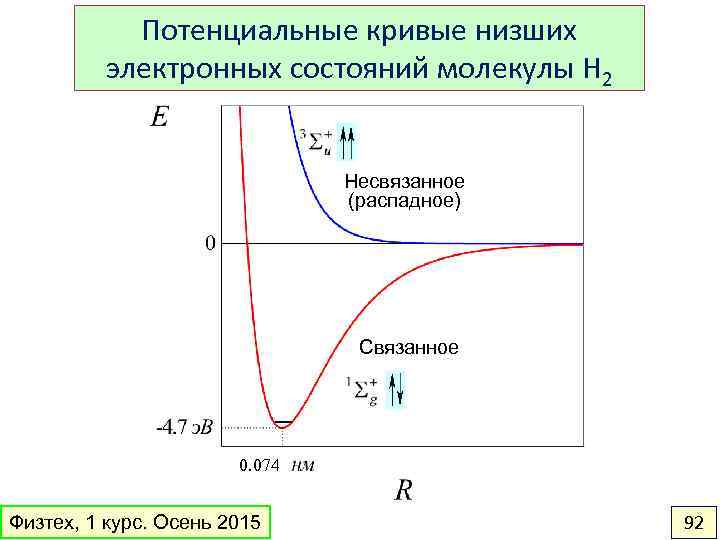 Потенциальные кривые низших электронных состояний молекулы H 2 Несвязанное (распадное) Связанное 0. 074 Физтех, 1 курс. Осень 2015 92
Потенциальные кривые низших электронных состояний молекулы H 2 Несвязанное (распадное) Связанное 0. 074 Физтех, 1 курс. Осень 2015 92
 Химическая связь • Химическая связь – взаимодействие между атомами, приводящее к понижению общей энергии системы. • Взаимодействие имеет преимущественно электростатический характер (обобществление электронов, переход электрона, кулоновское притяжение). Физтех, 1 курс. Осень 2015 93
Химическая связь • Химическая связь – взаимодействие между атомами, приводящее к понижению общей энергии системы. • Взаимодействие имеет преимущественно электростатический характер (обобществление электронов, переход электрона, кулоновское притяжение). Физтех, 1 курс. Осень 2015 93
 Виды химической связи • Ковалентная – внутримолекулярная связь между атомами, осуществляемая за счет общих пар электронов. • Ионная – связь между ионами, образовавшимися при переходе электрона от одного атома к другому. • Металлическая – связь между атомами металлов в твердой фазе • Водородная – межмолекулярная связь между положительно заряженным атомом водорода одной молекулы и отрицательно заряженным атомом неметалла другой молекулы • Ван-дер-ваальсова – межмолекулярная связь, притяжение дипольных моментов молекул (постоянных или индуцированных). Физтех, 1 курс. Осень 2015 94
Виды химической связи • Ковалентная – внутримолекулярная связь между атомами, осуществляемая за счет общих пар электронов. • Ионная – связь между ионами, образовавшимися при переходе электрона от одного атома к другому. • Металлическая – связь между атомами металлов в твердой фазе • Водородная – межмолекулярная связь между положительно заряженным атомом водорода одной молекулы и отрицательно заряженным атомом неметалла другой молекулы • Ван-дер-ваальсова – межмолекулярная связь, притяжение дипольных моментов молекул (постоянных или индуцированных). Физтех, 1 курс. Осень 2015 94
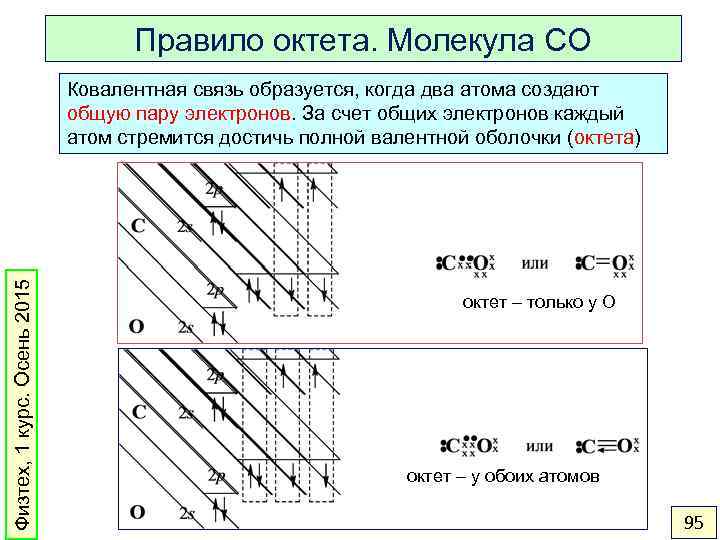 Правило октета. Молекула CO Физтех, 1 курс. Осень 2015 Ковалентная связь образуется, когда два атома создают общую пару электронов. За счет общих электронов каждый атом стремится достичь полной валентной оболочки (октета) октет – только у O октет – у обоих атомов 95
Правило октета. Молекула CO Физтех, 1 курс. Осень 2015 Ковалентная связь образуется, когда два атома создают общую пару электронов. За счет общих электронов каждый атом стремится достичь полной валентной оболочки (октета) октет – только у O октет – у обоих атомов 95
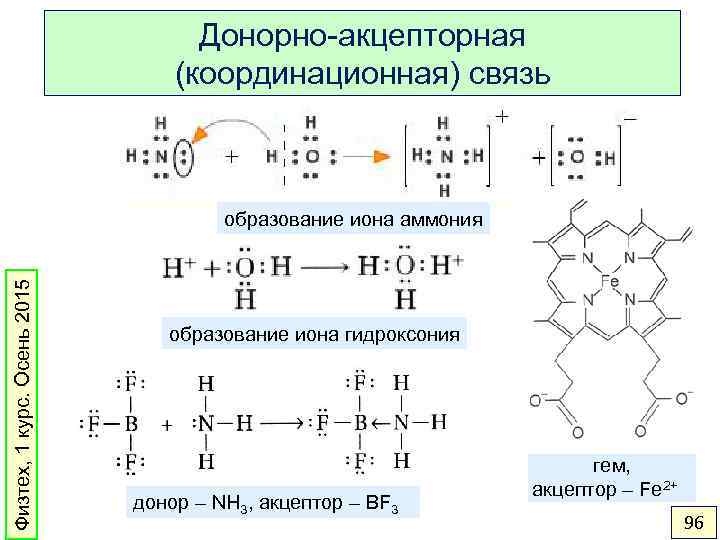 Донорно-акцепторная (координационная) связь Физтех, 1 курс. Осень 2015 образование иона аммония образование иона гидроксония донор – NH 3, акцептор – BF 3 гем, акцептор – Fe 2+ 96
Донорно-акцепторная (координационная) связь Физтех, 1 курс. Осень 2015 образование иона аммония образование иона гидроксония донор – NH 3, акцептор – BF 3 гем, акцептор – Fe 2+ 96
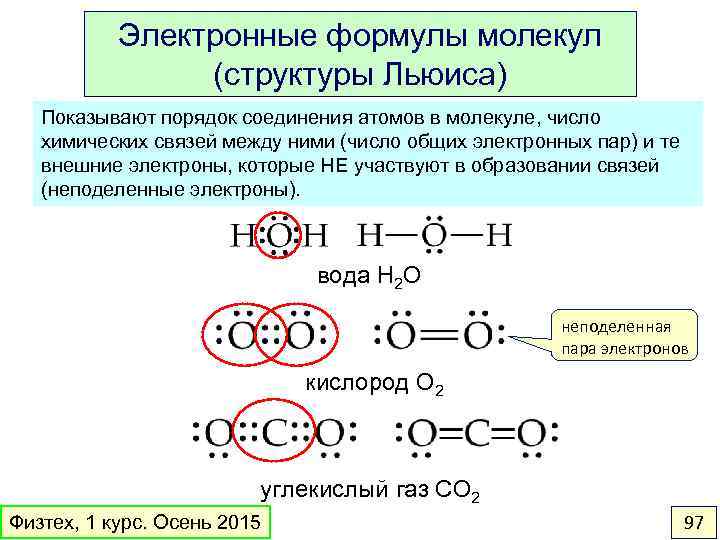 Электронные формулы молекул (структуры Льюиса) Показывают порядок соединения атомов в молекуле, число химических связей между ними (число общих электронных пар) и те внешние электроны, которые НЕ участвуют в образовании связей (неподеленные электроны). вода H 2 O неподеленная пара электронов кислород O 2 углекислый газ CO 2 Физтех, 1 курс. Осень 2015 97
Электронные формулы молекул (структуры Льюиса) Показывают порядок соединения атомов в молекуле, число химических связей между ними (число общих электронных пар) и те внешние электроны, которые НЕ участвуют в образовании связей (неподеленные электроны). вода H 2 O неподеленная пара электронов кислород O 2 углекислый газ CO 2 Физтех, 1 курс. Осень 2015 97
 Резонансные структуры Резонанс: молекула – суперпозиция льюисовских структур Физтех, 1 курс. Осень 2015 98
Резонансные структуры Резонанс: молекула – суперпозиция льюисовских структур Физтех, 1 курс. Осень 2015 98
 Валентность – одно из основных понятий в химии Валентность – число ковалентных химических связей (общих электронных пар), которые данный атом образует с другими атомами в молекуле или ионе. Пример – оксид азота (I) N 2 O Атомы азота: средняя степень окисления +1, валентность центрального атома – IV, крайнего – средняя между II или III Физтех, 1 курс. Осень 2015 99
Валентность – одно из основных понятий в химии Валентность – число ковалентных химических связей (общих электронных пар), которые данный атом образует с другими атомами в молекуле или ионе. Пример – оксид азота (I) N 2 O Атомы азота: средняя степень окисления +1, валентность центрального атома – IV, крайнего – средняя между II или III Физтех, 1 курс. Осень 2015 99
 Более общее определение валентности (ИЮПАК) Валентность - число одновалентных атомов (групп атомов), с которыми может соединиться данный атом или которые он может заместить. Пример: H – одновалентен H–Cl следовательно Cl одновалентен Na. Cl следовательно Na одновалентен H 2 SO 4 следовательно сульфат SO 4 двухвалентен Для молекулярных соединений эти два определения совпадают. У ионных соединений валентность элементов определена только по ИЮПАК. Физтех, 1 курс. Осень 2015 100
Более общее определение валентности (ИЮПАК) Валентность - число одновалентных атомов (групп атомов), с которыми может соединиться данный атом или которые он может заместить. Пример: H – одновалентен H–Cl следовательно Cl одновалентен Na. Cl следовательно Na одновалентен H 2 SO 4 следовательно сульфат SO 4 двухвалентен Для молекулярных соединений эти два определения совпадают. У ионных соединений валентность элементов определена только по ИЮПАК. Физтех, 1 курс. Осень 2015 100
 Химические ошибки в физических статьях (найдите две) Физтех, 1 курс. Осень 2015 101
Химические ошибки в физических статьях (найдите две) Физтех, 1 курс. Осень 2015 101
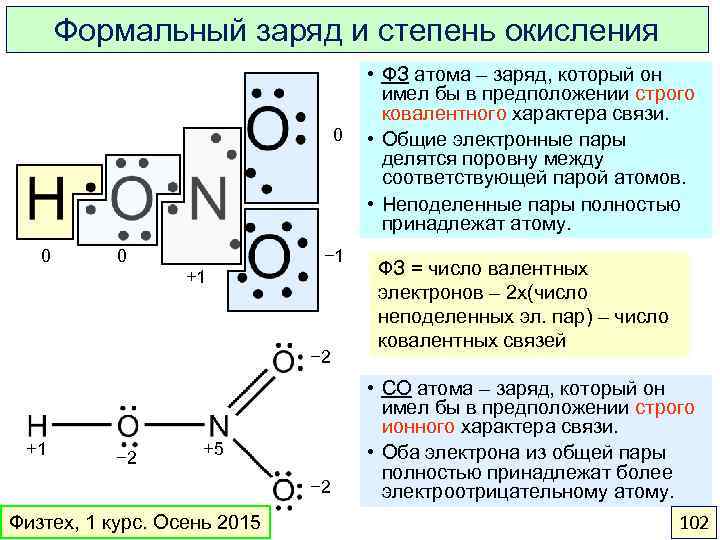 Формальный заряд и степень окисления 0 0 − 1 0 +1 − 2 +5 − 2 Физтех, 1 курс. Осень 2015 • ФЗ атома – заряд, который он имел бы в предположении строго ковалентного характера связи. • Общие электронные пары делятся поровну между соответствующей парой атомов. • Неподеленные пары полностью принадлежат атому. ФЗ = число валентных электронов – 2 x(число неподеленных эл. пар) – число ковалентных связей • СО атома – заряд, который он имел бы в предположении строго ионного характера связи. • Оба электрона из общей пары полностью принадлежат более электроотрицательному атому. 102
Формальный заряд и степень окисления 0 0 − 1 0 +1 − 2 +5 − 2 Физтех, 1 курс. Осень 2015 • ФЗ атома – заряд, который он имел бы в предположении строго ковалентного характера связи. • Общие электронные пары делятся поровну между соответствующей парой атомов. • Неподеленные пары полностью принадлежат атому. ФЗ = число валентных электронов – 2 x(число неподеленных эл. пар) – число ковалентных связей • СО атома – заряд, который он имел бы в предположении строго ионного характера связи. • Оба электрона из общей пары полностью принадлежат более электроотрицательному атому. 102
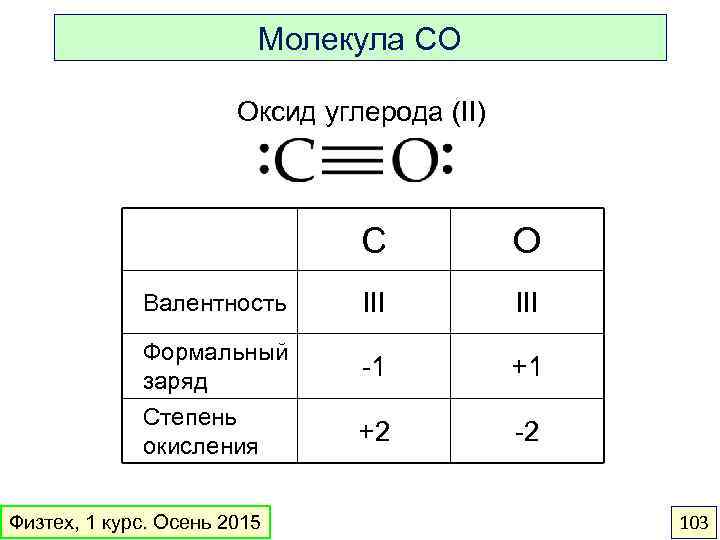 Молекула CO Оксид углерода (II) C O Валентность III Формальный заряд -1 +1 Степень окисления +2 -2 Физтех, 1 курс. Осень 2015 103
Молекула CO Оксид углерода (II) C O Валентность III Формальный заряд -1 +1 Степень окисления +2 -2 Физтех, 1 курс. Осень 2015 103
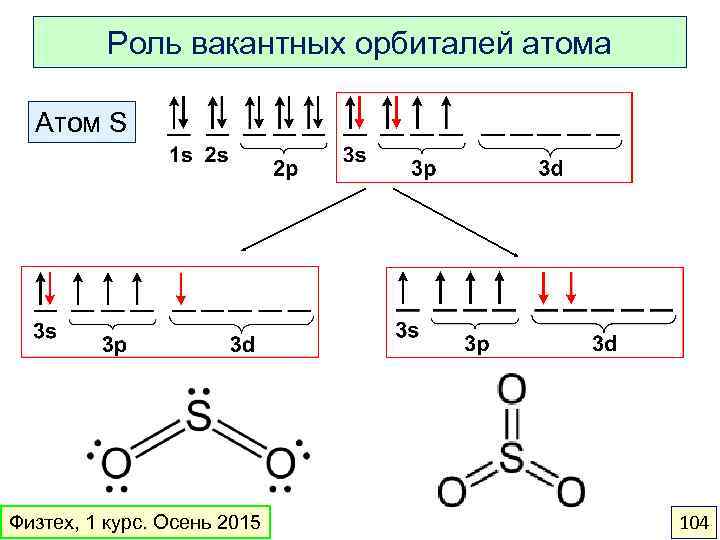 Роль вакантных орбиталей атома Атом S Физтех, 1 курс. Осень 2015 104
Роль вакантных орбиталей атома Атом S Физтех, 1 курс. Осень 2015 104
 Основные характеристики ковалентной связи 1. Кратность (порядок связи) – число электронных пар 2. Длина связи – расстояние между ядрами, при котором энергия молекулы – наименьшая 3. Энергия связи – выигрыш в энергии при образовании связи из разъединённых фрагментов (атомов) 4. Полярность связи – характеризует степень смещения электронной плотности к одному из двух атомов, образующих связь Физтех, 1 курс. Осень 2015 105
Основные характеристики ковалентной связи 1. Кратность (порядок связи) – число электронных пар 2. Длина связи – расстояние между ядрами, при котором энергия молекулы – наименьшая 3. Энергия связи – выигрыш в энергии при образовании связи из разъединённых фрагментов (атомов) 4. Полярность связи – характеризует степень смещения электронной плотности к одному из двух атомов, образующих связь Физтех, 1 курс. Осень 2015 105
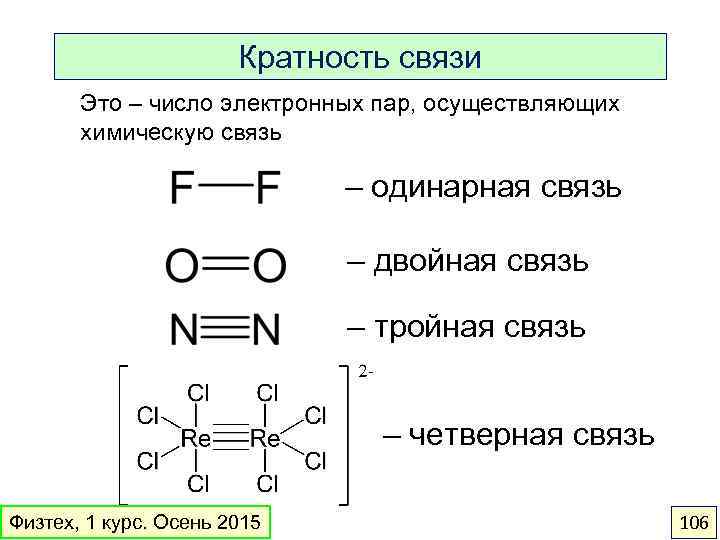 Кратность связи Это – число электронных пар, осуществляющих химическую связь – одинарная связь – двойная связь – тройная связь – четверная связь Физтех, 1 курс. Осень 2015 106
Кратность связи Это – число электронных пар, осуществляющих химическую связь – одинарная связь – двойная связь – тройная связь – четверная связь Физтех, 1 курс. Осень 2015 106
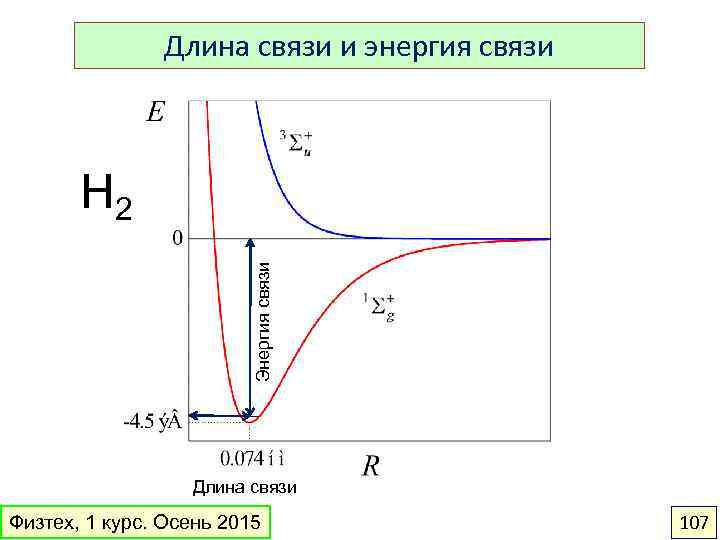 Длина связи и энергия связи Энергия связи H 2 Длина связи Физтех, 1 курс. Осень 2015 107
Длина связи и энергия связи Энергия связи H 2 Длина связи Физтех, 1 курс. Осень 2015 107
 Длина связи – расстояние между ядрами связанных атомов. Измеряют в нанометрах. 4 Физтех, 1 курс. Осень 2015 Самая короткая связь: H–H (0, 074 нм) Самая длинная связь: I–I (0, 267 нм) 108
Длина связи – расстояние между ядрами связанных атомов. Измеряют в нанометрах. 4 Физтех, 1 курс. Осень 2015 Самая короткая связь: H–H (0, 074 нм) Самая длинная связь: I–I (0, 267 нм) 108
 Энергия связи – энергия, необходимая для разрыва химической связи и разделения полученных фрагментов на бесконечное расстояние E(H–H) = 436 к. Дж/моль. H 2(г) = H(г) + H(г) – 436 к. Дж/моль H(г) + H(г) = H 2(г) + 436 к. Дж/моль Самая прочная ковалентная связь: C O (1076 к. Дж/моль) Самая слабая ковалентная связь: N–N в N 2 O 3 (41 к. Дж/моль) Физтех, 1 курс. Осень 2015 109
Энергия связи – энергия, необходимая для разрыва химической связи и разделения полученных фрагментов на бесконечное расстояние E(H–H) = 436 к. Дж/моль. H 2(г) = H(г) + H(г) – 436 к. Дж/моль H(г) + H(г) = H 2(г) + 436 к. Дж/моль Самая прочная ковалентная связь: C O (1076 к. Дж/моль) Самая слабая ковалентная связь: N–N в N 2 O 3 (41 к. Дж/моль) Физтех, 1 курс. Осень 2015 109
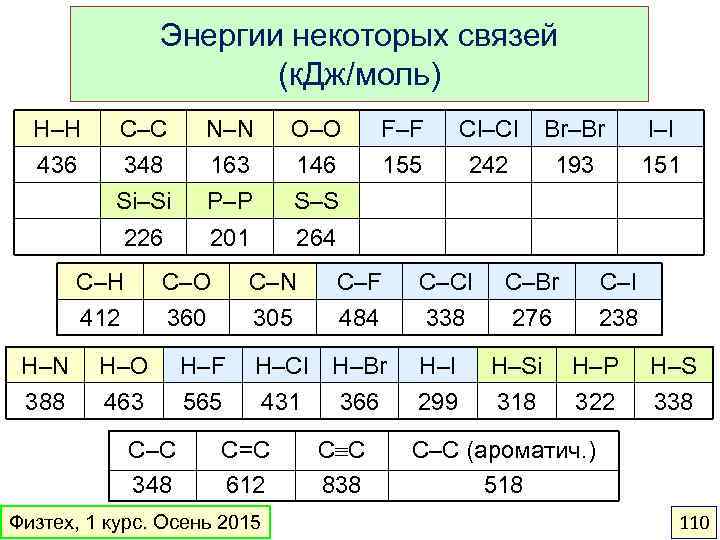 Энергии некоторых связей (к. Дж/моль) H–H 436 C–C 348 Si–Si N–N 163 P–P O–O 146 S–S 226 201 264 C–H 412 H–N 388 C–O 360 H–O 463 C–C 348 F–F 155 Cl–Cl 242 C–N 305 H–F 565 C–F 484 C–Cl 338 H–Cl 431 H–Br 366 H–I 299 C=C 612 Физтех, 1 курс. Осень 2015 C C 838 Br–Br 193 C–Br 276 H–Si 318 I–I 151 C–I 238 H–P 322 H–S 338 C–C (ароматич. ) 518 110
Энергии некоторых связей (к. Дж/моль) H–H 436 C–C 348 Si–Si N–N 163 P–P O–O 146 S–S 226 201 264 C–H 412 H–N 388 C–O 360 H–O 463 C–C 348 F–F 155 Cl–Cl 242 C–N 305 H–F 565 C–F 484 C–Cl 338 H–Cl 431 H–Br 366 H–I 299 C=C 612 Физтех, 1 курс. Осень 2015 C C 838 Br–Br 193 C–Br 276 H–Si 318 I–I 151 C–I 238 H–P 322 H–S 338 C–C (ароматич. ) 518 110
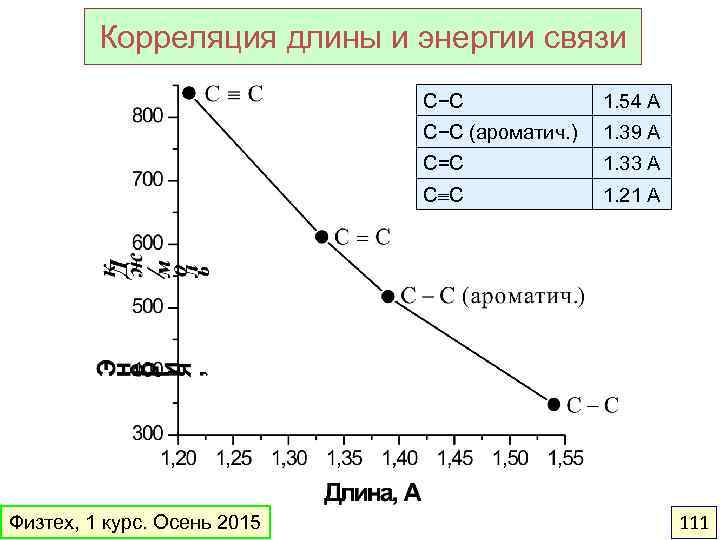 Корреляция длины и энергии связи С−С (ароматич. ) 1. 39 А С=С 1. 33 А С С Физтех, 1 курс. Осень 2015 1. 54 А 1. 21 А 111
Корреляция длины и энергии связи С−С (ароматич. ) 1. 39 А С=С 1. 33 А С С Физтех, 1 курс. Осень 2015 1. 54 А 1. 21 А 111
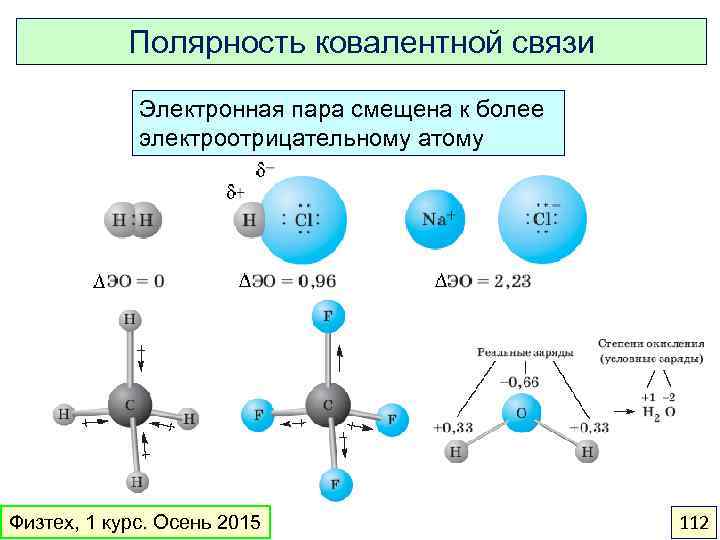 Полярность ковалентной связи Электронная пара смещена к более электроотрицательному атому Физтех, 1 курс. Осень 2015 112
Полярность ковалентной связи Электронная пара смещена к более электроотрицательному атому Физтех, 1 курс. Осень 2015 112
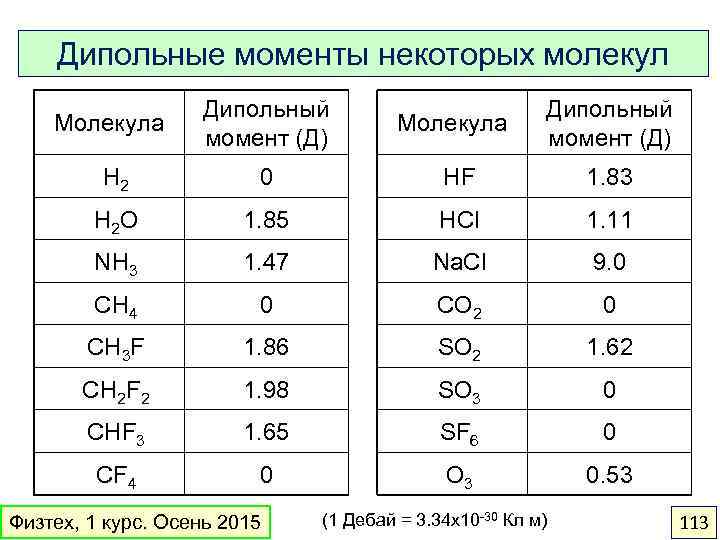 Дипольные моменты некоторых молекул Молекула Дипольный момент (Д) H 2 0 HF 1. 83 H 2 O 1. 85 HCl 1. 11 NH 3 1. 47 Na. Cl 9. 0 CH 4 0 CO 2 0 CH 3 F 1. 86 SO 2 1. 62 CH 2 F 2 1. 98 SO 3 0 CHF 3 1. 65 SF 6 0 CF 4 0 O 3 0. 53 Физтех, 1 курс. Осень 2015 (1 Дебай = 3. 34 х10 -30 Кл м) 113
Дипольные моменты некоторых молекул Молекула Дипольный момент (Д) H 2 0 HF 1. 83 H 2 O 1. 85 HCl 1. 11 NH 3 1. 47 Na. Cl 9. 0 CH 4 0 CO 2 0 CH 3 F 1. 86 SO 2 1. 62 CH 2 F 2 1. 98 SO 3 0 CHF 3 1. 65 SF 6 0 CF 4 0 O 3 0. 53 Физтех, 1 курс. Осень 2015 (1 Дебай = 3. 34 х10 -30 Кл м) 113
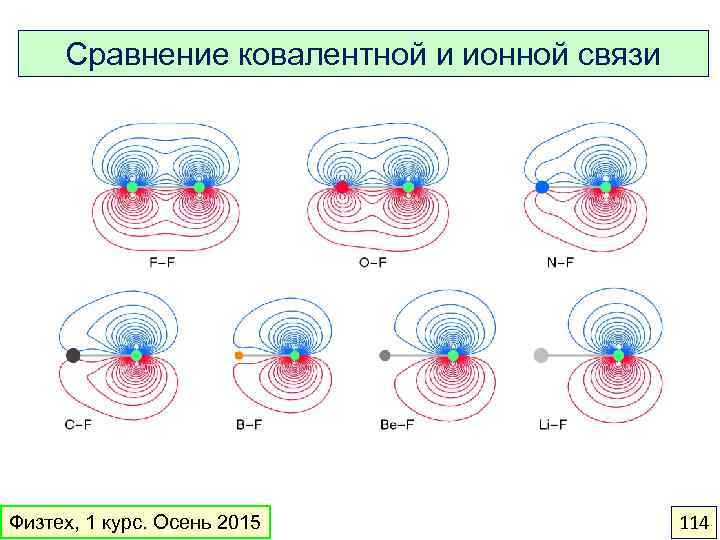 Сравнение ковалентной и ионной связи Физтех, 1 курс. Осень 2015 114
Сравнение ковалентной и ионной связи Физтех, 1 курс. Осень 2015 114
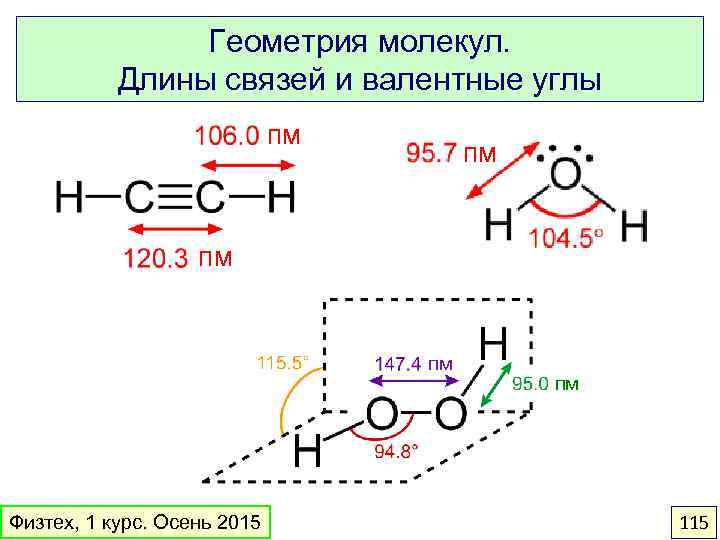 Геометрия молекул. Длины связей и валентные углы пм пм Физтех, 1 курс. Осень 2015 пм 115
Геометрия молекул. Длины связей и валентные углы пм пм Физтех, 1 курс. Осень 2015 пм 115
 Как предсказать геометрию? Модель ОЭПВО Области повышенной электронной плотности – электронные пары связей и неподеленные пары – располагаются на максимальном удалении друг от друга. Физтех, 1 курс. Осень 2015 116
Как предсказать геометрию? Модель ОЭПВО Области повышенной электронной плотности – электронные пары связей и неподеленные пары – располагаются на максимальном удалении друг от друга. Физтех, 1 курс. Осень 2015 116
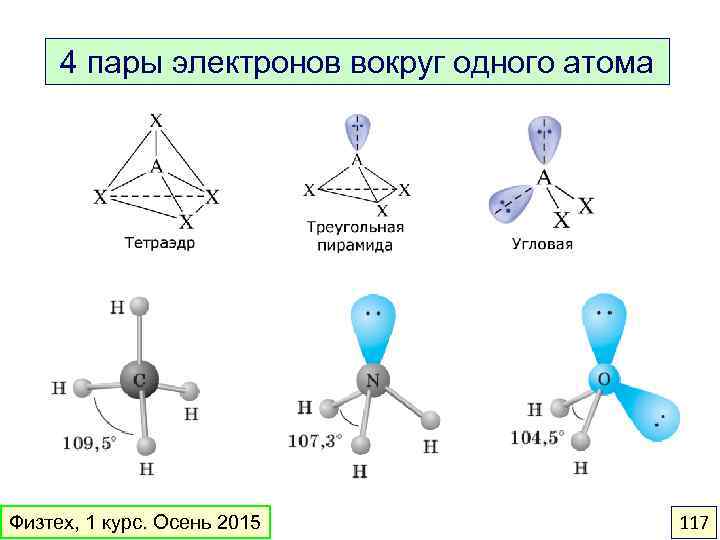 4 пары электронов вокруг одного атома Физтех, 1 курс. Осень 2015 117
4 пары электронов вокруг одного атома Физтех, 1 курс. Осень 2015 117
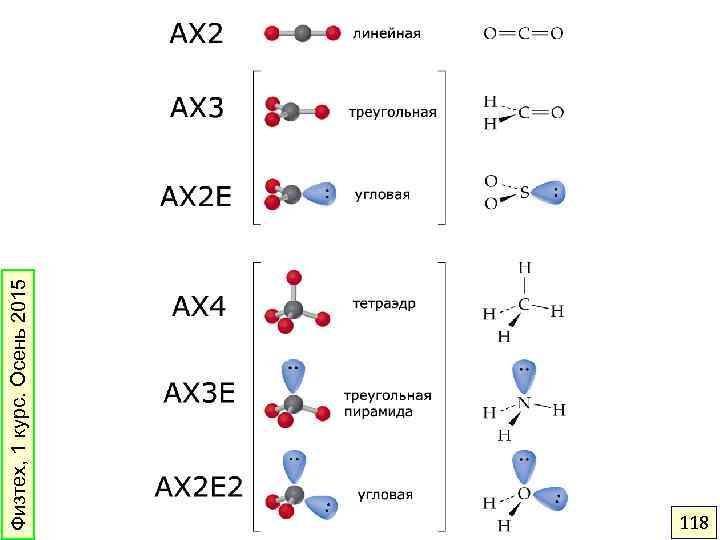 Физтех, 1 курс. Осень 2015 118
Физтех, 1 курс. Осень 2015 118
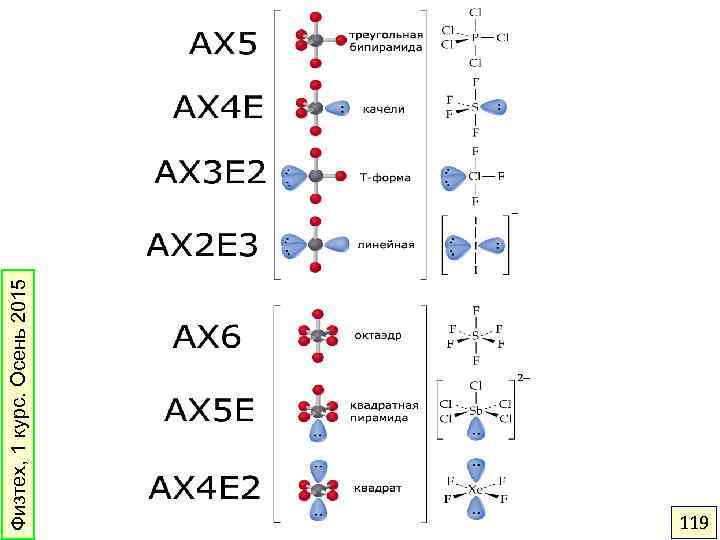 Физтех, 1 курс. Осень 2015 119
Физтех, 1 курс. Осень 2015 119
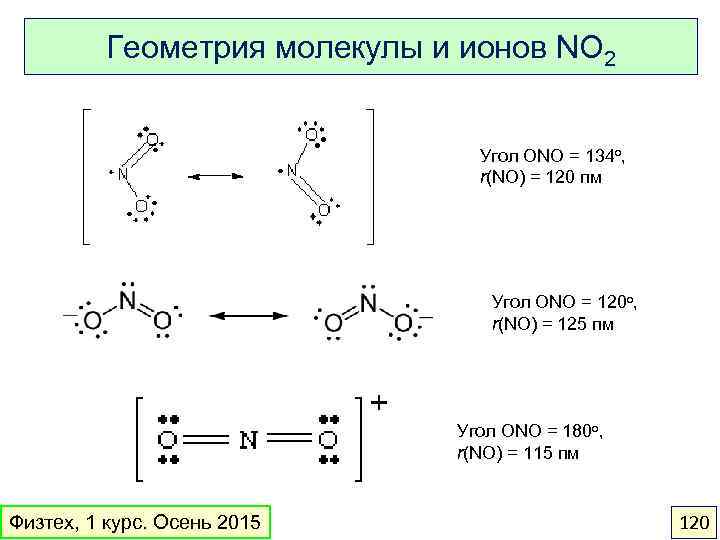 Геометрия молекулы и ионов NO 2 Угол ONO = 134 o, r(NO) = 120 пм Угол ONO = 120 o, r(NO) = 125 пм Угол ONO = 180 o, r(NO) = 115 пм Физтех, 1 курс. Осень 2015 120
Геометрия молекулы и ионов NO 2 Угол ONO = 134 o, r(NO) = 120 пм Угол ONO = 120 o, r(NO) = 125 пм Угол ONO = 180 o, r(NO) = 115 пм Физтех, 1 курс. Осень 2015 120
 Коротко о главном 1. Химическая связь – взаимодействие атомов, которое приводит к уменьшению энергии системы, в частности – к образованию молекул. 2. Ковалентная связь образуется, когда два атома создают общую пару электронов с тем, чтобы достичь полной валентной оболочки. 3. Основные характеристики химической связи: порядок (кратность), длина, энергия. С увеличением порядка длина связи уменьшается, а энергия увеличивается. 4. Геометрия молекул (валентные углы) определяется отталкиванием электронных пар химических связей и неподеленных электронных пар. Физтех, 1 курс. Осень 2015 121
Коротко о главном 1. Химическая связь – взаимодействие атомов, которое приводит к уменьшению энергии системы, в частности – к образованию молекул. 2. Ковалентная связь образуется, когда два атома создают общую пару электронов с тем, чтобы достичь полной валентной оболочки. 3. Основные характеристики химической связи: порядок (кратность), длина, энергия. С увеличением порядка длина связи уменьшается, а энергия увеличивается. 4. Геометрия молекул (валентные углы) определяется отталкиванием электронных пар химических связей и неподеленных электронных пар. Физтех, 1 курс. Осень 2015 121
 Основные понятия § § § Молекула Химическая связь Ковалентная связь. Правило октета Валентность, степень окисления Структура Льюиса Характеристики химической связи: - кратность связи - длина связи - энергия связи - полярность, дипольный момент § Геометрия молекул: длины связей, валентные углы § Модель отталкивания электронных пар Физтех, 1 курс. Осень 2015 122
Основные понятия § § § Молекула Химическая связь Ковалентная связь. Правило октета Валентность, степень окисления Структура Льюиса Характеристики химической связи: - кратность связи - длина связи - энергия связи - полярность, дипольный момент § Геометрия молекул: длины связей, валентные углы § Модель отталкивания электронных пар Физтех, 1 курс. Осень 2015 122
 Типичные задачи 1. Изобразите льюисову структуру молекулы озона (CO, CO 2, N 2 O, NH 3, H 2 SO 4, SO 42 -). Определите степени окисления и формальные заряды на атомах. 2. Предскажите геометрическую форму молекулы CO 2 (SO 2, NH 3, COCl 2, PCl 5, POCl 3). Установите, полярна данная молекула или нет. Физтех, 1 курс. Осень 2015 123
Типичные задачи 1. Изобразите льюисову структуру молекулы озона (CO, CO 2, N 2 O, NH 3, H 2 SO 4, SO 42 -). Определите степени окисления и формальные заряды на атомах. 2. Предскажите геометрическую форму молекулы CO 2 (SO 2, NH 3, COCl 2, PCl 5, POCl 3). Установите, полярна данная молекула или нет. Физтех, 1 курс. Осень 2015 123
 Литература 1. Еремин, Борщевский. Общая и неорганическая химия. – Гл. 13, §§ 13. 2 -13. 4. 2. Шрайвер, Эткинс. Неорганическая химия. – Том 1, глава 3, §§ 3. 1 -3. 3. (По этой теме – проще всего). 3. Еремин. Теоретическая и математическая химия. – Гл. 2. § 5. 4. Глинка. Общая химия. – Глава 4. (Сложновато и слишком длинно для первого чтения, упор сделан на теорию МО) 5. Полинг. Природа химической связи. – М. , 1947. (Совершенная классика! Только для дополнительного чтения) Физтех, 1 курс. Осень 2015 124
Литература 1. Еремин, Борщевский. Общая и неорганическая химия. – Гл. 13, §§ 13. 2 -13. 4. 2. Шрайвер, Эткинс. Неорганическая химия. – Том 1, глава 3, §§ 3. 1 -3. 3. (По этой теме – проще всего). 3. Еремин. Теоретическая и математическая химия. – Гл. 2. § 5. 4. Глинка. Общая химия. – Глава 4. (Сложновато и слишком длинно для первого чтения, упор сделан на теорию МО) 5. Полинг. Природа химической связи. – М. , 1947. (Совершенная классика! Только для дополнительного чтения) Физтех, 1 курс. Осень 2015 124
 Лекция 4 Электронные состояния молекул. Межмолекулярные связи Физтех, 1 курс. Осень 2015 12
Лекция 4 Электронные состояния молекул. Межмолекулярные связи Физтех, 1 курс. Осень 2015 12
 План лекции 1. Разделение движения ядер и электронов. Адиабатическое приближение. Электронные состояния молекул 2. Метод валентных связей. Гибридизация АО 3. Молекулярные орбитали. Метод МО-ЛКАО 4. Межмолекулярные взаимодействия: а) ван-дер-ваальсова связь б) водородная связь Физтех, 1 курс. Осень 2015 12
План лекции 1. Разделение движения ядер и электронов. Адиабатическое приближение. Электронные состояния молекул 2. Метод валентных связей. Гибридизация АО 3. Молекулярные орбитали. Метод МО-ЛКАО 4. Межмолекулярные взаимодействия: а) ван-дер-ваальсова связь б) водородная связь Физтех, 1 курс. Осень 2015 12
 Что может квантовая механика 1. Рассчитать уровни энергии и волновые функции молекулы. 2. Определить геометрию молекулы – расстояния между ядрами, при которых энергия имеет глобальный минимум. 3. Рассчитать свойства молекулы: заряды на атомах, дипольный момент, порядки связей Квантовая механика в состоянии адекватно объяснить: ü Спектры молекул. ü Соединение атомов в молекулу, ее устойчивость или неустойчивость. ü Порядок образования и свойства химических связей. Физтех, 1 курс. Осень 2015 12
Что может квантовая механика 1. Рассчитать уровни энергии и волновые функции молекулы. 2. Определить геометрию молекулы – расстояния между ядрами, при которых энергия имеет глобальный минимум. 3. Рассчитать свойства молекулы: заряды на атомах, дипольный момент, порядки связей Квантовая механика в состоянии адекватно объяснить: ü Спектры молекул. ü Соединение атомов в молекулу, ее устойчивость или неустойчивость. ü Порядок образования и свойства химических связей. Физтех, 1 курс. Осень 2015 12
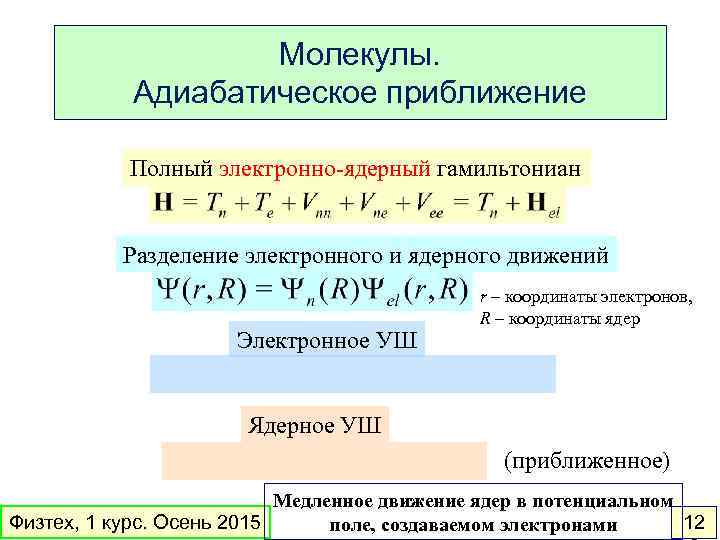 Молекулы. Адиабатическое приближение Полный электронно-ядерный гамильтониан Разделение электронного и ядерного движений Электронное УШ r – координаты электронов, R – координаты ядер Ядерное УШ (приближенное) Медленное движение ядер в потенциальном Физтех, 1 курс. Осень 2015 12 поле, создаваемом электронами
Молекулы. Адиабатическое приближение Полный электронно-ядерный гамильтониан Разделение электронного и ядерного движений Электронное УШ r – координаты электронов, R – координаты ядер Ядерное УШ (приближенное) Медленное движение ядер в потенциальном Физтех, 1 курс. Осень 2015 12 поле, создаваемом электронами
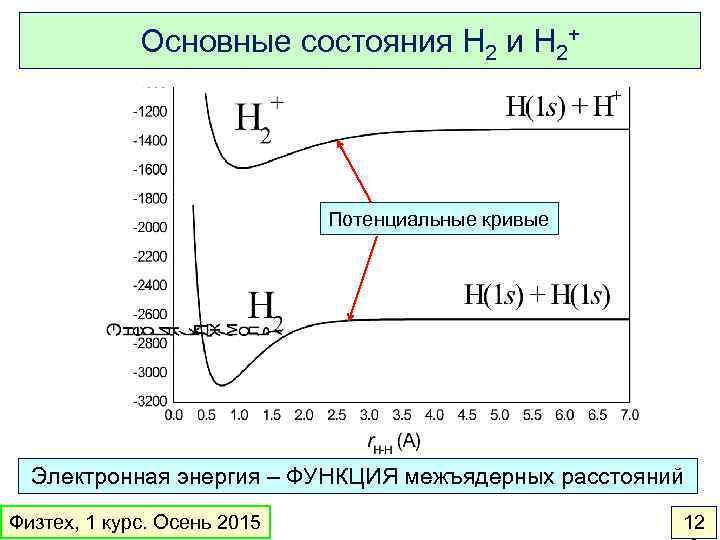 Основные состояния H 2 и H 2+ Потенциальные кривые Электронная энергия – ФУНКЦИЯ межъядерных расстояний Физтех, 1 курс. Осень 2015 12
Основные состояния H 2 и H 2+ Потенциальные кривые Электронная энергия – ФУНКЦИЯ межъядерных расстояний Физтех, 1 курс. Осень 2015 12
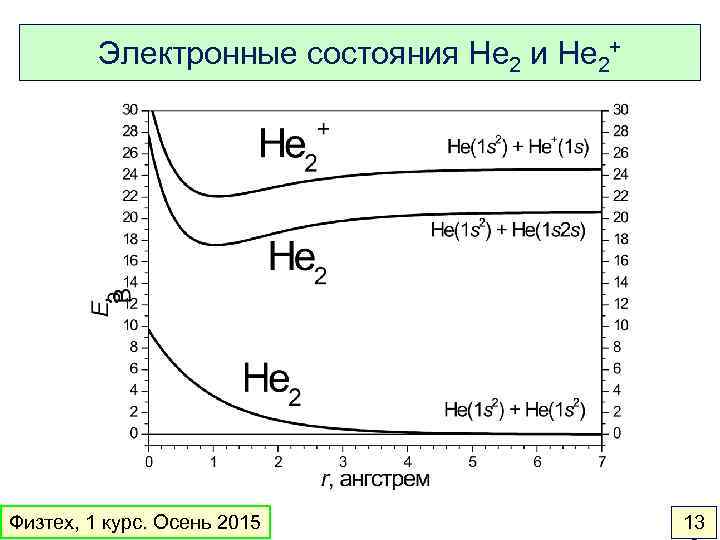 Электронные состояния He 2 и He 2+ Физтех, 1 курс. Осень 2015 13
Электронные состояния He 2 и He 2+ Физтех, 1 курс. Осень 2015 13
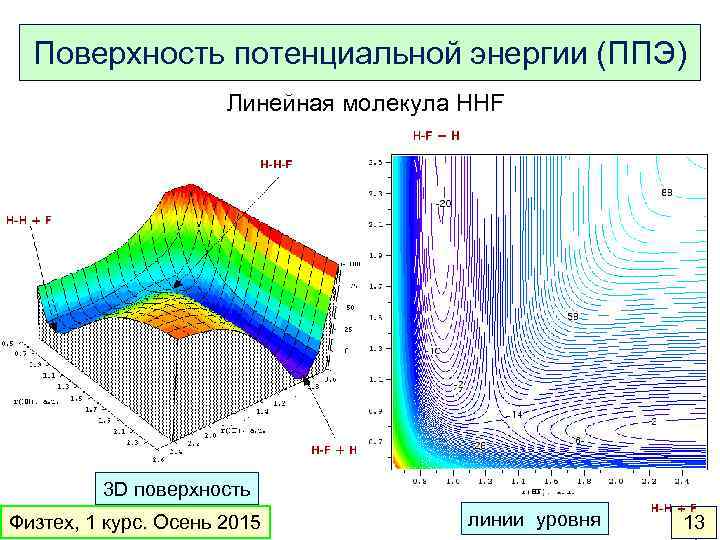 Поверхность потенциальной энергии (ППЭ) Линейная молекула HHF 3 D поверхность Физтех, 1 курс. Осень 2015 линии уровня 13
Поверхность потенциальной энергии (ППЭ) Линейная молекула HHF 3 D поверхность Физтех, 1 курс. Осень 2015 линии уровня 13
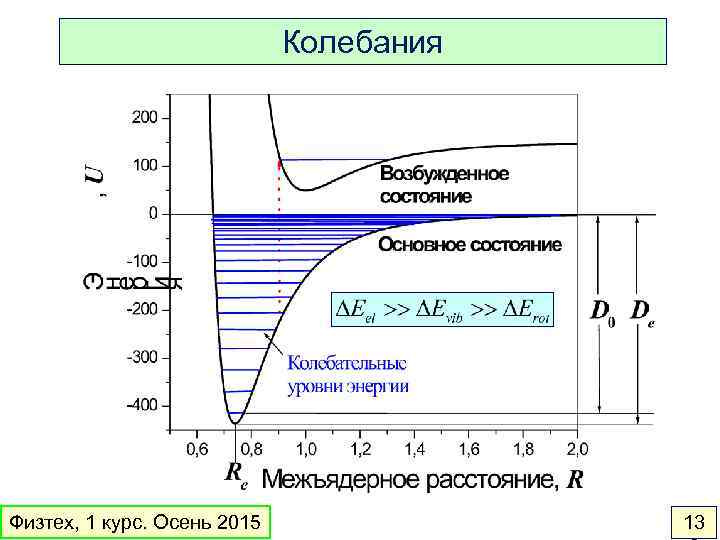 Колебания Физтех, 1 курс. Осень 2015 13
Колебания Физтех, 1 курс. Осень 2015 13
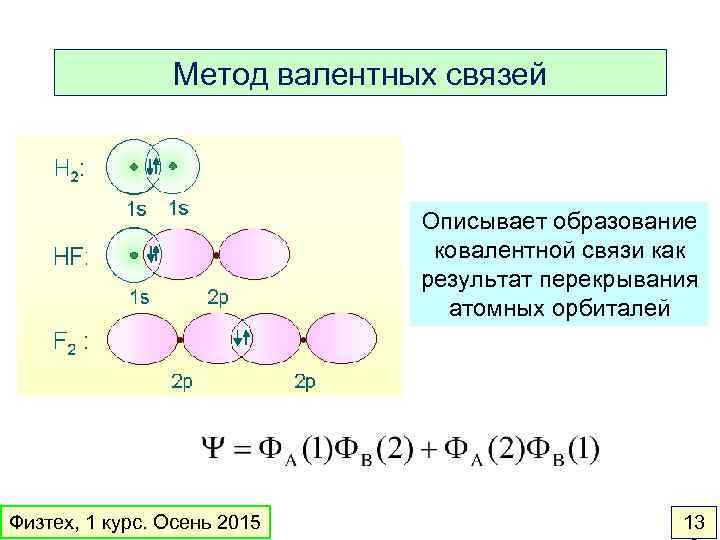 Метод валентных связей Описывает образование ковалентной связи как результат перекрывания атомных орбиталей Физтех, 1 курс. Осень 2015 13
Метод валентных связей Описывает образование ковалентной связи как результат перекрывания атомных орбиталей Физтех, 1 курс. Осень 2015 13
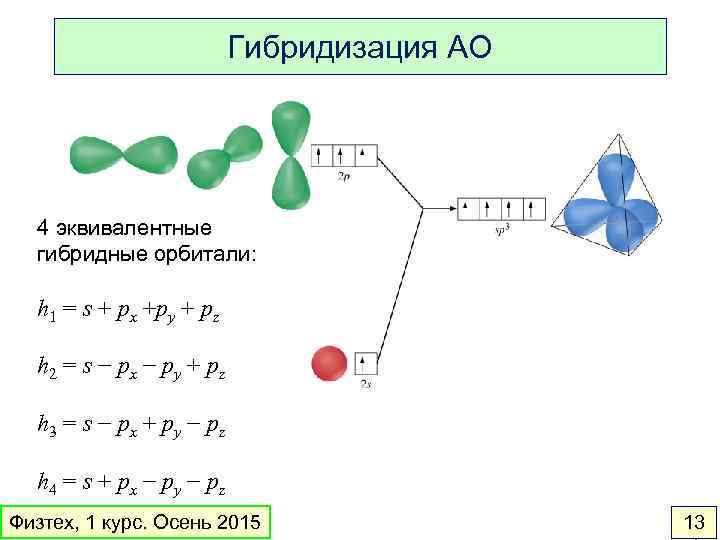 Гибридизация АО 4 эквивалентные гибридные орбитали: h 1 = s + px +py + pz h 2 = s − px − py + pz h 3 = s − px + py − pz h 4 = s + px − py − pz Физтех, 1 курс. Осень 2015 13
Гибридизация АО 4 эквивалентные гибридные орбитали: h 1 = s + px +py + pz h 2 = s − px − py + pz h 3 = s − px + py − pz h 4 = s + px − py − pz Физтех, 1 курс. Осень 2015 13
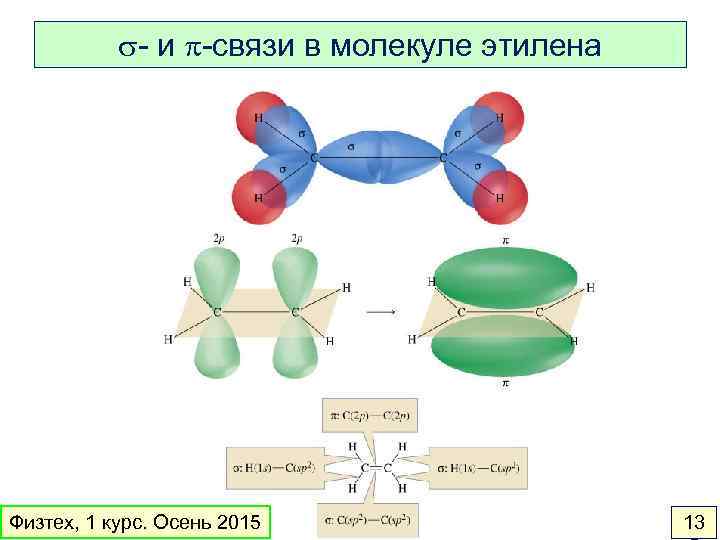 s- и p-связи в молекуле этилена Физтех, 1 курс. Осень 2015 13
s- и p-связи в молекуле этилена Физтех, 1 курс. Осень 2015 13
 Теория МО Основные идеи: • Орбитальное приближение: электронная волновая функция молекулы составляется из одноэлектронных волновых функций (МО) • МО – линейная комбинация АО: • Вклад в МО дают перекрывающиеся АО с близкой энергией Физтех, 1 курс. Осень 2015 13
Теория МО Основные идеи: • Орбитальное приближение: электронная волновая функция молекулы составляется из одноэлектронных волновых функций (МО) • МО – линейная комбинация АО: • Вклад в МО дают перекрывающиеся АО с близкой энергией Физтех, 1 курс. Осень 2015 13
 Простейшие понятия • Связывающая МО – энергия меньше, чем у АО Разрыхляющая МО – энергия больше, чем у АО Несвязывающая МО – энергия такая же, как у АО • Порядок связи = ½ (число электронов на связывающих МО – число электронов на разрыхляющих МО) Физтех, 1 курс. Осень 2015 13
Простейшие понятия • Связывающая МО – энергия меньше, чем у АО Разрыхляющая МО – энергия больше, чем у АО Несвязывающая МО – энергия такая же, как у АО • Порядок связи = ½ (число электронов на связывающих МО – число электронов на разрыхляющих МО) Физтех, 1 курс. Осень 2015 13
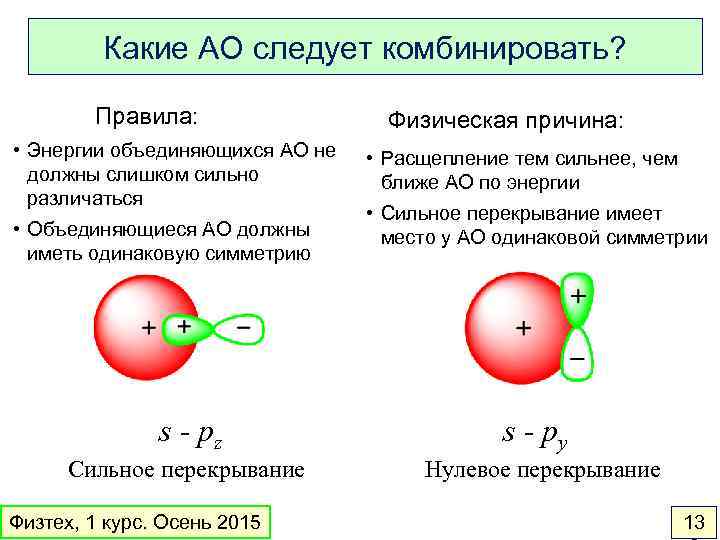 Какие АО следует комбинировать? Правила: • Энергии объединяющихся АО не должны слишком сильно различаться • Объединяющиеся АО должны иметь одинаковую симметрию Физическая причина: • Расщепление тем сильнее, чем ближе АО по энергии • Сильное перекрывание имеет место у АО одинаковой симметрии s - pz s - py Сильное перекрывание Нулевое перекрывание Физтех, 1 курс. Осень 2015 13
Какие АО следует комбинировать? Правила: • Энергии объединяющихся АО не должны слишком сильно различаться • Объединяющиеся АО должны иметь одинаковую симметрию Физическая причина: • Расщепление тем сильнее, чем ближе АО по энергии • Сильное перекрывание имеет место у АО одинаковой симметрии s - pz s - py Сильное перекрывание Нулевое перекрывание Физтех, 1 курс. Осень 2015 13
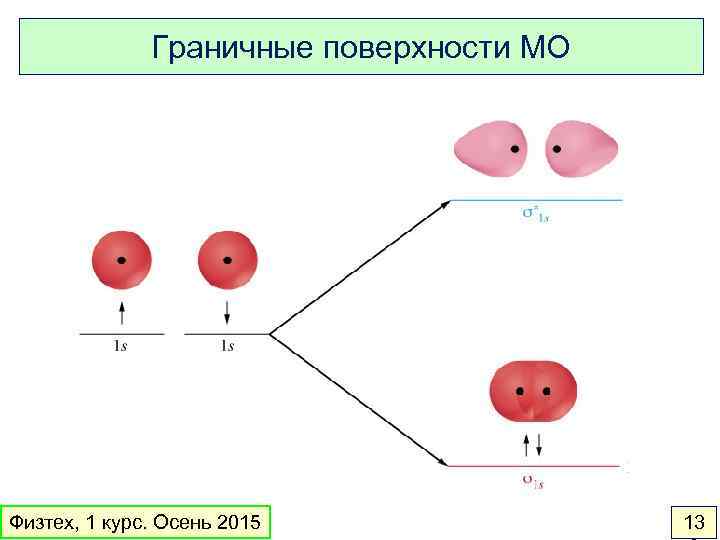 Граничные поверхности МО Физтех, 1 курс. Осень 2015 13
Граничные поверхности МО Физтех, 1 курс. Осень 2015 13
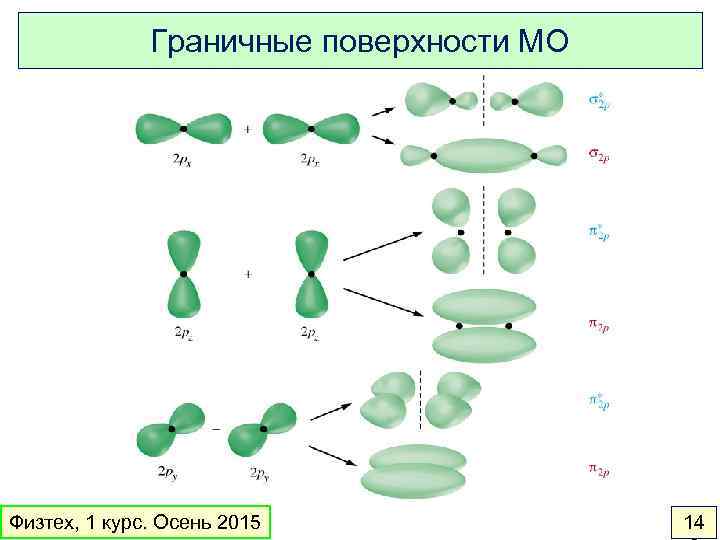 Граничные поверхности МО Физтех, 1 курс. Осень 2015 14
Граничные поверхности МО Физтех, 1 курс. Осень 2015 14
 Молекула H 2 АО МО Полная электронная ВФ молекулы (детерминант Слэтера): Физтех, 1 курс. Осень 2015 спин-орбиталь 14
Молекула H 2 АО МО Полная электронная ВФ молекулы (детерминант Слэтера): Физтех, 1 курс. Осень 2015 спин-орбиталь 14
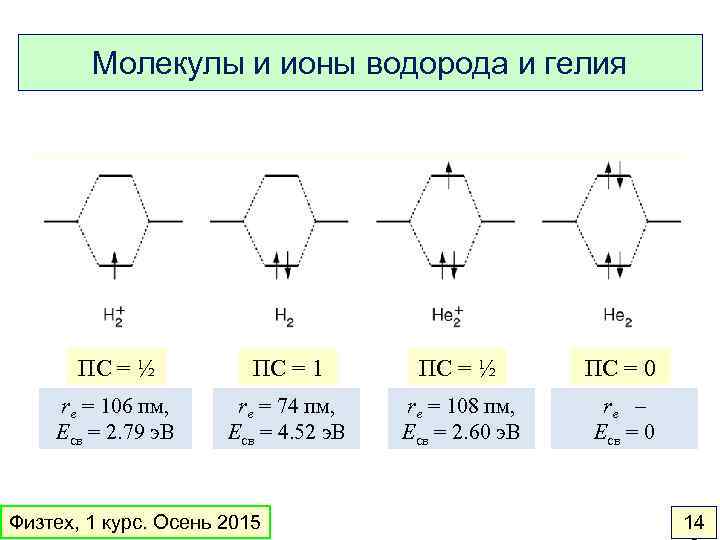 Молекулы и ионы водорода и гелия ПС = ½ ПС = 1 ПС = ½ ПС = 0 re = 106 пм, Eсв = 2. 79 э. В re = 74 пм, Eсв = 4. 52 э. В re = 108 пм, Eсв = 2. 60 э. В re – Eсв = 0 Физтех, 1 курс. Осень 2015 14
Молекулы и ионы водорода и гелия ПС = ½ ПС = 1 ПС = ½ ПС = 0 re = 106 пм, Eсв = 2. 79 э. В re = 74 пм, Eсв = 4. 52 э. В re = 108 пм, Eсв = 2. 60 э. В re – Eсв = 0 Физтех, 1 курс. Осень 2015 14
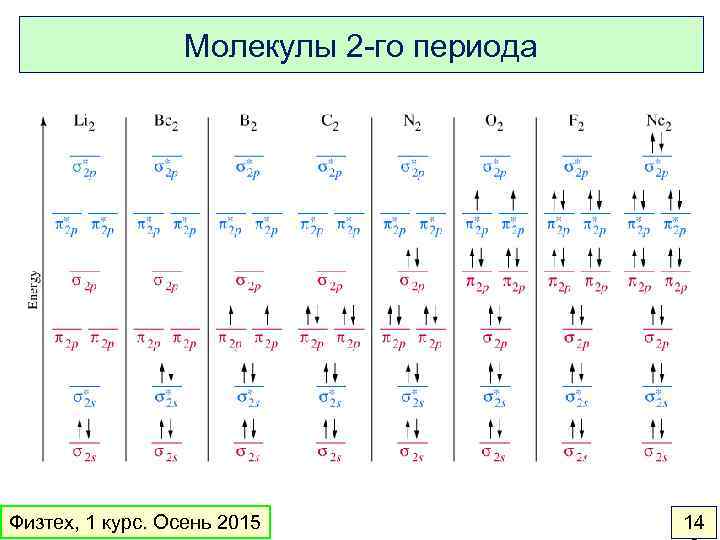 Молекулы 2 -го периода Физтех, 1 курс. Осень 2015 14
Молекулы 2 -го периода Физтех, 1 курс. Осень 2015 14
 Кислород O 2 – парамагнитен Физтех, 1 курс. Осень 2015 14
Кислород O 2 – парамагнитен Физтех, 1 курс. Осень 2015 14
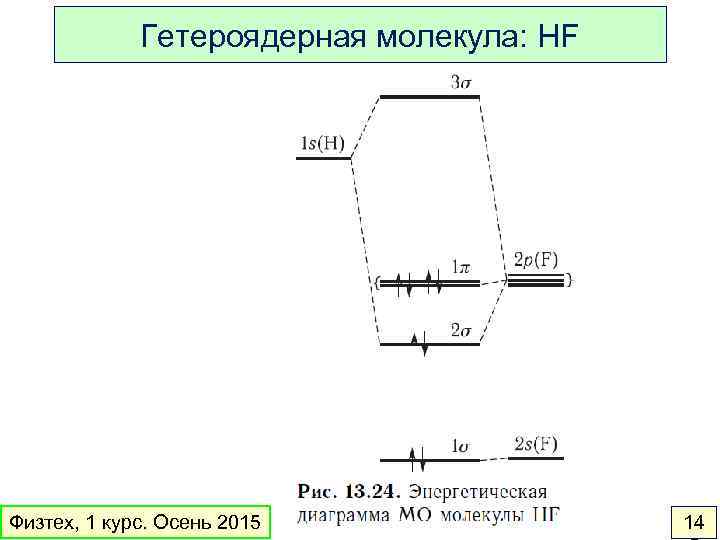 Гетероядерная молекула: HF Физтех, 1 курс. Осень 2015 14
Гетероядерная молекула: HF Физтех, 1 курс. Осень 2015 14
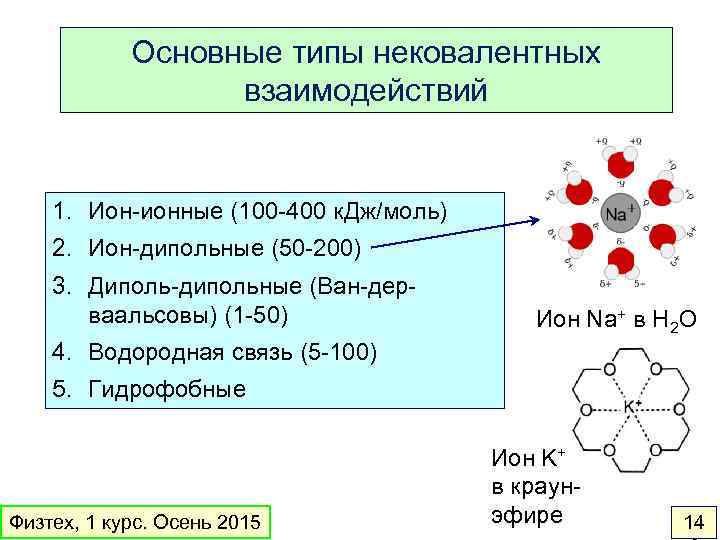 Основные типы нековалентных взаимодействий 1. Ион-ионные (100 -400 к. Дж/моль) 2. Ион-дипольные (50 -200) 3. Диполь-дипольные (Ван-дерваальсовы) (1 -50) Ион Na+ в H 2 O 4. Водородная связь (5 -100) 5. Гидрофобные Физтех, 1 курс. Осень 2015 Ион K+ в краунэфире 14
Основные типы нековалентных взаимодействий 1. Ион-ионные (100 -400 к. Дж/моль) 2. Ион-дипольные (50 -200) 3. Диполь-дипольные (Ван-дерваальсовы) (1 -50) Ион Na+ в H 2 O 4. Водородная связь (5 -100) 5. Гидрофобные Физтех, 1 курс. Осень 2015 Ион K+ в краунэфире 14
 Ван-дер-ваальсовы межмолекулярные взаимодействия Взаимодействие между диполями: 1) Ориентационное – между полярными молекулами (диполь-дипольное, например HCl – HCl) 2) Индукционное – между полярной и неполярной молекулами (постоянный диполь – наведенный диполь, Br 2 – H 2 O) 3) Дисперсионное – между неполярными молекулами (наведенный диполь – наведенный диполь, Cl 2 – Cl 2) Физтех, 1 курс. Осень 2015 14
Ван-дер-ваальсовы межмолекулярные взаимодействия Взаимодействие между диполями: 1) Ориентационное – между полярными молекулами (диполь-дипольное, например HCl – HCl) 2) Индукционное – между полярной и неполярной молекулами (постоянный диполь – наведенный диполь, Br 2 – H 2 O) 3) Дисперсионное – между неполярными молекулами (наведенный диполь – наведенный диполь, Cl 2 – Cl 2) Физтех, 1 курс. Осень 2015 14
 Ван-дер-ваальсовы межмолекулярные взаимодействия В-д-в притяжение тем сильнее, чем больше: 1) полярность; 2) размер молекул. Пример: метан (CH 4) – газ, гексан (C 6 H 14) – жидкость Одна из самых слабых в-д-в связей – между молекулами H 2 (т. пл. – 259 о. С, т. кип. – 253 о. С). Взаимодействие между молекулами во много раз слабее связи между атомами: Eков(Cl–Cl) = 244 к. Дж/моль, Eвдв(Cl 2–Cl 2) = 25 к. Дж/моль но именно обеспечивает существование жидкого и твердого состояния вещества Межмолекулярные взаимодействия слабы индивидуально, но сильны коллективно Физтех, 1 курс. Осень 2015 14
Ван-дер-ваальсовы межмолекулярные взаимодействия В-д-в притяжение тем сильнее, чем больше: 1) полярность; 2) размер молекул. Пример: метан (CH 4) – газ, гексан (C 6 H 14) – жидкость Одна из самых слабых в-д-в связей – между молекулами H 2 (т. пл. – 259 о. С, т. кип. – 253 о. С). Взаимодействие между молекулами во много раз слабее связи между атомами: Eков(Cl–Cl) = 244 к. Дж/моль, Eвдв(Cl 2–Cl 2) = 25 к. Дж/моль но именно обеспечивает существование жидкого и твердого состояния вещества Межмолекулярные взаимодействия слабы индивидуально, но сильны коллективно Физтех, 1 курс. Осень 2015 14
 Ван-дер-ваальсовы взаимодействия 1) Ориентационное – между полярными молекулами (диполь-диполь) 2) Индукционное – между полярной и неполярной молекулами (постоянный диполь – наведенный диполь) 3) Дисперсионное – между неполярными молекулами (наведенный диполь – наведенный диполь) Взаимодействие тем сильнее, чем больше: 1) полярность; 2) поляризуемость молекул. Пример: CH 4 – газ, C 6 H 14 – жидкость Eков. (Cl-Cl) = 244 к. Дж/моль Eвдв. (Cl 2 -Cl 2) = 25 к. Дж/моль Физтех, 1 курс. Осень 2015 14
Ван-дер-ваальсовы взаимодействия 1) Ориентационное – между полярными молекулами (диполь-диполь) 2) Индукционное – между полярной и неполярной молекулами (постоянный диполь – наведенный диполь) 3) Дисперсионное – между неполярными молекулами (наведенный диполь – наведенный диполь) Взаимодействие тем сильнее, чем больше: 1) полярность; 2) поляризуемость молекул. Пример: CH 4 – газ, C 6 H 14 – жидкость Eков. (Cl-Cl) = 244 к. Дж/моль Eвдв. (Cl 2 -Cl 2) = 25 к. Дж/моль Физтех, 1 курс. Осень 2015 14
 Водородная связь. Вода Притяжение между атомом водорода (+) при полярной связи одной молекулы и атомом F, O, N (–) при полярной связи другой молекулы Физтех, 1 курс. Осень 2015 15
Водородная связь. Вода Притяжение между атомом водорода (+) при полярной связи одной молекулы и атомом F, O, N (–) при полярной связи другой молекулы Физтех, 1 курс. Осень 2015 15
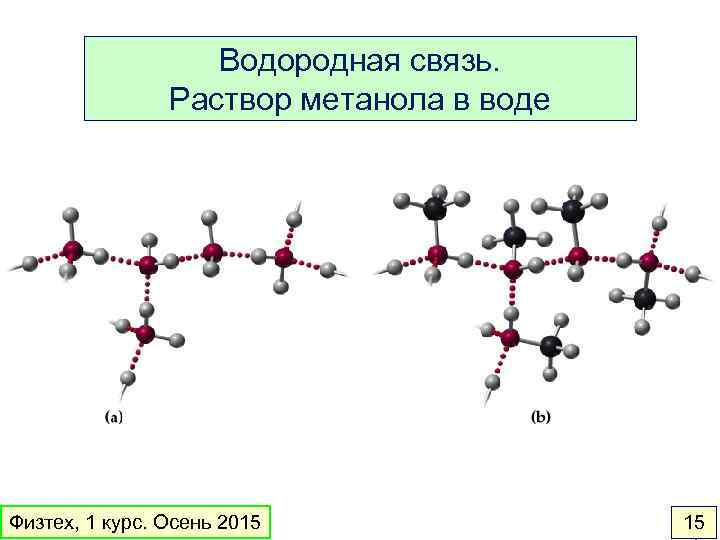 Водородная связь. Раствор метанола в воде Физтех, 1 курс. Осень 2015 15
Водородная связь. Раствор метанола в воде Физтех, 1 курс. Осень 2015 15
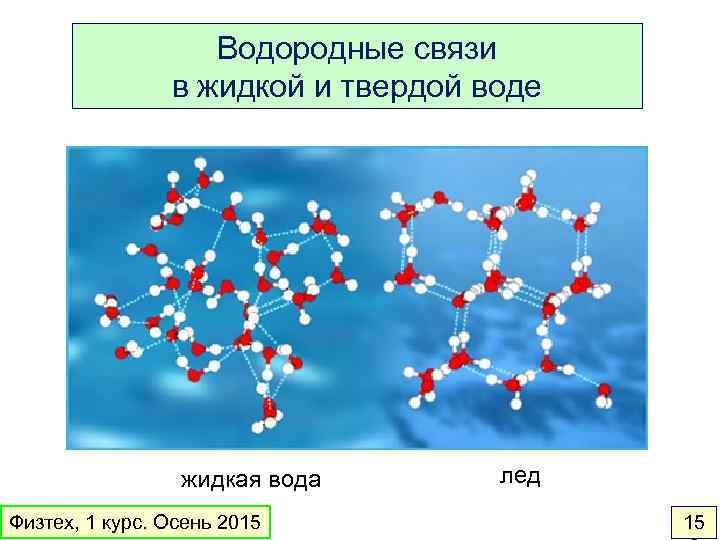 Водородные связи в жидкой и твердой воде жидкая вода Физтех, 1 курс. Осень 2015 лед 15
Водородные связи в жидкой и твердой воде жидкая вода Физтех, 1 курс. Осень 2015 лед 15
 Ложные слухи о воде Утверждения о том, что вода якобы «запоминает» то, что с ней делали – нагревали или замораживали, «омагничивали» или «диспергировали» , - основаны на плохих опытах и не имеют отношения к науке. Равно как и сообщения о «живой» и «мертвой» воде, получаемой посредством электролиза. К выдумкам относятся и особые свойства талой воды или воды, «термически активированной» (М. В. Волькенштейн, «Биофизика» ) Физтех, 1 курс. Осень 2015 15
Ложные слухи о воде Утверждения о том, что вода якобы «запоминает» то, что с ней делали – нагревали или замораживали, «омагничивали» или «диспергировали» , - основаны на плохих опытах и не имеют отношения к науке. Равно как и сообщения о «живой» и «мертвой» воде, получаемой посредством электролиза. К выдумкам относятся и особые свойства талой воды или воды, «термически активированной» (М. В. Волькенштейн, «Биофизика» ) Физтех, 1 курс. Осень 2015 15
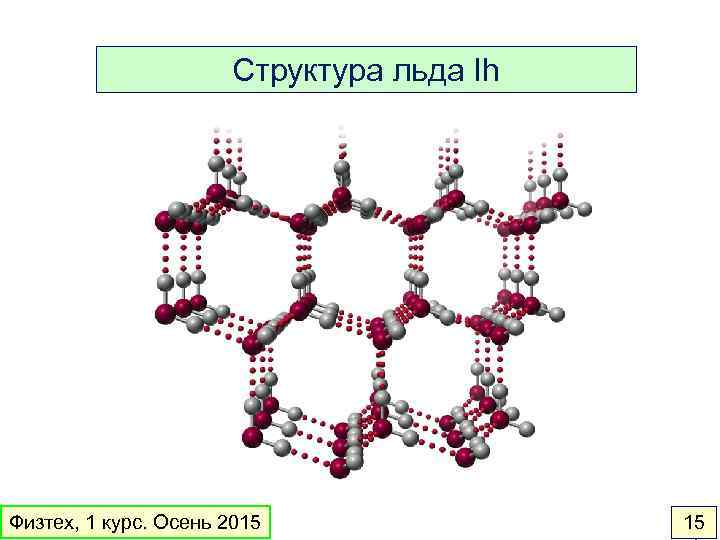 Структура льда Ih Физтех, 1 курс. Осень 2015 15
Структура льда Ih Физтех, 1 курс. Осень 2015 15
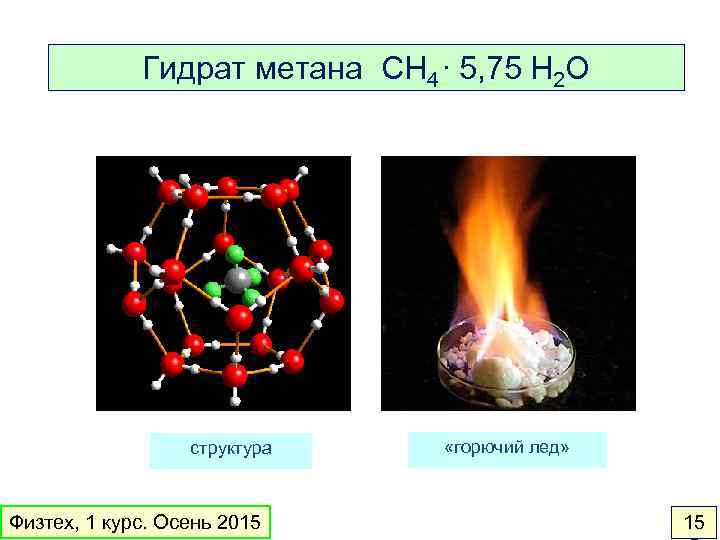 Гидрат метана CH 4. 5, 75 H 2 O структура Физтех, 1 курс. Осень 2015 «горючий лед» 15
Гидрат метана CH 4. 5, 75 H 2 O структура Физтех, 1 курс. Осень 2015 «горючий лед» 15
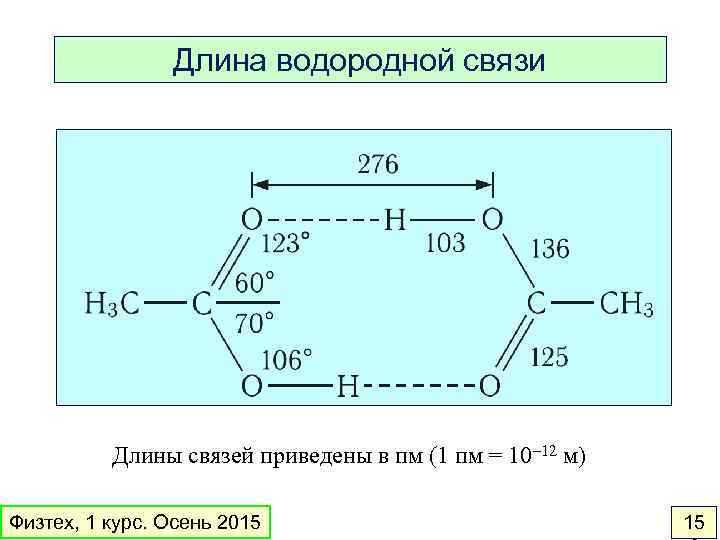 Длина водородной связи Длины связей приведены в пм (1 пм = 10– 12 м) Физтех, 1 курс. Осень 2015 15
Длина водородной связи Длины связей приведены в пм (1 пм = 10– 12 м) Физтех, 1 курс. Осень 2015 15
 Энергия водородной связи Энергия некоторых водородных связей (к. Дж/моль) Физтех, 1 курс. Осень 2015 15
Энергия водородной связи Энергия некоторых водородных связей (к. Дж/моль) Физтех, 1 курс. Осень 2015 15
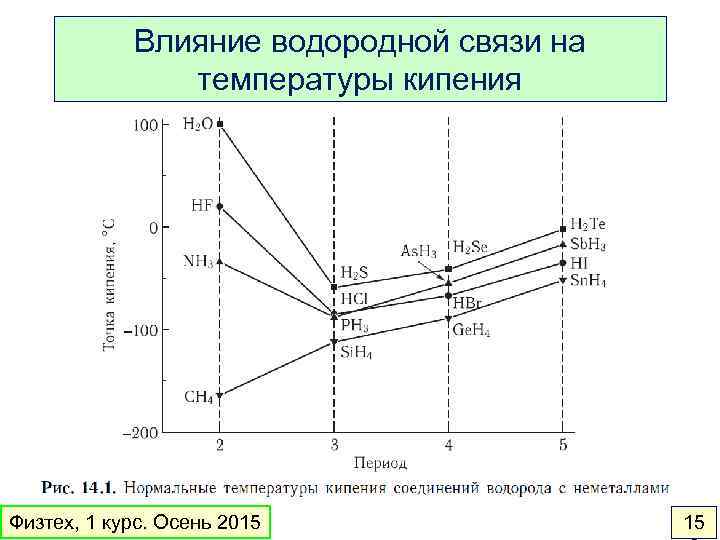 Влияние водородной связи на температуры кипения Физтех, 1 курс. Осень 2015 15
Влияние водородной связи на температуры кипения Физтех, 1 курс. Осень 2015 15
 Коротко о главном 1. Благодаря разной массе ядер и электронов возможно разделить электронное и ядерное движения в молекулах. Электронная энергия молекулы – функция межъядерных расстояний. В связанных электронных состояниях эта функция имеет минимум. 2. В теории молекулярных орбиталей (МО) одноэлектронная волновая функция составляется как линейная комбинация атомных орбиталей (АО). 3. Все молекулы способны взаимодействовать между собой. Межмолекулярные взаимодействия обеспечивают устойчивость веществ в конденсированном (жидком и твердом) состоянии. 4. Энергия этих взаимодействий на порядок меньше энергии ковалентной связи – они слабы индивидуально, но сильны коллективно. Длина межмолекулярных связей в несколько раз больше длины ковалентных связей. 5. Основные виды межмолекулярных взаимодействий – водородная связь и диполь-дипольное (ван-дер-ваальсово) взаимодействие. Физтех, 1 курс. Осень 2015 15
Коротко о главном 1. Благодаря разной массе ядер и электронов возможно разделить электронное и ядерное движения в молекулах. Электронная энергия молекулы – функция межъядерных расстояний. В связанных электронных состояниях эта функция имеет минимум. 2. В теории молекулярных орбиталей (МО) одноэлектронная волновая функция составляется как линейная комбинация атомных орбиталей (АО). 3. Все молекулы способны взаимодействовать между собой. Межмолекулярные взаимодействия обеспечивают устойчивость веществ в конденсированном (жидком и твердом) состоянии. 4. Энергия этих взаимодействий на порядок меньше энергии ковалентной связи – они слабы индивидуально, но сильны коллективно. Длина межмолекулярных связей в несколько раз больше длины ковалентных связей. 5. Основные виды межмолекулярных взаимодействий – водородная связь и диполь-дипольное (ван-дер-ваальсово) взаимодействие. Физтех, 1 курс. Осень 2015 15
 Основные понятия § Адиабатическое приближение § Электронное состояние молекулы. Потенциальная кривая (поверхность потенциальной энергии – ППЭ) § Гибридизация орбиталей. Сигма- и пи-связи § Молекулярные орбитали - связывающие - разрыхляющие - несвязывающие § Порядок связи § Межмолекулярные взаимодействия: - водородная связь - ван-дер-ваальсово (дипольное) взаимодействие § Энергия связи. Длина связи Физтех, 1 курс. Осень 2015 16
Основные понятия § Адиабатическое приближение § Электронное состояние молекулы. Потенциальная кривая (поверхность потенциальной энергии – ППЭ) § Гибридизация орбиталей. Сигма- и пи-связи § Молекулярные орбитали - связывающие - разрыхляющие - несвязывающие § Порядок связи § Межмолекулярные взаимодействия: - водородная связь - ван-дер-ваальсово (дипольное) взаимодействие § Энергия связи. Длина связи Физтех, 1 курс. Осень 2015 16
 Типичные задачи 1. В рамках теории МО изобразите электронную конфигурацию основного состояния молекулы H 2 (N 2, O 2) или иона H 2+ (H 2 -, He 2+, O 22+). Определите порядок связи между атомами. 2. На графике (например, слайд 6) изображены потенциальные кривые нескольких электронных состояний двухатомной молекулы. 1) Укажите связанные и несвязанные состояния. 2) Определите, каким электронным состояниям атомов соответствуют эти кривые. 3) Оцените длину и энергию связи в основном состоянии. 3. Теплота плавления льда равна 6 к. Дж/моль, а теплота испарения воды – 44 к. Дж/моль. Определите среднюю энергию водородной связи в твердой H 2 O (в к. Дж/моль), если известно, что каждая молекула в кристалле льда участвует в 4 водородных связях, а в газовой фазе молекулы друг с другом не взаимодействуют. Физтех, 1 курс. Осень 2015 16
Типичные задачи 1. В рамках теории МО изобразите электронную конфигурацию основного состояния молекулы H 2 (N 2, O 2) или иона H 2+ (H 2 -, He 2+, O 22+). Определите порядок связи между атомами. 2. На графике (например, слайд 6) изображены потенциальные кривые нескольких электронных состояний двухатомной молекулы. 1) Укажите связанные и несвязанные состояния. 2) Определите, каким электронным состояниям атомов соответствуют эти кривые. 3) Оцените длину и энергию связи в основном состоянии. 3. Теплота плавления льда равна 6 к. Дж/моль, а теплота испарения воды – 44 к. Дж/моль. Определите среднюю энергию водородной связи в твердой H 2 O (в к. Дж/моль), если известно, что каждая молекула в кристалле льда участвует в 4 водородных связях, а в газовой фазе молекулы друг с другом не взаимодействуют. Физтех, 1 курс. Осень 2015 16
 Литература 1. Еремин, Борщевский. Общая и неорганическая химия. – Глава 13, § 13. 5; глава 14. 2. Шрайвер, Эткинс. Неорганическая химия. – Том 1, глава 3, §§ 3. 4 -3. 10. 3. Глинка. Общая химия. – Глава 4. 4. Еремин. Теоретическая и математическая химия. – Глава 2. § 5. Физтех, 1 курс. Осень 2015 16
Литература 1. Еремин, Борщевский. Общая и неорганическая химия. – Глава 13, § 13. 5; глава 14. 2. Шрайвер, Эткинс. Неорганическая химия. – Том 1, глава 3, §§ 3. 4 -3. 10. 3. Глинка. Общая химия. – Глава 4. 4. Еремин. Теоретическая и математическая химия. – Глава 2. § 5. Физтех, 1 курс. Осень 2015 16
 Лекция 5 Строение твердых веществ Физтех, 1 курс. Осень 2015
Лекция 5 Строение твердых веществ Физтех, 1 курс. Осень 2015
 План лекции 1. 2. 3. 4. Кристаллы, их классификация по типу связи. Элементарная ячейка кристаллической решетки. Атомные и молекулярные кристаллы. Плотнейшие шаровые упаковки. Основные типы кристаллических решеток металлов. 5. Ионные соединения. Важнейшие типы кристаллических решеток ионных соединений. Ионные радиусы и их определение. 6. Энергия кристаллической решетки. Цикл Борна. Габера. Физтех, 1 курс. Осень 2015 164
План лекции 1. 2. 3. 4. Кристаллы, их классификация по типу связи. Элементарная ячейка кристаллической решетки. Атомные и молекулярные кристаллы. Плотнейшие шаровые упаковки. Основные типы кристаллических решеток металлов. 5. Ионные соединения. Важнейшие типы кристаллических решеток ионных соединений. Ионные радиусы и их определение. 6. Энергия кристаллической решетки. Цикл Борна. Габера. Физтех, 1 курс. Осень 2015 164
 Кристаллы Кристалл – это бесконечная периодическая структура, составленная из атомов, молекул или ионов Как любая геометрическая фигура, кристалл обладает симметрией Совокупность всех операций симметрии кристалла - пространственная группа Физтех, 1 курс. Осень 2015 165
Кристаллы Кристалл – это бесконечная периодическая структура, составленная из атомов, молекул или ионов Как любая геометрическая фигура, кристалл обладает симметрией Совокупность всех операций симметрии кристалла - пространственная группа Физтех, 1 курс. Осень 2015 165
 Древние кристаллы (музей естествознания, Оксфорд) Кварц (1. 1 млрд. лет) Физтех, 1 курс. Осень 2015 Fe-Ni (4. 5 млрд. лет) 166
Древние кристаллы (музей естествознания, Оксфорд) Кварц (1. 1 млрд. лет) Физтех, 1 курс. Осень 2015 Fe-Ni (4. 5 млрд. лет) 166
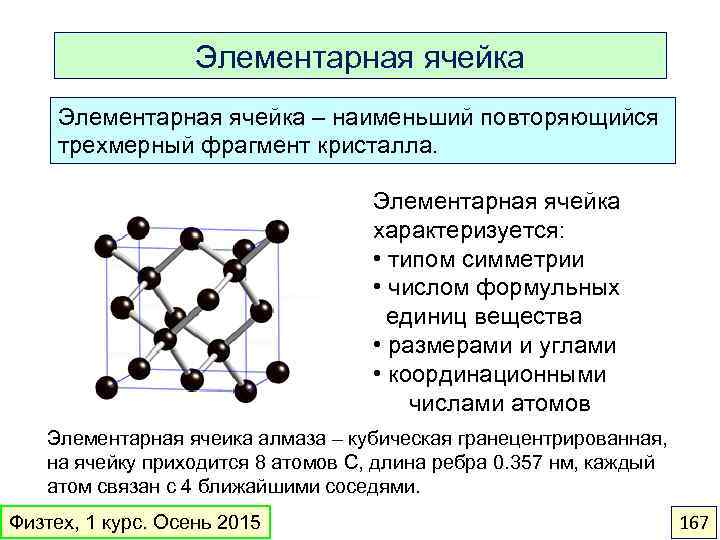 Элементарная ячейка – наименьший повторяющийся трехмерный фрагмент кристалла. Элементарная ячейка характеризуется: • типом симметрии • числом формульных единиц вещества • размерами и углами • координационными числами атомов Элементарная ячейка алмаза – кубическая гранецентрированная, на ячейку приходится 8 атомов C, длина ребра 0. 357 нм, каждый атом связан с 4 ближайшими соседями. Физтех, 1 курс. Осень 2015 167
Элементарная ячейка – наименьший повторяющийся трехмерный фрагмент кристалла. Элементарная ячейка характеризуется: • типом симметрии • числом формульных единиц вещества • размерами и углами • координационными числами атомов Элементарная ячейка алмаза – кубическая гранецентрированная, на ячейку приходится 8 атомов C, длина ребра 0. 357 нм, каждый атом связан с 4 ближайшими соседями. Физтех, 1 курс. Осень 2015 167
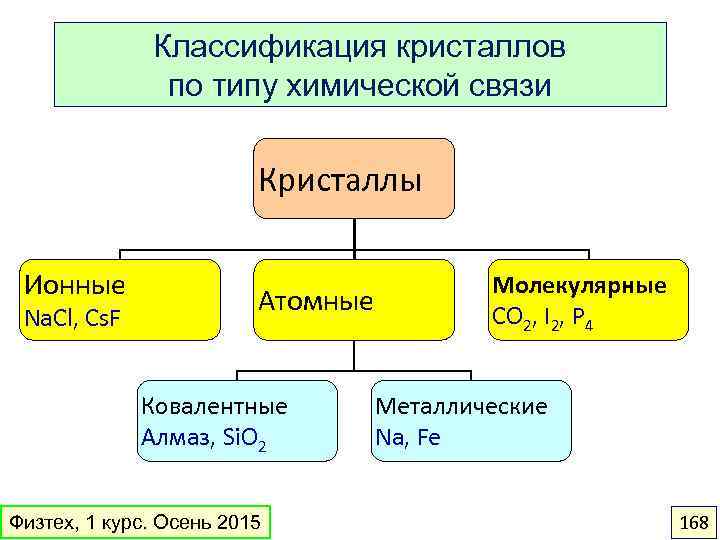 Классификация кристаллов по типу химической связи Кристаллы Ионные Na. Cl, Cs. F Атомные Ковалентные Алмаз, Si. O 2 Физтех, 1 курс. Осень 2015 Молекулярные CO 2, I 2, P 4 Металлические Na, Fe 168
Классификация кристаллов по типу химической связи Кристаллы Ионные Na. Cl, Cs. F Атомные Ковалентные Алмаз, Si. O 2 Физтех, 1 курс. Осень 2015 Молекулярные CO 2, I 2, P 4 Металлические Na, Fe 168
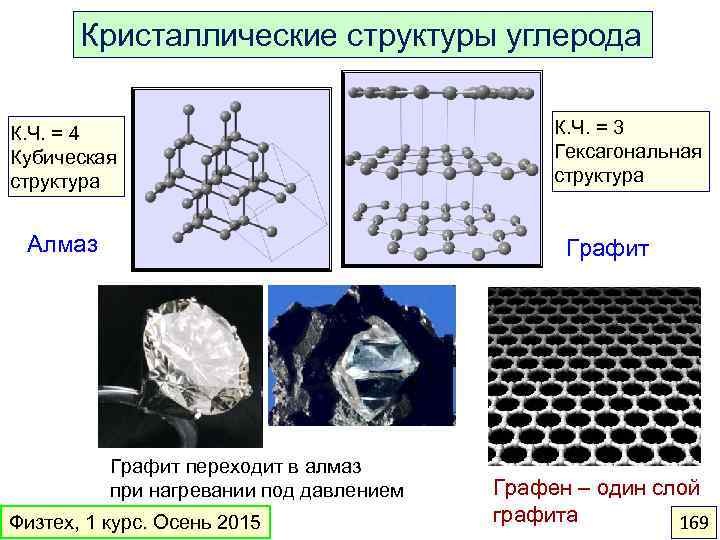 Кристаллические структуры углерода К. Ч. = 4 Кубическая структура Алмаз К. Ч. = 3 Гексагональная структура Графит переходит в алмаз при нагревании под давлением Физтех, 1 курс. Осень 2015 Графен – один слой графита 169
Кристаллические структуры углерода К. Ч. = 4 Кубическая структура Алмаз К. Ч. = 3 Гексагональная структура Графит переходит в алмаз при нагревании под давлением Физтех, 1 курс. Осень 2015 Графен – один слой графита 169
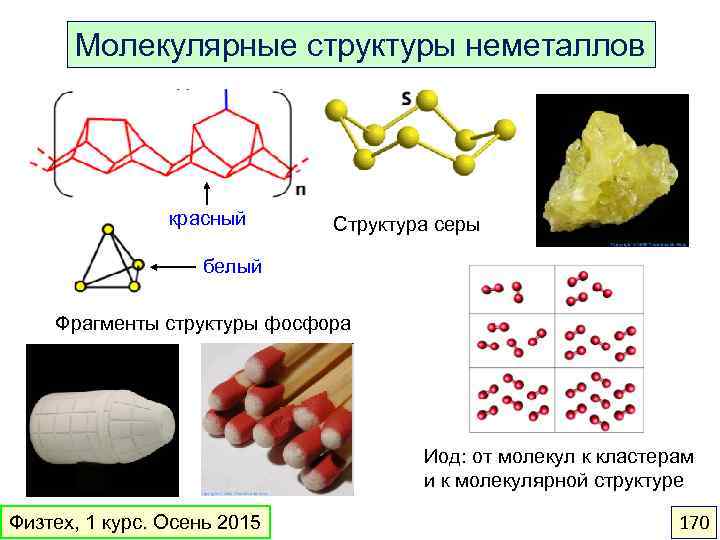 Молекулярные структуры неметаллов красный Структура серы белый Фрагменты структуры фосфора Иод: от молекул к кластерам и к молекулярной структуре Физтех, 1 курс. Осень 2015 170
Молекулярные структуры неметаллов красный Структура серы белый Фрагменты структуры фосфора Иод: от молекул к кластерам и к молекулярной структуре Физтех, 1 курс. Осень 2015 170
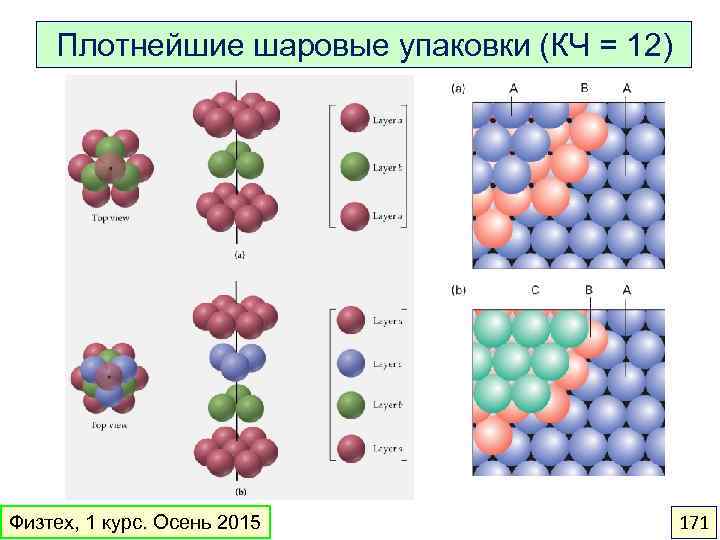 Плотнейшие шаровые упаковки (КЧ = 12) Физтех, 1 курс. Осень 2015 171
Плотнейшие шаровые упаковки (КЧ = 12) Физтех, 1 курс. Осень 2015 171
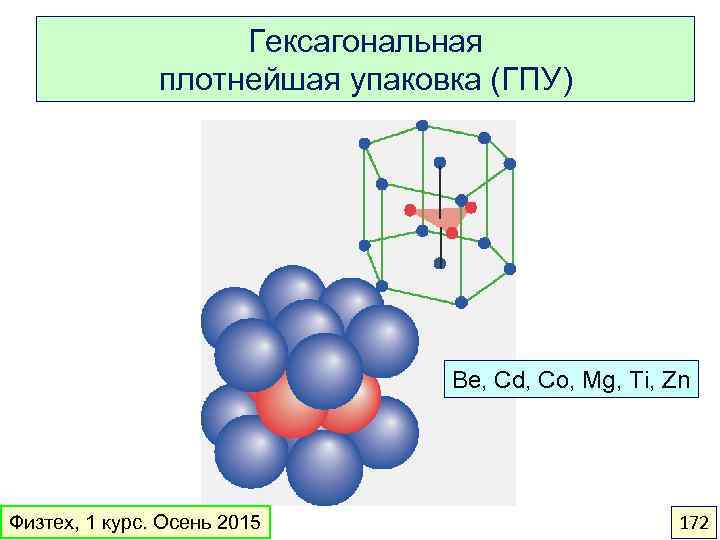 Гексагональная плотнейшая упаковка (ГПУ) Be, Cd, Co, Mg, Ti, Zn Физтех, 1 курс. Осень 2015 172
Гексагональная плотнейшая упаковка (ГПУ) Be, Cd, Co, Mg, Ti, Zn Физтех, 1 курс. Осень 2015 172
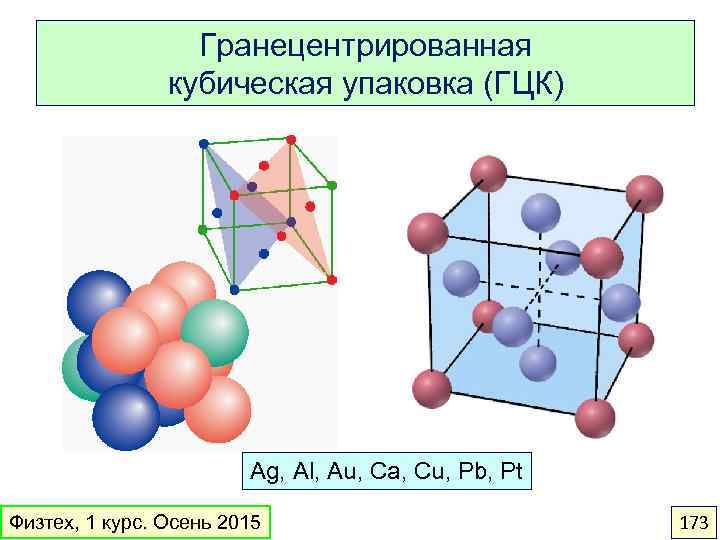 Гранецентрированная кубическая упаковка (ГЦК) Ag, Al, Au, Ca, Cu, Pb, Pt Физтех, 1 курс. Осень 2015 173
Гранецентрированная кубическая упаковка (ГЦК) Ag, Al, Au, Ca, Cu, Pb, Pt Физтех, 1 курс. Осень 2015 173
 Степень заполнения пространства Физтех, 1 курс. Осень 2015 174
Степень заполнения пространства Физтех, 1 курс. Осень 2015 174
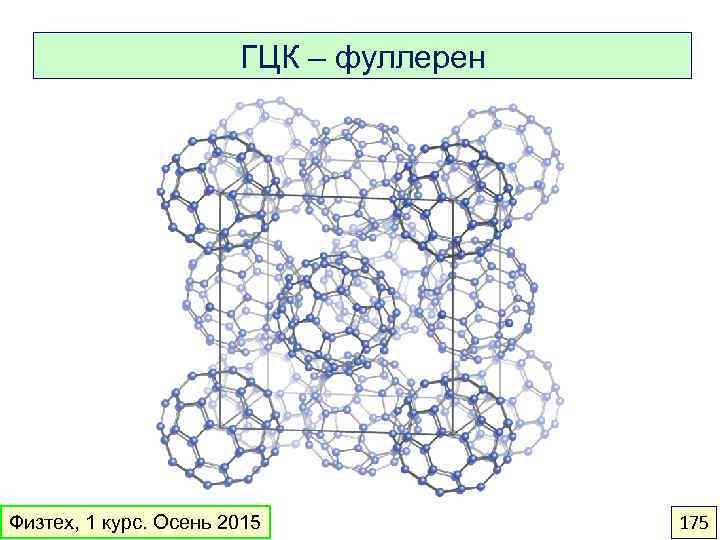 ГЦК – фуллерен Физтех, 1 курс. Осень 2015 175
ГЦК – фуллерен Физтех, 1 курс. Осень 2015 175
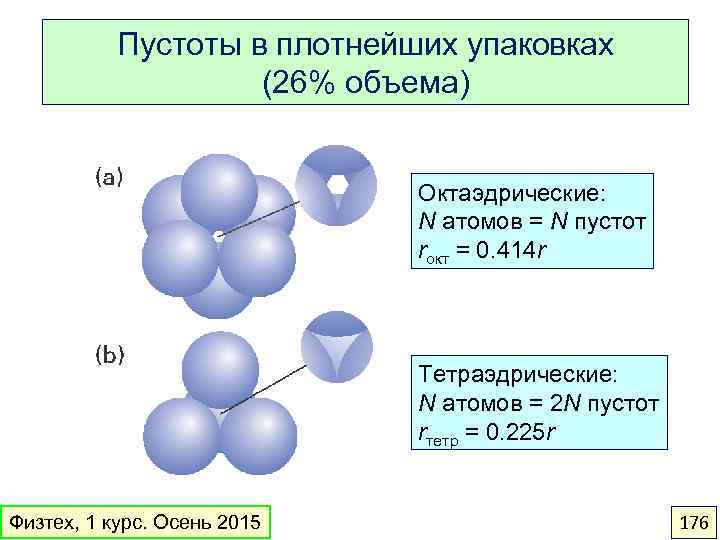 Пустоты в плотнейших упаковках (26% объема) Октаэдрические: N атомов = N пустот rокт = 0. 414 r Тетраэдрические: N атомов = 2 N пустот rтетр = 0. 225 r Физтех, 1 курс. Осень 2015 176
Пустоты в плотнейших упаковках (26% объема) Октаэдрические: N атомов = N пустот rокт = 0. 414 r Тетраэдрические: N атомов = 2 N пустот rтетр = 0. 225 r Физтех, 1 курс. Осень 2015 176
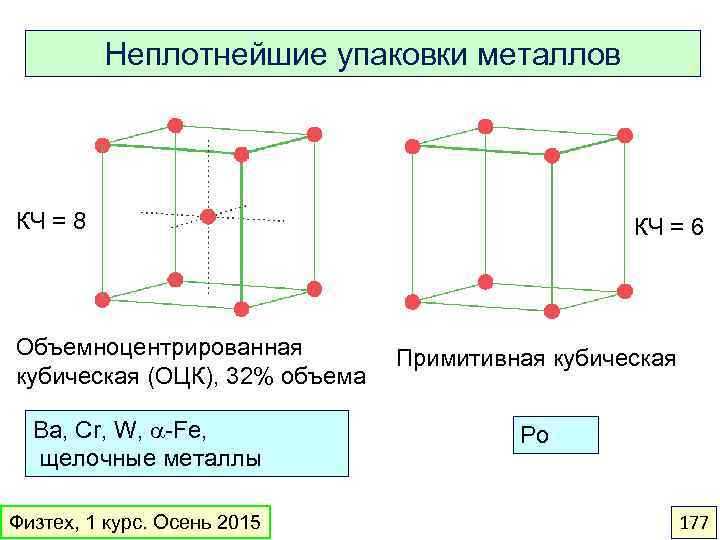 Неплотнейшие упаковки металлов КЧ = 8 Объемноцентрированная кубическая (ОЦК), 32% объема Ba, Cr, W, a-Fe, щелочные металлы Физтех, 1 курс. Осень 2015 КЧ = 6 Примитивная кубическая Po 177
Неплотнейшие упаковки металлов КЧ = 8 Объемноцентрированная кубическая (ОЦК), 32% объема Ba, Cr, W, a-Fe, щелочные металлы Физтех, 1 курс. Осень 2015 КЧ = 6 Примитивная кубическая Po 177
 Полиморфизм металлов Способность образовывать разные кристаллические формы при различных условиях (p, T) Железо a-Fe: ОЦК, t < 906 o. C, t > 1401 o. C g-Fe: ГЦК, 906 o. C < t < 1401 o. C -Fe: ГПУ высокое давление Олово -Sn: t > 14 o. C = 7. 31 г/см 3 a-Sn: t < 14 o. C = 5. 75 г/см 3 Физтех, 1 курс. Осень 2015 178
Полиморфизм металлов Способность образовывать разные кристаллические формы при различных условиях (p, T) Железо a-Fe: ОЦК, t < 906 o. C, t > 1401 o. C g-Fe: ГЦК, 906 o. C < t < 1401 o. C -Fe: ГПУ высокое давление Олово -Sn: t > 14 o. C = 7. 31 г/см 3 a-Sn: t < 14 o. C = 5. 75 г/см 3 Физтех, 1 курс. Осень 2015 178
 Ионные кристаллы 1. Высокие температуры плавления 2. Низкая электропроводность в твердом состоянии 3. Высокая электропроводность в расплаве § Структура состоит из противоположно заряженных ионов, соединенных ионной связью § Ионы считаются твердыми шарами § Ионы расположены так, что общая энергия минимальна § Положительные ионы занимают пустоты в решетке, образованной отрицательными Физтех, 1 курс. Осень 2015 ионами 179
Ионные кристаллы 1. Высокие температуры плавления 2. Низкая электропроводность в твердом состоянии 3. Высокая электропроводность в расплаве § Структура состоит из противоположно заряженных ионов, соединенных ионной связью § Ионы считаются твердыми шарами § Ионы расположены так, что общая энергия минимальна § Положительные ионы занимают пустоты в решетке, образованной отрицательными Физтех, 1 курс. Осень 2015 ионами 179
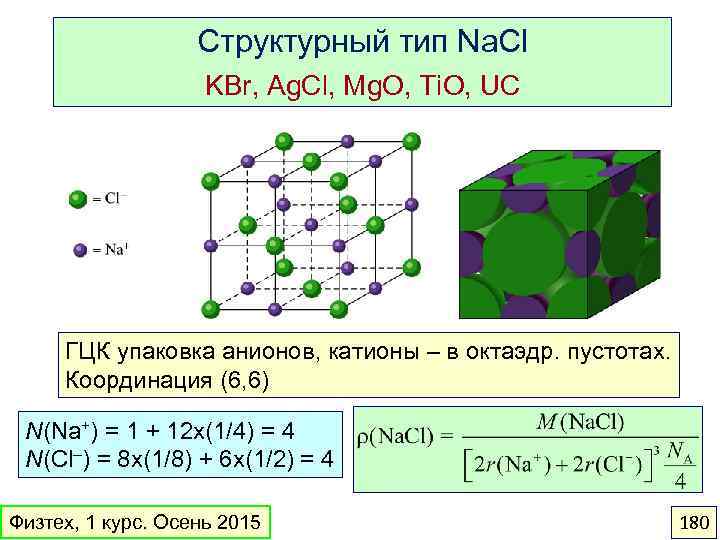 Структурный тип Na. Cl KBr, Ag. Cl, Mg. O, Ti. O, UC ГЦК упаковка анионов, катионы – в октаэдр. пустотах. Координация (6, 6) N(Na+) = 1 + 12 x(1/4) = 4 N(Cl–) = 8 x(1/8) + 6 x(1/2) = 4 Физтех, 1 курс. Осень 2015 180
Структурный тип Na. Cl KBr, Ag. Cl, Mg. O, Ti. O, UC ГЦК упаковка анионов, катионы – в октаэдр. пустотах. Координация (6, 6) N(Na+) = 1 + 12 x(1/4) = 4 N(Cl–) = 8 x(1/8) + 6 x(1/2) = 4 Физтех, 1 курс. Осень 2015 180
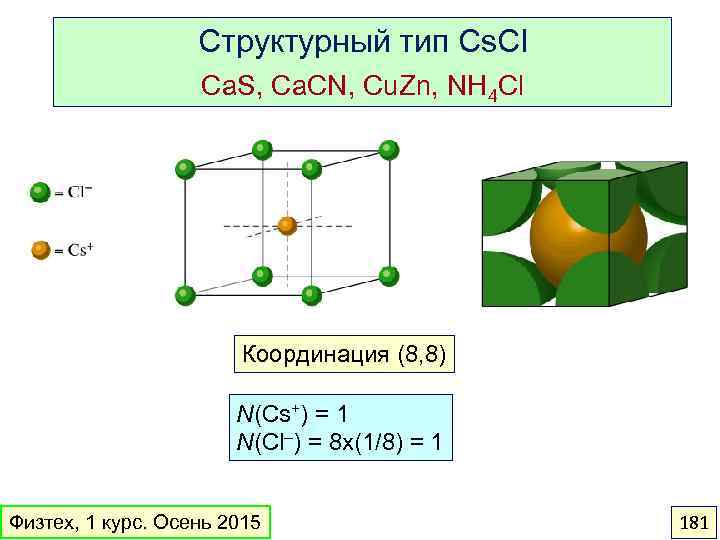 Структурный тип Cs. Cl Ca. S, Ca. CN, Cu. Zn, NH 4 Cl Координация (8, 8) N(Cs+) = 1 N(Cl–) = 8 x(1/8) = 1 Физтех, 1 курс. Осень 2015 181
Структурный тип Cs. Cl Ca. S, Ca. CN, Cu. Zn, NH 4 Cl Координация (8, 8) N(Cs+) = 1 N(Cl–) = 8 x(1/8) = 1 Физтех, 1 курс. Осень 2015 181
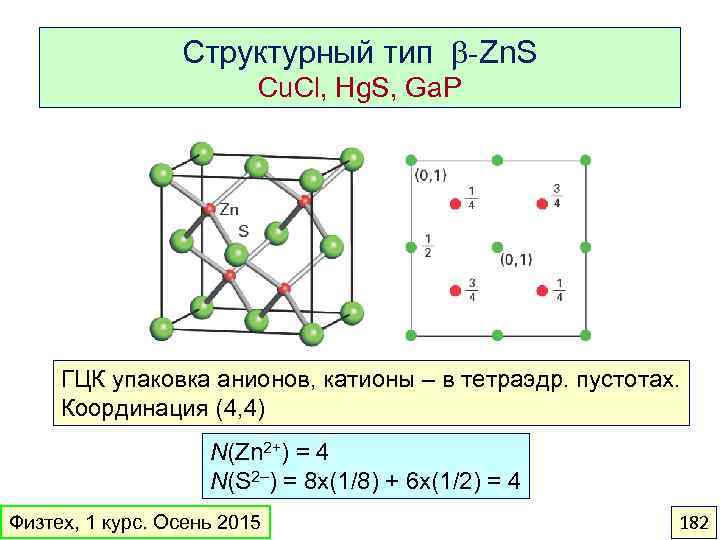 Структурный тип -Zn. S Cu. Cl, Hg. S, Ga. P ГЦК упаковка анионов, катионы – в тетраэдр. пустотах. Координация (4, 4) N(Zn 2+) = 4 N(S 2–) = 8 x(1/8) + 6 x(1/2) = 4 Физтех, 1 курс. Осень 2015 182
Структурный тип -Zn. S Cu. Cl, Hg. S, Ga. P ГЦК упаковка анионов, катионы – в тетраэдр. пустотах. Координация (4, 4) N(Zn 2+) = 4 N(S 2–) = 8 x(1/8) + 6 x(1/2) = 4 Физтех, 1 курс. Осень 2015 182
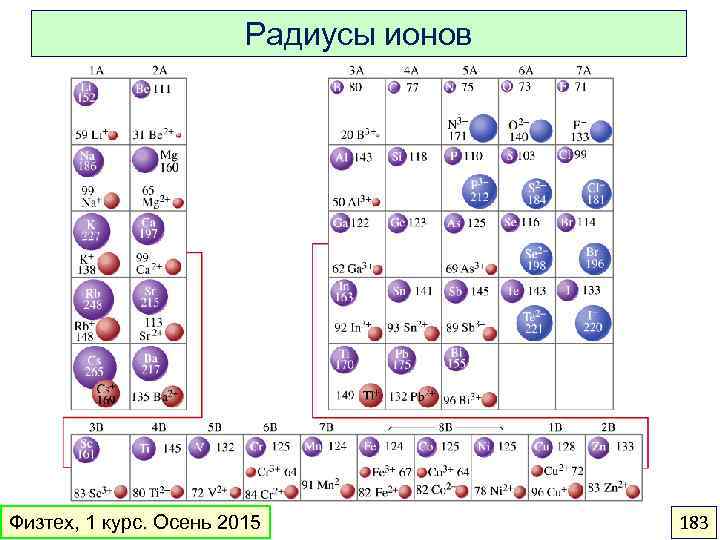 Радиусы ионов Физтех, 1 курс. Осень 2015 183
Радиусы ионов Физтех, 1 курс. Осень 2015 183
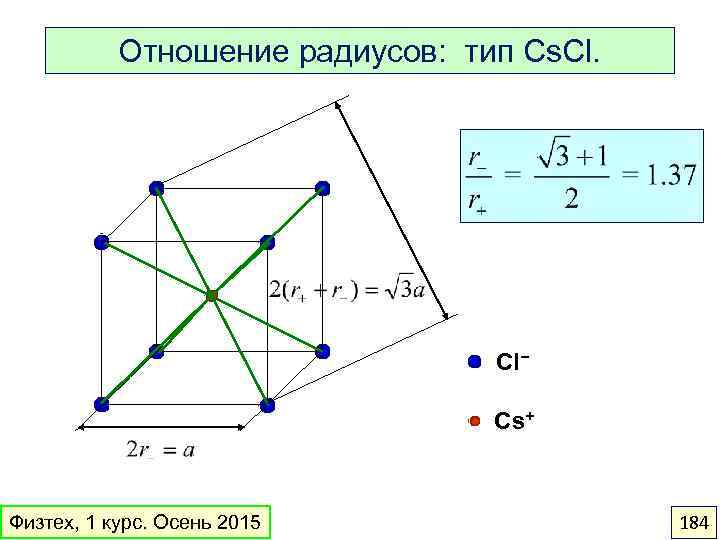 Отношение радиусов: тип Cs. Cl. Cl− Cs+ Физтех, 1 курс. Осень 2015 184
Отношение радиусов: тип Cs. Cl. Cl− Cs+ Физтех, 1 курс. Осень 2015 184
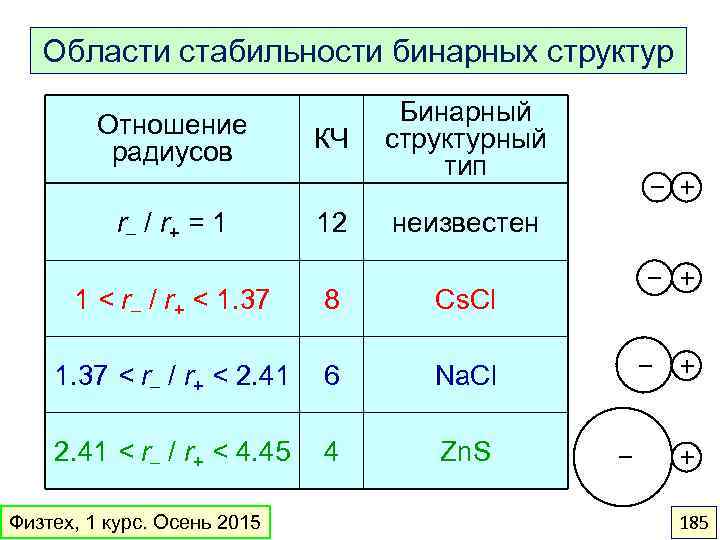 Области стабильности бинарных структур Отношение радиусов r– / r+ = 1 КЧ 12 Бинарный структурный тип − + неизвестен 1 < r– / r+ < 1. 37 8 Cs. Cl 1. 37 < r– / r+ < 2. 41 6 Na. Cl 2. 41 < r– / r+ < 4. 45 4 Zn. S − + Физтех, 1 курс. Осень 2015 − + 185
Области стабильности бинарных структур Отношение радиусов r– / r+ = 1 КЧ 12 Бинарный структурный тип − + неизвестен 1 < r– / r+ < 1. 37 8 Cs. Cl 1. 37 < r– / r+ < 2. 41 6 Na. Cl 2. 41 < r– / r+ < 4. 45 4 Zn. S − + Физтех, 1 курс. Осень 2015 − + 185
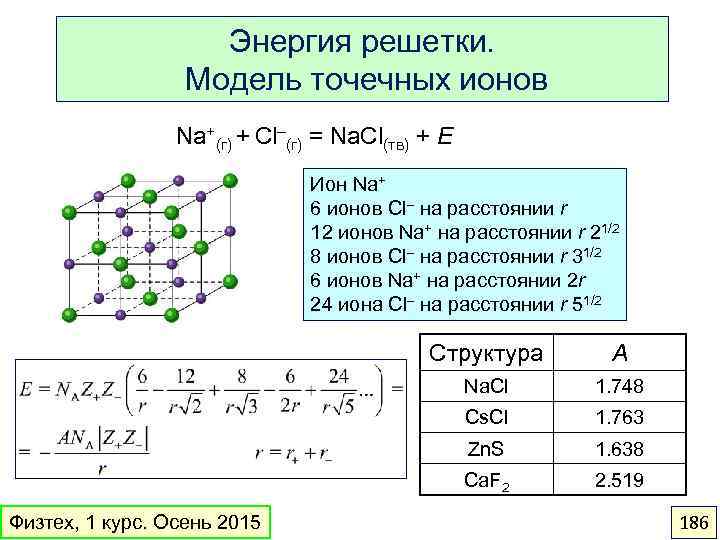 Энергия решетки. Модель точечных ионов Na+(г) + Cl–(г) = Na. Cl(тв) + E Ион Na+ 6 ионов Cl– на расстоянии r 12 ионов Na+ на расстоянии r 21/2 8 ионов Cl– на расстоянии r 31/2 6 ионов Na+ на расстоянии 2 r 24 иона Cl– на расстоянии r 51/2 Структура Na. Cl 1. 748 Cs. Cl 1. 763 Zn. S 1. 638 Ca. F 2 Физтех, 1 курс. Осень 2015 A 2. 519 186
Энергия решетки. Модель точечных ионов Na+(г) + Cl–(г) = Na. Cl(тв) + E Ион Na+ 6 ионов Cl– на расстоянии r 12 ионов Na+ на расстоянии r 21/2 8 ионов Cl– на расстоянии r 31/2 6 ионов Na+ на расстоянии 2 r 24 иона Cl– на расстоянии r 51/2 Структура Na. Cl 1. 748 Cs. Cl 1. 763 Zn. S 1. 638 Ca. F 2 Физтех, 1 курс. Осень 2015 A 2. 519 186
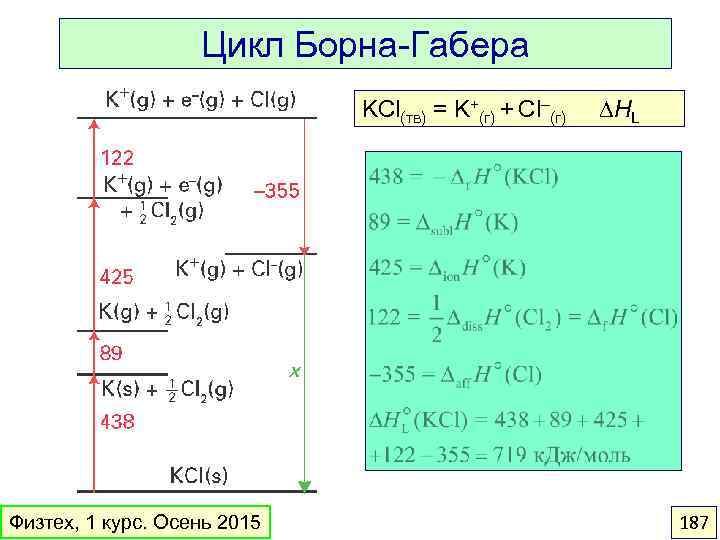 Цикл Борна-Габера KCl(тв) = K+(г) + Cl–(г) Физтех, 1 курс. Осень 2015 DHL 187
Цикл Борна-Габера KCl(тв) = K+(г) + Cl–(г) Физтех, 1 курс. Осень 2015 DHL 187
 Влияние размеров ионов на растворимость в воде Соли с ионами близкого размера, как правило, хуже растворимы в воде, чем те, у которых размеры ионов сильно различаются Mg(OH)2 < Ca(OH)2 < Sr(OH)2 < Ba(OH)2 Mg. SO 4 > Ca. SO 4 > Sr. SO 4 > Ba. SO 4 MX(тв) = M+(aq) + X–(aq) DH ~ DHL + Dhydr. H Физтех, 1 курс. Осень 2015 188
Влияние размеров ионов на растворимость в воде Соли с ионами близкого размера, как правило, хуже растворимы в воде, чем те, у которых размеры ионов сильно различаются Mg(OH)2 < Ca(OH)2 < Sr(OH)2 < Ba(OH)2 Mg. SO 4 > Ca. SO 4 > Sr. SO 4 > Ba. SO 4 MX(тв) = M+(aq) + X–(aq) DH ~ DHL + Dhydr. H Физтех, 1 курс. Осень 2015 188
 Коротко о главном 1. Большинство твердых веществ находится в кристаллическом состоянии. Кристалл – структура с пространственной периодичностью. В основе структуры кристалла – элементарная ячейка. 2. В простейшей модели кристалла атомы или ионы представляют собой твердые сферы. 3. Основные типы шаровых упаковок металлов – ГПУ (КЧ=12), ГЦК (КЧ=12), ОЦК (КЧ=8). Первые две относятся к плотнейшим упаковкам. 4. В ионной модели твердое вещество представляется совокупностью противоположно заряженных сфер. Ионные кристаллы можно рассматривать как совокупность противоположно заряженных шаров. Катионы в них занимают пустоты в упаковках, образованных анионами. Соотношение радиусов ионов определяет тип решетки. 5. Энергия кристаллической решетки – это разность между энергиями кристалла и изолированных газообразных ионов. Она определяется зарядами и радиусами ионов, а также типом решетки. 6. Энергия решетки определяет физико-химические свойства кристаллов – их устойчивость к нагреванию и растворимость в воде. Ее можно экспериментально измерить, используя цикл Борна-Габера. Физтех, 1 курс. Осень 2015 189
Коротко о главном 1. Большинство твердых веществ находится в кристаллическом состоянии. Кристалл – структура с пространственной периодичностью. В основе структуры кристалла – элементарная ячейка. 2. В простейшей модели кристалла атомы или ионы представляют собой твердые сферы. 3. Основные типы шаровых упаковок металлов – ГПУ (КЧ=12), ГЦК (КЧ=12), ОЦК (КЧ=8). Первые две относятся к плотнейшим упаковкам. 4. В ионной модели твердое вещество представляется совокупностью противоположно заряженных сфер. Ионные кристаллы можно рассматривать как совокупность противоположно заряженных шаров. Катионы в них занимают пустоты в упаковках, образованных анионами. Соотношение радиусов ионов определяет тип решетки. 5. Энергия кристаллической решетки – это разность между энергиями кристалла и изолированных газообразных ионов. Она определяется зарядами и радиусами ионов, а также типом решетки. 6. Энергия решетки определяет физико-химические свойства кристаллов – их устойчивость к нагреванию и растворимость в воде. Ее можно экспериментально измерить, используя цикл Борна-Габера. Физтех, 1 курс. Осень 2015 189
 Основные понятия § § § § § Кристалл Элементарная ячейка Координационное число атома (иона) Шаровые упаковки (плотнейшие), пустоты Структуры ГПУ, ГЦК, ОЦК Ионные кристаллы, катионы, анионы Радиус иона Структурный тип Na. Cl Энергия кристаллической решетки Цикл Борна-Габера Физтех, 1 курс. Осень 2015 190
Основные понятия § § § § § Кристалл Элементарная ячейка Координационное число атома (иона) Шаровые упаковки (плотнейшие), пустоты Структуры ГПУ, ГЦК, ОЦК Ионные кристаллы, катионы, анионы Радиус иона Структурный тип Na. Cl Энергия кристаллической решетки Цикл Борна-Габера Физтех, 1 курс. Осень 2015 190
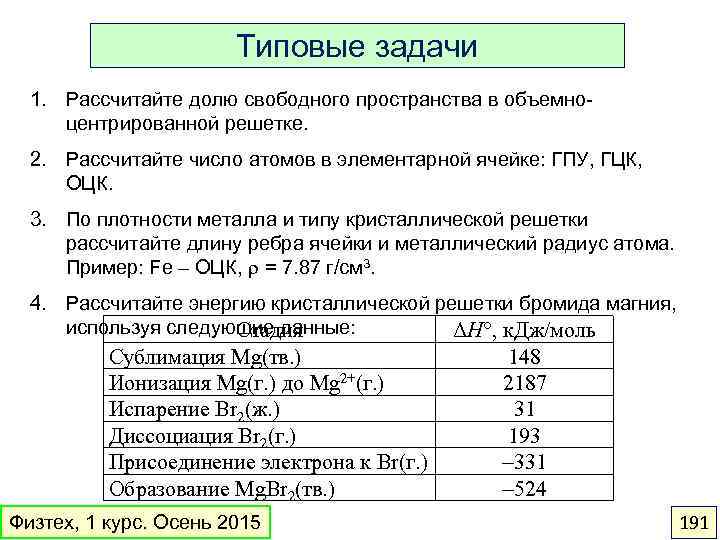 Типовые задачи 1. Рассчитайте долю свободного пространства в объемноцентрированной решетке. 2. Рассчитайте число атомов в элементарной ячейке: ГПУ, ГЦК, ОЦК. 3. По плотности металла и типу кристаллической решетки рассчитайте длину ребра ячейки и металлический радиус атома. Пример: Fe – ОЦК, = 7. 87 г/см 3. 4. Рассчитайте энергию кристаллической решетки бромида магния, используя следующие данные: Стадия ΔH , к. Дж/моль Сублимация Mg(тв. ) Ионизация Mg(г. ) до Mg 2+(г. ) Испарение Br 2(ж. ) Диссоциация Br 2(г. ) Присоединение электрона к Br(г. ) Образование Mg. Br 2(тв. ) Физтех, 1 курс. Осень 2015 148 2187 31 193 331 524 191
Типовые задачи 1. Рассчитайте долю свободного пространства в объемноцентрированной решетке. 2. Рассчитайте число атомов в элементарной ячейке: ГПУ, ГЦК, ОЦК. 3. По плотности металла и типу кристаллической решетки рассчитайте длину ребра ячейки и металлический радиус атома. Пример: Fe – ОЦК, = 7. 87 г/см 3. 4. Рассчитайте энергию кристаллической решетки бромида магния, используя следующие данные: Стадия ΔH , к. Дж/моль Сублимация Mg(тв. ) Ионизация Mg(г. ) до Mg 2+(г. ) Испарение Br 2(ж. ) Диссоциация Br 2(г. ) Присоединение электрона к Br(г. ) Образование Mg. Br 2(тв. ) Физтех, 1 курс. Осень 2015 148 2187 31 193 331 524 191
 Литература 1. Еремин, Борщевский. Общая и неорганическая химия. – Главы 15, 16. 2. Шрайвер, Эткинс. Неорганическая химия. – Т. 1, глава 2 (проще всего и ближе всего к материалу лекции). 3. Глинка. Общая химия. – Глава 5, § 5. 1. Физтех, 1 курс. Осень 2015 192
Литература 1. Еремин, Борщевский. Общая и неорганическая химия. – Главы 15, 16. 2. Шрайвер, Эткинс. Неорганическая химия. – Т. 1, глава 2 (проще всего и ближе всего к материалу лекции). 3. Глинка. Общая химия. – Глава 5, § 5. 1. Физтех, 1 курс. Осень 2015 192


