Лекция 1 по биохимии.ppt
- Количество слайдов: 46

Лекция 1 Наука биохимия

План лекции 1. Определение, цели, задачи, связь с другими науками, классификация 2. Химический состав и особенности обмена в живых организмах 3. Динамическое состояние постоянства биохимических параметров живых организмов

Биологическая химия – наука о химии жизни, о химических явлениях живой природы. Задача биохимии - идентификация основных закономерностей биохимических процессов, выяснение взаимосвязи между структурой и функциями биомолекул, участвующих в реакциях клеточного метаболизма, а также выяснение вопроса о происхождении жизни Предмет изучения - химический состав живых организмов, химические процессы , обеспечивающие их существование. Общая биохимия рассматривает общие для всех живых систем закономерности. Частная биохимия рассматривает биохимические особенности отдельных систем, органов, тканей, клеток.

Связь с другими науками биологическими науками : Ø генетика Ø ботаника Ø зоология Ø микробиология Ø физиология Ø фармакология Ø фармация Ø токсикология Ø патология другими науками: Ø экология Ø почвоведение Ø физика Ø математика Ø биоинформатика Ø химия

Классификация науки биохимия: 1. По виду объекта: Ø биохимия человека Ø биохимия животных Ø биохимия растений Ø биохимия микроорганизмов Ø биохимия вирусов

2. По направлению изучения: Ø статическая – изучает химический состав и свойства исследуемого объекта Ø динамическая (метаболическая) – обмен веществ и энергии Ø функциональная – изучает химические основы физиологической деятельности организма в целом, органа, ткани, клетки, взаимосвязь меду химическими превращениями веществ в организме и их функциями

3. По объектам исследования: Ø медицинская биохимия Ø фармацевтическая биохимия Ø биохимия почв Ø биохимическая экология Ø биохимическая фармакология

Общие экспериментальные подходы 1. Выделение биомолекул и органелл из клетки 2. Определение структуры биомолекул 3. Использование различных препаратов для анализа функций биомолекул и их метаболизма

Биологически важные химические элементы. Классификация 15 + 8 -10 элементов обнаружены в составе живой материи из 81 стабильных природных химических элементов 99% (60 -70%)-Н, О, С, N (основные элементы) 60 -70% - Н и О Макроэлементы - Н, О, С, N, P, S – входят в состав большинства живых организмов – составляющие органических соединений 0, 5%(0, 1%) - ионы: Микроэлементы: щелочные Ме –Na, K Щелочноземельные Ме - Mg, Ca галоген Cl –анион Следовые элементы: Переходные Ме – Fe, Zn, Co, Mn Неметаллы - I, Se

Универсальные элементы: - N, Н, Fe, К, О, Na, S, С, Р - имеют структурно – функциональное значение для всех организмов Минорные элементы (Микро – и следовые элементы) –Cu, Co, Na, Cl, Mn, Zn, Se, Ni, W Классификация молекул: Малые молекулы: молекулы – предшественники поступающие извне-H 2 O, CO 2, N 2, Mg 2+, Ca 2+, NO 3 -, SO 4(2), PO 4(2 -), Cl-, K+, промежуточные молекулы -органических кислот, рибозы, молекулы строительных блоков –аминокислоты, амино-, моно - нуклеотиды, монозы, глицерин, жирные кислоты Масса - 1 k Da Большие молекулы : нуклеиновые кислоты, белки, полисахариды, липиды, витамины, гормоны - 1 -103 k Da
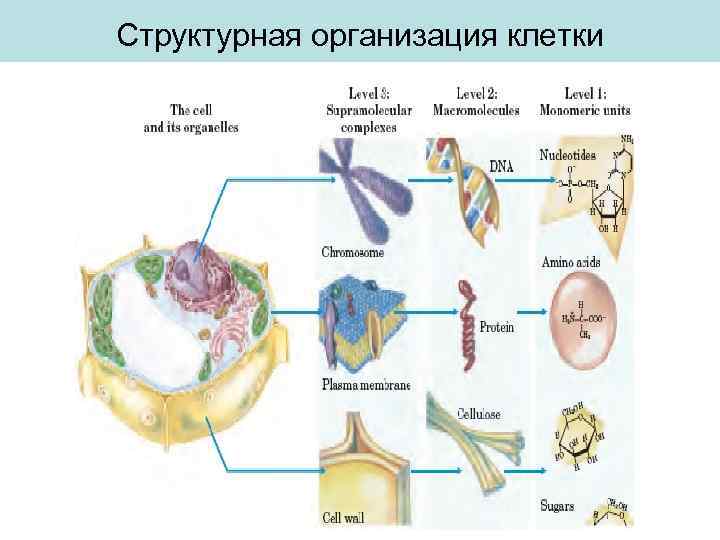
Структурная организация клетки

Белки Белок (Фермент) Рибонуклеаза барназа
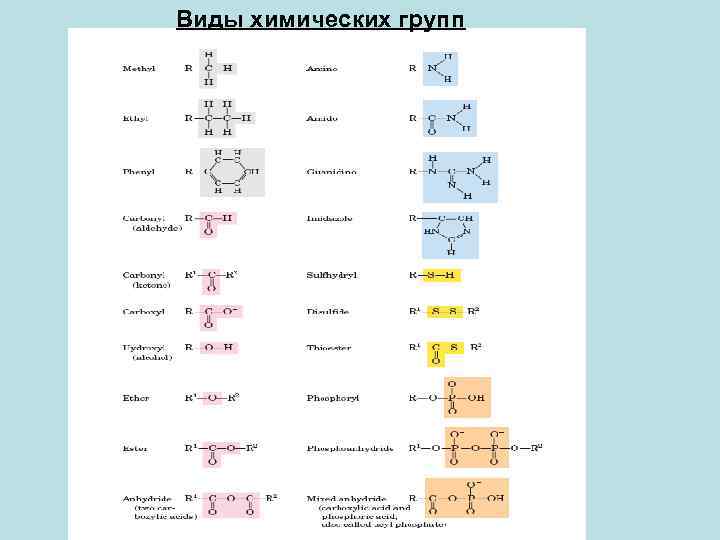
Виды химических групп
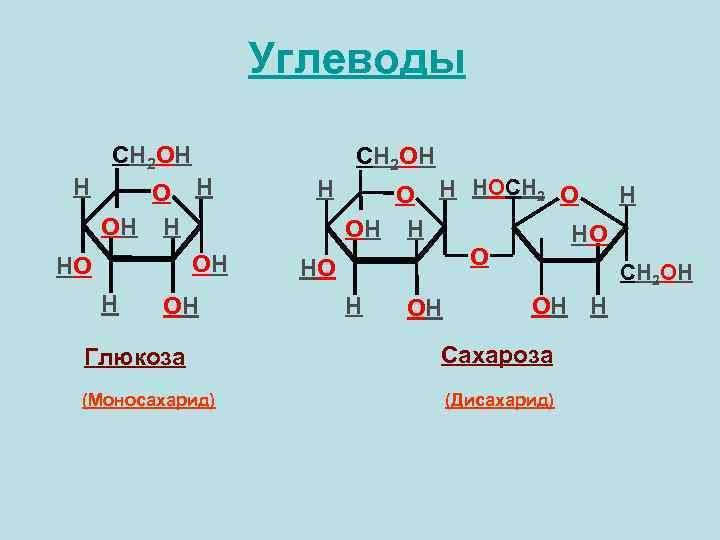
Углеводы CH 2 OH H OH HO H OH CH 2 OH H O H HOCH 2 O H OH H HO O HO CH 2 OH H OH Глюкоза Сахароза (Моносахарид) (Дисахарид)
Углеводы полисахариды Амилоза (фрагмент)
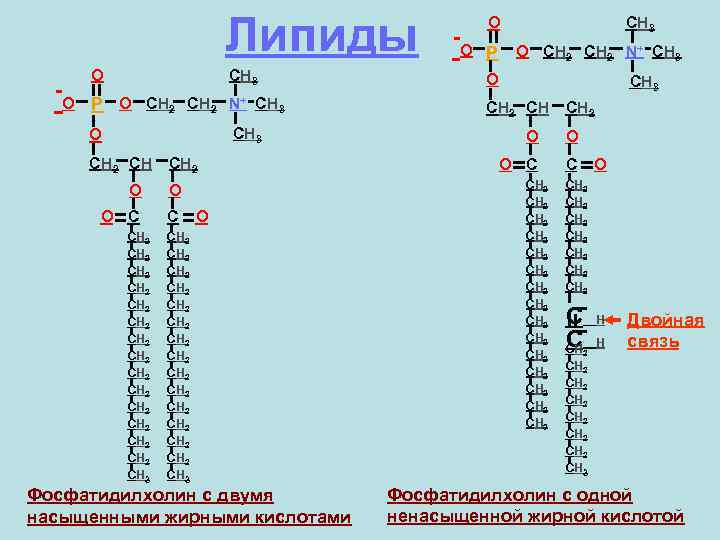
Липиды -O O CH 3 P O CH 2 N+ CH 3 O CH 2 CH CH 2 O O O C C CH 2 CH 2 CH 2 CH 2 CH 3 O CH 2 CH 2 CH 2 CH 2 CH 3 Фосфатидилхолин с двумя насыщенными жирными кислотами -O O CH 3 P O CH 2 N+ CH 3 O CH 3 CH 2 CH CH 2 O O O C C CH 2 CH 2 CH 2 CH 2 CH 3 O CH 2 CH 2 C C CH 2 H H Двойная связь CH 2 CH 2 CH 3 Фосфатидилхолин с одной ненасыщенной жирной кислотой
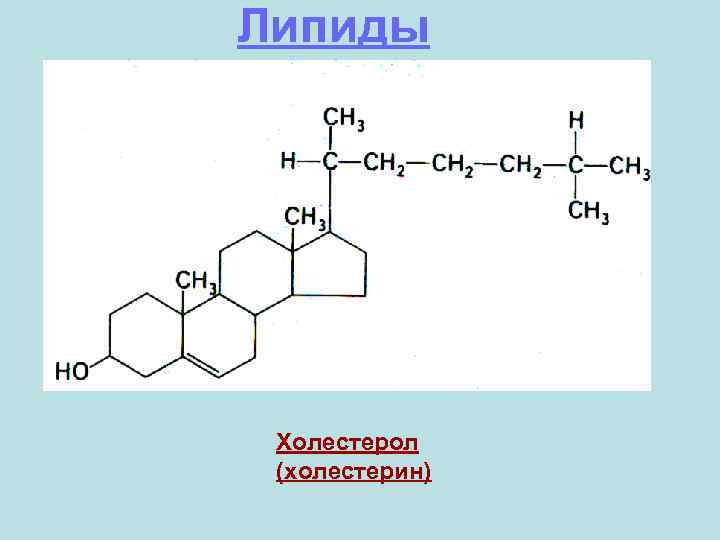
Липиды Холестерол (холестерин)

Биомолекулы – производные 4 элементов O, N, S, P Биомолекулы с O, N, S, P могут рассматриваться как производные H 2 O, NH 3, H 2 S, H 3 PO 4 Органические вещества содержат полярные группировки – ОН, - NH 3 - функциональные группы, как наиболее реакционноспособные

АМИНОКИСЛОТЫ
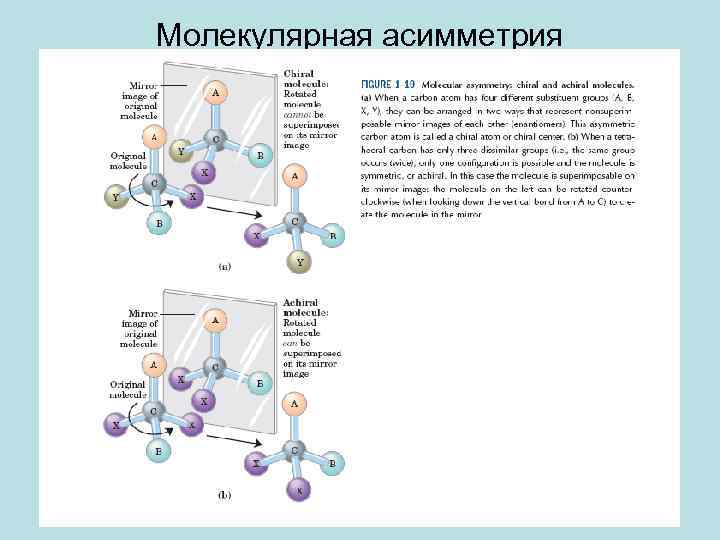
Молекулярная асимметрия
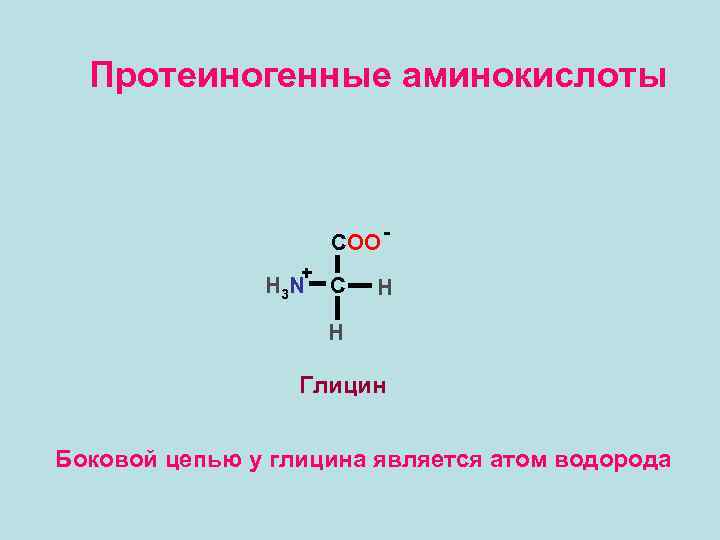
Протеиногенные аминокислоты COO + H 3 N C H H Глицин Боковой цепью у глицина является атом водорода
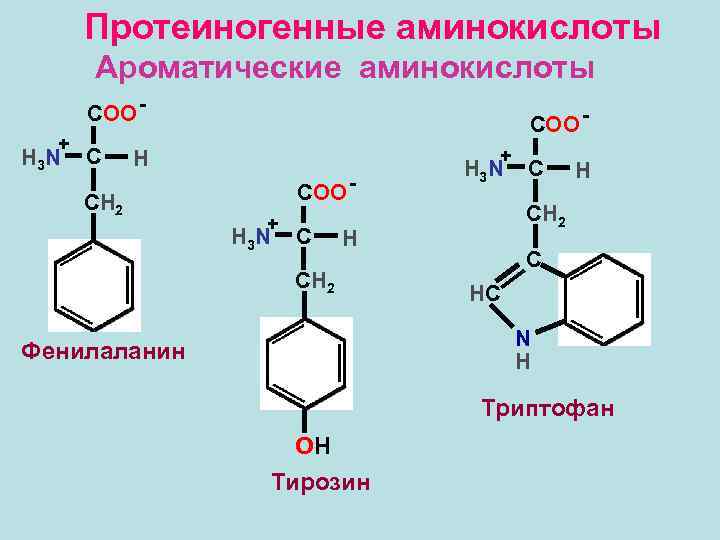
Протеиногенные аминокислоты Ароматические аминокислоты COO + H 3 N C COO + H СН 2 COO + H 3 N C H 3 N H СН 2 C С HC N H Фенилаланин Триптофан OH Тирозин
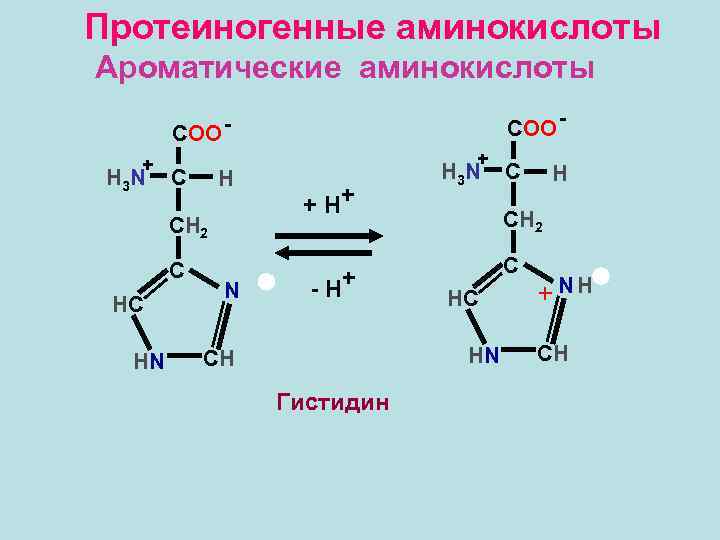
Протеиногенные аминокислоты Ароматические аминокислоты COO - COO + H 3 N C H СН 2 C HC HN N + + H+ - H+ H 3 N Гистидин H СН 2 C HC HN CH C N Н+ + CH
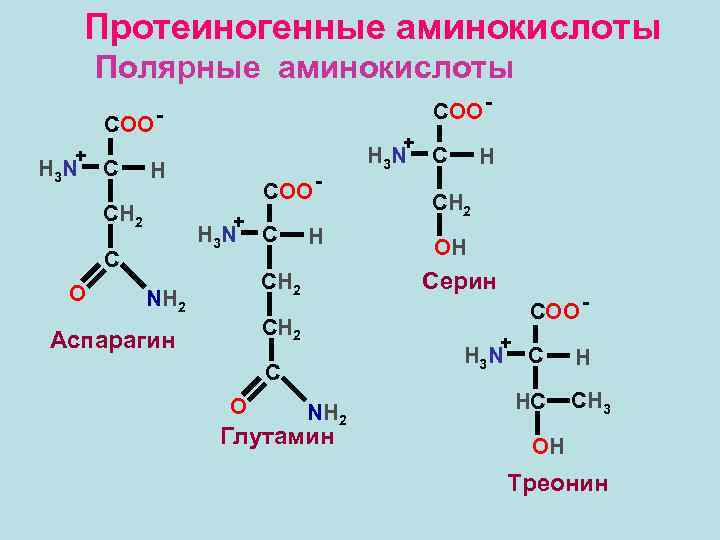
Протеиногенные аминокислоты Полярные аминокислоты COO - COO + H 3 N C H СН 2 COO + H 3 N C O + C H CH 2 Аспарагин H СН 2 OH COO + H 3 N C O C Серин СН 2 NH 2 H 3 N NH 2 Глутамин C HС H CH 3 OH Треонин
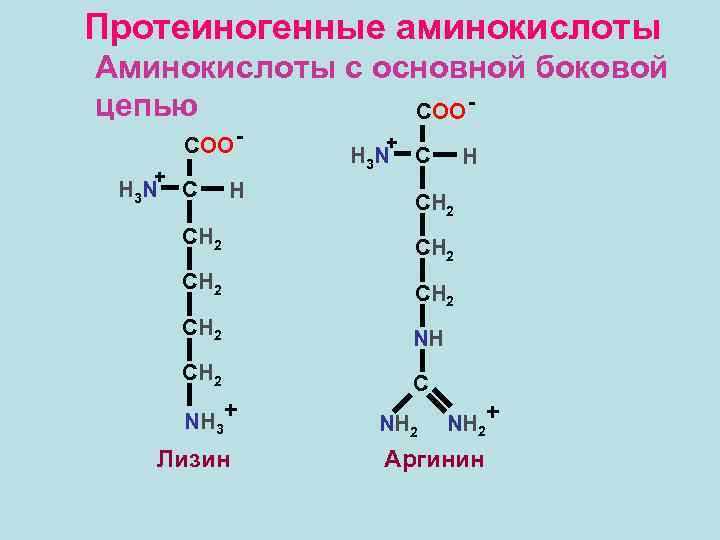
Протеиногенные аминокислоты Аминокислоты с основной боковой цепью COO - + H 3 N C H СН 2 СН 2 NH СН 2 C NH 3+ Лизин NH 2+ Аргинин
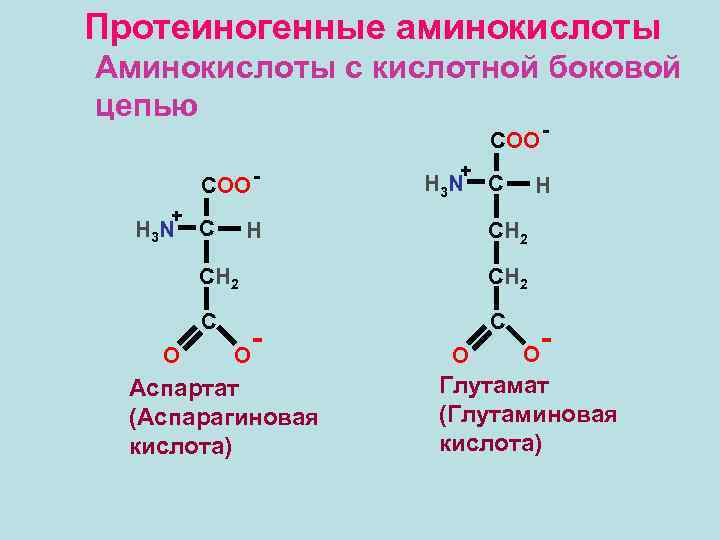
Протеиногенные аминокислоты Аминокислоты с кислотной боковой цепью COO - COO + H 3 N C + H 3 N H C H СН 2 С O Аспартат (Аспарагиновая кислота) O O Глутамат (Глутаминовая кислота)
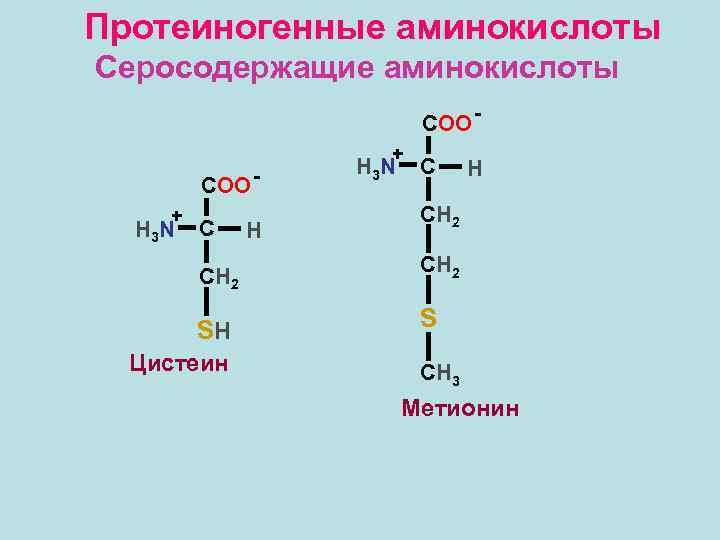
Протеиногенные аминокислоты Серосодержащие аминокислоты COO + H 3 N C СН 2 SH Цистеин H + H 3 N C H СН 2 S СН 3 Метионин
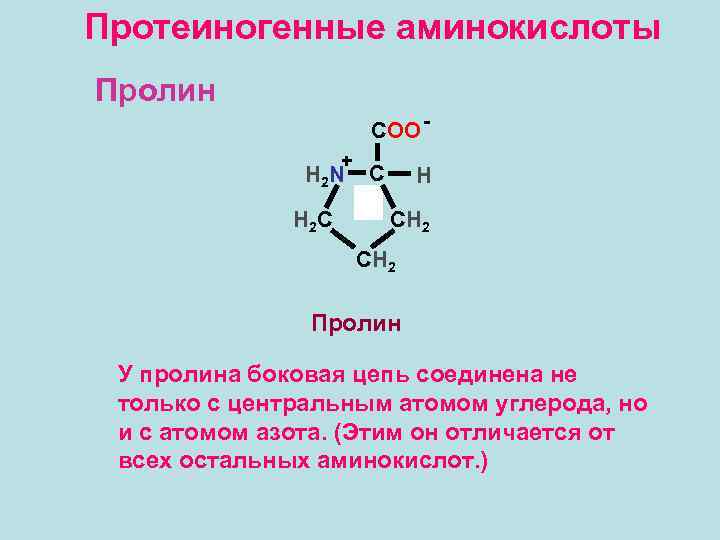
Протеиногенные аминокислоты Пролин COO + H 2 N Н 2 С C H СН 2 Пролин У пролина боковая цепь соединена не только с центральным атомом углерода, но и с атомом азота. (Этим он отличается от всех остальных аминокислот. )
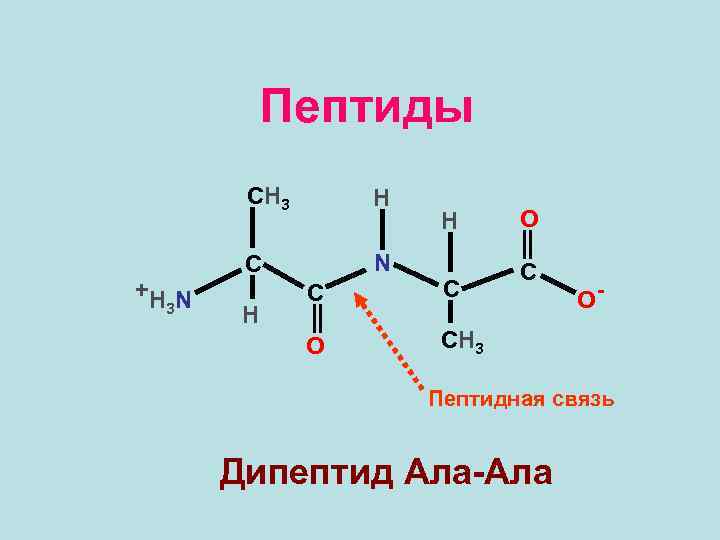
Пептиды CH 3 +H N 3 H C N H C O C CH 3 O- Пептидная связь Дипептид Ала-Ала
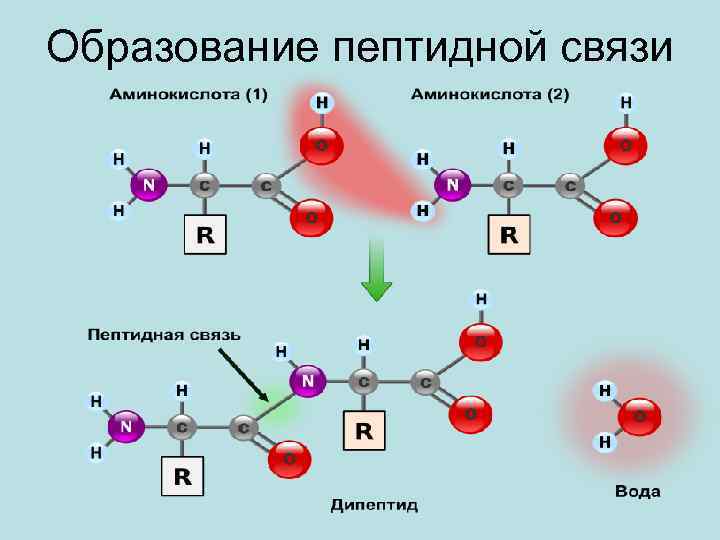
Образование пептидной связи

Белки • Высокомолекулярные азотсодержащие органические вещества, молекулы которых построены из остатков аминокислот. Название протеины (от греч. protos – первый, важнейший) – точно отражает первостепенное биологическое значение белков. • Белковые вещества в природе находятся в различных состояниях. Например, белки молока, сыворотки крови представляют коллоидные растворы (золи), другие – твердые вещества, нерастворимые в воде (кератин шерсти, рога и т. д. ). В некоторых органах белки находятся в полужидком состоянии (кожа, мышцы).

Функции белков: 1. Каталитическая функция. Все открытые биологические катализаторы – ферменты являются белками, известных ферментов сейчас свыше 3000. Эта функция белков является уникальной, не свойственной другим полимерным молекулам. Правда, в последнее время стало известно, что рибонуклеиновые кислоты также могут обладать ферментативной активностью. Их называют рибозимами. 2. Питательная (резервная) функция. К таким белкам относятся так называемые резервные белки, являющиеся источником питания для развития плода; белки яйца (овальбумины) и основной белок молока (казеин), также выполняют главным образом питательную функцию. Ряд белков используется в качестве источника аминокислот, которые в свою очередь являются предшественниками биологически активных веществ.

3. Транспортная функция. Дыхательная функция крови, в частности, перенос O 2, целиком осуществляется молекулами гемоглобина – белка эритроцитов. В транспорте липидов принимают участие альбумины сыворотки крови. Белки сыворотки образуют комплексы с жирами, медью, железом, тироксином, витамином А и другими соединениями, обеспечивая их доставку в соответствующие органы. 4. Защитная функция. Основную функцию защиты в организме выполняет иммунологическая система, которая обеспечивает синтез специфических защитных белков – антител в ответ на поступление в организм бактерий, токсинов или вирусов. Взаимодействие антител с антигенами (чужеродными белками) способствует нейтрализации их биологического действия, что обеспечивает безопасность организма от генетически чужеродной информации. Способ свертывания крови это тоже защитная реакция: свертывание белка плазмы крови фибриногена приводит к образованию сгустка крови, что предохраняет от потери крови при ранениях. Интерферон – универсальный противовирусный белок также выполняет защитную функцию.

5. Сократительная функция. В сокращении и расслаблении мышц участвуют белки актин и миозин – специфические белки мышечной ткани. Сократительная функция присуща не только мышечным белкам, но и белкам ряда субклеточных структур, что обеспечивает определенные процессы жизнедеятельности клеток. 6. Структурная функция белков занимает очень большое место. Например: коллаген в соединительной ткани, кератин в волосах, ногтях, роговой ткани, эластин в сосудистой стенке выполняют пластические и опорные функции. Важную роль играют белки в комплексе с углеводами в формировании ряда секретов – мукоидов, муцинов и т. д. В комплексе с липидами (фосфолипидами) белки участвуют в образовании биомембран клетки. 7. Гормональная функция. В регуляции обмена веществ в организме важную роль играют гормоны, которые вырабатываются в железах внутренней секреции. Ряд гормонов являются белками или полипептидами: гормоны гипофиза – соматотропин, окситоцин, вазопрессин; гормон поджелудочной железы – инсулин и т. д.

Кроме указанных функций, следует отметить, что белки в организме играют важную роль в поддержании онкотического давления и в создании буферных систем. Белки осуществляют генерирование и передачу нервных импульсов. Например, родопсин является фоторецепторным белком клеток палочек сетчатки глаза, имеются белки – вкусовые рецепторы, обонятельные рецепторы.

Физико-химические свойства белков Ø Молекулярная масса белков колеблется в широких пределах: от нескольких тысяч дальтон (инсулин – 5700) до сотен миллионов (белок вируса гриппа – 322∙ 106). Форма белковых молекул бывает глобулярная (шаровидная) и фибриллярная (нитевидная. Ø Форма белковых молекул изменяется под влиянием различных факторов: р. Н, температуры среды, ионной силы, природы растворителя, концентрации раствора.

Ø В глобулярных белках полипептидная цепь свернута так, что образуется компактная структура. Эти белки обычно растворимы в водной среде. Ø В кератине, фибриллярном белке шерсти, полипептидные цепи вытянуты вдоль одной оси. На рисунке показаны три молекулы кератина, навитые одна на другую наподобие каната. Фибриллярные белки нерастворимы в воде. Ø Большинство белков растворяется в воде. Они образуют лиофильные коллоидные растворы. Молекулы белков имеют большие размеры и не проходят через поры полупроницаемых мембран. Ø Молекулярно-кинетические свойства коллоидных растворов белков связаны с размерами и перемещением мицелл в среде, р. Н раствора и т. д. Белки имеют низкий коэффициент диффузии, низкое осмотическое давление, высокую относительную вязкость и большую степень набухания – белки связывают до 80 -90% всей воды организма.

• Вода обеспечивает формирование структуры белков. Общее количество связанной воды составляет в миоглобине, лизоциме, цитохроме около 22% от общей массы белка. Под влиянием различных факторов белки могут выпадать из коллоидных растворов в осадок (коагулировать); это легче происходит в изоэлектрической точке белка. • Коагуляция бывает обратимая, когда нарушается в коллоидной частице только сольватная оболочка и необратимая, когда произошли глубокие нарушения структуры белковой молекулы. Необратимую коагуляцию называют денатурацией. Она вызывается кипячением, действием солей тяжелых металлов, алкалоидов, минеральных кислот и т. д.
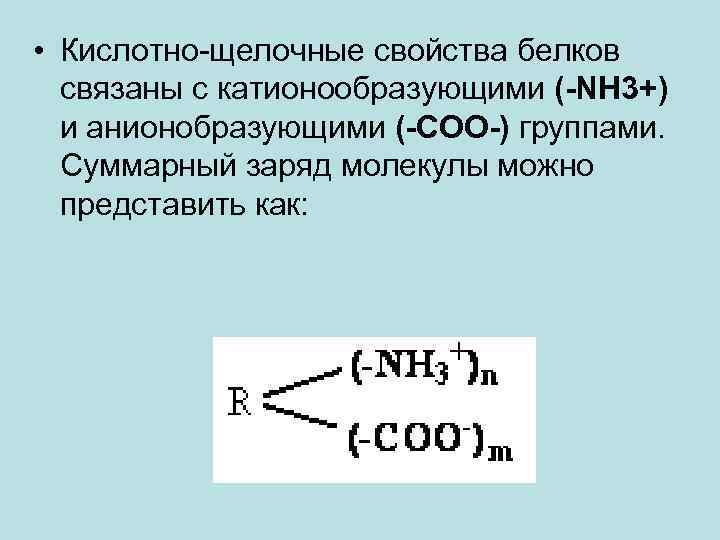
• Кислотно-щелочные свойства белков связаны с катионообразующими (-NH 3+) и анионобразующими (-COO-) группами. Суммарный заряд молекулы можно представить как:

• Знак заряда зависит от соотношения аминных и карбоксильных групп, соответственно различают белки кислые, нейтральные и щелочные (основные).
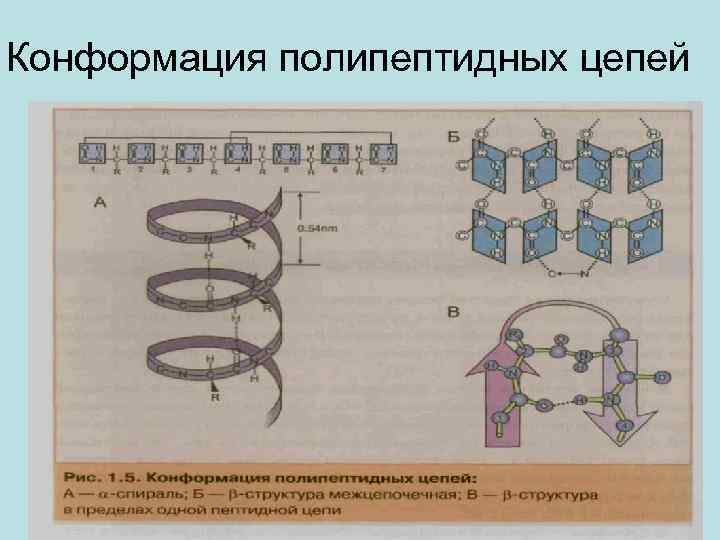
Конформация полипептидных цепей
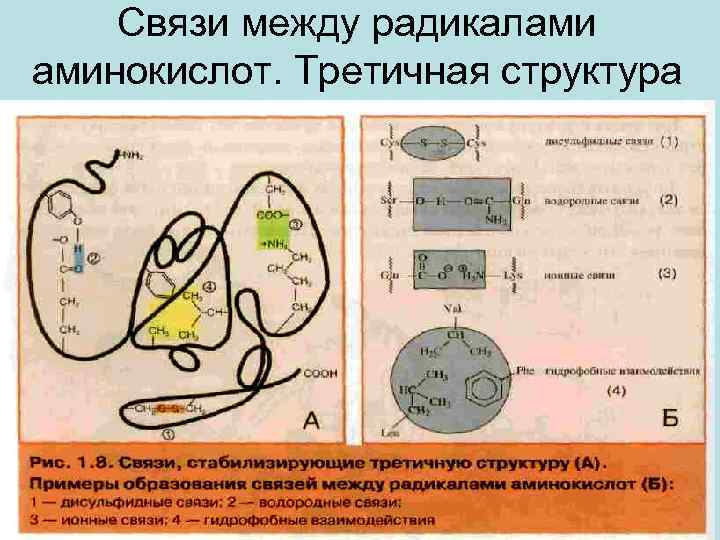
Связи между радикалами аминокислот. Третичная структура
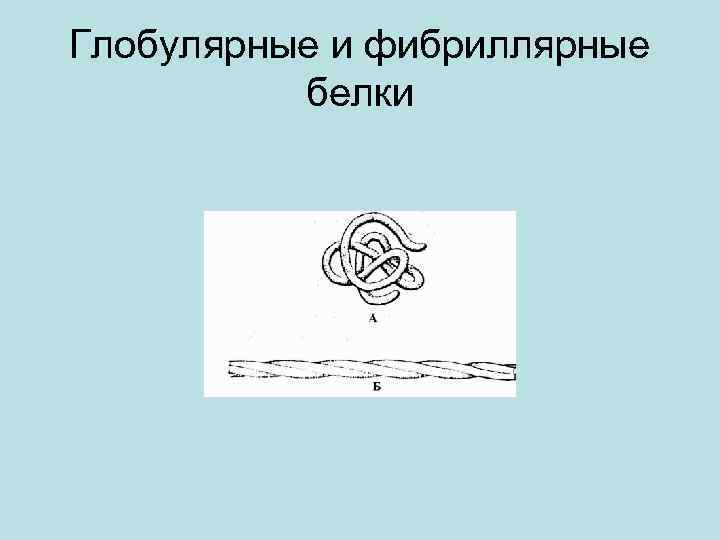
Глобулярные и фибриллярные белки
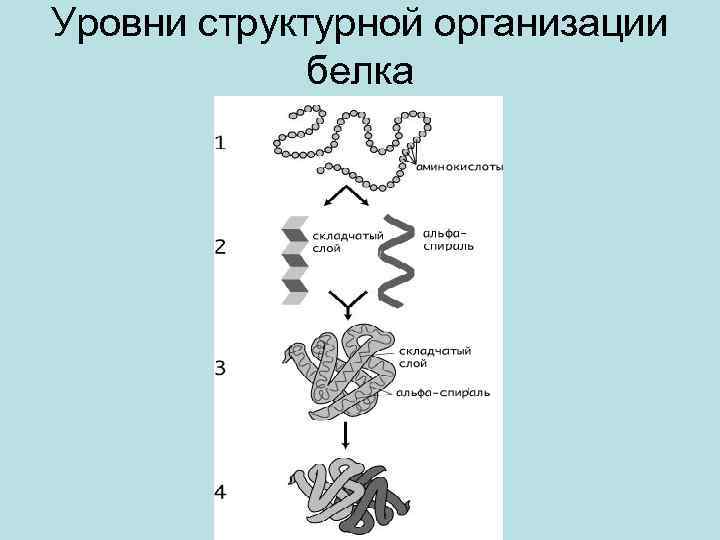
Уровни структурной организации белка

Учебно-методическое и информационное обеспечение дисциплины «Биохимия» а) основная литература: 1. Северин Е. С. , Алейникова Т. Л. , Осипов Е. В. Биологическая химия: учебник для студентов медицинских вузов – М. : ООО «Медицинское информационное агентство» , 2008. – 368 с. 2. Филиппович Ю. Б. , Ковалевская Н. И. , Севастьянова Г. А. Биологическая химия – 2 -е издание, перераб. и доп. – М. : Издательский центр «Академия» , 2008. – 256 с. 3. Березов Т. Т. , Коровкин Б. Ф. Биологическая химия: учебник – Изд. 3 -е, стер. – М. : Медицина, 2007. – 703 с. 4. Комов В. П. , Шведова В. Н. Биохимия: Учебник для ВУЗов, 2 -е изд. , испр. - М. : Дрофа, 2006. – 638 с. 5. Хазипов Н. З. , Аскарова А. Н. Биохимия животных. - Казань: Изд-во Казан. гос. акад. вет. медицины, 2003. — 310 с. : ил.

б) дополнительная литература: 1. Биологическая химия: учебник. В. К. Кухта, Т. С. Морозкина, Э. И. Олецкий, А. Д. Таганович; под ред. А. Д. Тагановича. – Минск: Асар, М. : Издательство БИНОМ, 2008. – 688 с. : ил. 2. Комов В. П. Шведова В. Н. Биохимия: Учебник для ВУЗов, 3 -е изд, стереот. - М. : Дрофа, 2008. - 640 с. 3. Коничев А. С. , Севастьянова Г. А. Биохимия: задачи и упражнения. - М. : Колос. С, 2007 г. - 144 с. 4. Кольман Я. , Рем К. -Г. Наглядная биохимия. М. : Мир. , 2004. 469 с. 5. Обмен нуклеиновых кислот: Учебное пособие для вузов / Ф. К. Алимова, Т. А. Невзорова; под ред. Т. А. Невзоровой. – Казань: КГУ, 2009. – 62 с. : ил. 6. Кнорре Д. Г. Мызина С. Д. Биологическая химия. – М. : 2002. - 479 с. 7. Хазипов Н. З. , Аскарова А. Н. , Тюрикова Р. П. Биохимия животных с основами физколлоидной химии. – М. : Колос. С, 2010. – 328 с. : ил.
Лекция 1 по биохимии.ppt