Лекция1 введение.ppt
- Количество слайдов: 56
 Лекция 1. Место химии в системе естественных наук. Атомно-молекулярное учение. Основные понятия и законы химии.
Лекция 1. Место химии в системе естественных наук. Атомно-молекулярное учение. Основные понятия и законы химии.
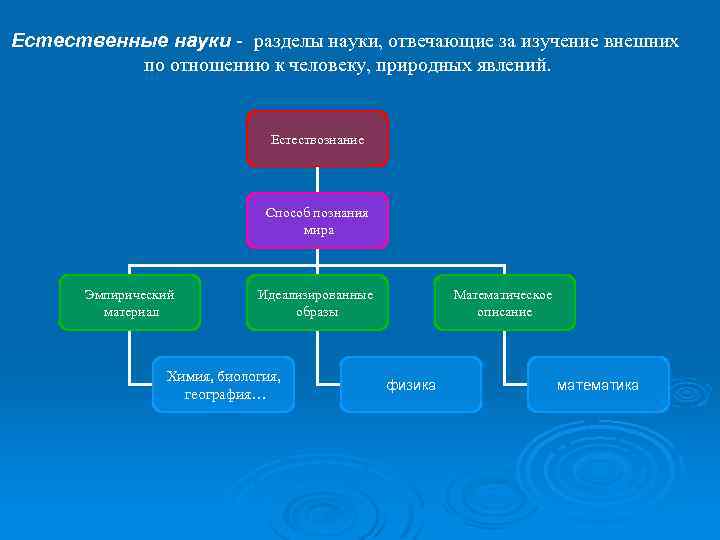 Естественные науки - разделы науки, отвечающие за изучение внешних по отношению к человеку, природных явлений. Естествознание Способ познания мира Эмпирический материал Идеализированные образы Химия, биология, география… Математическое описание физика математика
Естественные науки - разделы науки, отвечающие за изучение внешних по отношению к человеку, природных явлений. Естествознание Способ познания мира Эмпирический материал Идеализированные образы Химия, биология, география… Математическое описание физика математика
 Идеализированные образы
Идеализированные образы
 Математическое описание
Математическое описание
 “Пока математические законы описывают действительность, они неопределённы, а когда они перестают быть неопределенными, они теряют связь с действительностью” (А. Эйнштейн)
“Пока математические законы описывают действительность, они неопределённы, а когда они перестают быть неопределенными, они теряют связь с действительностью” (А. Эйнштейн)
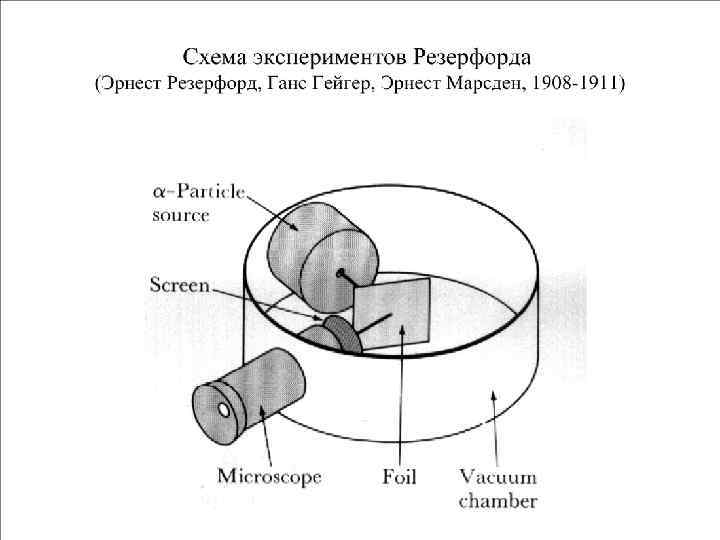
 Эксперимент Э. Резерфорда с рассеянием альфа-частиц толщина золотой фольги - 4· 10 -5 см вероятный угол рассеяния частиц - 0, 870. Для чрезвычайно редких (1 из 20000 измерений) случаев рассеяние на угол более 90 градусов по теории вероятностей составляет - 3 10 -2174
Эксперимент Э. Резерфорда с рассеянием альфа-частиц толщина золотой фольги - 4· 10 -5 см вероятный угол рассеяния частиц - 0, 870. Для чрезвычайно редких (1 из 20000 измерений) случаев рассеяние на угол более 90 градусов по теории вероятностей составляет - 3 10 -2174
 ТРИ признака естественнонаучного знания Истинность - определяется принципом достаточного основания: всякая истинная мысль должна быть обоснована другими мыслями, истинность которых доказана.
ТРИ признака естественнонаучного знания Истинность - определяется принципом достаточного основания: всякая истинная мысль должна быть обоснована другими мыслями, истинность которых доказана.
 Интерсубъективность – каждый исследователь должен получать одинаковые результаты при изучении одного и того же объекта в одних и тех же условиях.
Интерсубъективность – каждый исследователь должен получать одинаковые результаты при изучении одного и того же объекта в одних и тех же условиях.
 Системность научного знания подразумевает его строгую индуктивно-дедуктивную структуру.
Системность научного знания подразумевает его строгую индуктивно-дедуктивную структуру.
 Ø Парадигма – набор убеждений, ценностей и техник, разделяемых членами данного научного сообщества. Ø Запретная зона – та область в данной научной дисциплине, исследования в которой подавляющим большинством ученых принято считать «ненаучными» , «антинаучными» и т. д.
Ø Парадигма – набор убеждений, ценностей и техник, разделяемых членами данного научного сообщества. Ø Запретная зона – та область в данной научной дисциплине, исследования в которой подавляющим большинством ученых принято считать «ненаучными» , «антинаучными» и т. д.
 Основные парадигмы современной химии: - атомно-молекулярное строение вещества, - электронная природа химической связи, - периодический закон Запретные зоны: трансмутация (алхимическое превращение элементов)
Основные парадигмы современной химии: - атомно-молекулярное строение вещества, - электронная природа химической связи, - периодический закон Запретные зоны: трансмутация (алхимическое превращение элементов)
 Ø Химия – наука о превращениях веществ, связанных с изменением электронного окружения ядер.
Ø Химия – наука о превращениях веществ, связанных с изменением электронного окружения ядер.
 Объект изучения: Вещество – форма материи, обладающая массой покоя, состоящая из элементарных частиц: электронов, протонов, нейтронов и т. д.
Объект изучения: Вещество – форма материи, обладающая массой покоя, состоящая из элементарных частиц: электронов, протонов, нейтронов и т. д.
 Простые вещества Образованы атомами одного хим. элемента и потому являются формой его существования в свободном состоянии, например, сера, железо, озон, алмаз.
Простые вещества Образованы атомами одного хим. элемента и потому являются формой его существования в свободном состоянии, например, сера, железо, озон, алмаз.
 Химический элемент – это вид атомов, характеризующийся определенными зарядами ядер и строением электронных оболочек.
Химический элемент – это вид атомов, характеризующийся определенными зарядами ядер и строением электронных оболочек.
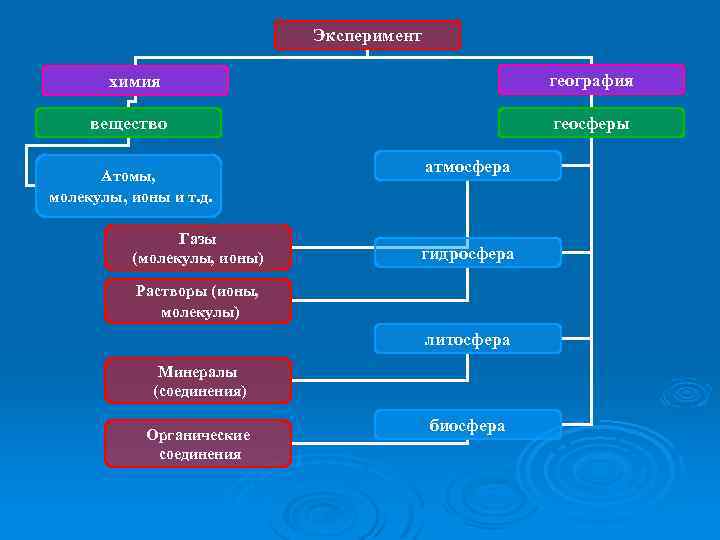 Эксперимент география химия вещество Атомы, молекулы, ионы и т. д. Газы (молекулы, ионы) геосферы атмосфера гидросфера Растворы (ионы, молекулы) литосфера Минералы (соединения) Органические соединения биосфера
Эксперимент география химия вещество Атомы, молекулы, ионы и т. д. Газы (молекулы, ионы) геосферы атмосфера гидросфера Растворы (ионы, молекулы) литосфера Минералы (соединения) Органические соединения биосфера
 Атомно-молекулярное учение Ø Все вещества состоят из молекул. Ø Молекула - наименьшая частица вещества, обладающая его химическими свойствами.
Атомно-молекулярное учение Ø Все вещества состоят из молекул. Ø Молекула - наименьшая частица вещества, обладающая его химическими свойствами.
 ØМолекулы состоят из атомов. ØАтом – наименьшая частица химического элемента, сохраняющая все его химические свойства. Различным элементам соответствуют различные атомы.
ØМолекулы состоят из атомов. ØАтом – наименьшая частица химического элемента, сохраняющая все его химические свойства. Различным элементам соответствуют различные атомы.
 ØМолекулы и атомы находятся в непрерывном движении; между ними существуют силы притяжения и отталкивания.
ØМолекулы и атомы находятся в непрерывном движении; между ними существуют силы притяжения и отталкивания.
 Ø Атомное ядро – центральная часть атома, состоящая и Z протонов и N нейтронов, в которой сосредоточена основная масса атомов. 63 Сu и 2965 Cu 29
Ø Атомное ядро – центральная часть атома, состоящая и Z протонов и N нейтронов, в которой сосредоточена основная масса атомов. 63 Сu и 2965 Cu 29
 ØЗаряд ядра – положительный, по величине равен количеству протонов в ядре или электронов в нейтральном атоме и совпадает с порядковым номером элемента в ПС.
ØЗаряд ядра – положительный, по величине равен количеству протонов в ядре или электронов в нейтральном атоме и совпадает с порядковым номером элемента в ПС.
 ØМассовое число А = Z + N.
ØМассовое число А = Z + N.
 Изотопы – химические элементы с одинаковыми зарядами ядер, но различными массовыми числами за счет разного числа нейтронов в ядре
Изотопы – химические элементы с одинаковыми зарядами ядер, но различными массовыми числами за счет разного числа нейтронов в ядре
 Химическая формула – это условная запись состава вещества с помощью химических знаков и индексов. (Й. Берцелиус, 1814).
Химическая формула – это условная запись состава вещества с помощью химических знаков и индексов. (Й. Берцелиус, 1814).
 Химические реакции явления, при которых одни вещества, обладающие определенным составом и свойствами, превращаются в другие вещества - с другим составом и другими свойствами. При этом в составе атомных ядер изменений не происходит.
Химические реакции явления, при которых одни вещества, обладающие определенным составом и свойствами, превращаются в другие вещества - с другим составом и другими свойствами. При этом в составе атомных ядер изменений не происходит.
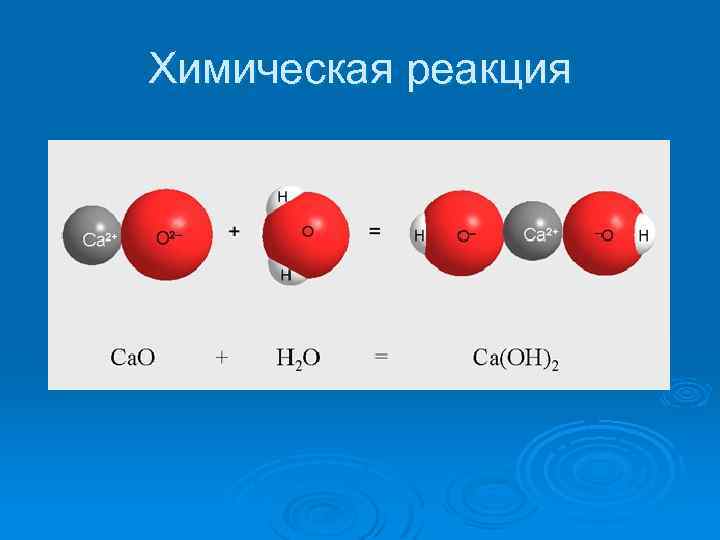 Химическая реакция
Химическая реакция
 Ø Международная единица атомных масс: 1 а. е. м. = 1/12 m (12 C) = 1, 66057 10 -24 г Ø Относительная атомная масса:
Ø Международная единица атомных масс: 1 а. е. м. = 1/12 m (12 C) = 1, 66057 10 -24 г Ø Относительная атомная масса:
 Средняя абсолютная масса атома: m = Ar а. е. м. m(Mg) = 24, 312· 1, 66057· 10 -24 = 4, 037· 10 -23 г.
Средняя абсолютная масса атома: m = Ar а. е. м. m(Mg) = 24, 312· 1, 66057· 10 -24 = 4, 037· 10 -23 г.
 относительная молекулярная масса:
относительная молекулярная масса:
 Ø абсолютная масса молекулы: Ø mм = Мr а. е. м.
Ø абсолютная масса молекулы: Ø mм = Мr а. е. м.
 ØМоль – количество вещества, содержащее столько же частиц, сколько содержится атомов в 12 г углерода, Молярная масса: г/моль
ØМоль – количество вещества, содержащее столько же частиц, сколько содержится атомов в 12 г углерода, Молярная масса: г/моль
 Валентность (от лат. valentia – сила), способность атома присоединять или замещать определенное число других атомов или атомных групп с образованием химической связи. Количественной мерой валентности атома элемента Э служит число атомов водорода или кислорода (эти элементы принято считать соответственно одно- и двухвалентными), которые Э присоединяет, образуя гидрид ЭНх или оксид Эn. Оm.
Валентность (от лат. valentia – сила), способность атома присоединять или замещать определенное число других атомов или атомных групп с образованием химической связи. Количественной мерой валентности атома элемента Э служит число атомов водорода или кислорода (эти элементы принято считать соответственно одно- и двухвалентными), которые Э присоединяет, образуя гидрид ЭНх или оксид Эn. Оm.
 Закон сохранения массы веществ (М. В. Ломоносов, 1748 г. , А. Лавуазье, 1789 г. ) Ø Масса всех веществ, вступивших в химическую реакцию, равна массе всех продуктов реакции.
Закон сохранения массы веществ (М. В. Ломоносов, 1748 г. , А. Лавуазье, 1789 г. ) Ø Масса всех веществ, вступивших в химическую реакцию, равна массе всех продуктов реакции.
 Закон постоянства состава (Ж. Пруст, 1808 г. ) (классическая формулировка) Ø Все индивидуальные химические вещества имеют постоянный качественный и количественный состав и определенное химическое строение, независимо от способа получения.
Закон постоянства состава (Ж. Пруст, 1808 г. ) (классическая формулировка) Ø Все индивидуальные химические вещества имеют постоянный качественный и количественный состав и определенное химическое строение, независимо от способа получения.
 Сложные вещества образованы разными элементами и могут иметь состав постоянный (стехиометрические соединения или дальтониды)
Сложные вещества образованы разными элементами и могут иметь состав постоянный (стехиометрические соединения или дальтониды)
 Ø меняющиеся в некоторых пределах (нестехиометрические соединения или бертоллиды). Соединения переменного состава: Fe. O 1, 02 – Fe. O 1, 19
Ø меняющиеся в некоторых пределах (нестехиометрические соединения или бертоллиды). Соединения переменного состава: Fe. O 1, 02 – Fe. O 1, 19
 Новая формулировка Химические соединения с молекулярной структурой имеют один и тот же состав и свойства независимо от способа получения; химические соединения с ионной структурой имеют в кристаллическом (или жидком) состоянии один и тот же состав только при строгом соблюдении постоянства всех условий получения вещества
Новая формулировка Химические соединения с молекулярной структурой имеют один и тот же состав и свойства независимо от способа получения; химические соединения с ионной структурой имеют в кристаллическом (или жидком) состоянии один и тот же состав только при строгом соблюдении постоянства всех условий получения вещества
 Закон эквивалентов Ø Массы веществ, вступающих в химическую реакцию, равны или кратны мольным (молярным массам их эквивалентов. Ø Эквивалент – химическая единица, которая может присоединять или выделять в реакции один атом или ион водорода.
Закон эквивалентов Ø Массы веществ, вступающих в химическую реакцию, равны или кратны мольным (молярным массам их эквивалентов. Ø Эквивалент – химическая единица, которая может присоединять или выделять в реакции один атом или ион водорода.
 Эквивалентная масса – масса элемента, которая присоединяет или замещает в соединении 1, 008 массовых частей водорода или 8, 000 частей кислорода (или 12 массовых частей углерода 12 С)
Эквивалентная масса – масса элемента, которая присоединяет или замещает в соединении 1, 008 массовых частей водорода или 8, 000 частей кислорода (или 12 массовых частей углерода 12 С)
 Закон кратных отношений (Д. Дальтон, 1803 г. ) Ø Если два химических элемента дают несколько соединений, то весовые доли одного и того же элемента в этих соединениях, приходящиеся на одну и ту же весовую долю второго элемента, относятся между собой как небольшие целые числа.
Закон кратных отношений (Д. Дальтон, 1803 г. ) Ø Если два химических элемента дают несколько соединений, то весовые доли одного и того же элемента в этих соединениях, приходящиеся на одну и ту же весовую долю второго элемента, относятся между собой как небольшие целые числа.
 валентность
валентность
 Закон объемных отношений (Гей-Люссак, 1808 г. ) Ø Объемы газов, вступающих в химические реакции, и объемы газов, образующихся в результате реакции, относятся между собой как небольшие целые числа.
Закон объемных отношений (Гей-Люссак, 1808 г. ) Ø Объемы газов, вступающих в химические реакции, и объемы газов, образующихся в результате реакции, относятся между собой как небольшие целые числа.
 Следствие Стехеометрические коэффициенты в уравнениях химических реакций для молекул газообразных веществ показывают, в каких объемных отношениях реагируют или получают газообразные вещества
Следствие Стехеометрические коэффициенты в уравнениях химических реакций для молекул газообразных веществ показывают, в каких объемных отношениях реагируют или получают газообразные вещества
 Закон Авогадро (1811 г. ) 1 моль – 6, 02 · 1023 частиц - NA Ø В равных объемах различных газов при одинаковых условиях (температура, давление и т. д. ) содержится одинаковое число молекул.
Закон Авогадро (1811 г. ) 1 моль – 6, 02 · 1023 частиц - NA Ø В равных объемах различных газов при одинаковых условиях (температура, давление и т. д. ) содержится одинаковое число молекул.
 Следствия: Одно и то же число молекул различных газов при одинаковых условиях занимает одинаковые объемы. При нормальных условиях (00 С (273 К), 1 атм (101, 3 к. Па, 760 мм. рт. ст. ) 1 моль любого газа занимает объем 22, 4 л.
Следствия: Одно и то же число молекул различных газов при одинаковых условиях занимает одинаковые объемы. При нормальных условиях (00 С (273 К), 1 атм (101, 3 к. Па, 760 мм. рт. ст. ) 1 моль любого газа занимает объем 22, 4 л.
 Объединенный газовый закон
Объединенный газовый закон
 ØПри р = const (закон Гей-Люссака)
ØПри р = const (закон Гей-Люссака)
 ØПри Т = const (закон Бойля – Мариотта)
ØПри Т = const (закон Бойля – Мариотта)
 ØПри V = const (закон Шарля)
ØПри V = const (закон Шарля)
 Уравнение состояния идеального газа (Клайперона) Ø при m = const
Уравнение состояния идеального газа (Клайперона) Ø при m = const
 Уравнение Менделеева – Клайперона
Уравнение Менделеева – Клайперона
 Относительная плотность газа –
Относительная плотность газа –
 Средняя молекулярная масса смеси газов
Средняя молекулярная масса смеси газов
 Роль химии
Роль химии
 Химический состав Земли и Космических тел
Химический состав Земли и Космических тел


