
ЛЕКЦИИ: ОБМЕН ЛИПИДОВ Дисциплина: С. 2. Б. 5. Биологическая химия, биохимия полости рта Специальность: 060201 Стоматология НГМУ, КАФЕДРА МЕДИЦИНСКОЙ ХИМИИ Д. Б. Н. , ДОЦЕНТ УМЕНКОВА ДИНА ВАЛЕРЬЕВНА С

ЛЕКЦИЯ 5 (1) 2 Ассимиляция пищевого жира Липопротеины плазмы крови Липогенез

АКТУАЛЬНОСТЬ ТЕМЫ Липиды играют важную роль в функционировании живых организмов: Ø фосфолипиды – основа клеточных мембран Знание биохимии липидов необходимо для понимания научных основ профилактики заболеваний: Ø незаменимые ЖК – кардиопротекторы Знание биохимии липидов необходимо для понимания некоторых медицинских проблем: ü атеросклероз, в том числе сосудов десен Нарушения процессов переваривания, всасывания, транспорта липидов, синтеза жирных кислот и ТАГ играют важную роль в патогенезе ряда заболеваний человека 3

ПЛАН ЛЕКЦИИ Общие понятия о липидах (самостоятельное повторение курса химии): структура, классификация, биологическая роль Ассимиляция пищевых жиров Липопротеины плазмы крови Липогенез: синтез ВЖК и ТАГ Цель лекции: Знать: химическую сущность процессов усвоения пищевого жира: переваривания, всасывания и транспорта липидов в ткани Знать: химическую сущность процесса липогенеза в тканях (синтез жирных кислот и триацилглицеридов) 4

ОБЩИЕ ПОНЯТИЯ О ЛИПИДАХ (ПОВТОРЕНИЕ КУРСА ХИМИИ) 5 ХИМИЯ ЛИПИДОВ: ОБЩИЕ СВОЙСТВА КЛАССИФИКАЦИЯ ЛИПИДОВ БИОЛОГИЧЕСКАЯ РОЛЬ ЛИПИДОВ

ОПРЕДЕЛЕНИЕ ПОНЯТИЯ «ЛИПИДЫ» Липиды (греч. «жир» ) - это химически гетерогенная группа органических соединений, непосредственно или опосредованно связанных с жирными кислотами (ЖК) Общие свойства липидов: относительная нерастворимость в воде растворимость в неполярных растворителях наличие высших алкильных радикалов в структуре молекул 6

ЖИРНЫЕ КИСЛОТЫ АЛИФАТИЧЕСКИЕ КАРБОНОВЫЕ КИСЛОТЫ Насыщенные: Сn. H 2 n+1 COOH ω α 1 Н 3 С – (СН 2)10 – СН 2 – СООН тетрадекановая (миристиновая С 13 Н 27 СООН) Ненасыщенные: Сn H(2 n+1)-2 m COOH m – количество двойных связей (моно-, полиеновые) 13 12 10 9 Н 3 С – (СН 2)4 – СН = СН – СН 2 – СН = СН – (СН 2)7 – СООН октадекадиеновая (линолевая С 17 Н 31 СООН) 18: 2; ∆9, 12 ряд ω-6 § § в природных жирах – четное число атомов С (12 – 24) природные полиеновые ЖК имеют цис-конфигурацию 7
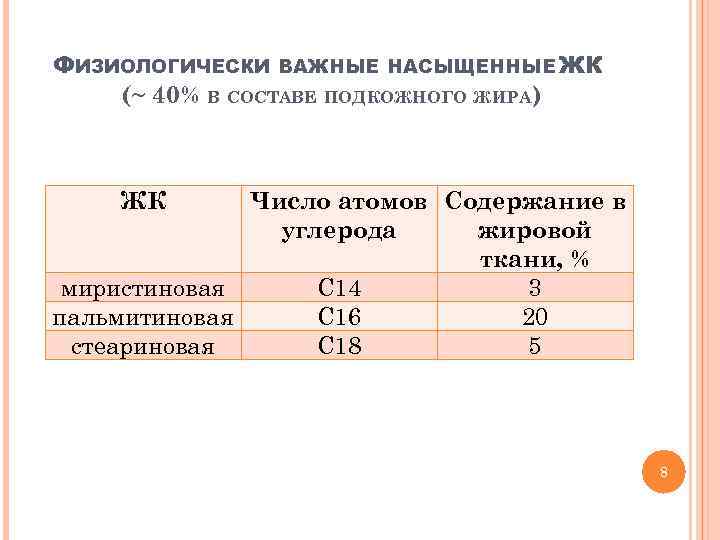
ФИЗИОЛОГИЧЕСКИ ВАЖНЫЕ НАСЫЩЕННЫЕ ЖК (~ 40% В СОСТАВЕ ПОДКОЖНОГО ЖИРА) ЖК Число атомов Содержание в углерода жировой ткани, % миристиновая С 14 3 пальмитиновая С 16 20 стеариновая С 18 5 8
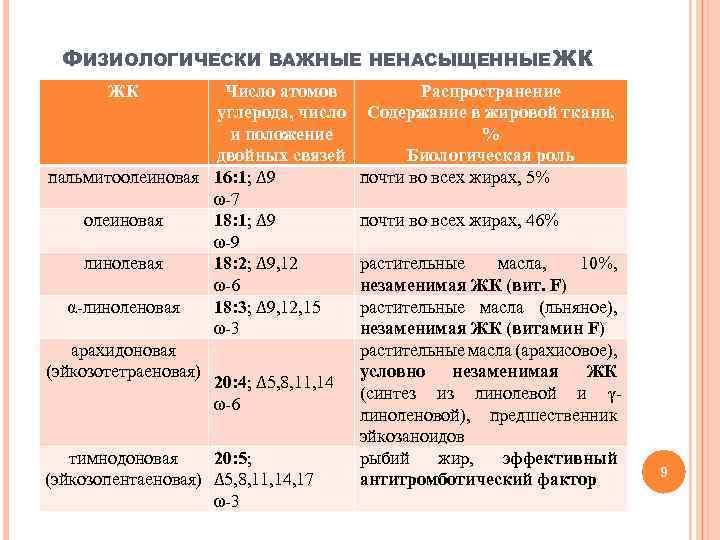
ФИЗИОЛОГИЧЕСКИ ВАЖНЫЕ НЕНАСЫЩЕННЫЕ ЖК ЖК Число атомов углерода, число и положение двойных связей пальмитоолеиновая 16: 1; ∆9 ω-7 олеиновая 18: 1; ∆9 ω-9 линолевая 18: 2; ∆9, 12 ω-6 α-линоленовая 18: 3; ∆9, 12, 15 ω-3 арахидоновая (эйкозотетраеновая) 20: 4; ∆5, 8, 11, 14 ω-6 тимнодоновая 20: 5; (эйкозопентаеновая) ∆5, 8, 11, 14, 17 ω-3 Распространение Содержание в жировой ткани, % Биологическая роль почти во всех жирах, 5% почти во всех жирах, 46% растительные масла, 10%, незаменимая ЖК (вит. F) растительные масла (льняное), незаменимая ЖК (витамин F) растительные масла (арахисовое), условно незаменимая ЖК (синтез из линолевой и γлиноленовой), предшественник эйкозаноидов рыбий жир, эффективный антитромботический фактор 9

КЛАССИФИКАЦИЯ ЛИПИДОВ КЛАССИФИКАЦИЯ БЛОРА Предшественники и производные липидов: ЖК, спирты, альдегиды ЖК, кетоновые тела, жирорастворимые витамины, стероидные гормоны v Простые липиды: ЖК + спирт → сложные эфиры Жиры (масла): ЖК + глицерол → ацилглицеролы v Воска: ЖК + высшие одноатомные спирты Сложные липиды: ЖК + спирт + другие группы → сложные эфиры v ü ü Фосфолипиды (ФЛ): ЖК + спирт + Р и другие компоненты: глицерофосфолипиды (спирт - глицерол); сфингофосфолипиды (спирт - сфингозин); ЖК + сфингозин → церамид v Гликолипиды: ЖК + сфингозин + углеводный компонент галактозилцерамид, глюкозилцерамид, ганглиозиды (сиаловая кислота) v Другие сложные липиды: сульфолипиды, аминолипиды, липопротеины 10
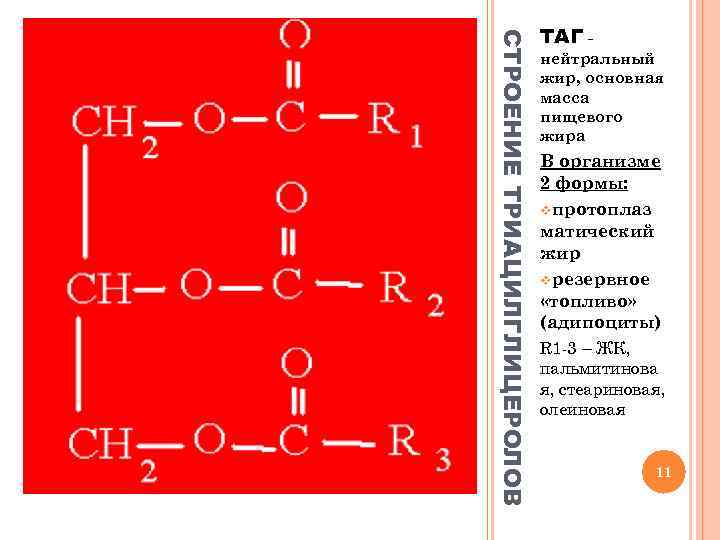
СТРОЕНИЕ ТРИАЦИЛГЛИЦЕРОЛОВ ТАГ - нейтральный жир, основная масса пищевого жира В организме 2 формы: vпротоплаз матический жир vрезервное «топливо» (адипоциты) R 1 -3 – ЖК, пальмитинова я, стеариновая, олеиновая 11
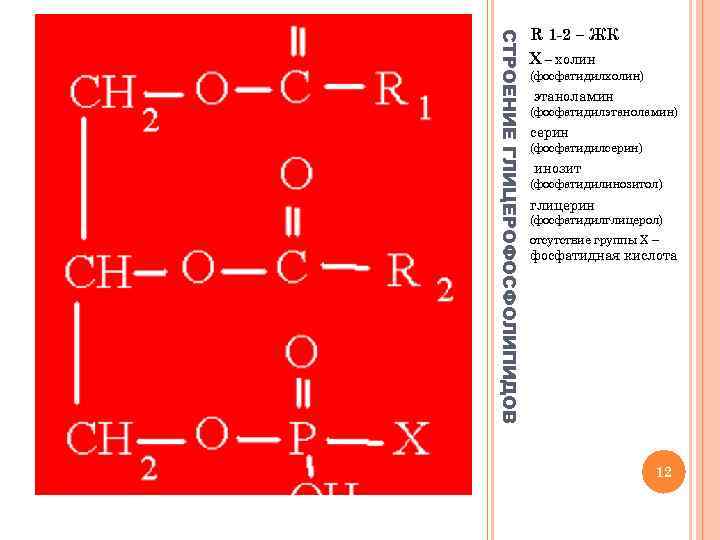
СТРОЕНИЕ ГЛИЦЕРОФОСФОЛИПИДОВ R 1 -2 – ЖК Х – холин (фосфатидилхолин) этаноламин (фосфатидилэтаноламин) серин (фосфатидилсерин) инозит (фосфатидилинозитол) глицерин (фосфатидилглицерол) отсутствие группы Х – фосфатидная кислота 12

БИОЛОГИЧЕСКАЯ ОСНОВНЫЕ Ø РОЛЬ ЛИПИДОВ ФУНКЦИИ И ПРИМЕРЫ Энергетическая (1 г жира – 9, 3 ккал = 38, 9 к. Дж) и запасная (ТАГ жировой ткани – депонированное «топливо» ) Ø Структурная (глицерофосфолипиды, гликолипиды, холестерол - компоненты биомембран) Ø Пластическая (холестерол используется для синтеза желчных кислот, стероидных гормонов, витамина Д 3; дигидронафтохинон, или восстановленный витамин К – кофактор глутамилкарбоксилазы) Ø Теплоизоляционная (подкожная жировая клетчатка) Ø Механическая защита (висцеральный жир) Ø Электроизоляционная (неполярные липиды обеспечивают распространение волн деполяризации вдоль миелинизированных нервных волокон) Ø Транспортная (переносчики жирорастворимых витаминов) Ø Регуляторная (передача гормонального сигнала в клетку) 13

АССИМИЛЯЦИЯ ПИЩЕВОГО ЖИРА (УСВОЕНИЕ) 14 ПЕРЕВАРИВАНИЕ ВСАСЫВАНИЕ ТРАНСПОРТ

ЭТАП 1. ЭМУЛЬГИРОВАНИЕ ПИЩЕВОГО ЖИРА Эмульгирование – образование мелких капелек жира (до 0, 5 мкм) из больших липидных капель с участием амфифильных соединений (желчных кислот, конъюгированных с глицином или таурином) в 12 -перстной кишке. Значение процесса: создание условий для эффективного переваривания: увеличение поверхности контакта гидролаз с молекулами жира. Механизм процесса: гидрофобная часть амфифильных соединений погружается в липидную каплю, а полярные группы, имеющие отрицательный заряд, отталкиваются, разрывая ее и стабилизируя (обратное слипание невозможно). 15
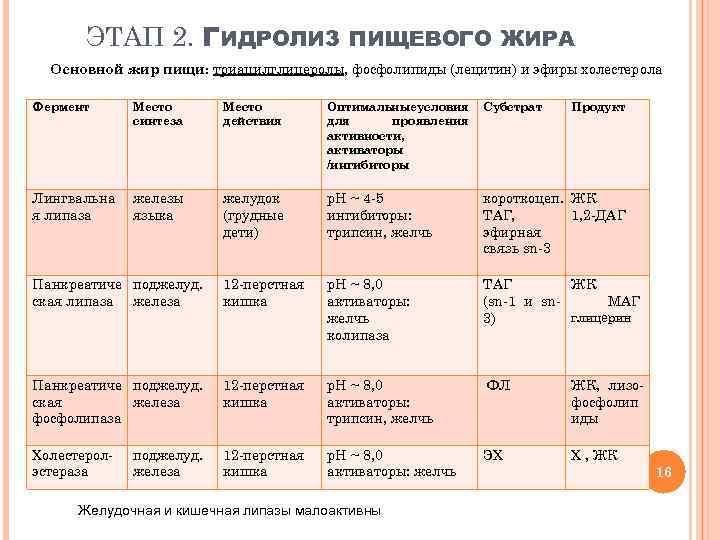
ЭТАП 2. ГИДРОЛИЗ ПИЩЕВОГО ЖИРА Основной жир пищи: триацилглицеролы, фосфолипиды (лецитин) и эфиры холестерола Фермент Место синтеза Место действия Оптимальныеусловия для проявления активности, активаторы /ингибиторы Субстрат Лингвальна я липаза железы языка желудок (грудные дети) р. Н ~ 4 -5 ингибиторы: трипсин, желчь короткоцеп. ЖК ТАГ, 1, 2 -ДАГ эфирная связь sn-3 Панкреатиче поджелуд. ская липаза железа 12 -перстная кишка р. Н ~ 8, 0 активаторы: желчь колипаза ТАГ ЖК (sn-1 и sn. МАГ глицерин 3) Панкреатиче поджелуд. ская железа фосфолипаза 12 -перстная кишка р. Н ~ 8, 0 активаторы: трипсин, желчь ФЛ ЖК, лизофосфолип иды Холестеролэстераза 12 -перстная кишка р. Н ~ 8, 0 активаторы: желчь ЭХ Х , ЖК поджелуд. железа Желудочная и кишечная липазы малоактивны Продукт 16
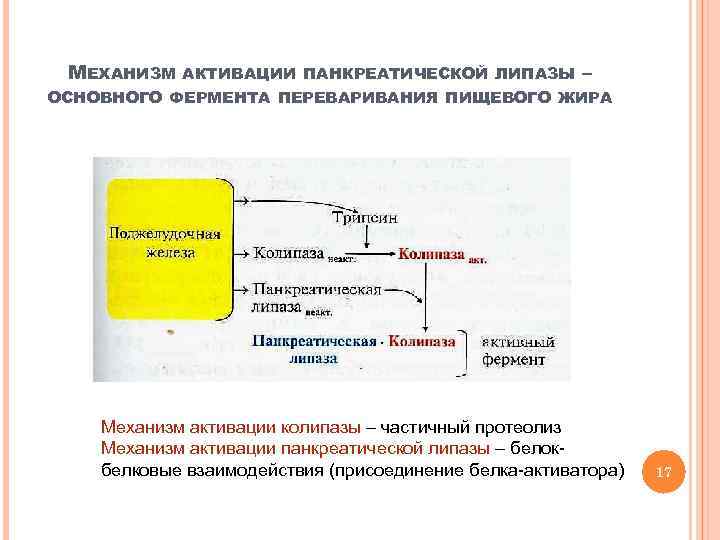
МЕХАНИЗМ АКТИВАЦИИ ПАНКРЕАТИЧЕСКОЙ ЛИПАЗЫ – ОСНОВНОГО ФЕРМЕНТА ПЕРЕВАРИВАНИЯ ПИЩЕВОГО ЖИРА Механизм активации колипазы – частичный протеолиз Механизм активации панкреатической липазы – белокбелковые взаимодействия (присоединение белка-активатора) 17

ГИДРОЛИЗ ТАГ q Основной путь – неполный гидролиз ( ~ 72% ТАГ): ТАГ + 2 Н 2 О → 2 -МАГ + 2 ЖК (панкреатическая липаза) q Дополнительный путь – полный гидролиз (~ 22% ТАГ): 2 -МАГ → 1 -МАГ (панкреатическая изомераза) 1 -МАГ + Н 2 О → ЖК + глицерин (панкреатическая липаза) 18

ЭТАП 3. ОБРАЗОВАНИЕ И ВСАСЫВАНИЕ СМЕШАННЫХ (МИЦЕЛЛ ВСАСЫВАНИЯ) МИЦЕЛЛ v ЖК (< 10 С) всасываются самостоятельно (жир молока) v Глицерин поступает в кровь или участвует в ресинтезе жира в энтероцитах v ЖК (> 10 С), 2 -МАГ, холестерол, лизофосфатидная кислота, жирорастворимые витамины всасываются в составе смешанных мицелл и участвует в ресинтезе жира в энтероцитах q. Мицеллы всасывания формируются самопроизвольно q. Ядро мицеллы гидрофобно, оболочка – гидрофильна (желчные кислоты) q. Механизм всасывания: пиноцитоз или диффузия q. Желчные кислоты (95%) после всасывания мицелл возвращаются в печень (энтерогепатическая циркуляция желчных кислот) 19
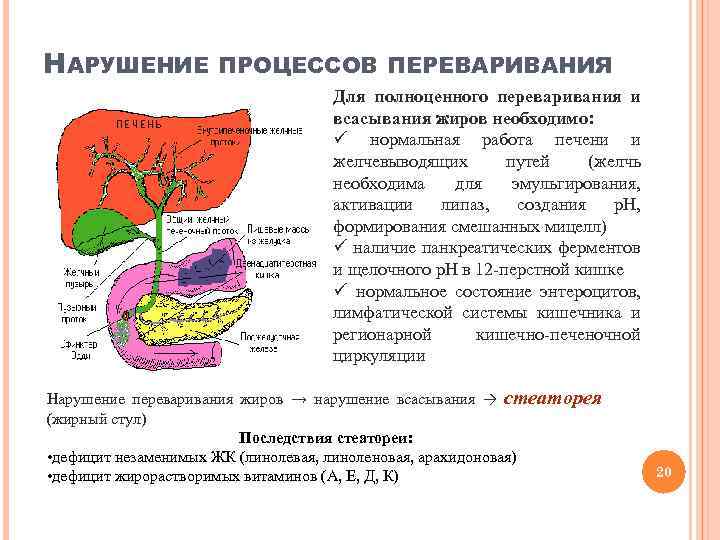
НАРУШЕНИЕ ПРОЦЕССОВ ПЕРЕВАРИВАНИЯ Для полноценного переваривания и всасывания жиров необходимо: ü нормальная работа печени и желчевыводящих путей (желчь необходима для эмульгирования, активации липаз, создания р. Н, формирования смешанных мицелл) ü наличие панкреатических ферментов и щелочного р. Н в 12 -перстной кишке ü нормальное состояние энтероцитов, лимфатической системы кишечника и регионарной кишечно-печеночной циркуляции Нарушение переваривания жиров → нарушение всасывания → стеаторея (жирный стул) Последствия стеатореи: • дефицит незаменимых ЖК (линолевая, линоленовая, арахидоновая) • дефицит жирорастворимых витаминов (А, Е, Д, К) 20

ЭТАП 4. РЕСИНТЕЗ ЖИРА В ЭНТЕРОЦИТАХ (ОБРАТНЫЙ СИНТЕЗ ЖИРА) Биологический смысл: синтезируются жиры, специфичные для человека и качественно отличающиеся от пищевого жира (жирные кислоты, их положение в молекуле ТАГ) Этапы: q образование активной формы ЖК – ацил-Ко. А: RCOOH + HS-Кo. A + АТФ → RCO~SKo. A (ацил-Ко. А) +АМФ + Н 4 Р 2 О 7 (РРI) фермент: ацил-Ко. А синтетаза (лигаза), HS-Кo. A – кофермент А (производное витамина В 5, пантотеновой кислоты) q ресинтез ТАГ, ФЛ, эфиров холестерина 21
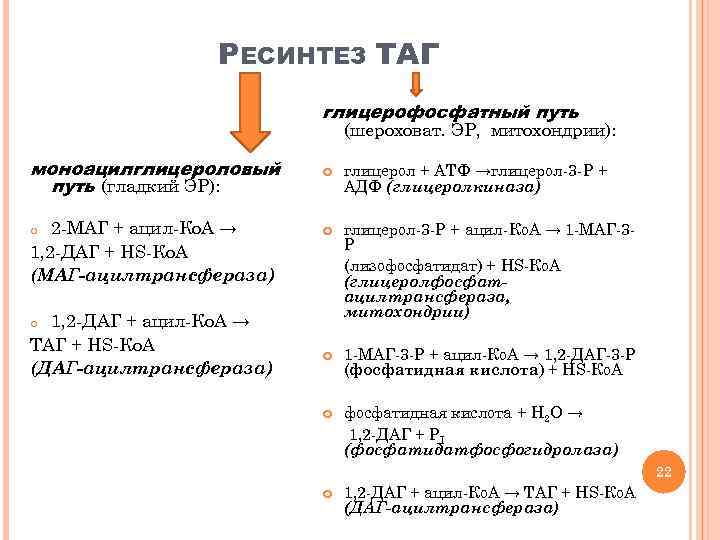
РЕСИНТЕЗ ТАГ глицерофосфатный путь (шероховат. ЭР, митохондрии): моноацилглицероловый путь (гладкий ЭР): глицерол + АТФ →глицерол-3 -Р + АДФ (глицеролкиназа) глицерол-3 -Р + ацил-Кo. A → 1 -МАГ-3 Р (лизофосфатидат) + HS-Кo. A (глицеролфосфатацилтрансфераза, митохондрии) 1 -МАГ-3 -Р + ацил-Кo. A → 1, 2 -ДАГ-3 -Р (фосфатидная кислота) + HS-Кo. A фосфатидная кислота + Н 2 О → 1, 2 -ДАГ + РI (фосфатидатфосфогидролаза) 2 -МАГ + ацил-Ко. А → 1, 2 -ДАГ + HS-Кo. A (МАГ-ацилтрансфераза) o 1, 2 -ДАГ + ацил-Ко. А → ТАГ + HS-Кo. A (ДАГ-ацилтрансфераза) o 22 1, 2 -ДАГ + ацил-Ко. А → ТАГ + HS-Кo. A (ДАГ-ацилтрансфераза)

РЕСИНТЕЗ ЭФИРОВ ХОЛЕСТЕРОЛА холестерол + ацил-Кo. A → ацилхолестерол + HS-Кo. A Фермент: ацил-холестеролацилтрансфераза (АХАТ) Ингибирование активности АХАТ снижает всасывание пищевого холестерина (лекарственные препараты для лечения атеросклероза) Ресинтез фосфолипидов (как и синтез в тканях): 1) с использованием 1, 2 -ДАГи присоединением активной (фосфорилированной) формы холина и этаноламина 2) через образование фосфатидной кислоты (ресинтез фосфатидилинозитола) 23

ЭТАП 5. ФОРМИРОВАНИЕ ХИЛОМИКРОНОВ ( М) И ИХ Х ТРАНСПОРТ ЧЕРЕЗ ЛИМФУ В КРОВЬ Молекулы ресинтезированного жира гидрофобны или амфифильны, поэтому в кровотоке нуждаются в переносчике ХМ – транспортная форма экзогенного жира ХМ – липопротеиновые частицы (100 – 1000 нм, плотность менее 1) Состав: 85% ТАГ, 5% Х и ЭХ, 3% ФЛ, 2% белка (интегральный апо. В-48, поверхностный апо. А-I) Транспорт экзогенного жира из кишечника в кровоток осуществляется по лимфатическим путям, а не через систему воротной вены из-за крупных размеров ХМ 24

ЭТАП 6. МЕТАБОЛИЗМ ХМ: «СОЗРЕВАНИЕ» (ОБМЕН АПОЛИПОПРОТЕИНАМИ С ЛПВП) апо. С-II – активатор липопротеиновой липазы (ЛП-липазы) апо. Е – лиганд к В, Е-рецептору клеточной мембраны гепатоцитов 25
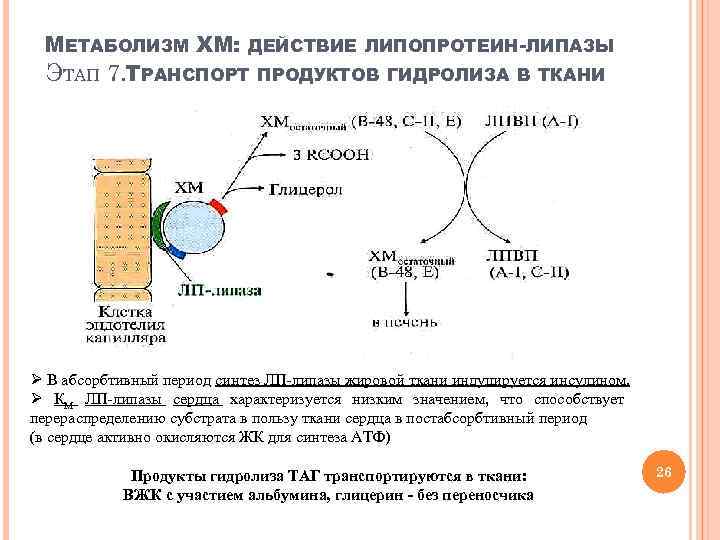
МЕТАБОЛИЗМ ХМ: ДЕЙСТВИЕ ЛИПОПРОТЕИН-ЛИПАЗЫ ЭТАП 7. ТРАНСПОРТ ПРОДУКТОВ ГИДРОЛИЗА В ТКАНИ Ø В абсорбтивный период синтез ЛП-липазы жировой ткани индуцируется инсулином. Ø КМ ЛП-липазы сердца характеризуется низким значением, что способствует перераспределению субстрата в пользу ткани сердца в постабсорбтивный период (в сердце активно окисляются ЖК для синтеза АТФ) Продукты гидролиза ТАГ транспортируются в ткани: ВЖК с участием альбумина, глицерин - без переносчика 26
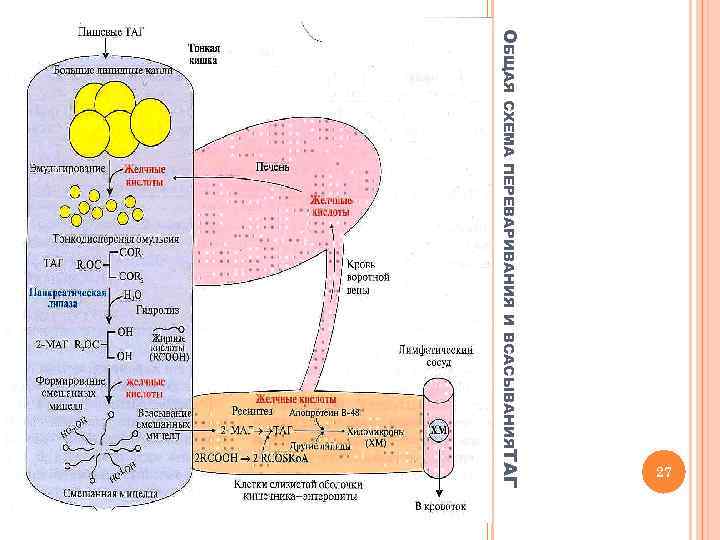
ОБЩАЯ СХЕМА ПЕРЕВАРИВАНИЯ И ВСАСЫВАНИЯТАГ 27

ЛИПОПРОТЕИНЫ ПЛАЗМЫ КРОВИ 28 СТРУКТУРА КЛАССИФИКАЦИЯ МЕТАБОЛИЗМ БИОЛОГИЧЕСКАЯ РОЛЬ
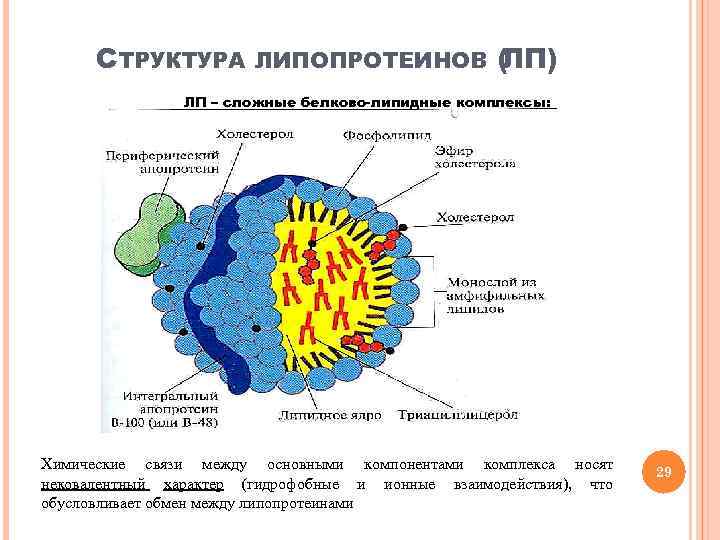
СТРУКТУРА ЛИПОПРОТЕИНОВ ( ЛП) ЛП – сложные белково-липидные комплексы: Химические связи между основными компонентами комплекса носят нековалентный характер (гидрофобные и ионные взаимодействия), что обусловливает обмен между липопротеинами 29
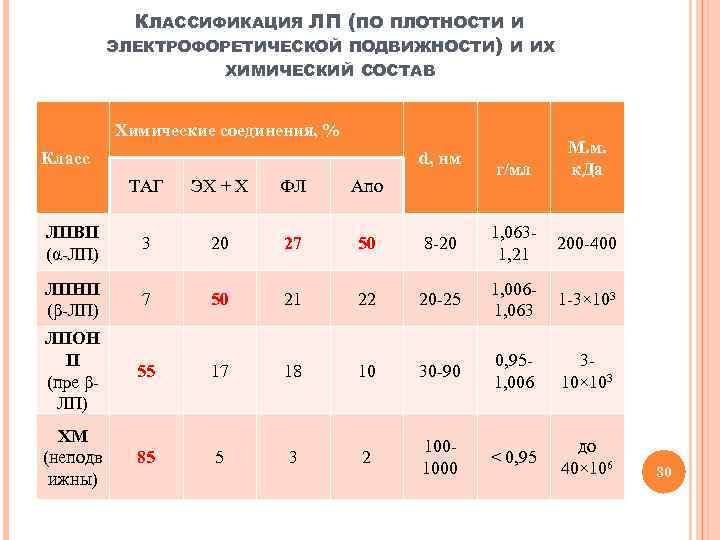
КЛАССИФИКАЦИЯ ЛП (ПО ПЛОТНОСТИ И ЭЛЕКТРОФОРЕТИЧЕСКОЙ ПОДВИЖНОСТИ) И ИХ ХИМИЧЕСКИЙ СОСТАВ Химические соединения, % Класс d, нм г/мл М. м. к. Да ТАГ ЭХ + Х ФЛ Апо ЛПВП (α-ЛП) 3 20 27 50 8 -20 1, 0631, 21 200 -400 ЛПНП (β-ЛП) 7 50 21 22 20 -25 1, 0061, 063 1 -3× 103 ЛПОН П (пре βЛП) 55 17 18 10 30 -90 0, 951, 006 310× 103 ХМ (неподв ижны) 85 5 3 2 1001000 < 0, 95 до 40× 106 30

БИОЛОГИЧЕСКАЯ q Ø Ø q q РОЛЬ ЛП Транспорт липидов: ХМ (хиломикроны) – экзогенный жир ЛПОНП (липопротеины очень низкой плотности) – эндогенный жир, синтезированный в печени ЛПНП (липопротеины низкой плотности) – холестерин, синтезированный в печени, в ткани через В, Е-рецепторы ЛПВП (липопротеины высокой плотности) – холестерин из тканей и ЛПНП в печень ( «обратный» транспорт холестерина) при участии рецептора SR-BI и АТФ-связанных кассетных транспортеров семейства ABC Транспорт стероидных и тиреоидных гормонов, жирорастворимых витаминов, ксенобиотиков производственной и окружающей среды, лекарственных препаратов, генетического материала (работы последних лет!) Регуляция метаболических процессов (например, противовоспалительный эффект ЛПВП) 31
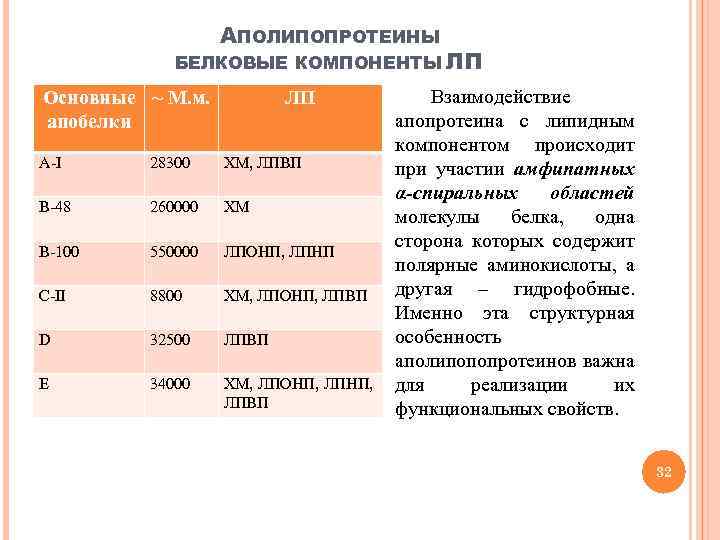
АПОЛИПОПРОТЕИНЫ БЕЛКОВЫЕ КОМПОНЕНТЫ ЛП Основные ~ М. м. апобелки ЛП А-I 28300 ХМ, ЛПВП B-48 260000 ХМ B-100 550000 ЛПОНП, ЛПНП С-II 8800 ХМ, ЛПОНП, ЛПВП D 32500 ЛПВП E 34000 ХМ, ЛПОНП, ЛПВП Взаимодействие апопротеина с липидным компонентом происходит при участии амфипатных α-спиральных областей молекулы белка, одна сторона которых содержит полярные аминокислоты, а другая – гидрофобные. Именно эта структурная особенность аполипопопротеинов важна для реализации их функциональных свойств. 32

ФУНКЦИИ АПОЛИПОПРОТЕИНОВ Ø структурообразующая: ü интегральные белки (апо. В-48, апо. В-100) ü периферические белки (апо. Е, апо. С, апо. А-I) Ø рецепторная (апо. Е-лиганд В, Е-рецептора, апо. А-I – лиганд ЛПВП-рецептора) Ø Ø Ø кофакторная (апо. С-II для ЛП-липазы, апо. А-I для ЛХАТ) транспортная (связывание лигандов различной химической природы) регуляторная (регуляторная роль ЛП обусловлена прежде всего белковым компонентом) 33
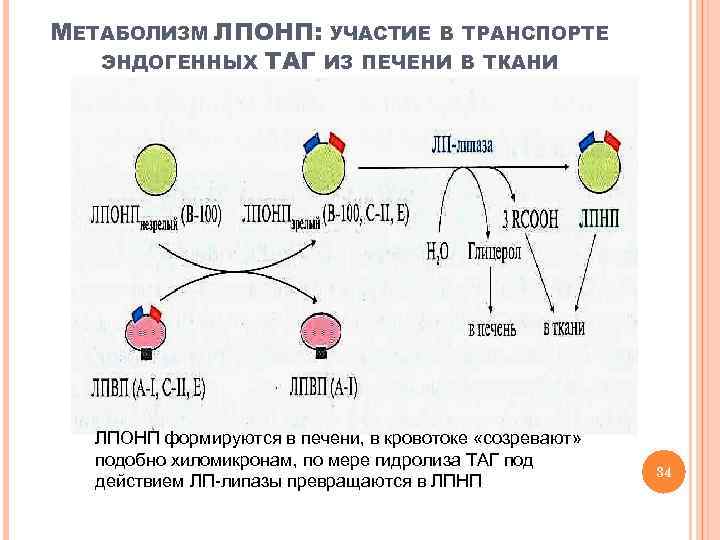
МЕТАБОЛИЗМ ЛПОНП: УЧАСТИЕ В ТРАНСПОРТЕ ЭНДОГЕННЫХ ТАГ ИЗ ПЕЧЕНИ В ТКАНИ ЛПОНП формируются в печени, в кровотоке «созревают» подобно хиломикронам, по мере гидролиза ТАГ под действием ЛП-липазы превращаются в ЛПНП 34

МЕТАБОЛИЗМ ЛПНП: УЧАСТИЕ В ТРАНСПОРТЕ ХОЛЕСТЕРИНА В КЛЕТКИ ТКАНЕЙ образуются главным образом в кровотоке из ЛПОНП, переносят холестерин захват клетками различных тканей осуществляется путем рецептор-опосредованного эндоцитоза (при участии В, Е-рецептора) деградация 50% ЛПНП происходит в печени период полужизни в крови составляет ≈ 2, 5 суток подвержены химическим модификациям (например, перекисное окисление липидов, гликозилирование аполипопротеинов), что лежит в основе патогенеза атеросклероза концентрация ЛПНП в крови прямо пропорциональна вероятности возникновения атеросклероза 35

МЕТАБОЛИЗМ ЛПВП Пояснения к схеме см. на следующем слайде 36

МЕТАБОЛИЗМ ЛПВП: УЧАСТИЕ В «ОБРАТНОМ» ТРАНСПОРТЕ ХОЛЕСТЕРИНА В ПЕЧЕНЬ 1. Образование предшественников ЛПВП (насцентных частиц в форме «шайбы» ) в печени 2. Обмен белками с ЛП других классов в кровотоке (в процессе «созревания» ХМ и ЛПОНП) 3. Формирование сферической частицы ЛПВП 3 в результате образования эфиров холестерола с участием фермента ЛХАТ 4. Формирование ЛПВП 2 в результате обмена липидами с ЛП других классов для восполнения недостатка лецитина 5. Катаболизм в печени 37

РОЛЬ ФЕРМЕНТА ЛХАТ В МЕТАБОЛИЗМЕ ЛПВП Основная роль ЛПВП: «обратный» транспорт холестерина из клеток и ЛПНП в печень. «Перекачка» холестерина осуществляется за счет образования эфиров холестерина при участии фермента ЛХАТ – лецитин: холестрол ацилтрансфераза Ø Лецитин + холестерол → ЭХ + лизолецитин (перенос остатка ЖК с лецитина в составе ЛПВП на холестерол с образованием эфира) Лецитин – фосфатидилхолин (вспомните структуру!) Источник холестерина – мембраны клеток и ЛПНП Активатор ЛХАТ: апо. А-I Эфиры холестерина формируют ядро ЛПВП, образуя сферическую частицу ЛПВП 3 38

ЛИПОГЕНЕЗ 39 Синтез высших жирных кислот (ВЖК) и триацилглицеридов (ТАГ)

СИНТЕЗ ТАГ В ТКАНЯХ Происходит в абсорбтивный период (после приема пищи, содержащей жиры и углеводы) Место синтеза: печень, жировая ткань Синтез ТАГ в печени активируется при употреблении алкоголя и при повышении ЖК в крови Субстраты: активные формы ВЖК (ацил-Ко. А) и глицерола (глицерол-3 -Р) Источник образования субстратов: Ø гидролиз пищевого жира, глюкоза пищи 2 этапа: 1) образование активных форм субстратов 2) присоединение ацильных остатков к глицерол-3 -Р ТАГ, синтезированные в жировой ткани, депонируются в адипоцитах ТАГ, синтезированные в печени, в составе ЛПОНП транспортируются в кровь 40
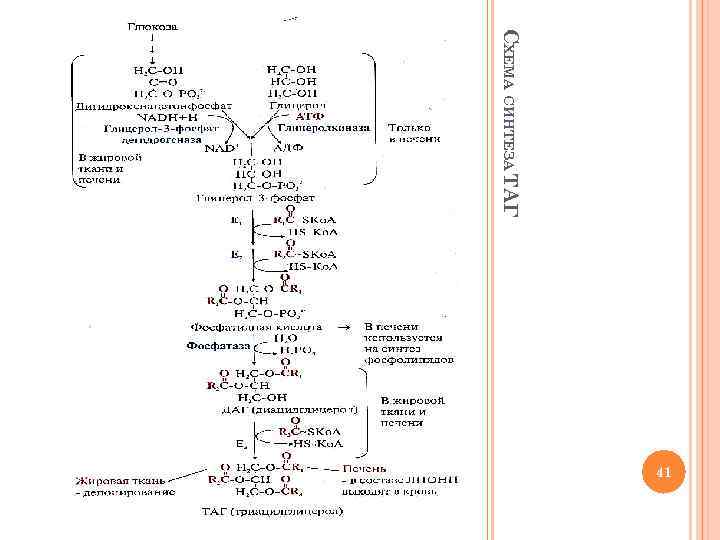
СХЕМА СИНТЕЗА ТАГ 41

СИНТЕЗ ЖК Значение: трансформация избытка углеводов пищи и аккумулирование их энергии в виде ТАГ Субстрат: ацетил-Ко. А, образующийся из пирувата в митохондриях при аэробном окислении глюкозы Продукт: пальмитиновая кислота (С 15 Н 31 СООН) Другие ВЖК синтезируются из пальмитиновой кислоты Кофакторы, косубстраты: NADPH (ПФП окисления глюкозы, реакция малик-фермента), АТФ (гликолиз), СО 2 (общий путь катаболизма) Основное место синтеза: печень (ЭР гепатоцитов) Ацетил-Ко. А идет на построение С 2 и С 16 Малонил-Ко. А (образуется из ацетил-Ко. А) – источник образования остальных атомов углерода в пальмитиновой кислоте (необходимо 7 молекул малонил-Ко. А) 42

ОСНОВНЫЕ ЭТАПЫ СИНТЕЗАЖК перенос ацетильных групп из митохондрий в цитозоль в составе цитрата Ø Митохондрии: ацетил-Ко. А + ЩУК + Н 2 О → цитрат + НS-Ко. А (цитратсинтаза) Цитозоль: цитрат + НS-Ко. А + АТФ → ацетил-Ко. А + ЩУК + АДФ + Рi (цитратлиаза) образование малонил-Ко. А Ø ацетил-Ко. А + СО 2 + АТФ → малонил-Ко. А + АДФ + Рi (ацетил-Ко. А карбоксилаза, кофермент биотин, витамин Н) удлинение углеродной цепи (пальмитоилсинтаза) 43

Использование ЩУК в цитоплазме: дополнительный источник образования NADPH ЩУК + NADН+Н+ → малат + NAD+ фермент: NAD-малатдегидрогеназа Малат + NADP+ → пируват + NADPH + Н+ + СО 2 фермент: NADP-малатдегидрогеназа, или малик-фермент 44

УДЛИНЕНИЕ УГЛЕРОДНОЙ ЦЕПИ Мультиферментный комплекс пальмитоилсинтаза Структура комплекса: димер, состоящий из 2 -х идентичных полипептидных мономеров Синтазный комплекс активен только в виде димера Комплекс одновременно синтезирует 2 молекулы ВЖК Реакции восстановления с участием NADPН обеспечивают образование насыщенного алифатического радикала 45

СТРУКТУРА МОНОМЕРОВ ПАЛЬМИТОИЛСИНТАЗНОГО КОМПЛЕКСА Ø Ø 7 доменов ацилпереносящий белок (АПБ), содержащий витамин В 5 - пантотеновую кислоту в виде 4´-фосфопантетеина 6 ферментов: трансацилаза, кетоацил-синтаза, кетоацил-редуктаза, гидратаза, еноил-редуктаза, тиоэстераза активные центры каждого мономера содержат 2 SHгруппы: SH-группа 4´-фосфопантетеина АПБ Ø SH-группа цистеина кетоацил-синтазы мономеры расположены по типу «голова к хвосту» : SHгруппа АПБ одного мономера расположена в непосредственной близости от SH-группа кетоацил-синтазы другого мономера Ø 46
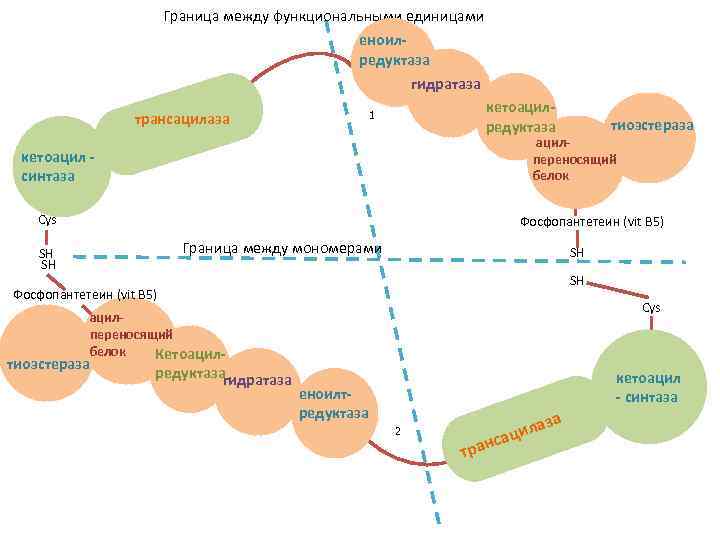
Граница между функциональными единицами еноил. Еноилтредуктаза гидратаза трансацилаза кетоацилредуктаза 1 тиоэстеpaзa ацилпереносящий белок кетоацил синтаза Cys Фосфопантетеин (vit B 5) Граница между мономерами SH SH Фосфопантетеин (vit B 5) Cys ацилпереносящий белок Кетоацил- тиоэстеpaзa редуктазагидратаза кетоацил - синтаза еноилтредуктаза 2 за тран ла аци с

ЭТАПЫ СИНТЕЗА ПАЛЬМИТИНОВОЙ КИСЛОТЫ Перенос ацетильного и малонильного остатков на активные центры пальмитоилсинтазы (реакции 1, 2) (трансацилаза) Декарбоксилирование малонила и присоединение ацетила (реакция 3) (кетоацил синтаза) Восстановление с участием NADPH (кетоацил редуктаза) Дегидратация (гидратаза) Восстановление с участием NADPH с образованием бутирила (еноил редуктаза) Повторение реакций 7 раз Отщепление пальмитиновой кислоты от комплекса (тиоэстераза) Схему реакций см. на след. слайде 48
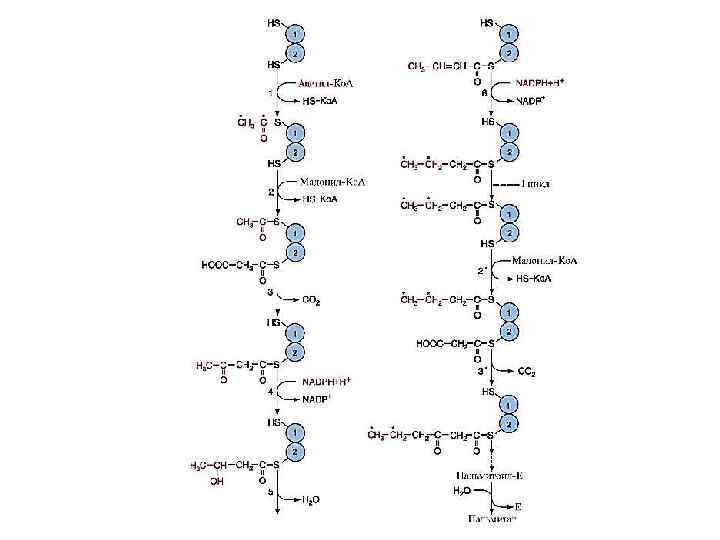

СУММАРНОЕ УРАВНЕНИЕ СИНТЕЗА ПАЛЬМИТИНОВОЙ КИСЛОТЫ ацетил-Ко. А + 7 малонил-Ко. А + 14 (NADPН + Н+ ) → С 15 Н 31 СООН + 7 СО 2 + 8 HS-Кo. A + 14 NADP+ + 7 Н 2 О Дальнейшее удлинение углеродной цепи ЖК происходит при участии элонгаз Образование ненасыщенных ВЖК происходит 50

РЕГУЛЯЦИЯ ЛИПОГЕНЕЗА Синтез ВЖК и ТАГ происходит в абсорбтивный период и регулируется инсулином Механизм регуляции: индукция синтеза ключевых ферментов: Ø липогенеза (цитратлиаза, ацетил-Ко. А карбоксилаза, пальмитоилсинтаза) Ø гликолиза (глюкокиназа, фосфофруктокиназа, пируваткиназа) Ø NADPН-генерирующих систем (глюкозо-6 -фосфат дегидрогеназа) активация ферментов (фосфофруктокиназы, пируваткиназы, ПДК, ацетил-Ко. А-карбоксилазы) путем дефосфорилирования с участием фосфопротеинфосфатазы стимулирование встраивания белков-переносчиков глюкозы51 (ГЛЮТ-4) в ЦПМ клеток жировой ткани

АЛЛОСТЕРИЧЕСКАЯ РЕГУЛЯЦИЯ ЛИПОГЕНЕЗА При избыточном содержании легкоусвояемых углеводов и активации гликолиза, реакций ОПК энергетический статус клеток характеризуется: ↑ NADН / NAD+ и ↑ АТФ/АДФ NADН и АТФ – аллостерические ингибиторы регуляторных ферментов цикла Кребса Самую медленную реакцию цикла Кребса катализирует изоцитратдегидрогеназа, поэтому при ↑ NADН и АТФ в наибольшей степени снижается активность данного фермента, что приводит к накоплению цитрата и образованию из него ацетил. Ко. А в цитоплазме 52

РЕГУЛЯЦИЯ АКТИВНОСТИ АЦЕТИЛ- ОА К КАРБОКСИЛАЗЫ Ø Способы регуляции индукция синтеза (инсулин) Ø ассоциация /диссоциация протомеров активатор (ассоциация): цитрат ингибитор (диссоциация): пальмитоил-Ко. А Ø фосфорилирование (адреналин, глюкагон) / дефосфорилирование (инсулин) 53

«ТОЧКИ СОПРИКОСНОВЕНИЯ» ЛИПОГЕНЕЗА И ОБМЕНА ГЛЮКОЗЫ Гликолиз – источник АТФ для реакций синтеза ВЖК и ТАГ (цитратлиазная, ацетил-Ко. А карбоксилазная, ацил-Ко. А синтетазная) Гликолиз – источник диацилглицеролфосфата для образования глицерол-3 -фосфата и синтеза ТАГ ПФП окисления глюкозы – источник NADPН ОПК – источник образования ацетил-Ко. А и СО 2 54

АБСОРБТИВНЫЙ ПЕРИОД После приема пищи, содержащей липиды и углеводы в крови повышается v. Уровень хиломикронов v. Концентрация глюкозы (7 -8 ммоль/л) v. Инсулино-глюкагоновый индекс Создаются условия для липогенеза Избыточное потребление углеводов активирует липогенез и приводит к ожирению. Норма потребления углеводов: 5 г/кг идеального веса 55

ЗАКЛЮЧЕНИЕ Ассимиляция – многоэтапный процесс усвоения пищевых жиров от переваривания до транспорта в ткани Липопротеины плазмы крови – транспортная форма липидов в плазме крови Липогенез (синтез ВЖК и ТАГ) в организме протекает в абсорбтивный период, тесно связан с обменом глюкозы и регулируется инсулином. Синтез жирных кислот и ТАГ – источник образования в организме «резервного» топлива 56

ЛИТЕРАТУРА 1. 2. Березов Т. Т. Биологическая химия: учебник для студентов медицинских вузов [Рекомендовано отраслевым министерством] / Т. Т. Березов, Б. Ф. Коровкин. -3 -е изд. , перераб. и доп. -М. : Медицина, 2004. -704 с. (глава 6, глава 11 С. 363 -373, 381 -395) Биохимия: учебник для студентов медицинских вузов [Рекомендовано отраслевым министерством] / Е. С. Северин -М. : ГЭОТАРМедиа, 2007. -784 с. (раздел 8 выборочно в соответствии с рассматриваемыми вопросами) 57