ХАООС Лекции 6-7.ppt
- Количество слайдов: 24
 Лекции № 6 -7 Анализ компонентов и параметров гидросферы План 1. 2. 3. 4. 5. Общие сведения о воде Требования, предъявляемые к воде Показатели контроля качества воды и их определение Анализ воды Тяжёлые металлы как токсиканты в природных водах
Лекции № 6 -7 Анализ компонентов и параметров гидросферы План 1. 2. 3. 4. 5. Общие сведения о воде Требования, предъявляемые к воде Показатели контроля качества воды и их определение Анализ воды Тяжёлые металлы как токсиканты в природных водах
 Общие сведения о воде Дождь
Общие сведения о воде Дождь
 Подземная река
Подземная река
 Горная река Озеро
Горная река Озеро
 Карибское море Атлантический океан
Карибское море Атлантический океан
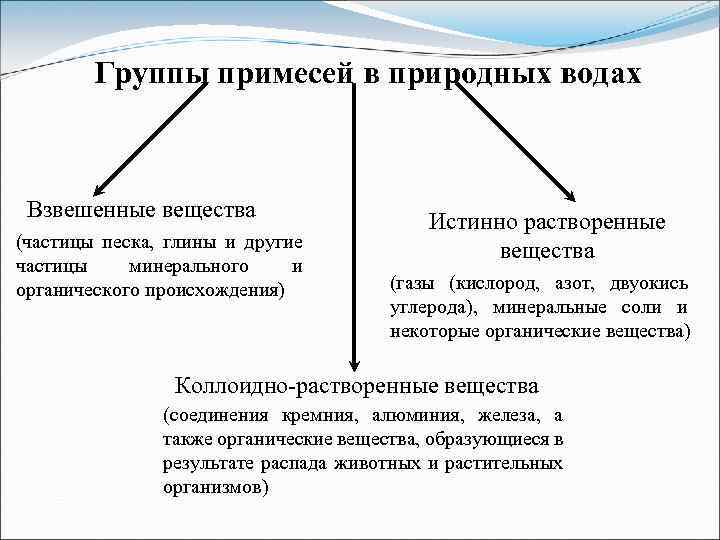 Группы примесей в природных водах Взвешенные вещества (частицы песка, глины и другие частицы минерального и органического происхождения) Истинно растворенные вещества (газы (кислород, азот, двуокись углерода), минеральные соли и некоторые органические вещества) Коллоидно-растворенные вещества (соединения кремния, алюминия, железа, а также органические вещества, образующиеся в результате распада животных и растительных организмов)
Группы примесей в природных водах Взвешенные вещества (частицы песка, глины и другие частицы минерального и органического происхождения) Истинно растворенные вещества (газы (кислород, азот, двуокись углерода), минеральные соли и некоторые органические вещества) Коллоидно-растворенные вещества (соединения кремния, алюминия, железа, а также органические вещества, образующиеся в результате распада животных и растительных организмов)
 Требования, предъявляемые к воде Нормы качества воды: а) запах и привкус при температуре 20° не более 2 баллов; б) содержание свинца не более 0, 1 мг/л; в) мышьяка не более 0, 05 мг/л; г) фтора не более 1, 5 мг/л; д) меди не более 3 мг/л; е) цинка не более 15 мг/л; ж) фенол-содержащих веществ в пересчете на фенол не более 0, 001 мг/л; з) взвешенных частиц не должно превышать 1, 5 мг/л; и) органических веществ должно быть не более 3 мг/л; к) р. Н 6, 5 - 9, 5; л) вода не должна содержать других ядовитых веществ; м) жёсткость воды не должна превышать 7, 0 ммоль/л; н) содержание хлора, вводимого для уничтожения микроорганизмов, не должно превышать 0, 5 мг/л.
Требования, предъявляемые к воде Нормы качества воды: а) запах и привкус при температуре 20° не более 2 баллов; б) содержание свинца не более 0, 1 мг/л; в) мышьяка не более 0, 05 мг/л; г) фтора не более 1, 5 мг/л; д) меди не более 3 мг/л; е) цинка не более 15 мг/л; ж) фенол-содержащих веществ в пересчете на фенол не более 0, 001 мг/л; з) взвешенных частиц не должно превышать 1, 5 мг/л; и) органических веществ должно быть не более 3 мг/л; к) р. Н 6, 5 - 9, 5; л) вода не должна содержать других ядовитых веществ; м) жёсткость воды не должна превышать 7, 0 ммоль/л; н) содержание хлора, вводимого для уничтожения микроорганизмов, не должно превышать 0, 5 мг/л.
 Промышленное применение воды Охладитель на ТЭЦ Рабочее тело в гидропрессах
Промышленное применение воды Охладитель на ТЭЦ Рабочее тело в гидропрессах
 Требования, предъявляемые к качеству промышленной воды Требования, предъявляемые к качеству воды, применяемой в промышленности, разнообразны и сводятся в основном к условию: примеси не должны препятствовать или вредить ее производственному использованию.
Требования, предъявляемые к качеству промышленной воды Требования, предъявляемые к качеству воды, применяемой в промышленности, разнообразны и сводятся в основном к условию: примеси не должны препятствовать или вредить ее производственному использованию.
 Показатели контроля качества воды и их определение 1. Температура. 2. Органолептические показатели: а) цветность; б) мутность; в) запах; г) вкус и привкус; д) пенистость. 3. Водородный показатель. 4. Окисляемость. 5. Щелочность и кислотность. 6. Содержание хлоридов и силикатов.
Показатели контроля качества воды и их определение 1. Температура. 2. Органолептические показатели: а) цветность; б) мутность; в) запах; г) вкус и привкус; д) пенистость. 3. Водородный показатель. 4. Окисляемость. 5. Щелочность и кислотность. 6. Содержание хлоридов и силикатов.
 Нарушения некоторых показателей качества воды Последствия теплового загрязнения: а) при повышенной температуре многие водные организмы, и в частности рыбы, находятся в состоянии стресса, что снижает их естественный иммунитет; б) происходит массовое размножение сине-зеленых водорослей; в) образуются тепловые барьеры на путях миграций рыбы; г) уменьшается видовое разнообразие.
Нарушения некоторых показателей качества воды Последствия теплового загрязнения: а) при повышенной температуре многие водные организмы, и в частности рыбы, находятся в состоянии стресса, что снижает их естественный иммунитет; б) происходит массовое размножение сине-зеленых водорослей; в) образуются тепловые барьеры на путях миграций рыбы; г) уменьшается видовое разнообразие.
 Цветная вода Мутная вода
Цветная вода Мутная вода
 Пенящаяся вода Пенистость – это способность воды сохранять искусственно созданную пену.
Пенящаяся вода Пенистость – это способность воды сохранять искусственно созданную пену.
 Основные органолептические показатели Цветность – естественное свойство природной воды, обусловленное присутствием гуминовых веществ и комплексных соединений железа. Различают следующие оттенки: cлабо-желтоватый, светложелтоватый, жёлтый, коричневый, красно-коричневый, другой (указать). Мутность воды – содержание взвешенных в воде мелкодисперсных примесей – нерастворимых или коллоидных частиц различного происхождения. Вкус – это свойство воды, обусловленное наличием в ней растворимых веществ, которые попадают в воду естественным путем либо со сточными водами. Различают 4 вкуса: соленый, кислый, горький, сладкий. Остальные вкусовые ощущения считаются привкусами: (солоноватый, горьковатый, металлический, хлорный и т. д. ).
Основные органолептические показатели Цветность – естественное свойство природной воды, обусловленное присутствием гуминовых веществ и комплексных соединений железа. Различают следующие оттенки: cлабо-желтоватый, светложелтоватый, жёлтый, коричневый, красно-коричневый, другой (указать). Мутность воды – содержание взвешенных в воде мелкодисперсных примесей – нерастворимых или коллоидных частиц различного происхождения. Вкус – это свойство воды, обусловленное наличием в ней растворимых веществ, которые попадают в воду естественным путем либо со сточными водами. Различают 4 вкуса: соленый, кислый, горький, сладкий. Остальные вкусовые ощущения считаются привкусами: (солоноватый, горьковатый, металлический, хлорный и т. д. ).
 Водородный показатель Для всего живого в воде минимально возможная величина р. Н=5, дождь, имеющий р. Н<5, 5, считается кислотным. В питьевой воде допускается р. Н= 6, 0 -9, 0, в воде водоемов хозяйственно-бытового и культурно-бытового водопользования – 6, 5 -8, 5. Запах – это свойство воды, обусловленное наличием в ней летучих пахнущих веществ, которые попадают в воду естественным путем либо со сточными водами. Практически все органические вещества имеют запах и передают его в воде. Количественно интенсивность запаха оценивают, определяя «пороговое число» запаха N – степень разбавления анализируемой воды водой, лишенной запаха (обрабатывают активированным углем (0, 6 г на 1 л), либо пропустив воду через бытовой фильтр для очистки воды). N = V 0/Va, где V 0 – суммарный объем воды (с запахом и без запаха); Va – объем анализируемой воды (с запахом), мл.
Водородный показатель Для всего живого в воде минимально возможная величина р. Н=5, дождь, имеющий р. Н<5, 5, считается кислотным. В питьевой воде допускается р. Н= 6, 0 -9, 0, в воде водоемов хозяйственно-бытового и культурно-бытового водопользования – 6, 5 -8, 5. Запах – это свойство воды, обусловленное наличием в ней летучих пахнущих веществ, которые попадают в воду естественным путем либо со сточными водами. Практически все органические вещества имеют запах и передают его в воде. Количественно интенсивность запаха оценивают, определяя «пороговое число» запаха N – степень разбавления анализируемой воды водой, лишенной запаха (обрабатывают активированным углем (0, 6 г на 1 л), либо пропустив воду через бытовой фильтр для очистки воды). N = V 0/Va, где V 0 – суммарный объем воды (с запахом и без запаха); Va – объем анализируемой воды (с запахом), мл.
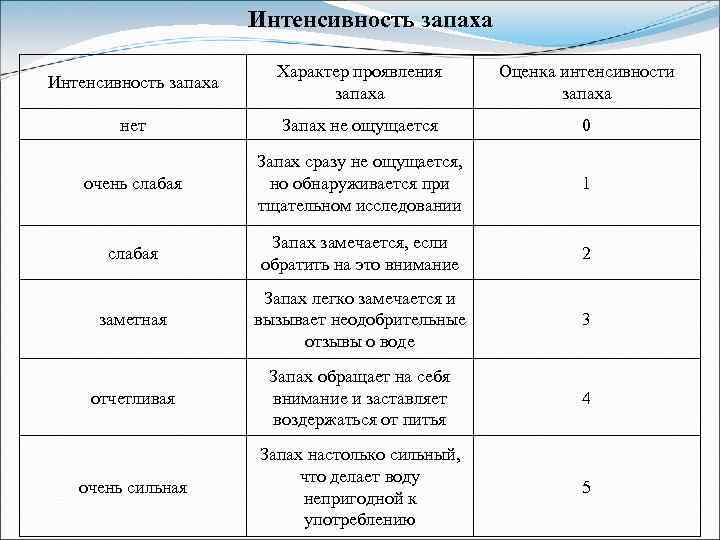 Интенсивность запаха Характер проявления запаха Оценка интенсивности запаха нет Запах не ощущается 0 очень слабая Запах сразу не ощущается, но обнаруживается при тщательном исследовании 1 слабая Запах замечается, если обратить на это внимание 2 заметная Запах легко замечается и вызывает неодобрительные отзывы о воде 3 отчетливая Запах обращает на себя внимание и заставляет воздержаться от питья 4 очень сильная Запах настолько сильный, что делает воду непригодной к употреблению 5
Интенсивность запаха Характер проявления запаха Оценка интенсивности запаха нет Запах не ощущается 0 очень слабая Запах сразу не ощущается, но обнаруживается при тщательном исследовании 1 слабая Запах замечается, если обратить на это внимание 2 заметная Запах легко замечается и вызывает неодобрительные отзывы о воде 3 отчетливая Запах обращает на себя внимание и заставляет воздержаться от питья 4 очень сильная Запах настолько сильный, что делает воду непригодной к употреблению 5
 Если анализируемая вода содержит какое-либо пахнущее вещество, то можно определить его концентрацию в пробе. Cx = C 0· (N 0/Nx), мг/л; С 0 – концентрация определяемого вещества в стандартном растворе, N 0 и Nx – «пороговое число» запаха стандартного раствора и пробы соответственно. Окисляемость Метод основан на обработке воды перманганатом калия в кислой среде: 2 КМn. O 4 + 3 H 2 SO 4 ↔ K 2 SO 4 + 2 Mn. SO 4 + 3 H 2 O + 5 O Количество кислорода, израсходованное на окисление органических соединений, определяют, восстанавливая избыток перманганата калия щавелевой кислотой: 2 KMn. O 4 + 5 H 2 C 2 O 4 ↔ 2 Mn. SO 4 + K 2 SO 4 + 8 H 2 O + 10 CO 2
Если анализируемая вода содержит какое-либо пахнущее вещество, то можно определить его концентрацию в пробе. Cx = C 0· (N 0/Nx), мг/л; С 0 – концентрация определяемого вещества в стандартном растворе, N 0 и Nx – «пороговое число» запаха стандартного раствора и пробы соответственно. Окисляемость Метод основан на обработке воды перманганатом калия в кислой среде: 2 КМn. O 4 + 3 H 2 SO 4 ↔ K 2 SO 4 + 2 Mn. SO 4 + 3 H 2 O + 5 O Количество кислорода, израсходованное на окисление органических соединений, определяют, восстанавливая избыток перманганата калия щавелевой кислотой: 2 KMn. O 4 + 5 H 2 C 2 O 4 ↔ 2 Mn. SO 4 + K 2 SO 4 + 8 H 2 O + 10 CO 2
 Щелочность и кислотность Щелочность – это свойство воды, обусловленное присутствием в ней веществ, содержащих гидроксо-анион, а также веществ, реагирующих с сильными (соляной, серной) кислотами. К таким соединениям относятся: - сильные щелочи (КОН, Na. OH) и летучие основания (например, NH 4 OH), а также анионы, обуславливающие высокую щелочность в результате гидролиза в водном растворе при р. Н>8, 4 (CO 32 -, S 2 -, PO 43 -, Si. O 32 - и др. ); - слабые основания и анионы летучих и нелетучих слабых кислот (НСО 3 -, Н 2 РО 4 -, НРО 42 -, СН 3 СОО-, HS-, анионы гуминовых кислот и др. ). Кислотность – это свойство воды, обусловленное содержанием в ней веществ, реагирующих с гидроксо-анионами. К таким соединениям относятся: - сильные кислоты: соляная (НСl), азотная (HNO 3), серная (H 2 SO 4); - слабые кислоты: уксусная (СН 3 СООН), сернистая (H 2 SO 3), угольная (H 2 CO 3), сероводородная (H 2 S); - катионы слабых оснований: аммоний (NH 4+); катионы органических аммонийных соединений.
Щелочность и кислотность Щелочность – это свойство воды, обусловленное присутствием в ней веществ, содержащих гидроксо-анион, а также веществ, реагирующих с сильными (соляной, серной) кислотами. К таким соединениям относятся: - сильные щелочи (КОН, Na. OH) и летучие основания (например, NH 4 OH), а также анионы, обуславливающие высокую щелочность в результате гидролиза в водном растворе при р. Н>8, 4 (CO 32 -, S 2 -, PO 43 -, Si. O 32 - и др. ); - слабые основания и анионы летучих и нелетучих слабых кислот (НСО 3 -, Н 2 РО 4 -, НРО 42 -, СН 3 СОО-, HS-, анионы гуминовых кислот и др. ). Кислотность – это свойство воды, обусловленное содержанием в ней веществ, реагирующих с гидроксо-анионами. К таким соединениям относятся: - сильные кислоты: соляная (НСl), азотная (HNO 3), серная (H 2 SO 4); - слабые кислоты: уксусная (СН 3 СООН), сернистая (H 2 SO 3), угольная (H 2 CO 3), сероводородная (H 2 S); - катионы слабых оснований: аммоний (NH 4+); катионы органических аммонийных соединений.
 Анализ воды В лаборатории анализа качества воды
Анализ воды В лаборатории анализа качества воды
 Общая жёсткость – это свойство природной воды, зависящее от суммарного содержания в ней растворенных солей кальция и магния. Общая жесткость подразделяется на карбонатную (временную), обусловленную концентрацией гидрокарбонатов (и карбонатов при р. Н 8, 3) кальция и магния, и некарбонатную (постоянную) – концентрацию в воде кальциевых и магниевых солей сильных кислот. Общая жесткость определяется методом комплексонометрического титрования по схеме: Me 2+ + H 2 Y 2 - = Me. Y 2 - + 2 H+; Me 3+ + H 2 Y 2 - = Me. Y- + 2 H+; Me 4+ + H 2 Y 2 - =Me. Y + 2 H+. Сухой остаток – это масса остатка, получаемого выпариванием профильтрованной пробы воды и высушиванием при 103 -105 0 С или 178 -182 0 С.
Общая жёсткость – это свойство природной воды, зависящее от суммарного содержания в ней растворенных солей кальция и магния. Общая жесткость подразделяется на карбонатную (временную), обусловленную концентрацией гидрокарбонатов (и карбонатов при р. Н 8, 3) кальция и магния, и некарбонатную (постоянную) – концентрацию в воде кальциевых и магниевых солей сильных кислот. Общая жесткость определяется методом комплексонометрического титрования по схеме: Me 2+ + H 2 Y 2 - = Me. Y 2 - + 2 H+; Me 3+ + H 2 Y 2 - = Me. Y- + 2 H+; Me 4+ + H 2 Y 2 - =Me. Y + 2 H+. Сухой остаток – это масса остатка, получаемого выпариванием профильтрованной пробы воды и высушиванием при 103 -105 0 С или 178 -182 0 С.
 Комплексон III – динатриевая соль этилендиаминтетрауксусной кислоты Na 2 H 2 Y - ЭДТА (торговое название – трилон Б). При взаимодействии этого комплексона с ионами металлов образуются внутрикомплексные соединения (хелаты). Комплексоны катионов металлов с трилоном Б, как правило, бесцветны и очень прочны, они могут образовываться даже, если первоначально ион-комплексообразователь связан в другой, менее прочный комплекс.
Комплексон III – динатриевая соль этилендиаминтетрауксусной кислоты Na 2 H 2 Y - ЭДТА (торговое название – трилон Б). При взаимодействии этого комплексона с ионами металлов образуются внутрикомплексные соединения (хелаты). Комплексоны катионов металлов с трилоном Б, как правило, бесцветны и очень прочны, они могут образовываться даже, если первоначально ион-комплексообразователь связан в другой, менее прочный комплекс.
 Тяжёлые металлы как токсиканты в природных водах Самый емкий аккумулятор соединений ртути (до 97%) – поверхностные воды океанов
Тяжёлые металлы как токсиканты в природных водах Самый емкий аккумулятор соединений ртути (до 97%) – поверхностные воды океанов
 Снег способен в значительной степени аккумулировать свинец. Фитопланктон хорошо удерживает свинец.
Снег способен в значительной степени аккумулировать свинец. Фитопланктон хорошо удерживает свинец.
 Адсорбция ионов кадмия донными Наименьшее содержание кадмия в осадками сильно зависит от кислотности океане зарегистрировано к востоку от среды. Японских островов (~ 0, 8 -9, 6 нг/л на глубине 8 -5500 м).
Адсорбция ионов кадмия донными Наименьшее содержание кадмия в осадками сильно зависит от кислотности океане зарегистрировано к востоку от среды. Японских островов (~ 0, 8 -9, 6 нг/л на глубине 8 -5500 м).


