Lektsii-ISKN-20-22-sterespets.pptx
- Количество слайдов: 32
 Лекции 16 -18 Иткулова Ш. С. Стереоспецифичность и стереоспецифический катализ
Лекции 16 -18 Иткулова Ш. С. Стереоспецифичность и стереоспецифический катализ
 Специфичность действия катализаторов Характерной особенностью катализаторов является их избирательность «специфичность» , т. е. способность действовать ускоряюще только на определенную реакцию или группу реакций. Это позволяет получать различные продукты из одних и тех же исходных веществ. Превращения этанола: 1) на Al 2 O 3 дегидратация с получением этилена 2) c H 3 PO 4 С 2 Н 5 ОН = С 2 Н 4 + Н 2 О получение диэтилового эфира 2 С 2 Н 5 ОН = С 2 Н 5 О С 2 Н 5 + Н 2 О 3) на Mg. O или Sn. O 2 дегидрогенизация с получением этаналя С 2 Н 5 ОН = СН 3 СНО +Н 2
Специфичность действия катализаторов Характерной особенностью катализаторов является их избирательность «специфичность» , т. е. способность действовать ускоряюще только на определенную реакцию или группу реакций. Это позволяет получать различные продукты из одних и тех же исходных веществ. Превращения этанола: 1) на Al 2 O 3 дегидратация с получением этилена 2) c H 3 PO 4 С 2 Н 5 ОН = С 2 Н 4 + Н 2 О получение диэтилового эфира 2 С 2 Н 5 ОН = С 2 Н 5 О С 2 Н 5 + Н 2 О 3) на Mg. O или Sn. O 2 дегидрогенизация с получением этаналя С 2 Н 5 ОН = СН 3 СНО +Н 2
 Изомерия Явление изомерии — когда два вещества имеют одну и ту же брутто-формулу (отражающую только количество разных атомов в веществе), но разные свойства — из-за разного порядка соединения атомов. Особенно богата изомерами органическая химия. К примеру, этиловый спирт и диметиловый эфир имеют одну и ту же брутто-формулу: C 3 H 6 O, но структурная формула спирта CH 3–CH 2–OH, а эфира — CH 3–O–CH 3 Эти вещества имеют разные свойства — как химические, так и физические (температура плавления, вязкость и т. д. ).
Изомерия Явление изомерии — когда два вещества имеют одну и ту же брутто-формулу (отражающую только количество разных атомов в веществе), но разные свойства — из-за разного порядка соединения атомов. Особенно богата изомерами органическая химия. К примеру, этиловый спирт и диметиловый эфир имеют одну и ту же брутто-формулу: C 3 H 6 O, но структурная формула спирта CH 3–CH 2–OH, а эфира — CH 3–O–CH 3 Эти вещества имеют разные свойства — как химические, так и физические (температура плавления, вязкость и т. д. ).
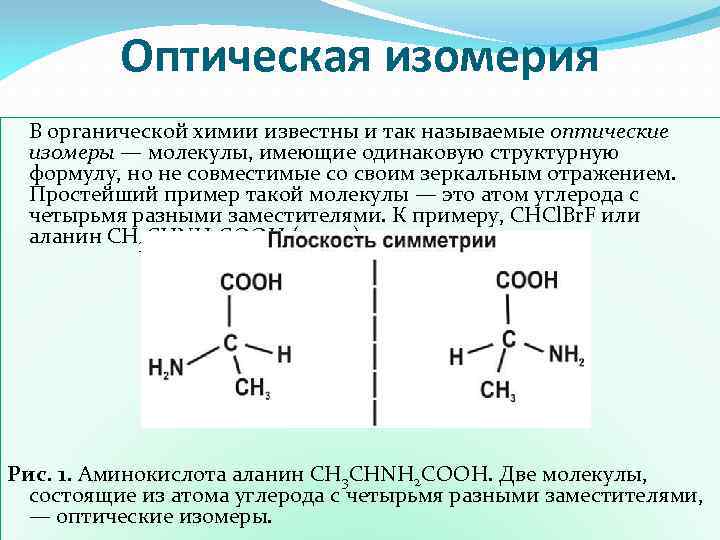 Оптическая изомерия В органической химии известны и так называемые оптические изомеры — молекулы, имеющие одинаковую структурную формулу, но не совместимые со своим зеркальным отражением. Простейший пример такой молекулы — это атом углерода с четырьмя разными заместителями. К примеру, СHCl. Br. F или аланин CH 3 CHNH 2 COOH (рис. 1). Рис. 1. Аминокислота аланин CH 3 CHNH 2 COOH. Две молекулы, состоящие из атома углерода с четырьмя разными заместителями, — оптические изомеры.
Оптическая изомерия В органической химии известны и так называемые оптические изомеры — молекулы, имеющие одинаковую структурную формулу, но не совместимые со своим зеркальным отражением. Простейший пример такой молекулы — это атом углерода с четырьмя разными заместителями. К примеру, СHCl. Br. F или аланин CH 3 CHNH 2 COOH (рис. 1). Рис. 1. Аминокислота аланин CH 3 CHNH 2 COOH. Две молекулы, состоящие из атома углерода с четырьмя разными заместителями, — оптические изомеры.
 Оптическая изомерия Наличие у такой молекулы двух разных конфигураций связано с тем, что у атома углерода, образующего четыре одинарные связи, эти связи направлены к вершинам тетраэдра. Живые существа используют только левовращающие изомеры аминокислот (на рисунке справа)
Оптическая изомерия Наличие у такой молекулы двух разных конфигураций связано с тем, что у атома углерода, образующего четыре одинарные связи, эти связи направлены к вершинам тетраэдра. Живые существа используют только левовращающие изомеры аминокислот (на рисунке справа)
 Опти ческая изомери я (энантиомерия) — разновидность пространственной изомерии, являющаяся прямым следствием хиральности молекул, проявляется способностью некоторых веществ поворачивать плоскость поляризованного луча в противоположные стороны. Оптическая изомерия свойственна молекулам органических веществ, не имеющим плоскости симметрии, которые относятся друг к другу как предмет к своему зеркальному отражению. Таким образом, оптическая активность – следствие пространственной изомерии (стереоизомерии) молекул.
Опти ческая изомери я (энантиомерия) — разновидность пространственной изомерии, являющаяся прямым следствием хиральности молекул, проявляется способностью некоторых веществ поворачивать плоскость поляризованного луча в противоположные стороны. Оптическая изомерия свойственна молекулам органических веществ, не имеющим плоскости симметрии, которые относятся друг к другу как предмет к своему зеркальному отражению. Таким образом, оптическая активность – следствие пространственной изомерии (стереоизомерии) молекул.
 Ассиметрический атом углерода Атом углерода, связанный с четырьмя различными заместителями, называется асимметрическим. Асимметрическими могут быть и атомы других элементов – кремния, азота, фосфора, серы. Однако оптически активными могут быть и соединения без асимметрических атомов углерода, если они могут существовать в виде двух зеркальных изомеров. Молекула будет асимметрической, если в ней нет ни одного элемента симметрии – ни центра, ни осей, ни плоскости симметрии. Примером может служить молекула аллена H 2 C=C=CH 2, в которой имеются два различных заместителя: R 1 R 2 C=C=CR 1 R 2. Эти заместители находятся не в одной плоскости (как, например, у алкенов), а в двух взаимно перпендикулярных плоскостях. Поэтому возможно существование двух зеркальных изомеров, которые никакими перемещениями и поворотами невозможно совместить друг с другом.
Ассиметрический атом углерода Атом углерода, связанный с четырьмя различными заместителями, называется асимметрическим. Асимметрическими могут быть и атомы других элементов – кремния, азота, фосфора, серы. Однако оптически активными могут быть и соединения без асимметрических атомов углерода, если они могут существовать в виде двух зеркальных изомеров. Молекула будет асимметрической, если в ней нет ни одного элемента симметрии – ни центра, ни осей, ни плоскости симметрии. Примером может служить молекула аллена H 2 C=C=CH 2, в которой имеются два различных заместителя: R 1 R 2 C=C=CR 1 R 2. Эти заместители находятся не в одной плоскости (как, например, у алкенов), а в двух взаимно перпендикулярных плоскостях. Поэтому возможно существование двух зеркальных изомеров, которые никакими перемещениями и поворотами невозможно совместить друг с другом.
 Ассиметрический атом углерода Более сложные отношения встречаются в случае молекул с несколькими асимметрическими атомами углерода. Например, в винной кислоте две гидроксильные группы у двух соседних атомов углерода могут быть расположены так, что молекула окажется симметричной и зеркальных изомеров у нее не будет. Это приводит к образованию еще одного, оптически неактивного, изомера, которых называется мезовинной (или антивинной) кислотой. Таким образом, дигидроксиянтарная кислота может находиться в виде четырех изомеров: правовращающего (D-винная кислота, которую в медицине называют виннокаменной), левовращающего (L-винная кислота), оптически неактивного (мезовинная кислота), а также в виде смеси L- и R-изомеров, то есть рацемата (i-винная, или виноградная кислота). Оптически активные винные кислоты при длительном нагревании их водных растворов рацемизуются, превращаясь в смесь антиподов.
Ассиметрический атом углерода Более сложные отношения встречаются в случае молекул с несколькими асимметрическими атомами углерода. Например, в винной кислоте две гидроксильные группы у двух соседних атомов углерода могут быть расположены так, что молекула окажется симметричной и зеркальных изомеров у нее не будет. Это приводит к образованию еще одного, оптически неактивного, изомера, которых называется мезовинной (или антивинной) кислотой. Таким образом, дигидроксиянтарная кислота может находиться в виде четырех изомеров: правовращающего (D-винная кислота, которую в медицине называют виннокаменной), левовращающего (L-винная кислота), оптически неактивного (мезовинная кислота), а также в виде смеси L- и R-изомеров, то есть рацемата (i-винная, или виноградная кислота). Оптически активные винные кислоты при длительном нагревании их водных растворов рацемизуются, превращаясь в смесь антиподов.
 Многоцентровые ассиметрические молекулы Еще сложнее обстоит дело, когда асимметрических центров у молекулы множество. Например, в молекуле глюкозы их четыре. Поэтому для нее теоретически возможно существование 16 стереоизомеров, которые образуют 8 пар зеркальных антиподов: это сама глюкоза, а также аллоза, альтроза, манноза, гулоза, идоза, галактоза и талоза. Многие из них встречаются в природе, например, D-глюкоза (но не L-глюкоза, которая была получена синтетически). Если в веществе поровну «правых» и «левых» молекул, оно будет оптически неактивным. Именно такие вещества и получаются в результате обычного химического синтеза. И только в живых организмах, при участии асимметричных агентов (например, ферментов) образуются оптически активные соединения.
Многоцентровые ассиметрические молекулы Еще сложнее обстоит дело, когда асимметрических центров у молекулы множество. Например, в молекуле глюкозы их четыре. Поэтому для нее теоретически возможно существование 16 стереоизомеров, которые образуют 8 пар зеркальных антиподов: это сама глюкоза, а также аллоза, альтроза, манноза, гулоза, идоза, галактоза и талоза. Многие из них встречаются в природе, например, D-глюкоза (но не L-глюкоза, которая была получена синтетически). Если в веществе поровну «правых» и «левых» молекул, оно будет оптически неактивным. Именно такие вещества и получаются в результате обычного химического синтеза. И только в живых организмах, при участии асимметричных агентов (например, ферментов) образуются оптически активные соединения.
 Хиральность Атом углерода с четырьмя разными заместителями называется хиральным атомом (от греческого heiros «ладонь» — тот же корень, что и в слове «хиромантия» ). Чем больше хиральных атомов в молекуле, тем больше у вещества может быть оптических изомеров. Интересно, что возможны органические вещества, которые имеют оптические изомеры, хотя в них формально нет ни одного хирального атома — центра изомерии.
Хиральность Атом углерода с четырьмя разными заместителями называется хиральным атомом (от греческого heiros «ладонь» — тот же корень, что и в слове «хиромантия» ). Чем больше хиральных атомов в молекуле, тем больше у вещества может быть оптических изомеров. Интересно, что возможны органические вещества, которые имеют оптические изомеры, хотя в них формально нет ни одного хирального атома — центра изомерии.
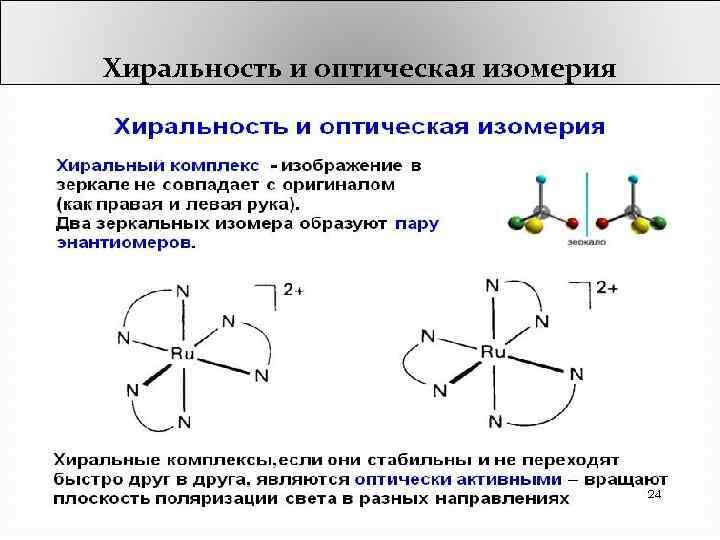 Хиральность и оптическая изомерия
Хиральность и оптическая изомерия
 ОПТИЧЕСКИЕ ИЗОМЕРЫ (энантиомеры) ОПТИЧЕСКИЕ ИЗОМЕРЫ(энантиомеры, оптические антиподы) - изомеры молекул, содержащих хиральный центр симметрии (напр. , асимметричный атом углерода, относительно которого атомы могут располагаться двумя зеркально противоположными способами). Такие молекулы называются хиральными. * энантиомеры - от греч. enantios – противоположный. Физ. и хим. свойства оптических изомеров одинаковы, различие проявляется только при их взаимодействии с плоскополяризованным светом или с другими хиральными молекулами. Так, о. и. вращают плоскость поляризации в противоположные стороны. Один из о. и. молекулы считают правым (D-dexter), другой левым (L –laevus), названия предложены Пастером.
ОПТИЧЕСКИЕ ИЗОМЕРЫ (энантиомеры) ОПТИЧЕСКИЕ ИЗОМЕРЫ(энантиомеры, оптические антиподы) - изомеры молекул, содержащих хиральный центр симметрии (напр. , асимметричный атом углерода, относительно которого атомы могут располагаться двумя зеркально противоположными способами). Такие молекулы называются хиральными. * энантиомеры - от греч. enantios – противоположный. Физ. и хим. свойства оптических изомеров одинаковы, различие проявляется только при их взаимодействии с плоскополяризованным светом или с другими хиральными молекулами. Так, о. и. вращают плоскость поляризации в противоположные стороны. Один из о. и. молекулы считают правым (D-dexter), другой левым (L –laevus), названия предложены Пастером.
 Рацематы Правые и левые оптические изомеры одной молекулы иногда, соединяясь друг с другом, образуют довольно прочные соединения- рацематы. Название получено от латинского racemus – виноград, два оптических изомера винной кислоты были открыты Пастером. Такие соединения (а также смеси D- и L –изомеров в равном отношении) оптически неактивны, другие физические свойства рацематов также отличны от свойств энантиомеров, из которых они образовались. В 1956 по предложению английских химиков Роберта Кана и Кристофера Ингольда и швейцарского химика Владимира Прелога для оптических изомеров были введены обозначения S (от лат. sinister – левый) и R (лат. rectus – правый); рацемат обозначают символом RS. Однако по традиции широко используются и старые обозначения (например, для углеводов, аминокислот). Следует отметить, что эти буквы указывают лишь на строение молекулы ( «правое» или «левое» расположение определенных химических групп) и не связаны с направлением оптического вращения; последнее обозначают знаками плюс и минус, например, D(–)-фруктоза, D(+)глюкоза.
Рацематы Правые и левые оптические изомеры одной молекулы иногда, соединяясь друг с другом, образуют довольно прочные соединения- рацематы. Название получено от латинского racemus – виноград, два оптических изомера винной кислоты были открыты Пастером. Такие соединения (а также смеси D- и L –изомеров в равном отношении) оптически неактивны, другие физические свойства рацематов также отличны от свойств энантиомеров, из которых они образовались. В 1956 по предложению английских химиков Роберта Кана и Кристофера Ингольда и швейцарского химика Владимира Прелога для оптических изомеров были введены обозначения S (от лат. sinister – левый) и R (лат. rectus – правый); рацемат обозначают символом RS. Однако по традиции широко используются и старые обозначения (например, для углеводов, аминокислот). Следует отметить, что эти буквы указывают лишь на строение молекулы ( «правое» или «левое» расположение определенных химических групп) и не связаны с направлением оптического вращения; последнее обозначают знаками плюс и минус, например, D(–)-фруктоза, D(+)глюкоза.
 Возникновение энантиомеров? Как же появились на Земле такие соединения? Как был осуществлен направленный синтез оптически активных веществ и разделение кристаллов на правые и левые? Например, та же природная правовращающая винная кислота, или «асимметричные» микроорганизмы, питающиеся только одним из энантиомеров? Никто не знает, почему почти все природные аминокислоты, из которых построены белки, относятся к L-ряду (S-конфигурация), а их антиподы только изредка встречаются у некоторых антибиотиков.
Возникновение энантиомеров? Как же появились на Земле такие соединения? Как был осуществлен направленный синтез оптически активных веществ и разделение кристаллов на правые и левые? Например, та же природная правовращающая винная кислота, или «асимметричные» микроорганизмы, питающиеся только одним из энантиомеров? Никто не знает, почему почти все природные аминокислоты, из которых построены белки, относятся к L-ряду (S-конфигурация), а их антиподы только изредка встречаются у некоторых антибиотиков.
 Оптическая изомерия и жизнь Химики часто относятся к энантиомерам, как к одному соединению, поскольку их химические свойства идентичны. Однако их биологическая активность может быть совершенно различной. Это стало очевидным после трагической истории с талидом – лекарственным средством, которое в 60 -е годы 20 в. врачи во многих странах прописывали беременными женщинами как эффективное снотворное и успокаивающее. Однако со временем проявилось его ужасное побочное действие: вещество оказалось тератогенным (повреждающим зародыш, от греческого teratos – чудовище, урод), и на свет появилась масса младенцев с врожденными уродствами. Лишь в конце 80 -х годов выяснилась, что причиной несчастий был только один из энантиомеров талидомида – его правовращающая форма. К сожалению, такое различие в действии лекарственных форм раньше не было известно, и талидомид был рацемической смесью обоих антиподов.
Оптическая изомерия и жизнь Химики часто относятся к энантиомерам, как к одному соединению, поскольку их химические свойства идентичны. Однако их биологическая активность может быть совершенно различной. Это стало очевидным после трагической истории с талидом – лекарственным средством, которое в 60 -е годы 20 в. врачи во многих странах прописывали беременными женщинами как эффективное снотворное и успокаивающее. Однако со временем проявилось его ужасное побочное действие: вещество оказалось тератогенным (повреждающим зародыш, от греческого teratos – чудовище, урод), и на свет появилась масса младенцев с врожденными уродствами. Лишь в конце 80 -х годов выяснилась, что причиной несчастий был только один из энантиомеров талидомида – его правовращающая форма. К сожалению, такое различие в действии лекарственных форм раньше не было известно, и талидомид был рацемической смесью обоих антиподов.
 Оптическая чистота энантиомеров Необходимость в оптически чистых энантиомерах объясняется тем, часто только один из них обладает требуемым терапевтическим эффектом, тогда как второй антипод может вызвать нежелательные побочные эффекты или даже быть токсичным. Каждый энантиомер может обладать своим специфическим действием. Так, S(–)-тироксин ( «левотроид» ) – это природный гормон щитовидной железы. А правовращающий R(+)-тироксин ( «декстроид» ) понижает содержание холестерина в крови. Некоторые производители придумывают для подобных случаев торговые названия-палиндромы, например, Darvo. N и Novra. D.
Оптическая чистота энантиомеров Необходимость в оптически чистых энантиомерах объясняется тем, часто только один из них обладает требуемым терапевтическим эффектом, тогда как второй антипод может вызвать нежелательные побочные эффекты или даже быть токсичным. Каждый энантиомер может обладать своим специфическим действием. Так, S(–)-тироксин ( «левотроид» ) – это природный гормон щитовидной железы. А правовращающий R(+)-тироксин ( «декстроид» ) понижает содержание холестерина в крови. Некоторые производители придумывают для подобных случаев торговые названия-палиндромы, например, Darvo. N и Novra. D.
 Различное действие энантиомеров Чем же объясняется различное действие энантиомеров? Человек – существо хиральное. Асимметрично и его тело, и молекулы биологически активных веществ, из которых оно состоит. Молекулы хиральных лекарств, взаимодействуя с определенными хиральными центрами организма, например, ферментами, могут действовать по-разному в зависимости от того, каким именно энантиомером является лекарство. «Правильное» лекарство подходит к своему рецептору, как ключ к замку и запускает желаемую биохимическую реакцию. Действие же «неправильного» антипода можно уподобить попытке пожать правой рукой правую же руку своего гостя.
Различное действие энантиомеров Чем же объясняется различное действие энантиомеров? Человек – существо хиральное. Асимметрично и его тело, и молекулы биологически активных веществ, из которых оно состоит. Молекулы хиральных лекарств, взаимодействуя с определенными хиральными центрами организма, например, ферментами, могут действовать по-разному в зависимости от того, каким именно энантиомером является лекарство. «Правильное» лекарство подходит к своему рецептору, как ключ к замку и запускает желаемую биохимическую реакцию. Действие же «неправильного» антипода можно уподобить попытке пожать правой рукой правую же руку своего гостя.
 Оптическая чистота лекарств В настоящее время многие лекарственные средства выпускаются в виде оптически чистых соединений. Так, из 25 наиболее распространенных с США лекарств только шесть являются нехиральными соединениями, три – это рацематы, остальные – чистые энантиомеры. Последние получают тремя методами: разделением рацемических смесей, модификацией природных оптически активных соединений (к ним относятся углеводы, аминокислоты, терпены, молочная и винная кислоты и др. ) и прямым синтезом. Химическая фирма Merck разработала способ производства гипотензивного препарата метилдофа, включающий самопроизвольную кристаллизацию только нужного энантиомера путем введения в раствор небольшой затравки этого изомера. Прямой синтез также требует хиральных источников, поскольку любые другие традиционные методы синтеза дают оба энантиомера в равных пропорциях – рацемат. Это, кстати, одна из причин очень высокой стоимости некоторых лекарств, поскольку направленный синтез только одного из них – очень сложная задача. Поэтому не удивительно, что из более 500 синтетических хиральных препаратов, выпускаемых во всем мире, примерно лишь десятая часть являются оптически чистыми. В то же время из 517 препаратов, полученных из природного сырья, только восемь – это рацематы.
Оптическая чистота лекарств В настоящее время многие лекарственные средства выпускаются в виде оптически чистых соединений. Так, из 25 наиболее распространенных с США лекарств только шесть являются нехиральными соединениями, три – это рацематы, остальные – чистые энантиомеры. Последние получают тремя методами: разделением рацемических смесей, модификацией природных оптически активных соединений (к ним относятся углеводы, аминокислоты, терпены, молочная и винная кислоты и др. ) и прямым синтезом. Химическая фирма Merck разработала способ производства гипотензивного препарата метилдофа, включающий самопроизвольную кристаллизацию только нужного энантиомера путем введения в раствор небольшой затравки этого изомера. Прямой синтез также требует хиральных источников, поскольку любые другие традиционные методы синтеза дают оба энантиомера в равных пропорциях – рацемат. Это, кстати, одна из причин очень высокой стоимости некоторых лекарств, поскольку направленный синтез только одного из них – очень сложная задача. Поэтому не удивительно, что из более 500 синтетических хиральных препаратов, выпускаемых во всем мире, примерно лишь десятая часть являются оптически чистыми. В то же время из 517 препаратов, полученных из природного сырья, только восемь – это рацематы.
 Детектирование оптических изомеров Различить оптические изомеры можно с помощью поляриметра – прибора, измеряющего угол поворота плоскости поляризации. Для растворов этот угол линейно зависит от толщины слоя и концентрации оптически активного вещества (закон Био). Для разных веществ оптическая активность может изменяться в очень широких пределах. Современные поляриметры позволяют измерять оптическое вращение с очень высокой точностью (до 0, 001°). Подобные измерения позволяют быстро и точно определить концентрацию оптически активных веществ, например, содержание сахара в растворах на всех стадиях его производства – начиная от сырых продуктов и кончая концентрированным раствором и патокой.
Детектирование оптических изомеров Различить оптические изомеры можно с помощью поляриметра – прибора, измеряющего угол поворота плоскости поляризации. Для растворов этот угол линейно зависит от толщины слоя и концентрации оптически активного вещества (закон Био). Для разных веществ оптическая активность может изменяться в очень широких пределах. Современные поляриметры позволяют измерять оптическое вращение с очень высокой точностью (до 0, 001°). Подобные измерения позволяют быстро и точно определить концентрацию оптически активных веществ, например, содержание сахара в растворах на всех стадиях его производства – начиная от сырых продуктов и кончая концентрированным раствором и патокой.
 АСИММЕТРИЧЕСКИЙ СИНТЕЗ - способ получения оптически активных соединений. А. С. осуществляют с помощью реакций в результате которых в молекуле исходного оптически неактивного соединения возникает хиральный элемент, гл. обр. асимметрический атом углерода (отсюда название), при этом в продуктах реакции оптические изомеры (энантиомеры) содержатся в неравных количествах. В качестве исходных веществ используют прохиральные соединения, т. е. такие, молекулы которых могут быть превращены в хиральные при замене лишь одного атома или одной группы атомов. Иногда под А. С. понимают возникновение нового хирального фрагмента в молекуле, уже имеющей элемент хиральности. Идею А. с. впервые высказал Э. Фишер в 1894, а первые синтезы осуществили в начале 20 в. В. Марквальд и А. Мак-Кензи. Выходы энантиомеров , однако, долгое время оставались очень небольшими. Сейчас А. С. - реальный путь получения оптически активных веществ.
АСИММЕТРИЧЕСКИЙ СИНТЕЗ - способ получения оптически активных соединений. А. С. осуществляют с помощью реакций в результате которых в молекуле исходного оптически неактивного соединения возникает хиральный элемент, гл. обр. асимметрический атом углерода (отсюда название), при этом в продуктах реакции оптические изомеры (энантиомеры) содержатся в неравных количествах. В качестве исходных веществ используют прохиральные соединения, т. е. такие, молекулы которых могут быть превращены в хиральные при замене лишь одного атома или одной группы атомов. Иногда под А. С. понимают возникновение нового хирального фрагмента в молекуле, уже имеющей элемент хиральности. Идею А. с. впервые высказал Э. Фишер в 1894, а первые синтезы осуществили в начале 20 в. В. Марквальд и А. Мак-Кензи. Выходы энантиомеров , однако, долгое время оставались очень небольшими. Сейчас А. С. - реальный путь получения оптически активных веществ.
 Осуществление Асимметрического Синтеза А. С. происходит благодаря участию в нем асимметризующего агента, в зависимости от типа которого различают частичный и абсолютный А. с. Первый осуществляют с помощью вспомогательных оптически активных органических веществ. Второй - под действием асимметрического физического фактора, например, при использовании в реакциях энантиоморфных кристаллов в качестве носителей катализаторов. Эффективность А. С. оценивается оптическим выходом (в %), который равен отношению величины оптического вращения продукта реакции к величине оптического вращения целевого оптически чистого вещества, или по энантиомерной чистоте. Последняя характеризует состав оптически активного вещества и равна (в %) 100(R - S)/(R + S), где R и S - доли энантиомеров, определяемые с помощью газо-жидкостной хроматографии, ЯМР-спектроскопии и др. методами.
Осуществление Асимметрического Синтеза А. С. происходит благодаря участию в нем асимметризующего агента, в зависимости от типа которого различают частичный и абсолютный А. с. Первый осуществляют с помощью вспомогательных оптически активных органических веществ. Второй - под действием асимметрического физического фактора, например, при использовании в реакциях энантиоморфных кристаллов в качестве носителей катализаторов. Эффективность А. С. оценивается оптическим выходом (в %), который равен отношению величины оптического вращения продукта реакции к величине оптического вращения целевого оптически чистого вещества, или по энантиомерной чистоте. Последняя характеризует состав оптически активного вещества и равна (в %) 100(R - S)/(R + S), где R и S - доли энантиомеров, определяемые с помощью газо-жидкостной хроматографии, ЯМР-спектроскопии и др. методами.
 Частичный асимметрический синтез Обычно для проведения А. С. осуществляют р-цию вспомогат. оптически активного в-ва с исходным прохиральным соед. либо со вторым компонентом рции - реагентом (напр. , магнийорг. соед. ), в результате чего хиральный фрагмент молекулы вспомогат. в-ва входит соотв. в молекулу исходного соед. или реагента. Если хиральный фрагмент молекулы вспомогат. в-ва войдет в состав исходного прохирального соед. , то в результате А. С. образуются неравные кол-ва диастереомеров (диастереоселективный синтез), т. к. молекулы полученного соед. будут содержать два хиральных элемента. Для получения оптич. изомера проводят отщепление хирального фрагмента молекулы вспомогат. в-ва от молекул диастереомеров. Будучи введенным в молекулу реагента, хиральный фрагмент молекулы вспомогат. в-ва может и не войти в состав продукта р-ции, а лишь содействовать образованию избытка одного из энантиомеров. Такой А. С. называют энантиоселективным. Осуществлены и др. виды энантиоселективных синтезов - превращения в присут. оптически активных растворителей, а также гомог. и гетерог. катализаторов (асимметрич. катализ).
Частичный асимметрический синтез Обычно для проведения А. С. осуществляют р-цию вспомогат. оптически активного в-ва с исходным прохиральным соед. либо со вторым компонентом рции - реагентом (напр. , магнийорг. соед. ), в результате чего хиральный фрагмент молекулы вспомогат. в-ва входит соотв. в молекулу исходного соед. или реагента. Если хиральный фрагмент молекулы вспомогат. в-ва войдет в состав исходного прохирального соед. , то в результате А. С. образуются неравные кол-ва диастереомеров (диастереоселективный синтез), т. к. молекулы полученного соед. будут содержать два хиральных элемента. Для получения оптич. изомера проводят отщепление хирального фрагмента молекулы вспомогат. в-ва от молекул диастереомеров. Будучи введенным в молекулу реагента, хиральный фрагмент молекулы вспомогат. в-ва может и не войти в состав продукта р-ции, а лишь содействовать образованию избытка одного из энантиомеров. Такой А. С. называют энантиоселективным. Осуществлены и др. виды энантиоселективных синтезов - превращения в присут. оптически активных растворителей, а также гомог. и гетерог. катализаторов (асимметрич. катализ).
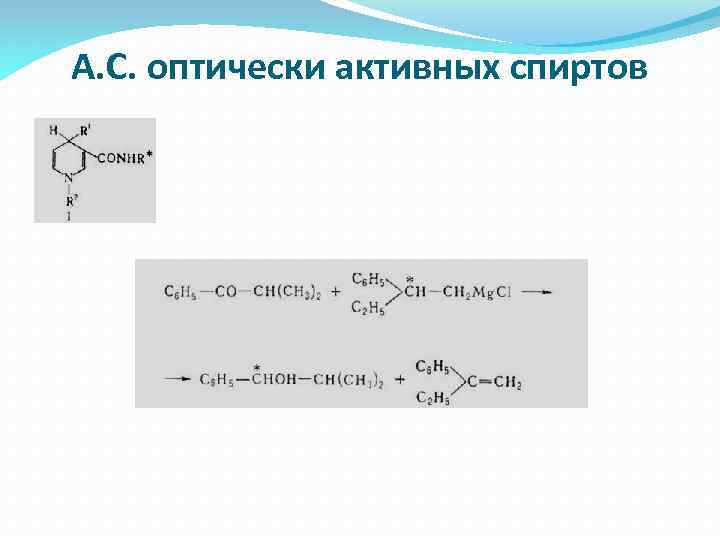
 А. С. оптически активных спиртов А. с. оптически активных спиртов часто осуществляют восстановлением карбонильных соед. с помощью хиральных комплексов, образующихся при взаимодействии Li[Al. H 4] или Na[BH 4] с оптически активными диаминами, аминоспиртами, диолами, углеводами [напр. , с N-метилэфедрином, 1, 4 -бис(диметиламино)-2, 3 -бутандиолом]. Так, алюмогидридный комплекс ( Ч )-N-метилэфедрина и Nэтиланилина восстанавливает карбонильную группу бензальацетона с оптич. выходом до 98%. Действием дигидропиридиновых реагентов (ф-ла I, R 1 -H или СН 3, R 2 - алкил; звездочкой обозначен хиральный радикал) осуществлены эффективные асимметрич. р-ции восстановления кетогрупп. Высокие оптич. выходы достигаются при восстановлении карбонильных групп оптически активными пространственно затрудненными магнийорганическими соединениями, напр. :
А. С. оптически активных спиртов А. с. оптически активных спиртов часто осуществляют восстановлением карбонильных соед. с помощью хиральных комплексов, образующихся при взаимодействии Li[Al. H 4] или Na[BH 4] с оптически активными диаминами, аминоспиртами, диолами, углеводами [напр. , с N-метилэфедрином, 1, 4 -бис(диметиламино)-2, 3 -бутандиолом]. Так, алюмогидридный комплекс ( Ч )-N-метилэфедрина и Nэтиланилина восстанавливает карбонильную группу бензальацетона с оптич. выходом до 98%. Действием дигидропиридиновых реагентов (ф-ла I, R 1 -H или СН 3, R 2 - алкил; звездочкой обозначен хиральный радикал) осуществлены эффективные асимметрич. р-ции восстановления кетогрупп. Высокие оптич. выходы достигаются при восстановлении карбонильных групп оптически активными пространственно затрудненными магнийорганическими соединениями, напр. :
 А. С. оптически активных спиртов
А. С. оптически активных спиртов
 Ассиметричный катализ С помощью А. С. осуществлены разнообразные реакции присоединения по связям С=С, например реакция Михаэля, диеновый синтез, аминопалладирование, присоединение литийкупратов Li. Cu. R 2. Высокие оптич. выходы (до 100%) достигаются при гидроборировании с помощью моно- или дипинанилборанов (соотв. H 2 BR* или HBR 2*), получаемых взаимод. В 2 Н 6 с (-)пиненом, напр. :
Ассиметричный катализ С помощью А. С. осуществлены разнообразные реакции присоединения по связям С=С, например реакция Михаэля, диеновый синтез, аминопалладирование, присоединение литийкупратов Li. Cu. R 2. Высокие оптич. выходы (до 100%) достигаются при гидроборировании с помощью моно- или дипинанилборанов (соотв. H 2 BR* или HBR 2*), получаемых взаимод. В 2 Н 6 с (-)пиненом, напр. :
 Абсолютный ассиметричный синтез Абсолютный асимметрический синтез осуществляют без участия оптически активного вспомогательного вещества, асимметризующее действие оказывает тот или иной физический фактор. Напр. , в А. С. , в которых носителями для катализатора (металлы, щелочи) служат энантиоморфные кристаллы (гл. обр. оптически активного кварца), роль асимметризующего агента выполняет кристаллич. решетка носителя. Этим способом осуществлены (хотя и с ничтожными оптич. выходами) термическая деструкция рацемических спиртов, изомеризация пропиленоксида, гидрирование рацемич. пинена и фенилкоричной к-ты, цианэтилирование 2 метилциклогексанона. Механизм асимметризующего действия связан с неодинаковой адсорбируемостью энантиомеров на оптически активном кварце.
Абсолютный ассиметричный синтез Абсолютный асимметрический синтез осуществляют без участия оптически активного вспомогательного вещества, асимметризующее действие оказывает тот или иной физический фактор. Напр. , в А. С. , в которых носителями для катализатора (металлы, щелочи) служат энантиоморфные кристаллы (гл. обр. оптически активного кварца), роль асимметризующего агента выполняет кристаллич. решетка носителя. Этим способом осуществлены (хотя и с ничтожными оптич. выходами) термическая деструкция рацемических спиртов, изомеризация пропиленоксида, гидрирование рацемич. пинена и фенилкоричной к-ты, цианэтилирование 2 метилциклогексанона. Механизм асимметризующего действия связан с неодинаковой адсорбируемостью энантиомеров на оптически активном кварце.
 Абсолютный ассиметричный синтез К абс. А. С. относятся также процессы под действием света с круговой поляризацией, напр, деструкция производных бром - и азидопропионовой кислот, синтез гелиценовых структур в нематич. жидких кристаллах, синтез (+)-винной к-ты гидроксилированием диэтилового эфира фумаровой к-ты под действием Н 2 О 2. Решающее значение для осуществления фотохимического абсолютного А. с. имеет эффект Коттона, важной особенностью которого является неравенство коэф. поглощения правого и левого циркулярно-поляризованного света оптическими изомерами в области оптически активных полос поглощения (такое явление называют круговым дихроизмом). Иными словами, один энантиомер сильнее поглощает одну компоненту циркулярно-поляризованного света, другой изомер - другую.
Абсолютный ассиметричный синтез К абс. А. С. относятся также процессы под действием света с круговой поляризацией, напр, деструкция производных бром - и азидопропионовой кислот, синтез гелиценовых структур в нематич. жидких кристаллах, синтез (+)-винной к-ты гидроксилированием диэтилового эфира фумаровой к-ты под действием Н 2 О 2. Решающее значение для осуществления фотохимического абсолютного А. с. имеет эффект Коттона, важной особенностью которого является неравенство коэф. поглощения правого и левого циркулярно-поляризованного света оптическими изомерами в области оптически активных полос поглощения (такое явление называют круговым дихроизмом). Иными словами, один энантиомер сильнее поглощает одну компоненту циркулярно-поляризованного света, другой изомер - другую.
 Абсолютный ассиметричный синтез Иными словами, один энантиомер сильнее поглощает одну компоненту циркулярно-поляризованного света, другой изомер - другую. Если, напр. , освещать рацемат однородным (правым или левым) циркулярно-поляризованным светом, то один из энантиомеров будет поглощать световой энергии больше, чем другой, и тем самым в большей степени подвергаться химической реакции (напр. , разложению). Асимметризующее действие циркулярнополяризованного света наблюдалось также в реакциях присоединения галогенов к триарилметильному радикалу и тринитростильбену.
Абсолютный ассиметричный синтез Иными словами, один энантиомер сильнее поглощает одну компоненту циркулярно-поляризованного света, другой изомер - другую. Если, напр. , освещать рацемат однородным (правым или левым) циркулярно-поляризованным светом, то один из энантиомеров будет поглощать световой энергии больше, чем другой, и тем самым в большей степени подвергаться химической реакции (напр. , разложению). Асимметризующее действие циркулярнополяризованного света наблюдалось также в реакциях присоединения галогенов к триарилметильному радикалу и тринитростильбену.
 Абсолютный ассиметричный синтез На границе между А. С. и расщеплением рацематов находятся два способа получения оптически активных веществ: 1) – кинетическое расщепление 2) асимметрические превращения. С А. С. их объединяет то, что в этих процессах происходят химические превращения, а с расщеплением рацематов - тот факт, что исходными веществами являются рацематы.
Абсолютный ассиметричный синтез На границе между А. С. и расщеплением рацематов находятся два способа получения оптически активных веществ: 1) – кинетическое расщепление 2) асимметрические превращения. С А. С. их объединяет то, что в этих процессах происходят химические превращения, а с расщеплением рацематов - тот факт, что исходными веществами являются рацематы.
 Стереоспецифический катализ Важное место в А. с. занимает катализ, при котором асимметризующим агентом является катализатор. Различают следующие виды катализа: 1)Межфазный катализ в присутствии оптически активных аммониевых оснований, получаемых из эфедрина, хинина и его аналогов. Однако в различных реакциях (борогидридное восстановление кетонов, получение вицинальных дигалогенидов, циангидринов, сульфоксидов и др. ), осуществленных этим способом, достигнуты лишь умеренные оптические выходы. 2) Гетерог. катализ в присутствии металлов, модифицированных оптически активными соединениями. Высокие оптические выходы (до 97%) достигнуты при восстановлении группы С=О метилацетоацетата и ацетилацетона над скелетным Ni, модифицированным (+)-винной к-той с добавкой Na. Br. 3) Гомог. катализ с использованием хиральных родиево-фосфиновых катализаторов - наиболее быстро развивающаяся область А. С. Чаще всего этот способ используют для получения оптически активных аминокислот гидрированием их предшественников - ациламиноакриловых кислот
Стереоспецифический катализ Важное место в А. с. занимает катализ, при котором асимметризующим агентом является катализатор. Различают следующие виды катализа: 1)Межфазный катализ в присутствии оптически активных аммониевых оснований, получаемых из эфедрина, хинина и его аналогов. Однако в различных реакциях (борогидридное восстановление кетонов, получение вицинальных дигалогенидов, циангидринов, сульфоксидов и др. ), осуществленных этим способом, достигнуты лишь умеренные оптические выходы. 2) Гетерог. катализ в присутствии металлов, модифицированных оптически активными соединениями. Высокие оптические выходы (до 97%) достигнуты при восстановлении группы С=О метилацетоацетата и ацетилацетона над скелетным Ni, модифицированным (+)-винной к-той с добавкой Na. Br. 3) Гомог. катализ с использованием хиральных родиево-фосфиновых катализаторов - наиболее быстро развивающаяся область А. С. Чаще всего этот способ используют для получения оптически активных аминокислот гидрированием их предшественников - ациламиноакриловых кислот
 Задачи стереоспецифического катализа 1) установление пространственных корреляцией между конфигурацией реагирующей молекулы и катализатором и 2) количественное изучение пространственных влияний в катализе. Руководящим принципом является представление о существовании таких корреляций в стереоспецифической адсорбции и катализе. На основании изучения оптически избирательного «кварцевого катализа» было высказано предположение о механизме действия таких катализаторов, основанного на асимметрической адсорбции молекулы субстрата на поверхности диссимметрического носителя, сопровождаемой обычным, неспецифическим катализом на кристаллах металла, который нанесен на оптически активный носитель.
Задачи стереоспецифического катализа 1) установление пространственных корреляцией между конфигурацией реагирующей молекулы и катализатором и 2) количественное изучение пространственных влияний в катализе. Руководящим принципом является представление о существовании таких корреляций в стереоспецифической адсорбции и катализе. На основании изучения оптически избирательного «кварцевого катализа» было высказано предположение о механизме действия таких катализаторов, основанного на асимметрической адсорбции молекулы субстрата на поверхности диссимметрического носителя, сопровождаемой обычным, неспецифическим катализом на кристаллах металла, который нанесен на оптически активный носитель.
 Стереоспецифический катализ Таким образом, стадия катализа сама по себе не асимметрична. Это согласуется с представлениями мультиплетной теории катализа Баландина, по которой индекс реакции не может обнаруживать стереоспецифичность действия, так как оно обусловлено внеиндексными заместителями. Термин «носитель» в таком случае следует трактовать очень широко, понимая под этим и защитный коллоид, и модификаторы катализаторов, и хелатные катализаторы. В общем случае правильнее рассматривать не диссимметрический носитель, а диссимметрический компонент, входящий в активированный комплекс, который стереохимически контролирует процесс.
Стереоспецифический катализ Таким образом, стадия катализа сама по себе не асимметрична. Это согласуется с представлениями мультиплетной теории катализа Баландина, по которой индекс реакции не может обнаруживать стереоспецифичность действия, так как оно обусловлено внеиндексными заместителями. Термин «носитель» в таком случае следует трактовать очень широко, понимая под этим и защитный коллоид, и модификаторы катализаторов, и хелатные катализаторы. В общем случае правильнее рассматривать не диссимметрический носитель, а диссимметрический компонент, входящий в активированный комплекс, который стереохимически контролирует процесс.


