ЛЕКЦИИ 15 -16 СООТНОШЕНИЕ НЕОПРЕДЕЛЁННОСТЕЙ ГЕЙЗЕНБЕРГА Микрочастица




























































lekciya_biologov_161216_po_fizike.ppt
- Размер: 804.5 Кб
- Автор:
- Количество слайдов: 62
Описание презентации ЛЕКЦИИ 15 -16 СООТНОШЕНИЕ НЕОПРЕДЕЛЁННОСТЕЙ ГЕЙЗЕНБЕРГА Микрочастица по слайдам
 ЛЕКЦИИ 15 —
ЛЕКЦИИ 15 —
 СООТНОШЕНИЕ НЕОПРЕДЕЛЁННОСТЕЙ ГЕЙЗЕНБЕРГА Микрочастица (микрообъект) не может иметь одновре-менно и определённую координату ( ), и определё-нную соответствующую проекцию импульса ( ), причем неопределённости этих величин удовлетво-ряют условиям : Произведение неопределённостей координаты и соот-ветствующей ей проекции импульса не может быть меньше величины порядка . zyx, , zyxppp, , hpz hpy hpx z y x h hpxx
СООТНОШЕНИЕ НЕОПРЕДЕЛЁННОСТЕЙ ГЕЙЗЕНБЕРГА Микрочастица (микрообъект) не может иметь одновре-менно и определённую координату ( ), и определё-нную соответствующую проекцию импульса ( ), причем неопределённости этих величин удовлетво-ряют условиям : Произведение неопределённостей координаты и соот-ветствующей ей проекции импульса не может быть меньше величины порядка . zyx, , zyxppp, , hpz hpy hpx z y x h hpxx
 Неспособность одновременно точно определить коорди-нату и соответствующую ей составляющую импульса, не связана с несовершенством методов измерения или приборов, а является следствием специфики мик-рообъектов, отражающей особенности их объективных свойств, а именно двойственной корпускулярно-волно-вой природы. Соотношение неопределённостей полу-чено при одновременном использовании классических характеристиках движения частицы (координаты, им-пульса) и наличия у неё волновых свойств. В классической механике принимается, что измерение координаты и импульса может быть определено с лю-бой точностью, и соотношение неопределённостей является квантовым ограничением применимости классической механики к микрообъектам.
Неспособность одновременно точно определить коорди-нату и соответствующую ей составляющую импульса, не связана с несовершенством методов измерения или приборов, а является следствием специфики мик-рообъектов, отражающей особенности их объективных свойств, а именно двойственной корпускулярно-волно-вой природы. Соотношение неопределённостей полу-чено при одновременном использовании классических характеристиках движения частицы (координаты, им-пульса) и наличия у неё волновых свойств. В классической механике принимается, что измерение координаты и импульса может быть определено с лю-бой точностью, и соотношение неопределённостей является квантовым ограничением применимости классической механики к микрообъектам.
 ВОЛНОВАЯ ФУНКЦИЯ И ЕЁ СТАТИСТИЧЕСКИЙ СМЫСЛ
ВОЛНОВАЯ ФУНКЦИЯ И ЕЁ СТАТИСТИЧЕСКИЙ СМЫСЛ
 Экспериментальное подтверждение идеи де-Бройля об универсальности корпускулярно-волнового дуализма и ограниченности применения классической механики привели к созданию КВАНТОВОЙ МЕХАНИКИ описыва-ющей законы движения и взаимодействия микрочас-тиц, с учетом их волновых свойств. При этом возникли новые проблемы, в частности проблема физической природы волн де-Бройля. Можно ли волны де-Бройля считать волнами вероятности, то есть считать что вероятность обнаружения микрочастиц в различных точках пространства меняется по волновому закону? НЕЛЬЗЯ!!! Такое толкование волн де-Бройля неверно, потому что тогда вероятность обнаружить частицу в не-которых точках пространства будет отрицательной, что не имеет смысла.
Экспериментальное подтверждение идеи де-Бройля об универсальности корпускулярно-волнового дуализма и ограниченности применения классической механики привели к созданию КВАНТОВОЙ МЕХАНИКИ описыва-ющей законы движения и взаимодействия микрочас-тиц, с учетом их волновых свойств. При этом возникли новые проблемы, в частности проблема физической природы волн де-Бройля. Можно ли волны де-Бройля считать волнами вероятности, то есть считать что вероятность обнаружения микрочастиц в различных точках пространства меняется по волновому закону? НЕЛЬЗЯ!!! Такое толкование волн де-Бройля неверно, потому что тогда вероятность обнаружить частицу в не-которых точках пространства будет отрицательной, что не имеет смысла.
 Что бы устранить эти трудности немецкий физик М. Борн (1882 -1970) в 1926 г. Предположил что по волновому закону изменяется НЕ сама вероятность , а величина называемая амплитудой вероятности или волновой функцией . Амплитуда вероятности может быть комплексной, и ве-роятность пропорциональна квадрату её модуля. Таким образом, описание состояния микрообъекта с помощью волновой функции имеет статистический, вероятностный характер : квадрат мо — дуля волновой функции (квадрат модуля амплитуды волн де-Бройля) определяет вероятность нахождения частицы в момент времени t в области с координата-ми и , и . tzyx, , , W 2 , , , tzyx. W xxxyyyzzz
Что бы устранить эти трудности немецкий физик М. Борн (1882 -1970) в 1926 г. Предположил что по волновому закону изменяется НЕ сама вероятность , а величина называемая амплитудой вероятности или волновой функцией . Амплитуда вероятности может быть комплексной, и ве-роятность пропорциональна квадрату её модуля. Таким образом, описание состояния микрообъекта с помощью волновой функции имеет статистический, вероятностный характер : квадрат мо — дуля волновой функции (квадрат модуля амплитуды волн де-Бройля) определяет вероятность нахождения частицы в момент времени t в области с координата-ми и , и . tzyx, , , W 2 , , , tzyx. W xxxyyyzzz
 Состояние микрочастицы в квантовой механике описы-вается с помощью волновой функции, которая является основным носителем информации об волновых и кор-пускулярных свойствах микрочастиц. Вероятность на-хождения частицы в элементе объемом равна: Квадрат модуля волновой функции: имеет смысл плотности вероятности, то есть определяет ве-роятность нахождения частицы в единичном объеме в окрестности точки с координатами . То есть физический смысл имеет не сама функция, а ква-драт её модуля , которым задаётся интенсивность волн де-Бройля. d. Vd. W 2 zyx, ,
Состояние микрочастицы в квантовой механике описы-вается с помощью волновой функции, которая является основным носителем информации об волновых и кор-пускулярных свойствах микрочастиц. Вероятность на-хождения частицы в элементе объемом равна: Квадрат модуля волновой функции: имеет смысл плотности вероятности, то есть определяет ве-роятность нахождения частицы в единичном объеме в окрестности точки с координатами . То есть физический смысл имеет не сама функция, а ква-драт её модуля , которым задаётся интенсивность волн де-Бройля. d. Vd. W 2 zyx, ,
 Вероятность найти частицу в момент времени в конеч-ном объеме равна: Так как определяется как вероятность, необходимо волновую функцию нормировать так. Что бы вероят-ность достоверного события обращалась в единицу, ес-ли за объем принять бесконечный объем всего прос-транства. Это означает, что при данном условии части-ца находится где то в пространстве. Значит, условие нормировки вероятностей , где данный интеграл вычисляется по всему бесконеч-ному пространству, то есть координатам от до . Таким образом данное условие говорит об объективном существовании частицы в пространстве и времени. d. Vd. WW VV 2 t V d. V 2 V 1 2 d. V zyx, ,
Вероятность найти частицу в момент времени в конеч-ном объеме равна: Так как определяется как вероятность, необходимо волновую функцию нормировать так. Что бы вероят-ность достоверного события обращалась в единицу, ес-ли за объем принять бесконечный объем всего прос-транства. Это означает, что при данном условии части-ца находится где то в пространстве. Значит, условие нормировки вероятностей , где данный интеграл вычисляется по всему бесконеч-ному пространству, то есть координатам от до . Таким образом данное условие говорит об объективном существовании частицы в пространстве и времени. d. Vd. WW VV 2 t V d. V 2 V 1 2 d. V zyx, ,
 Что бы волновая функция являлась объективной харак-теристикой состояния микрочастицы, она должна удо-влетворять ряду ограничивающих условий : • Быть конечной (не больше единицы) • Быть однозначной (вероятность не может быть неоднозначной величиной) • Быть непрерывной (вероятность не может изменяться скачком) Волновая функция удовлетворяет принципу суперпози-ции : если система может находиться в различных сос-тояниях, описываемых волновыми функциями , то она может так же находиться в состоя-нии описываемым линейной комбинацией этих функций: n, , 321 n n n.
Что бы волновая функция являлась объективной харак-теристикой состояния микрочастицы, она должна удо-влетворять ряду ограничивающих условий : • Быть конечной (не больше единицы) • Быть однозначной (вероятность не может быть неоднозначной величиной) • Быть непрерывной (вероятность не может изменяться скачком) Волновая функция удовлетворяет принципу суперпози-ции : если система может находиться в различных сос-тояниях, описываемых волновыми функциями , то она может так же находиться в состоя-нии описываемым линейной комбинацией этих функций: n, , 321 n n n.
 – произвольные комплексные числа Сложение волновых функций (амплитуд вероятностей), а не вероятностей (определяемых квадратами модулей волновых функций принципиально отличают кванто-вую теорию от классической статистической теории, в которой для независимых событий справедлива теоре-ма сложения вероятностей. Волновая функция, являясь основной характеристикой состояния микрообъектов, позволяет в квантовой ме-ханике вычислять средние значения физических вели-чин, характеризующих данный микрообъект. Например , среднее расстояние электрона от ядра атома определяют по формуле: , 3, 2, 1 n. Cn r d. Vrr
– произвольные комплексные числа Сложение волновых функций (амплитуд вероятностей), а не вероятностей (определяемых квадратами модулей волновых функций принципиально отличают кванто-вую теорию от классической статистической теории, в которой для независимых событий справедлива теоре-ма сложения вероятностей. Волновая функция, являясь основной характеристикой состояния микрообъектов, позволяет в квантовой ме-ханике вычислять средние значения физических вели-чин, характеризующих данный микрообъект. Например , среднее расстояние электрона от ядра атома определяют по формуле: , 3, 2, 1 n. Cn r d. Vrr
 УРАВНЕНИЕ ШРЕДИНГЕРА
УРАВНЕНИЕ ШРЕДИНГЕРА
 Уравнением движения в квантовой механике, описываю-щим движение микрочастиц в различных силовых по-лях, должно быть уравнение, из которого бы вытекали наблюдаемые на опыте волновые свойства частиц. Ос-новное уравнение должно быть уравнением относи-тельно волновой функции , так как именно она (а точнее её квадрат ). Определяет вероятность пребывания частицы в момент времени в объеме , то есть в области с координатами , и . так как искомое уравнение должно учитывать волновые свойства частиц, то оно должно быть волно-вым уравнением. Основное уравнение нерелятивистской механики сфор-мулировано в 1926 г. Э. Шредингером. Оно не выводится, а постулируется. tzyx, , , 2 td. V dxxxdyyy dzzz
Уравнением движения в квантовой механике, описываю-щим движение микрочастиц в различных силовых по-лях, должно быть уравнение, из которого бы вытекали наблюдаемые на опыте волновые свойства частиц. Ос-новное уравнение должно быть уравнением относи-тельно волновой функции , так как именно она (а точнее её квадрат ). Определяет вероятность пребывания частицы в момент времени в объеме , то есть в области с координатами , и . так как искомое уравнение должно учитывать волновые свойства частиц, то оно должно быть волно-вым уравнением. Основное уравнение нерелятивистской механики сфор-мулировано в 1926 г. Э. Шредингером. Оно не выводится, а постулируется. tzyx, , , 2 td. V dxxxdyyy dzzz
 ОБЩЕЕ УРАВНЕНИЕ ШРЕДИНГЕРА (УРАВНЕНИЕ ШРЕДИНГЕРА ЗАВИСЯЩЕЕ ОТ ВРЕМЕНИ) Где: Джс – постоянная Планка – масса частицы – оператор Лапласа – потенциальная энергия частицы в силовом поле в котором совершается движение – искомая волновая функция частицыt itzyx. U m ), , , ( 2 2 34 1012, 1 2 h m 2 2 2 zyx ), , , (tzyx. U ), , , (tzyx
ОБЩЕЕ УРАВНЕНИЕ ШРЕДИНГЕРА (УРАВНЕНИЕ ШРЕДИНГЕРА ЗАВИСЯЩЕЕ ОТ ВРЕМЕНИ) Где: Джс – постоянная Планка – масса частицы – оператор Лапласа – потенциальная энергия частицы в силовом поле в котором совершается движение – искомая волновая функция частицыt itzyx. U m ), , , ( 2 2 34 1012, 1 2 h m 2 2 2 zyx ), , , (tzyx. U ), , , (tzyx
 Уравнение Шредингера справедливо для любой частицы (со спином (собственным неуничтожимым механичес-ким моментом импульса, не связанным с движением частицы в пространстве)равным 0)движущейся с ма-лой ( по сравнению со скоростью света) скоростью Оно дополняется условиями накладываемыми на вол-новую функцию: 1. Волновая функция должна быть конечной , однознач-ной и непрерывной. 2. Производные должны быть непреры — вны. 3. Функция должна быть интегрируема. c zyx , ,
Уравнение Шредингера справедливо для любой частицы (со спином (собственным неуничтожимым механичес-ким моментом импульса, не связанным с движением частицы в пространстве)равным 0)движущейся с ма-лой ( по сравнению со скоростью света) скоростью Оно дополняется условиями накладываемыми на вол-новую функцию: 1. Волновая функция должна быть конечной , однознач-ной и непрерывной. 2. Производные должны быть непреры — вны. 3. Функция должна быть интегрируема. c zyx , ,
 УПРОШЕННОЕ УРАВНЕНИЕ ШРЕДИНГЕРА (УРАВНЕНИЕ ШРЕДИНГЕРА ДЛЯ СТАЦИОНАРНЫХ СОСТОЯНИЙ ) Для многих физических явлений уравнение Шредингера можно упростить, исключив из него зависимость от времени, иными словами найдя уравнение Шрединге-ра для стационарных состояний – состояний с фиксиро-ванными значениями энергии. Это возможно, если силовое поле в котором частица дви-жется стационарно, то есть –не зависит явно от времени и имеет смысл потенциальной энер-гии. В этом случае уравнение Шредингера может быть представлено в виде произведения двух функций, одна из которых есть функция только координат, другая zyx. UU, ,
УПРОШЕННОЕ УРАВНЕНИЕ ШРЕДИНГЕРА (УРАВНЕНИЕ ШРЕДИНГЕРА ДЛЯ СТАЦИОНАРНЫХ СОСТОЯНИЙ ) Для многих физических явлений уравнение Шредингера можно упростить, исключив из него зависимость от времени, иными словами найдя уравнение Шрединге-ра для стационарных состояний – состояний с фиксиро-ванными значениями энергии. Это возможно, если силовое поле в котором частица дви-жется стационарно, то есть –не зависит явно от времени и имеет смысл потенциальной энер-гии. В этом случае уравнение Шредингера может быть представлено в виде произведения двух функций, одна из которых есть функция только координат, другая zyx. UU, ,
 только времени, причем зависимость от времени выра-жается как: Так что: – полная энергия частицы, постоянная в случае стационарного поля. В более общей форме уравнение имеет вид: После проведения ряда преобразований уравнение будет иметь вид: t E i ti ee t E i ezyxtzyx , , ), , , ( E t E it E i ei. Eie. Ue m 2 2 0)( 2 2 UE m
только времени, причем зависимость от времени выра-жается как: Так что: – полная энергия частицы, постоянная в случае стационарного поля. В более общей форме уравнение имеет вид: После проведения ряда преобразований уравнение будет иметь вид: t E i ti ee t E i ezyxtzyx , , ), , , ( E t E it E i ei. Eie. Ue m 2 2 0)( 2 2 UE m
 ДВИЖЕНИЕ СВОБОДНОЙ ЧАСТИЦЫ
ДВИЖЕНИЕ СВОБОДНОЙ ЧАСТИЦЫ
 При движении свободной частицы ( ) её полная энергия совпадает с кинетической. Для свободной час-тицы двигающейся вдоль оси х уравнение Шредингера для стационарных состояний будет иметь вид: Частным решением этого уравнения является функция: Где , с собственным значением энер-гии . Функция представляет со-бой плоскую монохроматическую волну де-Бройля (здесь и ). 0 x. U 0 2 22 2 E m x ikx Aex const. A constk mk. E 2 22 xp. Etiikxx. Aex Expk
При движении свободной частицы ( ) её полная энергия совпадает с кинетической. Для свободной час-тицы двигающейся вдоль оси х уравнение Шредингера для стационарных состояний будет иметь вид: Частным решением этого уравнения является функция: Где , с собственным значением энер-гии . Функция представляет со-бой плоскую монохроматическую волну де-Бройля (здесь и ). 0 x. U 0 2 22 2 E m x ikx Aex const. A constk mk. E 2 22 xp. Etiikxx. Aex Expk
 Зависимость энергии от импульса обы-чная для нерелятивистских частиц , значит энергия свободной частицы может принимать любые значения и её энергетический спектр является непрерывным. Таким образом свободная квантовая частица описыва-ется плоской монохроматической волной де-Бройля. Этому соответствует не зависящая от времени плот-ность вероятности обнаружения частицы в данной точке пространства. Значит все положения свободной частицы в пространстве считаются равновероятными. mpmk. Ex
Зависимость энергии от импульса обы-чная для нерелятивистских частиц , значит энергия свободной частицы может принимать любые значения и её энергетический спектр является непрерывным. Таким образом свободная квантовая частица описыва-ется плоской монохроматической волной де-Бройля. Этому соответствует не зависящая от времени плот-ность вероятности обнаружения частицы в данной точке пространства. Значит все положения свободной частицы в пространстве считаются равновероятными. mpmk. Ex
 ЧАСТИЦА В ОДНОМЕРНОЙ ПРЯМОУГОЛЬНОЙ «ПОТЕНЦИАЛЬНОЙ ЯМЕ» С БЕСКОНЕЧНО ВЫСОКИМИ СТЕНКАМИ
ЧАСТИЦА В ОДНОМЕРНОЙ ПРЯМОУГОЛЬНОЙ «ПОТЕНЦИАЛЬНОЙ ЯМЕ» С БЕСКОНЕЧНО ВЫСОКИМИ СТЕНКАМИ
 Уравнение Шредингера ха- рактеризующее микрочастицы может быть применено к частице в одномерной «потенциальной яме» с беско-нечно высокими стенками. Такая «яма» описывается потенциальной энергией вида( если частица движется вдоль оси х ): Где – ширина ямы, а энергия отсчитывается от её дна. Уравнение Шредингера для стационарных состояний в случае одномерной задачи записывается в виде: 0 UUU 0 l t itzyx. U m ), , , ( 2 2 lx lx x x. U 00 0 )( l 0)( 2 22 2 UE m x
Уравнение Шредингера ха- рактеризующее микрочастицы может быть применено к частице в одномерной «потенциальной яме» с беско-нечно высокими стенками. Такая «яма» описывается потенциальной энергией вида( если частица движется вдоль оси х ): Где – ширина ямы, а энергия отсчитывается от её дна. Уравнение Шредингера для стационарных состояний в случае одномерной задачи записывается в виде: 0 UUU 0 l t itzyx. U m ), , , ( 2 2 lx lx x x. U 00 0 )( l 0)( 2 22 2 UE m x
 По условию задачи (бесконечно высокие стенки) частица не проникает за пределы ямы, и вероятность её обна-ружения (а значит и волновая функция) за пределами ямы равна нулю. На границах ямы ( при и ) непрерывная волновая функция тоже должна обра-щаться в нуль, а значит граничные условия в этом слу-чае имеют вид В пределах ямы уравнение Шредингера сводится к уравнению: или иначе Где: 0 xlx 00 l lx 0 0 2 22 2 E m x 0 2 2 2 k x 22 2 m. Ek
По условию задачи (бесконечно высокие стенки) частица не проникает за пределы ямы, и вероятность её обна-ружения (а значит и волновая функция) за пределами ямы равна нулю. На границах ямы ( при и ) непрерывная волновая функция тоже должна обра-щаться в нуль, а значит граничные условия в этом слу-чае имеют вид В пределах ямы уравнение Шредингера сводится к уравнению: или иначе Где: 0 xlx 00 l lx 0 0 2 22 2 E m x 0 2 2 2 k x 22 2 m. Ek
 Общее решение данного дифференциального уравнения: Так как то , а значит Условие выполняется только при где – целое число, то есть необходимо что бы выполнялось равенство , а значит: Стационарное уравнение Шредингера описывающее движение частицы в «потенциальной яме» , с беско-нечно высокими « стенками» удовлетворяется только при собственных значениях энергии зависящих от целого числа . kx. Bkx. Axcossin 00 0 sinkl. Al 0 Bkx. Axsin nkl , 3, 2, 1 n lnk 2 222 2 ml n En n. E , 3, 2, 1 n
Общее решение данного дифференциального уравнения: Так как то , а значит Условие выполняется только при где – целое число, то есть необходимо что бы выполнялось равенство , а значит: Стационарное уравнение Шредингера описывающее движение частицы в «потенциальной яме» , с беско-нечно высокими « стенками» удовлетворяется только при собственных значениях энергии зависящих от целого числа . kx. Bkx. Axcossin 00 0 sinkl. Al 0 Bkx. Axsin nkl , 3, 2, 1 n lnk 2 222 2 ml n En n. E , 3, 2, 1 n
 Энергия частицы в «потенциальной» яме с бесконеч-но высокими «стенками» принимает лишь определён-ные дискретные значения или квантуется. Квантован-ные значения энергии называются уровнями энер-гии , а число определяющее энергетические уровни частицы, называется главным квантовым числом. Микрочастица в «потенциальной яме» с бесконечно вы-сокими «стенками» может находиться только на опре-делённом энергетическом уровне , или, иначе гово-ря, частица находится в квантовом состоянии . n. E n
Энергия частицы в «потенциальной» яме с бесконеч-но высокими «стенками» принимает лишь определён-ные дискретные значения или квантуется. Квантован-ные значения энергии называются уровнями энер-гии , а число определяющее энергетические уровни частицы, называется главным квантовым числом. Микрочастица в «потенциальной яме» с бесконечно вы-сокими «стенками» может находиться только на опре-делённом энергетическом уровне , или, иначе гово-ря, частица находится в квантовом состоянии . n. E n
 Подставив в уравнение волновой функции , значе-ние найдем собственные функции: Постоянную интегрирования А найдём из условия нор-мировки: То есть: Проинтегрировав получим , а собственные функ-ции будут иметь вид: x x l n Ax sin k 1 2 d. V 1 sin 22 xdx l n A l A 2 x l n l xn sin
Подставив в уравнение волновой функции , значе-ние найдем собственные функции: Постоянную интегрирования А найдём из условия нор-мировки: То есть: Проинтегрировав получим , а собственные функ-ции будут иметь вид: x x l n Ax sin k 1 2 d. V 1 sin 22 xdx l n A l A 2 x l n l xn sin
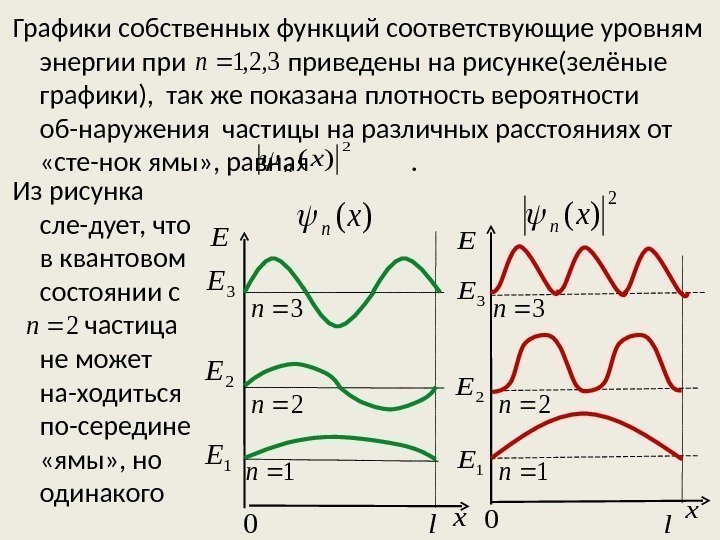
 Графики собственных функций соответствующие уровням энергии при приведены на рисунке(зелёные графики), так же показана плотность вероятности об-наружения частицы на различных расстояниях от «сте-нок ямы» , равная . Из рисунка сле-дует, что в квантовом состоянии с частица не может на-ходиться по-середине «ямы» , но одинакого. E 3 E 2 E 1 E xl 0 )(xn 3 E 1 E 2 E E x l 0 2 )(xn 3, 2, 1 n 2 )(xn 2 n 2 n 2 n 1 n 1 n 3 n 3 n
Графики собственных функций соответствующие уровням энергии при приведены на рисунке(зелёные графики), так же показана плотность вероятности об-наружения частицы на различных расстояниях от «сте-нок ямы» , равная . Из рисунка сле-дует, что в квантовом состоянии с частица не может на-ходиться по-середине «ямы» , но одинакого. E 3 E 2 E 1 E xl 0 )(xn 3 E 1 E 2 E E x l 0 2 )(xn 3, 2, 1 n 2 )(xn 2 n 2 n 2 n 1 n 1 n 3 n 3 n
 часто может быть в левой и правой частях. Такое пове-дение показывает, что представление о траекториях частицы в квантовой механике несостоятельны. Энергетический интервал между соседними уровнями: Для электрона, при размере «ямы» (для свобод-ных электронов в металле) , то есть энергетические уровни расположены столь тесно, что спектр практически можно считать непрерывным, если же размеры «ямы» сопоставимы с атомными то, для электрона , то есть получается явно дискретное значение (линейчатый спектр). Применение уравнения Шредингера к частице n ml EEEnnn 2 22 1)12( 2 м 10 1 l э. Вn 10 Дж 10 -1635 n. En м 10 10 lэ. В 10 Дж 10 217 nn. En
часто может быть в левой и правой частях. Такое пове-дение показывает, что представление о траекториях частицы в квантовой механике несостоятельны. Энергетический интервал между соседними уровнями: Для электрона, при размере «ямы» (для свобод-ных электронов в металле) , то есть энергетические уровни расположены столь тесно, что спектр практически можно считать непрерывным, если же размеры «ямы» сопоставимы с атомными то, для электрона , то есть получается явно дискретное значение (линейчатый спектр). Применение уравнения Шредингера к частице n ml EEEnnn 2 22 1)12( 2 м 10 1 l э. Вn 10 Дж 10 -1635 n. En м 10 10 lэ. В 10 Дж 10 217 nn. En
 в «потенциальной яме» с бесконечно высокими «стен-ками» приводит к квантованным значениям энергии, в то время как классическая механикаких ограниче-ний на энергию этой частицы не накладывает. Частица в «потенциальной яме» не может иметь энергию меньшую чем , это не случайно и зависит от сложения неопределённостей. Неопределённость координаты частицы в «яме» равна . Тогда импульс не может (по соотношению нео-пределённостей ) иметь точное, в данном случае нулевое значение. Неопределенность импульса . Такому разбросу значений импульса соответст-вует кинетическая энергия . Все остальные уровни имеют энергию превышающую это минимальное значение. 2 22 1 2 ml E x lx hpx lhp 222 min 22 mlhmp.
в «потенциальной яме» с бесконечно высокими «стен-ками» приводит к квантованным значениям энергии, в то время как классическая механикаких ограниче-ний на энергию этой частицы не накладывает. Частица в «потенциальной яме» не может иметь энергию меньшую чем , это не случайно и зависит от сложения неопределённостей. Неопределённость координаты частицы в «яме» равна . Тогда импульс не может (по соотношению нео-пределённостей ) иметь точное, в данном случае нулевое значение. Неопределенность импульса . Такому разбросу значений импульса соответст-вует кинетическая энергия . Все остальные уровни имеют энергию превышающую это минимальное значение. 2 22 1 2 ml E x lx hpx lhp 222 min 22 mlhmp.
 При больших квантовых числах ( ) , то есть со-седние уровни расположены тесно: тем теснее, чем боль-ше . Если очень велико, то можно говорить о практи-чески непрерывной последовательности уровней и харак-терная особенность квантовых процессов – дискретность, сглаживается это частный случай ПРИНЦИПА СООТВЕТ-СТВИЯ БОРА , по которому: законы квантовой механики должны, при больших значениях квантовых чисел пере-ходить в законы классической механики. ОБЩАЯ ТРАКТОВКА ЗАКОНА СООТВЕТСТВИЯ БОРА : Всякая новая теория, более общая, являющаяся развитием классической, не отвергает её полностью, а включает в себя классическую теорию, указывая границы её приме-нения, и в определённых случаях новая теория переходит в старую. 1 n n 12 n. EEnn n
При больших квантовых числах ( ) , то есть со-седние уровни расположены тесно: тем теснее, чем боль-ше . Если очень велико, то можно говорить о практи-чески непрерывной последовательности уровней и харак-терная особенность квантовых процессов – дискретность, сглаживается это частный случай ПРИНЦИПА СООТВЕТ-СТВИЯ БОРА , по которому: законы квантовой механики должны, при больших значениях квантовых чисел пере-ходить в законы классической механики. ОБЩАЯ ТРАКТОВКА ЗАКОНА СООТВЕТСТВИЯ БОРА : Всякая новая теория, более общая, являющаяся развитием классической, не отвергает её полностью, а включает в себя классическую теорию, указывая границы её приме-нения, и в определённых случаях новая теория переходит в старую. 1 n n 12 n. EEnn n
 ЭЛЕМЕНТЫ СОВРЕМЕННОЙ ФИЗИКИ АТОМОВ И МОЛЕКУЛ
ЭЛЕМЕНТЫ СОВРЕМЕННОЙ ФИЗИКИ АТОМОВ И МОЛЕКУЛ
 АТОМ ВОДОРОДА В КВАНТОВОЙ МЕХАНИКЕ
АТОМ ВОДОРОДА В КВАНТОВОЙ МЕХАНИКЕ
 Решение задачи об энергетичес-ких уровнях электрона для ато-ма водорода (а так же водоро-доподобных систем), сводится к задаче о движении электрона в кулоновском поле ядра. Потенциальная энергия взаимодействия электрона с яд-ром, обладающим зарядом (для водорода ): Где – расстояние между электроном и ядром. Функция графически изображена на графике красной кривой. неограниченно убывающая (возрастаю-щая по модулю) , с уменьшением (при приближении электрона к ядру). i. Е 1 Е 2 Е 3 Е 0 UЕ, r 0 Е Ze 1 Z r Ze r. U 0 2 4 )( r r )(r. U
Решение задачи об энергетичес-ких уровнях электрона для ато-ма водорода (а так же водоро-доподобных систем), сводится к задаче о движении электрона в кулоновском поле ядра. Потенциальная энергия взаимодействия электрона с яд-ром, обладающим зарядом (для водорода ): Где – расстояние между электроном и ядром. Функция графически изображена на графике красной кривой. неограниченно убывающая (возрастаю-щая по модулю) , с уменьшением (при приближении электрона к ядру). i. Е 1 Е 2 Е 3 Е 0 UЕ, r 0 Е Ze 1 Z r Ze r. U 0 2 4 )( r r )(r. U
 Состояние электрона в атоме водорода описывается вол-новой функцией удовлетворяющему стационарному уравнению Шредингера: Где: – масса электрона – полная энергия электрона в атоме Так как поле, в котором движется электрон, является це-нтрально симметричным, то для решения данного уравнения используют сферическую систему коорди-нат . Не вдаваясь в математическое решение этой задачи, ограничимся рассмотрением важнейших результатов, которые из него следуют, выявив его физический смысл. 0 4 2 0 2 2 r Ze E m , , r m
Состояние электрона в атоме водорода описывается вол-новой функцией удовлетворяющему стационарному уравнению Шредингера: Где: – масса электрона – полная энергия электрона в атоме Так как поле, в котором движется электрон, является це-нтрально симметричным, то для решения данного уравнения используют сферическую систему коорди-нат . Не вдаваясь в математическое решение этой задачи, ограничимся рассмотрением важнейших результатов, которые из него следуют, выявив его физический смысл. 0 4 2 0 2 2 r Ze E m , , r m
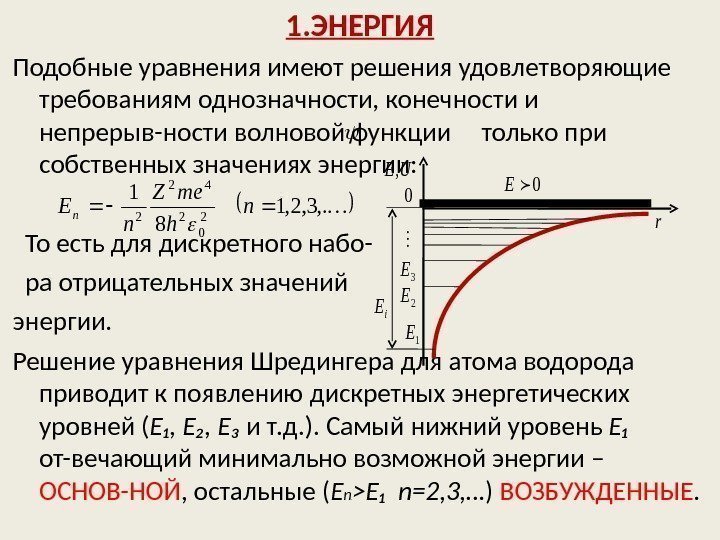
 1. ЭНЕРГИЯ Подобные уравнения имеют решения удовлетворяющие требованиям однозначности, конечности и непрерыв-ности волновой функции только при собственных значениях энергии: То есть для дискретного набо- ра отрицательных значений энергии. Решение уравнения Шредингера для атома водорода приводит к появлению дискретных энергетических уровней ( Е ₁, E₂ , E₃ и т. д. ). Самый нижний уровень Е ₁ от-вечающий минимально возможной энергии – ОСНОВ-НОЙ , остальные ( Е n > > Е₁ n=2, 3, … ) ВОЗБУЖДЕННЫЕ. , . 3, 2, 1 8 1 2 0 2 42 2 n h me. Z n En i. Е 1 Е 2 Е 3 Е 0 UЕ, r 0 Е
1. ЭНЕРГИЯ Подобные уравнения имеют решения удовлетворяющие требованиям однозначности, конечности и непрерыв-ности волновой функции только при собственных значениях энергии: То есть для дискретного набо- ра отрицательных значений энергии. Решение уравнения Шредингера для атома водорода приводит к появлению дискретных энергетических уровней ( Е ₁, E₂ , E₃ и т. д. ). Самый нижний уровень Е ₁ от-вечающий минимально возможной энергии – ОСНОВ-НОЙ , остальные ( Е n > > Е₁ n=2, 3, … ) ВОЗБУЖДЕННЫЕ. , . 3, 2, 1 8 1 2 0 2 42 2 n h me. Z n En i. Е 1 Е 2 Е 3 Е 0 UЕ, r 0 Е
 При движение электрона является связанным – он находится внутри гиперболической «потенциальной ямы» . По мере роста главного квантового числа n энер-гетические уровни располагаются теснее и при . При движение электрона является свобод-ным, область непрерывного спектра (заштрихова-на) соответствует ионизированному атому. Энергия ионизации атома водорода: Выражение для совпадает с формулой полученной Бором для энергии атома водорода. Однако, если Бору пришлось вводить дополнительные гипотезы (посту-латы), то в квантовой механике дискретные значения энергии, являясь следствием самой теории, вытекают непосредственно из уравнения Шредингера. n 0 E 0 E Джэ. В h me EEi 19 2 0 2 4 11068, 2155, 13 8 n.
При движение электрона является связанным – он находится внутри гиперболической «потенциальной ямы» . По мере роста главного квантового числа n энер-гетические уровни располагаются теснее и при . При движение электрона является свобод-ным, область непрерывного спектра (заштрихова-на) соответствует ионизированному атому. Энергия ионизации атома водорода: Выражение для совпадает с формулой полученной Бором для энергии атома водорода. Однако, если Бору пришлось вводить дополнительные гипотезы (посту-латы), то в квантовой механике дискретные значения энергии, являясь следствием самой теории, вытекают непосредственно из уравнения Шредингера. n 0 E 0 E Джэ. В h me EEi 19 2 0 2 4 11068, 2155, 13 8 n.
 2. КВАНТОВЫЕ ЧИСЛА В квантовой механике указывалось, что уравнению Шре-дингера удовлетворяют собственные функции определяемые тремя квантовыми числами : главным , орбитальным и магнитным . • Главное квантовое число – определяет энергетичес-кие уровни электрона в атоме и может принимать лю-бые целочисленные значения . Из решения уравнения Шредингера вытекает момент импульса (механический орбитальный момент) элект-рона квантуется, то есть не может быть произвольным, а принимает дискретные значения: , , rlnlm n llm n , . 3, 2, 1 n 1 ll. Le
2. КВАНТОВЫЕ ЧИСЛА В квантовой механике указывалось, что уравнению Шре-дингера удовлетворяют собственные функции определяемые тремя квантовыми числами : главным , орбитальным и магнитным . • Главное квантовое число – определяет энергетичес-кие уровни электрона в атоме и может принимать лю-бые целочисленные значения . Из решения уравнения Шредингера вытекает момент импульса (механический орбитальный момент) элект-рона квантуется, то есть не может быть произвольным, а принимает дискретные значения: , , rlnlm n llm n , . 3, 2, 1 n 1 ll. Le
 • Орбитальное квантовое число – определяет момент импульса электрона в атоме, при заданном значении принимает значения то есть всего зна-чений. • Магнитное квантовое число – определяет проекцию момента импульса электрона на заданное направле-ние, причем вектор момента импульса электрона в атоме может иметь в пространстве ориентаций. При заданном значении может принимать значения то есть значений. Наличие должно привести в магнитном поле к расще-плению уровня с главным квантовым числом на подуровней. Соответственно в спектре атома должно наблюдаться расщепление спектральных линий. (эффект Зеемана). l n 1, 2, 1, 0 nl 12 l lml, , 2, 1, 012 l lm n 12 l
• Орбитальное квантовое число – определяет момент импульса электрона в атоме, при заданном значении принимает значения то есть всего зна-чений. • Магнитное квантовое число – определяет проекцию момента импульса электрона на заданное направле-ние, причем вектор момента импульса электрона в атоме может иметь в пространстве ориентаций. При заданном значении может принимать значения то есть значений. Наличие должно привести в магнитном поле к расще-плению уровня с главным квантовым числом на подуровней. Соответственно в спектре атома должно наблюдаться расщепление спектральных линий. (эффект Зеемана). l n 1, 2, 1, 0 nl 12 l lml, , 2, 1, 012 l lm n 12 l
 Хотя энергия электрона и зависит только от главного ква-нтового числа , но каждому собственному значению (кроме ) соответствуют несколько собственных функций отличающихся значениями и . Значит, атом может иметь одно и то же значение энергии на-ходясь в нескольких различных состояниях. Так при данном орбитальное квантовое число может изменяться от 0 до , и каждому значению соот-ветствует различных состояний , то число раз-личных состояний, соответствующих данному равно n n. E 1 E lnlmllm nl 12 l 1 nl lm n 2 1 0 12 nl n
Хотя энергия электрона и зависит только от главного ква-нтового числа , но каждому собственному значению (кроме ) соответствуют несколько собственных функций отличающихся значениями и . Значит, атом может иметь одно и то же значение энергии на-ходясь в нескольких различных состояниях. Так при данном орбитальное квантовое число может изменяться от 0 до , и каждому значению соот-ветствует различных состояний , то число раз-личных состояний, соответствующих данному равно n n. E 1 E lnlmllm nl 12 l 1 nl lm n 2 1 0 12 nl n
 Квантовые числа и их значения являются следствием ре-шений уравнения Шредингера и условий однозначнос-ти, непрерывности и конечности налагаемых на волно-вую функцию . Кроме того, так как при движении электрона в атоме существенны волновые свойства электрона, квантовая механика отказывается от клас-сического представления о электронных орбитах. Сог-ласно квантовой механике каждому энергетическому состоянию соответствует волновая функция, квадрат модуля которой определяет вероятность обнаружения электрона в единице объема. Вероятность обнаружения электрона в различных частях атома различна. Электрон при своем движении как бы «размазан» по всему объему, образуя электронное об-лако, плотность (густота) которого характеризует веро-
Квантовые числа и их значения являются следствием ре-шений уравнения Шредингера и условий однозначнос-ти, непрерывности и конечности налагаемых на волно-вую функцию . Кроме того, так как при движении электрона в атоме существенны волновые свойства электрона, квантовая механика отказывается от клас-сического представления о электронных орбитах. Сог-ласно квантовой механике каждому энергетическому состоянию соответствует волновая функция, квадрат модуля которой определяет вероятность обнаружения электрона в единице объема. Вероятность обнаружения электрона в различных частях атома различна. Электрон при своем движении как бы «размазан» по всему объему, образуя электронное об-лако, плотность (густота) которого характеризует веро-
 ятность нахождения электрона в различных точках объ-ема атома. Квантовые числа и характеризуют раз-мер и форму электронного облака, а квантовое число характеризует ориентацию электронного облака в про-странстве. В атомной физике, по аналогии со спектроскопией, состо-яние электрона, характеризующееся квантовыми чис-лами называют s -состоянием (электрон в этом сос-тоянии называется s- электрон). При – р -состоянием при – d -состоянием, при – f -состоянием, и т. д. Значение главного квантового числа указывается перед условным обозначением орбитального квантового числа. Например, электроны в состояниях с и обозначаются соответственно символами 2 s и 2 p. ln lm 0 l 1 l 2 l 3 l 0, 2 ln 1, 2 ln
ятность нахождения электрона в различных точках объ-ема атома. Квантовые числа и характеризуют раз-мер и форму электронного облака, а квантовое число характеризует ориентацию электронного облака в про-странстве. В атомной физике, по аналогии со спектроскопией, состо-яние электрона, характеризующееся квантовыми чис-лами называют s -состоянием (электрон в этом сос-тоянии называется s- электрон). При – р -состоянием при – d -состоянием, при – f -состоянием, и т. д. Значение главного квантового числа указывается перед условным обозначением орбитального квантового числа. Например, электроны в состояниях с и обозначаются соответственно символами 2 s и 2 p. ln lm 0 l 1 l 2 l 3 l 0, 2 ln 1, 2 ln
 3. СПЕКТР Квантовые числа позволяют более полно описать спектр испускания (поглощения) атома водорода полученный в теории Бора. В квантовой механике вводятся правила отбора, ограни-чивающие число возможных переходов в атоме, свя-занных с испусканием и поглощением света. Теоретически доказано, что для дипольного излучения электрона движущегося в центрально-симметричном поле ядра могут осуществляться только такие переходы для которых: 1. Изменение орбитального квантового числа удов-летворяет условию . 2. Изменение магнитного квантового числа удовлет-воряет условию . lmln, , l 1 l lm 1, 0 lm
3. СПЕКТР Квантовые числа позволяют более полно описать спектр испускания (поглощения) атома водорода полученный в теории Бора. В квантовой механике вводятся правила отбора, ограни-чивающие число возможных переходов в атоме, свя-занных с испусканием и поглощением света. Теоретически доказано, что для дипольного излучения электрона движущегося в центрально-симметричном поле ядра могут осуществляться только такие переходы для которых: 1. Изменение орбитального квантового числа удов-летворяет условию . 2. Изменение магнитного квантового числа удовлет-воряет условию . lmln, , l 1 l lm 1, 0 lm
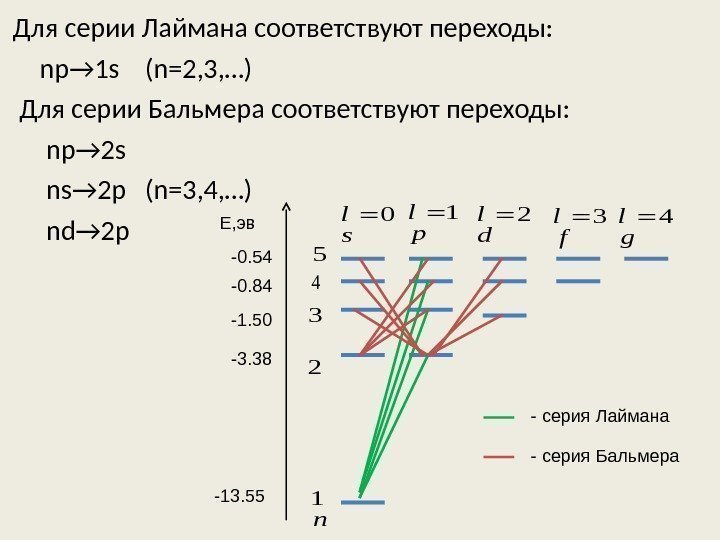
 Для серии Лаймана соответствуют переходы: np → 1 s (n=2, 3, …) Для серии Бальмера соответствуют переходы: np → 2 s ns → 2 p (n=3, 4, …) nd→ 2 ps l 0 p l 1 g l 4 f l 3 d l 2 n 1 2 3 4 5 E, эв -13. 55 -3. 38 -1. 50 -0. 84 -0. 54 — серия Лаймана — серия Бальмера
Для серии Лаймана соответствуют переходы: np → 1 s (n=2, 3, …) Для серии Бальмера соответствуют переходы: np → 2 s ns → 2 p (n=3, 4, …) nd→ 2 ps l 0 p l 1 g l 4 f l 3 d l 2 n 1 2 3 4 5 E, эв -13. 55 -3. 38 -1. 50 -0. 84 -0. 54 — серия Лаймана — серия Бальмера
 Переход электронов из основного состояния в возбуж-денное обусловлен увеличением энергии атома и мо-жет проходить только при сообщении атому энергии извне, например за счет поглощения атомом фотона. Так как поглощающий атом находится обычно в воз- бужденном состоянии, то спектр атома водорода дол-жен состоять из линий соответствующих переходам 1 s →np (n=2, 3, …) , что находится в полном согласии с опытом. Возможны иногда и слабые «запрещенные» линии. Нап-ример переход при , но их вероятность ничтожна по сравнению с правильными. 2 l
Переход электронов из основного состояния в возбуж-денное обусловлен увеличением энергии атома и мо-жет проходить только при сообщении атому энергии извне, например за счет поглощения атомом фотона. Так как поглощающий атом находится обычно в воз- бужденном состоянии, то спектр атома водорода дол-жен состоять из линий соответствующих переходам 1 s →np (n=2, 3, …) , что находится в полном согласии с опытом. Возможны иногда и слабые «запрещенные» линии. Нап-ример переход при , но их вероятность ничтожна по сравнению с правильными. 2 l
 СПИН ЭЛЕКТРОНА СПИНОВОЕ КВАНТОВОЕ ЧИСЛО
СПИН ЭЛЕКТРОНА СПИНОВОЕ КВАНТОВОЕ ЧИСЛО
 Опыты показали, что узкий пучок атомов водорода, заве-домо находящихся в s- состоянии, в неоднородном ма-гнитном поле расщепляется на два пучка. В этом сос-тоянии момент импульса электрона равен нулю. Магнитный момент атома, связанный с орбитальным движением электрона пропорционален механическо-му моменту, поэтому он равен нулю, и магнитное поле не должно оказывать влияние на движение атомов во-дорода в основном состоянии, то есть расщепления быть не должно. – орбитальный механический момент электрона Однако в дальнейшем, применении спектральныхм приборов с большей разрешающей способностью бы-ло доказано, что спектральные линии атомов водородаem. L m e p 2 e. L
Опыты показали, что узкий пучок атомов водорода, заве-домо находящихся в s- состоянии, в неоднородном ма-гнитном поле расщепляется на два пучка. В этом сос-тоянии момент импульса электрона равен нулю. Магнитный момент атома, связанный с орбитальным движением электрона пропорционален механическо-му моменту, поэтому он равен нулю, и магнитное поле не должно оказывать влияние на движение атомов во-дорода в основном состоянии, то есть расщепления быть не должно. – орбитальный механический момент электрона Однако в дальнейшем, применении спектральныхм приборов с большей разрешающей способностью бы-ло доказано, что спектральные линии атомов водородаem. L m e p 2 e. L
 обнаруживают тонкую структуру (являются дуплетами) даже в отсутствие магнитного поля. Для объяснения тонкой структуры спектральных линий было предположено что: Электрон обладает собственным неуничтожимым меха-ническим моментом импульса , не связанным с дви-жением электрона в пространстве – СПИНОМ. СПИН электрона (или другой микрочастицы) – квантовая величина, у неё НЕТ классического аналога , это внут-реннее неотъемлимое свойство электрона, подобное его заряду и массе. Если электрону приписывается собственный механичес-кий момент импульса (спин) , то ему соответствует собственный магнитный момент s. L msp
обнаруживают тонкую структуру (являются дуплетами) даже в отсутствие магнитного поля. Для объяснения тонкой структуры спектральных линий было предположено что: Электрон обладает собственным неуничтожимым меха-ническим моментом импульса , не связанным с дви-жением электрона в пространстве – СПИНОМ. СПИН электрона (или другой микрочастицы) – квантовая величина, у неё НЕТ классического аналога , это внут-реннее неотъемлимое свойство электрона, подобное его заряду и массе. Если электрону приписывается собственный механичес-кий момент импульса (спин) , то ему соответствует собственный магнитный момент s. L msp
 По общим выводам квантовой механики спин квантуется по закону: Где: – спиновое квантовое число По аналогии с орбитальным моментом импульса, проек-ция может принимать значений. Так как в опы-тах Штерна и Герлаха наблюдались только две ориен-тации, то . Проекция спина на направ-ление внешнего магнитного поля , являясь квантовой величиной, определяется выражением Где: – магнитное спиновое число. Которое может иметь только 2 значения: 1 ss. Ls s sz. L 12 s 21212 ss sszm. L sm 2 1 sm
По общим выводам квантовой механики спин квантуется по закону: Где: – спиновое квантовое число По аналогии с орбитальным моментом импульса, проек-ция может принимать значений. Так как в опы-тах Штерна и Герлаха наблюдались только две ориен-тации, то . Проекция спина на направ-ление внешнего магнитного поля , являясь квантовой величиной, определяется выражением Где: – магнитное спиновое число. Которое может иметь только 2 значения: 1 ss. Ls s sz. L 12 s 21212 ss sszm. L sm 2 1 sm
 Таким образом микрочастицы необходимо охарактери-зовать дополнительной внутренней степенью свобо-ды. И для полного описания состояния электрона в атоме наряду с главным , орбитальным и магнитным квантовыми числами необходимо задавать ещё и маг-нитное спиновое квантовое число.
Таким образом микрочастицы необходимо охарактери-зовать дополнительной внутренней степенью свобо-ды. И для полного описания состояния электрона в атоме наряду с главным , орбитальным и магнитным квантовыми числами необходимо задавать ещё и маг-нитное спиновое квантовое число.
 ПРИНЦИП НЕРАЗЛИЧИМОСТИ ТОЖДЕСТВЕННЫХ ЧАСТИЦ
ПРИНЦИП НЕРАЗЛИЧИМОСТИ ТОЖДЕСТВЕННЫХ ЧАСТИЦ
 Если перейти от рассмотрения одной микрочастицы (эле-ктрона) к многоэлектронным системам, то проявляют-ся особые свойства НЕ ИМЕЮЩИЕ АНАЛОГОВ в класси-ческой физике. Пусть квантово-механическая система состоит из одинаковых частиц , (например электронов), имеющих одинаковые характеристики (спин, массу, электрический заряд и другие внутренние характерис-тики (например квантовые числа)). Такие частицы назы-аются тождественными. Существует фундаментальный механизм квантовой меха-ники – ПРИНЦИП НЕРАЗЛИЧИМОСТИ ТОЖДЕСТВЕННЫХ ЧАСТИЦ : невозможно экспериментально различить тождественные частицы.
Если перейти от рассмотрения одной микрочастицы (эле-ктрона) к многоэлектронным системам, то проявляют-ся особые свойства НЕ ИМЕЮЩИЕ АНАЛОГОВ в класси-ческой физике. Пусть квантово-механическая система состоит из одинаковых частиц , (например электронов), имеющих одинаковые характеристики (спин, массу, электрический заряд и другие внутренние характерис-тики (например квантовые числа)). Такие частицы назы-аются тождественными. Существует фундаментальный механизм квантовой меха-ники – ПРИНЦИП НЕРАЗЛИЧИМОСТИ ТОЖДЕСТВЕННЫХ ЧАСТИЦ : невозможно экспериментально различить тождественные частицы.
 В классической механике даже одинаковые частицы мо-жно различить, например по положению в пространст-ве или импульсам, можно проследить за траекторией каждой частицы, и классическая механика систем сос-тоящих из одинаковых частиц не отличается от механи-ки систем состоящих из различных частиц. В квантовой механике из соотношения неопределеннос-тей вытекает, что для микрочастиц вообще непримени-мо понятие траектории; состояние микрочастицы опи-сывается волновой функцией, позволяющей опреде-лить лишь вероятность нахождения микрочастицы в той или иной точке пространства. Если же волновые функции двух тождественных частиц в пространстве перекрываются, то можно лишь говорить о вероятнос-ти нахождения в данной области одной из тождествен-
В классической механике даже одинаковые частицы мо-жно различить, например по положению в пространст-ве или импульсам, можно проследить за траекторией каждой частицы, и классическая механика систем сос-тоящих из одинаковых частиц не отличается от механи-ки систем состоящих из различных частиц. В квантовой механике из соотношения неопределеннос-тей вытекает, что для микрочастиц вообще непримени-мо понятие траектории; состояние микрочастицы опи-сывается волновой функцией, позволяющей опреде-лить лишь вероятность нахождения микрочастицы в той или иной точке пространства. Если же волновые функции двух тождественных частиц в пространстве перекрываются, то можно лишь говорить о вероятнос-ти нахождения в данной области одной из тождествен-
 ных частиц. Таким образом в квантовой механике тожде-ственные частицы полностью теряют свою индивидуаль-ность и становятся неразличимыми. Принцип неразличимости вводится в квантовую механику как новый принцип являющийся фундаментальным. Принцип неразличимости можно записать в виде: – совокупность пространственных и спиновых коор-динат первой и второй частиц. Принцип неразличимости тождественных частиц ведёт к определённому свойству симметрии волновой функции. Если при перемене частиц местами волновая функция не меняет знака, то она симметричная , если же меняет , то она антисимметричная. 2 12 2 21, , xxxx 21 xx 1221, , xxxx
ных частиц. Таким образом в квантовой механике тожде-ственные частицы полностью теряют свою индивидуаль-ность и становятся неразличимыми. Принцип неразличимости вводится в квантовую механику как новый принцип являющийся фундаментальным. Принцип неразличимости можно записать в виде: – совокупность пространственных и спиновых коор-динат первой и второй частиц. Принцип неразличимости тождественных частиц ведёт к определённому свойству симметрии волновой функции. Если при перемене частиц местами волновая функция не меняет знака, то она симметричная , если же меняет , то она антисимметричная. 2 12 2 21, , xxxx 21 xx 1221, , xxxx
 Симметрия или антисимметрия определяется спином час-тиц. Частицы с полуцелым спином (электроны, протоны, нейтроны) описываются антисимметричными волновы-ми функциями и подчиняются статистике Ферми-Дирака. Эти частицы называются фермионами. Частицы с нулевым или целочисленным спином (фотоны, π -мезоны) описываются симметричными волновыми функциями и подчиняются статистике Бозе-Эйнштейна, они называются бозонами. Сложные частицы (например атомные ядра), состоящие из нечетного числа фермионов, являются фермионами (сум-марный спин полуцелый), а из четного числа – бозонами (суммарный спин – целый ). Зависимость характера симметрии волновых функций сис-темы тождественных частиц от спина частиц обоснована В. Паули. (1900 -1958).
Симметрия или антисимметрия определяется спином час-тиц. Частицы с полуцелым спином (электроны, протоны, нейтроны) описываются антисимметричными волновы-ми функциями и подчиняются статистике Ферми-Дирака. Эти частицы называются фермионами. Частицы с нулевым или целочисленным спином (фотоны, π -мезоны) описываются симметричными волновыми функциями и подчиняются статистике Бозе-Эйнштейна, они называются бозонами. Сложные частицы (например атомные ядра), состоящие из нечетного числа фермионов, являются фермионами (сум-марный спин полуцелый), а из четного числа – бозонами (суммарный спин – целый ). Зависимость характера симметрии волновых функций сис-темы тождественных частиц от спина частиц обоснована В. Паули. (1900 -1958).
 ПРИНЦИП ПАУЛИ. РАСПРЕДЕЛЕНИЕ ЭЛЕКТРОНОВ В АТОМЕ ПО СОСТОЯНИЯМ
ПРИНЦИП ПАУЛИ. РАСПРЕДЕЛЕНИЕ ЭЛЕКТРОНОВ В АТОМЕ ПО СОСТОЯНИЯМ
 Если тождественные частицы имеют одинаковые квантовые числа, то их волновая функция симметрична относительно перестановки частиц. Значит, два одинаковых фермиона, входяхих в одну систему не могут находится в одинаковых состояниях, так как для фермионов волновая функция должна быть антисимметрична. Обобщая опытные данные, Паули сформулировал принцип: Системы фермионов встречаются в природе только в состо-яниях описываемых антисимметричными волновыми функциями. ( квантово-механическая формулировка принципа Паули ). Существует более простая формулировка принципа Паули: В системе одинаковых фермионов любые два из них не мо-гут одновременно находиться в одном и том же состоянии (число однотипных бозонов в одном и том же состоянии не ограничено).
Если тождественные частицы имеют одинаковые квантовые числа, то их волновая функция симметрична относительно перестановки частиц. Значит, два одинаковых фермиона, входяхих в одну систему не могут находится в одинаковых состояниях, так как для фермионов волновая функция должна быть антисимметрична. Обобщая опытные данные, Паули сформулировал принцип: Системы фермионов встречаются в природе только в состо-яниях описываемых антисимметричными волновыми функциями. ( квантово-механическая формулировка принципа Паули ). Существует более простая формулировка принципа Паули: В системе одинаковых фермионов любые два из них не мо-гут одновременно находиться в одном и том же состоянии (число однотипных бозонов в одном и том же состоянии не ограничено).
 Состояние электрона в атоме однозначно определяется набором четырёх квантовых чисел: • Главного • Орбитального • Магнитного • Магнитного спинового Распределение электронов в атоме подчиняется принци-пу Паули: в одном и том же атоме не может быть более одного электрона с одинаковым набором четырёх квантовых чисел то есть: Где – число электронов находящихся в кван-товом состоянии, описываемом набором четырёх квантовых чисел, и принцип Паули утверждает, что два, 3, 2, 1 nn 1, , 2, 1, 0 nll llmmll, , 2, 1, 0, 1, 2 1 , 2 1 ssmm slmmln, , , 0 или 1, , slmmln. Z, ,
Состояние электрона в атоме однозначно определяется набором четырёх квантовых чисел: • Главного • Орбитального • Магнитного • Магнитного спинового Распределение электронов в атоме подчиняется принци-пу Паули: в одном и том же атоме не может быть более одного электрона с одинаковым набором четырёх квантовых чисел то есть: Где – число электронов находящихся в кван-товом состоянии, описываемом набором четырёх квантовых чисел, и принцип Паули утверждает, что два, 3, 2, 1 nn 1, , 2, 1, 0 nll llmmll, , 2, 1, 0, 1, 2 1 , 2 1 ssmm slmmln, , , 0 или 1, , slmmln. Z, ,
 электрона, связанные в одном и том же атоме, разли-чаются значениями по крайней мере одного квантово-го числа. Данному соответствует различных состояний, отли-чающихся значениями и . Квантовое число при-нимает два значения, значит число электронов нахо-дящихся в состояниях определяемых данным главным квантовым числом: Совокупность электронов в многоэлектронном атоме, имеющих одно и то же главное квантовое число на-зывают – электронной оболочкой. В каждой из электронных оболочек электроны распреде-n 2 n llmsm 2 1 0 2122 nln. Z n l n
электрона, связанные в одном и том же атоме, разли-чаются значениями по крайней мере одного квантово-го числа. Данному соответствует различных состояний, отли-чающихся значениями и . Квантовое число при-нимает два значения, значит число электронов нахо-дящихся в состояниях определяемых данным главным квантовым числом: Совокупность электронов в многоэлектронном атоме, имеющих одно и то же главное квантовое число на-зывают – электронной оболочкой. В каждой из электронных оболочек электроны распреде-n 2 n llmsm 2 1 0 2122 nln. Z n l n
 ляются по подоболочкам соответствующих данному . Так как орбитальное квантовое число принимает зна-чения от 0 до , число подоболочек равно порядко-вому номеру оболочки . Количество электронов в подоболочке определяется магнитным и магнитным спиновым квантовыми числами, максимальное число электронов в подоболочке с данным равно . l n 1 n 122 ll
ляются по подоболочкам соответствующих данному . Так как орбитальное квантовое число принимает зна-чения от 0 до , число подоболочек равно порядко-вому номеру оболочки . Количество электронов в подоболочке определяется магнитным и магнитным спиновым квантовыми числами, максимальное число электронов в подоболочке с данным равно . l n 1 n 122 ll
 ПЕРИОДИЧЕСКАЯ СИСТЕМА ЭЛЕМЕНТОВ Д. И. МЕНДЕЛЕЕВА
ПЕРИОДИЧЕСКАЯ СИСТЕМА ЭЛЕМЕНТОВ Д. И. МЕНДЕЛЕЕВА
 Принцип Паули, лежащий в основе систематики заполне-ния электронных состояний в атомах, позволяет объяс-нить ПЕРИОДИЧЕСКУЮ СИСТЕМУ Д. И. МЕНДЕЛЕЕВА (1869) – фундаментальный закон природы. Д. И. Менделеев ввёл понятие порядкового номера хи-мического элемента Z , равному числу протонов в ядре и общему числу электронов в электронной оболочке атома. Расположив химические элементы по мере воз-растания порядковых номеров, он получил периодич-ность в изменении химических свойств элементов. Так как химические и некоторые физические свойства элементов объясняются внешними (валентными) элек- тронами в атомах, то периодичность свойств химичес-ких элементов должна быть связана с периодичностью расположения электронов в атомах. Будем считать что
Принцип Паули, лежащий в основе систематики заполне-ния электронных состояний в атомах, позволяет объяс-нить ПЕРИОДИЧЕСКУЮ СИСТЕМУ Д. И. МЕНДЕЛЕЕВА (1869) – фундаментальный закон природы. Д. И. Менделеев ввёл понятие порядкового номера хи-мического элемента Z , равному числу протонов в ядре и общему числу электронов в электронной оболочке атома. Расположив химические элементы по мере воз-растания порядковых номеров, он получил периодич-ность в изменении химических свойств элементов. Так как химические и некоторые физические свойства элементов объясняются внешними (валентными) элек- тронами в атомах, то периодичность свойств химичес-ких элементов должна быть связана с периодичностью расположения электронов в атомах. Будем считать что
 каждый следующий элемент образован из предыдуще-го прибавлением к ядру одного протона, и электрона в электронную оболочку. Взаимодействием электронов пренебрегаем. Рассмотрим атомы химических элемен-тов в основном состоянии. • Для водорода Н единственный электрон находится в состоянии 1 s , характеризуемом квантовыми числами: (ориентация спина произвольна). • Оба электрона атома гелия Н e находятся в состоянии 1 s , но с антипараллельной организацией спина. Элект-ронная конфигурация записывается как 1 s ² (2 -1 s элект-рона). На гелии заканчивается заполнение К-оболочки, что соответствует завершению I периода Периоди-ческой системы Менделеева. 21, 0, 0, 1 slmmln
каждый следующий элемент образован из предыдуще-го прибавлением к ядру одного протона, и электрона в электронную оболочку. Взаимодействием электронов пренебрегаем. Рассмотрим атомы химических элемен-тов в основном состоянии. • Для водорода Н единственный электрон находится в состоянии 1 s , характеризуемом квантовыми числами: (ориентация спина произвольна). • Оба электрона атома гелия Н e находятся в состоянии 1 s , но с антипараллельной организацией спина. Элект-ронная конфигурация записывается как 1 s ² (2 -1 s элект-рона). На гелии заканчивается заполнение К-оболочки, что соответствует завершению I периода Периоди-ческой системы Менделеева. 21, 0, 0, 1 slmmln
 • Третий электрон атома лития Li ( Z=3) , согласно принци-пу Паули уже не может разместиться в целиком запол-неной К-оболочке и занимает наинизшее энергетиче-ское состояние с ( L -оболочка), то есть 2 s состоя-ние. Электронная конфигурация для атома лития 1 s ² 2 s. Атомом лития открывается второй периоди-ческой системы Менделеева. Четвертым электроном бериллия Ве ( Z=4) заканчивается заполнение оболочки 2 s и так далее… Таким образом, открытая Менделеевым периодичность в химических свойствах элементов объясняется повто-ряемостью в структуре внешних оболочек у атомов родственных элементов. 2 n
• Третий электрон атома лития Li ( Z=3) , согласно принци-пу Паули уже не может разместиться в целиком запол-неной К-оболочке и занимает наинизшее энергетиче-ское состояние с ( L -оболочка), то есть 2 s состоя-ние. Электронная конфигурация для атома лития 1 s ² 2 s. Атомом лития открывается второй периоди-ческой системы Менделеева. Четвертым электроном бериллия Ве ( Z=4) заканчивается заполнение оболочки 2 s и так далее… Таким образом, открытая Менделеевым периодичность в химических свойствах элементов объясняется повто-ряемостью в структуре внешних оболочек у атомов родственных элементов. 2 n

