Lektsii_ISKN-11-12-13-2014-gom_k-z_2.pptx
- Количество слайдов: 28
 Лекции 11 -12 Иткулова Ш. С. ГОМОГЕННЫЕ КАТАЛИТИЧЕСКИЕ ПРОЦЕССЫ 1. Общие сведения о гомогенном катализе 2. Классификация гомогенно-каталитических реакций 3. Промежуточные соединения в гомогенных каталитических процессах. Роль образования промежуточных соединений. 4. Уравнение кинетики гомогенно-каталитических реакций 5. Гомогенные катализаторы 6. Механизм ГКР 7. Применение гомогенного катализа в отраслях нефтехимической технологии (самостоятельно).
Лекции 11 -12 Иткулова Ш. С. ГОМОГЕННЫЕ КАТАЛИТИЧЕСКИЕ ПРОЦЕССЫ 1. Общие сведения о гомогенном катализе 2. Классификация гомогенно-каталитических реакций 3. Промежуточные соединения в гомогенных каталитических процессах. Роль образования промежуточных соединений. 4. Уравнение кинетики гомогенно-каталитических реакций 5. Гомогенные катализаторы 6. Механизм ГКР 7. Применение гомогенного катализа в отраслях нефтехимической технологии (самостоятельно).
 ГОМОГЕННЫЙ КАТАЛИЗ, ускорение химической реакции в присутствии катализатора, который находится в одной фазе с исходными реагентами (субстратами) в газовой фазе или растворе. При гомогенном катализе, как и при гетерогенном катализе, катализатор в реакции не расходуется, однако является ее необходимым участником; без катализатора реакция протекает гораздо медленнее или не идет вовсе. Т. о. гомогенный катализ характеризуется тем, что реакционная смесь и катализатор находятся в одном агрегатном состоянии: в жидком или в газообразном. Примером газофазной гомогенной каталитической реакции является окисление оксида серы (IV) кислородом в присутствии оксида азота (VI). Гомогенные каталитические процессы в газовой фазе встречаются относительно редко, так как лишь немногие вещества, обладающие каталитическими свойствами, могут быть переведены в газообразное состояние при условиях, когда не разрушались бы молекулы реагирующих веществ. Жидкофазные гомогенные каталитические процессы осуществляют обычно в реакторах с различного рода перемешивающими устройствами.
ГОМОГЕННЫЙ КАТАЛИЗ, ускорение химической реакции в присутствии катализатора, который находится в одной фазе с исходными реагентами (субстратами) в газовой фазе или растворе. При гомогенном катализе, как и при гетерогенном катализе, катализатор в реакции не расходуется, однако является ее необходимым участником; без катализатора реакция протекает гораздо медленнее или не идет вовсе. Т. о. гомогенный катализ характеризуется тем, что реакционная смесь и катализатор находятся в одном агрегатном состоянии: в жидком или в газообразном. Примером газофазной гомогенной каталитической реакции является окисление оксида серы (IV) кислородом в присутствии оксида азота (VI). Гомогенные каталитические процессы в газовой фазе встречаются относительно редко, так как лишь немногие вещества, обладающие каталитическими свойствами, могут быть переведены в газообразное состояние при условиях, когда не разрушались бы молекулы реагирующих веществ. Жидкофазные гомогенные каталитические процессы осуществляют обычно в реакторах с различного рода перемешивающими устройствами.
 Классификация гомогенно-каталитических реакций - Процессы гомогенного катализа классифицируются по типам взаимодействия, фазовому состоянию системы и механизму катализа. По фазовому состоянию гомогенные каталитические процессы делят на: жидкофазные ( в растворах) и газофазные. По механизму катализа различают: ионные, радикальные и молекулярные каталитические реакции. Процессы гомогенного катализа классифицируются по типу взаимодействия между реагирующими веществами и катализатором на: -окислительно-восстановительное и - кислотно-основное взаимодействие.
Классификация гомогенно-каталитических реакций - Процессы гомогенного катализа классифицируются по типам взаимодействия, фазовому состоянию системы и механизму катализа. По фазовому состоянию гомогенные каталитические процессы делят на: жидкофазные ( в растворах) и газофазные. По механизму катализа различают: ионные, радикальные и молекулярные каталитические реакции. Процессы гомогенного катализа классифицируются по типу взаимодействия между реагирующими веществами и катализатором на: -окислительно-восстановительное и - кислотно-основное взаимодействие.
 ГОМОГЕННЫЕ КАТАЛИТИЧЕСКИЕ ПРОЦЕССЫ. - - - имеют ряд преимуществ перед традиционными гетерогенными: высокую общую активность и низкие температуры и, как следствие, высокую селективность и др. Однако они имеют и ряд существенных недостатков. Прежде всего, как правило, они не технологичны. Это объясняется тем, что осуществление таких процессов требует введения в технологический процесс сложной стадии отделения катализатора от реагентов и продуктов, что увеличивает трудоемкость, металлоемкость и затрудняет создание непрерывного процесса. Большие трудности возникают при регенерации, например, металлокомплексных катализаторов, тогда как регенерация традиционных гетерогенных катализаторов обычно сводится к выжиганию смолообразных продуктов в токе воздуха. Кроме того, гомогенные металлокомплексные катализаторы не могут быть применены для реакций, которые по требованиям термодинамики должны проводиться при высоких температурах. Верхняя температурная граница применения гомогенных катализаторов определяется прежде всего температурой кипения растворителей и температурой разрушения комплексов.
ГОМОГЕННЫЕ КАТАЛИТИЧЕСКИЕ ПРОЦЕССЫ. - - - имеют ряд преимуществ перед традиционными гетерогенными: высокую общую активность и низкие температуры и, как следствие, высокую селективность и др. Однако они имеют и ряд существенных недостатков. Прежде всего, как правило, они не технологичны. Это объясняется тем, что осуществление таких процессов требует введения в технологический процесс сложной стадии отделения катализатора от реагентов и продуктов, что увеличивает трудоемкость, металлоемкость и затрудняет создание непрерывного процесса. Большие трудности возникают при регенерации, например, металлокомплексных катализаторов, тогда как регенерация традиционных гетерогенных катализаторов обычно сводится к выжиганию смолообразных продуктов в токе воздуха. Кроме того, гомогенные металлокомплексные катализаторы не могут быть применены для реакций, которые по требованиям термодинамики должны проводиться при высоких температурах. Верхняя температурная граница применения гомогенных катализаторов определяется прежде всего температурой кипения растворителей и температурой разрушения комплексов.
 Скорость гомогенного каталитического процесса - зависит от ряда факторов: концентрации реагирующих веществ, концентрации катализатора, температуры, давления, интенсивности перемешивания. Зависимость скорости процесса от концентрации реагентов и катализатора определяется прежде всего соотношением скоростей элементарных стадий каталитического акта и условиями их равновесия.
Скорость гомогенного каталитического процесса - зависит от ряда факторов: концентрации реагирующих веществ, концентрации катализатора, температуры, давления, интенсивности перемешивания. Зависимость скорости процесса от концентрации реагентов и катализатора определяется прежде всего соотношением скоростей элементарных стадий каталитического акта и условиями их равновесия.
 Активные столкновения Энергетическая диаграмма химической реакции. Eисх – средняя энергия частиц исходных веществ, Eпрод – средняя энергия частиц продуктов реакции • Очевидно, что взаимодействие частиц осуществляется при их столкновениях; однако число столкновений молекул очень велико и, если бы каждое столкновение приводило к химическому взаимодействию частиц, все реакции протекали бы практически мгновенно. • С. Аррениус постулировал, что столкновения молекул будут эффективны (т. е. будут приводить к реакции) только в том случае, если сталкивающиеся молекулы обладают некоторым запасом энергии – энергией активации.
Активные столкновения Энергетическая диаграмма химической реакции. Eисх – средняя энергия частиц исходных веществ, Eпрод – средняя энергия частиц продуктов реакции • Очевидно, что взаимодействие частиц осуществляется при их столкновениях; однако число столкновений молекул очень велико и, если бы каждое столкновение приводило к химическому взаимодействию частиц, все реакции протекали бы практически мгновенно. • С. Аррениус постулировал, что столкновения молекул будут эффективны (т. е. будут приводить к реакции) только в том случае, если сталкивающиеся молекулы обладают некоторым запасом энергии – энергией активации.
 Образование активированного комплекса Рассмотрим путь некоторой элементарной реакции А + В ––> С Поскольку химическое взаимодействие частиц связано с разрывом старых химических связей и образованием новых, считается, что всякая элементарная реакция проходит через образование некоторого неустойчивого промежуточного соединения, называемого активированным комплексом: А ––> K# ––> B Образование активированного комплекса всегда требует затраты некоторого количества энергии, что вызвано, во-первых, отталкиванием электронных оболочек и атомных ядер при сближении частиц и, во-вторых, необходимостью построения определенной пространственной конфигурации атомов в активированном комплексе и перераспределения электронной плотности. Таким образом, по пути из начального состояния в конечное система должна преодолеть своего рода энергетический барьер. Энергия активации реакции приближённо равна превышению средней энергии активированного комплекса над средним уровнем энергии реагентов. Очевидно, что если прямая реакция является экзотермической, то энергия активации обратной реакции Е'А выше, нежели энергия активации прямой реакции EA. Энергии активации прямой и обратной реакции связаны друг с другом через изменение внутренней энергии в ходе реакции.
Образование активированного комплекса Рассмотрим путь некоторой элементарной реакции А + В ––> С Поскольку химическое взаимодействие частиц связано с разрывом старых химических связей и образованием новых, считается, что всякая элементарная реакция проходит через образование некоторого неустойчивого промежуточного соединения, называемого активированным комплексом: А ––> K# ––> B Образование активированного комплекса всегда требует затраты некоторого количества энергии, что вызвано, во-первых, отталкиванием электронных оболочек и атомных ядер при сближении частиц и, во-вторых, необходимостью построения определенной пространственной конфигурации атомов в активированном комплексе и перераспределения электронной плотности. Таким образом, по пути из начального состояния в конечное система должна преодолеть своего рода энергетический барьер. Энергия активации реакции приближённо равна превышению средней энергии активированного комплекса над средним уровнем энергии реагентов. Очевидно, что если прямая реакция является экзотермической, то энергия активации обратной реакции Е'А выше, нежели энергия активации прямой реакции EA. Энергии активации прямой и обратной реакции связаны друг с другом через изменение внутренней энергии в ходе реакции.
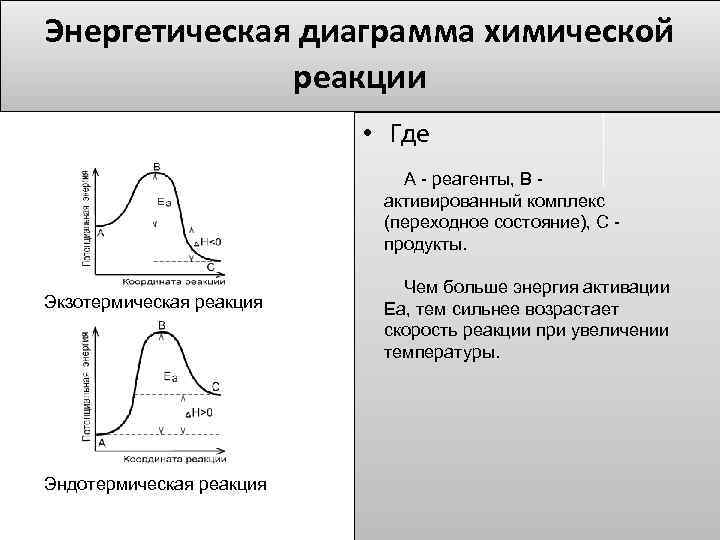 Энергетическая диаграмма химической реакции • Где А - реагенты, В активированный комплекс (переходное состояние), С продукты. Экзотермическая реакция Эндотермическая реакция Чем больше энергия активации Ea, тем сильнее возрастает скорость реакции при увеличении температуры.
Энергетическая диаграмма химической реакции • Где А - реагенты, В активированный комплекс (переходное состояние), С продукты. Экзотермическая реакция Эндотермическая реакция Чем больше энергия активации Ea, тем сильнее возрастает скорость реакции при увеличении температуры.
![. Энергия активации (Е, [Дж/моль]) - это минимальная энергия, которой должны обладать реагирующие частицы, . Энергия активации (Е, [Дж/моль]) - это минимальная энергия, которой должны обладать реагирующие частицы,](https://present5.com/presentation/164262399_378597841/image-9.jpg) . Энергия активации (Е, [Дж/моль]) - это минимальная энергия, которой должны обладать реагирующие частицы, чтобы столкновения между ними приводили к химическому взаимодействию. Зависимость k скорости реакции и Е отражает уравнение Аррениуса: k = A • e –Ea/RT где A - постоянная, зависящая от природы реагирующих веществ; R - универсальная газовая постоянная [8, 314 Дж/(моль • К) = 0, 082 л • атм/(моль • К)]; Ea - энергия активации, т. е. энергия, которой должны обладать сталкивающиеся молекулы, чтобы столкновение привело к химическому превращению. lg k = lg. A - E/2, 3 · R · T, где А - константа Аррениуса, характеризующая конкретную реакцию. Находится графическим методом зависимости lg k= f (1/T). tg угла наклона к оси абсцисс дает величину Е/2, 3 · R · T.
. Энергия активации (Е, [Дж/моль]) - это минимальная энергия, которой должны обладать реагирующие частицы, чтобы столкновения между ними приводили к химическому взаимодействию. Зависимость k скорости реакции и Е отражает уравнение Аррениуса: k = A • e –Ea/RT где A - постоянная, зависящая от природы реагирующих веществ; R - универсальная газовая постоянная [8, 314 Дж/(моль • К) = 0, 082 л • атм/(моль • К)]; Ea - энергия активации, т. е. энергия, которой должны обладать сталкивающиеся молекулы, чтобы столкновение привело к химическому превращению. lg k = lg. A - E/2, 3 · R · T, где А - константа Аррениуса, характеризующая конкретную реакцию. Находится графическим методом зависимости lg k= f (1/T). tg угла наклона к оси абсцисс дает величину Е/2, 3 · R · T.
 Механизм гомогенного катализа • Энергия активации гомогенных каталитических процессов обычно больше энергии активации гетерогенных каталитических процессов. • Одно из первых теоретических объяснений механизма катализа было изложено в трудах Оствальда в 1894 - 1911 гг. Исходное положение этой теории - предположение, что в течение реакции образуются неустойчивые промежуточные соединения катализатора с реагирующими веществами, которые затем распадаются с образованием продуктов реакции, а катализатор регенерируется. • Механизм гомогенного катализа состоит в образовании между реагентами и катализаторами нестойких промежуточных соединений, существующих в той же фазе ( газ или раствор), после распада которых катализатор регенерируется.
Механизм гомогенного катализа • Энергия активации гомогенных каталитических процессов обычно больше энергии активации гетерогенных каталитических процессов. • Одно из первых теоретических объяснений механизма катализа было изложено в трудах Оствальда в 1894 - 1911 гг. Исходное положение этой теории - предположение, что в течение реакции образуются неустойчивые промежуточные соединения катализатора с реагирующими веществами, которые затем распадаются с образованием продуктов реакции, а катализатор регенерируется. • Механизм гомогенного катализа состоит в образовании между реагентами и катализаторами нестойких промежуточных соединений, существующих в той же фазе ( газ или раствор), после распада которых катализатор регенерируется.
 Ход любой реакции можно представить схемой: Исходные реагенты Промежуточные вещества (переходное состояние) Продукты реакции
Ход любой реакции можно представить схемой: Исходные реагенты Промежуточные вещества (переходное состояние) Продукты реакции
 ПРЕДСТАВЛЕНИЕ ОБ ОБРАЗОВАНИИ НЕУСТОЙЧИВЫХ ПРОМЕЖУТОЧНЫХ СОЕДИНЕНИЙ КАТАЛИЗАТОРА С РЕАГИРУЮЩИМИ ВЕЩЕСТВАМИ - является основным положением теории каталитических процессов. Для описания механизма протекания каталитических реакций в настоящее время используют две концепции. Одна из них соответствует слитной (одностадийной) схеме катализа, другая – стадийной (раздельной) схеме катализа. Согласно слитной теории катализа, некаталитическая реакция типа А+В=Р В присутствии катализатора К проходит по схеме А + В + К (АВК) ¹ Р+К здесь (АВК) ¹ -активированный комплекс исходных веществ и катализатора. Этот процесс в присутствии катализатора проходит в одну стадию и его скорость описывается кинетическим уравнением: r = k СА СВ СК В присутствии катализатора процесс идет с меньшей энергией активации.
ПРЕДСТАВЛЕНИЕ ОБ ОБРАЗОВАНИИ НЕУСТОЙЧИВЫХ ПРОМЕЖУТОЧНЫХ СОЕДИНЕНИЙ КАТАЛИЗАТОРА С РЕАГИРУЮЩИМИ ВЕЩЕСТВАМИ - является основным положением теории каталитических процессов. Для описания механизма протекания каталитических реакций в настоящее время используют две концепции. Одна из них соответствует слитной (одностадийной) схеме катализа, другая – стадийной (раздельной) схеме катализа. Согласно слитной теории катализа, некаталитическая реакция типа А+В=Р В присутствии катализатора К проходит по схеме А + В + К (АВК) ¹ Р+К здесь (АВК) ¹ -активированный комплекс исходных веществ и катализатора. Этот процесс в присутствии катализатора проходит в одну стадию и его скорость описывается кинетическим уравнением: r = k СА СВ СК В присутствии катализатора процесс идет с меньшей энергией активации.
 Стадийная схема протекания КР Чаще протекают каталитические реакции, осуществляемые по стадийной схеме. В соответствии с этой схемой вещества-реагенты последовательно взаимодействуют, образуя на каждой стадии соответствующий активированный комплекс: • • • 1) А + К <--> (АК) ->АК 2)АК + В <--> (АКВ) -> Р + К Согласно записанным уравнениям, промежуточное соединение АК может превратиться по обратной реакции с константой скорости k— 1 в исходное вещество и катализатор или в продукты реакции Р и катализатор по второй реакции (константа скорости k 2. Каталитические реакции протекают по слитной и стадийной схемам, обычно в разных температурных интервалах. По слитной схеме часто осуществляются гомогенные каталитические реакции при температурах 300… 400 К и ферментативные реакции. По стадийной схеме протекают, как правило гетерогенные каталитические реакции при температурах 600… 800 К. Обе приведенные схемы отражают общую и характерную особенность механизма протекания каталитических реакций, а именно цикличность. В каталитических реакциях один и тот же активный центр или молекула катализатора может многократно (103 -1011 раз) вступать в химическое взаимодействие с молекулами реагента.
Стадийная схема протекания КР Чаще протекают каталитические реакции, осуществляемые по стадийной схеме. В соответствии с этой схемой вещества-реагенты последовательно взаимодействуют, образуя на каждой стадии соответствующий активированный комплекс: • • • 1) А + К <--> (АК) ->АК 2)АК + В <--> (АКВ) -> Р + К Согласно записанным уравнениям, промежуточное соединение АК может превратиться по обратной реакции с константой скорости k— 1 в исходное вещество и катализатор или в продукты реакции Р и катализатор по второй реакции (константа скорости k 2. Каталитические реакции протекают по слитной и стадийной схемам, обычно в разных температурных интервалах. По слитной схеме часто осуществляются гомогенные каталитические реакции при температурах 300… 400 К и ферментативные реакции. По стадийной схеме протекают, как правило гетерогенные каталитические реакции при температурах 600… 800 К. Обе приведенные схемы отражают общую и характерную особенность механизма протекания каталитических реакций, а именно цикличность. В каталитических реакциях один и тот же активный центр или молекула катализатора может многократно (103 -1011 раз) вступать в химическое взаимодействие с молекулами реагента.
 ПРОМЕЖУТОЧНЫЕ СОЕДИНЕНИЯ ПРИ ГОМОГЕННЫЕХ КАТАЛИТИЧЕСКИХ РЕАКЦИЯХ В случае гомогенно-каталитических процессов катализатор образует с реагентами промежуточные реакционноспособные продукты. Рассмотрим некоторую реакцию А + В ––> С В присутствии катализатора осуществляются две быстро протекающие стадии, в результате которых образуются частицы промежуточного соединения АК и затем (через активированный комплекс АВК#) конечный продукт реакции с регенерацией катализатора: А + К ––> АК АК + В ––> С + К Примером такого процесса может служить реакция разложения ацетальдегида, энергия активации которой EA = 190 к. Дж/моль: СН 3 СНО ––> СН 4 + СО
ПРОМЕЖУТОЧНЫЕ СОЕДИНЕНИЯ ПРИ ГОМОГЕННЫЕХ КАТАЛИТИЧЕСКИХ РЕАКЦИЯХ В случае гомогенно-каталитических процессов катализатор образует с реагентами промежуточные реакционноспособные продукты. Рассмотрим некоторую реакцию А + В ––> С В присутствии катализатора осуществляются две быстро протекающие стадии, в результате которых образуются частицы промежуточного соединения АК и затем (через активированный комплекс АВК#) конечный продукт реакции с регенерацией катализатора: А + К ––> АК АК + В ––> С + К Примером такого процесса может служить реакция разложения ацетальдегида, энергия активации которой EA = 190 к. Дж/моль: СН 3 СНО ––> СН 4 + СО
 ПРОМЕЖУТОЧНЫЕ СОЕДИНЕНИЯ ПРИ ГОМОГЕННЫЕХ КАТАЛИТИЧЕСКИХ РЕАКЦИЯХ В присутствии паров йода этот процесс протекает в две стадии: СН 3 СНО + I 2 ––> СН 3 I + НI + СО СН 3 I + НI ––> СН 4 + I 2 Уменьшение энергии активации этой реакции в присутствии катализатора составляет 54 к. Дж/моль; константа скорости реакции при этом увеличивается приблизительно в 105 раз. Наиболее распространенным типом гомогенного катализа является кислотный катализ, при котором в роли катализатора выступают ионы водорода Н+.
ПРОМЕЖУТОЧНЫЕ СОЕДИНЕНИЯ ПРИ ГОМОГЕННЫЕХ КАТАЛИТИЧЕСКИХ РЕАКЦИЯХ В присутствии паров йода этот процесс протекает в две стадии: СН 3 СНО + I 2 ––> СН 3 I + НI + СО СН 3 I + НI ––> СН 4 + I 2 Уменьшение энергии активации этой реакции в присутствии катализатора составляет 54 к. Дж/моль; константа скорости реакции при этом увеличивается приблизительно в 105 раз. Наиболее распространенным типом гомогенного катализа является кислотный катализ, при котором в роли катализатора выступают ионы водорода Н+.
 Сущность механизма действия катализатора при гомогенном катализе заключается в образовании промежуточного реакционноспособного соединения. Механизм объясняют теорией активированной адсорбции. Адсорбция – свойство вещества поглощать на поверхности других веществ. В результате адсорбции реагентов на поверхности катализатора концентрация компонентов акта столкновения молекул увеличивается, что повышает скорость химической реакции. При адсорбировании реагентов на поверхности катализаторов происходит ослабление связей в молекулах реагирующих веществ, что приводит к повышению их активности. Процесс протекает в несколько стадий, а промежуточными в этом случае являются поверхностные соединения. I стадия: А + К = АК, II стадия: АК + В = К + С. Е – энергия активации без участия катализатора; Е 1 – энергия активации при образовании промежуточного соединения; Е 2 – энергия активации при разложении промежуточного соединения. Е 1 + Е 2 < E. Таким образом, при участии катализатора в химической реакции энергия активации уменьшается.
Сущность механизма действия катализатора при гомогенном катализе заключается в образовании промежуточного реакционноспособного соединения. Механизм объясняют теорией активированной адсорбции. Адсорбция – свойство вещества поглощать на поверхности других веществ. В результате адсорбции реагентов на поверхности катализатора концентрация компонентов акта столкновения молекул увеличивается, что повышает скорость химической реакции. При адсорбировании реагентов на поверхности катализаторов происходит ослабление связей в молекулах реагирующих веществ, что приводит к повышению их активности. Процесс протекает в несколько стадий, а промежуточными в этом случае являются поверхностные соединения. I стадия: А + К = АК, II стадия: АК + В = К + С. Е – энергия активации без участия катализатора; Е 1 – энергия активации при образовании промежуточного соединения; Е 2 – энергия активации при разложении промежуточного соединения. Е 1 + Е 2 < E. Таким образом, при участии катализатора в химической реакции энергия активации уменьшается.
 Теория гомогенного катализа может быть сформулирована в виде следующих основных положений: 1) катализ осуществляется путем образования неустойчивого активированного комплекса (промежуточного соединения) реагирующего вещества и катализатора; 2) образование промежуточного соединения является обратимым и относительно быстрым процессом; 3) разложение промежуточного соединения с образованием продуктов реакции и восстановлением катализатора происходит относительно медленно, поэтому общая скорость процесса пропорциональна концентрации промежуточного соединения. Например, А + В → С. Без Kt: А + В → АВ* → С С Kt: А + Kt → АKt Аkt + В → (АВ*)Kt → С + Kt
Теория гомогенного катализа может быть сформулирована в виде следующих основных положений: 1) катализ осуществляется путем образования неустойчивого активированного комплекса (промежуточного соединения) реагирующего вещества и катализатора; 2) образование промежуточного соединения является обратимым и относительно быстрым процессом; 3) разложение промежуточного соединения с образованием продуктов реакции и восстановлением катализатора происходит относительно медленно, поэтому общая скорость процесса пропорциональна концентрации промежуточного соединения. Например, А + В → С. Без Kt: А + В → АВ* → С С Kt: А + Kt → АKt Аkt + В → (АВ*)Kt → С + Kt
 . ГОМОГЕННЫЕ КАТАЛИТИЧЕСКИЕ ПРОЦЕССЫ • Как правило, гомогенные каталитические процессы протекают в гораздо более мягких условиях, чем гетерогенные. В ряде случаев координационные соединения позволяют проводить процесс весьма избирательно и стереоселективно. • Во многих случаях гомогенные каталитические процессы состоят из сложной последовательности элементарных стадий и имеют непростой порядок. Кроме того, на характер кинетической кривой сильно влияют два основных фактора - наличие индукционного периода.
. ГОМОГЕННЫЕ КАТАЛИТИЧЕСКИЕ ПРОЦЕССЫ • Как правило, гомогенные каталитические процессы протекают в гораздо более мягких условиях, чем гетерогенные. В ряде случаев координационные соединения позволяют проводить процесс весьма избирательно и стереоселективно. • Во многих случаях гомогенные каталитические процессы состоят из сложной последовательности элементарных стадий и имеют непростой порядок. Кроме того, на характер кинетической кривой сильно влияют два основных фактора - наличие индукционного периода.
 ГОМОГЕННЫЕ КАТАЛИТИЧЕСКИЕ ПРОЦЕССЫ Примером гомогенного катализа является разложение пероксида водорода в присутствии ионов йода. Реакция протекает в две стадии: Н О + I = H O + IO Н O + IO = Н O + I При гомогенном катализе действие катализатора связано с тем, что он вступает во взаимодействие с реагирующими веществами с образованием промежуточных соединений, это приводит к снижению энергии активации.
ГОМОГЕННЫЕ КАТАЛИТИЧЕСКИЕ ПРОЦЕССЫ Примером гомогенного катализа является разложение пероксида водорода в присутствии ионов йода. Реакция протекает в две стадии: Н О + I = H O + IO Н O + IO = Н O + I При гомогенном катализе действие катализатора связано с тем, что он вступает во взаимодействие с реагирующими веществами с образованием промежуточных соединений, это приводит к снижению энергии активации.
 . ГОМОГЕННЫЕ КАТАЛИТИЧЕСКИЕ ПРОЦЕССЫ • Одной из наиболее интересных каталитических реакций является так называемая оксореакция. Оксореакция состоит в каталитическом присоединении окиси углерода и водорода к олефинам с первоначальным образованием альдегидов, обладающих на один углеродный атом больше, чем исходный олефин. Эта реакция гидроформилирования была открыта во время второй мировой войны Реленом и его сотрудниками в Германии. Несмотря на то, что указанные авторы применили твердый кобальто-ториевый катализатор Фишера - Тропша, для них стало ясно, что эта реакция является гомогенным каталитическим процессом.
. ГОМОГЕННЫЕ КАТАЛИТИЧЕСКИЕ ПРОЦЕССЫ • Одной из наиболее интересных каталитических реакций является так называемая оксореакция. Оксореакция состоит в каталитическом присоединении окиси углерода и водорода к олефинам с первоначальным образованием альдегидов, обладающих на один углеродный атом больше, чем исходный олефин. Эта реакция гидроформилирования была открыта во время второй мировой войны Реленом и его сотрудниками в Германии. Несмотря на то, что указанные авторы применили твердый кобальто-ториевый катализатор Фишера - Тропша, для них стало ясно, что эта реакция является гомогенным каталитическим процессом.
 . ГОМОГЕННЫЕ КАТАЛИТИЧЕСКИЕ ПРОЦЕССЫ • Гидроформилирование представляет собой гомогенный каталитический процесс, действительный механизм которого до сего времени точно не установлен. В противном случае трудно было бы объяснить замедление реакции при повышении парциального давления окиси углерода. Предложенные механизмы различаются предполагаемым типом карбонильных соединений, участвующих в реакции, и объяснением роли окиси углерода. Из сказанного следует, что скорость гомогенного каталитического процесса будет зависеть от скорости образования и разложения промежуточного соединения. Эти положения в общем справедливы для гомогенных каталитических процессов. • На практике при изучении кинетики реакций приходится встречаться с различными отклонениями от них, что обусловлено особенностями конкретных реакций.
. ГОМОГЕННЫЕ КАТАЛИТИЧЕСКИЕ ПРОЦЕССЫ • Гидроформилирование представляет собой гомогенный каталитический процесс, действительный механизм которого до сего времени точно не установлен. В противном случае трудно было бы объяснить замедление реакции при повышении парциального давления окиси углерода. Предложенные механизмы различаются предполагаемым типом карбонильных соединений, участвующих в реакции, и объяснением роли окиси углерода. Из сказанного следует, что скорость гомогенного каталитического процесса будет зависеть от скорости образования и разложения промежуточного соединения. Эти положения в общем справедливы для гомогенных каталитических процессов. • На практике при изучении кинетики реакций приходится встречаться с различными отклонениями от них, что обусловлено особенностями конкретных реакций.
 Окисление SO 2 в SO 3 с участием NO Например, SO 2 + ½ O 2 = SO 3 ; NO + ½ O 2 = NO 2 С + B = СB ; K + B = KB медленная реакция промежуточное соединение SO 2 + NO 2 = SO 3 + NO С + KB = СB + K быстро протекающая реакция
Окисление SO 2 в SO 3 с участием NO Например, SO 2 + ½ O 2 = SO 3 ; NO + ½ O 2 = NO 2 С + B = СB ; K + B = KB медленная реакция промежуточное соединение SO 2 + NO 2 = SO 3 + NO С + KB = СB + K быстро протекающая реакция
 . ГОМОГЕННЫЕ КАТАЛИТИЧЕСКИЕ ПРОЦЕССЫ • Синтез серной кислоты с помощью окислов азота - гомогенный каталитический процесс; серная кислота образуется преимущественно в жидкой фазе в результате взаимодействия растворенных двуокиси серы и трехокиси азота. Часть двуокиси серы окисляется в газовой фазе. В настоящее время серную кислоту получают двумя способами: башенным, или нитрозным, и контактным. В первом случае в реакции участвуют двуокись серы, окислы азота, кислород воздуха и вода. Здесь окислы азота являются катализатором и служат как бы передатчиком кислорода иоздуха сернистому газу.
. ГОМОГЕННЫЕ КАТАЛИТИЧЕСКИЕ ПРОЦЕССЫ • Синтез серной кислоты с помощью окислов азота - гомогенный каталитический процесс; серная кислота образуется преимущественно в жидкой фазе в результате взаимодействия растворенных двуокиси серы и трехокиси азота. Часть двуокиси серы окисляется в газовой фазе. В настоящее время серную кислоту получают двумя способами: башенным, или нитрозным, и контактным. В первом случае в реакции участвуют двуокись серы, окислы азота, кислород воздуха и вода. Здесь окислы азота являются катализатором и служат как бы передатчиком кислорода иоздуха сернистому газу.
 Роль растворителя • С другой стороны, практически в любом гомогенном каталитическом процессе мы сталкиваемся с тем, что молекулы растворителя принимают непосредственное участие в отдельных стадиях каталитической реакции. Это обусловлено тем, что первой стадией металлокомплексного катализа является образование комплекса с молекулой реагента. • Если все координационные места в комплексе заняты лигандами, прочно связанными с центральным атомом, то такая стадия весьма затруднена. • Поэтому практически в любом каталитическом процессе катализатор должен иметь свободное координационное место, которое в отсутствие реагентов занимает молекула растворителя. • Учет молекул растворителя в первой координационной сфере, с точки зрения квантовохимического расчета сводится просто к учету дополнительных лигандов и не доставляет
Роль растворителя • С другой стороны, практически в любом гомогенном каталитическом процессе мы сталкиваемся с тем, что молекулы растворителя принимают непосредственное участие в отдельных стадиях каталитической реакции. Это обусловлено тем, что первой стадией металлокомплексного катализа является образование комплекса с молекулой реагента. • Если все координационные места в комплексе заняты лигандами, прочно связанными с центральным атомом, то такая стадия весьма затруднена. • Поэтому практически в любом каталитическом процессе катализатор должен иметь свободное координационное место, которое в отсутствие реагентов занимает молекула растворителя. • Учет молекул растворителя в первой координационной сфере, с точки зрения квантовохимического расчета сводится просто к учету дополнительных лигандов и не доставляет
 ГОМОГЕННЫЕ КАТАЛИТИЧЕСКИЕ ПРОЦЕССЫ Соли металлов часто применяются при проведении некоторых гомогенных каталитических процессов, при этом важным условием является растворимость катализатора в реакционной среде. Этому требованию для определенных реагентоврастворителей отвечают соли органических кислот, в частности, жирных и нафтеновых. В полярных растворителях эти соли при растворении диссоциируют на ионы, в неполярных растворителях диссоциация не происходит.
ГОМОГЕННЫЕ КАТАЛИТИЧЕСКИЕ ПРОЦЕССЫ Соли металлов часто применяются при проведении некоторых гомогенных каталитических процессов, при этом важным условием является растворимость катализатора в реакционной среде. Этому требованию для определенных реагентоврастворителей отвечают соли органических кислот, в частности, жирных и нафтеновых. В полярных растворителях эти соли при растворении диссоциируют на ионы, в неполярных растворителях диссоциация не происходит.
 ПРАКТИЧЕСКОЕ ПРИМЕНЕНИЕ ГОМОГЕННЫХ КАТАЛИТИЧЕСКИХ ПРОЦЕССОВ Гомогенный катализ используют для промышленного получения: - спиртов-гидратацией олефинов в присут. к-т (H 2 SO 4, H 3 PO 4); - нитробензола и др. нитросоединений-нитрованием ароматич. соед. в присут. H 2 SO 4; - уксусной к-ты-карбонилированиемметанола в присут. комплексов Rh (сокатализатор-HI); - терефталевой к-ты-окислением п-ксилола в присут. солей Со; альдегидов - гидроформилированиемолефинов в присут. карбонилов Со; - лекарств, напр. L-ДОФА, -энантиоселективнымгидрированием аминокислоты в присут. комплекса Rh с хиральными лигандамии др. - Многие р-ции с участием металлокомплексных соед. по высокой региои стереоселективности приближаются к реакциям ферментативного катализа. Использование принципов действия ферментов позволяет разрабатывать принципиально новые гомогенно-каталитические процессы.
ПРАКТИЧЕСКОЕ ПРИМЕНЕНИЕ ГОМОГЕННЫХ КАТАЛИТИЧЕСКИХ ПРОЦЕССОВ Гомогенный катализ используют для промышленного получения: - спиртов-гидратацией олефинов в присут. к-т (H 2 SO 4, H 3 PO 4); - нитробензола и др. нитросоединений-нитрованием ароматич. соед. в присут. H 2 SO 4; - уксусной к-ты-карбонилированиемметанола в присут. комплексов Rh (сокатализатор-HI); - терефталевой к-ты-окислением п-ксилола в присут. солей Со; альдегидов - гидроформилированиемолефинов в присут. карбонилов Со; - лекарств, напр. L-ДОФА, -энантиоселективнымгидрированием аминокислоты в присут. комплекса Rh с хиральными лигандамии др. - Многие р-ции с участием металлокомплексных соед. по высокой региои стереоселективности приближаются к реакциям ферментативного катализа. Использование принципов действия ферментов позволяет разрабатывать принципиально новые гомогенно-каталитические процессы.
 Стереоэлектронные эффекты • Стереоэлектронные эффекты, обычно наблюдаемые во многих реакциях циклоприсоединения с участием органических ненасыщенных соединений, по-видимому, оказывают большое влияние на стереоселективность некоторых гомогенных каталитических процессов.
Стереоэлектронные эффекты • Стереоэлектронные эффекты, обычно наблюдаемые во многих реакциях циклоприсоединения с участием органических ненасыщенных соединений, по-видимому, оказывают большое влияние на стереоселективность некоторых гомогенных каталитических процессов.
 ГОМОГЕННЫЕ КАТАЛИТИЧЕСКИЕ ПРОЦЕССЫ Под термином абсолютный асимметрический синтез обычно понимают возникновение оптически активных продуктов без использования каких -либо хиральных агентов, имеющих происхождение, связанное с живой природой. Согласно этому определению асимметрическое каталитическое разложение метилэтилмалоната на хиральной поверхности кварца следует рассматривать как абсолютный асимметрический синтез. Однако мы не относим к абсолютному асимметрическому синтезу те процессы, в которых участвуют ахиральный субстрат и ахиральный реагент в присутствии либо гомогенного, либо гетерогенного катализатора. Основания для исключения гомогенных каталитических процессов ясны, так катализатор является непосредственным участником реакции на молекулярном уровне. Исключение из рассмотрения гетерогенных каталитических реакций, протекающих под воздействием хиральной кристаллической поверхности, вещества, которое хирально благодаря только своей кристаллической диссимметрии, а не молекулярной структуре, как, например, кварца, является дискуссионным вопросом.
ГОМОГЕННЫЕ КАТАЛИТИЧЕСКИЕ ПРОЦЕССЫ Под термином абсолютный асимметрический синтез обычно понимают возникновение оптически активных продуктов без использования каких -либо хиральных агентов, имеющих происхождение, связанное с живой природой. Согласно этому определению асимметрическое каталитическое разложение метилэтилмалоната на хиральной поверхности кварца следует рассматривать как абсолютный асимметрический синтез. Однако мы не относим к абсолютному асимметрическому синтезу те процессы, в которых участвуют ахиральный субстрат и ахиральный реагент в присутствии либо гомогенного, либо гетерогенного катализатора. Основания для исключения гомогенных каталитических процессов ясны, так катализатор является непосредственным участником реакции на молекулярном уровне. Исключение из рассмотрения гетерогенных каталитических реакций, протекающих под воздействием хиральной кристаллической поверхности, вещества, которое хирально благодаря только своей кристаллической диссимметрии, а не молекулярной структуре, как, например, кварца, является дискуссионным вопросом.


