Лекарственные средства производные пиридина



![2. Колба – приёмник 3. Титрование NH 4[B(OH)4] + HCl → NH 4 2. Колба – приёмник 3. Титрование NH 4[B(OH)4] + HCl → NH 4](https://present5.com/presentation/3/163375934_439625969.pdf-img/163375934_439625969.pdf-25.jpg)




Произв. пиридина .ppt
- Количество слайдов: 43
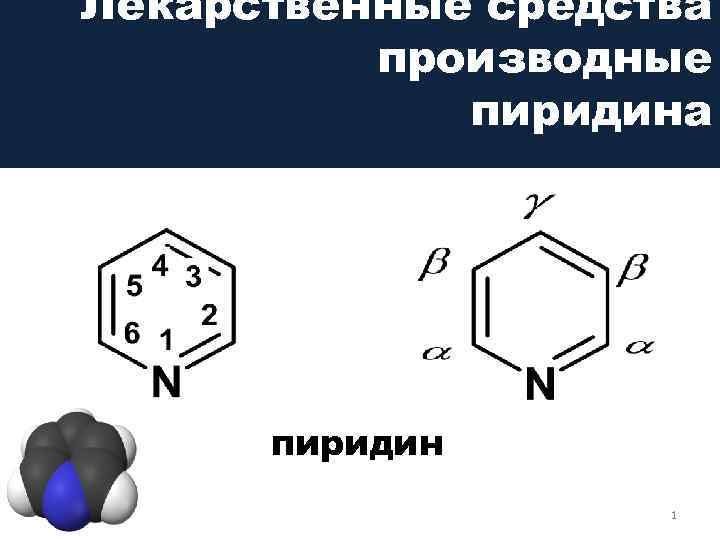
 Лекарственные средства производные пиридина пиридин 1
Лекарственные средства производные пиридина пиридин 1
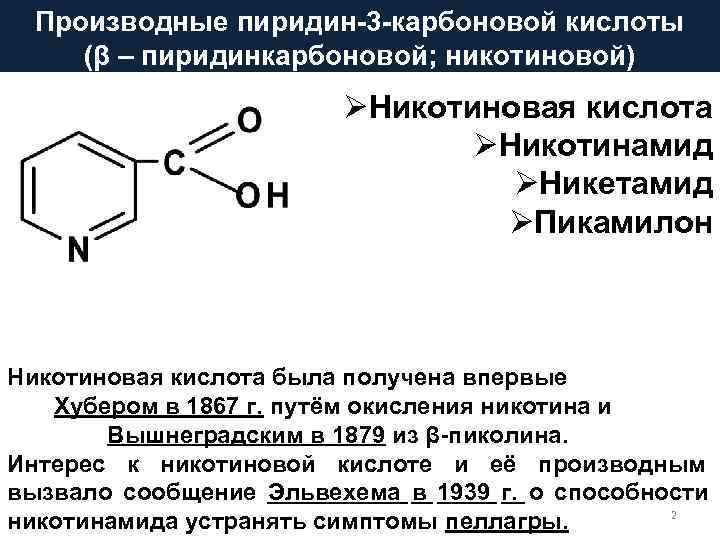
 Производные пиридин-3 -карбоновой кислоты (β – пиридинкарбоновой; никотиновой) Ø Никотиновая кислота Ø Никотинамид Ø Никетамид Ø Пикамилон Никотиновая кислота была получена впервые Хубером в 1867 г. путём окисления никотина и Вышнеградским в 1879 из β-пиколина. Интерес к никотиновой кислоте и её производным вызвало сообщение Эльвехема в 1939 г. о способности никотинамида устранять симптомы пеллагры. 2
Производные пиридин-3 -карбоновой кислоты (β – пиридинкарбоновой; никотиновой) Ø Никотиновая кислота Ø Никотинамид Ø Никетамид Ø Пикамилон Никотиновая кислота была получена впервые Хубером в 1867 г. путём окисления никотина и Вышнеградским в 1879 из β-пиколина. Интерес к никотиновой кислоте и её производным вызвало сообщение Эльвехема в 1939 г. о способности никотинамида устранять симптомы пеллагры. 2
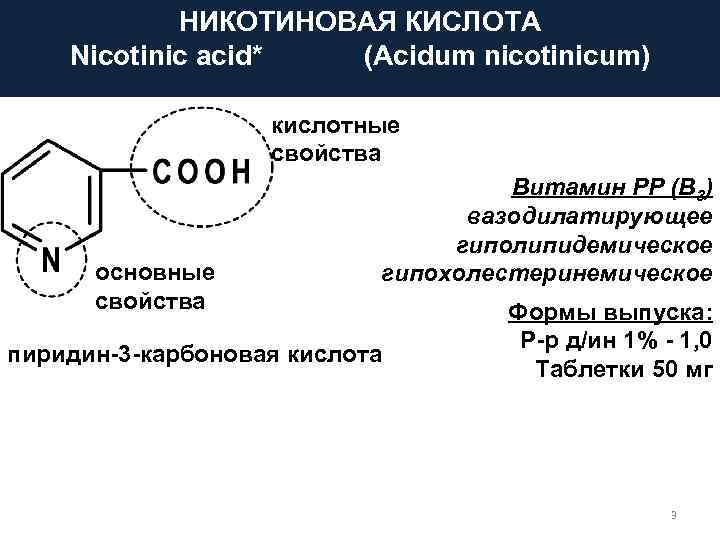
 НИКОТИНОВАЯ КИСЛОТА Nicotinic acid* (Acidum nicotinicum) кислотные свойства Витамин PP (B 3) вазодилатирующее гиполипидемическое основные гипохолестеринемическое свойства Формы выпуска: Р-р д/ин 1% - 1, 0 пиридин-3 -карбоновая кислота Таблетки 50 мг 3
НИКОТИНОВАЯ КИСЛОТА Nicotinic acid* (Acidum nicotinicum) кислотные свойства Витамин PP (B 3) вазодилатирующее гиполипидемическое основные гипохолестеринемическое свойства Формы выпуска: Р-р д/ин 1% - 1, 0 пиридин-3 -карбоновая кислота Таблетки 50 мг 3
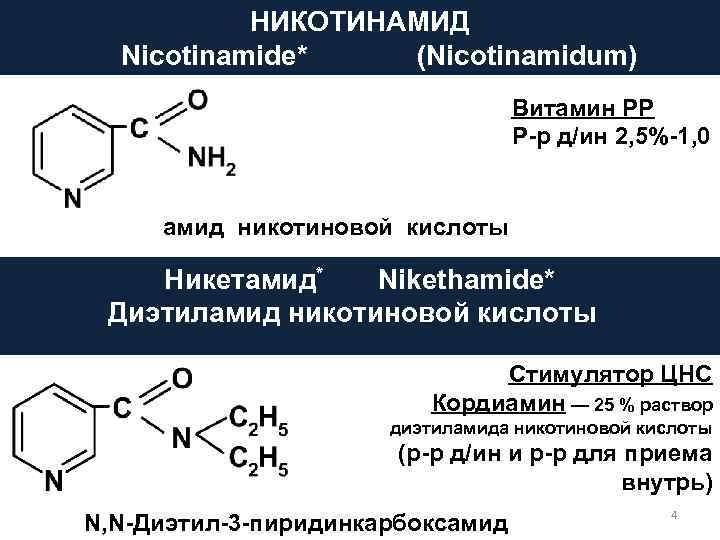
 НИКОТИНАМИД Nicotinamide* (Nicotinamidum) Витамин РР Р-р д/ин 2, 5%-1, 0 амид никотиновой кислоты Никетамид* Nikethamide* Диэтиламид никотиновой кислоты Стимулятор ЦНС Кордиамин — 25 % раствор диэтиламида никотиновой кислоты (р-р д/ин и р-р для приема внутрь) 4 N, N-Диэтил-3 -пиридинкарбоксамид
НИКОТИНАМИД Nicotinamide* (Nicotinamidum) Витамин РР Р-р д/ин 2, 5%-1, 0 амид никотиновой кислоты Никетамид* Nikethamide* Диэтиламид никотиновой кислоты Стимулятор ЦНС Кордиамин — 25 % раствор диэтиламида никотиновой кислоты (р-р д/ин и р-р для приема внутрь) 4 N, N-Диэтил-3 -пиридинкарбоксамид
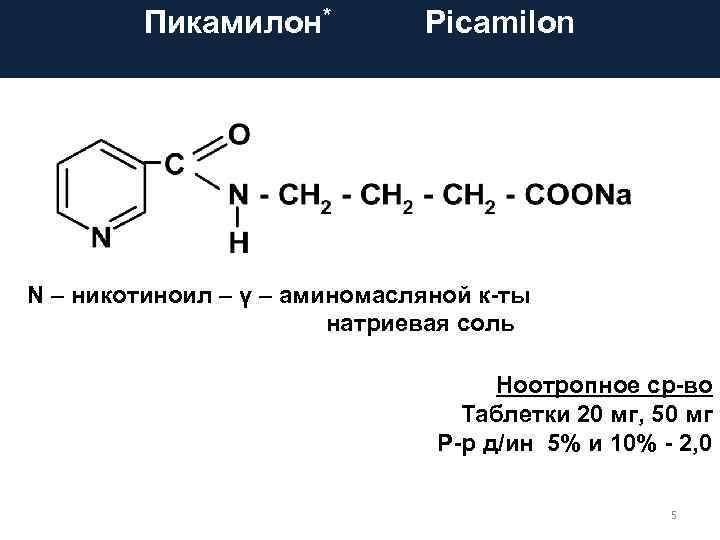
 Пикамилон* Picamilon N – никотиноил – γ – аминомасляной к-ты натриевая соль Ноотропное ср-во Таблетки 20 мг, 50 мг Р-р д/ин 5% и 10% - 2, 0 5
Пикамилон* Picamilon N – никотиноил – γ – аминомасляной к-ты натриевая соль Ноотропное ср-во Таблетки 20 мг, 50 мг Р-р д/ин 5% и 10% - 2, 0 5
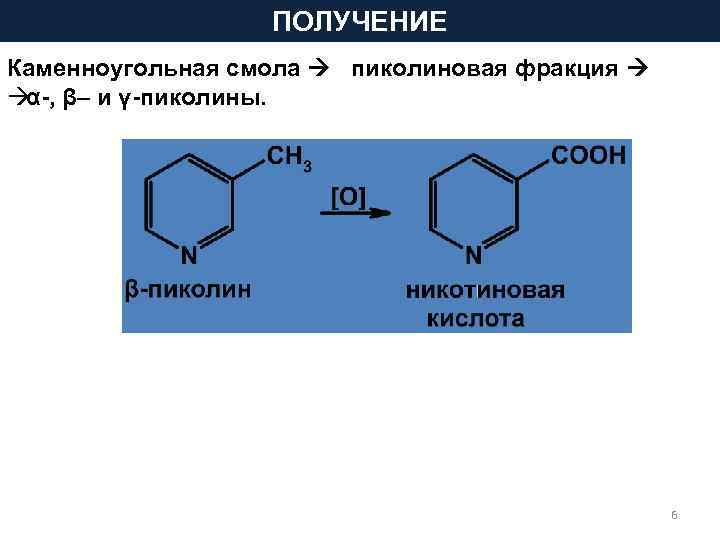
 ПОЛУЧЕНИЕ Каменноугольная смола пиколиновая фракция à α-, β– и γ-пиколины. 6
ПОЛУЧЕНИЕ Каменноугольная смола пиколиновая фракция à α-, β– и γ-пиколины. 6
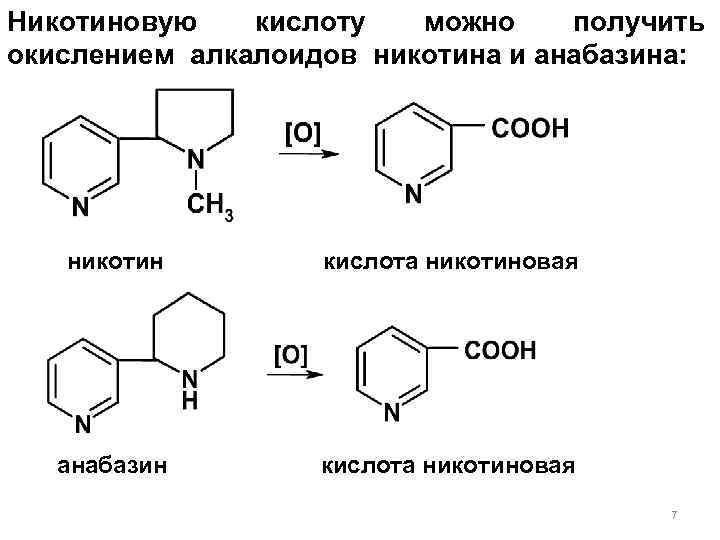
 Никотиновую кислоту можно получить окислением алкалоидов никотина и анабазина: никотин кислота никотиновая анабазин кислота никотиновая 7
Никотиновую кислоту можно получить окислением алкалоидов никотина и анабазина: никотин кислота никотиновая анабазин кислота никотиновая 7
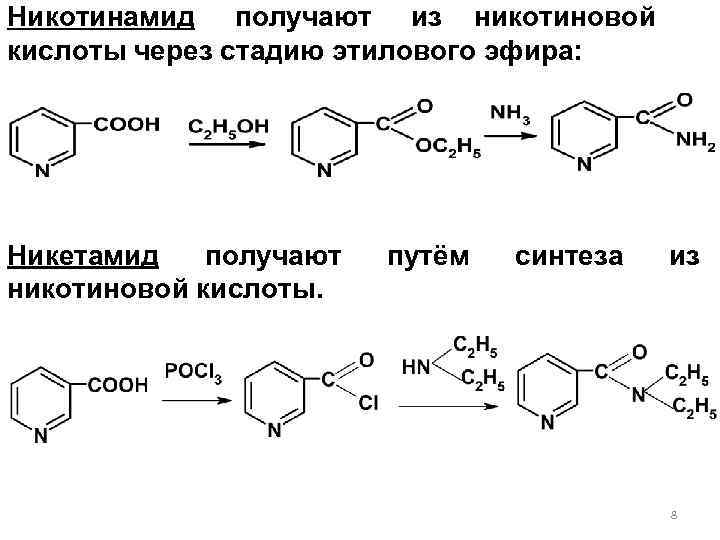
 Никотинамид получают из никотиновой кислоты через стадию этилового эфира: Никетамид получают путём синтеза из никотиновой кислоты. 8
Никотинамид получают из никотиновой кислоты через стадию этилового эфира: Никетамид получают путём синтеза из никотиновой кислоты. 8
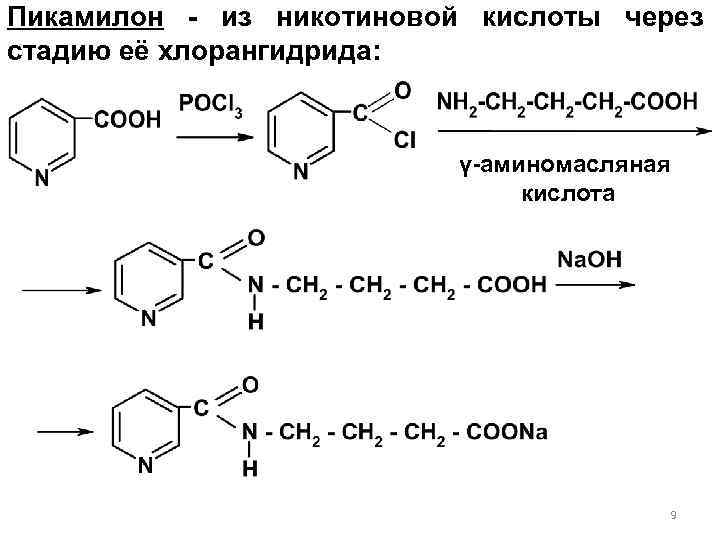
 Пикамилон - из никотиновой кислоты через стадию её хлорангидрида: γ-аминомасляная кислота 9
Пикамилон - из никотиновой кислоты через стадию её хлорангидрида: γ-аминомасляная кислота 9
 Физические свойства Никотиновая кислота, никотинамид и пикамилон — белые кристаллические вещества. Никетамид — бесцветная или желтоватая жидкость, смешивающаяся во всех соотношениях с водой, этанолом, эфиром, хлороформом. Растворимость: Никотинамид и пикамилон легко растворимы в воде и спирте. Никотиновая кислота умеренно растворима в воде, мало — в этаноле. 10
Физические свойства Никотиновая кислота, никотинамид и пикамилон — белые кристаллические вещества. Никетамид — бесцветная или желтоватая жидкость, смешивающаяся во всех соотношениях с водой, этанолом, эфиром, хлороформом. Растворимость: Никотинамид и пикамилон легко растворимы в воде и спирте. Никотиновая кислота умеренно растворима в воде, мало — в этаноле. 10
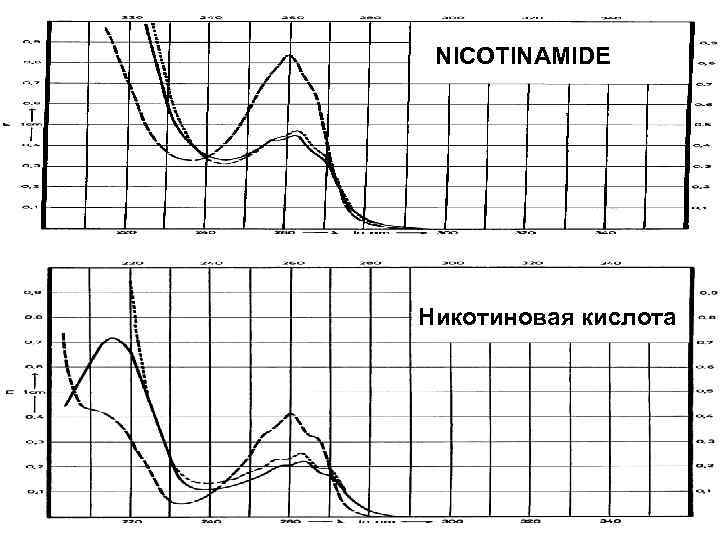
 Подлинность 1. ИК-спектр 2. УФ-спектр üникотиновая кислота (0, 002% р-р в 0, 1 М Na. OH) λmax 258, 264, 270 нм λmin 240 нм два плеча в области 240 -258 нм. ü никетамид (0, 0025% р-р в 0, 01 М HCl) λmax 264 нм λmin 243 нм ü никотинамид (в 0, 1 М HCl) λmax 261 нм. 11
Подлинность 1. ИК-спектр 2. УФ-спектр üникотиновая кислота (0, 002% р-р в 0, 1 М Na. OH) λmax 258, 264, 270 нм λmin 240 нм два плеча в области 240 -258 нм. ü никетамид (0, 0025% р-р в 0, 01 М HCl) λmax 264 нм λmin 243 нм ü никотинамид (в 0, 1 М HCl) λmax 261 нм. 11
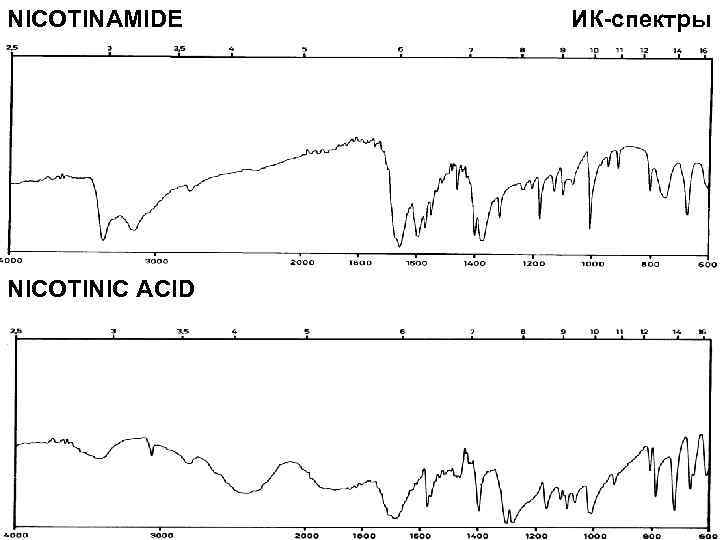
 NICOTINAMIDE ИК-спектры NICOTINIC ACID 12
NICOTINAMIDE ИК-спектры NICOTINIC ACID 12
 NICOTINAMIDE Никотиновая кислота 13
NICOTINAMIDE Никотиновая кислота 13
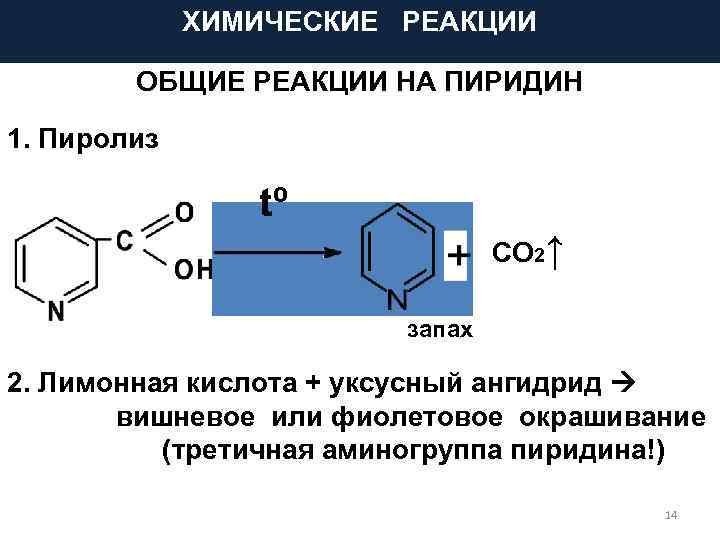
 ХИМИЧЕСКИЕ РЕАКЦИИ ОБЩИЕ РЕАКЦИИ НА ПИРИДИН 1. Пиролиз tº СО 2↑ запах 2. Лимонная кислота + уксусный ангидрид вишневое или фиолетовое окрашивание (третичная аминогруппа пиридина!) 14
ХИМИЧЕСКИЕ РЕАКЦИИ ОБЩИЕ РЕАКЦИИ НА ПИРИДИН 1. Пиролиз tº СО 2↑ запах 2. Лимонная кислота + уксусный ангидрид вишневое или фиолетовое окрашивание (третичная аминогруппа пиридина!) 14
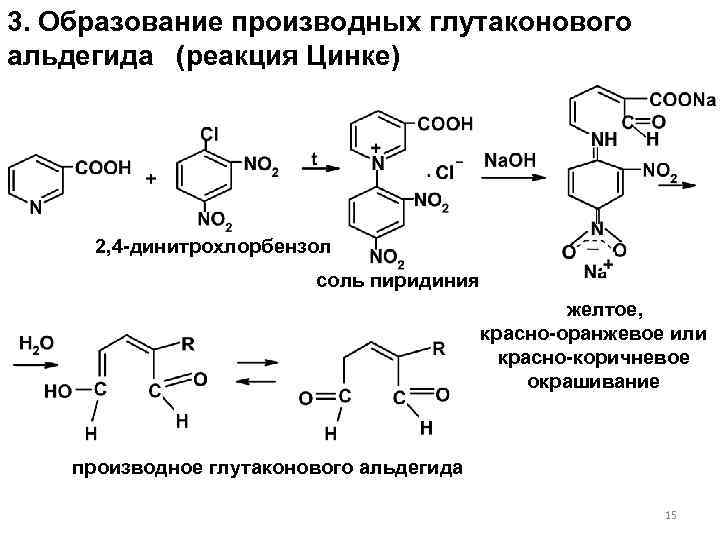
 3. Образование производных глутаконового альдегида (реакция Цинке) 2, 4 -динитрохлорбензол соль пиридиния желтое, красно-оранжевое или красно-коричневое окрашивание производное глутаконового альдегида 15
3. Образование производных глутаконового альдегида (реакция Цинке) 2, 4 -динитрохлорбензол соль пиридиния желтое, красно-оранжевое или красно-коричневое окрашивание производное глутаконового альдегида 15
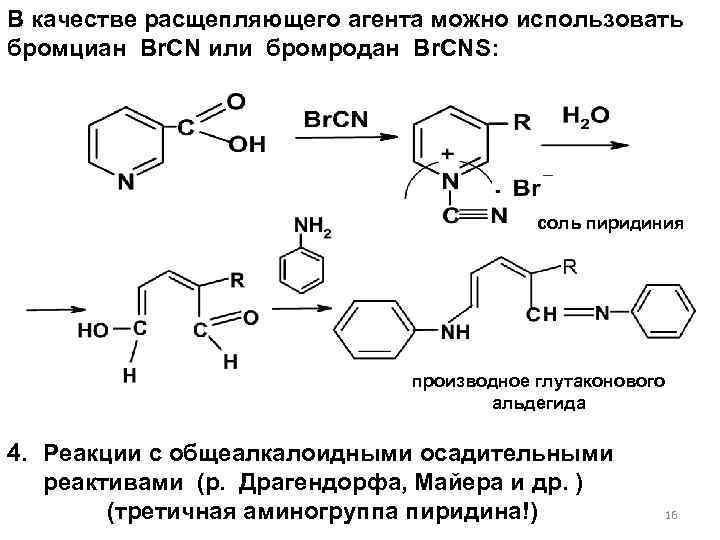
 В качестве расщепляющего агента можно использовать бромциан Br. CN или бромродан Br. CNS: соль пиридиния производное глутаконового альдегида 4. Реакции с общеалкалоидными осадительными реактивами (р. Драгендорфа, Майера и др. ) (третичная аминогруппа пиридина!) 16
В качестве расщепляющего агента можно использовать бромциан Br. CN или бромродан Br. CNS: соль пиридиния производное глутаконового альдегида 4. Реакции с общеалкалоидными осадительными реактивами (р. Драгендорфа, Майера и др. ) (третичная аминогруппа пиридина!) 16
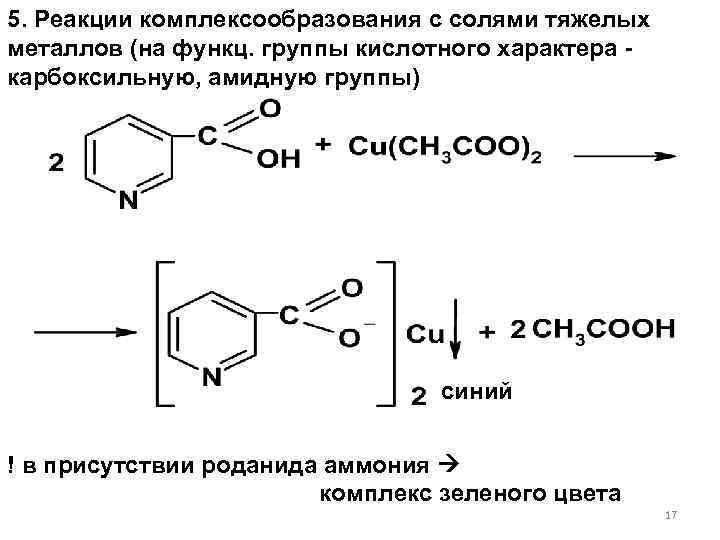
 5. Реакции комплексообразования с солями тяжелых металлов (на функц. группы кислотного характера - карбоксильную, амидную группы) синий ! в присутствии роданида аммония комплекс зеленого цвета 17
5. Реакции комплексообразования с солями тяжелых металлов (на функц. группы кислотного характера - карбоксильную, амидную группы) синий ! в присутствии роданида аммония комплекс зеленого цвета 17
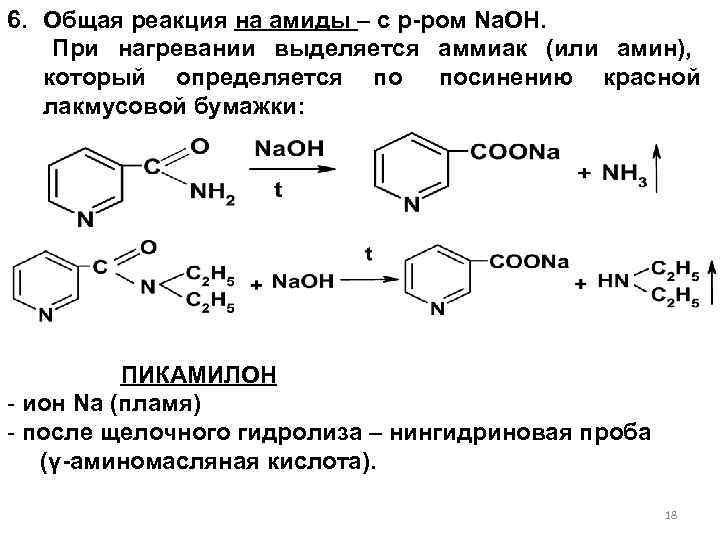
 6. Общая реакция на амиды – с р-ром Na. OH. При нагревании выделяется аммиак (или амин), который определяется по посинению красной лакмусовой бумажки: ПИКАМИЛОН - ион Na (пламя) - после щелочного гидролиза – нингидриновая проба (γ-аминомасляная кислота). 18
6. Общая реакция на амиды – с р-ром Na. OH. При нагревании выделяется аммиак (или амин), который определяется по посинению красной лакмусовой бумажки: ПИКАМИЛОН - ион Na (пламя) - после щелочного гидролиза – нингидриновая проба (γ-аминомасляная кислота). 18
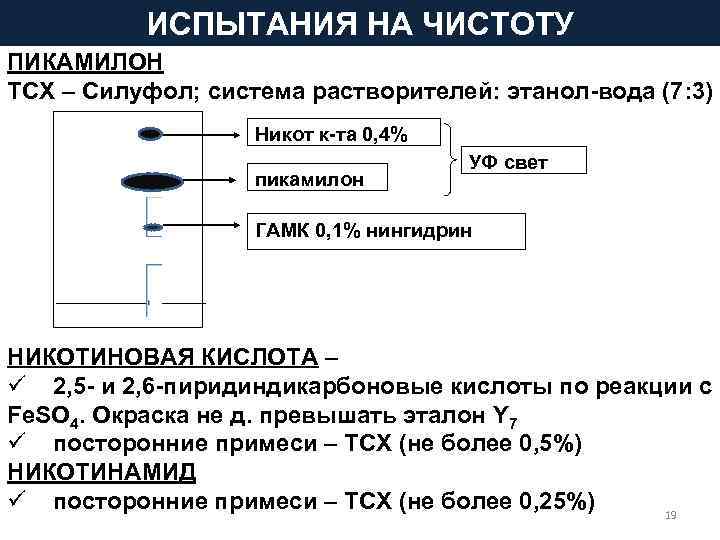
 ИСПЫТАНИЯ НА ЧИСТОТУ ПИКАМИЛОН ТСХ – Силуфол; система растворителей: этанол-вода (7: 3) Никот к-та 0, 4% УФ свет пикамилон ГАМК 0, 1% нингидрин НИКОТИНОВАЯ КИСЛОТА – ü 2, 5 - и 2, 6 -пиридиндикарбоновые кислоты по реакции с Fe. SO 4. Окраска не д. превышать эталон Y 7 ü посторонние примеси – ТСХ (не более 0, 5%) НИКОТИНАМИД ü посторонние примеси – ТСХ (не более 0, 25%) 19
ИСПЫТАНИЯ НА ЧИСТОТУ ПИКАМИЛОН ТСХ – Силуфол; система растворителей: этанол-вода (7: 3) Никот к-та 0, 4% УФ свет пикамилон ГАМК 0, 1% нингидрин НИКОТИНОВАЯ КИСЛОТА – ü 2, 5 - и 2, 6 -пиридиндикарбоновые кислоты по реакции с Fe. SO 4. Окраска не д. превышать эталон Y 7 ü посторонние примеси – ТСХ (не более 0, 5%) НИКОТИНАМИД ü посторонние примеси – ТСХ (не более 0, 25%) 19
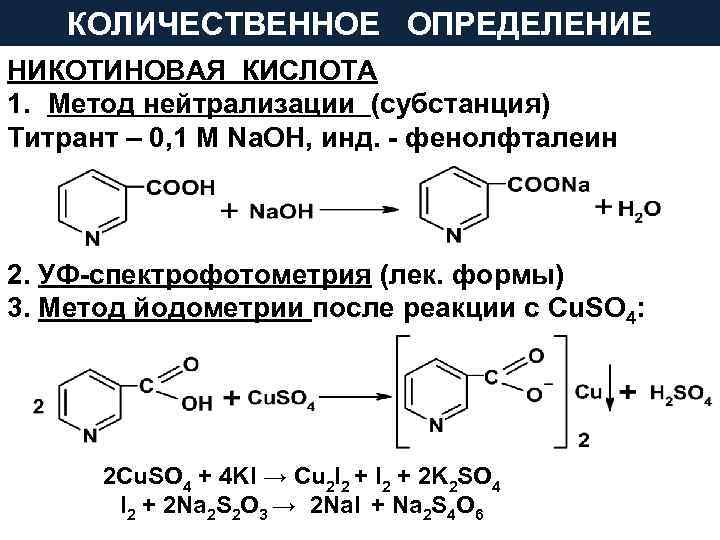
 КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ НИКОТИНОВАЯ КИСЛОТА 1. Метод нейтрализации (субстанция) Титрант – 0, 1 М Na. OH, инд. - фенолфталеин 2. УФ-спектрофотометрия (лек. формы) 3. Метод йодометрии после реакции с Cu. SO 4: 2 Cu. SO 4 + 4 KI → Cu 2 I 2 + 2 K 2 SO 4 I 2 + 2 Na 2 S 2 O 3 → 2 Na. I + Na 2 S 4 O 6
КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ НИКОТИНОВАЯ КИСЛОТА 1. Метод нейтрализации (субстанция) Титрант – 0, 1 М Na. OH, инд. - фенолфталеин 2. УФ-спектрофотометрия (лек. формы) 3. Метод йодометрии после реакции с Cu. SO 4: 2 Cu. SO 4 + 4 KI → Cu 2 I 2 + 2 K 2 SO 4 I 2 + 2 Na 2 S 2 O 3 → 2 Na. I + Na 2 S 4 O 6
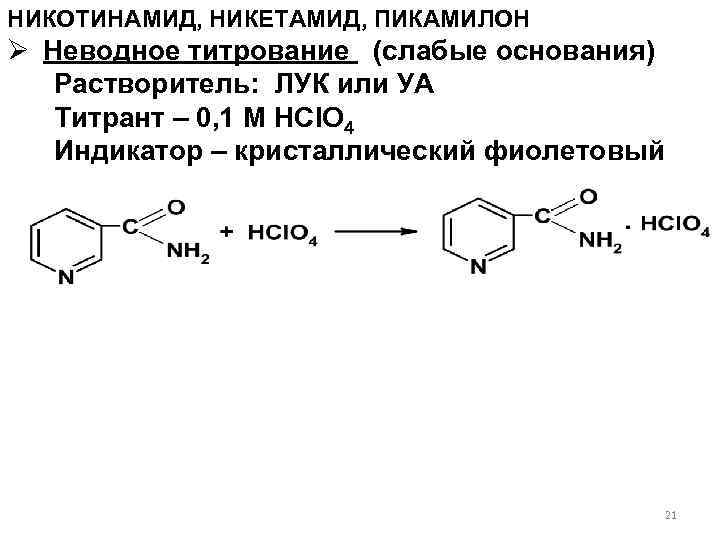
 НИКОТИНАМИД, НИКЕТАМИД, ПИКАМИЛОН Ø Неводное титрование (слабые основания) Растворитель: ЛУК или УА Титрант – 0, 1 М HCl. O 4 Индикатор – кристаллический фиолетовый 21
НИКОТИНАМИД, НИКЕТАМИД, ПИКАМИЛОН Ø Неводное титрование (слабые основания) Растворитель: ЛУК или УА Титрант – 0, 1 М HCl. O 4 Индикатор – кристаллический фиолетовый 21
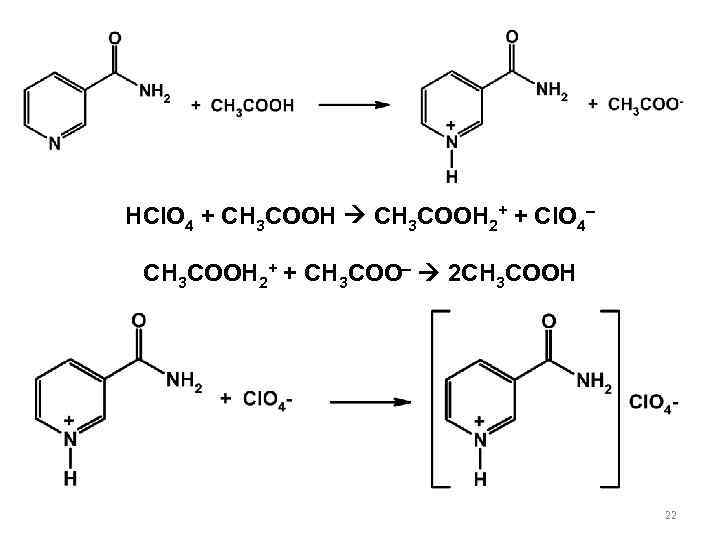
 HCl. O 4 + CH 3 COOH 2+ + Cl. O 4– CH 3 COOH 2+ + CH 3 COO– 2 CH 3 COOH 22
HCl. O 4 + CH 3 COOH 2+ + Cl. O 4– CH 3 COOH 2+ + CH 3 COO– 2 CH 3 COOH 22
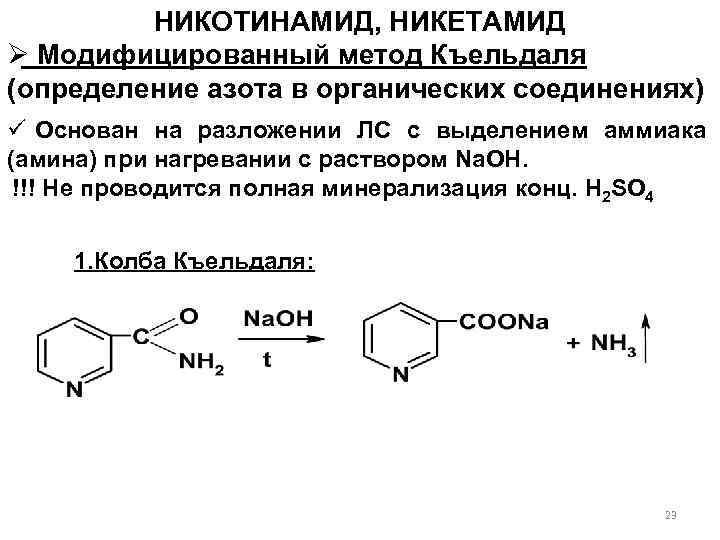
 НИКОТИНАМИД, НИКЕТАМИД Ø Модифицированный метод Къельдаля (определение азота в органических соединениях) ü Основан на разложении ЛС с выделением аммиака (амина) при нагревании с раствором Na. OH. !!! Не проводится полная минерализация конц. H 2 SO 4 1. Колба Къельдаля: 23
НИКОТИНАМИД, НИКЕТАМИД Ø Модифицированный метод Къельдаля (определение азота в органических соединениях) ü Основан на разложении ЛС с выделением аммиака (амина) при нагревании с раствором Na. OH. !!! Не проводится полная минерализация конц. H 2 SO 4 1. Колба Къельдаля: 23
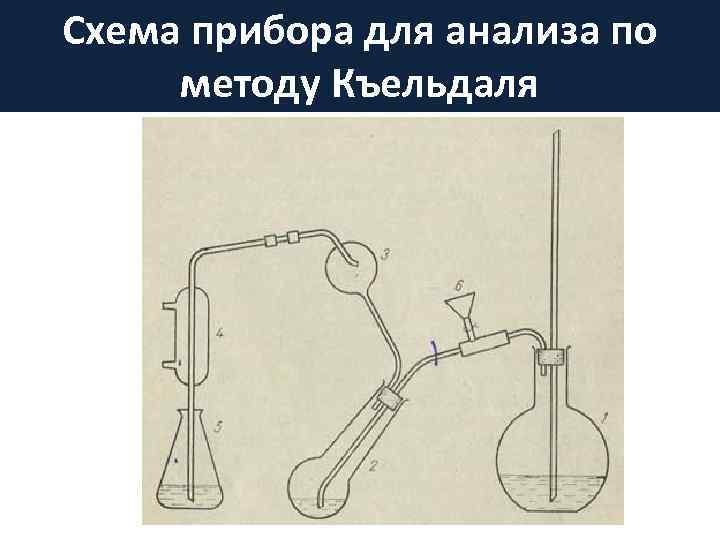
 Схема прибора для анализа по методу Къельдаля
Схема прибора для анализа по методу Къельдаля
![>2. Колба – приёмник 3. Титрование NH 4[B(OH)4] + HCl → NH 4 >2. Колба – приёмник 3. Титрование NH 4[B(OH)4] + HCl → NH 4](https://present5.com/presentation/3/163375934_439625969.pdf-img/163375934_439625969.pdf-25.jpg) 2. Колба – приёмник 3. Титрование NH 4[B(OH)4] + HCl → NH 4 Cl + H 3 BO 3 + H 2 O
2. Колба – приёмник 3. Титрование NH 4[B(OH)4] + HCl → NH 4 Cl + H 3 BO 3 + H 2 O
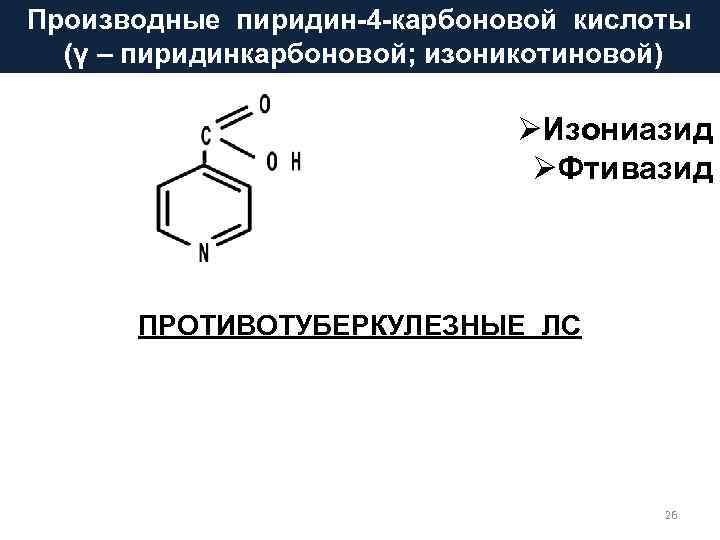
 Производные пиридин-4 -карбоновой кислоты (γ – пиридинкарбоновой; изоникотиновой) Ø Изониазид Ø Фтивазид ПРОТИВОТУБЕРКУЛЕЗНЫЕ ЛС 26
Производные пиридин-4 -карбоновой кислоты (γ – пиридинкарбоновой; изоникотиновой) Ø Изониазид Ø Фтивазид ПРОТИВОТУБЕРКУЛЕЗНЫЕ ЛС 26
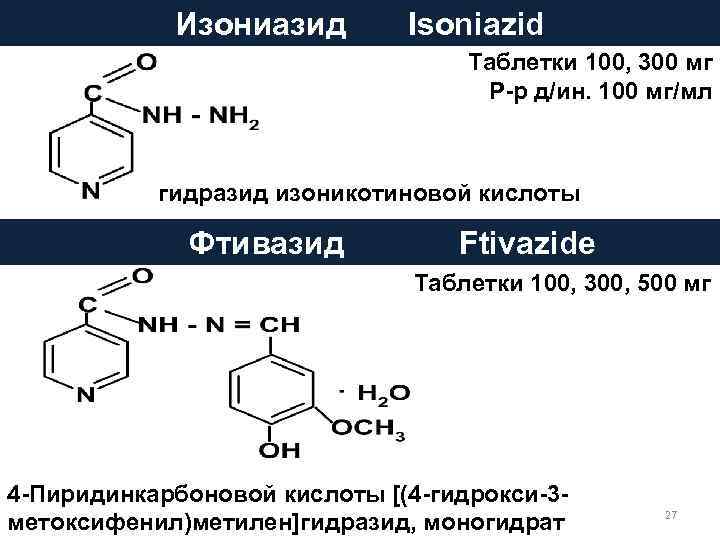
 Изониазид Isoniazid Таблетки 100, 300 мг Р-р д/ин. 100 мг/мл гидразид изоникотиновой кислоты Фтивазид Ftivazide Таблетки 100, 300, 500 мг 4 -Пиридинкарбоновой кислоты [(4 -гидрокси-3 - 27 метоксифенил)метилен]гидразид, моногидрат
Изониазид Isoniazid Таблетки 100, 300 мг Р-р д/ин. 100 мг/мл гидразид изоникотиновой кислоты Фтивазид Ftivazide Таблетки 100, 300, 500 мг 4 -Пиридинкарбоновой кислоты [(4 -гидрокси-3 - 27 метоксифенил)метилен]гидразид, моногидрат
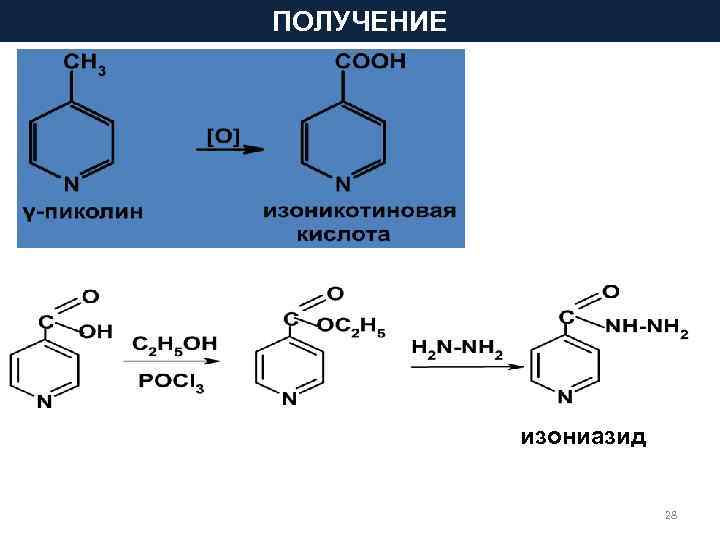
 ПОЛУЧЕНИЕ изониазид 28
ПОЛУЧЕНИЕ изониазид 28
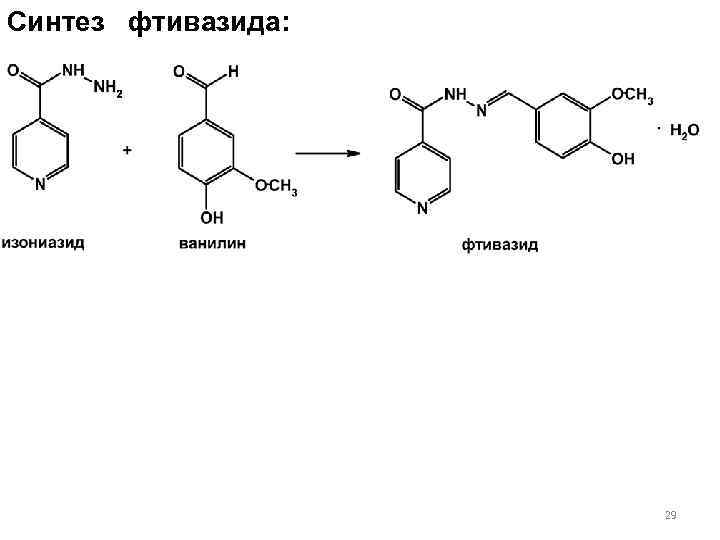
 Синтез фтивазида: 29
Синтез фтивазида: 29
 Физические свойства ИЗОНИАЗИД - белый крист. пор. без запаха. üлегко растворим в воде üрастворим в спирте üочень мало растворим в хлороформе. ФТИВАЗИД - светло-желтый или желтый мелкокрист. пор. со слабым запахом ванилина. üочень мало растворим в воде üлегко растворим в кислотах и щелочах. 30
Физические свойства ИЗОНИАЗИД - белый крист. пор. без запаха. üлегко растворим в воде üрастворим в спирте üочень мало растворим в хлороформе. ФТИВАЗИД - светло-желтый или желтый мелкокрист. пор. со слабым запахом ванилина. üочень мало растворим в воде üлегко растворим в кислотах и щелочах. 30
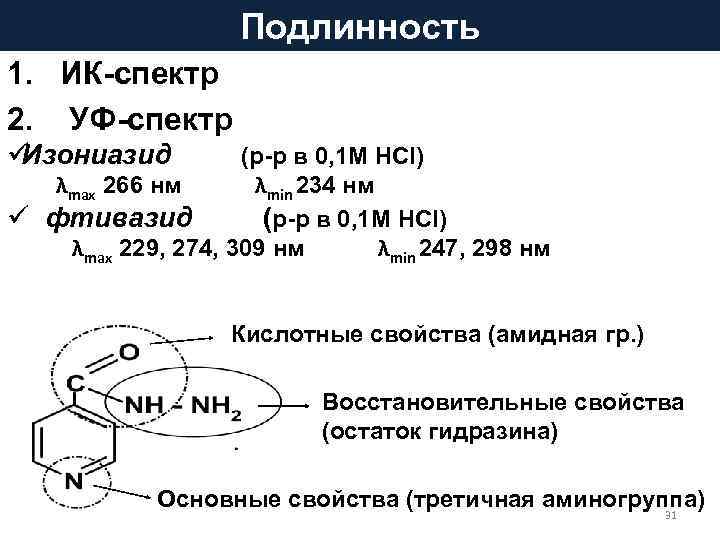
 Подлинность 1. ИК-спектр 2. УФ-спектр üИзониазид (р-р в 0, 1 М HCl) λmax 266 нм λmin 234 нм ü фтивазид (р-р в 0, 1 М HCl) λmax 229, 274, 309 нм λmin 247, 298 нм Кислотные свойства (амидная гр. ) Восстановительные свойства (остаток гидразина) Основные свойства (третичная аминогруппа) 31
Подлинность 1. ИК-спектр 2. УФ-спектр üИзониазид (р-р в 0, 1 М HCl) λmax 266 нм λmin 234 нм ü фтивазид (р-р в 0, 1 М HCl) λmax 229, 274, 309 нм λmin 247, 298 нм Кислотные свойства (амидная гр. ) Восстановительные свойства (остаток гидразина) Основные свойства (третичная аминогруппа) 31
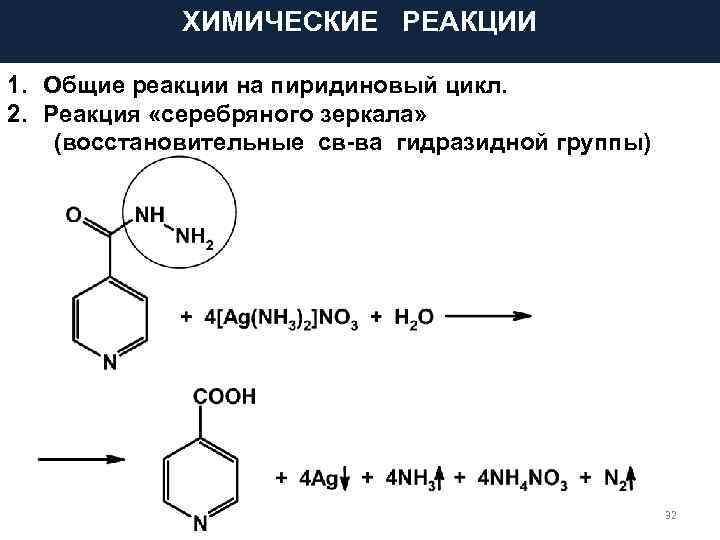
 ХИМИЧЕСКИЕ РЕАКЦИИ 1. Общие реакции на пиридиновый цикл. 2. Реакция «серебряного зеркала» (восстановительные св-ва гидразидной группы) 32
ХИМИЧЕСКИЕ РЕАКЦИИ 1. Общие реакции на пиридиновый цикл. 2. Реакция «серебряного зеркала» (восстановительные св-ва гидразидной группы) 32
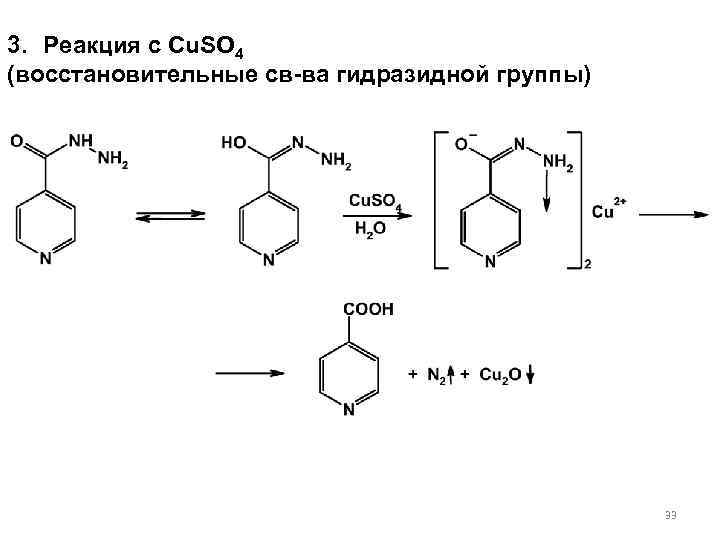
 3. Реакция с Cu. SO 4 (восстановительные св-ва гидразидной группы) 33
3. Реакция с Cu. SO 4 (восстановительные св-ва гидразидной группы) 33
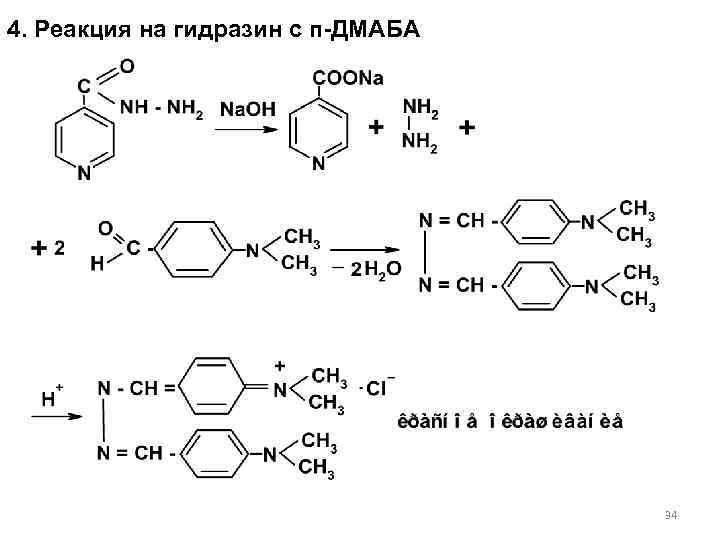
 4. Реакция на гидразин с п-ДМАБА 34
4. Реакция на гидразин с п-ДМАБА 34
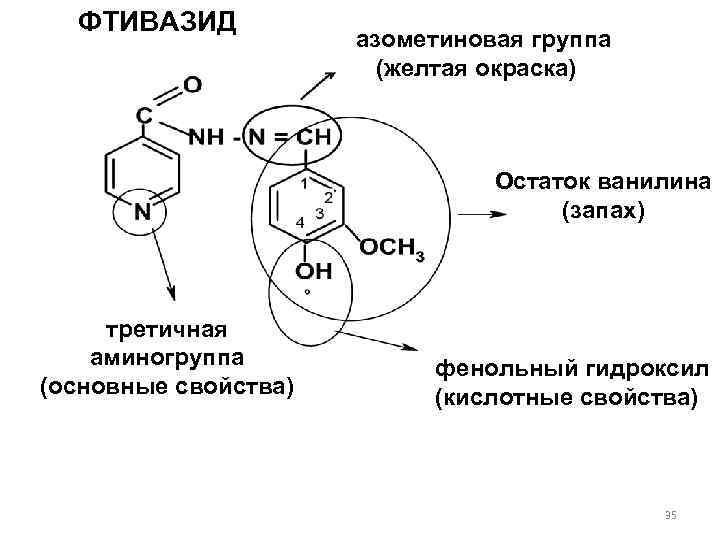
 ФТИВАЗИД азометиновая группа (желтая окраска) Остаток ванилина (запах) третичная аминогруппа фенольный гидроксил (основные свойства) (кислотные свойства) 35
ФТИВАЗИД азометиновая группа (желтая окраска) Остаток ванилина (запах) третичная аминогруппа фенольный гидроксил (основные свойства) (кислотные свойства) 35
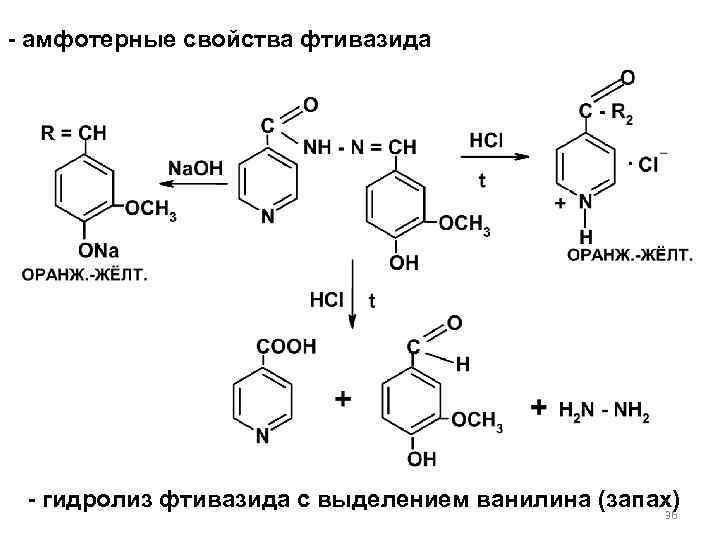
 - амфотерные свойства фтивазида - гидролиз фтивазида с выделением ванилина (запах) 36
- амфотерные свойства фтивазида - гидролиз фтивазида с выделением ванилина (запах) 36
 ИСПЫТАНИЯ НА ЧИСТОТУ ИЗОНИАЗИД - свободный гидразин (не более 0, 02%). ТСХ; Силуфол или Сорбфил УФ-254 Система: ацетон-вода Rf – 0, 5 (изониазид) УФ – свет Rf – 0, 3 (гидразин) n–ДМАБА ФТИВАЗИД - нитритометрический метод (изониазид) - нейтрализация 0, 05 М Na. OH по ф/ф (ванилин) 37
ИСПЫТАНИЯ НА ЧИСТОТУ ИЗОНИАЗИД - свободный гидразин (не более 0, 02%). ТСХ; Силуфол или Сорбфил УФ-254 Система: ацетон-вода Rf – 0, 5 (изониазид) УФ – свет Rf – 0, 3 (гидразин) n–ДМАБА ФТИВАЗИД - нитритометрический метод (изониазид) - нейтрализация 0, 05 М Na. OH по ф/ф (ванилин) 37
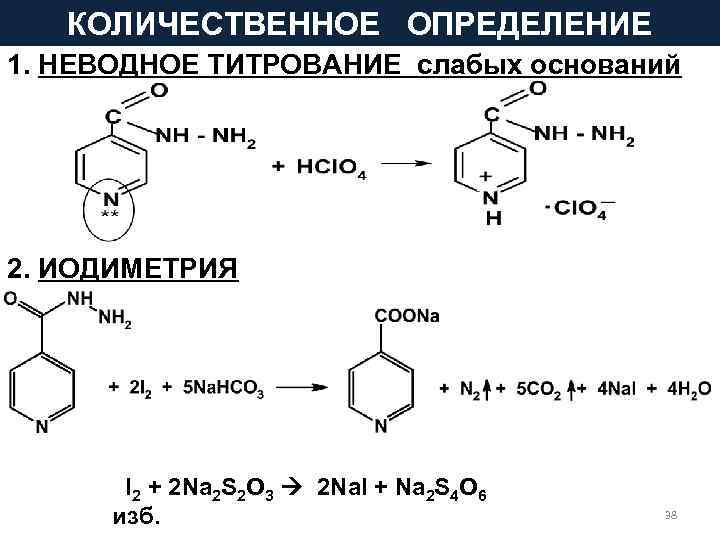
 КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ 1. НЕВОДНОЕ ТИТРОВАНИЕ слабых оснований 2. ИОДИМЕТРИЯ I 2 + 2 Na 2 S 2 O 3 2 Na. I + Na 2 S 4 O 6 изб. 38
КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ 1. НЕВОДНОЕ ТИТРОВАНИЕ слабых оснований 2. ИОДИМЕТРИЯ I 2 + 2 Na 2 S 2 O 3 2 Na. I + Na 2 S 4 O 6 изб. 38
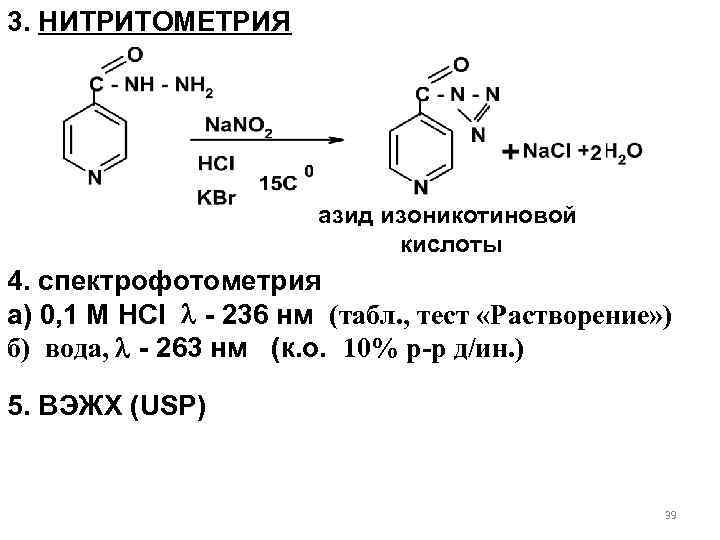
 3. НИТРИТОМЕТРИЯ азид изоникотиновой кислоты 4. спектрофотометрия а) 0, 1 М HCl - 236 нм (табл. , тест «Растворение» ) б) вода, - 263 нм (к. о. 10% р-р д/ин. ) 5. ВЭЖХ (USP) 39
3. НИТРИТОМЕТРИЯ азид изоникотиновой кислоты 4. спектрофотометрия а) 0, 1 М HCl - 236 нм (табл. , тест «Растворение» ) б) вода, - 263 нм (к. о. 10% р-р д/ин. ) 5. ВЭЖХ (USP) 39
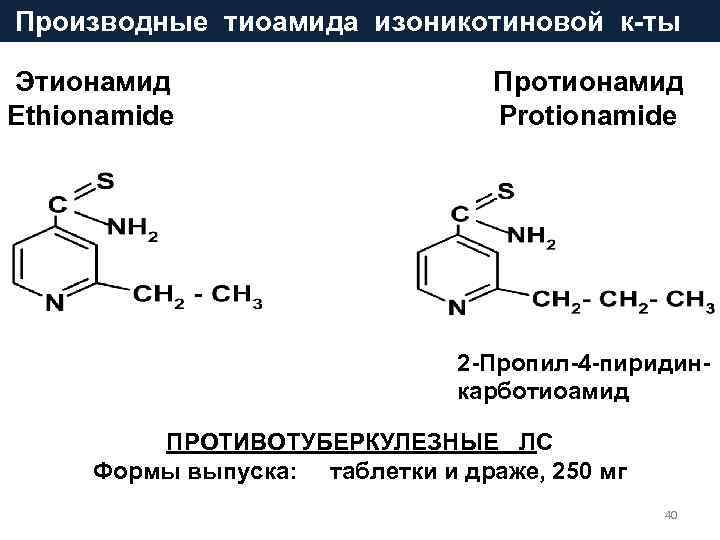
 Производные тиоамида изоникотиновой к-ты Этионамид Протионамид Ethionamide Protionamide 2 -Пропил-4 -пиридин- карботиоамид ПРОТИВОТУБЕРКУЛЕЗНЫЕ ЛС Формы выпуска: таблетки и драже, 250 мг 40
Производные тиоамида изоникотиновой к-ты Этионамид Протионамид Ethionamide Protionamide 2 -Пропил-4 -пиридин- карботиоамид ПРОТИВОТУБЕРКУЛЕЗНЫЕ ЛС Формы выпуска: таблетки и драже, 250 мг 40
 Физические свойства Желтые кристаллические порошки, нерастворимые в воде и спирте. Этионамид – с легким запахом сульфидов. Подлинность 1. ИК – СПЕКТР 2. Т пл. 3. УФ-спектр этионамида max 230, 278 нм (в 0, 1 М HCl) max 290 нм (в этаноле) 41
Физические свойства Желтые кристаллические порошки, нерастворимые в воде и спирте. Этионамид – с легким запахом сульфидов. Подлинность 1. ИК – СПЕКТР 2. Т пл. 3. УФ-спектр этионамида max 230, 278 нм (в 0, 1 М HCl) max 290 нм (в этаноле) 41
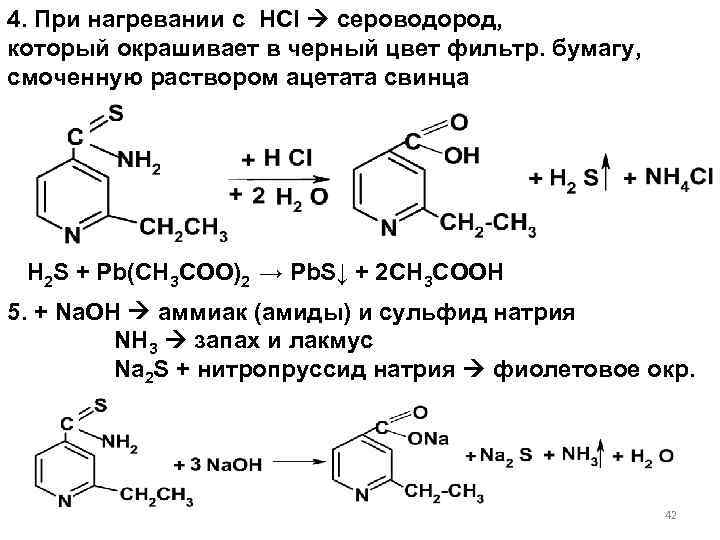
 4. При нагревании с HCl сероводород, который окрашивает в черный цвет фильтр. бумагу, смоченную раствором ацетата свинца H 2 S + Pb(CH 3 COO)2 → Pb. S↓ + 2 CH 3 COOH 5. + Na. OH аммиак (амиды) и сульфид натрия NH 3 запах и лакмус Na 2 S + нитропруссид натрия фиолетовое окр. 42
4. При нагревании с HCl сероводород, который окрашивает в черный цвет фильтр. бумагу, смоченную раствором ацетата свинца H 2 S + Pb(CH 3 COO)2 → Pb. S↓ + 2 CH 3 COOH 5. + Na. OH аммиак (амиды) и сульфид натрия NH 3 запах и лакмус Na 2 S + нитропруссид натрия фиолетовое окр. 42
 КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ 1. НЕВОДНОЕ ТИТРОВАНИЕ слабых оснований в лед. уксусной кислоте титрант – 0, 1 М HCl. O 4 2. СФ-метрия 43
КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ 1. НЕВОДНОЕ ТИТРОВАНИЕ слабых оснований в лед. уксусной кислоте титрант – 0, 1 М HCl. O 4 2. СФ-метрия 43

