Легочное сердце.PPT
- Количество слайдов: 42
 Легочное сердце Профессор А. Э. Макаревич
Легочное сердце Профессор А. Э. Макаревич
 Легочная гипертензия (ЛГ) – гемодинамическая патология, встречается при многих заболеваниях и характеризуется ростом постнагрузки на ПЖ. Анамнез, клинические проявления ЛГ, ее обратимость зависят от природы повреждения сосудов легких, этиологии и тяжести гемодинамических нарушений. Легкая-умеренная ЛГ может длительное время протекать без клинической симптоматики. Когда ЛГ становится манифестной, то и даже тогда, выявляемые симптомы, носят неспецифический характер. ЛГ бывает: • редко первичной (причины ее неизвестны); • чаще вторичной (возникает на фоне имеющихся заболеваний сердца и легких), нередко сопутствует очень тяжелой патологии левых отделов сердца (при которой повышается нагрузка и на ПЖ). Значение ЛГ -- если не контролируется, то приводит к ПЖ недостаточности (становится неизбежной, если ЛГ достигает системного уровня).
Легочная гипертензия (ЛГ) – гемодинамическая патология, встречается при многих заболеваниях и характеризуется ростом постнагрузки на ПЖ. Анамнез, клинические проявления ЛГ, ее обратимость зависят от природы повреждения сосудов легких, этиологии и тяжести гемодинамических нарушений. Легкая-умеренная ЛГ может длительное время протекать без клинической симптоматики. Когда ЛГ становится манифестной, то и даже тогда, выявляемые симптомы, носят неспецифический характер. ЛГ бывает: • редко первичной (причины ее неизвестны); • чаще вторичной (возникает на фоне имеющихся заболеваний сердца и легких), нередко сопутствует очень тяжелой патологии левых отделов сердца (при которой повышается нагрузка и на ПЖ). Значение ЛГ -- если не контролируется, то приводит к ПЖ недостаточности (становится неизбежной, если ЛГ достигает системного уровня).
 Определение ХЛС (ВОЗ, 1961), описывающее патологический эффект дисфункции легких (нарушения кровотока или газообмена в них) на правые отделы сердца (появление ГПЖ) не отражает всех изменений в сердце, в малом круге кровообращения и не включает ЛГ (комплекс изменений в сосудах легких, которые развиваются намного раньше, чем клинические, ЭКГ и рентгенологические признаки ГПЖ). Диагностика ХЛС базируется не на ЛГ (основе патологии), а на ГПЖ (следствии, вторичном проявлении ЛГ). Нередко ГПЖ (поздний, не обязательный признак ХЛС) может и не развиться (быстро формируется миокардиодистрофия, ХСН по ПЖ типу, минуя стадию ГПЖ ). В отличие от ГЛЖ и его дилятации, распознать ГПЖ иили его дилатацию (даже при аутопсии) на начальных стадиях многих заболеваний трудно (ЭКГ,
Определение ХЛС (ВОЗ, 1961), описывающее патологический эффект дисфункции легких (нарушения кровотока или газообмена в них) на правые отделы сердца (появление ГПЖ) не отражает всех изменений в сердце, в малом круге кровообращения и не включает ЛГ (комплекс изменений в сосудах легких, которые развиваются намного раньше, чем клинические, ЭКГ и рентгенологические признаки ГПЖ). Диагностика ХЛС базируется не на ЛГ (основе патологии), а на ГПЖ (следствии, вторичном проявлении ЛГ). Нередко ГПЖ (поздний, не обязательный признак ХЛС) может и не развиться (быстро формируется миокардиодистрофия, ХСН по ПЖ типу, минуя стадию ГПЖ ). В отличие от ГЛЖ и его дилятации, распознать ГПЖ иили его дилатацию (даже при аутопсии) на начальных стадиях многих заболеваний трудно (ЭКГ,
 ЛГ - начальная причина, обусловливающая рост постнагрузки на миокард ПЖ и приводящая к дилатации ПЖ сердца с гипертрофией или без нее (в зависимости от длительности и тяжести патологии) в цепи изменений, вызывающих формирование ХЛС. ЛГ- защитный механизм, способствующий росту перфузии легочных капилляров и ра. О 2. Последующие ГПЖ (сердце адаптируется к ЛГ, позволяя нормализовать работу ПЖ, несмотря на увеличение постнагрузки) и недостаточность ПЖ (когда он не может компенсировать ЛГ и начинает повышаться венозное давление) возникают не синхронно (разделены периодами, которые могут длиться многие годы и даже десятки лет). ЛГ (ранняя стадия ХЛС) - связующее звено между дисфункцией легких и развитием ГПЖ. Главное значение ЛГ -- в том, что она приводит к синдрому ХЛС и к ПЖ недостаточности.
ЛГ - начальная причина, обусловливающая рост постнагрузки на миокард ПЖ и приводящая к дилатации ПЖ сердца с гипертрофией или без нее (в зависимости от длительности и тяжести патологии) в цепи изменений, вызывающих формирование ХЛС. ЛГ- защитный механизм, способствующий росту перфузии легочных капилляров и ра. О 2. Последующие ГПЖ (сердце адаптируется к ЛГ, позволяя нормализовать работу ПЖ, несмотря на увеличение постнагрузки) и недостаточность ПЖ (когда он не может компенсировать ЛГ и начинает повышаться венозное давление) возникают не синхронно (разделены периодами, которые могут длиться многие годы и даже десятки лет). ЛГ (ранняя стадия ХЛС) - связующее звено между дисфункцией легких и развитием ГПЖ. Главное значение ЛГ -- в том, что она приводит к синдрому ХЛС и к ПЖ недостаточности.
 Трактовка понятия ХЛС, как наличие ГПЖ и (или) его дилатации не позволяет в большинстве случаев правильно диагностировать сердечно-сосудистые осложнения. Лечащий врач, не обнаруживая симптомов ГПЖ, оценивает состояние больного как благополучное, тем самым пропуская возможность проведения ранней коррекции гемодинамических нарушений. Поэтому наличие ГПЖ и ХСН по ПЖ типу -- не существенны для постановки диагноза ХЛС (Европейское общество кардиологов) -наличие ЛГ, сочетающейся или не сочетающейся с ГПЖ, наличием или отсутствием сердечной декомпенсации по ПЖ типу (ХЛС=ЛГ±ГПЖ± ХСН по ПЖ типу). Диагностика ХЛС сводится к выявлению ЛГ с ГПЖ или без нее и недостаточности ПЖ.
Трактовка понятия ХЛС, как наличие ГПЖ и (или) его дилатации не позволяет в большинстве случаев правильно диагностировать сердечно-сосудистые осложнения. Лечащий врач, не обнаруживая симптомов ГПЖ, оценивает состояние больного как благополучное, тем самым пропуская возможность проведения ранней коррекции гемодинамических нарушений. Поэтому наличие ГПЖ и ХСН по ПЖ типу -- не существенны для постановки диагноза ХЛС (Европейское общество кардиологов) -наличие ЛГ, сочетающейся или не сочетающейся с ГПЖ, наличием или отсутствием сердечной декомпенсации по ПЖ типу (ХЛС=ЛГ±ГПЖ± ХСН по ПЖ типу). Диагностика ХЛС сводится к выявлению ЛГ с ГПЖ или без нее и недостаточности ПЖ.
 ХЛС -- распространенная патология. ЛГ и вызванная ею патология сердца (ХСН по ПЖ типу), занимают 1 -е место среди осложнений ХОБЛ (в 12 случаев развивается ХЛС; до 40% всей летальности при ХСН приходится на ХЛС). Истинную частоту ХЛС определить трудно – т. к. возникает не во всех случаях хронических заболеваний легких, обычными клиниколабораторными методами выявить наличие ЛГ весьма трудно. Клиническая манифестация, обратимость ЛГ зависят от природы поражения легочных сосудов, этиологии и тяжести гемодинамических нарушений. Клиническое значение ЛГ связано с меньшей выживаемостью больных (наличие или отсутствие ЛГ - один из лучших предикторов прогноза). Больные с ХОБЛ и ЛГ (ДЛА>20 мм рт. ст. ) имели меньшую продолжительность жизни, чем пациенты без ЛГ. Наличие ЛГ у больного ХОБЛ связано с худшей эволюцией заболевания, более частой госпитализацией в ОИТР. Степень ЛГ у больных ХОБЛ обычно меньше, чем при интерстициальных заболеваниях легких, ДБСТ, хронической ТЭЛА или ИАЛГ. Вторичная ЛГ при ХОБЛ прогрессирует годами, тяжесть коррелирует со степенью обструкции бронхов и нарушением легочного газообмена. Скорость прогрессирования ЛГ при ХОБЛ медленная (~ 0, 6 мм рт. ст. г). Обычно ДЛА повышается умерено, даже у больных с тяжелой ХОБЛ. Когда адаптивные механизмы (дилатация и гипертрофия ПЖ) уже не могут компенсировать нарушений гемодинамики, возникает недостаточность насосной функции ПЖ (ДХЛС) и связанный с этим плохой прогноз (2/3 больных ХОБЛ умирают в течение 5 лет после появления ДХЛС).
ХЛС -- распространенная патология. ЛГ и вызванная ею патология сердца (ХСН по ПЖ типу), занимают 1 -е место среди осложнений ХОБЛ (в 12 случаев развивается ХЛС; до 40% всей летальности при ХСН приходится на ХЛС). Истинную частоту ХЛС определить трудно – т. к. возникает не во всех случаях хронических заболеваний легких, обычными клиниколабораторными методами выявить наличие ЛГ весьма трудно. Клиническая манифестация, обратимость ЛГ зависят от природы поражения легочных сосудов, этиологии и тяжести гемодинамических нарушений. Клиническое значение ЛГ связано с меньшей выживаемостью больных (наличие или отсутствие ЛГ - один из лучших предикторов прогноза). Больные с ХОБЛ и ЛГ (ДЛА>20 мм рт. ст. ) имели меньшую продолжительность жизни, чем пациенты без ЛГ. Наличие ЛГ у больного ХОБЛ связано с худшей эволюцией заболевания, более частой госпитализацией в ОИТР. Степень ЛГ у больных ХОБЛ обычно меньше, чем при интерстициальных заболеваниях легких, ДБСТ, хронической ТЭЛА или ИАЛГ. Вторичная ЛГ при ХОБЛ прогрессирует годами, тяжесть коррелирует со степенью обструкции бронхов и нарушением легочного газообмена. Скорость прогрессирования ЛГ при ХОБЛ медленная (~ 0, 6 мм рт. ст. г). Обычно ДЛА повышается умерено, даже у больных с тяжелой ХОБЛ. Когда адаптивные механизмы (дилатация и гипертрофия ПЖ) уже не могут компенсировать нарушений гемодинамики, возникает недостаточность насосной функции ПЖ (ДХЛС) и связанный с этим плохой прогноз (2/3 больных ХОБЛ умирают в течение 5 лет после появления ДХЛС).
 ХЛС приводит к ранней инвалидизации больного, в 12 случаев к летальности при ХОБЛ (из-за тяжелого обострения с формированием тяжелой ДН). ЛГ – общий финал гемодинамических последствий разной патологии и многообразных механизмов. У лиц старше 50 лет ХЛС -- наиболее частая патология сердца (после ИБС и АГ) и составляет 14 всех сердечнососудистых заболеваний. В Англии ХЛС ответственно за 13 всех клинических случаев ХСН, а в США -- ХЛС обуславливает 13 всех госпитализаций (из-за развития ХСН). Смертность от ХЛС занимает 3 -е место, после ИМ и АГ. В настоящее время выявляется рост частоты возникновения ХЛС (вследствие увеличения заболеваемости ХОБЛ, продления сроков жизни больных с хронической легочной патологий и формирования у них в последующем ХЛС). У пациентов идиопатической легочной артериальной гипертензией (ИЛАГ) и ТЭЛА, главная причина смерти -- ПЖ недостаточность. Все эти цифры указывают на большую медико-социальную значимость проблемы ХЛС.
ХЛС приводит к ранней инвалидизации больного, в 12 случаев к летальности при ХОБЛ (из-за тяжелого обострения с формированием тяжелой ДН). ЛГ – общий финал гемодинамических последствий разной патологии и многообразных механизмов. У лиц старше 50 лет ХЛС -- наиболее частая патология сердца (после ИБС и АГ) и составляет 14 всех сердечнососудистых заболеваний. В Англии ХЛС ответственно за 13 всех клинических случаев ХСН, а в США -- ХЛС обуславливает 13 всех госпитализаций (из-за развития ХСН). Смертность от ХЛС занимает 3 -е место, после ИМ и АГ. В настоящее время выявляется рост частоты возникновения ХЛС (вследствие увеличения заболеваемости ХОБЛ, продления сроков жизни больных с хронической легочной патологий и формирования у них в последующем ХЛС). У пациентов идиопатической легочной артериальной гипертензией (ИЛАГ) и ТЭЛА, главная причина смерти -- ПЖ недостаточность. Все эти цифры указывают на большую медико-социальную значимость проблемы ХЛС.
 • Классификация ХЛС -- по течению: острое (как правило, декомпенсированное, развивается за несколько ч): васкулярное (при ТЭЛА) и бронхолегочное (при астматическом статусе, тяжелой двухсторонней долевой пневмонии, клапанном пневмотораксе); • подострое (как правило, компенсированное, формируется за несколько недель или мес): бронхолегочное (повторные тяжелые приступы БА, милиарные метастазы рака в легкие), васкулярное (повторные, мелкие ТЭЛА), торакодиафрагмальное, вследствие хронической гиповентиляции центрального или периферического генеза. При остром и подостром легочном сердце формируется острая перегрузка правых отделов с расширением их полости, но ГПЖ не успевает развиться; • хроническое (обычно формируется за 10 -20 лет), чаще встречается в практике терапевта. по стадии компенсации: • компенсированное (концентрическая ГПЖ с тоногенным расширением); декомпенсированное (вследствие перегрузки ПЖ возникают эксцентрическая ГПЖ и миогенная кардиомегалия).
• Классификация ХЛС -- по течению: острое (как правило, декомпенсированное, развивается за несколько ч): васкулярное (при ТЭЛА) и бронхолегочное (при астматическом статусе, тяжелой двухсторонней долевой пневмонии, клапанном пневмотораксе); • подострое (как правило, компенсированное, формируется за несколько недель или мес): бронхолегочное (повторные тяжелые приступы БА, милиарные метастазы рака в легкие), васкулярное (повторные, мелкие ТЭЛА), торакодиафрагмальное, вследствие хронической гиповентиляции центрального или периферического генеза. При остром и подостром легочном сердце формируется острая перегрузка правых отделов с расширением их полости, но ГПЖ не успевает развиться; • хроническое (обычно формируется за 10 -20 лет), чаще встречается в практике терапевта. по стадии компенсации: • компенсированное (концентрическая ГПЖ с тоногенным расширением); декомпенсированное (вследствие перегрузки ПЖ возникают эксцентрическая ГПЖ и миогенная кардиомегалия).
 По причинам развития: бронхолегочное, гипоксическое • (поражение бронхиального дерева и легочной паренхимы – чаще ХОБЛ, тяжелая БА). Реже -тяжелые рестриктивные нарушения вентиляции на поздних стадиях интерстициальных фиброзов легких – очаговых (ТВС, бронхоэктазы, муковисцидоз) или диффузных (пневмокониоз, ИФА, легочной фиброз, вызванный ЛС) или гранулематозов (саркоидоз). • васкулярное (хронические заболевания, поражающие легочные сосуды): рецидивирующая ТЭЛА проксимальных или дистальных ЛА, опухолевй нетромботический эмболизм, ИЛАГ, ДБСТ (СКВ, дерматомиозит, ССД), васкулиты (УПА или аллергический из-за лекарственного поражения сосудов легких); сдавление легочных сосудов аневризмой, опухолью, лифоузлами средостения; • торако-диафрагмальное (альвеолярная гиповентиляция вследствие поражения костно-мышечной системы, нарушение движения грудной клетки или контроля за актом дыхания): кифосколиоз и др. деформации грудной клетки (стимулируют развитие ЛГ, когда уровень ЖЕЛ снижается >50% от Д); болезнь Бехтерева; торакопластика; фиброз плевры; хроническая нервно-мышечная слабость (миастения); нарушения центрального контроля за вентиляцией (энцефалит, прием высоких доз ряда ЛС - легкие у этих больных нормальные); сильное ожирение с альвеолярной гиповентиляцией (пиквикский синдром), синдром ночного апноэ (выраженная гипосемия возникает в период сна).
По причинам развития: бронхолегочное, гипоксическое • (поражение бронхиального дерева и легочной паренхимы – чаще ХОБЛ, тяжелая БА). Реже -тяжелые рестриктивные нарушения вентиляции на поздних стадиях интерстициальных фиброзов легких – очаговых (ТВС, бронхоэктазы, муковисцидоз) или диффузных (пневмокониоз, ИФА, легочной фиброз, вызванный ЛС) или гранулематозов (саркоидоз). • васкулярное (хронические заболевания, поражающие легочные сосуды): рецидивирующая ТЭЛА проксимальных или дистальных ЛА, опухолевй нетромботический эмболизм, ИЛАГ, ДБСТ (СКВ, дерматомиозит, ССД), васкулиты (УПА или аллергический из-за лекарственного поражения сосудов легких); сдавление легочных сосудов аневризмой, опухолью, лифоузлами средостения; • торако-диафрагмальное (альвеолярная гиповентиляция вследствие поражения костно-мышечной системы, нарушение движения грудной клетки или контроля за актом дыхания): кифосколиоз и др. деформации грудной клетки (стимулируют развитие ЛГ, когда уровень ЖЕЛ снижается >50% от Д); болезнь Бехтерева; торакопластика; фиброз плевры; хроническая нервно-мышечная слабость (миастения); нарушения центрального контроля за вентиляцией (энцефалит, прием высоких доз ряда ЛС - легкие у этих больных нормальные); сильное ожирение с альвеолярной гиповентиляцией (пиквикский синдром), синдром ночного апноэ (выраженная гипосемия возникает в период сна).
 Виды ЛГ: прекапиллярная -- ведущий патогенетический фактор развития ХЛС (чаще обусловлена ХОБЛ, реже -- рестриктивными нарушениями вентиляции или обструктивной васкулярной патологией); • посткапиллярная (венозная, пассивная) вследствие наличия стеноза митрального или аортального клапанов (с приступами ОЛЖН). • высокогорная, северная. По патофизиологическому механизму: • гипоксическая вазоконстрикция - ХОБЛ, хроническая гиповентиляция (ожирение, нервно-мышечные болезни, патология грудной стенки); • окклюзия сосудистого ложа легких (ТЭЛА, раковые эмболы, ИЛАГ, фиброзирующий медиастинит, опухоль средостения, легочные васкулиты на фоне системных заболеваний (ДБСТ, лекарственные поражения легких, УПА); • редукция сосудистого ложа из-за ряда паренхиматозных болезней буллезная ЭЛ, дефицит α 1 -антитрипсина, бронхоэктазы, муковисцидоз, диффузные интерстициальные болезни (пневмокониоз, саркоидоз, ТВС и хронические грибковые поражения легких). •
Виды ЛГ: прекапиллярная -- ведущий патогенетический фактор развития ХЛС (чаще обусловлена ХОБЛ, реже -- рестриктивными нарушениями вентиляции или обструктивной васкулярной патологией); • посткапиллярная (венозная, пассивная) вследствие наличия стеноза митрального или аортального клапанов (с приступами ОЛЖН). • высокогорная, северная. По патофизиологическому механизму: • гипоксическая вазоконстрикция - ХОБЛ, хроническая гиповентиляция (ожирение, нервно-мышечные болезни, патология грудной стенки); • окклюзия сосудистого ложа легких (ТЭЛА, раковые эмболы, ИЛАГ, фиброзирующий медиастинит, опухоль средостения, легочные васкулиты на фоне системных заболеваний (ДБСТ, лекарственные поражения легких, УПА); • редукция сосудистого ложа из-за ряда паренхиматозных болезней буллезная ЭЛ, дефицит α 1 -антитрипсина, бронхоэктазы, муковисцидоз, диффузные интерстициальные болезни (пневмокониоз, саркоидоз, ТВС и хронические грибковые поражения легких). •
 Классификация ЛГ (Венеция, 2003) 1. Легочная артериальная гипертензия (ЛАГ): • ИЛАГ; • ассоциированная с: ДБСТ (СКВ; РА; дерматомиозит; ССД, особенно при наличии CREST или «перехлест» синдромов; у ряда этих больных ЛГ – причина значительной летальности), портальной гипертензией, врожденными системными-легочными шунтами, ВИЧ-инфекцией, ЛС и токсины; болезни щитовидной железы или миелопролиферативные; 2. Ассоциированная со значительным поражением вен или капилляров легких (вено-окклюзивные заболевания легких). 3. Венозная, ассоциированная с поражением левых отделов сердца (уд. вес ~80%). Патология сердца приводит к ЛГ за счет роста легочного кровотока (шунт «слева-направо» ) или давления в ЛПр (как при ХСН по ЛЖ типу). Обычно эта ЛГ развивается в ходе прогрессирования патологии ЛЖ (с повышением давления его наполнения и последующим ростом венозного давления в легких, которое, в свою очередь, вызывает рост ДЛА). • левопредсердная, пассивная, посткапиллярная (из-за поражения ЛПр или ЛЖ вследствие повышения давления в ЛЖ из-за: его недостаточности или снижения растяжимости, ишемической кардиомиопатии, ДКМП, гипертонического cердца); • из-за поражения клапанов левых отделов сердца (аортального или митрального).
Классификация ЛГ (Венеция, 2003) 1. Легочная артериальная гипертензия (ЛАГ): • ИЛАГ; • ассоциированная с: ДБСТ (СКВ; РА; дерматомиозит; ССД, особенно при наличии CREST или «перехлест» синдромов; у ряда этих больных ЛГ – причина значительной летальности), портальной гипертензией, врожденными системными-легочными шунтами, ВИЧ-инфекцией, ЛС и токсины; болезни щитовидной железы или миелопролиферативные; 2. Ассоциированная со значительным поражением вен или капилляров легких (вено-окклюзивные заболевания легких). 3. Венозная, ассоциированная с поражением левых отделов сердца (уд. вес ~80%). Патология сердца приводит к ЛГ за счет роста легочного кровотока (шунт «слева-направо» ) или давления в ЛПр (как при ХСН по ЛЖ типу). Обычно эта ЛГ развивается в ходе прогрессирования патологии ЛЖ (с повышением давления его наполнения и последующим ростом венозного давления в легких, которое, в свою очередь, вызывает рост ДЛА). • левопредсердная, пассивная, посткапиллярная (из-за поражения ЛПр или ЛЖ вследствие повышения давления в ЛЖ из-за: его недостаточности или снижения растяжимости, ишемической кардиомиопатии, ДКМП, гипертонического cердца); • из-за поражения клапанов левых отделов сердца (аортального или митрального).
 4. ЛГ, ассоциированная с респираторными заболеваниями легких и/или хронической гипоксией (уд. вес ~20%): • • • ХОБЛ, бронхоэктазы; интерстициальные болезни легких (силикоз, асбестоз, саркоидоз, ТВС) и фиброзирующие процессы (фиброзирующий альвеолит и др. ); синдром ночного апноэ; нарушения, протекающие с альвеолярной гиповентиляцией (миастения, полиомиелит, центральные нарушения контроля за дыханием); длительное пребывание на большой высоте (у лиц без патологии легких); 5. ЛГ, обусловленная хроническими тромботическими и/или эмболическими поражениями сосудов легких (механическое • • препятствие кровотоку через крупные легочные сосуды): тромботическая обструкция проксимальных и дистальных отделов ЛА (ТЭЛА занимает 3 -е место, как причина ЛГ); нетромботическая легочная эмболия (опухолью, паразитами, инородными телами). Так, раковые эмболы могут заноситься в легочной кровоток из внелегочных мест, вызывая хронический проксимальный легочной эмболизм. 6. Другие причины (саркоидоз, гистиоцитоз, сдавление легочных сосудов извне – аденопатии, опухоли, фиброзирующий медиастинит).
4. ЛГ, ассоциированная с респираторными заболеваниями легких и/или хронической гипоксией (уд. вес ~20%): • • • ХОБЛ, бронхоэктазы; интерстициальные болезни легких (силикоз, асбестоз, саркоидоз, ТВС) и фиброзирующие процессы (фиброзирующий альвеолит и др. ); синдром ночного апноэ; нарушения, протекающие с альвеолярной гиповентиляцией (миастения, полиомиелит, центральные нарушения контроля за дыханием); длительное пребывание на большой высоте (у лиц без патологии легких); 5. ЛГ, обусловленная хроническими тромботическими и/или эмболическими поражениями сосудов легких (механическое • • препятствие кровотоку через крупные легочные сосуды): тромботическая обструкция проксимальных и дистальных отделов ЛА (ТЭЛА занимает 3 -е место, как причина ЛГ); нетромботическая легочная эмболия (опухолью, паразитами, инородными телами). Так, раковые эмболы могут заноситься в легочной кровоток из внелегочных мест, вызывая хронический проксимальный легочной эмболизм. 6. Другие причины (саркоидоз, гистиоцитоз, сдавление легочных сосудов извне – аденопатии, опухоли, фиброзирующий медиастинит).
 В развитии бронхолегочного ХЛС (легочно-сердечных нарушений) можно условно выделить 4 этапа: • 1 -- нарушения вентиляции и появление ХДН; • 2 -- прогрессирование ХДН, перестройка легочной циркуляции и появление транзиторной ЛГ (выявляется только после ФН или гипоксической пробы). Так как, поперечное сечение легочного сосудистого русла большое, то классические болезни легких (ХОБЛ) обычно вызывают умеренную ЛГ; • 3 -- стабильная ЛГ (имеется в покое, резко усиливается при ФН или обострениях ХОБЛ), имеются элементы ГПЖ по данным ЭКГ, Эхо. КГ, но нет явных признаков ХСН (компенсированное ХЛС); • 4 -- конечная стадия (выраженные дистрофические изменения ПЖ и появляются клинические симптомы его недостаточности ДХЛС). В развитии ХЛС отмечают две стадии: • вначале легкая дистрофия миокарда (вследствие работы миокарда в условиях кислородного голодания) и ГПЖ; • позднее -- дилатация ПЖ с его декомпенсацией. Последнее указывает на плохой прогноз у больных ХОБЛ, ИЛАГ и нейромышечными заболеваниями.
В развитии бронхолегочного ХЛС (легочно-сердечных нарушений) можно условно выделить 4 этапа: • 1 -- нарушения вентиляции и появление ХДН; • 2 -- прогрессирование ХДН, перестройка легочной циркуляции и появление транзиторной ЛГ (выявляется только после ФН или гипоксической пробы). Так как, поперечное сечение легочного сосудистого русла большое, то классические болезни легких (ХОБЛ) обычно вызывают умеренную ЛГ; • 3 -- стабильная ЛГ (имеется в покое, резко усиливается при ФН или обострениях ХОБЛ), имеются элементы ГПЖ по данным ЭКГ, Эхо. КГ, но нет явных признаков ХСН (компенсированное ХЛС); • 4 -- конечная стадия (выраженные дистрофические изменения ПЖ и появляются клинические симптомы его недостаточности ДХЛС). В развитии ХЛС отмечают две стадии: • вначале легкая дистрофия миокарда (вследствие работы миокарда в условиях кислородного голодания) и ГПЖ; • позднее -- дилатация ПЖ с его декомпенсацией. Последнее указывает на плохой прогноз у больных ХОБЛ, ИЛАГ и нейромышечными заболеваниями.
 Нормальное систолическое ДЛА (СДЛА) ~20 -30 мм рт. ст. , диастолическое ~ 8 -15 и среднее (Ср. ДЛА) ~15 мм рт. ст. ДЛА вариабельно -- может меняться днем и ночью. На наличие ЛГ указывают: рост СДЛА на 30 мм рт. ст. и Ср. ДЛА на 15 -20 мм рт. ст (>25 мм рт. ст. в покое или >30 мм рт. ст. при ФН) и дистолического ДЛА на 10 мм рт. ст. ЛГ у больных ХОБЛ или интерстициальными болезнями легких обычно невысока ~40 мм рт. ст. , в отличие от больных ИЛАГ или с рецидивирующей ТЭЛА (ЛГ может достигать очень высоких значений). В период ФН или обострения у больных ХОБЛ -ЛГ сильно увеличивается (до 50 -70 мм рт. ст. ). Четкой корреляции между уровнем ОФВ 1 и СДЛА при ХОБЛ нет.
Нормальное систолическое ДЛА (СДЛА) ~20 -30 мм рт. ст. , диастолическое ~ 8 -15 и среднее (Ср. ДЛА) ~15 мм рт. ст. ДЛА вариабельно -- может меняться днем и ночью. На наличие ЛГ указывают: рост СДЛА на 30 мм рт. ст. и Ср. ДЛА на 15 -20 мм рт. ст (>25 мм рт. ст. в покое или >30 мм рт. ст. при ФН) и дистолического ДЛА на 10 мм рт. ст. ЛГ у больных ХОБЛ или интерстициальными болезнями легких обычно невысока ~40 мм рт. ст. , в отличие от больных ИЛАГ или с рецидивирующей ТЭЛА (ЛГ может достигать очень высоких значений). В период ФН или обострения у больных ХОБЛ -ЛГ сильно увеличивается (до 50 -70 мм рт. ст. ). Четкой корреляции между уровнем ОФВ 1 и СДЛА при ХОБЛ нет.
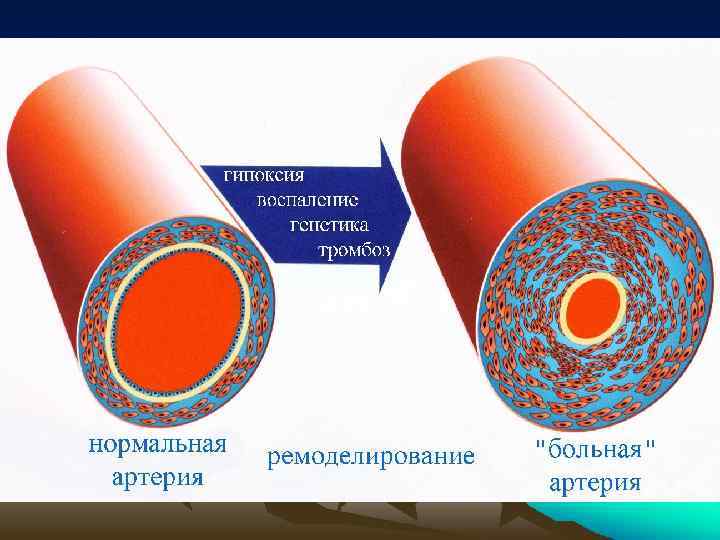
 Факторы патогенеза ЛГ: • связанные • • со стенкой сосуда: гипоксическая вазоконстрикция -- рефлекс Эйлера-Лильестранда (наиболее частая причина легкой и умеренной ЛГ), сужение капилляров из-за наличия ЭЛ, рост мышечного слоя стенок артериол, перибронхиальное и перивазальное воспаление. Если спазм легочных артерий длится >суток, начинается их ремоделирование. Все это благоприятствует формированию ЛГ. Хроническая гипоксия вызывает изменения в синтезе и высвобождении вазоактивных веществ (рост продукции эндотелина), стимулирует клеточную пролиферацию стенки сосудов (утолщение интимы), синтез внеклеточного матрикса (отложения эластических и коллагеновых волокон) и повышенную сократимость легочных артерий. Механическое сдавление сосудов при изменении объема легких на фоне легочной патологии также способствует формированию ЛГ. внутрисосудистые: полиглобулия, ухудшение реологических свойств крови (существенный рост ее вязкости) и увеличение ОЦК. ЛГ может резко усиливаться вследствие появления выраженного гипоксического эритроцитоза внесосудистые (влияние увеличенного плеврального, альвеолярного давления на легочные сосуды и ДЛА).
Факторы патогенеза ЛГ: • связанные • • со стенкой сосуда: гипоксическая вазоконстрикция -- рефлекс Эйлера-Лильестранда (наиболее частая причина легкой и умеренной ЛГ), сужение капилляров из-за наличия ЭЛ, рост мышечного слоя стенок артериол, перибронхиальное и перивазальное воспаление. Если спазм легочных артерий длится >суток, начинается их ремоделирование. Все это благоприятствует формированию ЛГ. Хроническая гипоксия вызывает изменения в синтезе и высвобождении вазоактивных веществ (рост продукции эндотелина), стимулирует клеточную пролиферацию стенки сосудов (утолщение интимы), синтез внеклеточного матрикса (отложения эластических и коллагеновых волокон) и повышенную сократимость легочных артерий. Механическое сдавление сосудов при изменении объема легких на фоне легочной патологии также способствует формированию ЛГ. внутрисосудистые: полиглобулия, ухудшение реологических свойств крови (существенный рост ее вязкости) и увеличение ОЦК. ЛГ может резко усиливаться вследствие появления выраженного гипоксического эритроцитоза внесосудистые (влияние увеличенного плеврального, альвеолярного давления на легочные сосуды и ДЛА).
 Два ведущих компонента в генезе ЛГ: функциональный: сужение легочных артериол (вазомоторное • увеличение общего легочного сосудистого сопротивления) при снижении в альвеолах р. О 2 и увеличении р. СО 2 (рефлекс Эйлера. Лильестранда); рост давления в бронхах и альвеолах; повышение МОК и концентрации метаболитов прессорного действия. Альвеолярная гипоксия -- главная причина возникновения легочной вазоконстрикции. Хроническая гипоксия (и последующая персистирующая вазоконстрикция) также благоприятствует повреждению легочных сосудов -- ремоделированию всех слоев сосудистой стенки из-за пролиферативных изменений (вазоактивные вещества высвобождающиеся из эндотелия, стимулируют пролиферацию эндотелия в стенке сосуда) и обструктивных изменений. Возникают -- мускуляризация артериол (продольный рост в них мышц и их гипертрофия), утолщение интимы (вследствие пролиферации ГМК и отложения коллагеновых и эластических волокон) и ее фиброз; • анатомический (органический): редукция сосудистого русла легких, сдавление извне или закрытие просвета сосудов в легочной артерии, мускуляризация артериол. Уровень ЛГ четко не коррелирует с КЩС крови. Это указывает на то, что и рестрикция легочного сосудистого ложа - важный фактор патогенеза.
Два ведущих компонента в генезе ЛГ: функциональный: сужение легочных артериол (вазомоторное • увеличение общего легочного сосудистого сопротивления) при снижении в альвеолах р. О 2 и увеличении р. СО 2 (рефлекс Эйлера. Лильестранда); рост давления в бронхах и альвеолах; повышение МОК и концентрации метаболитов прессорного действия. Альвеолярная гипоксия -- главная причина возникновения легочной вазоконстрикции. Хроническая гипоксия (и последующая персистирующая вазоконстрикция) также благоприятствует повреждению легочных сосудов -- ремоделированию всех слоев сосудистой стенки из-за пролиферативных изменений (вазоактивные вещества высвобождающиеся из эндотелия, стимулируют пролиферацию эндотелия в стенке сосуда) и обструктивных изменений. Возникают -- мускуляризация артериол (продольный рост в них мышц и их гипертрофия), утолщение интимы (вследствие пролиферации ГМК и отложения коллагеновых и эластических волокон) и ее фиброз; • анатомический (органический): редукция сосудистого русла легких, сдавление извне или закрытие просвета сосудов в легочной артерии, мускуляризация артериол. Уровень ЛГ четко не коррелирует с КЩС крови. Это указывает на то, что и рестрикция легочного сосудистого ложа - важный фактор патогенеза.
 Соотношение факторов патогенеза ХЛС, морфологических изменений и вида заболеваний Основной компонент Характер изменений Заболевания Первичные (главные) механизмы Анатомический (увеличение легочного сосудистого сопротивления из-за снижения поперечного сечения сосудистого ложа) Облитерация, обструкция и редукция резистивных сосудов ТЭЛА, васкулиты, ИЛАГ, диффузные интерстициальные фиброзы Функциональный (вазомоторное увеличение легочного сосудистого сопротивления) Вазоконстрикция из-за гипоксии и ацидоза Общая альвеолярная гиповен-тиляция при нормальных легких: кифосколиоз, пиквикский синдром Преимущественно функциональный Сочетание вышеназванных факторов Общая альвеолярная гиповентиляция с изменениями в легких -- ХОБЛ, БА Вторичные (дополнительные) механизмы Рост сердечного выброса и скорости легочного кровотока Увеличение скорости ФН, активность в течение метаболизма, гипоксия дня, ОРВИ Повышение вязкости крови Вторичная полицитемия Хроническая гипоксия Тахикардия Усиление гипоксии ХСН
Соотношение факторов патогенеза ХЛС, морфологических изменений и вида заболеваний Основной компонент Характер изменений Заболевания Первичные (главные) механизмы Анатомический (увеличение легочного сосудистого сопротивления из-за снижения поперечного сечения сосудистого ложа) Облитерация, обструкция и редукция резистивных сосудов ТЭЛА, васкулиты, ИЛАГ, диффузные интерстициальные фиброзы Функциональный (вазомоторное увеличение легочного сосудистого сопротивления) Вазоконстрикция из-за гипоксии и ацидоза Общая альвеолярная гиповен-тиляция при нормальных легких: кифосколиоз, пиквикский синдром Преимущественно функциональный Сочетание вышеназванных факторов Общая альвеолярная гиповентиляция с изменениями в легких -- ХОБЛ, БА Вторичные (дополнительные) механизмы Рост сердечного выброса и скорости легочного кровотока Увеличение скорости ФН, активность в течение метаболизма, гипоксия дня, ОРВИ Повышение вязкости крови Вторичная полицитемия Хроническая гипоксия Тахикардия Усиление гипоксии ХСН
 Диагноз ХЛС при ХОБЛ поставить сложно вследствие того, что проявления самого ХОБЛ могут быть выражены мало, а клинические признаки ЛГ появляются поздно и не очень надежны. Нет и специфических симптомов, связанных с увеличением ГПЖ. Клинические проявления ХЛС складываются из: неспецифических признаков основного заболевания, ХДН, ЛГ, ГПЖ и ПЖ недостаточности. Вначале болезни клиническая картина ХЛС скудная и определяется, прежде всего, вызвавшим ее заболеванием (так как, изменения в сердце формируются медленно). Поэтому диагноз ЛГ (ХЛС) ставится обычно поздно (на первых порах верифицировать его нелегко). Симптомы, обусловленные ЛГ (одышка при небольшой ФН, повышенная усталость, тахикардия) обычно появляются при ДЛА>45 мм рт. ст. , их трудно отличить от клинических проявлений ХОБЛ. Выявление ряда клинических симптомов может быть затруднено наличием выраженной ЭЛ или большими колебаниями внутригрудного давления. Обычно главное подозрение на ХЛС появляется при появлении у больного в период обострения ХОБЛ периферических отеков (часто не являются истинными проявлениями ПЖ недостаточности).
Диагноз ХЛС при ХОБЛ поставить сложно вследствие того, что проявления самого ХОБЛ могут быть выражены мало, а клинические признаки ЛГ появляются поздно и не очень надежны. Нет и специфических симптомов, связанных с увеличением ГПЖ. Клинические проявления ХЛС складываются из: неспецифических признаков основного заболевания, ХДН, ЛГ, ГПЖ и ПЖ недостаточности. Вначале болезни клиническая картина ХЛС скудная и определяется, прежде всего, вызвавшим ее заболеванием (так как, изменения в сердце формируются медленно). Поэтому диагноз ЛГ (ХЛС) ставится обычно поздно (на первых порах верифицировать его нелегко). Симптомы, обусловленные ЛГ (одышка при небольшой ФН, повышенная усталость, тахикардия) обычно появляются при ДЛА>45 мм рт. ст. , их трудно отличить от клинических проявлений ХОБЛ. Выявление ряда клинических симптомов может быть затруднено наличием выраженной ЭЛ или большими колебаниями внутригрудного давления. Обычно главное подозрение на ХЛС появляется при появлении у больного в период обострения ХОБЛ периферических отеков (часто не являются истинными проявлениями ПЖ недостаточности).
 Целенаправленный осмотр больного в ряде случаев помогает выявить причину ЛГ -- ее могут вызвать поражение клапанов сердца и врожденные пороки сердца, повреждение миокарда и болезни легких. Физикальное обследование выявляет кардиомегалию, эпигастральную пульсацию (вследствие ГПЖ). Большую информацию дает аускультация сердца: характеристики 2 тона (его раздвоение и акцент над ЛА); наличие 3 -го тона; шума регургитации над мечевидным отростком (из-за недостаточности ТК при ПЖ недостаточности в покое); шума диастолической регургитации Грэхэма-Стила над ЛА. Легочное сердце может быть: острым в период декомпенсации ХОБЛ, часто вследствие острой респираторной инфекции или хроническим в ходе прогрессирования заболевания, ухудшения газообмена, ведущего к необратимому моделированию легочных сосудов. О венозном застое будут свидетельствовать отеки, зависящие от положения тела и набухание вен шеи. ЛГ часто протекает латентно, поэтому надо наблюдать в динамике за больным, которому угрожает развитие ЛГ. Доминирующими симптомами (характерными для основной болезни) могут быть: одышка и ортопноэ в случае патологии ЛЖ; головокружения, обмороки, боли в грудной клетке, напоминающие стенокардитические (из-за растяжения ПЖ) при ИЛАГ или симптомы со стороны легких у больных ХОБЛ. На начальных этапах формирования бронхолегочного ХЛС длительно превалируют симптомы (чаще ХДН) имеющегося заболевания, заметно усиливающиеся в период обострения
Целенаправленный осмотр больного в ряде случаев помогает выявить причину ЛГ -- ее могут вызвать поражение клапанов сердца и врожденные пороки сердца, повреждение миокарда и болезни легких. Физикальное обследование выявляет кардиомегалию, эпигастральную пульсацию (вследствие ГПЖ). Большую информацию дает аускультация сердца: характеристики 2 тона (его раздвоение и акцент над ЛА); наличие 3 -го тона; шума регургитации над мечевидным отростком (из-за недостаточности ТК при ПЖ недостаточности в покое); шума диастолической регургитации Грэхэма-Стила над ЛА. Легочное сердце может быть: острым в период декомпенсации ХОБЛ, часто вследствие острой респираторной инфекции или хроническим в ходе прогрессирования заболевания, ухудшения газообмена, ведущего к необратимому моделированию легочных сосудов. О венозном застое будут свидетельствовать отеки, зависящие от положения тела и набухание вен шеи. ЛГ часто протекает латентно, поэтому надо наблюдать в динамике за больным, которому угрожает развитие ЛГ. Доминирующими симптомами (характерными для основной болезни) могут быть: одышка и ортопноэ в случае патологии ЛЖ; головокружения, обмороки, боли в грудной клетке, напоминающие стенокардитические (из-за растяжения ПЖ) при ИЛАГ или симптомы со стороны легких у больных ХОБЛ. На начальных этапах формирования бронхолегочного ХЛС длительно превалируют симптомы (чаще ХДН) имеющегося заболевания, заметно усиливающиеся в период обострения
 При физикальном осмотре больных определяются симптомы, свойственные ХОБЛ: признаки эмфиземы грудной клетки, коробочный звук при перкуссии, снижение звучности везикулярного дыхания и сухие (иногда и влажные) хрипы, визинг, набухание шейных вен, теплый цианоз (из-за перехода части артериальной крови по шунтам сразу в венозную систему), тахикардия. Тоны сердца обычно трудно выслушать из-за наличия выраженной ЭЛ и большого количества сухих хрипов. Обычно вначале оценивают тип и тяжесть легочной патологии, а потом -- признаки ХЛС. Анализ вентиляции выявляет легкую или умеренную бронхиальную обструкцию. В последующем усиливаются клинические проявления болезни и формируется транзиторная ЛГ (предстадия в формировании стабильного ХЛС), особенно при обострении ХОБЛ. Могут определяться: приглушение тонов сердца и акцент 2 -го тона над ЛА; тахикардия (следствие воспалительного процесса в дыхательных путях и ХДН); нижний край печени (но не из-за увеличения ее размеров, а вследствие опущения диафрагмы); давление на область печени не усиливает набухание шейных вен (отрицательный симптом Плеша).
При физикальном осмотре больных определяются симптомы, свойственные ХОБЛ: признаки эмфиземы грудной клетки, коробочный звук при перкуссии, снижение звучности везикулярного дыхания и сухие (иногда и влажные) хрипы, визинг, набухание шейных вен, теплый цианоз (из-за перехода части артериальной крови по шунтам сразу в венозную систему), тахикардия. Тоны сердца обычно трудно выслушать из-за наличия выраженной ЭЛ и большого количества сухих хрипов. Обычно вначале оценивают тип и тяжесть легочной патологии, а потом -- признаки ХЛС. Анализ вентиляции выявляет легкую или умеренную бронхиальную обструкцию. В последующем усиливаются клинические проявления болезни и формируется транзиторная ЛГ (предстадия в формировании стабильного ХЛС), особенно при обострении ХОБЛ. Могут определяться: приглушение тонов сердца и акцент 2 -го тона над ЛА; тахикардия (следствие воспалительного процесса в дыхательных путях и ХДН); нижний край печени (но не из-за увеличения ее размеров, а вследствие опущения диафрагмы); давление на область печени не усиливает набухание шейных вен (отрицательный симптом Плеша).
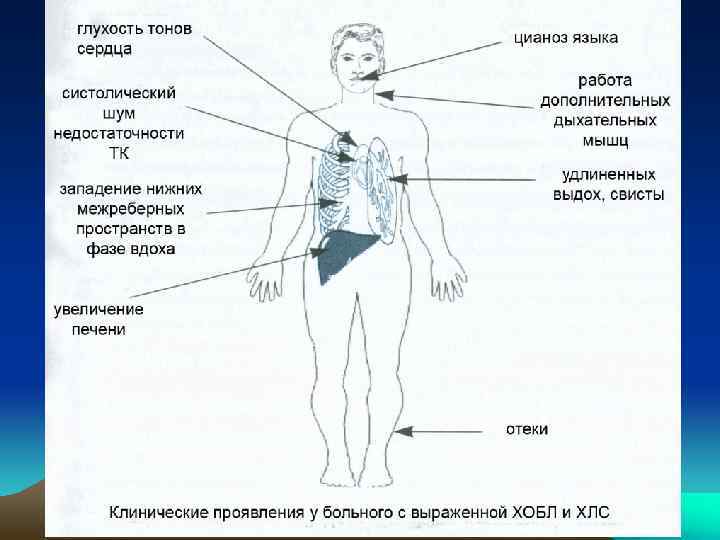
 Позднее формируется стабильная ЛГ с признаками компенсированного ХЛС (без явной ХСН), клиническая картина все еще определяется основным заболеванием, но заметно прогрессируют симптомы ХДН, нарушения микрокровотока. Больные нередко жалуются на: • ангинозные боли за грудиной (“легочная стенокардия”) вследствие гипоксемии, несоответствия доставки О 2 гипертрофированному миокарду ПЖ и пульмоно-кардиального рефлекса при ЛГ. Эта кардиалгия лучше лечится теофиллином (но плохо нитратами); • тяжесть в области печени и пастозность голеней к вечеру. У ряда больных ХОБЛ выявляется кашлево-обморочный синдром. При физикальном осмотре выявляются: выраженный, теплый, диффузный цианоз, одышка при умеренной ФН, тахикардия; опущение нижнего края печени (мягкий, безболезненный); набухание шейных вен в период выдоха и спадение при вдохе (может быть и в обе фазы, что четко указывает на ХЛС); участие вспомогательных мышц шеи и живота в акте дыхания; теплая кожа и ухудшение ментального статуса. Исследование сердца дает мало диагностической информации, из -за ЭЛ. Могут выявляться: эпигастральная пульсация (у 1/3 больных при выраженной патологии), разлитой сердечный толчок и перкуторное смещение границы сердца вправо; акцент 2 -го тона над ЛА (у 12 пациентов), реже -- диастолический шум Грехема-Стилла; очень редко -систолический шум на трехстворчатом клапане, усиливающийся при глубоком вдохе. Малая выраженность физикальных данных при ЛГ
Позднее формируется стабильная ЛГ с признаками компенсированного ХЛС (без явной ХСН), клиническая картина все еще определяется основным заболеванием, но заметно прогрессируют симптомы ХДН, нарушения микрокровотока. Больные нередко жалуются на: • ангинозные боли за грудиной (“легочная стенокардия”) вследствие гипоксемии, несоответствия доставки О 2 гипертрофированному миокарду ПЖ и пульмоно-кардиального рефлекса при ЛГ. Эта кардиалгия лучше лечится теофиллином (но плохо нитратами); • тяжесть в области печени и пастозность голеней к вечеру. У ряда больных ХОБЛ выявляется кашлево-обморочный синдром. При физикальном осмотре выявляются: выраженный, теплый, диффузный цианоз, одышка при умеренной ФН, тахикардия; опущение нижнего края печени (мягкий, безболезненный); набухание шейных вен в период выдоха и спадение при вдохе (может быть и в обе фазы, что четко указывает на ХЛС); участие вспомогательных мышц шеи и живота в акте дыхания; теплая кожа и ухудшение ментального статуса. Исследование сердца дает мало диагностической информации, из -за ЭЛ. Могут выявляться: эпигастральная пульсация (у 1/3 больных при выраженной патологии), разлитой сердечный толчок и перкуторное смещение границы сердца вправо; акцент 2 -го тона над ЛА (у 12 пациентов), реже -- диастолический шум Грехема-Стилла; очень редко -систолический шум на трехстворчатом клапане, усиливающийся при глубоком вдохе. Малая выраженность физикальных данных при ЛГ
 ХСН развивается на фоне выраженной первичной легочной патологии с наличием ЛГ и повышением общего легочного сосудистого сопротивления. Поэтому термин “легочно-сердечная недостаточность” удачнее отражает своеобразие формирования ХСН по ПЖ типу у больных ХОБЛ Клинические отличия ХДН от комбинации ХДН + ХСН по ПЖ типу (легочно-сердечная недостаточность) Симптомы ХДН+ХСН Одышка Умеренная Выраженная Цианоз Мало зависит от ФН Усиливается при ФН Набухание вен шеи Усиливается при кашле Постоянное Отеки Нет Есть Увеличение размеров сердца Нет Есть Венозное давление Нормальное Повышено Скорость кровотока в большом круге кровообращения Нормальная Снижена
ХСН развивается на фоне выраженной первичной легочной патологии с наличием ЛГ и повышением общего легочного сосудистого сопротивления. Поэтому термин “легочно-сердечная недостаточность” удачнее отражает своеобразие формирования ХСН по ПЖ типу у больных ХОБЛ Клинические отличия ХДН от комбинации ХДН + ХСН по ПЖ типу (легочно-сердечная недостаточность) Симптомы ХДН+ХСН Одышка Умеренная Выраженная Цианоз Мало зависит от ФН Усиливается при ФН Набухание вен шеи Усиливается при кашле Постоянное Отеки Нет Есть Увеличение размеров сердца Нет Есть Венозное давление Нормальное Повышено Скорость кровотока в большом круге кровообращения Нормальная Снижена
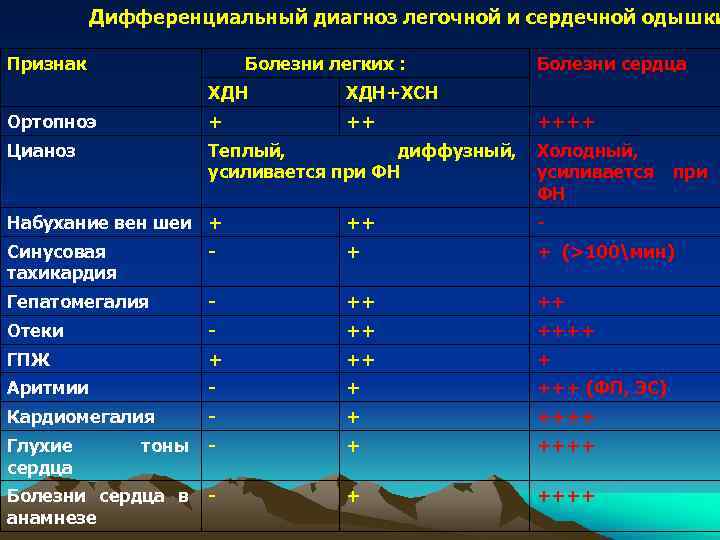 Дифференциальный диагноз легочной и сердечной одышки Признак Болезни легких : ХДН+ХСН Ортопноэ + ++ Цианоз Теплый, диффузный, усиливается при ФН Болезни сердца ++++ Холодный, усиливается ФН при Набухание вен шеи + ++ - Синусовая тахикардия - + + (>100мин) Гепатомегалия - ++ ++ Отеки - ++ ++++ ГПЖ + ++ + Аритмии - + +++ (ФП, ЭС) Кардиомегалия - + ++++ Глухие сердца тоны - + ++++ Болезни сердца в анамнезе - + ++++
Дифференциальный диагноз легочной и сердечной одышки Признак Болезни легких : ХДН+ХСН Ортопноэ + ++ Цианоз Теплый, диффузный, усиливается при ФН Болезни сердца ++++ Холодный, усиливается ФН при Набухание вен шеи + ++ - Синусовая тахикардия - + + (>100мин) Гепатомегалия - ++ ++ Отеки - ++ ++++ ГПЖ + ++ + Аритмии - + +++ (ФП, ЭС) Кардиомегалия - + ++++ Глухие сердца тоны - + ++++ Болезни сердца в анамнезе - + ++++
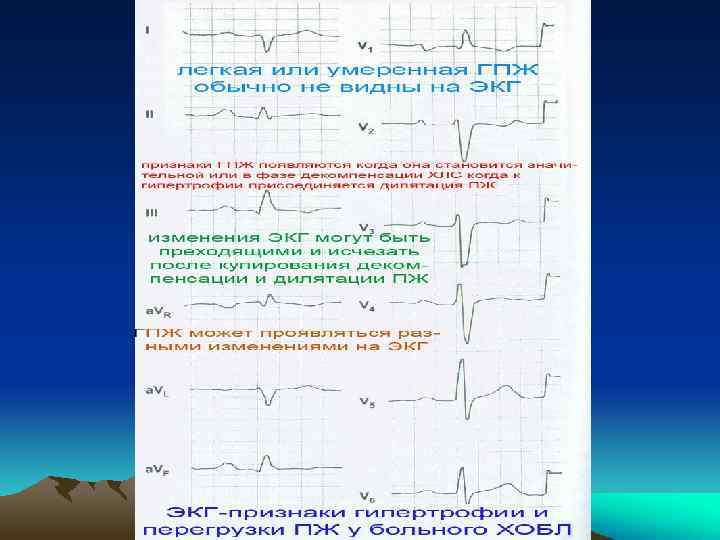
 Инструментальная диагностика ХЛС Главный патогенетический фактор его развития - ЛГ. Следовательно ее определение должно быть положено в основу ранней диагностики (ЛГ может быть обратимой в отличие от ГПЖ). Неинвазивные (косвенные) методики: антинуклеарные антитела при серологическом исследовании • (помогают исключить аутоиммунные заболевания - ДБСТ); • оценка КЩС (ночной гипоксемии -- ~25% больных с ночным апноэ имеют ЛГ); полисомнография и пульсоксиметрия (исключение ночных эпизодов гипоксии); • исследование вентиляции легких (обструкция дыхательных путей или рестриктивные нарушения). • ЭКГ- изменения могут быть обусловлены многими факторами: эпизодичностью и величиной ЛГ, смещением сердца эмфизематозными легкими, ишемией миокарда, метаболическими нарушениями. Критерии ХЛС у больных без обструкции бронхов: отклонение ЭОС вправо>110 o; зубец r. S (R/S<1, 0) в отведениях V 5 -6; зубец Rs (R/S>1, 0) в отв. V 1 -2; q. R в V 1 (указывает на тяжелую ЛГ); S 1 -S 2 -S 3 или S 1 -Q 3 -типы; нормальный вольтаж ЭКГ и P-pulmonale (амплитуда зубца Р>1, 5 мм). Недостаток ЭКГ методик -- появление характерных признаков ХЛС только при высокой ЛГ и значительной ГПЖ (чего часто нет при ХОБЛ). Обычно при высоком СДЛА (>75 мм рт. ст. ) ЭКГ симптомы выявляются всегда, при СДЛА ~5575 мм рт. ст. -- в половине случаев и при СДЛА ~ 35 -50 мм рт. ст. -- только в четверти случаев.
Инструментальная диагностика ХЛС Главный патогенетический фактор его развития - ЛГ. Следовательно ее определение должно быть положено в основу ранней диагностики (ЛГ может быть обратимой в отличие от ГПЖ). Неинвазивные (косвенные) методики: антинуклеарные антитела при серологическом исследовании • (помогают исключить аутоиммунные заболевания - ДБСТ); • оценка КЩС (ночной гипоксемии -- ~25% больных с ночным апноэ имеют ЛГ); полисомнография и пульсоксиметрия (исключение ночных эпизодов гипоксии); • исследование вентиляции легких (обструкция дыхательных путей или рестриктивные нарушения). • ЭКГ- изменения могут быть обусловлены многими факторами: эпизодичностью и величиной ЛГ, смещением сердца эмфизематозными легкими, ишемией миокарда, метаболическими нарушениями. Критерии ХЛС у больных без обструкции бронхов: отклонение ЭОС вправо>110 o; зубец r. S (R/S<1, 0) в отведениях V 5 -6; зубец Rs (R/S>1, 0) в отв. V 1 -2; q. R в V 1 (указывает на тяжелую ЛГ); S 1 -S 2 -S 3 или S 1 -Q 3 -типы; нормальный вольтаж ЭКГ и P-pulmonale (амплитуда зубца Р>1, 5 мм). Недостаток ЭКГ методик -- появление характерных признаков ХЛС только при высокой ЛГ и значительной ГПЖ (чего часто нет при ХОБЛ). Обычно при высоком СДЛА (>75 мм рт. ст. ) ЭКГ симптомы выявляются всегда, при СДЛА ~5575 мм рт. ст. -- в половине случаев и при СДЛА ~ 35 -50 мм рт. ст. -- только в четверти случаев.
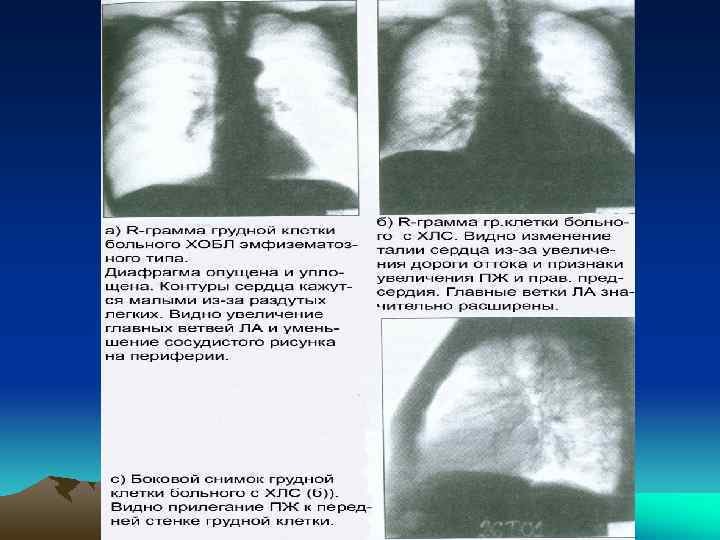
 • Эхо. КГ -- ведущий неинвазивный метод оценки функции сердца (патологии клапанов и миокарда), наличия и степени ЛГ, ГПЖ, позволяет визуализировать дилатацию правых отделов сердца (в норме диаметр ПЖ в диастолу <28 мм); верифицировать толщину передней стенки ПЖ (в норме толщина ПЖ составляет 2 -3 мм; диагноз ГПЖ ставится при толщине >3, 5 мм); нарушения профиля движения ПЖ, межжелудочковой перегородки и потоков в области клапанов ЛА и трехстворчатого клапана. Если на них есть регургитация (выявляется у ~50% больных ХОБЛ), то можно рассчитать и ДЛА; • рентгенологическое обследование легких иногда (при выраженной ХСН по ПЖ типу) помогает оценить паренхиму и значительное расширение прикорневых сосудов на фоне обеднения периферического легочного рисунка; выявить гипертрофию ППр и ПЖ на выраженных стадиях болезни; выбухание конуса и ствола ЛА; исключить или верифицировать умеренной тяжести болезни легких или существенное сужение сосудов в системе легочной циркуляции (ясные контры легочных полей на периферии на фоне скудного легочного рисунка и одновременного расширения крупных ветвей ЛА) или ЛГ, возникающую вследствие патологии левых отделов сердца (застой в легочном кровообращении, усиление рисунка легочных вен в верхних легочных полях). При большей части болезней, вызывающих ХЛС, у больных имеются патологические изменения на рентгенограмме легких (выраженная ЭЛ, кифосколиоз, фиброз легких) и выявить проявления ЛГ (дилатацию ствола ЛА и ее ветвей) и ГПЖ в этих условиях трудно.
• Эхо. КГ -- ведущий неинвазивный метод оценки функции сердца (патологии клапанов и миокарда), наличия и степени ЛГ, ГПЖ, позволяет визуализировать дилатацию правых отделов сердца (в норме диаметр ПЖ в диастолу <28 мм); верифицировать толщину передней стенки ПЖ (в норме толщина ПЖ составляет 2 -3 мм; диагноз ГПЖ ставится при толщине >3, 5 мм); нарушения профиля движения ПЖ, межжелудочковой перегородки и потоков в области клапанов ЛА и трехстворчатого клапана. Если на них есть регургитация (выявляется у ~50% больных ХОБЛ), то можно рассчитать и ДЛА; • рентгенологическое обследование легких иногда (при выраженной ХСН по ПЖ типу) помогает оценить паренхиму и значительное расширение прикорневых сосудов на фоне обеднения периферического легочного рисунка; выявить гипертрофию ППр и ПЖ на выраженных стадиях болезни; выбухание конуса и ствола ЛА; исключить или верифицировать умеренной тяжести болезни легких или существенное сужение сосудов в системе легочной циркуляции (ясные контры легочных полей на периферии на фоне скудного легочного рисунка и одновременного расширения крупных ветвей ЛА) или ЛГ, возникающую вследствие патологии левых отделов сердца (застой в легочном кровообращении, усиление рисунка легочных вен в верхних легочных полях). При большей части болезней, вызывающих ХЛС, у больных имеются патологические изменения на рентгенограмме легких (выраженная ЭЛ, кифосколиоз, фиброз легких) и выявить проявления ЛГ (дилатацию ствола ЛА и ее ветвей) и ГПЖ в этих условиях трудно.
 • ВПСЛ - для исключения ТЭЛА (как причины ХЛС); • нагрузочные пробы (вдыхание гипоксических и гипероксимических смесей или 6 мин ходьба) с изменением ЧСС, АД и вентиляции -позволяют выявить умеренную ЛГ и дисфункцию легких, которые не определяются в покое. На ранних стадиях ХОБЛ применение ФН (имеющаяся ХДН – главный ограничивающий фактор) приводит к ограничению вентиляции и ухудшению насыщения крови кислородом (гипоксемии), соответствующему росту СДЛА и снижению фракции выброса ПЖ (на 15%). • биопсия легких (посредством торакотомии или торакоскопии) – ее проводят редко, для идентификации этиологии ЛГ (подозрение на легочной васкулит). Таким образом, из неинвазивных методов прижизненной диагностики ЛГ (ХЛС), обычно применяемых в клинике, достаточно информативных нет. Достоверный метод определения ЛГ -- только прямое измерение СДЛА путем катетеризации правых отделов сердца, позволяющее отличить посткапиллярную ЛГ (вследствие митрального порока или ХСН по ЛЖ типу) от прекапиллярной, обусловленной ХОБЛ.
• ВПСЛ - для исключения ТЭЛА (как причины ХЛС); • нагрузочные пробы (вдыхание гипоксических и гипероксимических смесей или 6 мин ходьба) с изменением ЧСС, АД и вентиляции -позволяют выявить умеренную ЛГ и дисфункцию легких, которые не определяются в покое. На ранних стадиях ХОБЛ применение ФН (имеющаяся ХДН – главный ограничивающий фактор) приводит к ограничению вентиляции и ухудшению насыщения крови кислородом (гипоксемии), соответствующему росту СДЛА и снижению фракции выброса ПЖ (на 15%). • биопсия легких (посредством торакотомии или торакоскопии) – ее проводят редко, для идентификации этиологии ЛГ (подозрение на легочной васкулит). Таким образом, из неинвазивных методов прижизненной диагностики ЛГ (ХЛС), обычно применяемых в клинике, достаточно информативных нет. Достоверный метод определения ЛГ -- только прямое измерение СДЛА путем катетеризации правых отделов сердца, позволяющее отличить посткапиллярную ЛГ (вследствие митрального порока или ХСН по ЛЖ типу) от прекапиллярной, обусловленной ХОБЛ.
 Для верификации ХЛС необходимо последовательно выявить: • основное заболевание легких (или сосудов легких или патологии грудной клетки) и состояние активности воспалительного процесса в легких; • степень выраженности ХДН обструктивного или рестриктивного типа (анализ ФВД и КЩС, пульсоксиметрия); • ЛГ и ГПЖ; , • основной патогенетический механизм ЛГ (функциональный или анатомический); • течение ХЛС (острое, подострое или хроническое); • стадию болезни (компенсации или декомпенсации).
Для верификации ХЛС необходимо последовательно выявить: • основное заболевание легких (или сосудов легких или патологии грудной клетки) и состояние активности воспалительного процесса в легких; • степень выраженности ХДН обструктивного или рестриктивного типа (анализ ФВД и КЩС, пульсоксиметрия); • ЛГ и ГПЖ; , • основной патогенетический механизм ЛГ (функциональный или анатомический); • течение ХЛС (острое, подострое или хроническое); • стадию болезни (компенсации или декомпенсации).
 Дифференциальный диагноз “перегруженного” ПЖ и ЛЖ Симптомы «Перегруженный» ПЖ «Перегруженный» ЛЖ Основные заболевания ХОБЛ + ЛГ АГ, ИМ, пороки сердца и др. ЭКГ ГПЖ ГЛЖ Аускультация сердца Акцент 2 -го тона над ЛА Акцент 2 -го тона на аорте Боли в груди Часто связаны с дыханием Часто стенокардитические Объективные симптомы Мало, ортопноэ нет Ортопноэ Цианоз Выражен Умеренный Рентгенография легких Эмфизема, пневмосклероз, увеличение диаметра ЛА Симптомы застоя в легких Рентгенография сердца Нормальные размеры Увеличен размер ЛЖ (всего сердца), аортальная конфигурация Тип застоя Застой печени, почек, периферические отеки Застойные легкие Вентиляция Обструктивные, рестриктивные или смешанные нарушения Нормальная или слегка снижена МОК Норма или повышен Часто снижен ра. O 2 Снижено Нормальное АД в большом круге кровообращения Нормальное или снижено Чаще повышено
Дифференциальный диагноз “перегруженного” ПЖ и ЛЖ Симптомы «Перегруженный» ПЖ «Перегруженный» ЛЖ Основные заболевания ХОБЛ + ЛГ АГ, ИМ, пороки сердца и др. ЭКГ ГПЖ ГЛЖ Аускультация сердца Акцент 2 -го тона над ЛА Акцент 2 -го тона на аорте Боли в груди Часто связаны с дыханием Часто стенокардитические Объективные симптомы Мало, ортопноэ нет Ортопноэ Цианоз Выражен Умеренный Рентгенография легких Эмфизема, пневмосклероз, увеличение диаметра ЛА Симптомы застоя в легких Рентгенография сердца Нормальные размеры Увеличен размер ЛЖ (всего сердца), аортальная конфигурация Тип застоя Застой печени, почек, периферические отеки Застойные легкие Вентиляция Обструктивные, рестриктивные или смешанные нарушения Нормальная или слегка снижена МОК Норма или повышен Часто снижен ра. O 2 Снижено Нормальное АД в большом круге кровообращения Нормальное или снижено Чаще повышено



 Другие направления лечения начинают играть важную роль при выраженной степени гипоксии и гиперкапнии: • уменьшение пред-постнагрузки на ПЖ (ХЛС – «болезнь сердца» ) -- поддерживает его функционирование (рост обьема ПЖ приводит к снижению диастолического наполнения ЛЖ и недосточности трехстворчатого клапана): периферические вазодилататоры (БМКК после проведения исходной острой пробы), мочегонные (часто существенно улучшают клиническое состояние больных с симптомами ПЖ недостаточности), иногда (при отсутствии возможностей проведения ДОТ) курсы изоволемической гемодилюции у больных с гипоксическим эритроцитозом (кровопускание 300 мл с немедленным последующим вливанием реополиглюкина в том же объеме), позволяющие снизить гематокрит, вязкость крови и ДЛА; • улушение работоспособности миокарда и диафрагмальных мышц (милдронат, предуктал, ретаболил, чрескожная электростимуляция диафрагмы, специальная дыхательная гимнастика); коррекция микроциркуляторных и тромботических нарушений (улучшение реологических и коагулологических свойств • крови): антиагреганты (трентал, курантил, гепарин) и (варфарин) в случае тромбоза в системе ЛА (уровень МНО ~2, 0). АКНД
Другие направления лечения начинают играть важную роль при выраженной степени гипоксии и гиперкапнии: • уменьшение пред-постнагрузки на ПЖ (ХЛС – «болезнь сердца» ) -- поддерживает его функционирование (рост обьема ПЖ приводит к снижению диастолического наполнения ЛЖ и недосточности трехстворчатого клапана): периферические вазодилататоры (БМКК после проведения исходной острой пробы), мочегонные (часто существенно улучшают клиническое состояние больных с симптомами ПЖ недостаточности), иногда (при отсутствии возможностей проведения ДОТ) курсы изоволемической гемодилюции у больных с гипоксическим эритроцитозом (кровопускание 300 мл с немедленным последующим вливанием реополиглюкина в том же объеме), позволяющие снизить гематокрит, вязкость крови и ДЛА; • улушение работоспособности миокарда и диафрагмальных мышц (милдронат, предуктал, ретаболил, чрескожная электростимуляция диафрагмы, специальная дыхательная гимнастика); коррекция микроциркуляторных и тромботических нарушений (улучшение реологических и коагулологических свойств • крови): антиагреганты (трентал, курантил, гепарин) и (варфарин) в случае тромбоза в системе ЛА (уровень МНО ~2, 0). АКНД
 Дополнительные опции лечебной программы: • адекватный режим физической активности (ФН без усиления одышки, появления обмороков, болей в груди), избегание гипобарической гипоксии (уже на высоте 1500 м над уровнем моря, усиливает ЛГ) – не рекомендуются полеты в самолетах; • предупреждение инфекции (ВБП и гриппа), к ней больные с ЛГ очень чувствительны (вакцинация против гриппа и пневмонии); • предохранение от беременности женщинам с ЛГ (нежелательны гормональных контрацептивы из-за их тромбогенного влияния); • коррекция уровня Нв. Больные с хронической ЛГ очень чувствительны к снижению уровня Нв (любой вид анемии следует обязательно лечить). При развитии выраженного эритроцитоза (Ht>60%) показаны: ДОТ или кровопускания; • исключение ЛС, неблагоприятно влияющих на течение ЛГ: аноректики (фенфлурамин, дексафенфлюрамин), НПВС (резко повышают риск ЖКТ кровотечений), ИАПФ (усиливают гипотензию и ПЖ недостаточность); • психологическая поддержка (аутотренинг и психологическая релаксация).
Дополнительные опции лечебной программы: • адекватный режим физической активности (ФН без усиления одышки, появления обмороков, болей в груди), избегание гипобарической гипоксии (уже на высоте 1500 м над уровнем моря, усиливает ЛГ) – не рекомендуются полеты в самолетах; • предупреждение инфекции (ВБП и гриппа), к ней больные с ЛГ очень чувствительны (вакцинация против гриппа и пневмонии); • предохранение от беременности женщинам с ЛГ (нежелательны гормональных контрацептивы из-за их тромбогенного влияния); • коррекция уровня Нв. Больные с хронической ЛГ очень чувствительны к снижению уровня Нв (любой вид анемии следует обязательно лечить). При развитии выраженного эритроцитоза (Ht>60%) показаны: ДОТ или кровопускания; • исключение ЛС, неблагоприятно влияющих на течение ЛГ: аноректики (фенфлурамин, дексафенфлюрамин), НПВС (резко повышают риск ЖКТ кровотечений), ИАПФ (усиливают гипотензию и ПЖ недостаточность); • психологическая поддержка (аутотренинг и психологическая релаксация).
 Показания к неинвазивной ИВЛ: тяжелое обострение ХОБЛ с выраженной одышкой и явной работой дополнительных дыхательных мышц; умеренный – тяжелый ацидоз (р. Н<7, 35) или гиперкапния (Ра. СО 2>65 мм рт ст) или Ра. О 2<50 мм рт. ст. , несмотря на ДОТ
Показания к неинвазивной ИВЛ: тяжелое обострение ХОБЛ с выраженной одышкой и явной работой дополнительных дыхательных мышц; умеренный – тяжелый ацидоз (р. Н<7, 35) или гиперкапния (Ра. СО 2>65 мм рт ст) или Ра. О 2<50 мм рт. ст. , несмотря на ДОТ
 Предотвращение и лечение ПЖ недостаточности: • снижение постнагрузки на ПЖ за счет уменьшения общего легочного сопротивления и легочной вазоконстрикции (предотвращение гипоксемии); • оптимизация преднагрузки на ПЖ; • сохранение перфузии путем поддержания системного АД. Стратегия лечения также определяется и причиной развития ЛГ. Основные опции лечения тяжелой ЛГ: • бронхолитики и противовоспалительные ЛС; • антитромбоцитарные; • вазодилататоры (ДОТ, БМКК, антагонисты эндотелиновых рецепторов); • антикоагулянты (НМВГ, варфарин); • препятствие ремоделирования сосудов (донаторы NO, антагонисты эндотелиновых рецепторов). • предсердная баллоная септостомия (искусственный шунт крови справо-налево с разгрузкой ППр и ПЖ); • пересадка комплекса седце-легкие (при ИЛАГ и отсутствии эффекта от других лечебных опций)
Предотвращение и лечение ПЖ недостаточности: • снижение постнагрузки на ПЖ за счет уменьшения общего легочного сопротивления и легочной вазоконстрикции (предотвращение гипоксемии); • оптимизация преднагрузки на ПЖ; • сохранение перфузии путем поддержания системного АД. Стратегия лечения также определяется и причиной развития ЛГ. Основные опции лечения тяжелой ЛГ: • бронхолитики и противовоспалительные ЛС; • антитромбоцитарные; • вазодилататоры (ДОТ, БМКК, антагонисты эндотелиновых рецепторов); • антикоагулянты (НМВГ, варфарин); • препятствие ремоделирования сосудов (донаторы NO, антагонисты эндотелиновых рецепторов). • предсердная баллоная септостомия (искусственный шунт крови справо-налево с разгрузкой ППр и ПЖ); • пересадка комплекса седце-легкие (при ИЛАГ и отсутствии эффекта от других лечебных опций)
 В лечении тяжелой ЛГ у больных (которые не переносят БМКК или при их неэффективности) применяют: • простагландин Е 1 (в/в длительно, посредством специального портативного насоса в варьирующей дозе от 5 -30 нг/кг/мин); • блокаторы ЭТ (А, В)-рецепторов эндотелина (оказывающего неблагоприятный эффект на легочную гемодинамику, мощное сосудосуживающее и пролиферативное действие): бозентан (обладает антипролиферативным, антифибротическим и антивоспалительным эффектами и вызывает селективную вазодилатацию, пораженных легочных сосудов) -- внутрь (первые 4 недели по 62, 25 мг, 2 р/сут, позднее дозу повышают до 125 мг по 2 р/сут) или в/в 0, 5 г/сут); • аналоги простациклина, вырабатывающегося клетками эндотелия (вызывающие: расслабление гладких мышц сосудов и их расширение; антипролиферативное действие; сильную блокаду агрегации тромбоцитов; улучшающие функцию ПЖ и повышающие ТФН) – эпопростенол (в виде непрерывной в/в инфузии вначале 4 нгкгмин из-за короткого периода полужизни), трептостинил пк в инфузомате (1. 25 нгкгмин), илопрост (в/в или ингаляционно, по 6 -12 ингаляций/сут); • силденафил (ингибитор фосфодиэстеразы 5 -го типа, разрушающей гуанозин-монофосфат, который вызывает расслабление гладкой мускулатуры), оказывающий выраженный легочной вазодилятирующий эффект (по 20 -40 мг, 3 р/сут).
В лечении тяжелой ЛГ у больных (которые не переносят БМКК или при их неэффективности) применяют: • простагландин Е 1 (в/в длительно, посредством специального портативного насоса в варьирующей дозе от 5 -30 нг/кг/мин); • блокаторы ЭТ (А, В)-рецепторов эндотелина (оказывающего неблагоприятный эффект на легочную гемодинамику, мощное сосудосуживающее и пролиферативное действие): бозентан (обладает антипролиферативным, антифибротическим и антивоспалительным эффектами и вызывает селективную вазодилатацию, пораженных легочных сосудов) -- внутрь (первые 4 недели по 62, 25 мг, 2 р/сут, позднее дозу повышают до 125 мг по 2 р/сут) или в/в 0, 5 г/сут); • аналоги простациклина, вырабатывающегося клетками эндотелия (вызывающие: расслабление гладких мышц сосудов и их расширение; антипролиферативное действие; сильную блокаду агрегации тромбоцитов; улучшающие функцию ПЖ и повышающие ТФН) – эпопростенол (в виде непрерывной в/в инфузии вначале 4 нгкгмин из-за короткого периода полужизни), трептостинил пк в инфузомате (1. 25 нгкгмин), илопрост (в/в или ингаляционно, по 6 -12 ингаляций/сут); • силденафил (ингибитор фосфодиэстеразы 5 -го типа, разрушающей гуанозин-монофосфат, который вызывает расслабление гладкой мускулатуры), оказывающий выраженный легочной вазодилятирующий эффект (по 20 -40 мг, 3 р/сут).
 Профилактика ХЛС заключается в своевременном лечении обострений инфекции в дыхательных путях, активной коррекции ХДН, ограничении ФН, своевременном и рациональном трудоустройстве больных ХОБЛ. Прогноз зависит от: этиологии заболевания легких, осложнившегося ХЛС, лечебного контроля за ним и степени имеющейся ЛГ (“розовые, пыхтящие” больные ХОБЛ живут больше “синих, отечных”). Наличие сосуществующих ЛГ и ХОБЛ -- плохой прогностический признак (в течение 3 -5 лет наступает летальный исход от нарастающей ХДН или от комбинации кардио-легочной декомпенсации). Несмотря на определенные успехи в лечении ХЛС, прогноз становится неблагоприятным уже при первом появлении ДХЛС (средний срок жизни составляет ~15 мес). Больные ХОБЛ с ХЛС имеют 50% выживаемость в течение 7 лет, а без наличия ХЛС -- в 2 раза больше. С уровнем ЛГ тесно коррелирует и 5 -летняя выживаемость больных. Так, при ЛГ<25 мм рт. ст. прогноз хороший; при ЛГ ~ 2530 мм рт. ст. 5 -летняя выживаемость ~50%, при ЛГ ~40 мм рт. ст. -- ~40%, при ЛГ>45 мм рт. снижалась до 10%.
Профилактика ХЛС заключается в своевременном лечении обострений инфекции в дыхательных путях, активной коррекции ХДН, ограничении ФН, своевременном и рациональном трудоустройстве больных ХОБЛ. Прогноз зависит от: этиологии заболевания легких, осложнившегося ХЛС, лечебного контроля за ним и степени имеющейся ЛГ (“розовые, пыхтящие” больные ХОБЛ живут больше “синих, отечных”). Наличие сосуществующих ЛГ и ХОБЛ -- плохой прогностический признак (в течение 3 -5 лет наступает летальный исход от нарастающей ХДН или от комбинации кардио-легочной декомпенсации). Несмотря на определенные успехи в лечении ХЛС, прогноз становится неблагоприятным уже при первом появлении ДХЛС (средний срок жизни составляет ~15 мес). Больные ХОБЛ с ХЛС имеют 50% выживаемость в течение 7 лет, а без наличия ХЛС -- в 2 раза больше. С уровнем ЛГ тесно коррелирует и 5 -летняя выживаемость больных. Так, при ЛГ<25 мм рт. ст. прогноз хороший; при ЛГ ~ 2530 мм рт. ст. 5 -летняя выживаемость ~50%, при ЛГ ~40 мм рт. ст. -- ~40%, при ЛГ>45 мм рт. снижалась до 10%.


