ХМЛ-обновленная.ppt
- Количество слайдов: 56
 Лечение хронического миелоидного лейкоза : версия 2009 Масчан А. А. ФНКЦ Детской Гематологии, Онкологии и Иммунологии
Лечение хронического миелоидного лейкоза : версия 2009 Масчан А. А. ФНКЦ Детской Гематологии, Онкологии и Иммунологии
 ХМЛ § ежегодно выявляется 300, 000 новых случаев лейкемии (~3% всех онкологических заболеваний) § умирает от лейкемии 220, 000 пациентов • ХМЛ составляет 15 % лейкемий у взрослых • Частота 1 -2 /100 000 в год • Медиана возраста заболевших 45 -55 лет
ХМЛ § ежегодно выявляется 300, 000 новых случаев лейкемии (~3% всех онкологических заболеваний) § умирает от лейкемии 220, 000 пациентов • ХМЛ составляет 15 % лейкемий у взрослых • Частота 1 -2 /100 000 в год • Медиана возраста заболевших 45 -55 лет
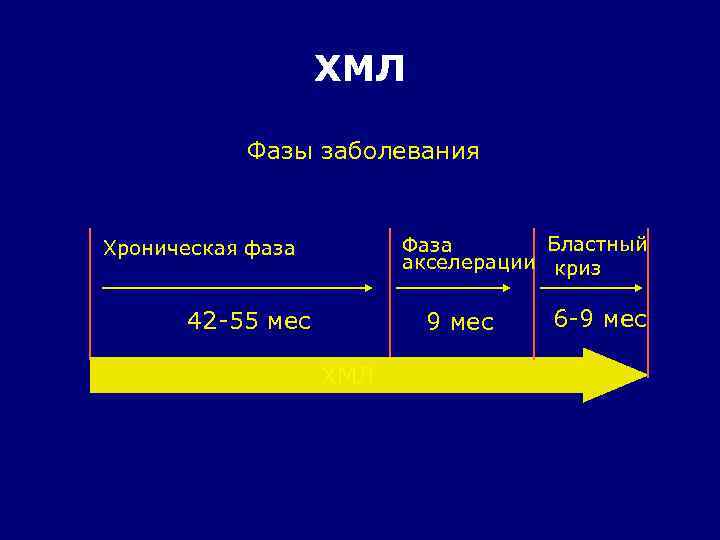 ХМЛ Фазы заболевания Бластный Фаза акселерации криз Хроническая фаза 42 -55 мес 9 мес ХМЛ 6 -9 мес
ХМЛ Фазы заболевания Бластный Фаза акселерации криз Хроническая фаза 42 -55 мес 9 мес ХМЛ 6 -9 мес
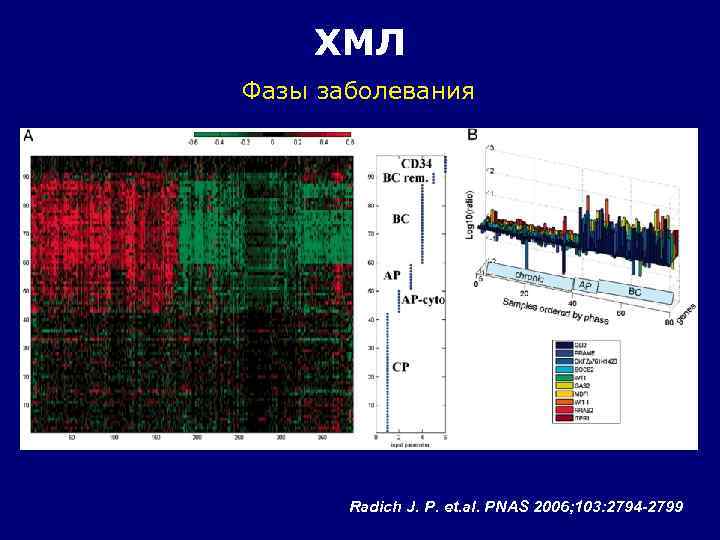 ХМЛ Фазы заболевания Radich J. P. et. al. PNAS 2006; 103: 2794 -2799
ХМЛ Фазы заболевания Radich J. P. et. al. PNAS 2006; 103: 2794 -2799
 ХМЛ : фаза акселерации ВОЗ Эксперты Leukemia Net Бластоз к/м или кровь 10 -19% 15 -29% Базофилы крови 20% Тромбоциты < 100 х109/л + + Бласты + промиелоциты - > 30% Лейкоцитоза и селезёнки + не учитывается несмотря на лечение Дополнительные + не учитывается хромосомные аномалии Тромбоцитоз > 1000 000/мкл + не учитывается
ХМЛ : фаза акселерации ВОЗ Эксперты Leukemia Net Бластоз к/м или кровь 10 -19% 15 -29% Базофилы крови 20% Тромбоциты < 100 х109/л + + Бласты + промиелоциты - > 30% Лейкоцитоза и селезёнки + не учитывается несмотря на лечение Дополнительные + не учитывается хромосомные аномалии Тромбоцитоз > 1000 000/мкл + не учитывается
 ХМЛ Бластный криз Бласты >30% (лимфобласты >20%) или Хлорома Миелоидный тип 2/3 Лимфобластный тип 1/3 Недифференцированный
ХМЛ Бластный криз Бласты >30% (лимфобласты >20%) или Хлорома Миелоидный тип 2/3 Лимфобластный тип 1/3 Недифференцированный
 ХМЛ: БЛАСТНЫЙ КРИЗ Дополнительные цитогенетические аномалии 60 -80% Трисомия 8 33% Доп Ph’(+) 30% Изохромосома 17 20% Трисомия 19 12% Потеря Y 8% Трисомия 21 7% Моносомия 7 5% Johansson et al Acta Hematol 2002; 107: 76 -94
ХМЛ: БЛАСТНЫЙ КРИЗ Дополнительные цитогенетические аномалии 60 -80% Трисомия 8 33% Доп Ph’(+) 30% Изохромосома 17 20% Трисомия 19 12% Потеря Y 8% Трисомия 21 7% Моносомия 7 5% Johansson et al Acta Hematol 2002; 107: 76 -94
 ХМЛ Диагноз Предположительный гематологическая картина клиника Окончательный обнаружение t(9; 22) и/или bcr/abl
ХМЛ Диагноз Предположительный гематологическая картина клиника Окончательный обнаружение t(9; 22) и/или bcr/abl
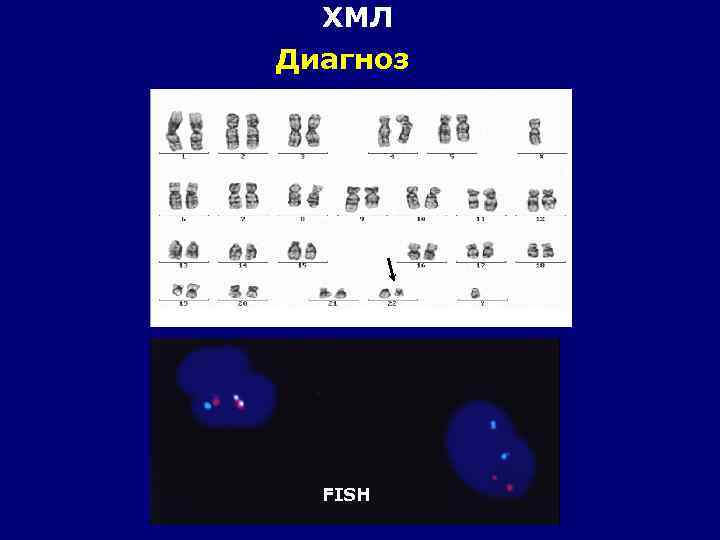 ХМЛ Диагноз FISH
ХМЛ Диагноз FISH
 ХМЛ дифференциальный диагноз • Атипичный ХМЛ • ЮММЛ • ХММо. Л • Миелофиброз • Эссенциальная тромбоцитемия • Истинная полицитемия • ОМЛ с t (8; 21) • Лейкемоидные реакции
ХМЛ дифференциальный диагноз • Атипичный ХМЛ • ЮММЛ • ХММо. Л • Миелофиброз • Эссенциальная тромбоцитемия • Истинная полицитемия • ОМЛ с t (8; 21) • Лейкемоидные реакции
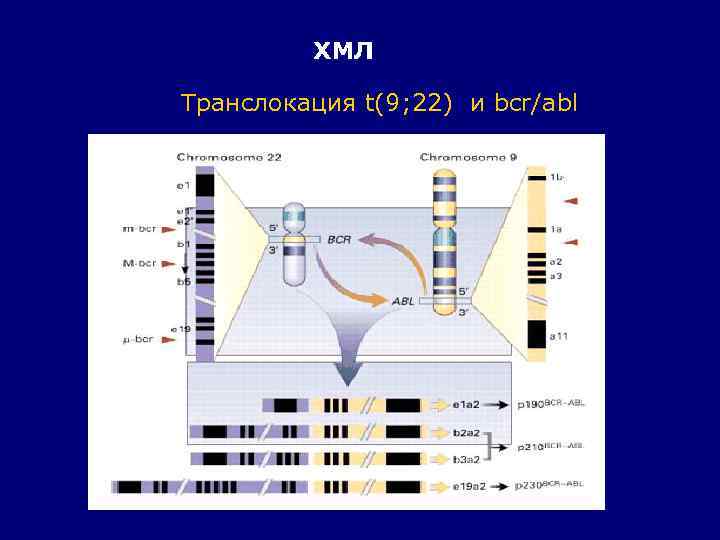 ХМЛ Транслокация t(9; 22) и bcr/abl
ХМЛ Транслокация t(9; 22) и bcr/abl
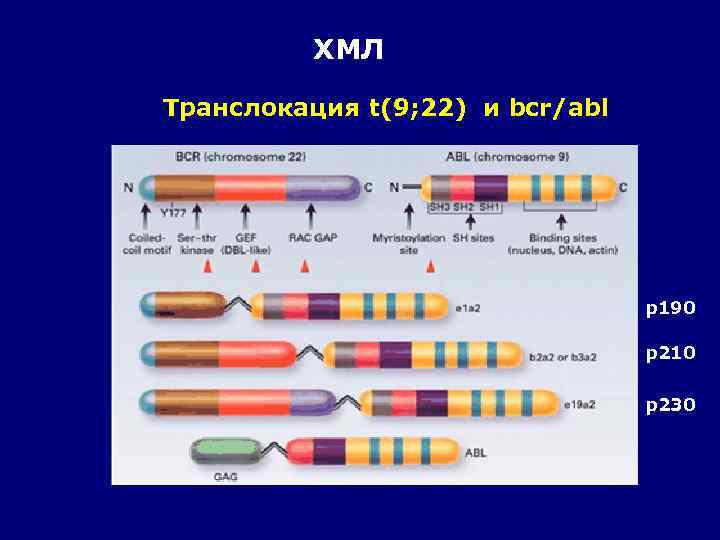 ХМЛ Транслокация t(9; 22) и bcr/abl p 190 p 210 p 230
ХМЛ Транслокация t(9; 22) и bcr/abl p 190 p 210 p 230
 ХМЛ Транслокация t(9; 22) и bcr/abl p 210 «Классический» ХМЛ p 190 1 -2% Гиперлейкоцитоз Моноцитоз Быстрая прогрессия
ХМЛ Транслокация t(9; 22) и bcr/abl p 210 «Классический» ХМЛ p 190 1 -2% Гиперлейкоцитоз Моноцитоз Быстрая прогрессия
 ХМЛ bcr/abl • Тирозинкиназный домен abl • C конституциональной активностью • Без внутренней ингибиции
ХМЛ bcr/abl • Тирозинкиназный домен abl • C конституциональной активностью • Без внутренней ингибиции
 ХМЛ события, модулируемые BCR/ABL • Сниженный апоптоз Ph’(+) клона • Нарушения связи Ph’(+) клеток и стромы • Независимость от G-CSF • Нестабильность генома (гипермутабельный фенотип) увеличение скорости мутаций вторичные лейкемогенные события
ХМЛ события, модулируемые BCR/ABL • Сниженный апоптоз Ph’(+) клона • Нарушения связи Ph’(+) клеток и стромы • Независимость от G-CSF • Нестабильность генома (гипермутабельный фенотип) увеличение скорости мутаций вторичные лейкемогенные события
 ХМЛ Возможности терапии • Алло ТКМ • Интерферон- • Гливек и другие ингибиторы ТК • Гидроксимочевина
ХМЛ Возможности терапии • Алло ТКМ • Интерферон- • Гливек и другие ингибиторы ТК • Гидроксимочевина
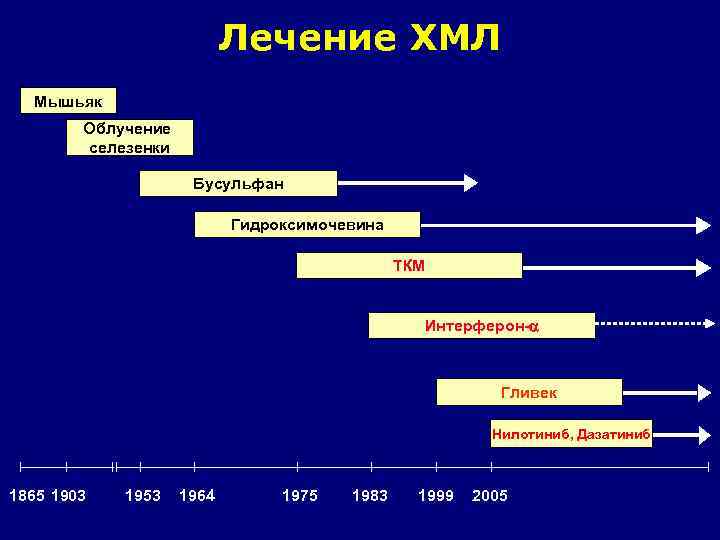 Лечение ХМЛ Мышьяк Облучение селезенки Бусульфан Гидроксимочевина ТКМ Интерферон- Гливек Нилотиниб, Дазатиниб 1865 1903 1953 1964 1975 1983 1999 2005
Лечение ХМЛ Мышьяк Облучение селезенки Бусульфан Гидроксимочевина ТКМ Интерферон- Гливек Нилотиниб, Дазатиниб 1865 1903 1953 1964 1975 1983 1999 2005
 Лечение ХМЛ Мышьяк Robert Fowler 1% As O 3
Лечение ХМЛ Мышьяк Robert Fowler 1% As O 3
 Лечение ХМЛ: мышьяк Lancet 1882 Artur Conan Doyle
Лечение ХМЛ: мышьяк Lancet 1882 Artur Conan Doyle
 Лечение ХМЛ
Лечение ХМЛ
 ХМЛ: лечение метод лечебный механизм Алло ТКМ • Циторедукция • Эффект «Graft- vs- leukemia» IFN- • антипролиферативный • стимуляция bcr/abl специфического иммунитета Гливек • Блокада bcr/abl - киназы • Генерация дендритных клеток • Снижение уровня мутаций до нормы
ХМЛ: лечение метод лечебный механизм Алло ТКМ • Циторедукция • Эффект «Graft- vs- leukemia» IFN- • антипролиферативный • стимуляция bcr/abl специфического иммунитета Гливек • Блокада bcr/abl - киназы • Генерация дендритных клеток • Снижение уровня мутаций до нормы
 ХМЛ: лечение Характеристика эффекта лечения Клинико-гематологическая ремиссия Нет спленомегалии Тромбоцитоз < 450 000/мкл L-цитоз <10 000/мкл нет молодых миелоидных форм базофилы < 5% Цитогенетическая ремиссия 100% метафаз(интерфаз) Ph(-) Молекулярная ремиссия bcr/abl 10 -5
ХМЛ: лечение Характеристика эффекта лечения Клинико-гематологическая ремиссия Нет спленомегалии Тромбоцитоз < 450 000/мкл L-цитоз <10 000/мкл нет молодых миелоидных форм базофилы < 5% Цитогенетическая ремиссия 100% метафаз(интерфаз) Ph(-) Молекулярная ремиссия bcr/abl 10 -5
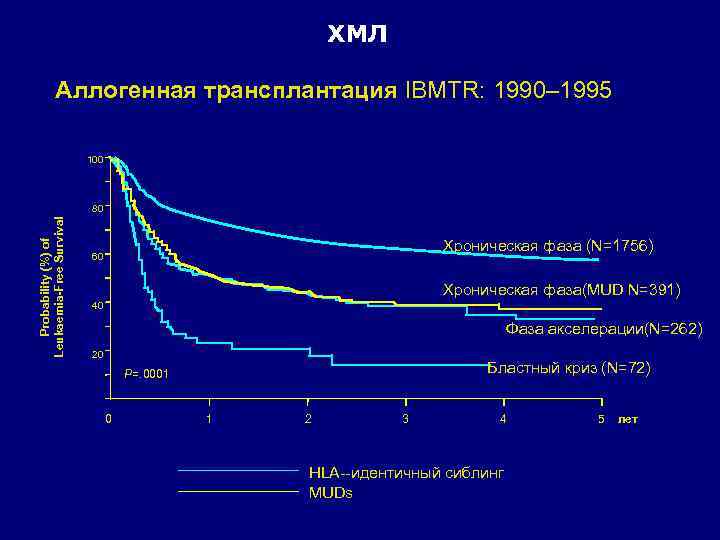 ХМЛ Аллогенная трансплантация IBMTR: 1990– 1995 100 Probability (%) of Leukaemia-Free Survival 80 Хроническая фаза (N=1756) 60 Хроническая фаза(MUD N=391) 40 Фаза акселерации(N=262) 20 Бластный криз (N=72) P=. 0001 0 1 2 3 4 HLA--идентичный сиблинг MUDs 5 лет
ХМЛ Аллогенная трансплантация IBMTR: 1990– 1995 100 Probability (%) of Leukaemia-Free Survival 80 Хроническая фаза (N=1756) 60 Хроническая фаза(MUD N=391) 40 Фаза акселерации(N=262) 20 Бластный криз (N=72) P=. 0001 0 1 2 3 4 HLA--идентичный сиблинг MUDs 5 лет
 ХМЛ Возможности терапии : алло ТКМ Родственная Неродственная • Есть донор у 20 -30% • Донор у 70% пациентов • Ранняя смертность ~ • Ранняя смертность ~ 15 10% • Излечение 50 -60% • Дети: возможность рождения донора -20% • Излечение 50 -60% • Стоимость
ХМЛ Возможности терапии : алло ТКМ Родственная Неродственная • Есть донор у 20 -30% • Донор у 70% пациентов • Ранняя смертность ~ • Ранняя смертность ~ 15 10% • Излечение 50 -60% • Дети: возможность рождения донора -20% • Излечение 50 -60% • Стоимость
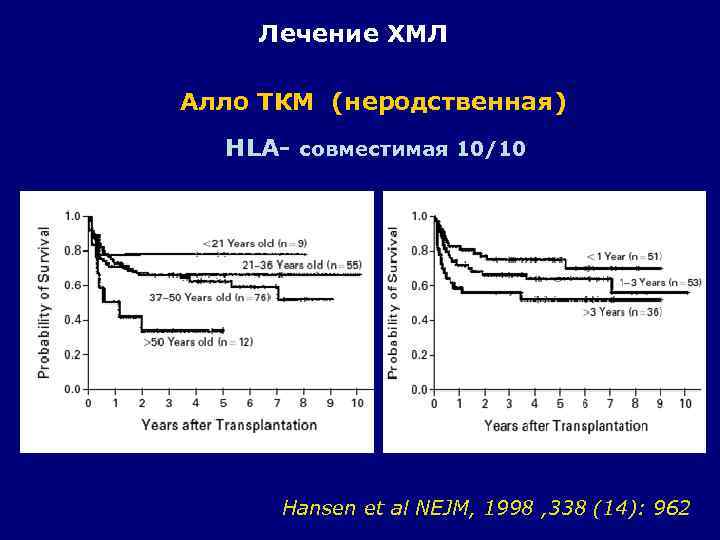 Лечение ХМЛ Алло ТКМ (неродственная) HLA- совместимая 10/10 Hansen et al NEJM, 1998 , 338 (14): 962
Лечение ХМЛ Алло ТКМ (неродственная) HLA- совместимая 10/10 Hansen et al NEJM, 1998 , 338 (14): 962
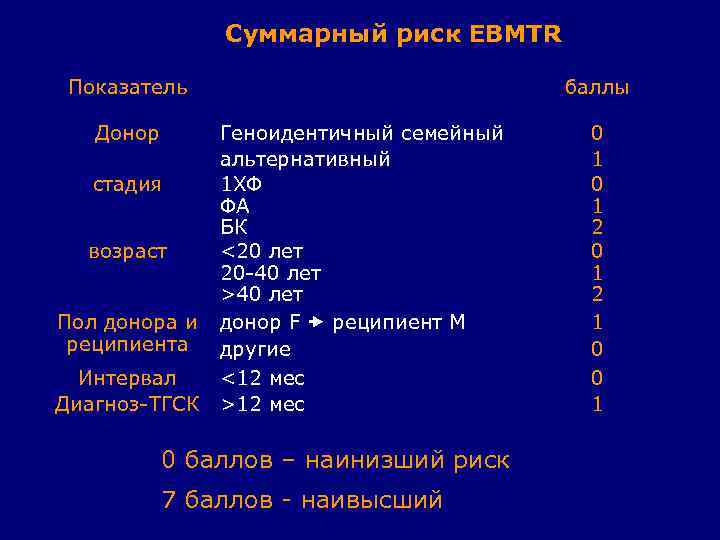 Суммарный риск EBMTR Показатель баллы Донор 0 1 2 1 0 0 1 Геноидентичный семейный альтернативный стадия 1 ХФ ФА БК возраст <20 лет 20 -40 лет >40 лет Пол донора и донор F реципиент М реципиента другие Интервал <12 мес Диагноз-ТГСК >12 мес 0 баллов – наинизший риск 7 баллов - наивысший
Суммарный риск EBMTR Показатель баллы Донор 0 1 2 1 0 0 1 Геноидентичный семейный альтернативный стадия 1 ХФ ФА БК возраст <20 лет 20 -40 лет >40 лет Пол донора и донор F реципиент М реципиента другие Интервал <12 мес Диагноз-ТГСК >12 мес 0 баллов – наинизший риск 7 баллов - наивысший
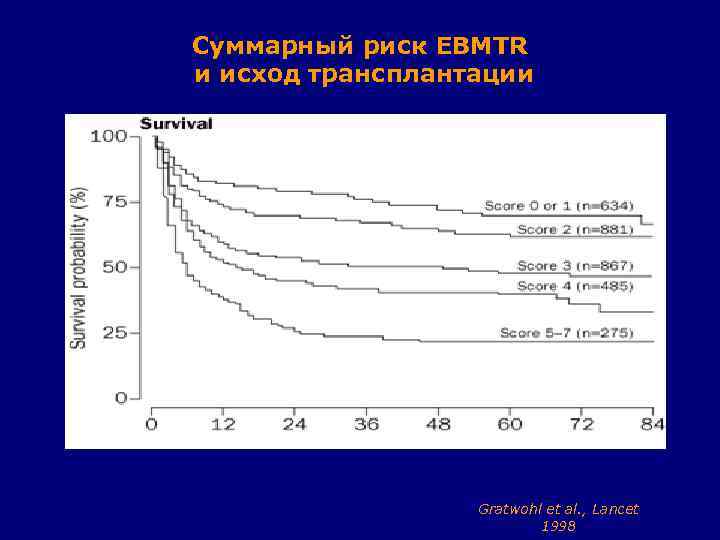 Суммарный риск EBMTR и исход трансплантации Gratwohl et al. , Lancet 1998
Суммарный риск EBMTR и исход трансплантации Gratwohl et al. , Lancet 1998
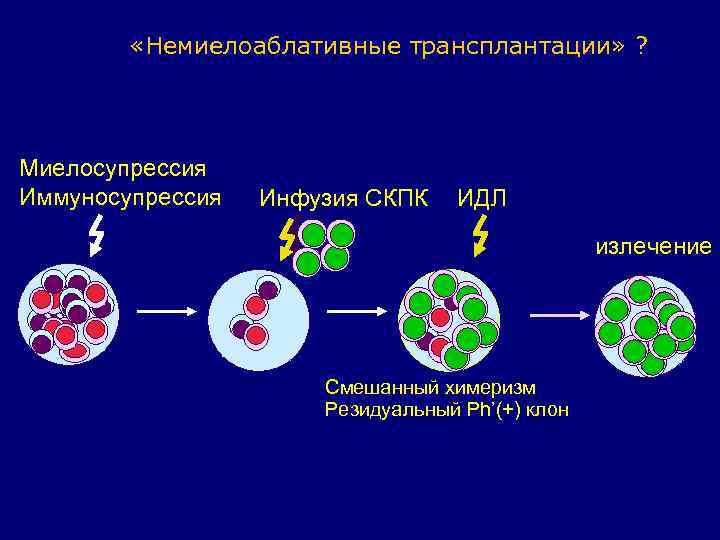 «Немиелоаблативные трансплантации» ? Миелосупрессия Иммуносупрессия Инфузия СКПК ИДЛ излечение Смешанный химеризм Резидуальный Ph’(+) клон
«Немиелоаблативные трансплантации» ? Миелосупрессия Иммуносупрессия Инфузия СКПК ИДЛ излечение Смешанный химеризм Резидуальный Ph’(+) клон
 Кто сегодня является кандидатом на ТГСК? На момент презентации Бластный криз + акселерация (ТКМ после ТКИ) После лечения иматинибом Первично резистентные T 315 I Дети ? ? ? После лечения дазатинибом/нилотинибом Не достигшие ПЦГО Утратившие ПЦГО Не переносящие ТКИ
Кто сегодня является кандидатом на ТГСК? На момент презентации Бластный криз + акселерация (ТКМ после ТКИ) После лечения иматинибом Первично резистентные T 315 I Дети ? ? ? После лечения дазатинибом/нилотинибом Не достигшие ПЦГО Утратившие ПЦГО Не переносящие ТКИ
 ХМЛ: Интерферон- Роферон, Интрон А, Пегасис, ПЕГ-Интрон Излечение < 5% Многолетняя терапия Стоимость (5 MU/m 2 в день) ~ $15 000/год Ранняя смертность 0% Негативное влияние на исход ТКМ
ХМЛ: Интерферон- Роферон, Интрон А, Пегасис, ПЕГ-Интрон Излечение < 5% Многолетняя терапия Стоимость (5 MU/m 2 в день) ~ $15 000/год Ранняя смертность 0% Негативное влияние на исход ТКМ
 ХМЛ лечение интерфероном- Виды цитогенетического ответа Ph’(+) метафаз Полный ответ 0% Частичный ответ 1 -35% Малый ответ 35 -95% большой ц/г ответ
ХМЛ лечение интерфероном- Виды цитогенетического ответа Ph’(+) метафаз Полный ответ 0% Частичный ответ 1 -35% Малый ответ 35 -95% большой ц/г ответ
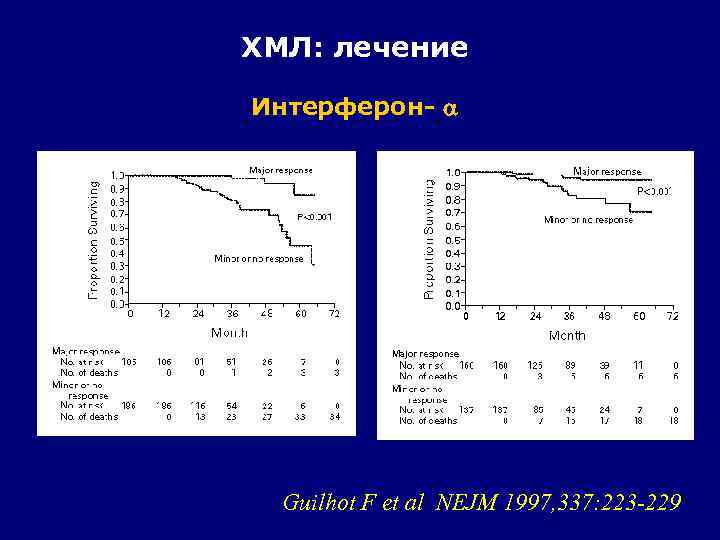 ХМЛ: лечение Интерферон- Guilhot F et al NEJM 1997, 337: 223 -229
ХМЛ: лечение Интерферон- Guilhot F et al NEJM 1997, 337: 223 -229
 ХМЛ и интерферон: прогноз Hasford Возраст 0, 666 при > 50 лет Селезенка 0. 042 x селезенка см Тромбоциты 1. 0956 при тромбоцитах ≥ 1500 x 109 /L Миелобласты 0. 0584 x миелобласты % Базофилы крови 0. 20399 при базофилах > 3% Эозинофилы крови 0. 0413 x Эозинофилы % х1000 Низкий рис <780 Промежуточный 781 -1480 Высокий >1480
ХМЛ и интерферон: прогноз Hasford Возраст 0, 666 при > 50 лет Селезенка 0. 042 x селезенка см Тромбоциты 1. 0956 при тромбоцитах ≥ 1500 x 109 /L Миелобласты 0. 0584 x миелобласты % Базофилы крови 0. 20399 при базофилах > 3% Эозинофилы крови 0. 0413 x Эозинофилы % х1000 Низкий рис <780 Промежуточный 781 -1480 Высокий >1480
 Вероятность выживания ХМЛ и интерферон 10 лет- 40% p<0. 0001 Низкий Промежуточный Высокий med med 100 мес 69 мес 45 мес Годы от диагноза Hasford et al. JNCI 90, 850 (1998)
Вероятность выживания ХМЛ и интерферон 10 лет- 40% p<0. 0001 Низкий Промежуточный Высокий med med 100 мес 69 мес 45 мес Годы от диагноза Hasford et al. JNCI 90, 850 (1998)
 Интерферон- Место интерферона в 2009 При непереносимости всех ТКИ Для поддержания ремиссии при беременности? Для поддержания полной молекулярной ремиссии? И… Отмены ТКИ? ? ?
Интерферон- Место интерферона в 2009 При непереносимости всех ТКИ Для поддержания ремиссии при беременности? Для поддержания полной молекулярной ремиссии? И… Отмены ТКИ? ? ?
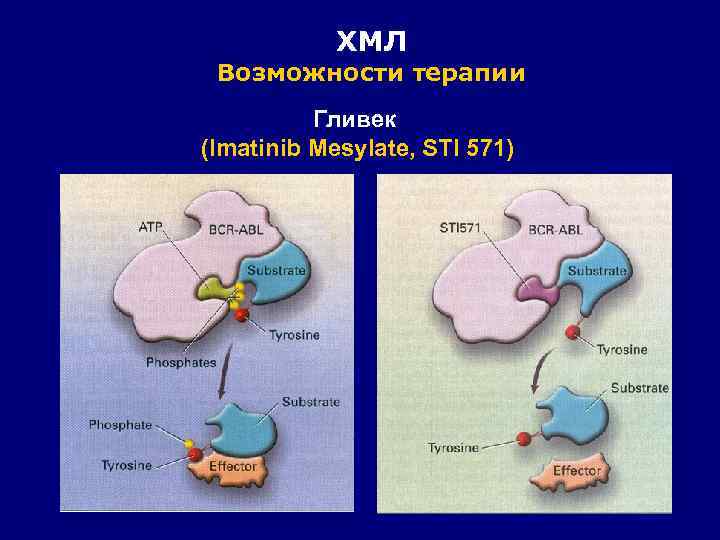 ХМЛ Возможности терапии Гливек (Imatinib Mesylate, STI 571)
ХМЛ Возможности терапии Гливек (Imatinib Mesylate, STI 571)
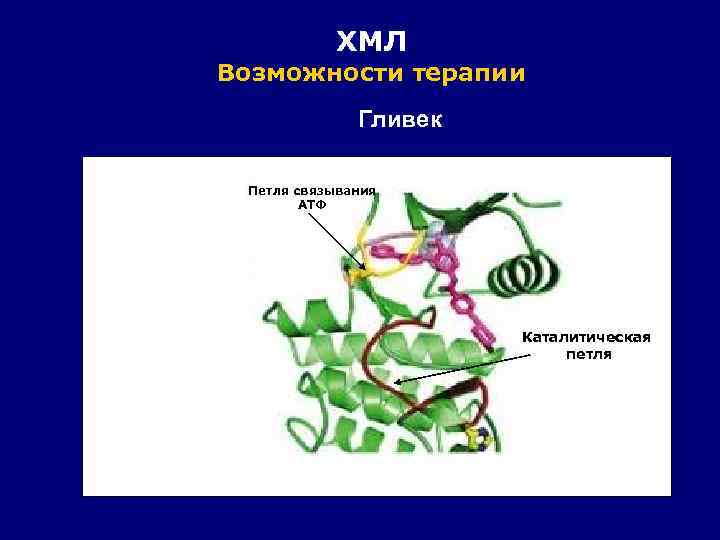 ХМЛ Возможности терапии Гливек Петля связывания АТФ Каталитическая петля
ХМЛ Возможности терапии Гливек Петля связывания АТФ Каталитическая петля
 ХМЛ Возможности терапии Гливек Кроме bcr/abl киназы блокирует PDGFR c-kit FRGF Кроме ХМЛ активен при ГИСТ Гиперэозинофильном с-ме FIP 1 L 1/PDGFRA Миелопролиферативной с-ме с t (5; 12) ETV 6/PDGFRB
ХМЛ Возможности терапии Гливек Кроме bcr/abl киназы блокирует PDGFR c-kit FRGF Кроме ХМЛ активен при ГИСТ Гиперэозинофильном с-ме FIP 1 L 1/PDGFRA Миелопролиферативной с-ме с t (5; 12) ETV 6/PDGFRB
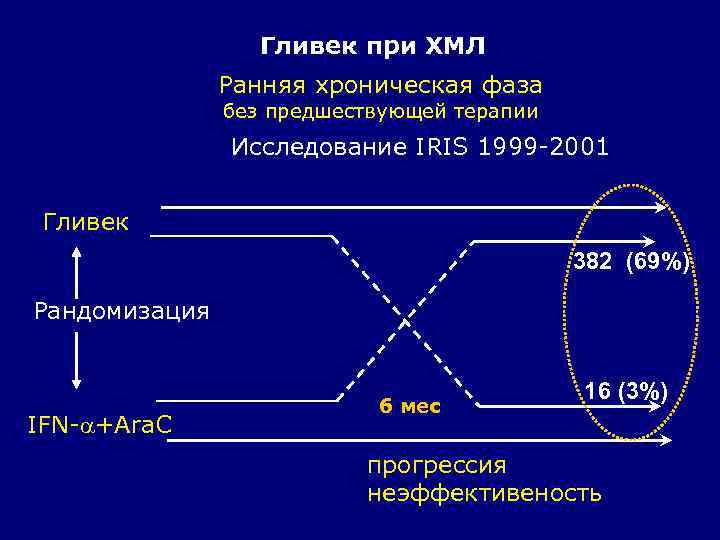 Гливек при ХМЛ Ранняя хроническая фаза без предшествующей терапии Исследование IRIS 1999 -2001 Гливек 382 (69%) Рандомизация IFN- +Ara. C 6 мес 16 (3%) прогрессия неэффективеность
Гливек при ХМЛ Ранняя хроническая фаза без предшествующей терапии Исследование IRIS 1999 -2001 Гливек 382 (69%) Рандомизация IFN- +Ara. C 6 мес 16 (3%) прогрессия неэффективеность
 Гливек Результаты IRIS, 54 мес. наблюдения Полная гематологическая ремиссия 98% Большой цитогенетический ответ 92% Полный цитогенетический ответ 86% У 97% больных с полным цитогенетическим ответом нет прогрессирования ХМЛ
Гливек Результаты IRIS, 54 мес. наблюдения Полная гематологическая ремиссия 98% Большой цитогенетический ответ 92% Полный цитогенетический ответ 86% У 97% больных с полным цитогенетическим ответом нет прогрессирования ХМЛ
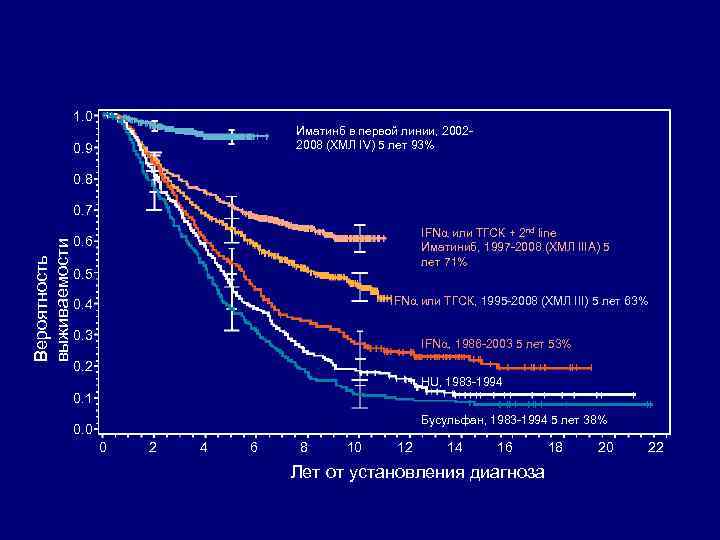 1. 0 Иматинб в первой линии, 20022008 (ХМЛ IV) 5 лет 93% 0. 9 0. 8 Вероятность выживаемости 0. 7 IFN или ТГСК + 2 nd line Иматиниб, 1997 -2008 (ХМЛ IIIA) 5 лет 71% 0. 6 0. 5 IFN или ТГСК, 1995 -2008 (ХМЛ III) 5 лет 63% 0. 4 0. 3 IFN , 1986 -2003 5 лет 53% 0. 2 HU, 1983 -1994 0. 1 Бусульфан, 1983 -1994 5 лет 38% 0. 0 0 2 4 6 8 10 12 14 16 Лет от установления диагноза 18 20 22
1. 0 Иматинб в первой линии, 20022008 (ХМЛ IV) 5 лет 93% 0. 9 0. 8 Вероятность выживаемости 0. 7 IFN или ТГСК + 2 nd line Иматиниб, 1997 -2008 (ХМЛ IIIA) 5 лет 71% 0. 6 0. 5 IFN или ТГСК, 1995 -2008 (ХМЛ III) 5 лет 63% 0. 4 0. 3 IFN , 1986 -2003 5 лет 53% 0. 2 HU, 1983 -1994 0. 1 Бусульфан, 1983 -1994 5 лет 38% 0. 0 0 2 4 6 8 10 12 14 16 Лет от установления диагноза 18 20 22
 Выживаемость без прогрессии IRIS, 42 мес Ц/г ответ полный без полного % больных без прогрессии 95 % 75 %
Выживаемость без прогрессии IRIS, 42 мес Ц/г ответ полный без полного % больных без прогрессии 95 % 75 %
 Гливек Результаты IRIS, 72 мес. наблюдения Остановили лечение Гливеком 175 пациентов 34% Неэффективность/ прогрессия 14% Побочные эффекты 5% Отзыв информированного согласия 6% ТКМ+потеря из под наблюдения 8% Смерть (не связанная с ХМЛ) 2% 84 месяца – 60% продолжают Гливек
Гливек Результаты IRIS, 72 мес. наблюдения Остановили лечение Гливеком 175 пациентов 34% Неэффективность/ прогрессия 14% Побочные эффекты 5% Отзыв информированного согласия 6% ТКМ+потеря из под наблюдения 8% Смерть (не связанная с ХМЛ) 2% 84 месяца – 60% продолжают Гливек
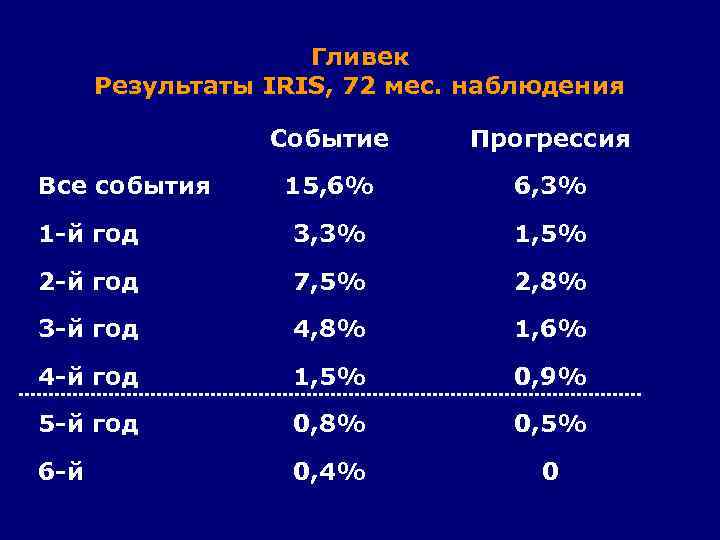 Гливек Результаты IRIS, 72 мес. наблюдения Событие Прогрессия 15, 6% 6, 3% 1 -й год 3, 3% 1, 5% 2 -й год 7, 5% 2, 8% 3 -й год 4, 8% 1, 6% 4 -й год 1, 5% 0, 9% 5 -й год 0, 8% 0, 5% 6 -й 0, 4% 0 Все события
Гливек Результаты IRIS, 72 мес. наблюдения Событие Прогрессия 15, 6% 6, 3% 1 -й год 3, 3% 1, 5% 2 -й год 7, 5% 2, 8% 3 -й год 4, 8% 1, 6% 4 -й год 1, 5% 0, 9% 5 -й год 0, 8% 0, 5% 6 -й 0, 4% 0 Все события
 Взаимосвязь «большого» молекулярного ответа и выживаемости без прогрессии (IRIS) Больные с полным цитогенетическим ответом Выживаемость без прогрессии, 42 мес. лечения Редукция bcr/abl • >3 log • < 3 log 98 % 90 %
Взаимосвязь «большого» молекулярного ответа и выживаемости без прогрессии (IRIS) Больные с полным цитогенетическим ответом Выживаемость без прогрессии, 42 мес. лечения Редукция bcr/abl • >3 log • < 3 log 98 % 90 %
 Гливек Результаты IRIS, 72 мес. наблюдения получают 300 мг 7% получают 400 мг 83% получают 600 мг 6% получают 800 мг 4%
Гливек Результаты IRIS, 72 мес. наблюдения получают 300 мг 7% получают 400 мг 83% получают 600 мг 6% получают 800 мг 4%
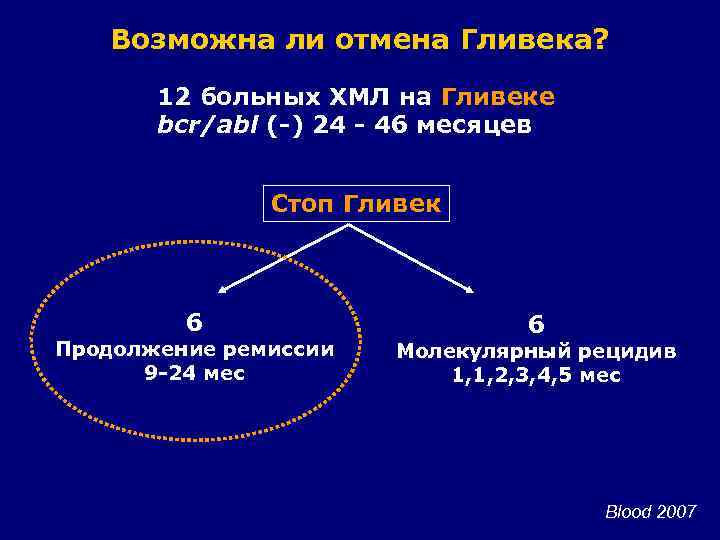 Возможна ли отмена Гливека? 12 больных ХМЛ на Гливеке bcr/abl (-) 24 - 46 месяцев Стоп Гливек 6 Продолжение ремиссии 9 -24 мес 6 Молекулярный рецидив 1, 1, 2, 3, 4, 5 мес Blood 2007
Возможна ли отмена Гливека? 12 больных ХМЛ на Гливеке bcr/abl (-) 24 - 46 месяцев Стоп Гливек 6 Продолжение ремиссии 9 -24 мес 6 Молекулярный рецидив 1, 1, 2, 3, 4, 5 мес Blood 2007
 Возможна ли отмена Гливека? Исследование STop IMatinib Критерии включения Минимум 24 мес ПЦР (-) Минимум 5 отрицательных ПЦР (качество РНК!!!) Частый мониторинг
Возможна ли отмена Гливека? Исследование STop IMatinib Критерии включения Минимум 24 мес ПЦР (-) Минимум 5 отрицательных ПЦР (качество РНК!!!) Частый мониторинг
 Возможна ли отмена Гливека? Исследование STIM N пациентов N с наблюдением > 1 мес М/Ж IFN иматиниб Мед наблюдения 69 60 22/38 31 29 5 мес (1 -16)
Возможна ли отмена Гливека? Исследование STIM N пациентов N с наблюдением > 1 мес М/Ж IFN иматиниб Мед наблюдения 69 60 22/38 31 29 5 мес (1 -16)
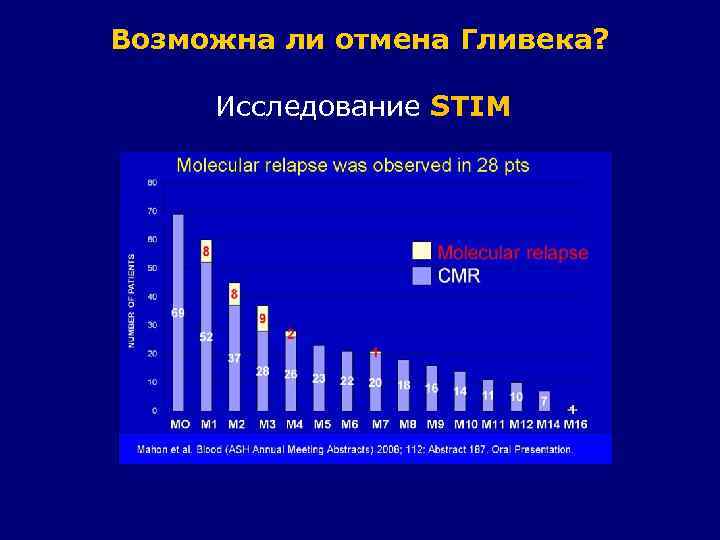 Возможна ли отмена Гливека? Исследование STIM
Возможна ли отмена Гливека? Исследование STIM
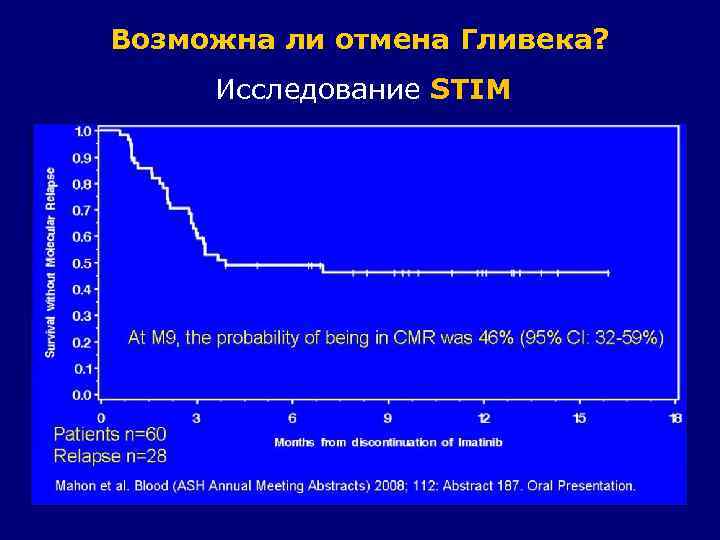 Возможна ли отмена Гливека? Исследование STIM Все рецидивировавшие восстановили ПМР после возобновления Гливека
Возможна ли отмена Гливека? Исследование STIM Все рецидивировавшие восстановили ПМР после возобновления Гливека
 Гливек при ХМЛ причины резистентности Предсуществующие Приобретенные Мутация bcr/abl Недостаточная биодоступность Амплификация bcr/abl Недостаточная экспозиция стволовых клеток (Pgp, Cyt P 450) Появление новых ц/г аномалий (del 9, i 17, Ph+)
Гливек при ХМЛ причины резистентности Предсуществующие Приобретенные Мутация bcr/abl Недостаточная биодоступность Амплификация bcr/abl Недостаточная экспозиция стволовых клеток (Pgp, Cyt P 450) Появление новых ц/г аномалий (del 9, i 17, Ph+)
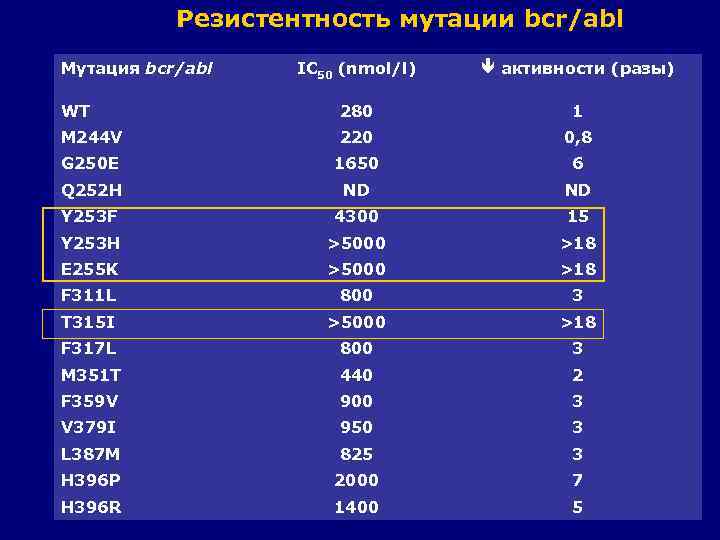 Резистентность мутации bcr/abl Мутация bcr/abl IC 50 (nmol/l) активности (разы) WT 280 1 M 244 V 220 0, 8 G 250 E 1650 6 Q 252 H ND ND Y 253 F 4300 15 Y 253 H >5000 >18 E 255 K >5000 >18 F 311 L 800 3 T 315 I >5000 >18 F 317 L 800 3 M 351 T 440 2 F 359 V 900 3 V 379 I 950 3 L 387 M 825 3 H 396 P 2000 7 H 396 R 1400 5
Резистентность мутации bcr/abl Мутация bcr/abl IC 50 (nmol/l) активности (разы) WT 280 1 M 244 V 220 0, 8 G 250 E 1650 6 Q 252 H ND ND Y 253 F 4300 15 Y 253 H >5000 >18 E 255 K >5000 >18 F 311 L 800 3 T 315 I >5000 >18 F 317 L 800 3 M 351 T 440 2 F 359 V 900 3 V 379 I 950 3 L 387 M 825 3 H 396 P 2000 7 H 396 R 1400 5
 Гливек при ХМЛ Резистентность Мутации bcr/abl Нилотиниб ( «Тасигна» )Новартис) CH 3 N N O H N N CH 3 N H 3 C N Дазатиниб (BMS) CH 3 H N S O Cl N N N H N N N OH
Гливек при ХМЛ Резистентность Мутации bcr/abl Нилотиниб ( «Тасигна» )Новартис) CH 3 N N O H N N CH 3 N H 3 C N Дазатиниб (BMS) CH 3 H N S O Cl N N N H N N N OH
 ТКИ 2 поколения Эффективность в первой линии Вероятность полной цитогенетической ремиссии Нилотиниб Дазатиниб Gimema MD Anderson 3 мес 78% 90% 79% 6 мес 96% 95% 93% 12 мес 94% 96% 95% !
ТКИ 2 поколения Эффективность в первой линии Вероятность полной цитогенетической ремиссии Нилотиниб Дазатиниб Gimema MD Anderson 3 мес 78% 90% 79% 6 мес 96% 95% 93% 12 мес 94% 96% 95% !
 Ближайшее будущее в лечении ХМЛ Ингибиторы 2 поколения в 1 -й линии
Ближайшее будущее в лечении ХМЛ Ингибиторы 2 поколения в 1 -й линии


