Лечение рака предстательной железы.ppt
- Количество слайдов: 19
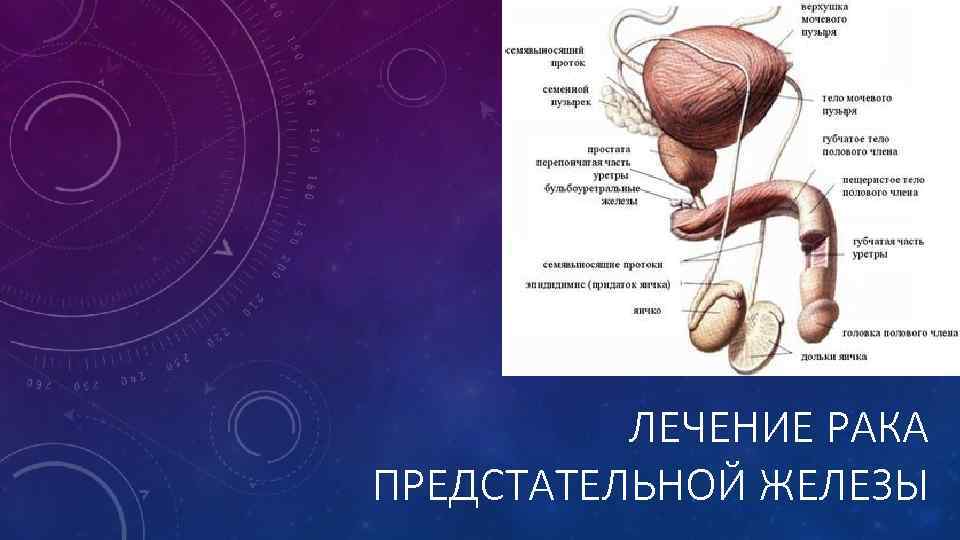 ЛЕЧЕНИЕ РАКА ПРЕДСТАТЕЛЬНОЙ ЖЕЛЕЗЫ
ЛЕЧЕНИЕ РАКА ПРЕДСТАТЕЛЬНОЙ ЖЕЛЕЗЫ
 ЦЕЛИ ЛЕЧЕНИЯ Локализованный и местно-рапространенный процесс: Полное излечение больного Наличие лимфогенных или гематогенных метастазов: Достижение максимально длительной ремиссии и сохранение качества жизни больного
ЦЕЛИ ЛЕЧЕНИЯ Локализованный и местно-рапространенный процесс: Полное излечение больного Наличие лимфогенных или гематогенных метастазов: Достижение максимально длительной ремиссии и сохранение качества жизни больного
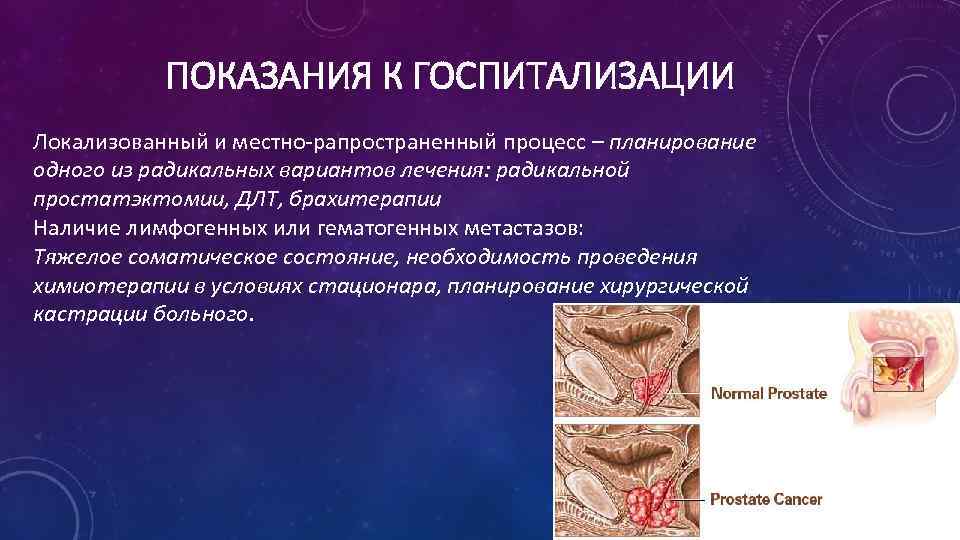 ПОКАЗАНИЯ К ГОСПИТАЛИЗАЦИИ Локализованный и местно-рапространенный процесс – планирование одного из радикальных вариантов лечения: радикальной простатэктомии, ДЛТ, брахитерапии Наличие лимфогенных или гематогенных метастазов: Тяжелое соматическое состояние, необходимость проведения химиотерапии в условиях стационара, планирование хирургической кастрации больного.
ПОКАЗАНИЯ К ГОСПИТАЛИЗАЦИИ Локализованный и местно-рапространенный процесс – планирование одного из радикальных вариантов лечения: радикальной простатэктомии, ДЛТ, брахитерапии Наличие лимфогенных или гематогенных метастазов: Тяжелое соматическое состояние, необходимость проведения химиотерапии в условиях стационара, планирование хирургической кастрации больного.
 ЛЕЧЕНИЕ ЛОКАЛИЗОВАННОГО РАКА ПРЕДСТАТЕЛЬНОЙ ЖЕЛЕЗЫ: T 1 -2 N 0 M 0 радикальная простатэктомия дистанционная лучевая терапия брахитерапия
ЛЕЧЕНИЕ ЛОКАЛИЗОВАННОГО РАКА ПРЕДСТАТЕЛЬНОЙ ЖЕЛЕЗЫ: T 1 -2 N 0 M 0 радикальная простатэктомия дистанционная лучевая терапия брахитерапия
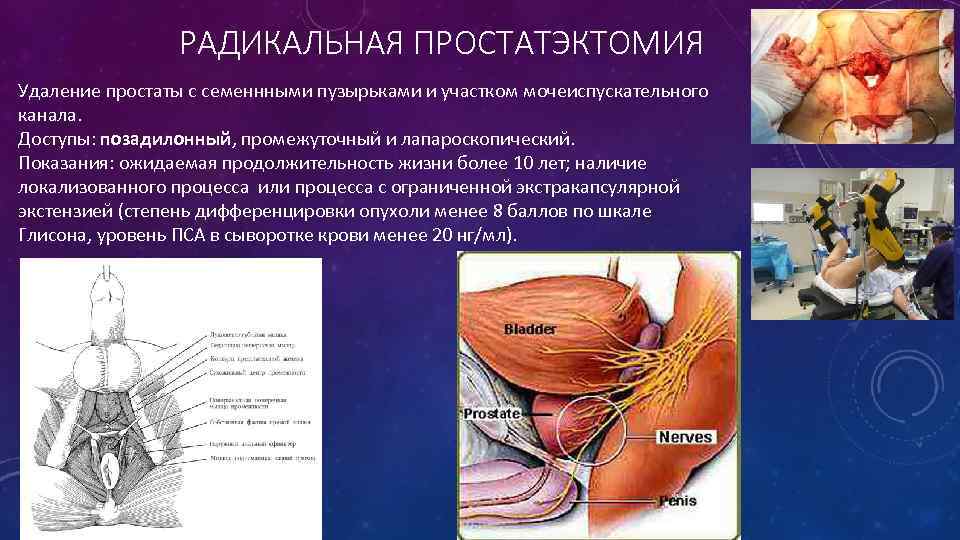 РАДИКАЛЬНАЯ ПРОСТАТЭКТОМИЯ Удаление простаты с семеннными пузырьками и участком мочеиспускательного канала. Доступы: позадилонный, промежуточный и лапароскопический. Показания: ожидаемая продолжительность жизни более 10 лет; наличие локализованного процесса или процесса с ограниченной экстракапсулярной экстензией (степень дифференцировки опухоли менее 8 баллов по шкале Глисона, уровень ПСА в сыворотке крови менее 20 нг/мл).
РАДИКАЛЬНАЯ ПРОСТАТЭКТОМИЯ Удаление простаты с семеннными пузырьками и участком мочеиспускательного канала. Доступы: позадилонный, промежуточный и лапароскопический. Показания: ожидаемая продолжительность жизни более 10 лет; наличие локализованного процесса или процесса с ограниченной экстракапсулярной экстензией (степень дифференцировки опухоли менее 8 баллов по шкале Глисона, уровень ПСА в сыворотке крови менее 20 нг/мл).
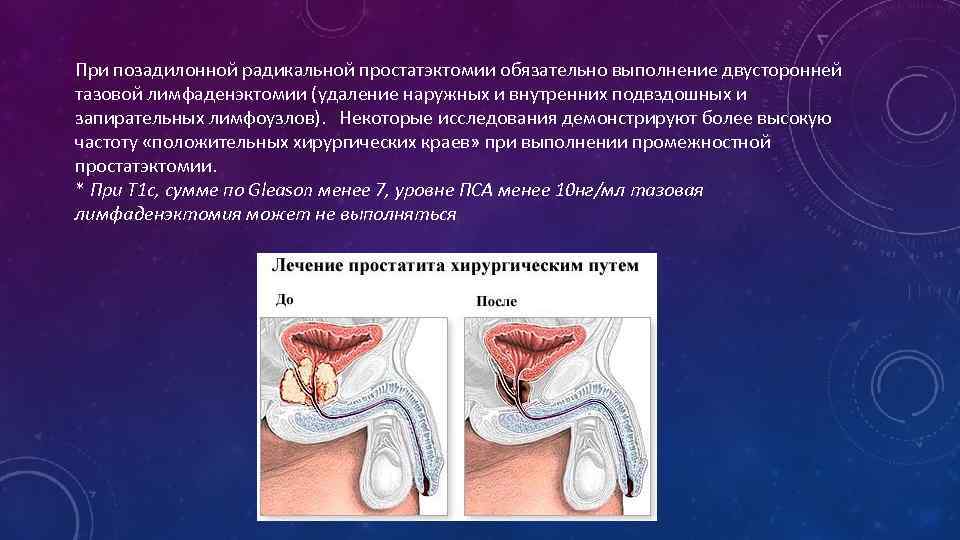 При позадилонной радикальной простатэктомии обязательно выполнение двусторонней тазовой лимфаденэктомии (удаление наружных и внутренних подвздошных и запирательных лимфоузлов). Некоторые исследования демонстрируют более высокую частоту «положительных хирургических краев» при выполнении промежностной простатэктомии. * При Т 1 с, сумме по Gleason менее 7, уровне ПСА менее 10 нг/мл тазовая лимфаденэктомия может не выполняться
При позадилонной радикальной простатэктомии обязательно выполнение двусторонней тазовой лимфаденэктомии (удаление наружных и внутренних подвздошных и запирательных лимфоузлов). Некоторые исследования демонстрируют более высокую частоту «положительных хирургических краев» при выполнении промежностной простатэктомии. * При Т 1 с, сумме по Gleason менее 7, уровне ПСА менее 10 нг/мл тазовая лимфаденэктомия может не выполняться
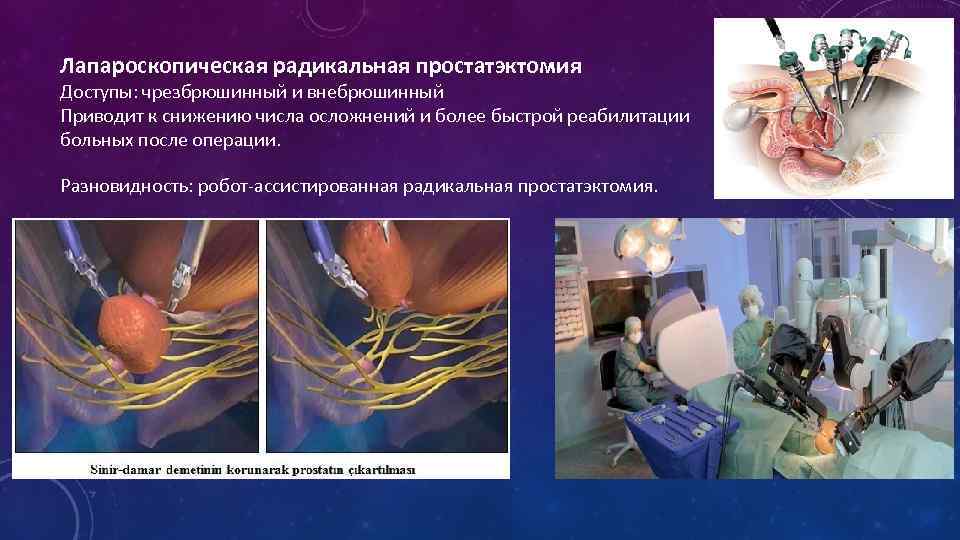 Лапароскопическая радикальная простатэктомия Доступы: чрезбрюшинный и внебрюшинный Приводит к снижению числа осложнений и более быстрой реабилитации больных после операции. Разновидность: робот-ассистированная радикальная простатэктомия.
Лапароскопическая радикальная простатэктомия Доступы: чрезбрюшинный и внебрюшинный Приводит к снижению числа осложнений и более быстрой реабилитации больных после операции. Разновидность: робот-ассистированная радикальная простатэктомия.
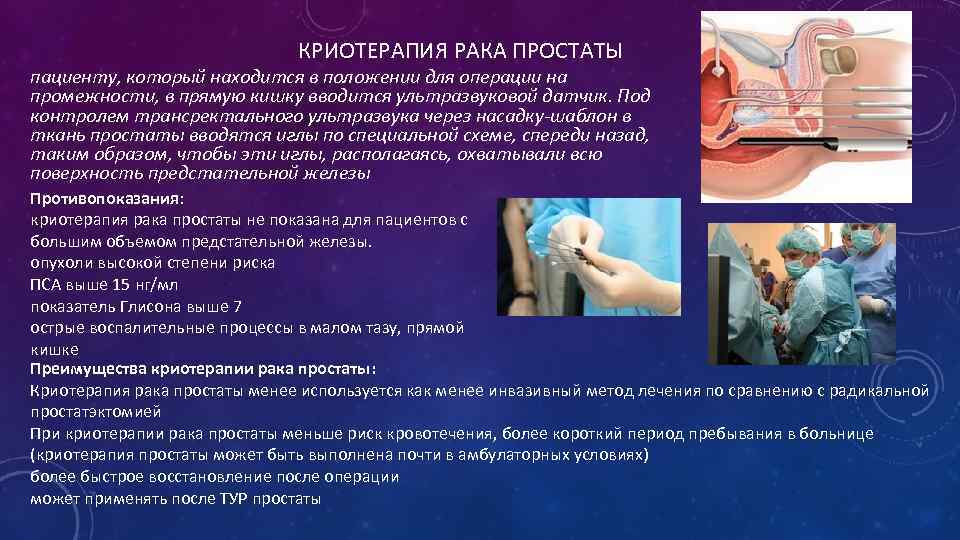 КРИОТЕРАПИЯ РАКА ПРОСТАТЫ пациенту, который находится в положении для операции на промежности, в прямую кишку вводится ультразвуковой датчик. Под контролем трансректального ультразвука через насадку-шаблон в ткань простаты вводятся иглы по специальной схеме, спереди назад, таким образом, чтобы эти иглы, располагаясь, охватывали всю поверхность предстательной железы Противопоказания: криотерапия рака простаты не показана для пациентов с большим объемом предстательной железы. опухоли высокой степени риска ПСА выше 15 нг/мл показатель Глисона выше 7 острые воспалительные процессы в малом тазу, прямой кишке Преимущества криотерапии рака простаты: Криотерапия рака простаты менее используется как менее инвазивный метод лечения по сравнению с радикальной простатэктомией При криотерапии рака простаты меньше риск кровотечения, более короткий период пребывания в больнице (криотерапия простаты может быть выполнена почти в амбулаторных условиях) более быстрое восстановление после операции может применять после ТУР простаты
КРИОТЕРАПИЯ РАКА ПРОСТАТЫ пациенту, который находится в положении для операции на промежности, в прямую кишку вводится ультразвуковой датчик. Под контролем трансректального ультразвука через насадку-шаблон в ткань простаты вводятся иглы по специальной схеме, спереди назад, таким образом, чтобы эти иглы, располагаясь, охватывали всю поверхность предстательной железы Противопоказания: криотерапия рака простаты не показана для пациентов с большим объемом предстательной железы. опухоли высокой степени риска ПСА выше 15 нг/мл показатель Глисона выше 7 острые воспалительные процессы в малом тазу, прямой кишке Преимущества криотерапии рака простаты: Криотерапия рака простаты менее используется как менее инвазивный метод лечения по сравнению с радикальной простатэктомией При криотерапии рака простаты меньше риск кровотечения, более короткий период пребывания в больнице (криотерапия простаты может быть выполнена почти в амбулаторных условиях) более быстрое восстановление после операции может применять после ТУР простаты
 При криоабляции применяются криозонды, которые проводятся через кожу. До настоящего времени была необходимость в осуществлении такого же разреза, как и при открытой операции, для того, чтобы обеспечить достаточный доступ для выполнения процедуры. Однако в настоящее время в нашем распоряжении имеются более эффективные криозонды. При более крупных размерах опухоли для охвата достаточной площади может потребоваться более одного криозонда. Сначала производится введение всех зондов, а затем одновременно запускают механизмы замораживания-размораживания. Хирург вводиткриозонды (иглы) через промежность в предварительно выбранные участки предстательной железы. Размещение криозондов хирург контролирует при помощи трансректального ультразвукового датчика. Техника криотерапии рака простаты Через криозонд подается охлаждающий газ (аргон), который замораживает предстательную железу. Как только область опухоли предстательной железы покрылась льдом, циркуляцию аргона по криозонду прекращают, и она оттаивает. Цикл замораживания – оттаивания опухоли повторяют несколько раз. Хирург контролирует процесс криоабляции рака простаты при помощи ультразвукового исследования. Иглы извлекают, мочевой катетер остается в мочевом пузыре. К катетеру прикрепляют стерильный мочеприемник.
При криоабляции применяются криозонды, которые проводятся через кожу. До настоящего времени была необходимость в осуществлении такого же разреза, как и при открытой операции, для того, чтобы обеспечить достаточный доступ для выполнения процедуры. Однако в настоящее время в нашем распоряжении имеются более эффективные криозонды. При более крупных размерах опухоли для охвата достаточной площади может потребоваться более одного криозонда. Сначала производится введение всех зондов, а затем одновременно запускают механизмы замораживания-размораживания. Хирург вводиткриозонды (иглы) через промежность в предварительно выбранные участки предстательной железы. Размещение криозондов хирург контролирует при помощи трансректального ультразвукового датчика. Техника криотерапии рака простаты Через криозонд подается охлаждающий газ (аргон), который замораживает предстательную железу. Как только область опухоли предстательной железы покрылась льдом, циркуляцию аргона по криозонду прекращают, и она оттаивает. Цикл замораживания – оттаивания опухоли повторяют несколько раз. Хирург контролирует процесс криоабляции рака простаты при помощи ультразвукового исследования. Иглы извлекают, мочевой катетер остается в мочевом пузыре. К катетеру прикрепляют стерильный мочеприемник.
 Дистанционная лучевая терапия Проводится при: противопоказаниях к хирургическому лечению, при отказе от операции. Проводится дистанционная лучевая терапия на высокоэнергетических ускорителях или на телегаммаустановках. Рекомендуется 3 -4 -х польное или конформное (3 Д) облучение: на предстательную железу СОД=65 -70 Гр (при РОД=2 Гр), на таз – СОД=44 Гр. В проведении лучевой терапии применяется расщепленный курс: СОД=40 Гр, далее 3 -х недельный перерыв, затем продолжение лучевой терапии. Противопоказаниями к проведению лучевой терапии является: НАЛИЧИЕ ЦИСТОСТОМЫ, ЦИСТИТ, КАМНИ МОЧЕВОГО ПУЗЫРЯ. Противопоказания: 1. Абсолютные: Предшествующее облучение малого таза Острый воспалительный процесс прямой кишки Постоянный уретральный катетер Ожирение 4 степени. 2. Относительные: Сниженная емкость мочевого пузыря Хронческая диарея Инфравезикальная обструкция, требующая надлобковой цистостомии. Язвенный колит в стадии ремиссии.
Дистанционная лучевая терапия Проводится при: противопоказаниях к хирургическому лечению, при отказе от операции. Проводится дистанционная лучевая терапия на высокоэнергетических ускорителях или на телегаммаустановках. Рекомендуется 3 -4 -х польное или конформное (3 Д) облучение: на предстательную железу СОД=65 -70 Гр (при РОД=2 Гр), на таз – СОД=44 Гр. В проведении лучевой терапии применяется расщепленный курс: СОД=40 Гр, далее 3 -х недельный перерыв, затем продолжение лучевой терапии. Противопоказаниями к проведению лучевой терапии является: НАЛИЧИЕ ЦИСТОСТОМЫ, ЦИСТИТ, КАМНИ МОЧЕВОГО ПУЗЫРЯ. Противопоказания: 1. Абсолютные: Предшествующее облучение малого таза Острый воспалительный процесс прямой кишки Постоянный уретральный катетер Ожирение 4 степени. 2. Относительные: Сниженная емкость мочевого пузыря Хронческая диарея Инфравезикальная обструкция, требующая надлобковой цистостомии. Язвенный колит в стадии ремиссии.
 Брахитерапия Введение (имплантация) радиоактивных источников в ткань простаты Показания: В самостоятельном виде при Т 1 -2 а, Gleason – 2 -6, ПСА менее 10 нг/мл; В качестве буста после дистанционной лучевой терапии брахитерапия применяется при Т 2 b, Т 2 с или меньших стадиях, но при Gleason 8 -10, или ПСА более 20 нг/мл. Противопоказания: При ожидаемой продолжительности жизни менее 5 лет; Большой или плохо заживающий дефект после ТУР Существуют два вида брахитерапии, применяемые при раке простаты - низкочастотная брахитерапия (имплантация радиоактивных зерен) и высокочастотная брахитерапия. При проведении низкочастотной брахитерапии, в опухоль помещают небольшие титановые имплантаты «зерна» , в которых содержится радиоактивное вещество. Операция проводится с использованием приборов визуального контроля под общим наркозом.
Брахитерапия Введение (имплантация) радиоактивных источников в ткань простаты Показания: В самостоятельном виде при Т 1 -2 а, Gleason – 2 -6, ПСА менее 10 нг/мл; В качестве буста после дистанционной лучевой терапии брахитерапия применяется при Т 2 b, Т 2 с или меньших стадиях, но при Gleason 8 -10, или ПСА более 20 нг/мл. Противопоказания: При ожидаемой продолжительности жизни менее 5 лет; Большой или плохо заживающий дефект после ТУР Существуют два вида брахитерапии, применяемые при раке простаты - низкочастотная брахитерапия (имплантация радиоактивных зерен) и высокочастотная брахитерапия. При проведении низкочастотной брахитерапии, в опухоль помещают небольшие титановые имплантаты «зерна» , в которых содержится радиоактивное вещество. Операция проводится с использованием приборов визуального контроля под общим наркозом.
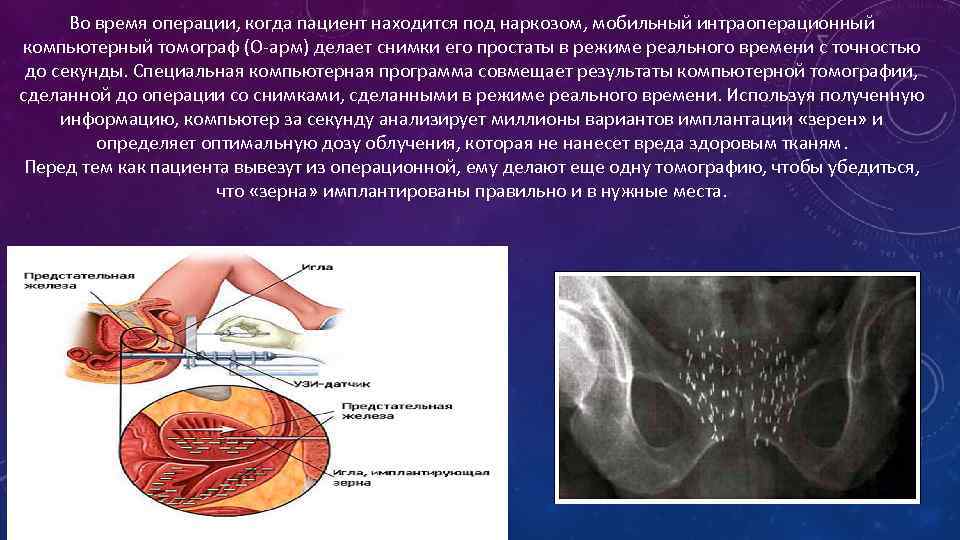 Во время операции, когда пациент находится под наркозом, мобильный интраоперационный компьютерный томограф (O-арм) делает снимки его простаты в режиме реального времени с точностью до секунды. Специальная компьютерная программа совмещает результаты компьютерной томографии, сделанной до операции со снимками, сделанными в режиме реального времени. Используя полученную информацию, компьютер за секунду анализирует миллионы вариантов имплантации «зерен» и определяет оптимальную дозу облучения, которая не нанесет вреда здоровым тканям. Перед тем как пациента вывезут из операционной, ему делают еще одну томографию, чтобы убедиться, что «зерна» имплантированы правильно и в нужные места.
Во время операции, когда пациент находится под наркозом, мобильный интраоперационный компьютерный томограф (O-арм) делает снимки его простаты в режиме реального времени с точностью до секунды. Специальная компьютерная программа совмещает результаты компьютерной томографии, сделанной до операции со снимками, сделанными в режиме реального времени. Используя полученную информацию, компьютер за секунду анализирует миллионы вариантов имплантации «зерен» и определяет оптимальную дозу облучения, которая не нанесет вреда здоровым тканям. Перед тем как пациента вывезут из операционной, ему делают еще одну томографию, чтобы убедиться, что «зерна» имплантированы правильно и в нужные места.
 Высокочастотная брахитерапия Высокочастотная или временная брахитерапия - разновидность брахитерапии, при которой пациент получает высокие дозы радиоактивного излучения в короткий промежуток времени. Пока пациент находится под наркозом, врачи помещают несколько пластмассовых катетеров рядом с его опухолью или непосредственно внутрь нее. Катетеры прикреплены к аппарату, в котором содержатся особые радиоактивные капсулы. Капсулы помещают в катетеры один или 2 раза по 15 минут каждый. Сеанс высокочастотной брахитерапии может проводиться всю ночь. Затем катетеры удаляют и пациента отпускают домой. При проведении высокочастотной брахитерапии также используют компьютерный томограф, чтобы повысить эффективность лечения. Результаты компьютерной томографии, полученные в режиме реального времени, могут быть совмещены с результатами компьютерной томографии, сделанной до операции. Это позволит врачам составить правильный план лечения пациента, а также усилить воздействия радиации на самые пораженные раком области предстательной железы.
Высокочастотная брахитерапия Высокочастотная или временная брахитерапия - разновидность брахитерапии, при которой пациент получает высокие дозы радиоактивного излучения в короткий промежуток времени. Пока пациент находится под наркозом, врачи помещают несколько пластмассовых катетеров рядом с его опухолью или непосредственно внутрь нее. Катетеры прикреплены к аппарату, в котором содержатся особые радиоактивные капсулы. Капсулы помещают в катетеры один или 2 раза по 15 минут каждый. Сеанс высокочастотной брахитерапии может проводиться всю ночь. Затем катетеры удаляют и пациента отпускают домой. При проведении высокочастотной брахитерапии также используют компьютерный томограф, чтобы повысить эффективность лечения. Результаты компьютерной томографии, полученные в режиме реального времени, могут быть совмещены с результатами компьютерной томографии, сделанной до операции. Это позволит врачам составить правильный план лечения пациента, а также усилить воздействия радиации на самые пораженные раком области предстательной железы.
 Активное наблюдение (отсроченное лечение) l Активное наблюдение (отсроченное лечение) обычно применяется при высокодифференцированном раке простаты в стадиях Т 1 а и Т 1 с, если ожидаемая продолжительность жизни менее 5 лет и ограничена из-за сопутствующих заболеваний. l Оно основано на нескольких положениях: больные – лица пожилого возраста и имеют сопутствующие заболевания, РПЖ часто медленно прогрессирует, требуются годы, чтобы рак привел к значительным симптомам. l l
Активное наблюдение (отсроченное лечение) l Активное наблюдение (отсроченное лечение) обычно применяется при высокодифференцированном раке простаты в стадиях Т 1 а и Т 1 с, если ожидаемая продолжительность жизни менее 5 лет и ограничена из-за сопутствующих заболеваний. l Оно основано на нескольких положениях: больные – лица пожилого возраста и имеют сопутствующие заболевания, РПЖ часто медленно прогрессирует, требуются годы, чтобы рак привел к значительным симптомам. l l
 Лечение местно-распространенного рака предстательной железы опухоли, выходящие за пределы предстательной железы: Т 3 -4 N 0 M 0 или T 1 -4 N 1 M 0. l Методом выбора в лечении больных местно-распространенным раком простаты является лучевая терапия (облучается простата + таз), l Сочетание гормональной терапии с лучевой терапией усиливает лечебный эффект, l Радикальная простатэктомия может применяться как метод лечения у молодых больных с индексом Gleason – менее 7, ПСА менее 20 нг/мл; но в этом случае необходима гормонотерапия
Лечение местно-распространенного рака предстательной железы опухоли, выходящие за пределы предстательной железы: Т 3 -4 N 0 M 0 или T 1 -4 N 1 M 0. l Методом выбора в лечении больных местно-распространенным раком простаты является лучевая терапия (облучается простата + таз), l Сочетание гормональной терапии с лучевой терапией усиливает лечебный эффект, l Радикальная простатэктомия может применяться как метод лечения у молодых больных с индексом Gleason – менее 7, ПСА менее 20 нг/мл; но в этом случае необходима гормонотерапия
 Послеоперационная радиотерапия может проводиться: l l l Больным раком предстательной железы с Т 3 N 0 M 0 и негативным после радикальной простатэктомии ПСА: при вовлечении семенных пузырьков, при повышении ПСА и при Gleason более 4; В случаях высокого местного рецидива; Отсроченно – в случае повышения уровня ПСА или верификации рецидива; После простатэктомии доза на область железы должна быть не более 60 Гр. Паллиативное облучение таза при опухолях замуровывающих таз (уменьшение дизурических расстройств, болей).
Послеоперационная радиотерапия может проводиться: l l l Больным раком предстательной железы с Т 3 N 0 M 0 и негативным после радикальной простатэктомии ПСА: при вовлечении семенных пузырьков, при повышении ПСА и при Gleason более 4; В случаях высокого местного рецидива; Отсроченно – в случае повышения уровня ПСА или верификации рецидива; После простатэктомии доза на область железы должна быть не более 60 Гр. Паллиативное облучение таза при опухолях замуровывающих таз (уменьшение дизурических расстройств, болей).
 Лечение распространенного рака предстательной железы Цель гормонального лечения РПЖ-устранение андрогенной стимуляции клеток опухоли предстательной железы: l устранить источник андрогенов, или l снизить максимально их уровень в организме больного, или l создать препятствие их взаимодействия с опухолевыми клетками. Золотой стандарт в лечении больных метастатическим раком предстательной железы является кастрация (хирургическая или медикаментозная) Так как после первого применения препаратов золадекс, диферелин возможна вспышка активизации метаболизма тестостерона, то до начала введения агонистов ЛГРГ-гормонов назначают антиандрогены в течении 7 -10 дней: стероидные антиандрогены (ципротерона ацетат) или нестероидные (флутамид, косадекс).
Лечение распространенного рака предстательной железы Цель гормонального лечения РПЖ-устранение андрогенной стимуляции клеток опухоли предстательной железы: l устранить источник андрогенов, или l снизить максимально их уровень в организме больного, или l создать препятствие их взаимодействия с опухолевыми клетками. Золотой стандарт в лечении больных метастатическим раком предстательной железы является кастрация (хирургическая или медикаментозная) Так как после первого применения препаратов золадекс, диферелин возможна вспышка активизации метаболизма тестостерона, то до начала введения агонистов ЛГРГ-гормонов назначают антиандрогены в течении 7 -10 дней: стероидные антиандрогены (ципротерона ацетат) или нестероидные (флутамид, косадекс).
 l Комбинированная блокада андрогенов – сочетание агонистов ЛГРГ с антиандрогенами или орхэктомия с антиандрогенами на период до 6 месяцев, в последующем антиандрогены могут быть отменены. l При выявлении роста уровня ПСА антиандрогены назначаются вновь. Отменяются они при снижении уровня ПСА или при дальнейшем продолжении роста ПСА и (или) усилении болевого синдрома, что свидетельствует о гормональной резистенции опухоли. С течением времени опухоль простаты теряет андрогеночувствительность. 15% первичных больных раком простаты являются гормононечувствительными. Этим больным назначается: гормонотерапия 2 линии: фосфэстрол (хонван) Различные схемы цитостатической терапии
l Комбинированная блокада андрогенов – сочетание агонистов ЛГРГ с антиандрогенами или орхэктомия с антиандрогенами на период до 6 месяцев, в последующем антиандрогены могут быть отменены. l При выявлении роста уровня ПСА антиандрогены назначаются вновь. Отменяются они при снижении уровня ПСА или при дальнейшем продолжении роста ПСА и (или) усилении болевого синдрома, что свидетельствует о гормональной резистенции опухоли. С течением времени опухоль простаты теряет андрогеночувствительность. 15% первичных больных раком простаты являются гормононечувствительными. Этим больным назначается: гормонотерапия 2 линии: фосфэстрол (хонван) Различные схемы цитостатической терапии
 Наблюдение за больными после проведенного лечения: Определение уровня ПСА, пальцевое ректальное исследование и рутинное клиническое обследование каждые 3 мес в течение 1 года, каждые 6 мес в течение 2 го и 3 го года, далее ежегодно. Повышение уровня ПСА после радикальной простатэктомии > 0. 2 нг/мл свидетельствует о рецидиве заболевания Три последовательных повышения уровня ПСА после минимального значения, достигнутого после лучевой терапии, определяют как рецидив Пальпируемый опухолевый узел и рост уровня ПСА свидетельствуют о развитии местного рецидива Биопсия рецидивной опухоли под контролем трансректального УЗИ показана при планировании второй линии радикального лечения При болях в костях показана сцинтиграфия скелета (независимо от ПСА)
Наблюдение за больными после проведенного лечения: Определение уровня ПСА, пальцевое ректальное исследование и рутинное клиническое обследование каждые 3 мес в течение 1 года, каждые 6 мес в течение 2 го и 3 го года, далее ежегодно. Повышение уровня ПСА после радикальной простатэктомии > 0. 2 нг/мл свидетельствует о рецидиве заболевания Три последовательных повышения уровня ПСА после минимального значения, достигнутого после лучевой терапии, определяют как рецидив Пальпируемый опухолевый узел и рост уровня ПСА свидетельствуют о развитии местного рецидива Биопсия рецидивной опухоли под контролем трансректального УЗИ показана при планировании второй линии радикального лечения При болях в костях показана сцинтиграфия скелета (независимо от ПСА)


