Лечение рака пищевода.ppt
- Количество слайдов: 15
 Лечение рака пищевода
Лечение рака пищевода
 Основными методами лечения рака пищевода являются: *хирургический лучевой комбинированный (сочетающий лучевой и хирургический компоненты) комплексный (представляющий сочетание хирургического, лучевого и лекарственного (химиотерапевтического) методов лечения). Низкая чувствительность опухоли к существующим химиопрепаратам, паллиативный и кратковременный эффект лучевой терапии делают хирургическое вмешательство методом выбора в лечении больных раком пищевода.
Основными методами лечения рака пищевода являются: *хирургический лучевой комбинированный (сочетающий лучевой и хирургический компоненты) комплексный (представляющий сочетание хирургического, лучевого и лекарственного (химиотерапевтического) методов лечения). Низкая чувствительность опухоли к существующим химиопрепаратам, паллиативный и кратковременный эффект лучевой терапии делают хирургическое вмешательство методом выбора в лечении больных раком пищевода.
 Применение хирургического лечения сдерживалось отсутствием надежных способов анестезии, что существенно удлиняло время оперативного вмешательства, и отсутствием отработанной методики пластического этапа хирургического лечения. Это обусловило длительное существование двухэтапного способа оперативного лечения. Первым этапом была операция Добромыслова. Торека (экстирпация пищевода с наложением шейной эзофагостомы и гастростомии), вторым этапом - пластика пищевода по одной из многочисленных разработанных методик. Для пластики использовались практически все отделы пищеварительного тракта: тонкая кишка и различные отделы толстой, применялись различные методы пластики целым желудком и желудочными лоскутами.
Применение хирургического лечения сдерживалось отсутствием надежных способов анестезии, что существенно удлиняло время оперативного вмешательства, и отсутствием отработанной методики пластического этапа хирургического лечения. Это обусловило длительное существование двухэтапного способа оперативного лечения. Первым этапом была операция Добромыслова. Торека (экстирпация пищевода с наложением шейной эзофагостомы и гастростомии), вторым этапом - пластика пищевода по одной из многочисленных разработанных методик. Для пластики использовались практически все отделы пищеварительного тракта: тонкая кишка и различные отделы толстой, применялись различные методы пластики целым желудком и желудочными лоскутами.
 Существовало множество способов расположения трансплантата: предгрудинный, ретростернальный, в ложе удаленного пищевода, и даже, ныне практически не применяемый, способ кожной пластики. Высокая послеоперационная летальность, техническая сложности вмешательства, громоздкая система многоэтапных операций - все эти факторы поделили хирургов на два лагеря. Большинство хирургов были сторонниками радикального удаления пораженного органа или его части при незапущенных формах заболевания и не возражали против лучевой терапии. Другие хирурги и онкологи критически оценивали возможности хирургического лечения рака пищевода, особенно его высоких локализаций, и отдавали предпочтение методам лучевой терапии. Совершенствование хирургической техники, анестезиологического пособия, выбор оптимальной лечебной тактики обусловили превалирующую роль хирургического лечения рака пищевода.
Существовало множество способов расположения трансплантата: предгрудинный, ретростернальный, в ложе удаленного пищевода, и даже, ныне практически не применяемый, способ кожной пластики. Высокая послеоперационная летальность, техническая сложности вмешательства, громоздкая система многоэтапных операций - все эти факторы поделили хирургов на два лагеря. Большинство хирургов были сторонниками радикального удаления пораженного органа или его части при незапущенных формах заболевания и не возражали против лучевой терапии. Другие хирурги и онкологи критически оценивали возможности хирургического лечения рака пищевода, особенно его высоких локализаций, и отдавали предпочтение методам лучевой терапии. Совершенствование хирургической техники, анестезиологического пособия, выбор оптимальной лечебной тактики обусловили превалирующую роль хирургического лечения рака пищевода.
 Современные принципы хирургии рака пищевода: * максимальная безопасность вмешательства: правильный выбор оперативного доступа и объема хирургического вмешательства; * онкологическая адекватность: мобилизация «острым путем» по принципу «от сосуда к пораженному органу» , правильная последовательность мобилизации пораженного органа с целью профилактики интраоперационной диссеминации, моноблочной лимфодиссекции; * высокая функциональность: выбор рационального метода пластики, формирование технически простого антирефлюксного анастомоза.
Современные принципы хирургии рака пищевода: * максимальная безопасность вмешательства: правильный выбор оперативного доступа и объема хирургического вмешательства; * онкологическая адекватность: мобилизация «острым путем» по принципу «от сосуда к пораженному органу» , правильная последовательность мобилизации пораженного органа с целью профилактики интраоперационной диссеминации, моноблочной лимфодиссекции; * высокая функциональность: выбор рационального метода пластики, формирование технически простого антирефлюксного анастомоза.
 Сравнительный анализ эффективности одномоментных и многоэтапных операций показал преимущество первых по показателям послеоперационной летальности (6, 6 %), завершенности лечения (98 %) и отдаленным результатам (33 % 5 -летней выживаемости). * При определении показании к хирургическому лечению необходимо учитывать, что раком пищевода чаще всего страдают лица в возрасте 60 лет и старше, имеющие целый ряд сопутствующих заболеваний, особенно сердечнососудистой и дыхательной систем, что ограничивает возможность применения операций. Кроме того, рак пищевода сравнительно рано приводит к нарушению питания и расстройству всех видов обмена веществ, что повышает риск оперативных вмешательств. * Таким образом, выбор оптимального метода лечения для каждого больного раком пищевода является трудной задачей. В каждом конкретном случае необходимо строго учитывать состояние больного, степень нарушения питания, распространенность процесса, технические возможности оперирующего хирурга, обеспечение адекватного послеоперационного ухода.
Сравнительный анализ эффективности одномоментных и многоэтапных операций показал преимущество первых по показателям послеоперационной летальности (6, 6 %), завершенности лечения (98 %) и отдаленным результатам (33 % 5 -летней выживаемости). * При определении показании к хирургическому лечению необходимо учитывать, что раком пищевода чаще всего страдают лица в возрасте 60 лет и старше, имеющие целый ряд сопутствующих заболеваний, особенно сердечнососудистой и дыхательной систем, что ограничивает возможность применения операций. Кроме того, рак пищевода сравнительно рано приводит к нарушению питания и расстройству всех видов обмена веществ, что повышает риск оперативных вмешательств. * Таким образом, выбор оптимального метода лечения для каждого больного раком пищевода является трудной задачей. В каждом конкретном случае необходимо строго учитывать состояние больного, степень нарушения питания, распространенность процесса, технические возможности оперирующего хирурга, обеспечение адекватного послеоперационного ухода.
 В настоящее время применяются два основных способа оперативных вмешательств: 1. Экстирпация пищевода с пластикой изоперистальтическим желудочным лоскутом с внеплевральным анастомозом на шее в виде трансплеврального удаления пищевода или внеплевральной экстирпации - трансхиатальным доступом. Метод позволяет подвергнуть хирургическому воздействия все отделы пищевода вплоть до глотки и даже с резекцией ротоглотки. Нахождение анастомоза на шее вне плевральной полости существенно снижает риск несостоятельности анастомоза, и она не является фатальной. В то же время часты случаи рубцового стеноза анастомоза. Следует подчеркнуть, что трасхиатальный способ (без торакотомии) резекции пищевода имеет ограниченное применение при опухолях больших размеров. К сожалению, большинство авторов заявляет о преобладании операций при распространенных опухолевых процессах.
В настоящее время применяются два основных способа оперативных вмешательств: 1. Экстирпация пищевода с пластикой изоперистальтическим желудочным лоскутом с внеплевральным анастомозом на шее в виде трансплеврального удаления пищевода или внеплевральной экстирпации - трансхиатальным доступом. Метод позволяет подвергнуть хирургическому воздействия все отделы пищевода вплоть до глотки и даже с резекцией ротоглотки. Нахождение анастомоза на шее вне плевральной полости существенно снижает риск несостоятельности анастомоза, и она не является фатальной. В то же время часты случаи рубцового стеноза анастомоза. Следует подчеркнуть, что трасхиатальный способ (без торакотомии) резекции пищевода имеет ограниченное применение при опухолях больших размеров. К сожалению, большинство авторов заявляет о преобладании операций при распространенных опухолевых процессах.
 2. Резекция пищевода с одномоментной внутриплевральной пластикой пищевода желудком - операция типа Льюиса. Этот способ практически исключает стенозирование анастомоза, обеспечивает лучшие функциональные результаты (отсутствие рефлюкс-эзофагита), однако верхние отделы внутригрудного отдела пищевода остаются недоступными для резекции (шейный, верхнегрудной отделы). При выполнении операции при раке пищевода обязательным является проведение лимфодиссекции как минимум в двух полостях по зонам лимфогенного метастазирования, а при экстирпации пищевода лимфодиссекции подвергаются и шейные лимфатические узлы. Летальность при таких видах операции находится в пределах 7 -10 %. В качестве трансплантата в ряде случаев используют, кроме желудка, тонкую ил толстую кишку.
2. Резекция пищевода с одномоментной внутриплевральной пластикой пищевода желудком - операция типа Льюиса. Этот способ практически исключает стенозирование анастомоза, обеспечивает лучшие функциональные результаты (отсутствие рефлюкс-эзофагита), однако верхние отделы внутригрудного отдела пищевода остаются недоступными для резекции (шейный, верхнегрудной отделы). При выполнении операции при раке пищевода обязательным является проведение лимфодиссекции как минимум в двух полостях по зонам лимфогенного метастазирования, а при экстирпации пищевода лимфодиссекции подвергаются и шейные лимфатические узлы. Летальность при таких видах операции находится в пределах 7 -10 %. В качестве трансплантата в ряде случаев используют, кроме желудка, тонкую ил толстую кишку.
 Не утратила своего значения операция Торека-Добромыслова в случаях возможности одномоментного этапа пластики (состояние больного, технические особенности операции). Следует указать на возможность выполнения при нерентабельном раке грудного отдела паллиативных вмешательств в виде шунтирования опухолевого стеноза наложением обходного анастомоза.
Не утратила своего значения операция Торека-Добромыслова в случаях возможности одномоментного этапа пластики (состояние больного, технические особенности операции). Следует указать на возможность выполнения при нерентабельном раке грудного отдела паллиативных вмешательств в виде шунтирования опухолевого стеноза наложением обходного анастомоза.
 Комбинированное и комплексное лечение Наиболее оправданно применение комбинированного лечения у больных с локализацией опухоли в среднегрудном отделе пищевода. * Доказано, что предоперационная лучевая терапия оказывает бластостатическии эффект, расширяет резектабельность, приводит к уменьшению количества местных рецидивов. * В качестве компонента комбинированного лечения лучевая терапия позволяет расширить показания к радикальному лечению местно-распространенных опухолей пищевода, повысить радикальность операций, снизить частоту местных рецидивов и метастазов. Предоперационная лучевая терапия проводится в различных вариантах. Применение методики укрупненного фракционирования дозы интенсивным ритмом по 4 Гр 5 -6 раз в неделю до СОД 20 -24 Гр оправдано при малой протяженности опухоли, при отсутствии глубокого изъязвления опухоли, при дисфагии I-II степени и отсутствии выраженных нарушений со стороны сердечно-сосудистой и дыхательной систем.
Комбинированное и комплексное лечение Наиболее оправданно применение комбинированного лечения у больных с локализацией опухоли в среднегрудном отделе пищевода. * Доказано, что предоперационная лучевая терапия оказывает бластостатическии эффект, расширяет резектабельность, приводит к уменьшению количества местных рецидивов. * В качестве компонента комбинированного лечения лучевая терапия позволяет расширить показания к радикальному лечению местно-распространенных опухолей пищевода, повысить радикальность операций, снизить частоту местных рецидивов и метастазов. Предоперационная лучевая терапия проводится в различных вариантах. Применение методики укрупненного фракционирования дозы интенсивным ритмом по 4 Гр 5 -6 раз в неделю до СОД 20 -24 Гр оправдано при малой протяженности опухоли, при отсутствии глубокого изъязвления опухоли, при дисфагии I-II степени и отсутствии выраженных нарушений со стороны сердечно-сосудистой и дыхательной систем.
 При большей протяженности опухоли более оправданно применение методики классического фракционирования по 2 Гр 5 раз в неделю до СОД 4045 Гр или схемы динамического фракционирования дозы - по 4 Гр 3 дня, затем по 2 Гр ежедневно до СОД 36 -42 Гр. Оптимальный интервал между окончанием лучевой терапии и операцией при методике укрупненного фракционирования дозы - 5 -7 дней, а при методике классического и динамического фракционирования 2 -3 недели. Лучевая терапия в традиционном варианте комбинированного лечения используется перед операцией, однако в клинической практике возникают такие ситуации, когда проведение лучевой терапии до операции осуществлено либо из-за высокого риска развития осложнений, связанных с распадом. В этих случаях целесообразно использовать послеоперационное облучение. В случаях, когда клетки опухоли вышли за пределы ее видимых границ или остались в ее ложе, сохранив биологическую активность, целесообразно использование химиотерапии. Химиотерапия применяется при низкодифференцированных формах рака пищевода и при мелкоклеточном раке пищевода.
При большей протяженности опухоли более оправданно применение методики классического фракционирования по 2 Гр 5 раз в неделю до СОД 4045 Гр или схемы динамического фракционирования дозы - по 4 Гр 3 дня, затем по 2 Гр ежедневно до СОД 36 -42 Гр. Оптимальный интервал между окончанием лучевой терапии и операцией при методике укрупненного фракционирования дозы - 5 -7 дней, а при методике классического и динамического фракционирования 2 -3 недели. Лучевая терапия в традиционном варианте комбинированного лечения используется перед операцией, однако в клинической практике возникают такие ситуации, когда проведение лучевой терапии до операции осуществлено либо из-за высокого риска развития осложнений, связанных с распадом. В этих случаях целесообразно использовать послеоперационное облучение. В случаях, когда клетки опухоли вышли за пределы ее видимых границ или остались в ее ложе, сохранив биологическую активность, целесообразно использование химиотерапии. Химиотерапия применяется при низкодифференцированных формах рака пищевода и при мелкоклеточном раке пищевода.
 Лучевое и химиотерапевтическое лечение необходимо проводить на фоне терапии, направленной на предупреждение и купирование возможных нарушений эритро- и лейкопоэза, иммунодепрессии (переливание препаратов крови, иммуностимуляция, инфузионная терапия, витаминотерапия). Пятилетняя выживаемость больных после комбинированного лечения достигает 56, 6% при радикальном характере оперативных вмешательств и 7, 0 % после паллиативных. При комплексном лечении после паллиативных операций выживаемость достигает 30, 8 %. Рак пищевода в большинстве случаев является относительно медленно прогрессирующим заболеванием. По степени злокачественности он находится между самыми злокачественно текущими заболеваниями и теми, которые достаточно доброкачественны. Нелеченный рак имеет плохой прогноз. Средняя продолжительность жизни таких больных не превышает 5 -8 месяцев с момента появления признаков болезни. Правда, при ранней диагностике зарегистрированы случаи продолжительности жизни до 6 лет без какого-либо лечения. Прогноз заболевания при лучевой терапии зависит от формы роста опухоли. Наихудшими являются результаты при эндофитной форме роста опухоли. Трехлетние результаты при этой форме роста составляют 6 %, тогда как при экзофитной форме - 27 %.
Лучевое и химиотерапевтическое лечение необходимо проводить на фоне терапии, направленной на предупреждение и купирование возможных нарушений эритро- и лейкопоэза, иммунодепрессии (переливание препаратов крови, иммуностимуляция, инфузионная терапия, витаминотерапия). Пятилетняя выживаемость больных после комбинированного лечения достигает 56, 6% при радикальном характере оперативных вмешательств и 7, 0 % после паллиативных. При комплексном лечении после паллиативных операций выживаемость достигает 30, 8 %. Рак пищевода в большинстве случаев является относительно медленно прогрессирующим заболеванием. По степени злокачественности он находится между самыми злокачественно текущими заболеваниями и теми, которые достаточно доброкачественны. Нелеченный рак имеет плохой прогноз. Средняя продолжительность жизни таких больных не превышает 5 -8 месяцев с момента появления признаков болезни. Правда, при ранней диагностике зарегистрированы случаи продолжительности жизни до 6 лет без какого-либо лечения. Прогноз заболевания при лучевой терапии зависит от формы роста опухоли. Наихудшими являются результаты при эндофитной форме роста опухоли. Трехлетние результаты при этой форме роста составляют 6 %, тогда как при экзофитной форме - 27 %.
 Применение лучевой терапии по паллиативной программе дает возможность 7 -10 % больных прожить более года. Повышение эффективности лучевого лечения связывается с совершенствованием методик облучения, увеличением чувствительности опухоли к облучению за счет использования радиосенсибилизирующих препаратов и сочетанием с химиотерапией и иммуностимулирующими воздействиями. Продолжительность жизни после радикальных операций по поводу рака пищевода является основным и наиболее важным показателем эффективности хирургического и комбинированного лечения. При хирургическом лечении, среди перенесших радикальные операции, 5 -летний срок выживания зависит от различных обстоятельств. Основным является распространенность опухолевого процесса. При малых размерах Т 1 опухоли 5 -летняя выживаемость составляет 46, 9 %, при Т 2 - 42, 9 %, при Т 3 - 33, 7 %, при Т 4 – 25 %. Наличие метастазов в лимфатические узлы является неблагоприятным фактором и значительно уменьшает срок 5 -летней выживаемости (вдвое). При III стадии процесса комбинированное лечение (предоперационная лучевая терапия и операция) позволяет увеличить сроки 5 -летней выживаемости с 10, 5 до 25, 4 %.
Применение лучевой терапии по паллиативной программе дает возможность 7 -10 % больных прожить более года. Повышение эффективности лучевого лечения связывается с совершенствованием методик облучения, увеличением чувствительности опухоли к облучению за счет использования радиосенсибилизирующих препаратов и сочетанием с химиотерапией и иммуностимулирующими воздействиями. Продолжительность жизни после радикальных операций по поводу рака пищевода является основным и наиболее важным показателем эффективности хирургического и комбинированного лечения. При хирургическом лечении, среди перенесших радикальные операции, 5 -летний срок выживания зависит от различных обстоятельств. Основным является распространенность опухолевого процесса. При малых размерах Т 1 опухоли 5 -летняя выживаемость составляет 46, 9 %, при Т 2 - 42, 9 %, при Т 3 - 33, 7 %, при Т 4 – 25 %. Наличие метастазов в лимфатические узлы является неблагоприятным фактором и значительно уменьшает срок 5 -летней выживаемости (вдвое). При III стадии процесса комбинированное лечение (предоперационная лучевая терапия и операция) позволяет увеличить сроки 5 -летней выживаемости с 10, 5 до 25, 4 %.
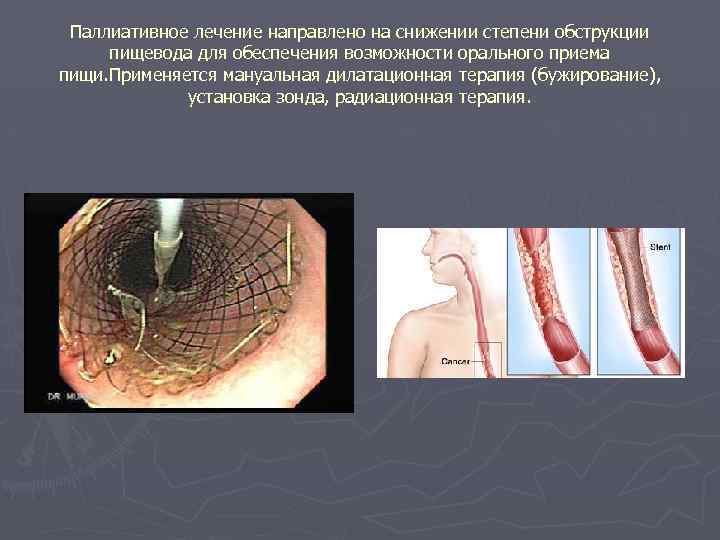 Паллиативное лечение направлено на снижении степени обструкции пищевода для обеспечения возможности орального приема пищи. Применяется мануальная дилатационная терапия (бужирование), установка зонда, радиационная терапия.
Паллиативное лечение направлено на снижении степени обструкции пищевода для обеспечения возможности орального приема пищи. Применяется мануальная дилатационная терапия (бужирование), установка зонда, радиационная терапия.



