Анальгезия с картинкой.ppt
- Количество слайдов: 60

Лечение острой боли

Определение боли n n Боль отнесена к категории чувств, таких как осязание, слух и другие Боль, как аффективное состояние организма, включающее эмоциональные, соматические и вегетативные реакции Боль – это мотивационное состояние, создающее соответствующую форму поведения Боль – это интегративная функция организма, которая мобилизует различные функциональные системы организма.

Определение боли n Боль – это неприятное ощущение и эмоциональное переживание, связанное с реальным или потенциальным повреждением тканей или описываемое в терминах такого повреждение.

Патогенез боли n n Рецепторы трансдукция Проводники боли трансмиссия Мозговой ствол модуляция Конечный или большой мозг перцепция
![Как человек ощущает боль? [N. Katz, F. M. Ferrante] Как человек ощущает боль? [N. Katz, F. M. Ferrante]](https://present5.com/presentation/3/-39337628_140491826.pdf-img/-39337628_140491826.pdf-5.jpg)
Как человек ощущает боль? [N. Katz, F. M. Ferrante]
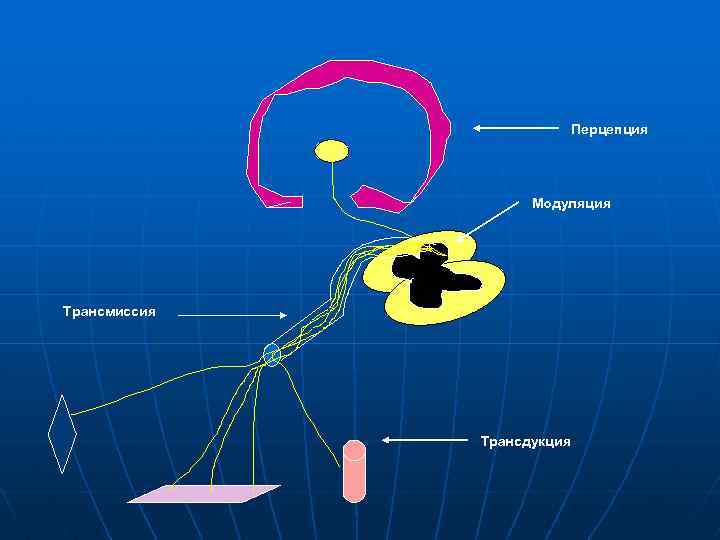
Перцепция Модуляция Трансмиссия Трансдукция

Сильная острая боль приводит: n n n К возбуждению различных отделов центральной и вегетативной нервных систем К усиленной выработке антидиуретического гормона и окситоцина Повышению продукции и выброса адреналина и норадреналина n Стимуляции метаболизма n Повышению температуры

Сильная острая боль приводит: n n n n n Усилению потребления кислорода Тахикардии Гипертензии Повышению периферического сосудистого тонуса Увеличению сердечного выброса К одышке К снижению секреции пищеварительных желез Рвоте диарее

Опиоидные анальгетики (E. Free 1987) 1. Полные агонисты (связь с -рецепторами) морфин, фентанил, промедол, омнопон, трамадол(? ) 2. Частичные агонисты (слабеее активируют рецепторы) бупренорфин(тамгезик, норфин, анфин) 3. Агонист – антагонисты ( +; -) бутарфанол(стадол, бефорал); налбуфин(нубаин) 4. Полные антагонисты( -) Налоксон, налтрексон
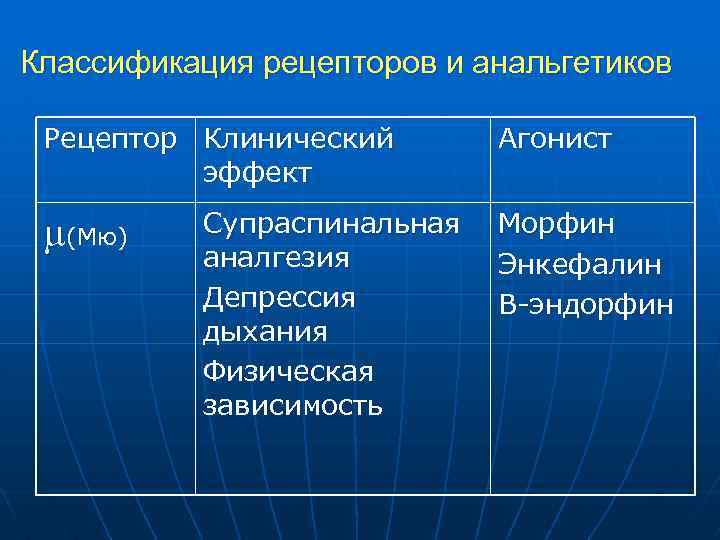
Классификация рецепторов и анальгетиков Рецептор Клинический эффект Агонист (Мю) Морфин Энкефалин В-эндорфин Супраспинальная аналгезия Депрессия дыхания Физическая зависимость
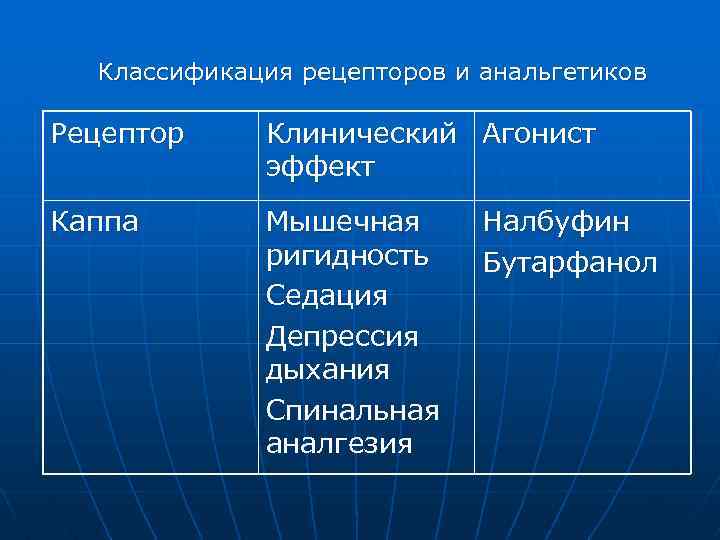
Классификация рецепторов и анальгетиков Рецептор Клинический Агонист эффект Каппа Мышечная ригидность Седация Депрессия дыхания Спинальная аналгезия Налбуфин Бутарфанол
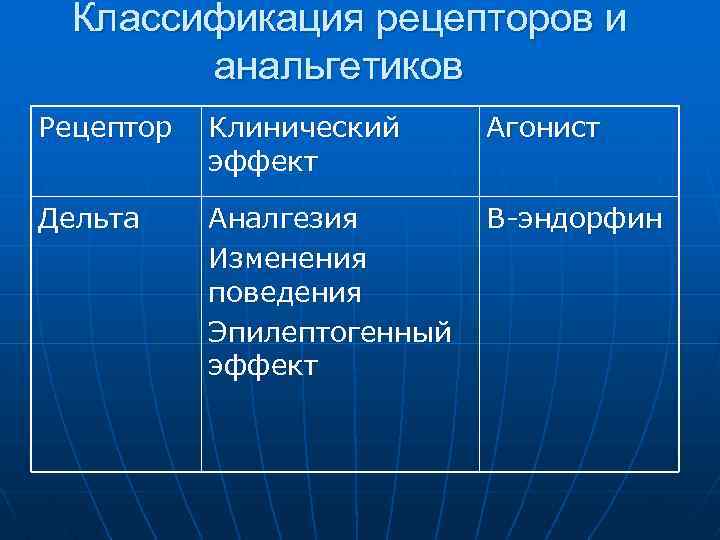
Классификация рецепторов и анальгетиков Рецептор Клинический эффект Агонист Дельта Аналгезия Изменения поведения Эпилептогенный эффект В-эндорфин
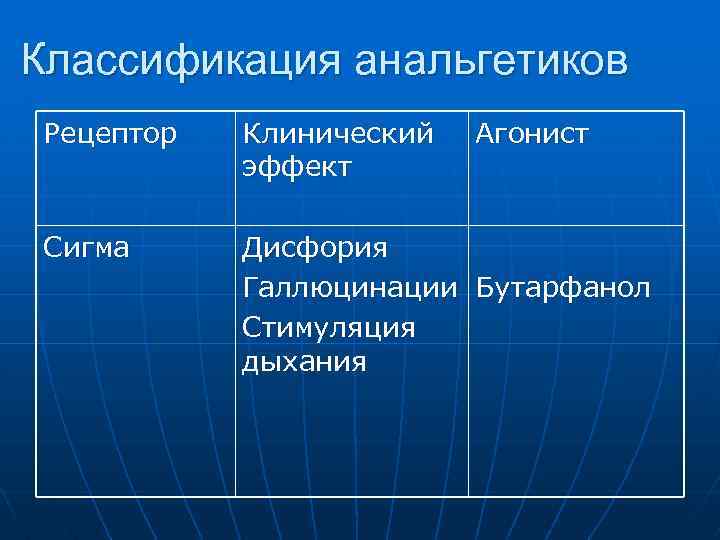
Классификация анальгетиков Рецептор Клинический эффект Агонист Сигма Дисфория Галлюцинации Бутарфанол Стимуляция дыхания

Механизм действия n n n Агонисты – активирующий опиоидные рецепторы Антагонисты – вытесняют опиоиды с рецепторов (налоксон) Агонисты - антогонисты

Морфин n n n Водорастворим При вм введении действие наступает через 20 – 30 минут и длится 4 - 5 часов Оказывает как угнетающее, так и стимулирующее действие на ЦНС: эйфория, сонливость

Морфин n n n n Вызывает депрессию дыхания Возбуждает центр глазодвигательного центра (миоз) Угнетает кашлевой рефлекс Вызывает тошноту, рвоту, атонию желудка и кишечника Спазм желчевыводящих путей Угнетает боль висцерального и соматического типа Эффективен при тупой и длительной боли

Омнопон n n Содержание морфина 48 – 50% Анальгетическая доза в 2 раза меньше, чем у морфина Содержит алкалоид из группы папаверина Чаще применяется при болях спастической природы

Группа фенилпипередина n n n Промедол В 3 – 4 раза уступает морфину по аналгетическим свойствам Слабее (морфина) угнетает дыхание Реже, чем морфин, вызывает тошноту и рвоту Расширяет зрачок

Фентанил n n n Жирорастворим В 100 раз превосходит морфин по анальгетическому эффекту Максимальный эффект отмечается через 1 – 2 минуты после вв и через 10 – 20 минут после вм введения

Дипидолор n n В 2 раза активнее морфина Не вызывает существенного угнетения дыхания Не вызывает рвоту Может применяться у больных с явлениями привыкания к морфину и промедолу

Трамадол - трамал n n n Слабый опиоид Мю – агонист(частичный) Сродство к Мю – рецепторам слабое (всего 13 дозы) Анальгетический потенциал средней силы Не обладает побочными свойствами

Опиоиды агонисты - антагонисты n n n Лексир, фортрал, морадол, стадол, нубаин Агонисты каппа – рецепторов Вызывают анальгезию и седацию Не угнетают дыхание Не вызывают тошноту и рвоту Хорошо купируют болевые приступы при печеночной и почечной коликах

Основные побочные эффекты опиоидов n n n Угнетение дыхания (дозо-зависимый эффект) Мышечная ригидность грудной клетки и живота Угнетение опорожнения желудка и перистальтики Повышение давления в общем желчном протоке, снижение продукции и оттока желчи, спазм сфинктера Одди Тошнота и рвота Артериальная гипотензия (редко)

НПВП Механизм действия n n n Периферические анальгетики Ингибируют циклооксигеназы и простагландины, участвуюшие в формировании болевого импульса в области болевого рецептора Купируют слабую и умеренной силы боль

Классификация наиболее известных НПВП n n n n n 1. производные арилкарбоновой кислоты -салициловая (аспирин) -трисалицилат -салициловая кислота и другие 2. Производные арилалкановой кислоты -диклофенак -ибупрофен -аклофенак -индометацин и другие

НПВП имеют следующие основные эффекты n n n Анальгетический Жаропонижающий Метаболические Снижают почечно – канальцевую реабсорбцию Снижают адгезивную способность тромбоцитов Вызывают гипотромбонемию

Побочные эффекты НПВП n n Острое повреждение слизистой желудка с интрамуральными гемморагиями Кровотечения (тромбоцитопения) из предшествующих повреждений слизистой желудка Провоцирует развитие солитарных язв Усугубляют изъязвление и вызывают осложнения у больных с предшествующей пептической язвенной болезнью

Длительное применение НПВП вызывает: n n Развитие капиллярного некроза Хронического интерстициального гепатита Кровоточивость и увеличение кровопотери во время операции У больных с бронхиальной астмой могут провоцировать бронхоспазм

Правила применения НПВП, разработанные ВОЗ n n При неэффективности препарата, необходимо назначить более сильный, а не другой анальгетик той же группы Лекарство должно вводиться регулярно, а не только при возникновении боли (снижения суточной дозы анальгетиков)

Правила применения НПВП, разработанные ВОЗ n n Добиваться анальгетического комфорта при минимальной дозе препарата Правильно подбирать оптимальные дозы препаратов, а не заменять их на более сильные Пероральные формы введения менее эффективны, чем парентеральные. Эффект развивается медленнее, но более продолжителен Врачу нужно больше остерегаться недостаточной дозы препарата, чем его передозировки

Преимущества и недостатки НПВП n n n Эффективен при лечении боли легкой и умеренной интенсивности Доступен для амбулаторного лечения Получение дополнительной аналгезии в комбинации с опиоидами Более дешевы Не вызывают толерантности или физической зависимости

n n n n n 3. Производные гетероарилуксусной кислоты -кеторолак -толметин -золиперак Клоперал 4. Производные эноликовой кислоты -лорноксикам -пироксикам -изоксикам -мелоксикам

Профилактика НПВП гастропатий n n Применение Н 2 блокаторов Н 2 – рецепторов второго (ранитидин) и третьего поколения (фамотидин) Синтетического аналога простогландинов Е - артротека

Критерии выбора анальгетика n n n Влияние препарата на интенсивность боли Индивидуальная переносимость Вероятность возникновения осложнений или побочных реакций

Проблема послеоперационной боли в XXI веке n n n От 30 до 75 % пациентов в послеоперационном периоде страдают от выраженного болевого синдрома Не менее 35 % пациентов, перенесших плановые и экстренные хирургические вмешательства страдают от острой боли В 17 % случаев интенсивность боли превышает ожидаемую [П. М. Овечкин, K. Davies, J. Svensson (Швеция) – IV Конгресс EFIC, Прага, 2003]

Данные исследований n Исследование Dolin S. , Cashman S, 2002 г. Великобритания. • Количество пациентов хирургических отделений - 20000 • Болевые ощущения средней интенсивности – 29, 7 % случаев • Боли высокой интенсивности – 10, 9 % n П. М. Овечкин и др. , 2001 г. , Россия • Количество пациентов хирургических отделений – 1550 • Неудовлетворенность качеством послеоперационного обезболивания выявлено у 40, 7 % пациентов

Чем опасна послеоперационная боль?

Критерии хронического болевого синдрома (ХБС) n n Развивается после хирургического вмешательства Длительность не менее 2 месяцев Исключены другие причины боли • Новообразования • Невриты • Хроническое воспаление и др. Частота ХБС составляет около 45 % • После торакотомии – 40 % • После мастэктомии – 35 -38 % • После «открытых» холецистэктомий – 25 % • После операции по поводу паховых грыж (генитофеморальный ХБС) – 12 % [F. Perkins, H. Kehlet, 2000 г. ]

Основные задачи послеоперационного обезболивания n n Повышение качества жизни пациентов в послеоперационном периоде Ускорение послеоперационной функциональной реабилитации Снижение частоты послеоперационных осложнений Сокращение сроков пребывания пациентов в клинике

Требования к анестезиологической защите пациента n n n Охват всех уровней ноцицепции (мультимодальность) Непрерывность анестезиологической защиты до, во время и после операции Индивидуальный выбор безопасных средств разных уровней

Классификация хирургических вмешательств по степени травматичности n n n Низкая • Артроскопические операции • Лапароскопические операции на желудочнокишечном тракте и органах малого таза • Флебэктомии и грыжесечения • Операции на щитовидной железе Средняя • Открытые гистерэктомия и холецистэктомия • Остеосинтез • Челюстно-лицевая хирургия Высокая • Реконструктивные операции на желудочно-кишечном тракте • Тотальное эндопротезирование крупных суставов • Операции по пересадке органов и тканей • Сердечно-сосудистая хирургия

Оценка интенсивности боли Визуальные шкалы для субъективной оценки боли
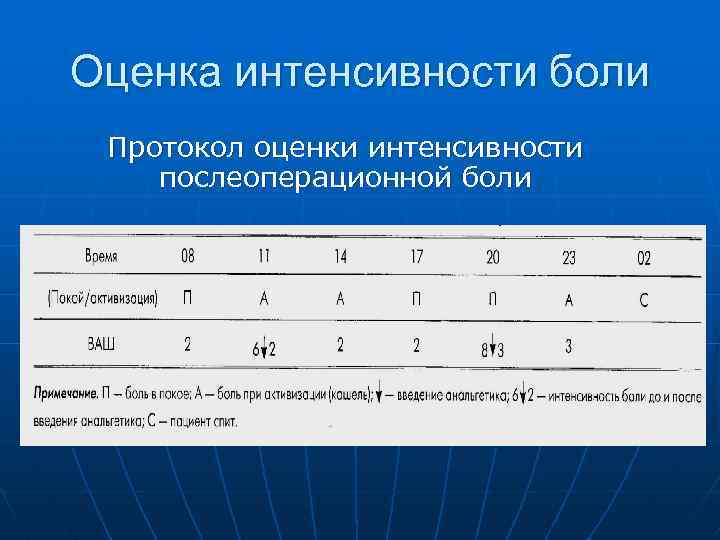
Оценка интенсивности боли Протокол оценки интенсивности послеоперационной боли

Принципы адекватной оценки боли n n n Исследование интенсивности боли осуществляется как в покое, так и при движении пациента Эффективность обезболивания определяется до и после назначения каждого анальгетика или метода анальгезии Для пациентов с болью высокой интенсивности, её оценка на начальном этапе производится каждые 15 мин, а затем, по мере снижения интенсивности, каждые 1 -2 часа Необходимость обезболивания определяется по критерию максимально допустимой интенсивности боли (пороги вмешательства). По 10 -бальной ВАШ максимально допустима интенсивность боли 3 балла в покое и 4 балла при движении Особого внимания заслуживают пациенты, контакт с которыми затруднен.

Данные опросов n А. М. Овечкин, С. В. Свиридов, 2006 г. , Россия. • Опрос врачей хирургических специальностей – 313 чел. • Наиболее часто используемые анальгетики в послеоперационном периоде: n n n метамизол натрия (анальгин) – 34 % промедол – 20% Конгресс “Euroanestesia – 2005”, Вена, Австрия. • Опрос участников конгресса – 2362 чел. • Наиболее часто используемые анальгетики в послеоперационном периоде: n n n n Морфин Парацетамол Трамадол Петидин Диклофенак Кеторолак Метамизол кетопрофен
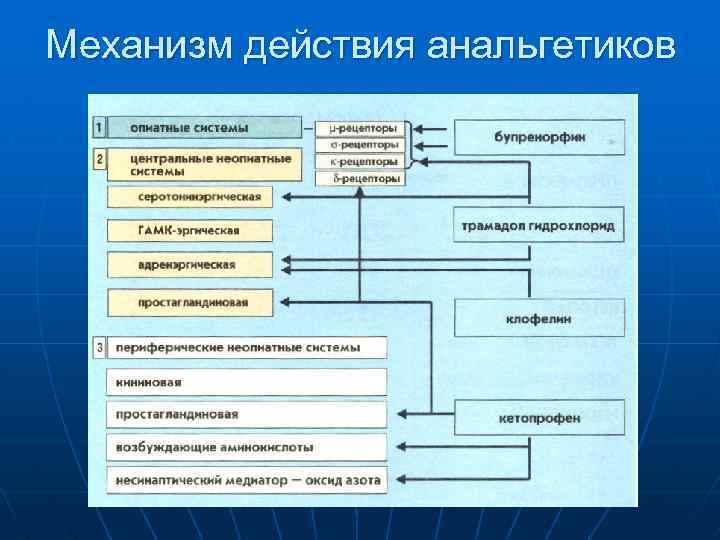
Механизм действия анальгетиков

Концепция послеоперационного обезболивания Мультимодальная анальгезия – это одновременное назначение двух и более анальгетиков, обладающих различными механизмами действияи позволяющих достичь адекватной анальгезии при минимуме побочных эффектов.
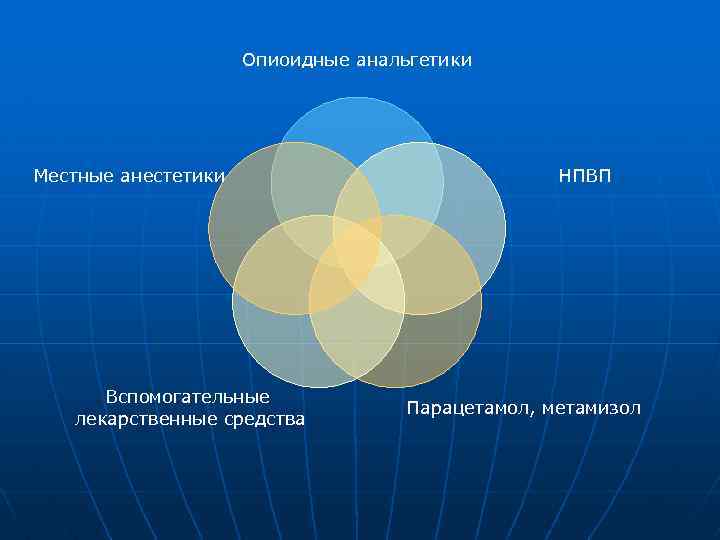
Опиоидные анальгетики Местные анестетики Вспомогательные лекарственные средства НПВП Парацетамол, метамизол

Анальгезия опиоидами n n n n Центральный механизм действия путем возбуждения µ, κ, δ, σ – рецепторов Чаще используется в качестве моноанальгезии Эффективность обезболивания составляет 25 -30% Эффективная анальгетическая доза близка к дозе, вызывающей депрессию дыхания Частота клинически значимых побочных эффектов опиоидов имеет дозозависимый характер (доказательство II уровня) Контролируемая пациентом анальгезия (КПА) современный вариант обезболивания опиоидами У взрослых пациентов возраст в большей степени, чем масса тела, определяет эффективную дозу опиоидов (доказательство IV уровня) Нарастание уровня седации является более ранним

Анальгезия опиоидами трамадол n n Изомер (+) оказывает агонистическое влияние на µ-, δ-, κ-рецепторы с более выраженным сродством к µ-рецепторам, таким образом, оказывая влияние на опиоидные рецепторы, опосредующие анальгезию. Изомер (-), активирующий центральную норадренэргическую и серотонинергическую системы путем подавления обратного захвата эндогенных трансмиттеров (норадреналина и серотонина), оказывает действие на неопиатные механизмы реализации обезболивания.

Анальгезия нестероидными противовоспалительными препаратами (НПВП) n n НПВП препятствуют развитию сенситизации периферических ноцицепторов Ингибируют ЦОГ-1 и ЦОГ-2 (кеторолак, кетопрофен, диклофенак) Селективные ингибиторы ЦОГ-2 обладают меньшими побочными эффектами (мелоксикам, нимесулид) Являются средствами патогенетической терапии боли

Анальгезия НПВП Кетопрофен (кетонал) n Периферический механизм • • • n Подавление синтеза простагландинов Воздействие на продукцию оксида азота Подавление нейрональной активности, вызываемой раздражающими аминокислотами и брадикинином Центральный механизм • Подавление высвобождения простагландинов в ЦНС • Влияние на высвобождение эндогенных опиоидных пептидов • Непосредственное действие на таламические центры болевой чувствительности n Усиление периферического механизма центральным и наоборот

Анальгезия парацетамолом n n n Не имеет эндогенных рецепторв и не подавляет активность ЦОГ на периферии Подавляет активность ЦОГ-2 в ЦНС Подавляет активность ЦОГ-3, которая обладает селективной чувствительностью к парацетамолу Повышает активность нисходящих тормозных серотониновых путей Препятствует продукции простагландинов на уровне клетки Является эффективным анальгетиком, потенциал которого несколько уступает стандартным дозам морфина или НПВП

Анальгезия клофелином n n Обладает центральным адреномиметическим действием (неопиатный механизм) Отсутствие депресси дыхания Медленное развитие толерантности к анальгезии Потенцирует действие общих анестетиков и опиоидов

Анальгезия кетамином n n n Является антагонистом N-метил-D-аспартат (NMDA)-рецепторов Как антагонист NMDA-рецепторов оказывает эффект предупреждающей анестезии (доказательство I уровня) Оказывает опиоидосберегающий эффект при назначении в дозах 0, 1 – 0, 2 мг/кг в послеоперационном периоде Повышает качество обезболивания у пациентов с интенсивной послеоперационной болью, резистентной к назначению опиоидов (доказательство II уровня) Целесообразность использования кетамина в схеме послеоперационного обезболивания подтверждена данными доказательной медицины (Acute Pain Management Scintific Evidence, 2 -nd edition, 2005)

Регионарная анальгезия n Механизм действия: Прерывание афферентного потока ноцицептивных стимулов от периферических болевых рецепторов в органах и тканях к сегментарным структурам ЦНС (задние рога спинного мозга)

Эпидуральная анальгезия (ЭА) n Исследование A. Rogers et al. , 2000 (доказательство I уровня) • Продленная ЭА, которая проводится в течение 24 часов после операции снижает количество послеоперационных осложнений: n n n Тромбоз глубоких вен (ТГВ) – на 44 % ТЭЛА – на 50 % Легочных инфекционных осложнений - на 39 % При всех типах хирургических операций ЭА обеспечивает более высокое качество обезболивания по сравнению с парентеральным введением опиоидов Наиболее эффективноя является ЭА на уровне грудного отдела позвоночника Продленная ЭА – преимущества: • • Стабильный уровень анальгезии Отсутствие выраженных изменений гемодинамики Менее выраженная моторная блокада или ее полное отсутствие Минимальный риск инфицирования эпидурального катетера

Euro. Pain руководство: фармакотерапия послеоперационной боли «Большая» хирургия - торакотомия - обширные абдоминальные операции «Малая хирургия» - грыжесечение - Сафенэктомия - гинекологические операции «Средняя» хирургия Гистерэктомия Черепно – лицевая Хирургия - - парацетамолНПВС Иинфильтрационная анестезия Периферическая блокада нервов - - - ПарацетамолНПВС Инфильтрационная анестезия Системное введение опиоидов Периферическая блокада ПарацетамолНПВС Эпидуральная анестезия - Опиоиды или комбинированное введение анальгетиков или системное введение опиоидов Euro. Pain – European Minmum Standards for the Management of Postoperative Pain - 1998

Варианты схем мультимодальной анальгезии

Варианты схем мультимодальной анальгезии n Схема 1 • Кетонал – 50 -10 мг (1 -2 мл) в/м, 2 -3 раза в сутки • Трамал – 50 -10 мг (1 -2 мл) в/м, 2 -3 раза в сутки n Схема 2 • • • n Кетонал – 50 -10 мг (1 -2 мл) в/м, 2 -3 раза в сутки Норфин – 0, 3 мг (1 мл) в/м, 1 раз в сутки Клофелин - 0, 05 – 0, 1 мг (0, 5 – 1 мл) в/м, 2 -3 раза в сутки Схема 3 • • • Кетонал – 50 -10 мг (1 -2 мл) в/м, 2 -3 раза в сутки Морадол – 2 мг (1 мл) в/м, 2 -4 раза в сутки Контрикал – 10 000 ЕД в/в капельно, 2 -3 раза в сутки
Анальгезия с картинкой.ppt