Лечение опухолей пищевода - короткая.ppt
- Количество слайдов: 59
 Лечение опухолей пищевода: лучевая и химиотерапия Подготовила студентка 28 группы 4 курса лечебного факультета Солнцева Алина Витальевна
Лечение опухолей пищевода: лучевая и химиотерапия Подготовила студентка 28 группы 4 курса лечебного факультета Солнцева Алина Витальевна
 Основные методы лечения: n 1. Хирургический n 2. Лучевой n 3. Комбинированный: лучевой и хирургический n 4. Комплексный: хирургический, лучевой и лекарственный (химиотерапевтический)
Основные методы лечения: n 1. Хирургический n 2. Лучевой n 3. Комбинированный: лучевой и хирургический n 4. Комплексный: хирургический, лучевой и лекарственный (химиотерапевтический)
 Варианты лечения в зависимости от стадии: Стадия: Метод лечения: I‑IIA (Т 1– 3 N 0 M 0) Хирургический IIВ – III (Т 1– 2 N 1 M 0; Т 3 N 1 M 0) Хирургический; комбинированный (неоадъювантная химиотерапия(ХТ) + хир. лечение) комплексный (периоперационная химиолучевая терапия (ХЛТ) + хир. лечение) III (Т 4 или множественные Комбинированный (ХЛТ; ХТ + хир. лечение); метастазы (мтс) в регионарные л. у. средостения) IV Химиотерапевтический
Варианты лечения в зависимости от стадии: Стадия: Метод лечения: I‑IIA (Т 1– 3 N 0 M 0) Хирургический IIВ – III (Т 1– 2 N 1 M 0; Т 3 N 1 M 0) Хирургический; комбинированный (неоадъювантная химиотерапия(ХТ) + хир. лечение) комплексный (периоперационная химиолучевая терапия (ХЛТ) + хир. лечение) III (Т 4 или множественные Комбинированный (ХЛТ; ХТ + хир. лечение); метастазы (мтс) в регионарные л. у. средостения) IV Химиотерапевтический
 Лучевая терапия n Дистанционный метод. Облучение производят на n n некотором расстоянии от поверхности кожного покрова. Контактный метод. Аппарат с радиоактивным источником располагают непосредственно на коже. Внутриполостной метод. Устройство вводят в поврежденный раком орган (матку, прямую кишку, пищевод и т. п. ). Внутритканевой метод. Источник радиоактивных лучей помещают в опухоль. Внутреннее облучение. Воздействие радионуклидами, которые избирательно накапливаются в каком-либо органе.
Лучевая терапия n Дистанционный метод. Облучение производят на n n некотором расстоянии от поверхности кожного покрова. Контактный метод. Аппарат с радиоактивным источником располагают непосредственно на коже. Внутриполостной метод. Устройство вводят в поврежденный раком орган (матку, прямую кишку, пищевод и т. п. ). Внутритканевой метод. Источник радиоактивных лучей помещают в опухоль. Внутреннее облучение. Воздействие радионуклидами, которые избирательно накапливаются в каком-либо органе.
 Лучевая терапия Рекомендованные периоды использования: n n n до операции (чтобы уменьшить размеры опухоли); после операции (чтобы убить оставшиеся раковые клетки); до и после операции; при рецидивах рака через длительное время; при метастазировании опухоли в кости и лимфатические узлы.
Лучевая терапия Рекомендованные периоды использования: n n n до операции (чтобы уменьшить размеры опухоли); после операции (чтобы убить оставшиеся раковые клетки); до и после операции; при рецидивах рака через длительное время; при метастазировании опухоли в кости и лимфатические узлы.
 Лучевая терапия Показания: 1. Наличие противопоказаний к хирургическому лечению: n Сопутствующая патология (СС, дыхательной и др. систем) n Преклонный возраст больных n Отказ от операции 2. в комплексе с другими методами лечения 3. паллиативное лечение
Лучевая терапия Показания: 1. Наличие противопоказаний к хирургическому лечению: n Сопутствующая патология (СС, дыхательной и др. систем) n Преклонный возраст больных n Отказ от операции 2. в комплексе с другими методами лечения 3. паллиативное лечение
 Лучевая терапия Противопоказания: n наличие фистулы; n распад опухоли с кровотечением; n прорастание всех слоев стенки трахеи, главных бронхов и аорты; n активная форма туберкулеза легких; n анемия (Hb < 80 г/л), лейкопения (Л < 2, 0 × 10, 9 л), тромбоцитопения (Тр < 75 × 10, 9 л); n перенесенный инфаркт миокарда и инсульт (по ВК); n психические расстройства в период обострения; n некупируемое состояние больного по шкале Карновского 40% и менее (шкала ECOG > 2). n выраженные явления интоксикации; тяжелое состояние пациента; n лихорадка; n кахексия;
Лучевая терапия Противопоказания: n наличие фистулы; n распад опухоли с кровотечением; n прорастание всех слоев стенки трахеи, главных бронхов и аорты; n активная форма туберкулеза легких; n анемия (Hb < 80 г/л), лейкопения (Л < 2, 0 × 10, 9 л), тромбоцитопения (Тр < 75 × 10, 9 л); n перенесенный инфаркт миокарда и инсульт (по ВК); n психические расстройства в период обострения; n некупируемое состояние больного по шкале Карновского 40% и менее (шкала ECOG > 2). n выраженные явления интоксикации; тяжелое состояние пациента; n лихорадка; n кахексия;
 Шкала Карновского – общая оценка функционального статуса больного. Функциональная активность Практически здоров: жалоб нет; признаков заболевания нет. 100 Сохранена нормальная ежедневная активность; незначительная степень выраженности проявлений заболевания. 90 Нормальная ежедневная активность поддерживается с усилием; умеренная степень выраженности проявлений заболевания. Сохранена нормальная ежедневная активность; медицинская помощь не требуется. Оценка(%) 80 Утрата трудоспособности, возможно проживание в домашних условиях; большей частью способен себя обслужить; требуется уход в различном объеме. Способен себя обслужить; не способен поддерживать нормальную 70 ежедневную активность или выполнять активную работу. Не способен себя обслужить, требуется госпитальная помощь; возможна быстрая прогрессия заболевания. Большей частью способен себя обслужить, однако в отдельных случаях нуждается в уходе. 60 Частично способен себя обслужить, частично нуждается в уходе, часто требуется медицинская помощь. 50 Не способен себя обслуживать, требуются специальный уход и медицинская помощь. 40 Не способен себя обслуживать, показана госпитализация, хотя непосредственная угроза для жизни отсутствует. 30 Тяжелое заболевание: необходима госпитализация, необходима активная поддерживающая терапия. 20 Терминальный период: быстро прогрессирующий фатальный процесс. 10 Смерть. 0
Шкала Карновского – общая оценка функционального статуса больного. Функциональная активность Практически здоров: жалоб нет; признаков заболевания нет. 100 Сохранена нормальная ежедневная активность; незначительная степень выраженности проявлений заболевания. 90 Нормальная ежедневная активность поддерживается с усилием; умеренная степень выраженности проявлений заболевания. Сохранена нормальная ежедневная активность; медицинская помощь не требуется. Оценка(%) 80 Утрата трудоспособности, возможно проживание в домашних условиях; большей частью способен себя обслужить; требуется уход в различном объеме. Способен себя обслужить; не способен поддерживать нормальную 70 ежедневную активность или выполнять активную работу. Не способен себя обслужить, требуется госпитальная помощь; возможна быстрая прогрессия заболевания. Большей частью способен себя обслужить, однако в отдельных случаях нуждается в уходе. 60 Частично способен себя обслужить, частично нуждается в уходе, часто требуется медицинская помощь. 50 Не способен себя обслуживать, требуются специальный уход и медицинская помощь. 40 Не способен себя обслуживать, показана госпитализация, хотя непосредственная угроза для жизни отсутствует. 30 Тяжелое заболевание: необходима госпитализация, необходима активная поддерживающая терапия. 20 Терминальный период: быстро прогрессирующий фатальный процесс. 10 Смерть. 0
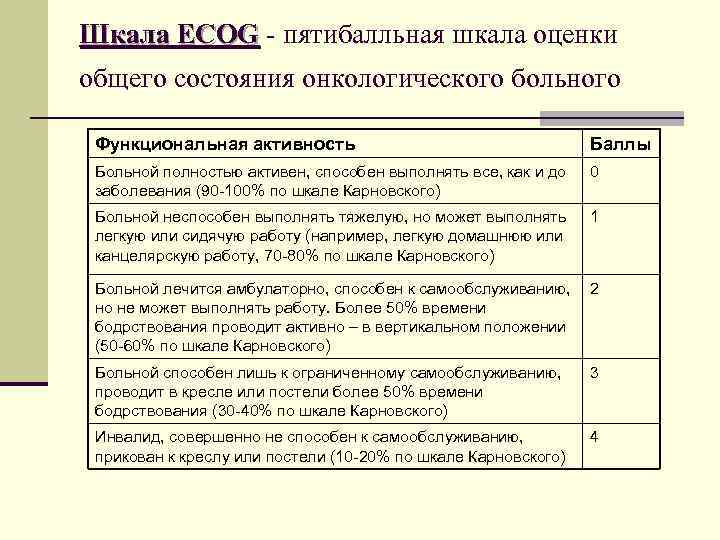 Шкала ECOG - пятибалльная шкала оценки общего состояния онкологического больного Функциональная активность Баллы Больной полностью активен, способен выполнять все, как и до заболевания (90 -100% по шкале Карновского) 0 Больной неспособен выполнять тяжелую, но может выполнять легкую или сидячую работу (например, легкую домашнюю или канцелярскую работу, 70 -80% по шкале Карновского) 1 Больной лечится амбулаторно, способен к самообслуживанию, 2 но не может выполнять работу. Более 50% времени бодрствования проводит активно – в вертикальном положении (50 -60% по шкале Карновского) Больной способен лишь к ограниченному самообслуживанию, проводит в кресле или постели более 50% времени бодрствования (30 -40% по шкале Карновского) 3 Инвалид, совершенно не способен к самообслуживанию, прикован к креслу или постели (10 -20% по шкале Карновского) 4
Шкала ECOG - пятибалльная шкала оценки общего состояния онкологического больного Функциональная активность Баллы Больной полностью активен, способен выполнять все, как и до заболевания (90 -100% по шкале Карновского) 0 Больной неспособен выполнять тяжелую, но может выполнять легкую или сидячую работу (например, легкую домашнюю или канцелярскую работу, 70 -80% по шкале Карновского) 1 Больной лечится амбулаторно, способен к самообслуживанию, 2 но не может выполнять работу. Более 50% времени бодрствования проводит активно – в вертикальном положении (50 -60% по шкале Карновского) Больной способен лишь к ограниченному самообслуживанию, проводит в кресле или постели более 50% времени бодрствования (30 -40% по шкале Карновского) 3 Инвалид, совершенно не способен к самообслуживанию, прикован к креслу или постели (10 -20% по шкале Карновского) 4
 Лучевая терапия Противопоказания: n n n • • • обширное поражение раком; раковый плеврит; множественные метастазы; лучевая болезнь; сопутствующие заболевания в тяжелой форме (по решению ВК): инфаркт миокарда, болезни почек, дыхательная недостаточность, активный туберкулез легких, третья степень сердечно-сосудистой недостаточности, декомпенсированный диабет и др.
Лучевая терапия Противопоказания: n n n • • • обширное поражение раком; раковый плеврит; множественные метастазы; лучевая болезнь; сопутствующие заболевания в тяжелой форме (по решению ВК): инфаркт миокарда, болезни почек, дыхательная недостаточность, активный туберкулез легких, третья степень сердечно-сосудистой недостаточности, декомпенсированный диабет и др.
 Лучевая терапия: плюсы и минусы Плюсы: v раковые клетки перестают делиться, часть их гибнет; опухоль уменьшается; v сосуды, питающие рак, частично зарастают; Минусы: ― гиперчувствительность к облучению кроветворной системы и эпителия кишечника; ― много побочных реакций, возникающих во время лечения.
Лучевая терапия: плюсы и минусы Плюсы: v раковые клетки перестают делиться, часть их гибнет; опухоль уменьшается; v сосуды, питающие рак, частично зарастают; Минусы: ― гиперчувствительность к облучению кроветворной системы и эпителия кишечника; ― много побочных реакций, возникающих во время лечения.
 Лучевая терапия Побочные эффекты: n При дистанционном методе лечения появляется зуд, шелушение кожи, сухость, краснота, мелкие пузырьки. n При облучении шеи может появиться першение в горле, сухость, боль при глотании, осиплость голоса. Нарушается аппетит. n При воздействии на органы грудной полости может появиться сухой кашель, боль в горле при глотании, одышка, болезненность мышц.
Лучевая терапия Побочные эффекты: n При дистанционном методе лечения появляется зуд, шелушение кожи, сухость, краснота, мелкие пузырьки. n При облучении шеи может появиться першение в горле, сухость, боль при глотании, осиплость голоса. Нарушается аппетит. n При воздействии на органы грудной полости может появиться сухой кашель, боль в горле при глотании, одышка, болезненность мышц.
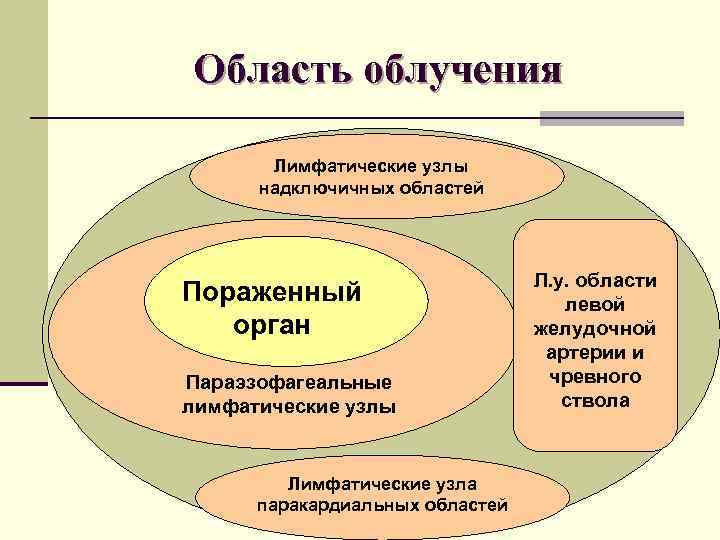 Область облучения Лимфатические узлы надключичных областей Пораженный орган Параэзофагеальные лимфатические узлы Лимфатические узла паракардиальных областей Л. у. области левой желудочной артерии и чревного ствола
Область облучения Лимфатические узлы надключичных областей Пораженный орган Параэзофагеальные лимфатические узлы Лимфатические узла паракардиальных областей Л. у. области левой желудочной артерии и чревного ствола
 Предоперационная лучевая терапия: n Оказывает бластостатический эффект n Расширяет резектабельность n Уменьшает количество местных рецидивов и метастазов
Предоперационная лучевая терапия: n Оказывает бластостатический эффект n Расширяет резектабельность n Уменьшает количество местных рецидивов и метастазов
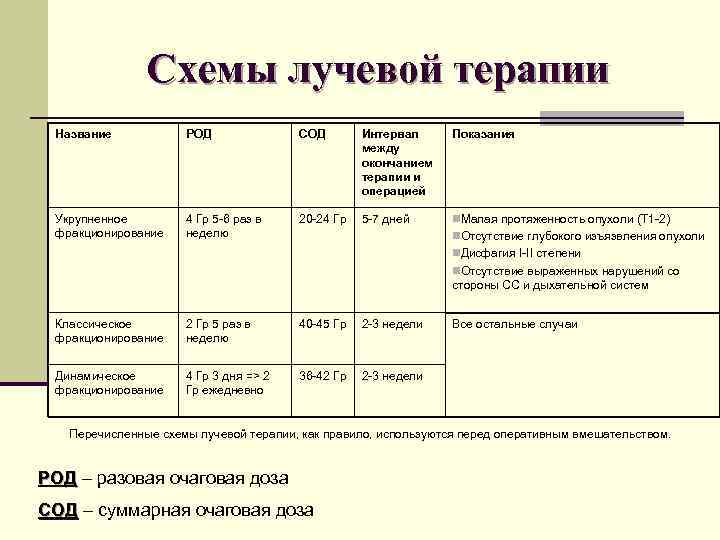 Схемы лучевой терапии Название РОД СОД Интервал между окончанием терапии и операцией Показания Укрупненное фракционирование 4 Гр 5 -6 раз в неделю 20 -24 Гр 5 -7 дней n. Малая протяженность опухоли (Т 1 -2) n. Отсутствие глубокого изъязвления опухоли n. Дисфагия I-II степени n. Отсутствие выраженных нарушений со стороны СС и дыхательной систем Классическое фракционирование 2 Гр 5 раз в неделю 40 -45 Гр 2 -3 недели Динамическое фракционирование 4 Гр 3 дня => 2 Гр ежедневно 36 -42 Гр Все остальные случаи 2 -3 недели Перечисленные схемы лучевой терапии, как правило, используются перед оперативным вмешательством. РОД – разовая очаговая доза РОД СОД – суммарная очаговая доза СОД
Схемы лучевой терапии Название РОД СОД Интервал между окончанием терапии и операцией Показания Укрупненное фракционирование 4 Гр 5 -6 раз в неделю 20 -24 Гр 5 -7 дней n. Малая протяженность опухоли (Т 1 -2) n. Отсутствие глубокого изъязвления опухоли n. Дисфагия I-II степени n. Отсутствие выраженных нарушений со стороны СС и дыхательной систем Классическое фракционирование 2 Гр 5 раз в неделю 40 -45 Гр 2 -3 недели Динамическое фракционирование 4 Гр 3 дня => 2 Гр ежедневно 36 -42 Гр Все остальные случаи 2 -3 недели Перечисленные схемы лучевой терапии, как правило, используются перед оперативным вмешательством. РОД – разовая очаговая доза РОД СОД – суммарная очаговая доза СОД
 Классическое фракционирование дозы 5 сеансов лучевой терапии в неделю в разовой очаговой дозе 1, 5 – 2 Гр Цель: создание в области облучаемого органа терапевтической дозы в 60 -70 Гр
Классическое фракционирование дозы 5 сеансов лучевой терапии в неделю в разовой очаговой дозе 1, 5 – 2 Гр Цель: создание в области облучаемого органа терапевтической дозы в 60 -70 Гр

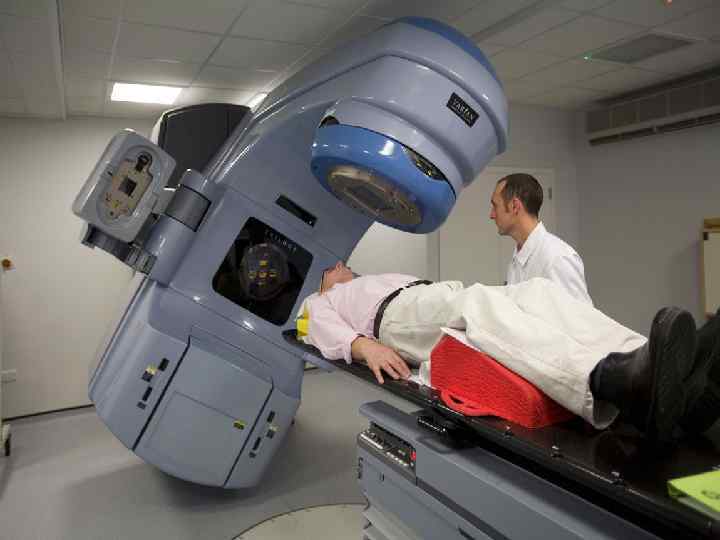
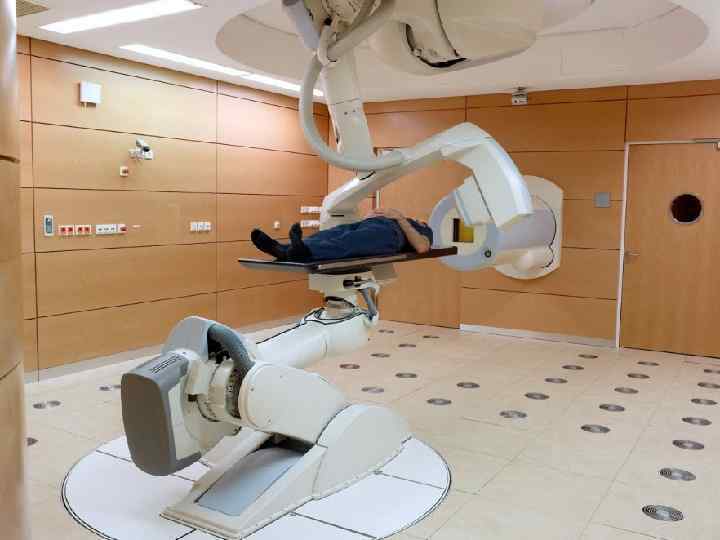
 Внутриполостное облучение брахитерапия n Аппарат АГАТ ВУ (тонкий зонд + радиоактивный кобальт)
Внутриполостное облучение брахитерапия n Аппарат АГАТ ВУ (тонкий зонд + радиоактивный кобальт)
 Брахитерапия Противопоказания: n протяженность опухоли по пищеводу более 10 см; n наличие отдаленных метастазов; n прорастание опухолью всех слоев трахеи и главных бронхов.
Брахитерапия Противопоказания: n протяженность опухоли по пищеводу более 10 см; n наличие отдаленных метастазов; n прорастание опухолью всех слоев трахеи и главных бронхов.
 Брахитерапия В исследовании Е. Левченко и соавт. (XVI Российский онкологический конгресс) была показана эффективность брахитерапии в комплексном лечении рака пищевода совместно с химиолучевой терапией. Данный метод лечений позволил в 30% случаев достигнуть полного местного регресса опухоли.
Брахитерапия В исследовании Е. Левченко и соавт. (XVI Российский онкологический конгресс) была показана эффективность брахитерапии в комплексном лечении рака пищевода совместно с химиолучевой терапией. Данный метод лечений позволил в 30% случаев достигнуть полного местного регресса опухоли.
 Брахитерапия Осложнения неоадъювантной терапии (36%): n Эзофагит (9%); n Гематологические осложнения (15%); n Постлучевой рубцовый стеноз (6%); n Внутрибольничная аспирационная пневмония (3%); n Кровотечение из хронической язвы желудка (3%).
Брахитерапия Осложнения неоадъювантной терапии (36%): n Эзофагит (9%); n Гематологические осложнения (15%); n Постлучевой рубцовый стеноз (6%); n Внутрибольничная аспирационная пневмония (3%); n Кровотечение из хронической язвы желудка (3%).
 Сочетанная лучевая терапия При отсутствии противопоказаний к проведению брахитерапии n I этап – дистанционная лучевая терапия в дозе СОД 50 Гр по 2 Гр 5 раз в неделю непрерывным курсом в течение 5 недель; n II этап – брахитерапия через 2– 3 недели после дистанционной лучевой терапии в 3 сеанса по 5 Гр с интервалом 7 дней.
Сочетанная лучевая терапия При отсутствии противопоказаний к проведению брахитерапии n I этап – дистанционная лучевая терапия в дозе СОД 50 Гр по 2 Гр 5 раз в неделю непрерывным курсом в течение 5 недель; n II этап – брахитерапия через 2– 3 недели после дистанционной лучевой терапии в 3 сеанса по 5 Гр с интервалом 7 дней.
 Электромагнитная гипертермия В исследовании Борисова В. А. и соавт. приводятся данные об использовании электромагнитной гипертермии в комплексном лечении с лучевой и химиолучевой терапией. Согласно полученным данным, применение гипертермии уменьшает продолжительность жизни пациентов, однако при этом наблюдается улучшение качества жизни пациентов. (10)
Электромагнитная гипертермия В исследовании Борисова В. А. и соавт. приводятся данные об использовании электромагнитной гипертермии в комплексном лечении с лучевой и химиолучевой терапией. Согласно полученным данным, применение гипертермии уменьшает продолжительность жизни пациентов, однако при этом наблюдается улучшение качества жизни пациентов. (10)
 Химиотерапия Показания: 1. 2. 3. 4. 5. 6. Выход клеток за пределы видимых границ опухоли Высокая биологическая активность клеток в ложе опухоли Низкодифференцированные формы рака пищевода Мелкоклеточный рак пищевода Нерадикальное удаление опухоли Наличие отдаленных метастазов
Химиотерапия Показания: 1. 2. 3. 4. 5. 6. Выход клеток за пределы видимых границ опухоли Высокая биологическая активность клеток в ложе опухоли Низкодифференцированные формы рака пищевода Мелкоклеточный рак пищевода Нерадикальное удаление опухоли Наличие отдаленных метастазов
 Применение химиопрепаратов в зависимости от экспрессии генов n ERCC-1 – участвует в восстановлении повреждений ДНК, индуцируемых алкилирующими агентами (препараты платины), путем эксцизионной репарации нуклеотидов. n Her-2/neu (c-erb. B 2) – онкоген семейства рецепторов эпидермального фактора роста. Her-2/neu определяет резистентность к химиотерапевтическим препаратам таким, как таксаны, цисплатин и фторпиримидины. Гиперэкспрессия c-erb. B 2 вне зависимости от проведения химиотерапии коррелирует с низкой безрецидивной (p=0, 0474) и общей выживаемостью (p=0, 0310) больных после резекции. n Ki-67 – ген, свойственный для пролиферирующих клеток, характеризует агрессивность, злокачественность течения опухолевого процесса и вероятность ответа на проводимую терапию. Результаты исследований этого гена, тем не менее, неоднозначны.
Применение химиопрепаратов в зависимости от экспрессии генов n ERCC-1 – участвует в восстановлении повреждений ДНК, индуцируемых алкилирующими агентами (препараты платины), путем эксцизионной репарации нуклеотидов. n Her-2/neu (c-erb. B 2) – онкоген семейства рецепторов эпидермального фактора роста. Her-2/neu определяет резистентность к химиотерапевтическим препаратам таким, как таксаны, цисплатин и фторпиримидины. Гиперэкспрессия c-erb. B 2 вне зависимости от проведения химиотерапии коррелирует с низкой безрецидивной (p=0, 0474) и общей выживаемостью (p=0, 0310) больных после резекции. n Ki-67 – ген, свойственный для пролиферирующих клеток, характеризует агрессивность, злокачественность течения опухолевого процесса и вероятность ответа на проводимую терапию. Результаты исследований этого гена, тем не менее, неоднозначны.
 Классификация основных химиотерапевтических препаратов, использующихся в лечении ЗНО пищевода: 1. Противоопухолевые алкилирущие средства: n Препараты платины: - Цисплатин - Оксалиплатин - Карбоплатин 2. Противоопухолевые средства, ингибиторы ДНК-топоизомераз: - Иринотекан 3. Противоопухолевые средства, антиметаболиты: n произв. фторпиримидины: - 5‑фторурацил - Капецитабин 4. Противоопухолевые средства, нарушающие митоз: - Доцетаксел - Паклитаксел 5. Противоопухолевые антибиотики: n Антрациклины: + прозв. доксорубицина: - Эпирубицин 6. Моноклональные антитела: - Трастузумаб
Классификация основных химиотерапевтических препаратов, использующихся в лечении ЗНО пищевода: 1. Противоопухолевые алкилирущие средства: n Препараты платины: - Цисплатин - Оксалиплатин - Карбоплатин 2. Противоопухолевые средства, ингибиторы ДНК-топоизомераз: - Иринотекан 3. Противоопухолевые средства, антиметаболиты: n произв. фторпиримидины: - 5‑фторурацил - Капецитабин 4. Противоопухолевые средства, нарушающие митоз: - Доцетаксел - Паклитаксел 5. Противоопухолевые антибиотики: n Антрациклины: + прозв. доксорубицина: - Эпирубицин 6. Моноклональные антитела: - Трастузумаб
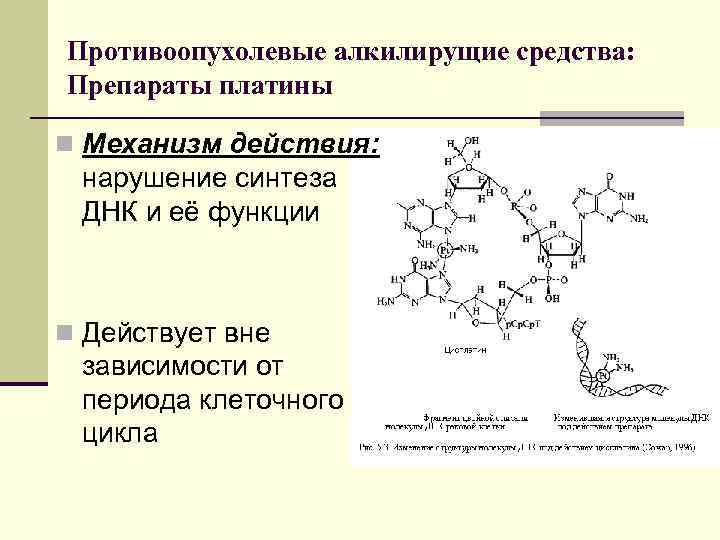 Противоопухолевые алкилирущие средства: Препараты платины n Механизм действия: нарушение синтеза ДНК и её функции n Действует вне зависимости от периода клеточного цикла
Противоопухолевые алкилирущие средства: Препараты платины n Механизм действия: нарушение синтеза ДНК и её функции n Действует вне зависимости от периода клеточного цикла
 Торговые названия препаратов
Торговые названия препаратов
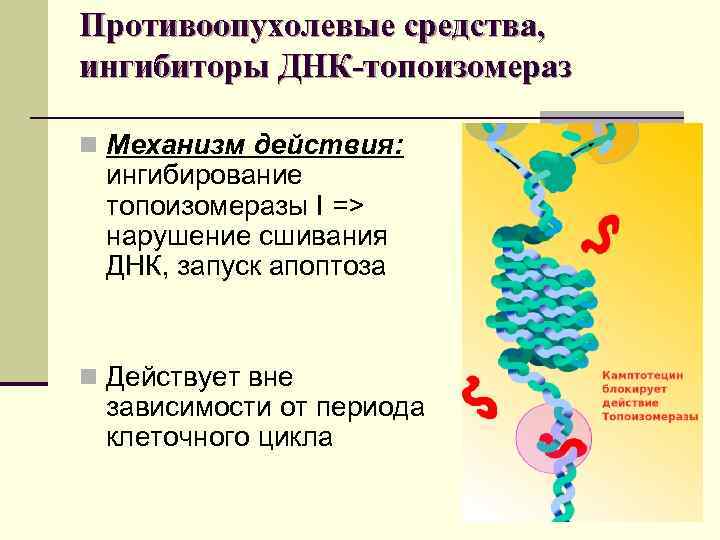 Противоопухолевые средства, ингибиторы ДНК-топоизомераз n Механизм действия: ингибирование топоизомеразы I => нарушение сшивания ДНК, запуск апоптоза n Действует вне зависимости от периода клеточного цикла
Противоопухолевые средства, ингибиторы ДНК-топоизомераз n Механизм действия: ингибирование топоизомеразы I => нарушение сшивания ДНК, запуск апоптоза n Действует вне зависимости от периода клеточного цикла
 Торговые названия препаратов
Торговые названия препаратов
 Противоопухолевые средства, антиметаболиты: произв. фторпиримидинов n Механизм действия: 1. Фтордезокси-УМФ – тимидилатсинтетазу => накопление дезокси-УМФ => нарушение репликации и функции ДНК:
Противоопухолевые средства, антиметаболиты: произв. фторпиримидинов n Механизм действия: 1. Фтордезокси-УМФ – тимидилатсинтетазу => накопление дезокси-УМФ => нарушение репликации и функции ДНК:
 Противоопухолевые средства, антиметаболиты: произв. фторпиримидинов n Механизм действия: 2. Фтор-УТФ – встраивается в РНК => нарушение процессинга и трансляции. 3. Фтордезокси-УТФ – встраивается в ДНК => нарушение репликации и функции ДНК. n Наиболее активен в периоде S.
Противоопухолевые средства, антиметаболиты: произв. фторпиримидинов n Механизм действия: 2. Фтор-УТФ – встраивается в РНК => нарушение процессинга и трансляции. 3. Фтордезокси-УТФ – встраивается в ДНК => нарушение репликации и функции ДНК. n Наиболее активен в периоде S.
 Торговые названия препаратов
Торговые названия препаратов
 Противоопухолевые средства, нарушающие митоз n Механизм действия: связывание с микротрубочками => их полимеризация => нарушение работы митотического веретена => препятствие делению клетки. n Наиболее активен в митозе.
Противоопухолевые средства, нарушающие митоз n Механизм действия: связывание с микротрубочками => их полимеризация => нарушение работы митотического веретена => препятствие делению клетки. n Наиболее активен в митозе.
 Торговые названия препаратов
Торговые названия препаратов
 Противоопухолевые антибиотики: n Механизм действия: 1. Встраивание в ДНК => нарушение репликации и функций ДНК. 2. Ингибирование РНК-полимеразы => подавление транскрипции. 3. Ингибирование топоизомеразы II => разрыв цепи ДНК.
Противоопухолевые антибиотики: n Механизм действия: 1. Встраивание в ДНК => нарушение репликации и функций ДНК. 2. Ингибирование РНК-полимеразы => подавление транскрипции. 3. Ингибирование топоизомеразы II => разрыв цепи ДНК.
 Торговые названия препаратов
Торговые названия препаратов
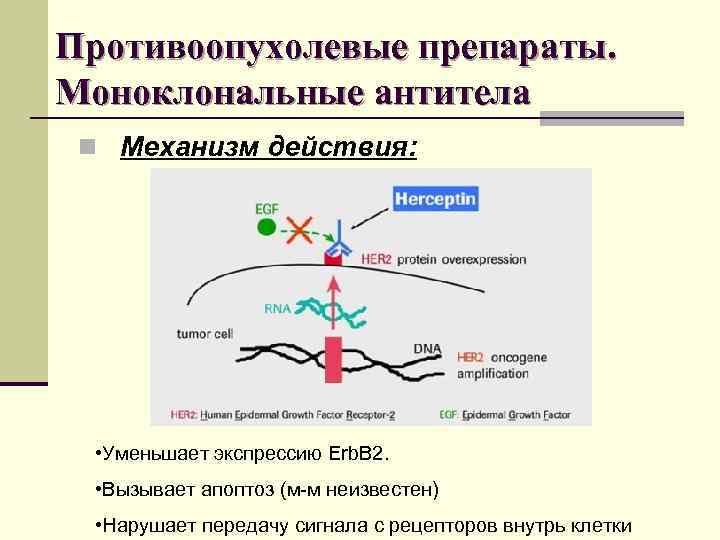 Противоопухолевые препараты. Моноклональные антитела n Механизм действия: • Уменьшает экспрессию Erb. B 2. • Вызывает апоптоз (м-м неизвестен) • Нарушает передачу сигнала с рецепторов внутрь клетки
Противоопухолевые препараты. Моноклональные антитела n Механизм действия: • Уменьшает экспрессию Erb. B 2. • Вызывает апоптоз (м-м неизвестен) • Нарушает передачу сигнала с рецепторов внутрь клетки
 Торговые названия препаратов
Торговые названия препаратов
 Предоперационная (неоадъювантная) химиотерапия n Показана при аденокарциноме. n При аденокарциноме нижнегрудного отдела пищевода или пищеводно-желудочного перехода наиболее оправдано проведение периоперационной химиотерапии: 2‑ 3 курса химиотерапии назначаются до операции, а 3‑ 4 курса – после нее. n При выявлении гиперэкспрессии HER 2 neu в режимы терапии включается трастузумаб в стандартных дозах. n При плоскоклеточном раке эффективность минимальна.
Предоперационная (неоадъювантная) химиотерапия n Показана при аденокарциноме. n При аденокарциноме нижнегрудного отдела пищевода или пищеводно-желудочного перехода наиболее оправдано проведение периоперационной химиотерапии: 2‑ 3 курса химиотерапии назначаются до операции, а 3‑ 4 курса – после нее. n При выявлении гиперэкспрессии HER 2 neu в режимы терапии включается трастузумаб в стандартных дозах. n При плоскоклеточном раке эффективность минимальна.
 Послеоперационная (адъювантная) химиотерапия n При плоскоклеточном раке пищевода ее проведение не показано. n При аденокарциноме нижнегрудного отдела пищевода или пищеводно-желудочного перехода послеоперационная химиотерапия показана, если она проводилась и предоперационно. n Адъювантная химиотерапия в самостоятельном виде при аденокарциноме пищевода в настоящее время не рекомендуется.
Послеоперационная (адъювантная) химиотерапия n При плоскоклеточном раке пищевода ее проведение не показано. n При аденокарциноме нижнегрудного отдела пищевода или пищеводно-желудочного перехода послеоперационная химиотерапия показана, если она проводилась и предоперационно. n Адъювантная химиотерапия в самостоятельном виде при аденокарциноме пищевода в настоящее время не рекомендуется.
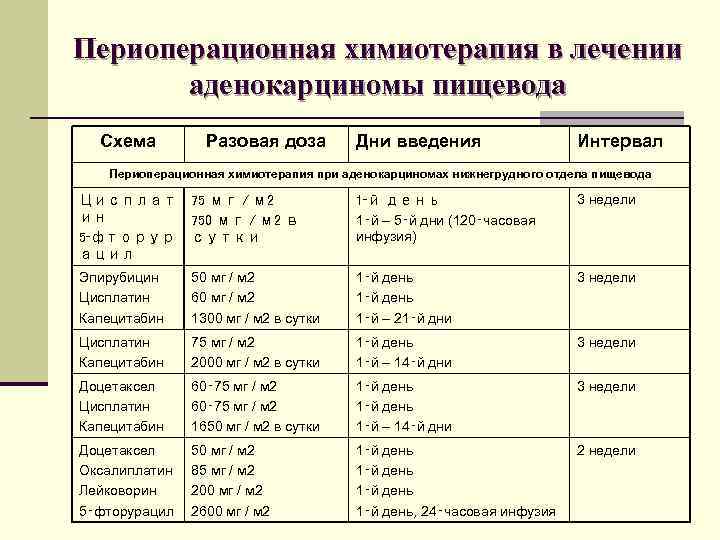 Периоперационная химиотерапия в лечении аденокарциномы пищевода Схема Разовая доза Дни введения Интервал Периоперационная химиотерапия при аденокарциномах нижнегрудного отдела пищевода Цисплат ин 5‑фторур ацил 75 мг / м 2 750 мг / м 2 в сутки 1‑й день 1‑й – 5‑й дни (120‑часовая инфузия) 3 недели Эпирубицин Цисплатин Капецитабин 50 мг / м 2 60 мг / м 2 1300 мг / м 2 в сутки 1‑й день 1‑й – 21‑й дни 3 недели Цисплатин Капецитабин 75 мг / м 2 2000 мг / м 2 в сутки 1‑й день 1‑й – 14‑й дни 3 недели Доцетаксел Цисплатин Капецитабин 60‑ 75 мг / м 2 1650 мг / м 2 в сутки 1‑й день 1‑й – 14‑й дни 3 недели Доцетаксел Оксалиплатин Лейковорин 5‑фторурацил 50 мг / м 2 85 мг / м 2 200 мг / м 2 2600 мг / м 2 1‑й день, 24‑часовая инфузия 2 недели
Периоперационная химиотерапия в лечении аденокарциномы пищевода Схема Разовая доза Дни введения Интервал Периоперационная химиотерапия при аденокарциномах нижнегрудного отдела пищевода Цисплат ин 5‑фторур ацил 75 мг / м 2 750 мг / м 2 в сутки 1‑й день 1‑й – 5‑й дни (120‑часовая инфузия) 3 недели Эпирубицин Цисплатин Капецитабин 50 мг / м 2 60 мг / м 2 1300 мг / м 2 в сутки 1‑й день 1‑й – 21‑й дни 3 недели Цисплатин Капецитабин 75 мг / м 2 2000 мг / м 2 в сутки 1‑й день 1‑й – 14‑й дни 3 недели Доцетаксел Цисплатин Капецитабин 60‑ 75 мг / м 2 1650 мг / м 2 в сутки 1‑й день 1‑й – 14‑й дни 3 недели Доцетаксел Оксалиплатин Лейковорин 5‑фторурацил 50 мг / м 2 85 мг / м 2 200 мг / м 2 2600 мг / м 2 1‑й день, 24‑часовая инфузия 2 недели
 Комбинированное лечение n Впервые предложено А. С. Мамонтовым в 1979 г. n Рекомендуется для лечения больных, у которых локализация опухоли в среднегрудном отделе пищевода
Комбинированное лечение n Впервые предложено А. С. Мамонтовым в 1979 г. n Рекомендуется для лечения больных, у которых локализация опухоли в среднегрудном отделе пищевода
 Одновременная химиолучевая терапия. Предоперационная химиолучевая терапия n Лечение: РОД 1, 8‑ 2 Гр, СОД – до 44‑ 45 Гр. , химиотерапия на основе цисплатина или карбоплатина. n При выраженной дисфагии перед началом облучения – эндоскопическую электрореканализацию / аргонно-плазменную реканализацию пищевода или пункционную гастростомию. n Хирургическое вмешательство обычно производится через 6‑ 8 недель после завершения химиолучевой терапии. n Оптимальным режимом химиолучевой терапии представляется еженедельное введение паклитаксела и карбоплатина на фоне 5 недель лучевой терапии.
Одновременная химиолучевая терапия. Предоперационная химиолучевая терапия n Лечение: РОД 1, 8‑ 2 Гр, СОД – до 44‑ 45 Гр. , химиотерапия на основе цисплатина или карбоплатина. n При выраженной дисфагии перед началом облучения – эндоскопическую электрореканализацию / аргонно-плазменную реканализацию пищевода или пункционную гастростомию. n Хирургическое вмешательство обычно производится через 6‑ 8 недель после завершения химиолучевой терапии. n Оптимальным режимом химиолучевой терапии представляется еженедельное введение паклитаксела и карбоплатина на фоне 5 недель лучевой терапии.
 Комбинированные схемы в химиолучевом лечении В исследовании эффективности комбинированного метода лечения по сравнению с хирургическим методом отмечается увеличение двухлетней общей выживаемости с 63, 2% до 87% (p<0, 05). Также в этом эксперименте выявлена высокая эффективность химиотерапии по схеме гентамицин/цисплатин как в комбинации с хирургическим методом, так и без него (38, 9%). (6) В эксперименте Юсупова А. М. и соавт. на фоне проводимой химиотерапии (доцетаксел+цисплатин) были изменены критерии операбельности опухоли. В связи с этим было рекомендовано комбинированное лечение (операция + лучевая терапия), которое позволило снизить частоту местных рецидивов и повысить трехлетнюю выживаемость больных. (7)
Комбинированные схемы в химиолучевом лечении В исследовании эффективности комбинированного метода лечения по сравнению с хирургическим методом отмечается увеличение двухлетней общей выживаемости с 63, 2% до 87% (p<0, 05). Также в этом эксперименте выявлена высокая эффективность химиотерапии по схеме гентамицин/цисплатин как в комбинации с хирургическим методом, так и без него (38, 9%). (6) В эксперименте Юсупова А. М. и соавт. на фоне проводимой химиотерапии (доцетаксел+цисплатин) были изменены критерии операбельности опухоли. В связи с этим было рекомендовано комбинированное лечение (операция + лучевая терапия), которое позволило снизить частоту местных рецидивов и повысить трехлетнюю выживаемость больных. (7)
 Послеоперационная химиолучевая терапия n Послеоперационная химиолучевая терапия может быть проведена пациентам в удовлетворительном состоянии при наличии микро- или макроскопической резидуальной опухоли (после R 1 - или R 2‑резекции). n Режимы и дозы аналогичные предоперационным. n Эффетивность пред- и послеоперационной лучевой и химиотерапии в своем исследовании отмечают А. В. Тобохов и соавт. (8) n В другом эксперименте (Е. Ш. Абзалбек) отмечается увеличение выживаемости в отдаленном периоде при проведении мультимодальной терапии больным с местнораспространенными формами рака. (9)
Послеоперационная химиолучевая терапия n Послеоперационная химиолучевая терапия может быть проведена пациентам в удовлетворительном состоянии при наличии микро- или макроскопической резидуальной опухоли (после R 1 - или R 2‑резекции). n Режимы и дозы аналогичные предоперационным. n Эффетивность пред- и послеоперационной лучевой и химиотерапии в своем исследовании отмечают А. В. Тобохов и соавт. (8) n В другом эксперименте (Е. Ш. Абзалбек) отмечается увеличение выживаемости в отдаленном периоде при проведении мультимодальной терапии больным с местнораспространенными формами рака. (9)
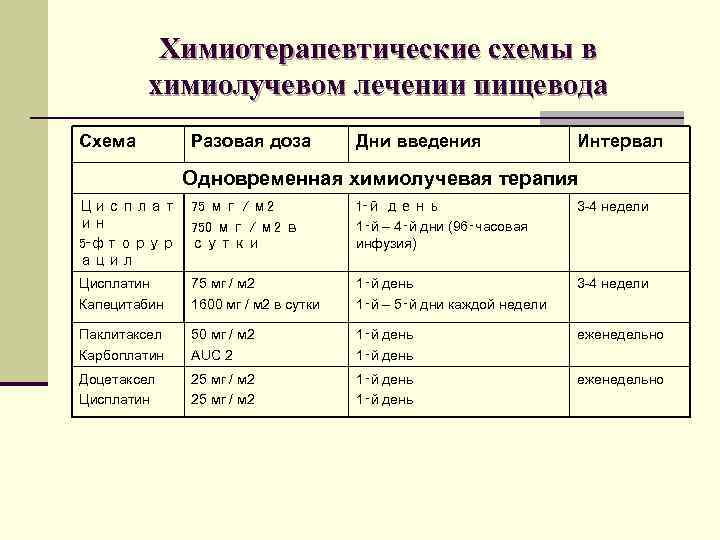 Химиотерапевтические схемы в химиолучевом лечении пищевода Схема Разовая доза Дни введения Интервал Одновременная химиолучевая терапия Цисплат ин 5‑фторур ацил 75 мг / м 2 750 мг / м 2 в сутки 1‑й день 1‑й – 4‑й дни (96‑часовая инфузия) 3 -4 недели Цисплатин Капецитабин 75 мг / м 2 1600 мг / м 2 в сутки 1‑й день 1‑й – 5‑й дни каждой недели 3 -4 недели Паклитаксел Карбоплатин 50 мг / м 2 AUC 2 1‑й день еженедельно Доцетаксел Цисплатин 25 мг / м 2 1‑й день еженедельно
Химиотерапевтические схемы в химиолучевом лечении пищевода Схема Разовая доза Дни введения Интервал Одновременная химиолучевая терапия Цисплат ин 5‑фторур ацил 75 мг / м 2 750 мг / м 2 в сутки 1‑й день 1‑й – 4‑й дни (96‑часовая инфузия) 3 -4 недели Цисплатин Капецитабин 75 мг / м 2 1600 мг / м 2 в сутки 1‑й день 1‑й – 5‑й дни каждой недели 3 -4 недели Паклитаксел Карбоплатин 50 мг / м 2 AUC 2 1‑й день еженедельно Доцетаксел Цисплатин 25 мг / м 2 1‑й день еженедельно
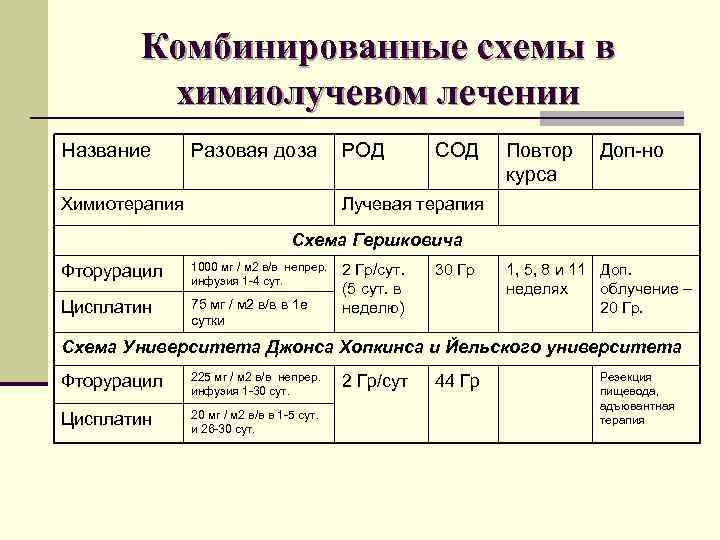 Комбинированные схемы в химиолучевом лечении Название Разовая доза Химиотерапия РОД СОД Повтор курса Доп-но Лучевая терапия Схема Гершковича Фторурацил 1000 мг / м 2 в/в непрер. инфузия 1 -4 сут. Цисплатин 75 мг / м 2 в/в в 1 е сутки 2 Гр/сут. (5 сут. в неделю) 30 Гр 1, 5, 8 и 11 Доп. неделях облучение – 20 Гр. Схема Университета Джонса Хопкинса и Йельского университета Фторурацил 225 мг / м 2 в/в непрер. инфузия 1 -30 сут. Цисплатин 20 мг / м 2 в/в в 1 -5 сут. и 26 -30 сут. 2 Гр/сут 44 Гр Резекция пищевода, адъювантная терапия
Комбинированные схемы в химиолучевом лечении Название Разовая доза Химиотерапия РОД СОД Повтор курса Доп-но Лучевая терапия Схема Гершковича Фторурацил 1000 мг / м 2 в/в непрер. инфузия 1 -4 сут. Цисплатин 75 мг / м 2 в/в в 1 е сутки 2 Гр/сут. (5 сут. в неделю) 30 Гр 1, 5, 8 и 11 Доп. неделях облучение – 20 Гр. Схема Университета Джонса Хопкинса и Йельского университета Фторурацил 225 мг / м 2 в/в непрер. инфузия 1 -30 сут. Цисплатин 20 мг / м 2 в/в в 1 -5 сут. и 26 -30 сут. 2 Гр/сут 44 Гр Резекция пищевода, адъювантная терапия
 Самостоятельная химиолучевая терапия n Лечение: РОД = 1, 8‑ 2 Гр, СОД – до 50‑ 55 Гр. , химиотерапия на основе цисплатина и 5‑фторурацила. n При наличии выраженной дисфагии перед началом облучения производят эндоскопическую электрореканализацию пищевода или пункционную микрогастростомию. n Выбор между самостоятельной химиолучевой терапией или с хирургическим лечением (с предоперационной химиолучевой терапией или без нее) зависит от локализации первичной опухоли, функционального состояния больного и опыта хирурга.
Самостоятельная химиолучевая терапия n Лечение: РОД = 1, 8‑ 2 Гр, СОД – до 50‑ 55 Гр. , химиотерапия на основе цисплатина и 5‑фторурацила. n При наличии выраженной дисфагии перед началом облучения производят эндоскопическую электрореканализацию пищевода или пункционную микрогастростомию. n Выбор между самостоятельной химиолучевой терапией или с хирургическим лечением (с предоперационной химиолучевой терапией или без нее) зависит от локализации первичной опухоли, функционального состояния больного и опыта хирурга.
 НЕРЕЗЕКТАБЕЛЬНЫЙ МЕСТНОРАСПРОСТРАНЕННЫЙ РАК ПИЩЕВОДА n Стадия III: Т 4 - единичные или множественные метастазы в регионарные лимфоузлы средостения n Основной метод лечения – самостоятельная химиолучевая терапия (режим как при операбельных опухолях). n При злокачественной пищеводной фистуле (пищеводно-медиастинальные, пищеводнолегочные и пищеводно-бронхиальные свищи), делающей невозможным проведение химиолучевой терапии, допустимо выполнение комбинированных операций.
НЕРЕЗЕКТАБЕЛЬНЫЙ МЕСТНОРАСПРОСТРАНЕННЫЙ РАК ПИЩЕВОДА n Стадия III: Т 4 - единичные или множественные метастазы в регионарные лимфоузлы средостения n Основной метод лечения – самостоятельная химиолучевая терапия (режим как при операбельных опухолях). n При злокачественной пищеводной фистуле (пищеводно-медиастинальные, пищеводнолегочные и пищеводно-бронхиальные свищи), делающей невозможным проведение химиолучевой терапии, допустимо выполнение комбинированных операций.
 IV стадия Основными задачами лечения пациентов с метастатическим раком пищевода: 1. устранение болезненных симптомов, 2. увеличение продолжительности жизни. Проведение химиотерапии рекомендуется: n пациентам в удовлетворительном состоянии (ECOG PS 0‑ 2) n отсутствием выраженной дисфагии (III‑IV) , затрудняющей адекватное питание пациента. В последнем случае на первом этапе показано восстановление проходимости пищевода (стентирование, реканализация). Наиболее активными препаратами при обоих гистологических вариантах являются цисплатин, фторпиримидины, таксаны. Кроме того, при аденокарциномах также эффективны оксалиплатин, иринотекан, трастузумаб (при гиперэкспрессии HER-2 neu).
IV стадия Основными задачами лечения пациентов с метастатическим раком пищевода: 1. устранение болезненных симптомов, 2. увеличение продолжительности жизни. Проведение химиотерапии рекомендуется: n пациентам в удовлетворительном состоянии (ECOG PS 0‑ 2) n отсутствием выраженной дисфагии (III‑IV) , затрудняющей адекватное питание пациента. В последнем случае на первом этапе показано восстановление проходимости пищевода (стентирование, реканализация). Наиболее активными препаратами при обоих гистологических вариантах являются цисплатин, фторпиримидины, таксаны. Кроме того, при аденокарциномах также эффективны оксалиплатин, иринотекан, трастузумаб (при гиперэкспрессии HER-2 neu).
 IV стадия n При плоскоклеточных раках: комбинация цисплатина с инфузией 5‑фторурацила/капецитабином. n Применение таксанов возможно в виде как двухкомпонентных схем с цисплатином, так и трехкомпонентных – с цисплатином и фторпиримидинами. n Оптимальная продолжительность первой линии химиотерапии неизвестна. Не существует стандартной второй линии терапии. n Обычно проводится 4 курса в случае стабилизации и 6 курсов – при достижении объективного ответа.
IV стадия n При плоскоклеточных раках: комбинация цисплатина с инфузией 5‑фторурацила/капецитабином. n Применение таксанов возможно в виде как двухкомпонентных схем с цисплатином, так и трехкомпонентных – с цисплатином и фторпиримидинами. n Оптимальная продолжительность первой линии химиотерапии неизвестна. Не существует стандартной второй линии терапии. n Обычно проводится 4 курса в случае стабилизации и 6 курсов – при достижении объективного ответа.
 Паллиативное лечение Наиболее частым симптомом является дисфагия. Устранение ее достигается различными подходами: n эндоскопическими процедурами (баллонная дилатация, электро-, аргонно-плазменная или лазерная деструкция, фотодинамическая терапия), n дистанционной или брахитерапией, n постановкой внутрипросветных стентов. Эндоскопические процедуры дают быстрый, но кратковременный эффект и подходят в случаях, когда в ближайшее время будет начато эффективное лечение. Если излечение больного невозможно, то оптимально проведение брахитерапия, стентирования пищевода или дистанционной лучевой терапии. В случае развития пищеводно-бронхиальных или медиастинальных свищей постановка покрытых стентов позволяет купировать данные осложнения у 70‑ 100 % больных.
Паллиативное лечение Наиболее частым симптомом является дисфагия. Устранение ее достигается различными подходами: n эндоскопическими процедурами (баллонная дилатация, электро-, аргонно-плазменная или лазерная деструкция, фотодинамическая терапия), n дистанционной или брахитерапией, n постановкой внутрипросветных стентов. Эндоскопические процедуры дают быстрый, но кратковременный эффект и подходят в случаях, когда в ближайшее время будет начато эффективное лечение. Если излечение больного невозможно, то оптимально проведение брахитерапия, стентирования пищевода или дистанционной лучевой терапии. В случае развития пищеводно-бронхиальных или медиастинальных свищей постановка покрытых стентов позволяет купировать данные осложнения у 70‑ 100 % больных.
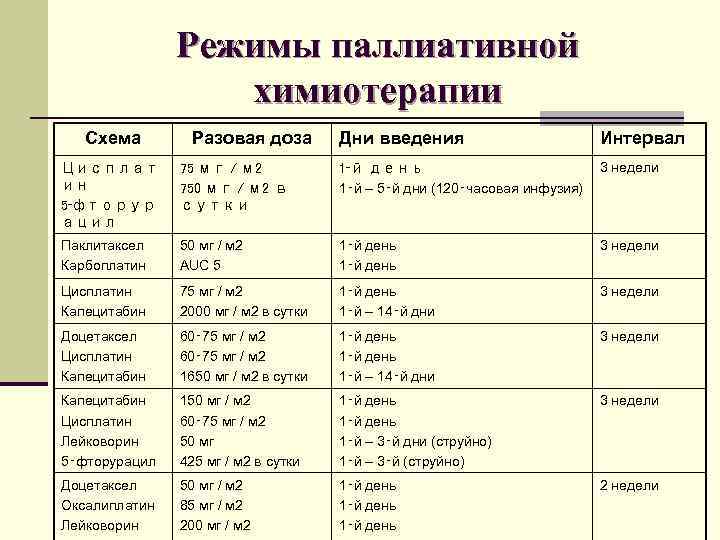 Режимы паллиативной химиотерапии Схема Разовая доза Дни введения Интервал Цисплат ин 5‑фторур ацил 75 мг / м 2 750 мг / м 2 в сутки 1‑й день 1‑й – 5‑й дни (120‑часовая инфузия) 3 недели Паклитаксел Карбоплатин 50 мг / м 2 AUC 5 1‑й день 3 недели Цисплатин Капецитабин 75 мг / м 2 2000 мг / м 2 в сутки 1‑й день 1‑й – 14‑й дни 3 недели Доцетаксел Цисплатин Капецитабин 60‑ 75 мг / м 2 1650 мг / м 2 в сутки 1‑й день 1‑й – 14‑й дни 3 недели Капецитабин Цисплатин Лейковорин 5‑фторурацил 150 мг / м 2 60‑ 75 мг / м 2 50 мг 425 мг / м 2 в сутки 1‑й день 1‑й – 3‑й дни (струйно) 1‑й – 3‑й (струйно) 3 недели Доцетаксел Оксалиплатин Лейковорин 50 мг / м 2 85 мг / м 2 200 мг / м 2 1‑й день 2 недели
Режимы паллиативной химиотерапии Схема Разовая доза Дни введения Интервал Цисплат ин 5‑фторур ацил 75 мг / м 2 750 мг / м 2 в сутки 1‑й день 1‑й – 5‑й дни (120‑часовая инфузия) 3 недели Паклитаксел Карбоплатин 50 мг / м 2 AUC 5 1‑й день 3 недели Цисплатин Капецитабин 75 мг / м 2 2000 мг / м 2 в сутки 1‑й день 1‑й – 14‑й дни 3 недели Доцетаксел Цисплатин Капецитабин 60‑ 75 мг / м 2 1650 мг / м 2 в сутки 1‑й день 1‑й – 14‑й дни 3 недели Капецитабин Цисплатин Лейковорин 5‑фторурацил 150 мг / м 2 60‑ 75 мг / м 2 50 мг 425 мг / м 2 в сутки 1‑й день 1‑й – 3‑й дни (струйно) 1‑й – 3‑й (струйно) 3 недели Доцетаксел Оксалиплатин Лейковорин 50 мг / м 2 85 мг / м 2 200 мг / м 2 1‑й день 2 недели
 Спасибо за внимание!
Спасибо за внимание!
 Список литературы: 1. 2. 3. 4. 5. 6. 7. 8. 9. 10. 11. Практические рекомендации по лечению злокачественных опухолей Российского общества клинической онкологии. Версия 2015 Онкология: Учебник для студентов медицинских вузов. – 2 -е изд. ; испр. и доп. – М. : ООО «Медицинское информационное агенство» , 2006. – 488 с. : ил. «Химиотерапия злокачественной новообразований» Пер. с англ. – М. , «Практика» , 2009. – 455 с. Приказ Минздрава РБ от 11. 03. 2012 № 258 утверждены «Алгоритмы диагностики и лечения злокачественных новообразований» . Ганцев Ш. Х. Левченко Е. В. и соавт. Опыт использования внутрипросветной брахитерапии в комплексном лечении рака пищевода. Ж. «Злокачественные новообразования» XVI Российский онкологический конгресс. Рудык Ю. В. И соавт. Эффективность комбинированного лечения больных раком пищевода с применением неоадъювантной химиотерапей. Сибирский онкологический журнал. 2013. № 4 (58). Юсупов А. М. , Арыбжанов Д. Т. , Колдыбаева Ш. А. Предоперационная регионарная химиотерапия в комплексном лечении больных раком пищевода. Тюменский медицинский журнал № 3 -4, 2011. Тобохов А. В. , Слепцов К. Н. , Неустроев П. А. , Николаев В. Н. Комплексный подход в лечении рака пищевода. Бюллетень ВСНЦ СО РАМН, 2012, № 4 (86), Часть 1. Е. Ш. Абзалбек. Отдаленные результаты мультимодальной терапии рака пищевода. Вестник КРСУ. 2013. Том 13. № 12. Борисов В. А. , Шинкарев С. А. , Ильин Н. В. , Флоровская Н. А. Лучевая терапия рака пищевода на основе применения электромагнитной гипертермии. Медицинская радиология и радиационная безопасность, 2010, Том 55, № 5. Луд А. Н. Значение молекулярно-биологических маркеров при раке желудка и пищевода. Российский биотерапевтический журнал. № 3. Том 6. 2007
Список литературы: 1. 2. 3. 4. 5. 6. 7. 8. 9. 10. 11. Практические рекомендации по лечению злокачественных опухолей Российского общества клинической онкологии. Версия 2015 Онкология: Учебник для студентов медицинских вузов. – 2 -е изд. ; испр. и доп. – М. : ООО «Медицинское информационное агенство» , 2006. – 488 с. : ил. «Химиотерапия злокачественной новообразований» Пер. с англ. – М. , «Практика» , 2009. – 455 с. Приказ Минздрава РБ от 11. 03. 2012 № 258 утверждены «Алгоритмы диагностики и лечения злокачественных новообразований» . Ганцев Ш. Х. Левченко Е. В. и соавт. Опыт использования внутрипросветной брахитерапии в комплексном лечении рака пищевода. Ж. «Злокачественные новообразования» XVI Российский онкологический конгресс. Рудык Ю. В. И соавт. Эффективность комбинированного лечения больных раком пищевода с применением неоадъювантной химиотерапей. Сибирский онкологический журнал. 2013. № 4 (58). Юсупов А. М. , Арыбжанов Д. Т. , Колдыбаева Ш. А. Предоперационная регионарная химиотерапия в комплексном лечении больных раком пищевода. Тюменский медицинский журнал № 3 -4, 2011. Тобохов А. В. , Слепцов К. Н. , Неустроев П. А. , Николаев В. Н. Комплексный подход в лечении рака пищевода. Бюллетень ВСНЦ СО РАМН, 2012, № 4 (86), Часть 1. Е. Ш. Абзалбек. Отдаленные результаты мультимодальной терапии рака пищевода. Вестник КРСУ. 2013. Том 13. № 12. Борисов В. А. , Шинкарев С. А. , Ильин Н. В. , Флоровская Н. А. Лучевая терапия рака пищевода на основе применения электромагнитной гипертермии. Медицинская радиология и радиационная безопасность, 2010, Том 55, № 5. Луд А. Н. Значение молекулярно-биологических маркеров при раке желудка и пищевода. Российский биотерапевтический журнал. № 3. Том 6. 2007


