f1bc01ae5260dcac43ab09cabdade39e.ppt
- Количество слайдов: 62

Le Rein : Un organe multifunction 1. L’équilibre hydrominérale et acido-basique. osmolarité et volume des fluides du corps balance des electrolytes balance acide-base 2. Excréteur produits du métabolisme: Déchets azotés: urée, créatinine, acide urique (métabolites pouvant être toxiques s’ils s’accumulent) substances exogènes (pesticides, médicaments, produits chimiques etc. ) 3. Maintien de la Pression sanguine Soit par sécrétion d’hormones : la rénine va provoquer une augmentation du taux d’angiotensine, Soit par le contrôle de la natrémie (sodium dans le plasma) et de la volémie (volume sanguin). 4. Fonction endocrine -erythropoiétine, EPO, Stimule la synthèse des globules rouges dans la moelle osseuse -1, 25 -dihydroxy vitamin D 3 (vitamin D active ) -rénine -prostaglandine, 5 - Fonction métabolique les reins sont les seuls organes (avec le foie), capables de néoglucogenèse. Dans le cas d’un jeune prolongé, le rein peut assurer jusqu’à 50% de la néoglucogenèse.

Circulation sanguine Pour un organe d’environ 150 g

Circulation sanguine
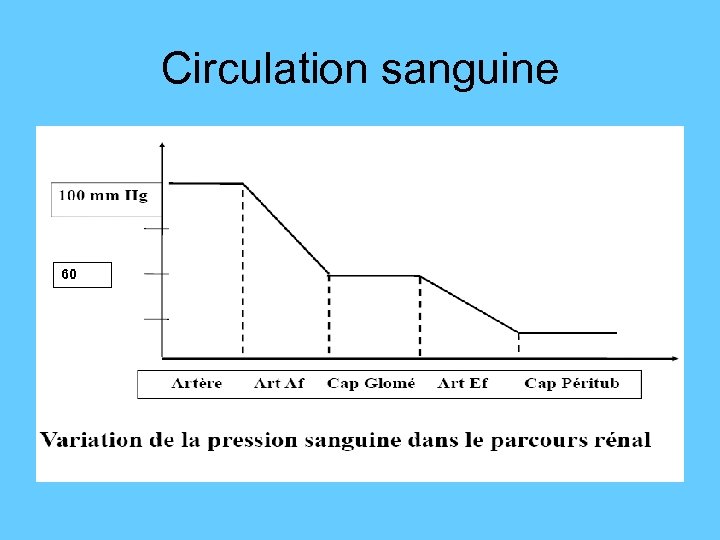
Circulation sanguine 60

Circulation sanguine 60 mm. Hg

Methodes d’étude in Vivo

Mesure de la fonction rénale : La clairance rénale est une mesure physiologique évaluant l'excrétion d'une substances filtrées, réabsorbées et/ou sécrétées par le rein. • Elle se définit comme étant le volume de plasma virtuel épuré par unité de temps par le rein rapporté a une surface corporelle (1, 73 m 2 chez l'Homme). • Plus une clairance est élevée, plus le pouvoir d'épuration pour cette substance est élevé.


Notion de clairance: • Le concept de clairance rénale repose sur la loi de conservation de masse à savoir que: ** la quantité d’une substance filtrée par le rein [P] x DFG , • où [P] = la concentration plasmatique de cette substance • où DFG = la filtration glomérulaire ** est égale à la quantité éliminée dans l’urine [U] x V, • où [U] = la concentration urinaire de la substance en question • où V = le débit urinaire
![Notion de clairance: • [P] x DFG = [U] x V la filtration glomérulaire Notion de clairance: • [P] x DFG = [U] x V la filtration glomérulaire](https://present5.com/presentation/f1bc01ae5260dcac43ab09cabdade39e/image-10.jpg)
Notion de clairance: • [P] x DFG = [U] x V la filtration glomérulaire peut être calculée très simplement DFG = [U] x V [P] • La clairance d’une substance librement filtrée et complètement éliminée par le rein, est égale au débit de filtration glomérulaire.

Notion de marqueurs ou traceurs: • La filtration glomérulaire peut être mesurée par la clairance d’un marqueur (endogène ou exogène) à condition que celui-ci remplisse les conditions suivantes : -Elimination exclusivement par filtration glomérulaire -Aucune sécrétion tubulaire -Aucune réabsorption tubulaire -Aucune excrétion extra-rénale -Absence de liaison avec des protéines plasmatiques -Aucune fixation dans les tissus -Absence de réaction métabolique -Absence de toxicité
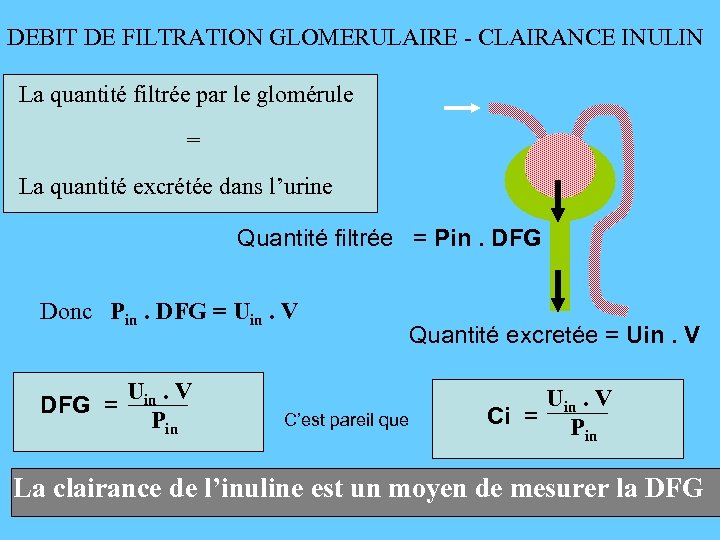
DEBIT DE FILTRATION GLOMERULAIRE - CLAIRANCE INULIN La quantité filtrée par le glomérule = La quantité excrétée dans l’urine Quantité filtrée = Pin. DFG Donc Pin. DFG = Uin. V DFG = Pin Quantité excretée = Uin. V C’est pareil que Uin. V Ci = P in La clairance de l’inuline est un moyen de mesurer la DFG

Notion de marqueurs ou traceurs: Inuline ou créatinine pour DFG • L’inuline est un polysaccharide végétale filtré, mais ni réabsorbé, ni secrété, ni métabolisé, et que l’on peut donc injecter dans l’organisme pour mesurer le débit de filtration glomérulaire. • La créatinine, produit de dégradation des protéines musculaires, est normalement présente dans le plasma, et présente une clairance proche de celle de l’inuline largement utilisée, en pratique clinique, pour évaluer la filtration glomérulaire.

90
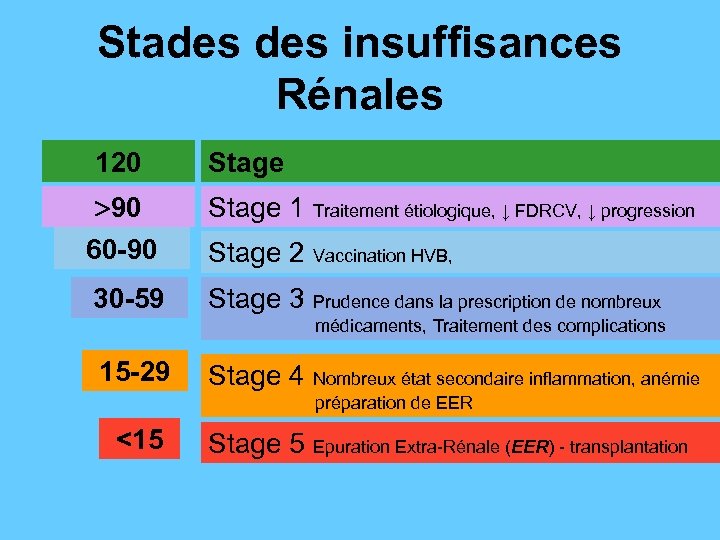
Stades insuffisances Rénales 120 Stage 90 60 -90 Stage 1 Traitement étiologique, ↓ FDRCV, ↓ progression 30 -59 Stage 3 Prudence dans la prescription de nombreux Stage 2 Vaccination HVB, médicaments, Traitement des complications 15 -29 Stage 4 Nombreux état secondaire inflammation, anémie préparation de EER <15 Stage 5 Epuration Extra-Rénale (EER) - transplantation
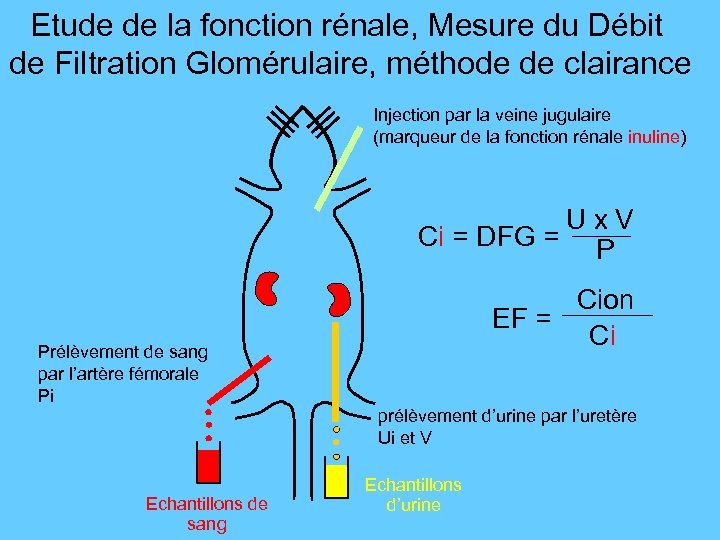
Etude de la fonction rénale, Mesure du Débit de Filtration Glomérulaire, méthode de clairance Injection par la veine jugulaire (marqueur de la fonction rénale inuline) U x V Ci = DFG = P Cion EF = Ci Prélèvement de sang par l’artère fémorale Pi prélèvement d’urine par l’uretère Ui et V Echantillons de sang Echantillons d’urine

L’essor des micro-techniques La méthode de clairance totale ne renseigne pas sur les zones du néphron impliquées dans le processus de transport. Le développement de microtechniques analytiques (Richards et col). a permis l’étude expérimentale (en laboratoire de recherche) des fonctions tubulaires qui caractérisent les principaux segments du néphron. L'utilisation systématique de ces méthodes complémentaires a permis de constituer entre les années 1930 et 1950 un corpus considérable de données expérimentales dont l'ouvrage de référence, « The kidney, structure and function in health and diseas publié par Homer Smith en 1951, représente une synthèse magistrale. (La bible des Néphrologues) (la bibliographie comporte 2300 références !).
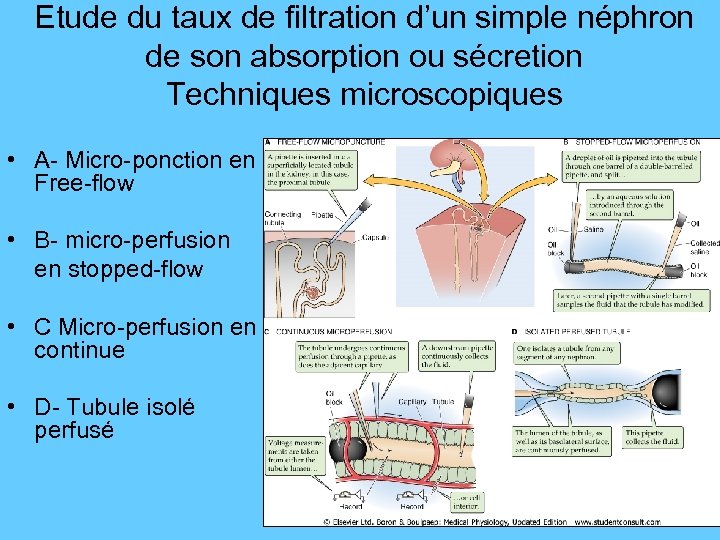
Etude du taux de filtration d’un simple néphron de son absorption ou sécretion Techniques microscopiques • A- Micro-ponction en Free-flow • B- micro-perfusion en stopped-flow • C Micro-perfusion en continue • D- Tubule isolé perfusé
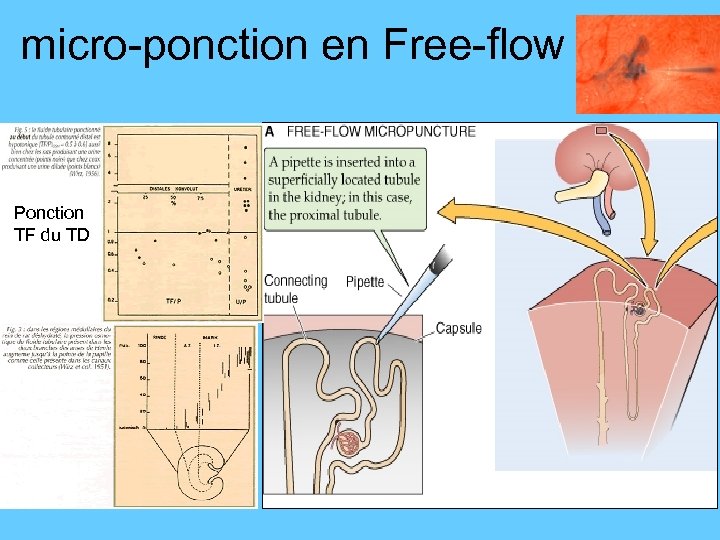
micro-ponction en Free-flow Ponction TF du TD
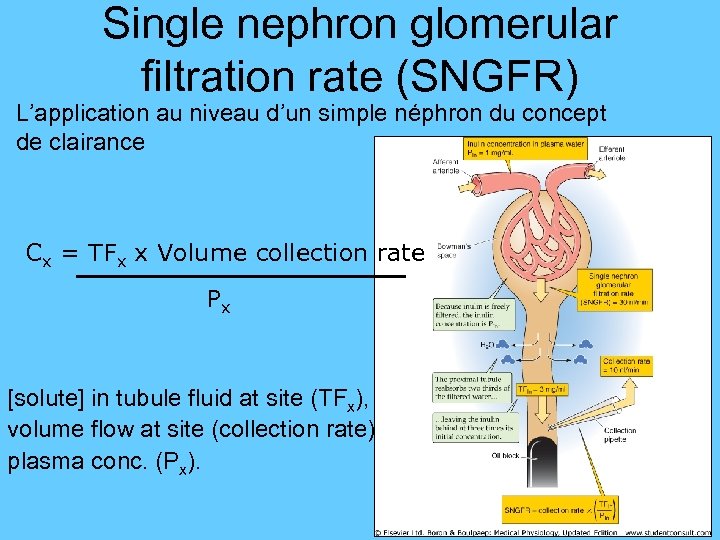
Single nephron glomerular filtration rate (SNGFR) L’application au niveau d’un simple néphron du concept de clairance Cx = TFx x Volume collection rate Px [solute] in tubule fluid at site (TFx), volume flow at site (collection rate) plasma conc. (Px).
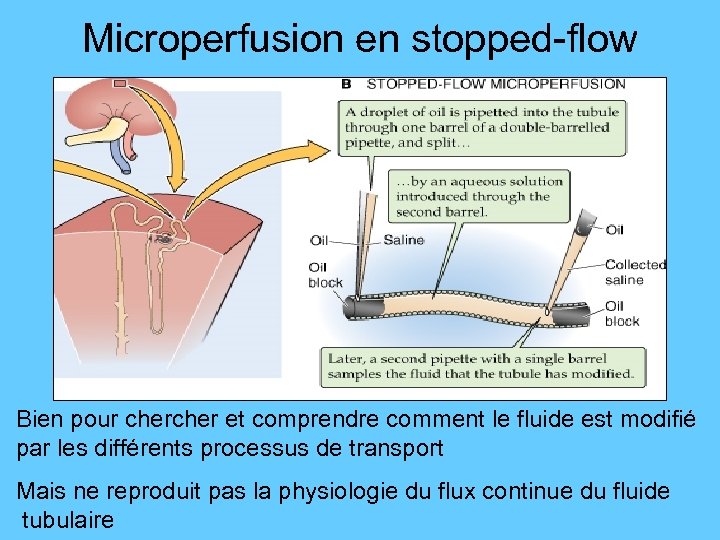
Microperfusion en stopped-flow Bien pour cher et comprendre comment le fluide est modifié par les différents processus de transport Mais ne reproduit pas la physiologie du flux continue du fluide tubulaire
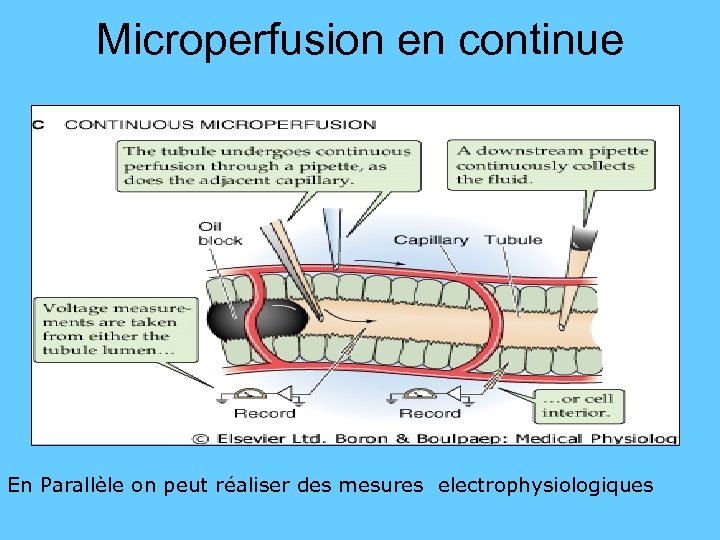
Microperfusion en continue En Parallèle on peut réaliser des mesures electrophysiologiques
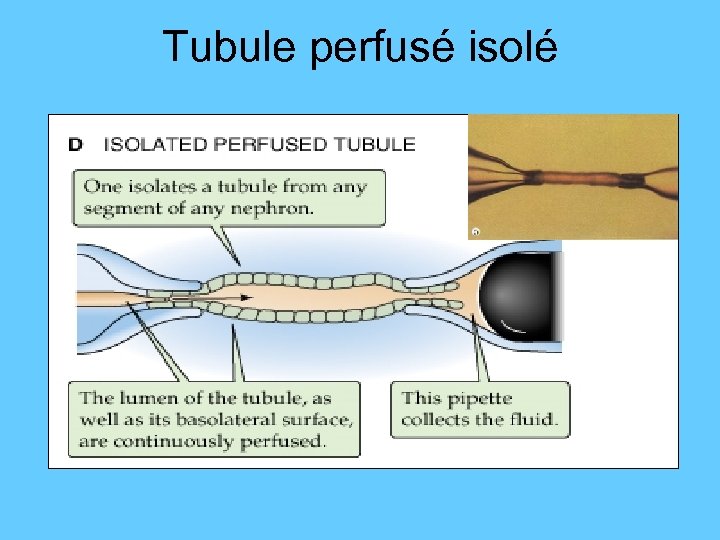
Tubule perfusé isolé

Physiologie Rénale et Méthode In vitro

Modèles IN VITRO (évaluation de la néphrotoxicité) • Devant la complexité du rein (hétérogénéité structurale et fonctionnelle), il sera difficile in vivo, voir impossible, de cerner les mécanismes cellulaires et biochimiques impliqués dans les pathologies et les toxicités induites par les médicaments • Il sera possible in vivo de détecter une insuffisance rénale ou une néphrotoxicité induite par un dosage de la GFR ou RPF, mais il sera impossible d’en étudier les mécanismes responsables
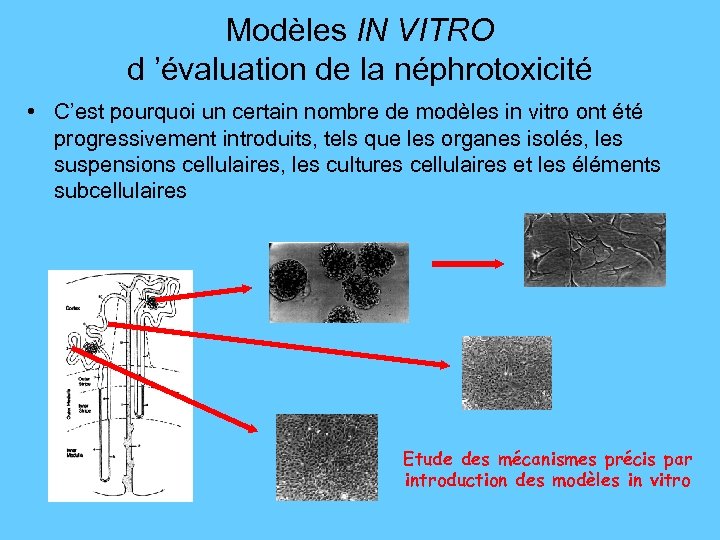
Modèles IN VITRO d ’évaluation de la néphrotoxicité • C’est pourquoi un certain nombre de modèles in vitro ont été progressivement introduits, tels que les organes isolés, les suspensions cellulaires, les cultures cellulaires et les éléments subcellulaires Etude des mécanismes précis par introduction des modèles in vitro

Méthodes IN VITRO d’évaluation de la cible rénale • Il est aujourd’hui admis que la contribution des tests in vitro peut être essentielle: • dans le screenning de molécules dans la phase initiale de leur découverte • dans l’identification des mécanismes impliqués dans la toxicité • dans l’identification des protéines impliquées • Génome, Transcriptome, Protéosome

Les cultures cellulaires Définition: Les cultures cellulaires, selon la définition du comité de terminologie de l’association américaine de culture de cellules, correspondent au maintien en dehors de l’organisme de cellules non-organisées en tissus mais capables de se diviser et d’exprimer in vitro des métabolismes spécifiques. “Maintenir in vitro des cellules possédant tout ou une partie des caractéristiques qu’elles manifestent in vivo et pouvant aboutir dans certaines conditions de culture à une véritable organisation tissulaire”.

Culture Primaire A partir de cellules isolées mécaniquement Avantages: Technique rapide et permet d’obtenir beaucoup de cellules. Pas d’utilisation enzymatique Tranche de cortex ou medullaire Broyage Tamisage Re-suspenssion du culot, puis mis en culture Inconvénients: Utilisable sur très peu d’espèce, mélange de type cellulaire
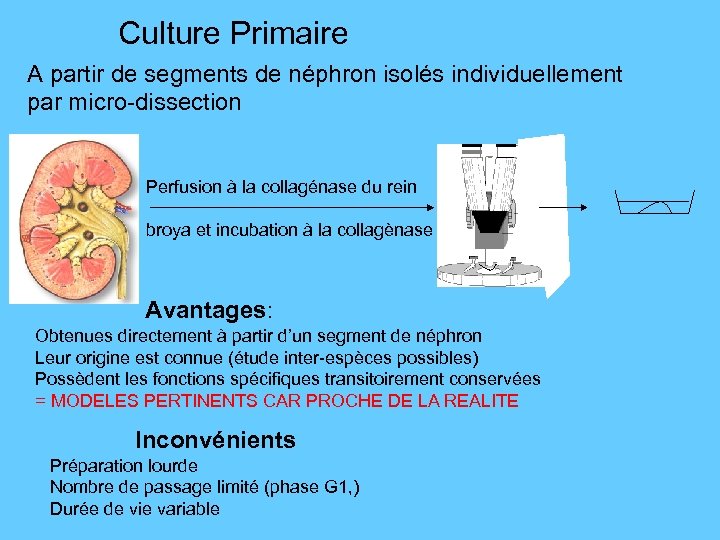
Culture Primaire A partir de segments de néphron isolés individuellement par micro-dissection Perfusion à la collagénase du rein broya et incubation à la collagènase Avantages: Obtenues directement à partir d’un segment de néphron Leur origine est connue (étude inter-espèces possibles) Possèdent les fonctions spécifiques transitoirement conservées = MODELES PERTINENTS CAR PROCHE DE LA REALITE Inconvénients Préparation lourde Nombre de passage limité (phase G 1, ) Durée de vie variable
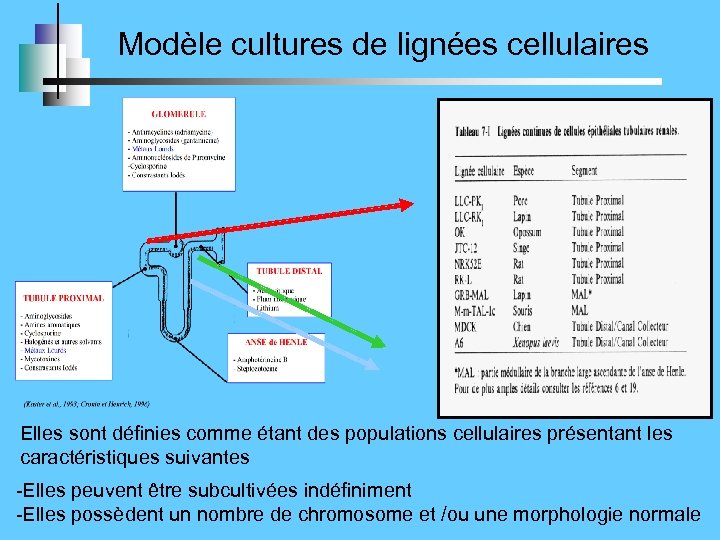
Modèle cultures de lignées cellulaires Elles sont définies comme étant des populations cellulaires présentant les caractéristiques suivantes -Elles peuvent être subcultivées indéfiniment -Elles possèdent un nombre de chromosome et /ou une morphologie normale
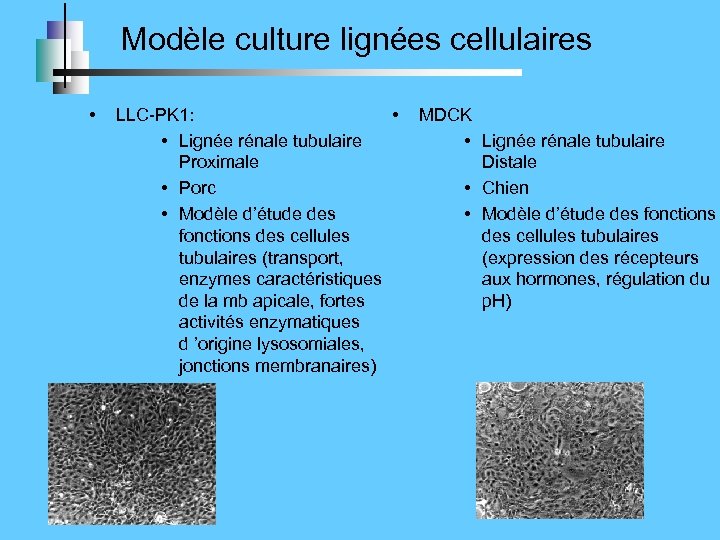
Modèle culture lignées cellulaires • • LLC-PK 1: • Lignée rénale tubulaire Proximale • Porc • Modèle d’étude des fonctions des cellules tubulaires (transport, enzymes caractéristiques de la mb apicale, fortes activités enzymatiques d ’origine lysosomiales, jonctions membranaires) MDCK • Lignée rénale tubulaire Distale • Chien • Modèle d’étude des fonctions des cellules tubulaires (expression des récepteurs aux hormones, régulation du p. H)

Réabsorption et Sécretion voie de transfert des solutés Etudes mouvements ioniques à travers le tissus isolé Méthode de la chambre de Ussing
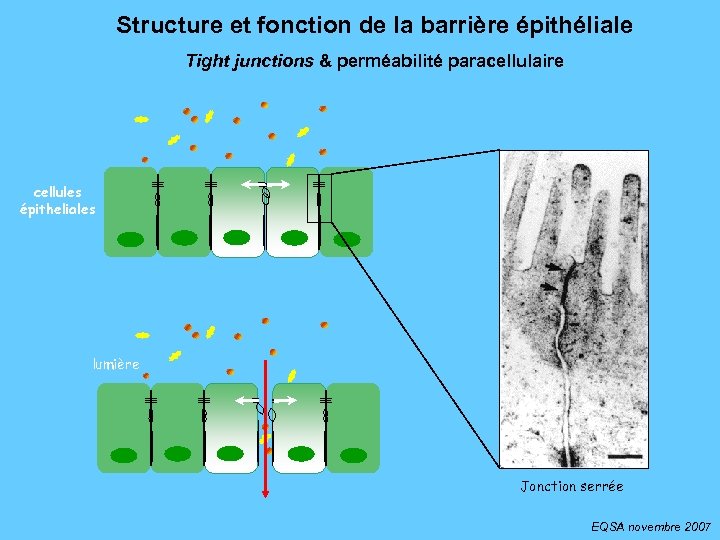
Structure et fonction de la barrière épithéliale Tight junctions & perméabilité paracellulaire cellules épitheliales lumière Jonction serrée EQSA novembre 2007

La chambre de Ussing un outil classique de la physiologie… -Démonstration du caractère actif du transport (pas de gradient électrochimique) Principe = pas de forces s’exerçant sur le mouvement des ions (gradient de concentration, p. H, gradient de pression, de température. . Donc seul l’activité des transporteurs est en cause = transport actif - Permet la mesure qualitative et quantitative des mouvements ioniques Ussing HH and. Zerahn. K. Active sodium as the source of electric current in the short circuited isolated frog skin. Acta Physiol Scand 23: 110, 1951 Schultz. SG and. Zalusky. R. Ion transport in isolated rabbit ileum. I. : Short circuit current and Na fluxes. J Gen Physiol 47: 567, 1964

La chambre de Ussing … un outil classique de la physiologie… -Démonstration du caractère actif du transport (pas de gradient électrochimique) : - Mesures qualitative et quantitative des mouvements ioniques - Accès aux faces séreuse et muqueuse de l’épithélium (application pharmacologiques. . ) - Application aux tissus, biopsies, cellules en culture sur filtre … Ussing HH and Zerahn K. Active sodium as the source of electric current in the short circuited isolated frog skin. Acta Physiol Scand 23: 110, 1951
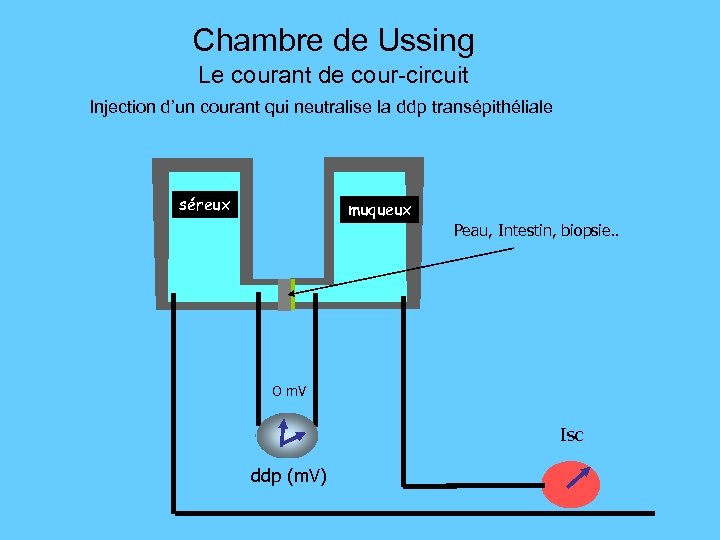
Chambre de Ussing Le courant de cour-circuit Injection d’un courant qui neutralise la ddp transépithéliale séreux muqueux Peau, Intestin, biopsie. . O m. V Isc ddp (m. V)
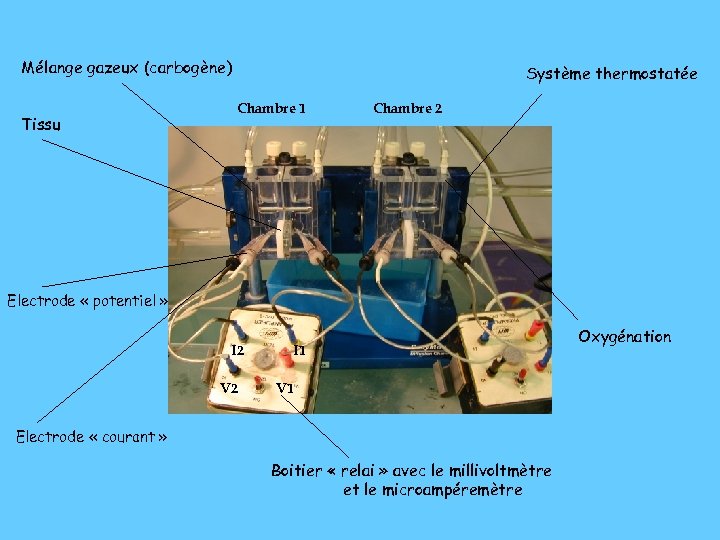
Mélange gazeux (carbogène) Tissu Système thermostatée Chambre 1 Chambre 2 Electrode « potentiel » I 2 V 2 I 1 V 1 Electrode « courant » Boitier « relai » avec le millivoltmètre et le microampéremètre Oxygénation

Un poste complet de mesure des courants de court-circuit. . Interface avec microordinateur Bain-marie Micro-voltmètre et Micro-ampèremètre réunis dans un Voltage Clamp automatique Microordinateur Oxygène, 95% CO 2, 5% Chambres de Ussing
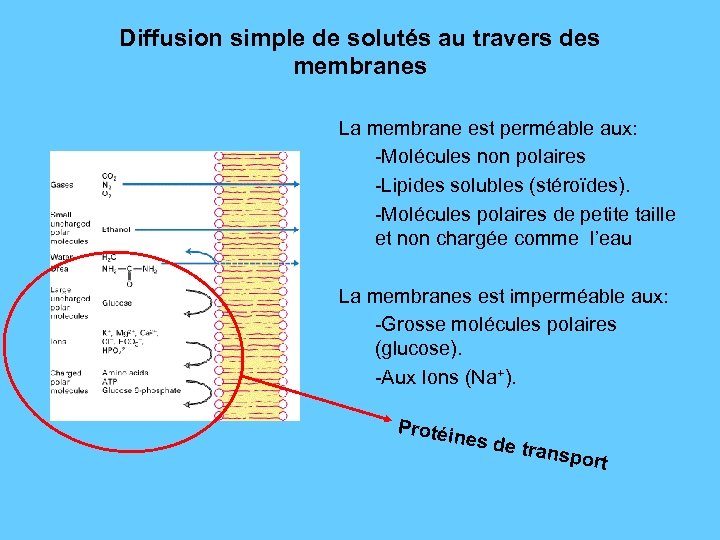
Diffusion simple de solutés au travers des membranes La membrane est perméable aux: -Molécules non polaires -Lipides solubles (stéroïdes). -Molécules polaires de petite taille et non chargée comme l’eau La membranes est imperméable aux: -Grosse molécules polaires (glucose). -Aux Ions (Na+). Protéin es de t ranspo rt

Voies de passage des solutés • Voie paracellulaire – Une barrière: les jonction serrées – Eau , Cl- Petites molécules hydrosolubles • Voie transcellulaire Multiples mécanismes de passage

Différence de potentiel trans-épithéliale Ddp = Vapi -Vbl + lumière V api - V bl Epithélium (tube rénal)
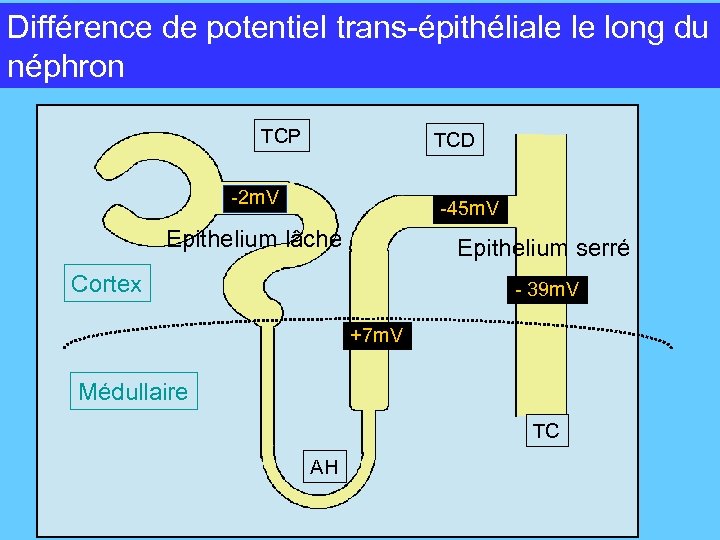
Différence de potentiel trans-épithéliale le long du POTENTIELLE TRANSEPITHELIAL LE LON DU NEPHRON néphron TCP TCD -2 m. V -45 m. V Epithelium lâche Epithelium serré Cortex - 39 m. V +7 m. V Médullaire TC AH
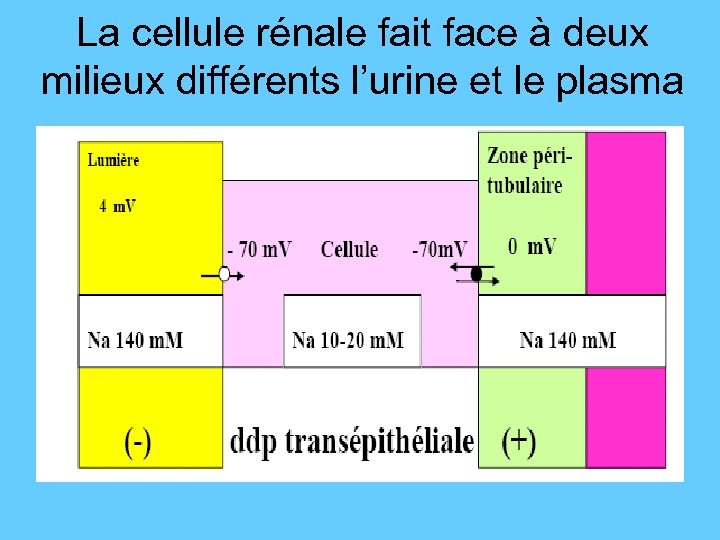
La cellule rénale fait face à deux milieux différents l’urine et le plasma

Les mécanismes de passage transcellulaire

Les mécanismes de passage transcellulaire • En masse – Endocytose (Pinocytose, phagocytose) • Sous forme moléculaire – Passif vs actif – Avec ou sans l’aide d’une protéine

Transports ioniques et moléculaires

Principe de passage à travers la membrane plasmique • La membrane est une bicouche lipidique dont la partie centrale est hydrophobe • L’hydrophobicité de la partie centrale de la membrane empêche le passage de la plupart des molécules polaires • La cellule a besoin de système de transport pour absorber (ou éliminer) des substances polaires
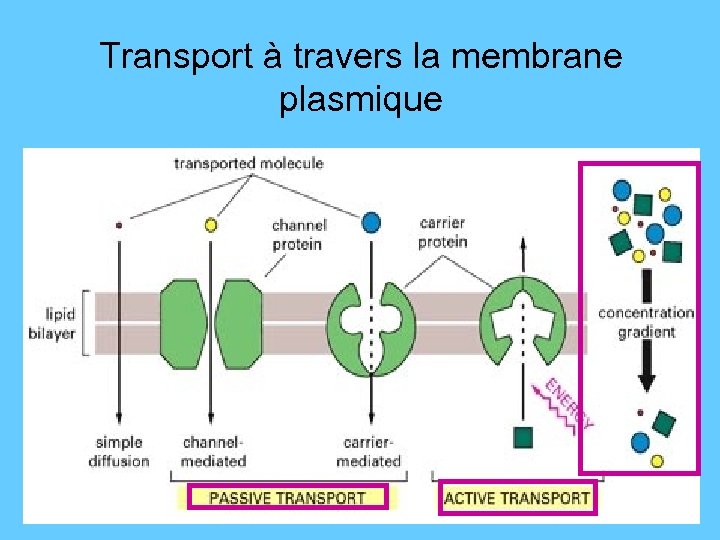
Transport à travers la membrane plasmique

Mécanismes de transport à travers les cellules 1. Directement à travers la membrane • Diffusion et osmose (osmose =diffusion de l’eau) 2. En lmpliquant une protéine membranaire: 1. Canaux (canaux ioniques) et pores (porines) • Débit=107 -108 ions par sec 2. Transporteurs • • • diffusion facilitée: uniport transport actif : symport; antiport Débit=102 -104 molécules par sec 3. Pompes – – Protéines qui hydrolysent l’ATP appelées ATPases Débit=102 -103 ions par sec
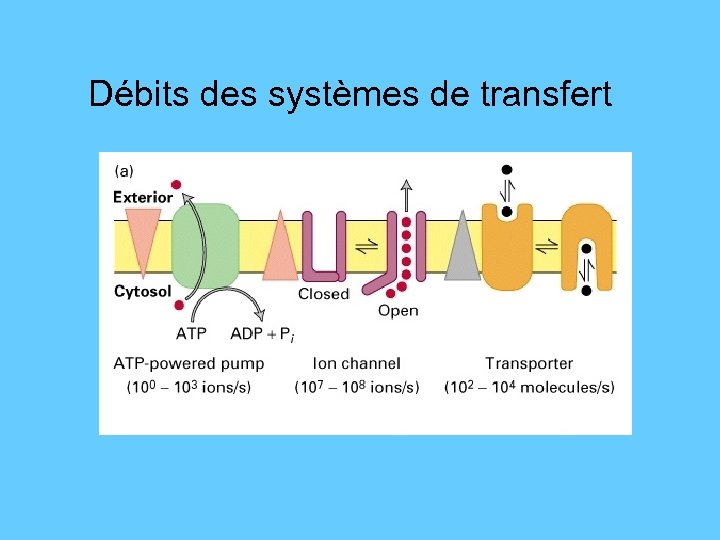
Débits des systèmes de transfert

Canaux, pores et transporteurs • • Aquaporines = transport de l’eau Ionophores = transport des ions Uniport = transport d’une seule substance Transports couplés : transport simultané de 2 substances ou plus – Symport: transport de 2 substances dans la même direction – Antiport: transport de 2 substances en direction opposée
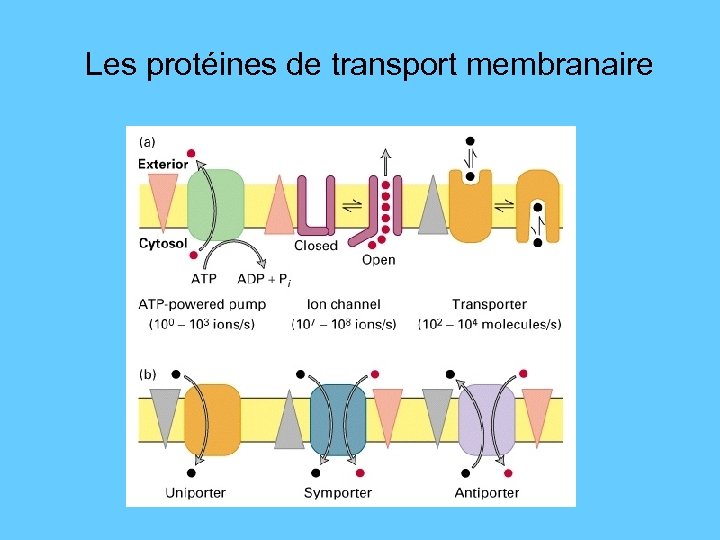
Les protéines de transport membranaire

Mécanismes de transport à travers les cellules Avec besoin ou non d’énergie: – Transport passif: • Le long d’un gradient de concentration – Ne nécessite pas d’ATP – Ex: osmose; diffusion & diffusion facilitée; – Transport actif • Mouvement net contre un gradient de concentration – Requiert directement ou indirectement de l’ ATP
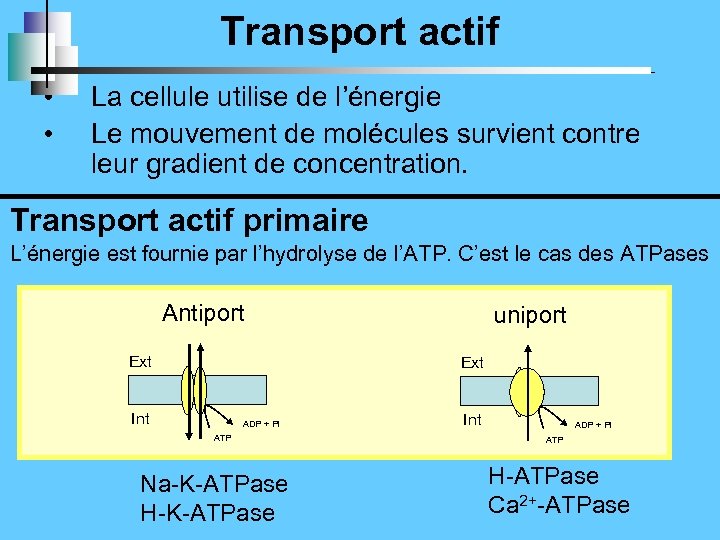
Transport actif • • La cellule utilise de l’énergie Le mouvement de molécules survient contre leur gradient de concentration. Transport actif primaire L’énergie est fournie par l’hydrolyse de l’ATP. C’est le cas des ATPases Antiport Ext uniport Ext Int ADP + Pi ATP Na-K-ATPase H-K-ATPase Int ADP + Pi ATP H-ATPase Ca 2+-ATPase
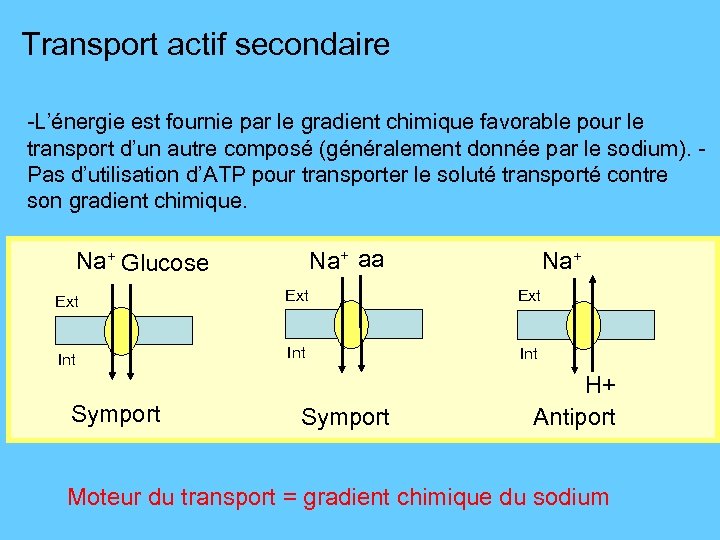
Transport actif secondaire -L’énergie est fournie par le gradient chimique favorable pour le transport d’un autre composé (généralement donnée par le sodium). Pas d’utilisation d’ATP pour transporter le soluté transporté contre son gradient chimique. Na+ aa Na+ Glucose Na+ Ext Ext Int Int Symport H+ Antiport Moteur du transport = gradient chimique du sodium
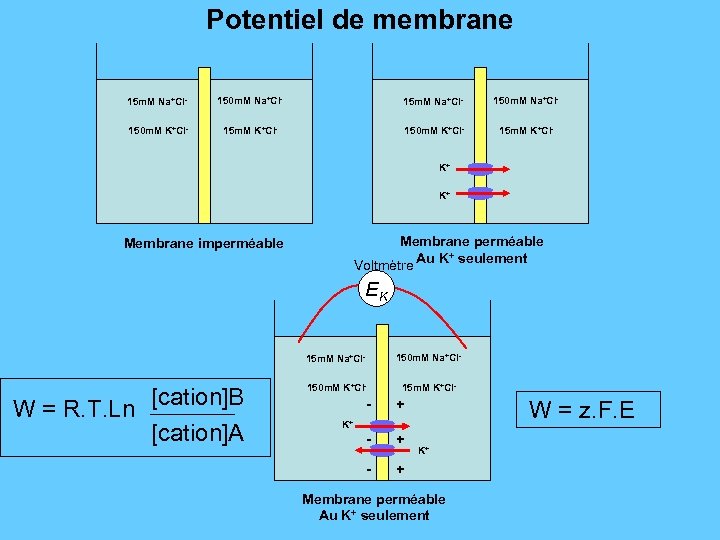
Potentiel de membrane 15 m. M Na+Cl- 150 m. M K+Cl- 15 m. M K+Cl- K+ K+ Membrane perméable + Voltmètre Au K seulement Membrane imperméable EK 15 m. M Na+Cl- W = R. T. Ln [cation]B [cation]A 150 m. M Na+Cl- 150 m. M K+Cl- 15 m. M K+Cl- - + - + W = z. F. E K+ K+ Membrane perméable Au K+ seulement

Potentiel d’équilibre : équation de NERNST EQUATION DE NERNST R= cte des gaz, T= température absolue, Z= valence et F= cte de Faraday Le flux ionique, né d’un gradient de concentration, est auto-limité par le gradient électrique qu’il génère z. F. E = R. T. Ln [cation]B [cation]A [cation]Ext R. T Eion = Ln z. F [cation]Int Eion = 58, 2. log [cation]Ext [cation]Int
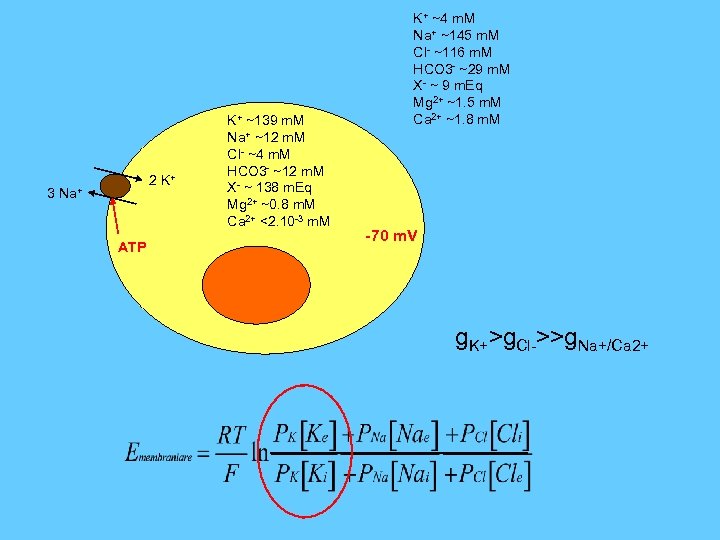
2 K+ 3 Na+ ATP K+ ~139 m. M Na+ ~12 m. M Cl- ~4 m. M HCO 3 - ~12 m. M X- ~ 138 m. Eq Mg 2+ ~0. 8 m. M Ca 2+ <2. 10 -3 m. M K+ ~4 m. M Na+ ~145 m. M Cl- ~116 m. M HCO 3 - ~29 m. M X- ~ 9 m. Eq Mg 2+ ~1. 5 m. M Ca 2+ ~1. 8 m. M -70 m. V g. K+>g. Cl->>g. Na+/Ca 2+
![Potentiel d’équilibre des ions 100 Eion (Volts) = 58. log [C+]2 / [C+]1 Potentiel Potentiel d’équilibre des ions 100 Eion (Volts) = 58. log [C+]2 / [C+]1 Potentiel](https://present5.com/presentation/f1bc01ae5260dcac43ab09cabdade39e/image-60.jpg)
Potentiel d’équilibre des ions 100 Eion (Volts) = 58. log [C+]2 / [C+]1 Potentiel (m. V) 75 50 ENa+ 25 0 On dépolarise ECl- -25 -50 Si g. Na augmente Em EK+ -75 -100 Si la perméabilité de la membrane cytoplasmique pour une espèce ionique augmente, le potentiel de membrane se rapproche au potentiel d’équilibre de cet ion

Potentiel electrochimique Jion = (Vm - Eion) POTENTIEL D'EQUILIBRE GRADIENT ELECTRO-CHIMIQUE FLUX NET EK = - 87 m. V Vm - EK = -70 - (-87) = + 17 m. V SORTANT ENa = + 60 m. V Vm - ENa = -70 - (+60) = - 130 m. V ENTRANT ECa = + 120 m. V Vm - ECa = -70 - (+120) = - 190 m. V ENTRANT ECl = - 61 m. V Vm - ECl = -70 - (-61) = + 9 m. V ÉQUILIBR Par convention, le flux net est positif quand un cation a tendance à sortir de la cellule et est négatif quand le cation a tendance à y entrer. +
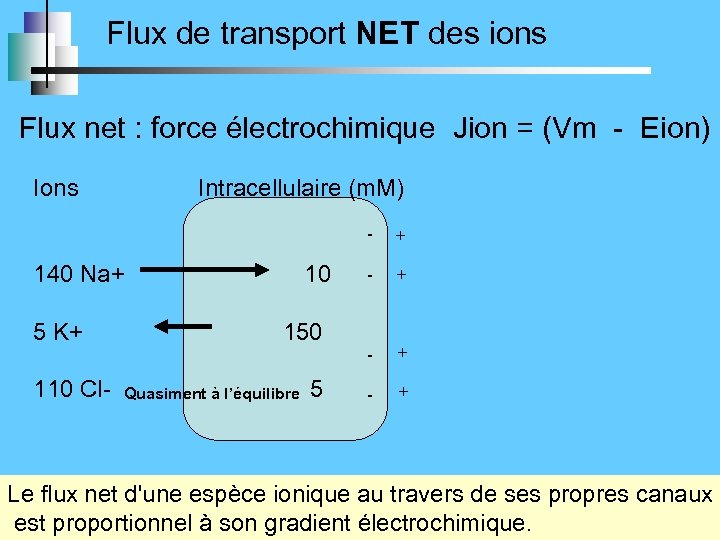
Flux de transport NET des ions Flux net : force électrochimique Jion = (Vm - Eion) Ions Intracellulaire (m. M) - + 140 Na+ 10 5 K+ 150 - + 110 Cl- 5 Quasiment à l’équilibre - + Le flux net d'une espèce ionique au travers de ses propres canaux est proportionnel à son gradient électrochimique.
f1bc01ae5260dcac43ab09cabdade39e.ppt