Главная версия от 09_02_12.ppt
- Количество слайдов: 144

Лабораторные методы диагностики в клинической генетике • Цитогенетические методы • Молекулярно-генетические методы • Биохимические методы

Создатели модели ДНК Фрэнсис Харри Комптон КРИК Francis Harry Compton Crick, 1916– 2004 Джеймс Дьюи УОТСОН James Dewey Watson, р. 1928 Фрэнсис Харри Комптон КРИК (Francis Harry Compton Crick), 1916– 2004 Джеймс Дьюи УОТСОН (James Dewey Watson), р. 1928 Нобелевская премия в области физиологии и медицины в 1962 году
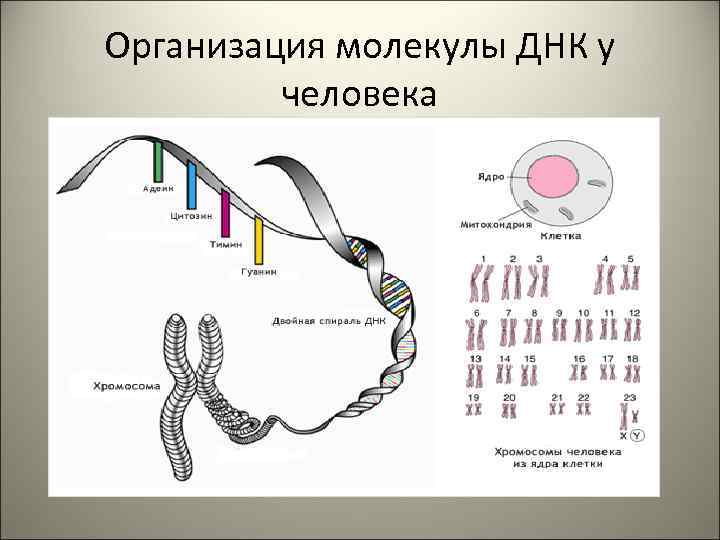
Организация молекулы ДНК у человека

СЛАЙД № 4 Изменения наследственного материала Г 1 Г 2 Г 3 Мутации могут возникать как в соматических, так и половых клетках. Различают геномные, хромосомные аберрации (мутации) и генные мутации. • Геномные мутации - изменение количества наследственного материала (анеуплоидии, полиплоидии). • Хромосомные аберрации - изменение структуры хромосом: делеция (отрыв части хромосомы), инверсия (поворот части хромосомы на 180°), транслокации (перемещение части одной хромосомы на другую) и др. • Генные мутации - изменение структуры ДНК в пределах одного гена. В НАЧАЛО НАЗАД ДАЛЕЕ В КОНЕЦ

Генетически детерминированные заболевания Группа болезней Число Хромосомные болезни 100 Моногенные болезни и синдромы 4500 для 1700 установлен генетический дефект Мультифакторные болезни 500
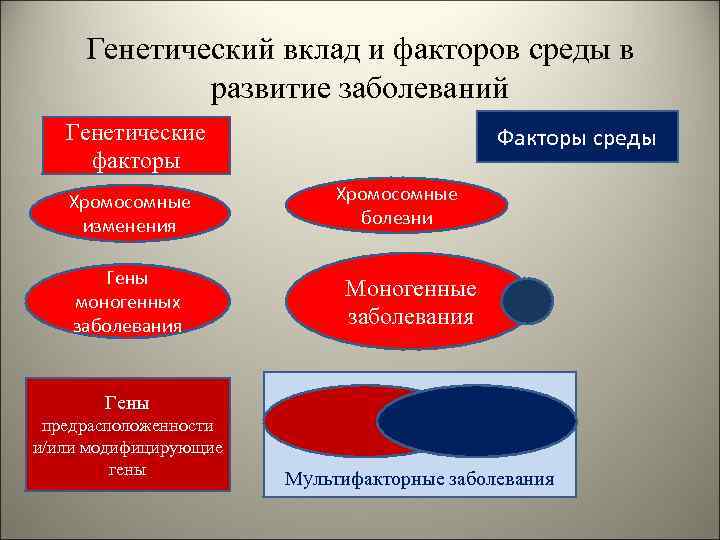
Генетический вклад и факторов среды в развитие заболеваний Генетические факторы Хромосомные изменения Гены моногенных заболевания Факторы среды Хромосомные болезни Моногенные заболевания Гены предрасположенности и/или модифицирующие гены Мультифакторные заболевания

Основные этапы в развитии цитогенетики человека СЛАЙД № 7 1956 г. Первое описание хромосомного набора человека – J. TJIO and A. LEVAN; C. FORD and J. HAMERTON 1959 г. Открытие хромосомной этиологии болезни Дауна, начало развития клинической цитогенетики. – J. LEJEUNE 1960 г. – DENVER CONFERENCE – принятие первой стандартной номенклатуры хромосом человека, дополнений в 1963 г. и 1966 г. на Лондонской и Чикагской конференциях 1968 -1971 г. г. Разработка методов дифференциальной окраски хромосом, Г 4 введение номенклатуры хромосом по особенностям Q-, G-, R-, C-, T-, NOR-сегментации 1981 -1991 г. г. Разработка высокоразрешающих методов и номенклатуры по характеру сегментации, открытие микроделеционных хромосомных синдромов и выяснение роли в патологии феноменов импринтинга и униродительской дисомии 1991 -1995 Разработка FISH-метода, введение в номенклатуру цитогенетики человека раздела “Молекулярная г. г цитогенетика” В НАЧАЛО НАЗАД ДАЛЕЕ В КОНЕЦ

СЛАЙД № 9 Метафазная пластинка при простой окраске В НАЧАЛО НАЗАД ДАЛЕЕ В КОНЕЦ

СЛАЙД № 11 Упорядоченный кариотип на стадии интерфазы: 46, ХХ В НАЧАЛО НАЗАД ДАЛЕЕ В КОНЕЦ

СЛАЙД № 12 Характеристика хромосом по расположению центромеры Виды метафазных хромосом человека: p – короткое плечо, q – длинное плечо В НАЧАЛО НАЗАД ДАЛЕЕ В КОНЕЦ
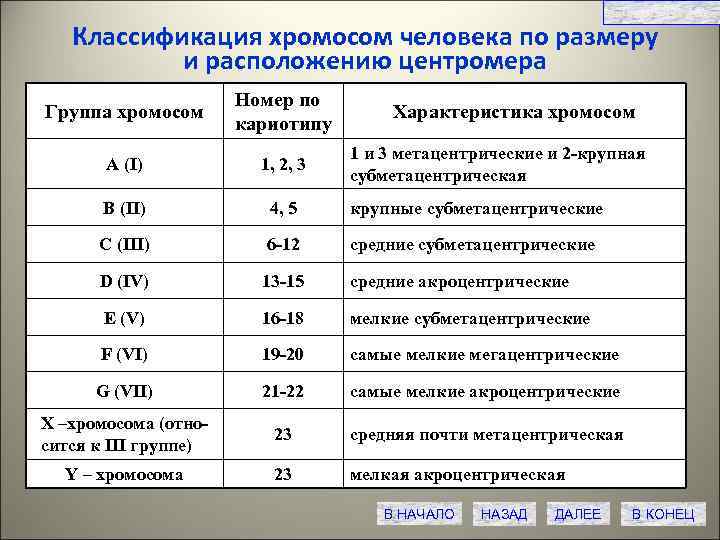
СЛАЙД № 13 Классификация хромосом человека по размеру и расположению центромера Группа хромосом Номер по кариотипу А (I) 1, 2, 3 B (II) 4, 5 крупные субметацентрические C (III) 6 -12 средние субметацентрические D (IV) 13 -15 средние акроцентрические E (V) 16 -18 мелкие субметацентрические F (VI) 19 -20 самые мелкие мегацентрические G (VII) 21 -22 самые мелкие акроцентрические X –хромосома (отно- сится к III группе) 23 средняя почти метацентрическая Y – хромосома 23 мелкая акроцентрическая Характеристика хромосом 1 и 3 метацентрические и 2 -крупная субметацентрическая В НАЧАЛО НАЗАД ДАЛЕЕ В КОНЕЦ
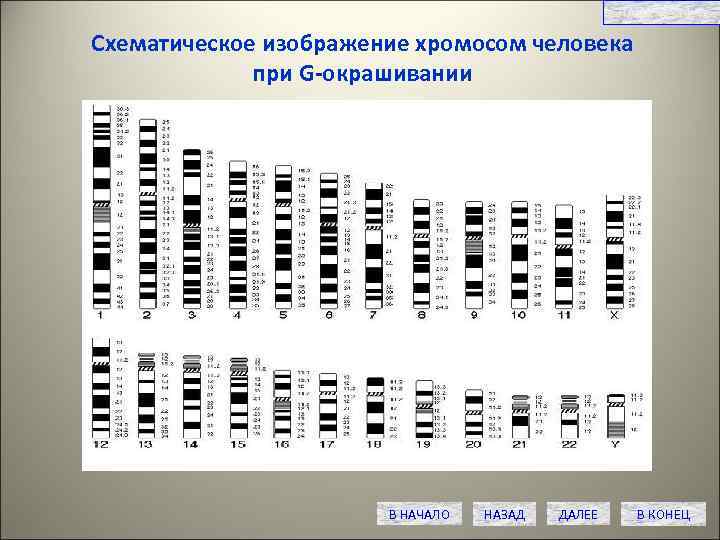
СЛАЙД № 14 Схематическое изображение хромосом человека при G-окрашивании В НАЧАЛО НАЗАД ДАЛЕЕ В КОНЕЦ

СЛАЙД № 16 Наиболее часто диагностируемые методом классического кариотипирования хромосомные аберрации Г 5 Г 6 Г 7 • • 21 -трисомия (синдром Дауна) — 1: 700; XXX (трисомия Х) — 1: 1000 (девочки); XYY (синдром дубль-Y) — 1: 1000 (мальчики); XXY (синдром Клайнфельтера) — 1: 1400 (мальчики); ХО (синдром Шерешевского — Тернера) — 1: 3300 (девочки); 46. 5 р (синдром «кошачьего крика» ) — 1: 4000; 18 -трисомия (синдром Эдвардса) — 1: 6800; 13 -трисомия (синдром Патау) — 1: 7600. В НАЧАЛО НАЗАД ДАЛЕЕ В КОНЕЦ

Синдром Дауна ГИПЕРССЫЛКА № 5 Синдром Дауна (СД) - наиболее изученная хромосомная болезнь. Описана в 1866 г. , в 1959 году установлена связь с аномалией набора 21 -й хромосомы. Примерно в 94% случаев синдром обусловлен трисомией по 21 -й хромосоме. При этом вклад материнского нерасхождения в эти гаметические формы болезни составляет 80%, а отцовского - только 20%. Причины такой разницы неясны. Небольшая (около 2%) доля детей с СД имеют мозаичные формы(47+21/46). Примерно 4% больных СД имеют транслокационную форму трисомии по типу робертсоновских транслакаций между акроцентриками (D/21 и G/21). Почти 50% транслокационных форм наследуется от родителейносителей, и 50% - это транслокации, возникшие de novo. Частота СД среди новорожденных равна 1: 700 - 1: 800, не имеет какой-либо этнической или географической разницы при сравнении одинакового возраста родителей. Частота рождения детей с СД зависит от возраста матери и в меньшей мере от возраста отца. СИМПТОМЫ: 1. Плоское лицо, монголоидный разрез глаз, открытый рот, короткий нос, плоская переносица, косоглазие, пигментные пятна по краю радужки; 2. Увеличение поперечного размера головы при относительном уменьшении продольного размера; 3. Плоский затылок; 4. Деформированные низко посаженные уши; 5. Аркообразное небо, зубные аномалии, бороздчатый язык; 6. Короткая широкая шея, кожная складка на шее у новорожденных; 7. Короткие конечности, повышенная подвижность суставов; 8. Деформация грудной клетки (килевидная или воронкообразная); 9. Мышечная слабость; 10. Врожденные пороки сердца; 11. Поперечная ладонная складка; 12. Умственная отсталость. ВЫХОД ИЗ ГИПЕРССЫЛКИ

ГИПЕРССЫЛКА № 5. 1 Кариотип девочки с синдромом Дауна 47, ХХ, +21 Трисомный случай – имеются три свободно лежащие хромосомы 21 (зелёный цвет) (цвет изменён для наглядности) ВЫХОД ИЗ ГИПЕРССЫЛКИ

ГИПЕРССЫЛКА № 5. 2. 1 Фотография кариотипа девочки с транслокационным случаем трисомии хромосомы 21 (синдром Дауна) 46, ХХ, tr(14; 21), +21 после G-окрашивания 1 21 -я хромосома (зелёная) (цвет изменен для наглядности) 2 3 4 14 -я хромосома (красная) (цвет изменен для наглядности) tr(14; 21) – транслокационная хромосома, в состав которой входят хромосомы 14 (красная) и 21 (зелёная) (цвет изменен для наглядности) Результат носительства Робертсоновской транслокации (14; 21) у одного из родителей

ГИПЕРССЫЛКА № 5. 2. 2 Синдром Дауна – транслокационная форма 46, ХХ, tr(21; 21), +21 21 -я хромосома (цвет изменен для наглядности) Транслокационная хромосома tr(21; 21) (цвет изменен для наглядности) 1 2 ВЫХОД ИЗ ГИПЕРССЫЛКИ НАЗАД

ГИПЕРССЫЛКА № 6 Синдром Клайнфельтера Описан доктором Harry Klinefelter в 1942 году. Классическим вариантом синдрома является кариотип 47, XXY. У 10% больных выявляется мозаицизм 46, XY/47, XXY Возможны кариотипы: 48, XXXY ; 49, XXXXY; 48, XXYY; 49, XXXYY, которые встречаются редко. До периода полового созревания мальчики развиваются почти нормально, лишь с небольшим отставанием в психическом развитии. В процессе возмужания у больных с этим синдромом складывается евнухоидный тип строения тела: узкие плечи и грудная клетка, широкий таз, слаборазвитые мускулатура и волосяной покров на лобке, подмышками, слабое оволосение лица, обычно имеют высокий рост, обычно безынициативны и редко способны к творческой деятельности. Они легко поддаются внушению и эмоционально не устойчивы. Больные предрасположены к сахарному диабету , заболеваниям щитовидной железы и раку молочной железы. ВЫХОД ИЗ ГИПЕРССЫЛКИ

ГИПЕРССЫЛКА № 6. 1 Кариотип синдрома Клайнфельтера; 47 XXY; G-окрашивание X-хромосома (зелёная) (цвет изменен для наглядности) 1 2 X-хромосома (зелёная) (цвет изменен для наглядности) 3 ВЫХОД ИЗ ГИПЕРССЫЛКИ Y-хромосома (красная) (цвет изменен для наглядности)
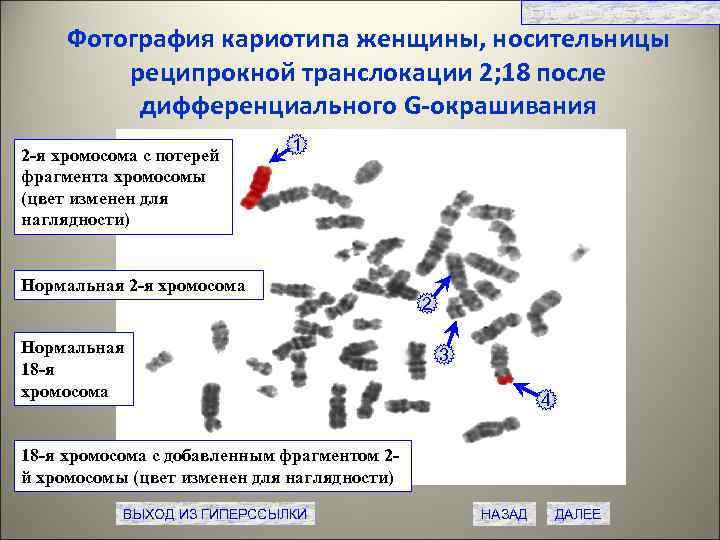
ГИПЕРССЫЛКА № 4. 1. 2 Фотография кариотипа женщины, носительницы реципрокной транслокации 2; 18 после дифференциального G-окрашивания 2 -я хромосома с потерей фрагмента хромосомы (цвет изменен для наглядности) 1 Нормальная 2 -я хромосома Нормальная 18 -я хромосома 2 3 4 18 -я хромосома с добавленным фрагментом 2 й хромосомы (цвет изменен для наглядности) ВЫХОД ИЗ ГИПЕРССЫЛКИ НАЗАД ДАЛЕЕ

Гибридизация in situ с флуоресцентной меткой (FISH) Принцип метода: комплементарность ДНК-зондов (коротких фрагментов ДНК с известной специфичностью) к ДНК-объекту с последующей регистрацией места локализацаии зонда по флуоресцентной метке.

СЛАЙД № 18 Типы зондов для FISH исследования • CEP – Chromosove Enumerator Probe, хромосомные нумераторы или центромерные зонды; • LSI – Locus Specific Identificator, локус специфические зонды; • Sub. Tel – Subtelomere specific, субтеломерные зонды; • WCP – Whole-Chromosome-Painting, зонды полного окрашивания хромосом, цельно-хромосомный зонд В НАЧАЛО НАЗАД ДАЛЕЕ В КОНЕЦ

СЛАЙД № 19 Центромерные пробы или хромосомные нумераторы CEP Центромерные пробы используются в диагностике численных хромосомных нарушений (моносомии и трисомии по отдельным хромосомам) как на хромосомных препаратах, так и на интерфазных ядрах. Эффективны в пренатальной цитогенетической диагностике, особенно в исследованиях хориальной ткани, когда не всегда возможно получение качественных хромосомных препаратов или требуется быстрое цитогенетическое заключение при риске на распространенные хромосомные болезни, обусловленные нерасхождением хромосом. Конкордантность (соответствие) между данными FISH-анализа и стандартного цитогенетического анализа составляет 99, 8%. Чувствительность FISH-анализа (вероятность того, что плод с анеуплоидией по хромосомам 13, 18, 21, Х, У будет позитивным по FISH-тесту) в среднем составляет 99, 6%. Специфичность (вероятность того, что плод с нормальным набором хромосом 13, 18, 21, Х и У будет иметь нормальный FISH-тест) – 99, 98%. В НАЧАЛО НАЗАД ДАЛЕЕ В КОНЕЦ

СЛАЙД № 20 Локус специфические зонды - LSI Применение этих зондов особенно показано для точной идентификации структурных перестроек – сайтов разрывов хромосом при транслокациях, инверсиях, делециях, инсерциях и др. Подтверждение клинико-генетического диагноза микроделеционных синдромов (с. Вольфа-Хиршхорна, с. кошачьего крика, с. Вильямса, с. Прадера. Вилли/Энжельмана и др. ) [М. Манвелян, 2004]. С использованием данного метода описана микроделеция длинного плеча хромосомы 22 – del(22 q 11. 2), которая встречается с частотой 1 случай на 4000 новорожденных и ассоциирована с врожденными пороками сердца (ВПС) [В. Г. Антоненко, 2004]. В НАЧАЛО НАЗАД ДАЛЕЕ В КОНЕЦ

СЛАЙД № 21 Субтеломерные зонды - Sub. Tel Показана существенную роль т. н. субтеломерных перестроек в генезе недифференцированной умственной отсталости (УО), частота которых достигает более 10% (разброс от 0, 5% до 11, 1%) [В. Аnderlid et al. , 2002; Biesecker, 2002; Knight et al. , 2000; Van Buggenhout et al. , 2001 и др]. На основе FISH-анализа с Sub. Tel-пробами были описаны: микротерминальная делеция 8 pter в результате семейной транслокации t(8; 20), явившейся причиной УО (De Vries et al. , 2001). В НАЧАЛО НАЗАД ДАЛЕЕ В КОНЕЦ

Types of probes Centromeric (satellite) probes Locus specific probes Whole chromosome painting probes

Lissencephaly- Miller dieker syndrome

Многоцветная флуоресцентная in situ гибридизация 24 цветный FISH (материалы фирмы “Meta. Systems Gmb. H”) СЛАЙД № 22 • Для их мечения вполне достаточно 5 флуорохромов. Хромосом специфические ДНК библиотеки метятся уникальными комбинациями трех флуорохромов. В результате флуоресцентной in situ гибридизации каждой хромосоме человека соответствует свой псевдоцвет. • a – метафазная пластинка; • b – pаскладка хромосом; • с – aнализ транслокации 8 -й и 11 -й хромосом человека В НАЧАЛО НАЗАД ДАЛЕЕ В КОНЕЦ
СЛАЙД № 24 Цветная исчерченность хромосом человека при RXFISH: a – метафазная пластинка; b – pаскладка хромосом (материалы фирмы “Applied Imaging”) В НАЧАЛО НАЗАД ДАЛЕЕ В КОНЕЦ

СЛАЙД № 25 Многоцветный FISH/высокоразрешающих бэндинг (1997 Уве Клауссен, Ильза Худоба в сотрудничестве с фирмой Meta. Systems) В отличие от RXFISH, она предназначена не для полного анализа всех хромосом, а для проведения детального анализа одной из них. В этих целях был получен комплект микродиссекционных ДНК проб и разработано специальное программное обеспечение “Meta. Systems’ isis m. FISH” для сравнительного анализа уровня свечения различных флуорохромов. В НАЧАЛО НАЗАД ДАЛЕЕ В КОНЕЦ

СЛАЙД № 26 Выявляемость хромосомных аномалий (ХА) у детей Клиническая 8 – 10 25 - 30 общая группа 6 - 8 20 -35 общая группа 0, 7 – 0, 9 с м. ВПР 13 - 17 С ВПР Новорожденные дети общая группа с ВПР Недоношенные дети: Частота ХА (в %) с ВПР Мертворожденные: Группа 35 - 45 Дети с задержкой психомоторного развития 12 - 20 Дети с УО и микроаномалиями 15 - 15 В НАЧАЛО НАЗАД ДАЛЕЕ В КОНЕЦ
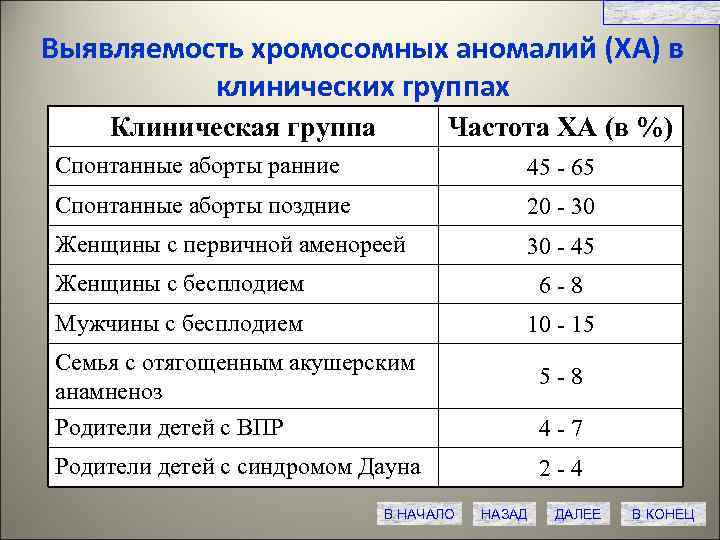
СЛАЙД № 27 Выявляемость хромосомных аномалий (ХА) в клинических группах Клиническая группа Частота ХА (в %) Спонтанные аборты ранние 45 - 65 Спонтанные аборты поздние 20 - 30 Женщины с первичной аменореей 30 - 45 Женщины с бесплодием 6 - 8 Мужчины с бесплодием 10 - 15 Семья с отягощенным акушерским анамненоз Родители детей с ВПР 5 - 8 4 - 7 Родители детей с синдромом Дауна В НАЧАЛО 2 - 4 НАЗАД ДАЛЕЕ В КОНЕЦ
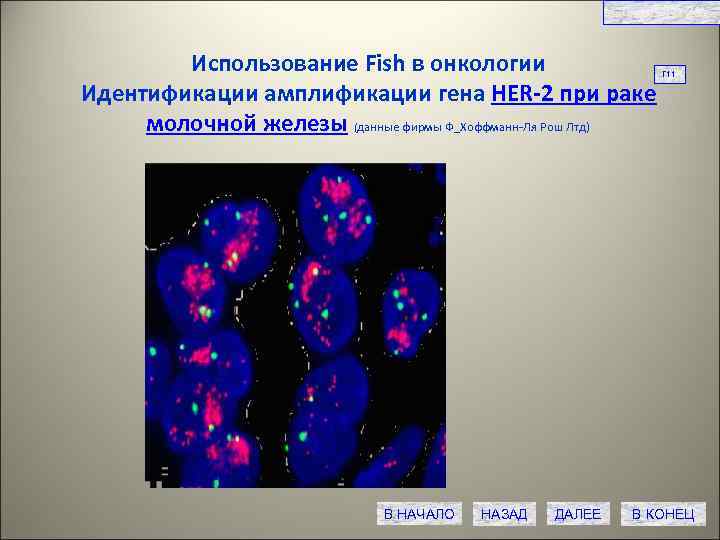
СЛАЙД № 29 Использование Fish в онкологии Идентификации амплификации гена HER-2 при раке молочной железы (данные фирмы Ф_Хоффманн-Ля Рош Лтд) В НАЧАЛО НАЗАД ДАЛЕЕ Г 11 В КОНЕЦ

СЛАЙД № 28 Г 10 Цитогенетический метод дозиметрии В НАЧАЛО НАЗАД ДАЛЕЕ В КОНЕЦ

СЛАЙД № 31 Молекулярно-генетические методы В НАЧАЛО НАЗАД ДАЛЕЕ В КОНЕЦ

СЛАЙД № 32 Моногенные болезни • Болезни, обусловленные мутациями в одном гене • Заболевания, подчиняющиеся менделевским законам наследования • В OMIM описано более 4, 5 тысяч фенотипов • Для ~ 1700 из них известен молекулярный дефект Г 12 • Частые наследственные заболевания – 1: 10 000 и чаще • Редкие наследственные заболевания – 1: 100 000 и реже • Каждый человек – гетерозиготный носитель 3 и более мутаций В НАЧАЛО НАЗАД ДАЛЕЕ В КОНЕЦ
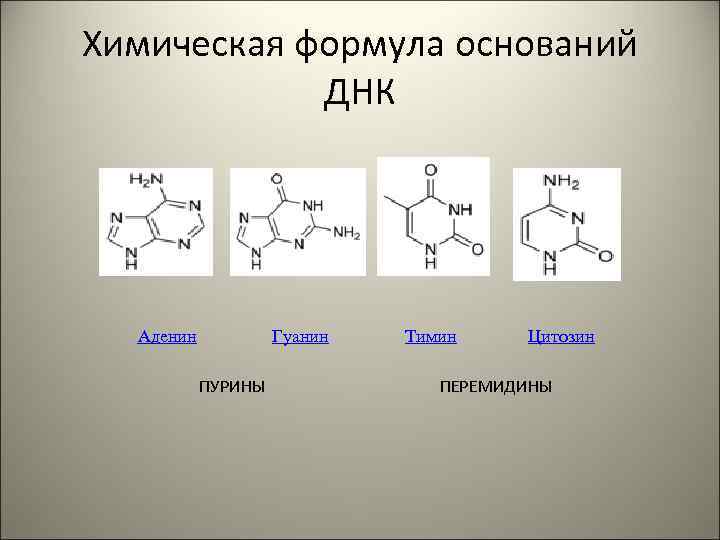
Химическая формула оснований ДНК Аденин Гуанин ПУРИНЫ Тимин Цитозин ПЕРЕМИДИНЫ

Основания формирующие ДНК
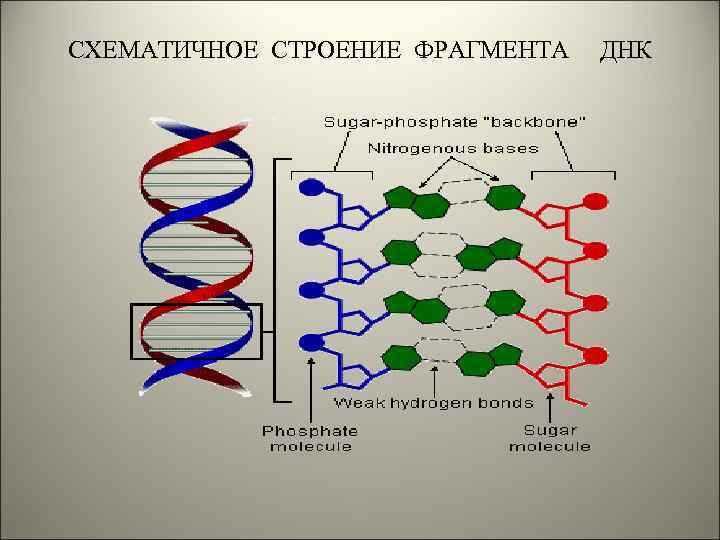
СХЕМАТИЧНОЕ СТРОЕНИЕ ФРАГМЕНТА ДНК

ВАРИАНТ ОТОБРАЖЕНИЯ СТРОЕНИЯ ДНК

СЛАЙД № 39 Базовые методы идентификации мутаций • Гибридизация • Полимеразная цепная реакция В НАЧАЛО НАЗАД ДАЛЕЕ В КОНЕЦ
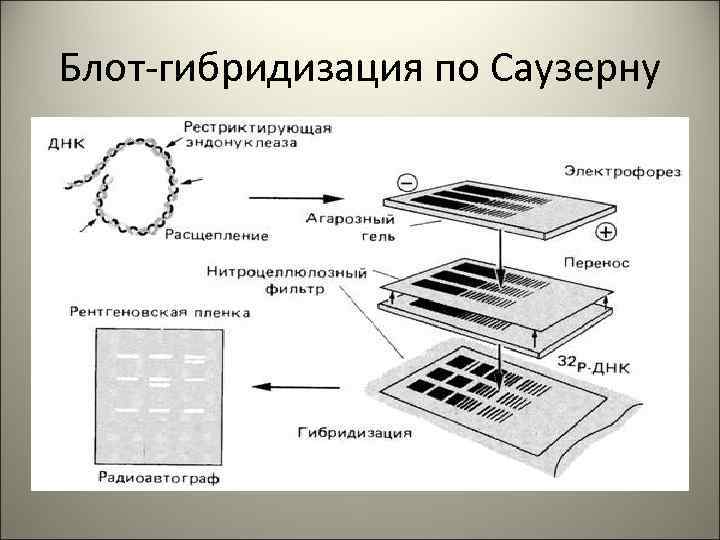
Блот-гибридизация по Саузерну

СЛАЙД № 41 Полимеразная цепная реакция ПЦР - искусственный процесс многократного копирования (амплификации) специфической последовательности ДНК, осуществляемый in vitro. Копирование ДНК при ПЦР осуществляется специальным ферментом – ДНК-полимеразой. ДНК - полимераза, двигаясь по одиночной цепи ДНК (матрице), синтезирует комплементарную ей последовательность ДНК - полимераза не может начать синтез цепи ДНК "с нуля", ей необходима короткая "затравочная" цепь РНК или ДНК, к которой она может начать присоединять нуклеотиды. В НАЧАЛО НАЗАД ДАЛЕЕ В КОНЕЦ

СЛАЙД № 42 Проведение ПЦР Необходимые составляющие: 1. матричная ДНК-мишень (достаточно даже одной молекулы) длиной от 100 до ~35000 п. н. ; 2. два искусственно синтезированных праймера – олигонуклеотидные последовательности длиной 15 -30 п. н. ; 3. термостабильная ДНК-полимераза, сохраняющая свою активность при температуре 94°С и выше; 4. четыре дезоксирибонуклеоида (d. ATP, d. TTP, d. GTP, d. CTP). Этапы реакции: 1. денатурация – перевод двунитевой матричной ДНК в однонитевую форму путем нагревания до t 94 – 98 °С в течение нескольких минут; 2. гибридизация или отжиг праймеров - температура смеси снижается до 37 -65°С, и олигопраймеры гибридизируются с одноцепочечной ДНК, содержащей комплементарные участки ограничивая тем самым амплифицирующий фрагмент; 3. этап синтеза - температура повышается до 68 -72°С (оптимальный режим для ДНКполимеразы), что запускает синтез ДНК в направлении от 5’- к 3 ‘ - концу геномной ДНК-матрицы 4. Далее циклическое повторение этапов реакции. Количество циклов: 28 -40 В НАЧАЛО НАЗАД ДАЛЕЕ В КОНЕЦ

СЛАЙД № 43 Полимеразная цепная реакция В НАЧАЛО НАЗАД ДАЛЕЕ В КОНЕЦ
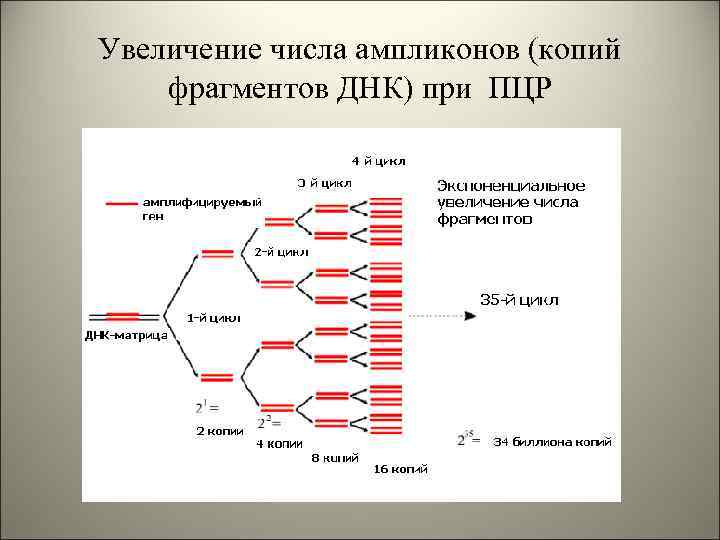
Увеличение числа ампликонов (копий фрагментов ДНК) при ПЦР

СЛАЙД № 61 Гель-электрофорез: сортировка фрагментов ДНК по размеру В НАЧАЛО НАЗАД ДАЛЕЕ В КОНЕЦ

СЛАЙД № 34 Методы молекулярной диагностики ПРЯМЫЕ v Предмет анализа - мутации в гене v Условие - необходимо знание структуры гена v Область применения: ü возможна при сомнительном диагнозе ü возможна при полилокусном заболевании v Точность 100% КОСВЕННЫЕ v v ü ü ü v Предмет анализа - полиморфные маркеры Условия: уверенность в клиническом диагнозе наличие одного локуса заболевания наличие пробанда Область применения: большая протяженность гена широкий спектр мутаций ген неизвестен, но известна его локализация Точность 90 -95% В НАЧАЛО НАЗАД ДАЛЕЕ В КОНЕЦ

СЛАЙД № 37 Принципы определения родства методом косвенной ДНК-диагностики Локус ДНК TH 01 расположен в коротком плече хромосомы 11 в регионе 15. 5 (обозначение по международной номенклатуре 11 p 15. 5). Он имеет 7 различных аллелей (с 5 по 11). С его помощью можно устанавливать происхождение хромосомы 11. Сравнение хромосом пациентов производят с помощью стандартов, называющихся аллельными лестницами. Мать имеет аллели 7 и 8, ребенок - 6 и 8, предполагаемый отец -6 и 10. Т. к. при исследовании материнство предполагается бесспорным, то ясно, что аллель 8 получен ребенком от матери. Поэтому от истинного биологического отца ребенок получил аллель 6. У предполагаемого отца этот аллель имеется, что не исключает его биологического отцовства. В НАЧАЛО НАЗАД ДАЛЕЕ В КОНЕЦ

СЛАЙД № 35 Принцип косвенной ДНК-диагностики для определения носительства рецессивного заболевания 1 1 2 4 3 2 3 4 1 В НАЧАЛО НАЗАД 3 ДАЛЕЕ В КОНЕЦ

СЛАЙД № 45 Некоторые прямые методы идентификации мутаций • Метод анализа конформационного полиморфизма однонитевой ДНК - SSCP; • Денатурирующий градиентный гельэлектрофорез - DGGE • Метод гетеродуплексного анализа - НА; • Метод химического расщепления некомплементарных сайтов (CMC); • Метод прямого секвенирования. В НАЧАЛО НАЗАД ДАЛЕЕ В КОНЕЦ

СЛАЙД № 47 Одноцепочечный конформационный полиморфизм (SSCP) Влияние расположения нуклеотидов на конформизм однонитевой ДНК и, как следствие, изменение электрофоретической подвижности коротких фрагментов (цитируется из книги В. Н. Горбунова, В. С. Баранова, 1997 г. ). В НАЧАЛО НАЗАД ДАЛЕЕ В КОНЕЦ

Исследования мутаций методом SSCP. Мажорный локус гена b-raf (а. ) и полиморфизма MDR 1 (б. ) а. SSCP электрофорез 15 экзон гена braf. 1 - 5, 7 -8 пробы ( 1 -2, 4 -5, 7 -8 –N, 3 – мутация (600 кодон, GTG на GAG, валин на глютамин)), 6 – контроль +, 9 контроль –. б. SSCP электрофорез гена MDR, полиморфизм C 3435 T (1 – СС, 2 – ТТ, 3 – СТ, 4 – ТТ, 5 – СТ, 6 -СС, 7 – ? ? , 8 – ТТ, 9 – СТ, 10 – ТТ).
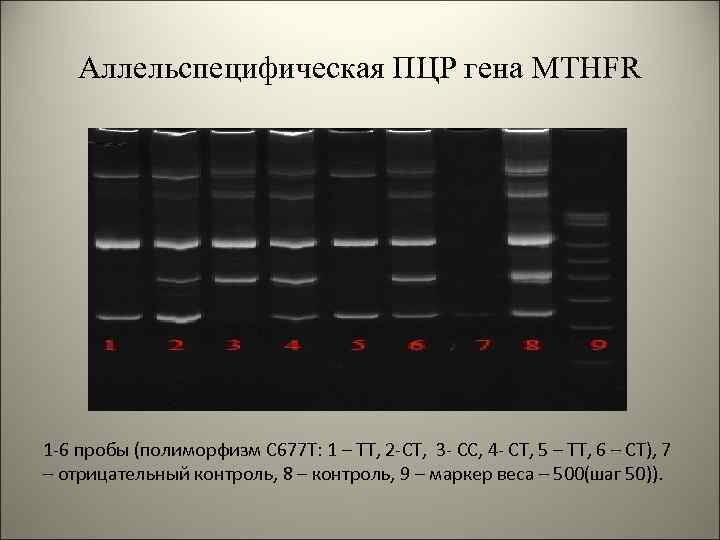
Аллельспецифическая ПЦР гена MTHFR 1 -6 пробы (полиморфизм C 677 T: 1 – TT, 2 -CT, 3 - CC, 4 - СТ, 5 – ТТ, 6 – СТ), 7 – отрицательный контроль, 8 – контроль, 9 – маркер веса – 500(шаг 50)).

СЛАЙД № 59 Полиморфизм длины рестрикционных фрагментов (ПДРФ) Метод ПДРФ основан на способности рестрикционных эндонуклеаз расщеплять двухцепочечную ДНК в участках с определенной нуклеотидной последовательностью – сайтах рестрикции. Благодаря этому любые изменения первичной структуры генов, связанные с исчезновением или появлением нового сайта рестрикции, могут быть обнаружены путем расщепления с помощью соответствующих рестриктаз и электрофоретического разделения полученных фрагментов ДНК. На сегодняшний день известно более 500 рестриктаз. В НАЧАЛО НАЗАД ДАЛЕЕ В КОНЕЦ

Полиморфизм длины рестрикционных фрагментов - ПДРФ. Метод ПДРФ основан на способности рестрикционных эндонуклеаз расщеплять двухцепочечную ДНК в участках с определенной нуклеотидной последовательностью – сайтах рестрикции.

Полиморфизм длины рестрикционных фрагментов - ПДРФ Ген MTHFR, полиморфизм C 677 T, 8% ПААГ, PCR Rest PCR Rest PCR Rest w 26 w 27 w 28 w 29 s w 29 w 30 w 31 w 32 w 35 w 36 +- -- отр. контр. +- --

СЛАЙД № 48 Денатурирующий градиентный гель электрофорез - DGGE В НАЧАЛО НАЗАД ДАЛЕЕ В КОНЕЦ

ПЦР с использованием Tag. Man зонда

Прибор для Real-time PCR фирмы Bio Rad на 96 пробирок (проб). Типичная кривая изменения флоресцентного сигнала.

СЛАЙД № 58 Прямое секвенирование • • • Реакция идет аналогично ПЦР по в реакционную смесь добавляют четыре дезоксирибонуклеоида обладающих способностью тормозить продолжение синтеза новой копии ДНК - dd. ATP, dd. TTP, dd. GTP, dd. CTP. Тем самым, в растворе оказываются синтезированные фрагменты ДНК разной длины, размер которых определяется различными способами и на основе числовых способов обсчета выстраивается нуклиотидная последовательность изучаемого фрагмента (слайд из книги «Генетика» , под ред. В. И. Иванова, М, 2006) В НАЧАЛО НАЗАД ДАЛЕЕ В КОНЕЦ

Локализация и количество нуклеотидов в гене CFTR • Start: 117, 119, 358 bp from pter • End: • Size: 189, 362 bases 117, 308, 719 bp from pter

Строение гена CFTR и спектр известных мутаций

Последовательность нуклеотидов в гене CFTR таблица 1 • • • • • 1 aattggaagc aaatgacatc acagcaggtc agagaaaaag ggttgagcgg caggcaccca 61 gagtagtagg tctttggcat taggagcttg agcccagacg gccctagcag ggaccccagc 121 gcccgagaga ccatgcagag gtcgcctctg gaaaaggcca gcgttgtctc caaacttttt 181 ttcagctgga ccagaccaat tttgaggaaa ggatacagac agcgcctgga attgtcagac 241 atataccaaa tcccttctgt tgattctgct gacaatctat ctgaaaaatt ggaaagagaa 301 tgggatagag agctggcttc aaagaaaaat cctaaactca ttaatgccct tcggcgatgt 361 tttttctgga gatttatgtt ctatggaatc tttttatatt taggggaagt caccaaagca 421 gtacagcctc tcttactggg aagaatcata gcttcctatg acccggataa caaggaggaa 481 cgctctatcg cgatttatct aggcataggc ttatgccttc tctttattgt gaggacactg 541 ctcctacacc cagccatttt tggccttcat cacattggaa tgcagatgag aatagctatg 601 tttagtttga tttataagaa gactttaaag ctgtcaagcc gtgttctaga taaaataagt 661 attggacaac ttgttagtct cctttccaac aacctgaaca aatttgatga aggacttgca 721 ttggcacatt tcgtgtggat cgctcctttg caagtggcac tcctcatggg gctaatctgg 781 gagttgttac aggcgtctgc cttctgtgga cttggtttcc tgatagtcct tgcccttttt 841 caggctgggc tagggagaat gatgatgaag tacagagatc agagagctgg gaagatcagt 901 gaaagacttg tgattacctc agaaatgatt gaaaatatcc aatctgttaa ggcatactgc 961 tgggaagaag caatggaaaa aatgattgaa aacttaagac aaacagaact gaaactgact 1021 cggaaggcag cctatgtgag atacttcaat agctcagcct tcttcttctc agggttcttt 1081 gtggtgtttt tatctgtgct tccctatgca ctaatcaaag gaatcatcct ccggaaaata

Последовательность нуклеотидов в гене CFTR таблица 2 1141 ttcaccacca tctcattctg cattgttctg cgcatggcgg tcactcggca atttccctgg 1201 gctgtacaaa catggtatga ctctcttgga gcaataaaca aaatacagga tttcttacaa 1261 aagcaagaat ataagacatt ggaatataac ttaacgacta cagaagtagt gatggagaat 1321 gtaacagcct tctgggagga gggatttggg gaattatttg agaaagcaaa acaaaacaat 1381 aacaatagaa aaacttctaa tggtgatgac agcctcttct tcagtaattt ctcacttctt 1441 ggtactcctgaaaga tattaatttc aagatagaaa gaggacagtt gttggcggtt 1501 gctggatcca ctggagcagg caagacttca cttctaatga tgattatggg agaactggag 1561 ccttcagagg gtaaaattaa gcacagtgga agaatttcat tctgttctca gttttcctgg 1621 attatgcctg gcaccattaa agaaaatatc atctttggtg tttcctatga tgaatataga 1681 tacagaagcg tcatcaaagc atgccaacta gaagaggaca tctccaagtt tgcagagaaa 1741 gacaatatag ttcttggaga aggtggaatc acactgagtg gaggtcaacg agcaagaatt 1801 tctttagcaa gagcagtata caaagatgct gatttgtattagactc tccttttgga 1861 tacctagatg ttttaacaga aaaagaaata tttgaaagct gtgtctgtaa actgatggct 1921 aacaaaacta ggattttggt cacttctaaa atggaacatt taaagc tgacaaaata 1981 ttaattttga atgaaggtag cagctatttt tatgggacat tttcagaact ccaaaatcta 2041 cagccagact ttagctcaaa actcatggga tgtgattctt tcgaccaatt tagtgcagaa 2101 agaagaaatt caatcctaac tgagacctta caccgtttct cattagaagg agatgctcct 2161 gtctcctgga cagaaacaaa aaaacaatct tttaaacaga ctggagagtt tggggaaaaa 2221 aggaagaatt ctattctcaa tccaatcaac tctatacgaa aattttccat tgtgcaaaag

Последовательность нуклеотидов в гене CFTR таблица 3 2281 actcccttac aaatgg catcgaagag gattctgatg agcctttaga gagaaggctg 2341 tccttagtac cagattctga gcagggagag gcgatactgc ctcgcatcag cgtgatcagc 2401 actggcccca cgcttcaggc acgaaggagg cagtctgtcc tgaacctgat gacacactca 2461 gttaaccaag gtcagaacat tcaccgaaag acaacagcat ccacacgaaa agtgtcactg 2521 gcccctcagg caaacttgac tgaactggat atatattcaa gaaggttatc tcaagaaact 2581 ggcttggaaa taagtgaaga aattaacgaa gaagacttaa aggagtgcct ttttgatgat 2641 atggagagca taccagcagt gactacatgg aacacatacc ttcgatatat tactgtccac 2701 aagagcttaa tttttgtgct aatttggtgc ttagtaattt ttctggcaga ggtggctgct 2761 tctttggttg tgctgtggct ccttggaaac actcctcttc aagacaaagg gaatagtact 2821 catagtagaa ataacagcta tgcagtgatt atcaccagca ccagttcgta ttatgtgttt 2881 tacatttacg tgggagtagc cgacactttg cttgctatgg gattcttcag aggtctacca 2941 ctggtgcata ctctaatcac agtgtcgaaa attttacacc acaaaatgtt acattctgtt 3001 cttcaagcac ctatgtcaac cctcaacacg ttgaaagcag gtgggattct taatagattc 3061 tccaaagata tagcaatttt ggatgacctt ctgcctctta ccatatttga cttcatccag 3121 ttgttattaa ttgtgattgg agctatagca gttgtcgcag ttttacaacc ctacatcttt 3181 gttgcaacag tgccagtgat agtggctttt attatgttga gagcatattt cctccaaacc 3241 tcacagcaac tcaaacaact ggaatctgaa ggcaggagtc caattttcac tcatcttgtt 3301 acaagcttaa aaggactatg gacacttcgt gccttcggac ggcagcctta ctttgaaact 3361 ctgttccaca aagctctgaa tttacatact gccaactggt tcttgtacct gtcaacactg 3421 cgctggttcc aaatgagaat agaaatgatt tttgtcatct tcttcattgc tgttaccttc

Последовательность нуклеотидов в гене CFTR таблица 4 3481 atttccattt taacaacagg agaaggagaa ggaagagttg gtattatcct gactttagcc 3541 atgaatatca tgagtacatt gcagtgggct gtaaactcca gcatagatgt ggatagcttg 3601 atgcgatctg tgagccgagt ctttaagttc attgacatgc caacagaagg taaacctacc 3661 aagtcaaccatacaa gaatggccaa ctctcgaaag ttatgattat tgagaattca 3721 cacgtgaagatgacat ctggccctca gggggccaaa tgactgtcaa agatctcaca 3781 gcaaaataca cagaaggtgg aaatgccata ttagagaaca tttccttctc aataagtcct 3841 ggccagaggg tgggcctctt gggaagaact ggatcaggga agagtacttt gttatcagct 3901 tttttgagac tactgaacac tgaaggagaa atccagatcg atggtgtgtc ttgggattca 3961 ataactttgc aacagtggag gaaagccttt ggagtgatac cacagaaagt attttt 4021 tctggaacat ttagaaaaaa cttggatccc tatgaacagt ggagtgatca agaaatatgg 4081 aaagttgcag atgaggttgg gctcagatct gtgatagaac agtttcctgg gaagcttgac 4141 tttgtccttg tggatggggg ctgtgtccta agccatggcc acaagcagtt gatgtgcttg 4201 gctagatctg ttctcagtaa ggcgaagatc ttgctgcttg atgaacccag tgctcatttg 4261 gatccagtaa cataccaaat aattagaaga actctaaaac aagcatttgc tgattgcaca 4321 gtaattctct gtgaacacag gatagaagca atgctggaat gccaacaatt tttggtcata 4381 gaagagaaca aagtgcggca gtacgattcc atccagaaac tgctgaacga gaggagcctc

Последовательность нуклеотидов в гене CFTR таблица 5 4441 ttccggcaag ccatcagccc ctccgacagg gtgaagctct ttccccaccg gaactcaagc 4501 aagtgcaagt ctaagcccca gattgctgct ctgaaagagg agacagaaga agaggtgcaa 4561 gatacaaggc tttagagagc agcataaatg ttgacatggg acatttgctc atggaattgg 4621 agctcgtggg acagtcacct catggaattg gagctcgtgg aacagttacc tctgcctcag 4681 aaaacaagga tgaattaagt ttttaa aaaagaaaca tttggtaagg ggaattgagg 4741 acactgatat gggtcttgat aaatggcttc ctggcaatag tcaaattgtg tgaaaggtac 4801 ttcaaatcct tgaagattta ccacttgtgt tttgcaagcc agattttcct gaaaaccctt 4861 gccatgtgct agtaattgga aaggcagctc taaatgtcaa tcagcctagt tgatcagctt 4921 attgtctagt gaaactcgtt aatttgtagt gttggagaag aactgaaatc atacttctta 4981 gggttatgat taagtaatga taactggaaa cttcagcggt ttatataagc ttgtattcct 5041 ttttctctccccatg atgtttagaa acacaactat attgtttgct aagcattcca 5101 actatctcat ttccaagcaa gtattagaat accacaggaa ccacaagact gcacatcaaa 5161 atatgcccca ttcaacatct agtgagcagt caggaaagag aacttccaga tcctggaaat 5221 cagggttagt attgtccagg tctaccaaaa atctcaatat ttcagataat cacaatacat 5281 cccttacctg ggaaagggct gttataatct ttcacagggg acaggatggt tcccttgatg 5341 aagaagttga tatgcctttt cccaactcca gaaagtgaca agctcacaga cctttgaact 5401 agagtttagc tggaaaagta tgttagtgca aattgtcaca ggacagccct tctttccaca 5461 gaagctccag gtagagggtg tgtaagtaga taggccatgg gcactgtggg tagacacaca 5521 tgaagtccaa gcatttagat gtataggttg atggtggtat gttttcaggc tagatgtatg

Последовательность нуклеотидов в гене CFTR таблица 5 5581 tacttcatgc tgtctacact aagagagaat gagagacaca ctgaagaagc accaatcatg 5641 aattagtttt atatgcttct gttttataat tttgtgaagc aaaatttttt ctctaggaaa 5701 tatttt aataatgttt caaacatata ttacaatgct gtattttaaa agaatgatta 5761 tgaattacat ttgtataaaa taatttttat atttgaaata ttgacttttt atggcactag 5821 tatttttatg aaatattatg ttaaaactgg gacaggggag aacctagggt gatattaacc 5881 aggggccatg aatcaccttt tggtctggag ggaagccttg gggctgatcg agttgttgcc 5941 cacagctgta tgattcccagacacag cctcttagat gcagttctga agaagatggt 6001 accaccagtc tgactgtttc catcaagggt acactgcctt ctcaactcca aactgactct 6061 taagaagact gcattatattactgta agaaaatatc acttgtcaat aaaatccata 6121 catttgtgt

AMERICAN COLLEGE OF MEDICAL GENETICS Technical Standards and Guidelines for CFTR Mutation Testing , 2006 Edition . ΔF 508 R 553 X R 1162 X 2184 del. A 3120+1 G>A ΔI 507 G 542 X G 551 D W 1282 X N 1303 K 621+1 G>T R 117 H 1717 -1 G>A A 455 E R 560 T G 85 E R 334 W R 347 P 711+1 G>T 1898+1 G>A 3849+10 kb. C>T 2789+5 G>A 3659 del. C

Наиболее часто встречаемая мутация гена CFTR del 508

Определение точечной мутации в гене CFTR методом секвенирования


Expected Percentage of Abnormal Alleles Detected in Individuals with CFTR Based on the Detection Frequency of the Test Method Used Calculated using Hardy-Weinberg Rule Percentage of Individuals with CF for Mutation Detection Frequency of Test which a Given Number of Abnormal Alleles is Identified Method Two Abnormal Alleles 98% 96% 95% 90% 81% 85% 72% 80% 64% 75% 56% 70% 49% 60% 36% 50% 25% 40% 16% 30% 9%

Схема проведения анализа на биочипе Забор материала (кровь) Выделение ДНК Ассиметричная ПЦР Гибридизация на микрочипе Анализ данных, результат Сканирование

Принцип анализа Метка – Су5 Зонд – одноцепочечный продукт ассиметричной ПЦР Мишень – синтетический олигонуклеотид Стекло

Топология биочипа A B C D E F G H I J K 1 2 • 25 мутантных аллелей и дикий тип в дублях + контроль; • 1 -2 чипа на стекло. 3 4 5 Дикий тип Мутации

Результат анализа A B C D E F G H I J K 1 2 3 4 5 A 1, F 1 – dele 2, 3 (21 kb) A 2, F 2 – G 85 E A 3, F 3 – 621+1 G>T A 4, F 4 – R 334 W A 5, F 5 – R 347 P B 1, G 1 – R 347 H B 2, G 2 – 1078 del. T B 3, G 3 – F 508 del B 4, G 4 – 1677 del. TA B 5, G 5 – I 507 del C 1, H 1 – 1717 -1 G>A C 2, H 2 – G 542 X C 3, H 3 – G 551 D C 4, H 4 – R 553 X C 5, H 5 – 2143 del. T D 1, I 1 – 2183 AA>G D 2, I 2 – 2184 ins. A D 3, I 3 – 2789+5 G>A D 4, I 4 – R 1162 X D 5, I 5 – S 1196 X E 1, J 1 – 3732 del. A E 2, J 2 – 3821 del. T E 3, J 3 – 3849+10 kb. C>T E 4, J 4 – W 1282 X E 5, J 5 – N 1303 K K – контроль

Оборудование для диагностической тест-система «MB 25 -чип»

Информативность прямых методов ДНК диагностики Заболевание Ахондроплазия Хорея Гентингтона Спинальная амиотрофия Невральная амиотрофия Шарко-Мари-Тута Атаксия Фридрейха Фенилкетонурия Адреногенитальный синдром Муковисцедоз Миодистрофия Дюшена/Бекера Болезнь Вильсона-Коновалова Информативность 100% 98% 97% 93% 80% 78% 72% 60% 45%

Сравнительная геномная гибридизация на чипе Array-CGH

Принципы ДНК-чиповой диагностики

Array

Микрочипы Affymetrix

Микрочипы Affymetrix

CGH ARRAY

Соответствие результатов CGH и Fish анализов


Технология общегеномного исследования ассоциаций (Genom Wide Association Stadies –GWAS) Цель – определение сцепления (ассоциаций) однонуклеодитных замен (SNP) с тем или иным заболеванием. Методология исполнения: сочетание молекулярных методов исследования на основе биочипов высокого разрешения (300 -500 тыс. SNP и выше для индивидуальной ДНК) с программами Hap. Map объединяющих информацию о точном положении каждого нуклеотида на физической карте генома человека и клиническим фенотипом болезни. Технология GWAS уверенно становится основной для поиска генов-кандидатов всех моногенных и мультифакторных заболеваний. «К сожалению, эта революционная технология, насколько нам известно, пока недоступна в России (академик РАМН В. С. Баранов, 2009) » .

Исследование выполнено с помощью микрочипа Human. Cyto. SNP-12 на платформе ILLUMINA Чип предназначен для анализа 220 000 SNP

Направления генетических исследований, количество генов и SNP выполняемых фирмой GENEX Название направления Количество нозологических форм болезней, фармпрепаратов, диета и метаболизм 1. Риск развития заболевания 25 заболевания 2. 76 заболеваний 3. Статус носительства наследственных заболеваний Реакция на медикаменты 4. Диета и метаболизм 4. 1. Диета 4. 2. 4. 3. Особенности пищевого поведения Физические упражнения 4. 4. Метаболизм Всего 11 препаратов Количество исследуемых генов SNP 161 генов 76 генов 163 762 12 генов 9 генов 7 генов 15 9 7 11 генов 63 гена 339 генов 11 63 1030

Рецессивные заболевания, включенные в панель Синдром Барттера 4 А типа Синдром Блума Синдром Гурлера (мукополисахаридоз I типа) Синдром Дабина — Джонсона Синдром Криглера-Найяра Синдром слабости синусового узла Синдром Элерса — Данлоса, гиперподвижность суставов Синдром Элерса — Данлоса, дерматоспараксис Синдром Элерса — Данлоса, кифосколиоз Болезнь Гоше Болезнь Канавана Болезнь Краббе Болезнь Сандхоффа Болезнь Тай-Сакса Болезнь фон Виллебранда 2 типа, нормандская Болезнь фон Виллебранда 3 типа Системная карнитиновая недостаточность

Рецессивные заболевания, включенные в панель Гиперлипопротеидемия семейная I типа Гликогенозы (болезнь накопления гликогена) Глютаровая ацидурия Гомоцистинурия cable типа Дефицит 3 -гидрокси-3 -метилглутарил-Ко. А-лиазы Дефицит 3 -метилкротонил-Ко. А-карбоксилазы Дефицит метилентетрагидрофолатредуктазы Классическая гомоцистинурия Лейциноз (болезнь кленового сиропа) Множественный дефицит карбоксилазы Муколипидоз II типа Муколипидоз IV типа

Статус носительства наследственных заболеваний 76 заболеваний , 76 генов, 762 SNP Заболевание 1. Муковисцидоз 1/1500 -2000 1 : 45 2. Боковой амиотрофический склероз 2 -5/100000 1 : 300 3. Фенилкетонурия 1/10000 1 : 50 4. Нейросенсорная тугоухость 1 / 25000 1 : 150 5. Анемия Фанкони 1 : 100 6. Галоктоземия 7. Болезнь Гоше 1 / 40 000 1 : 250 8. Недостаточность галоктокиназы 1 / 80000 1 : 80— 130 9. Синдром Элерса-Данлоса (гиперподвижность суставов) 10. Классическая гомоцистинурия Заболеваемость Носительство 1 / 40 000 - 100 000 1 : 200 -300 1 / 10 000 - 15 000 1 : 60 1 / 200000 1 : 400 -450 11. Бета-талассемия 1 / 250 1 : 100 12. Болезнь Ниммана-Пика 1 / 100 1 : 25

Перечень жизнеугрожающих и хронических прогрессирующих орфанных заболеваний, приводящих к сокращению продолжительности жизни или к инвалидности. № Наименование заболевания МКБ-10 1. Гемолитико-уремический синдром 2. Пароксизмальная ночная гемоглобинурия 3. Идиопатическая тромбоцитопеническая пурпура (синдром Эванса) 4. Классическая фенилкетонурия D 59. 3 13. Глютарикацидурия Е 72. 3 D 59. 5 14. Гиперлизинемия Е 72. 3 D 69. 3 I 27. 0 5. Другие виды гиперфенилаланинемии 6. Тирозинемия Е 70. 1 15. Легочная (артериальная) гипертензия (идиопатическая) (первичная) 16. Недостаточность галактокиназы 17. Галактоземия Е 70. 2 18. Болезнь Фабри E 75. 2 7. Нарушения обмена гистидина E 70. 8 19. Болезнь Нимана-Пика E 75. 2 8. Болезнь «кленового сиропа» Е 71. 0 20. Мукополисахаридоз, тип I Е 76. 0 9. Изовалериановая ацидемия Е 71. 1 21. Мукополисахаридоз, тип II Е 76. 1 10 Метилмалоновая ацидемия Е 71. 1 22. Мукополисахаридоз, тип VI Е 76. 2 11. Пропионовая ацидемия Е 71. 1 Е 83. 0 12. Гомоцистинурия Е 72. 1 23 Нарушения обмена меди (Болезнь Вильсона) 24. Болезнь Помпе Е 70. 0 E 74. 2 E 74. 0

Проведен анализ встречаемости генов 76 рецессивных заболеваний у 143 человек, проживающих в центральном регионе РФ. Женщин – 77, мужчин – 66. Всего выполнено исследование 108966 мутации.

При исследовании носительства генов 76 рецессивных заболеваний выявлены гены 26 заболеваний


Частота носительства генов рецессивных моногенных заболеваний, включенных в неонатальный скрининг и в перечень жизнеугрожающих и прогрессирующих орфанных заболеваний Заболевание 1. Муковисцидоз Число наблюдений Частота носительства Типы мутаций 6 1 : 25 3 - del 508 3 - I 148 T Изолейцин - треонин 2. Галактоземия 29 1 : 5 N 314 D L 218 L 3. Классическая гомоцистинурия Фенилкетонурия 4 1 : 35 R 369 C 1 < 1 : 143 R 408 W Болезнь Нимана. Пика 1 < 1 : 143 R 496 L 4. 5.

AMERICAN COLLEGE OF MEDICAL GENETICS Technical Standards and Guidelines for CFTR Mutation Testing 2006 Edition. Reviewed and Revised: 2005 by the Molecular Subcommittee of the Laboratory Quality Assurance Committee Minimum Mutation Panel for Population-Based Carrier Screening Purposes: 1 ΔF 508 R 553 X R 1162 X 2184 del. A 3120+1 G>A ΔI 507 G 542 X G 551 D W 1282 X N 1303 K 621+1 G>T R 117 H 1717 -1 G>A A 455 E R 560 T G 85 E R 334 W R 347 P 711+1 G>T 1898+1 G>A 3849+10 kb. C>T 2789+5 G>A 3659 del. C

Точки мутаций определяемые при диагностировании носительства муковисцидоза по программе GENEX ГЕН CFTR 1078 del. T, 1677 del. TA, 1717 -1 G>A, 1812 -1 G>A, 1898+1 G>A, 1949 del 84, 2043 del. G, 2055 del 9>A, 2105 del 13 ins 5, 2108 del. A, 2307 ins. A, 2869 ins. G, 3120 G>A, 3171 del. C, 3272 -26 A>G, 3659 del. C, 3667 ins 4, 3791 del. C, 3849+10 k. C>T, 3876 del. A, 3905 ins. T, 394 del. TT, 405+1 G>A, 405+3 A>C, 444 del. A, 574 del. A, 621+1 G>T, 663 del. T, 711+1 G>T, 712 -1 G>T, 846 del. T, 935 del. A, A 455 E, A 561 E, C 524 X, D 1152 H, del. F 311, del. F 508, G 1349 D, G 178 R, G 330 X, G 551 D, G 622 D, G 85 E, I 148 T, K 710 X, L 206 W, L 558 S, M 1101 K, N 1303 K, P 205 S, P 574 H, P 750 L, Q 1100 P, Q 1238 X, Q 359 K/T 360 K, Q 493 X, R 1158 X, R 1162 X, R 117 H, R 334 W, R 347 P, R 352 Q, R 709 X, S 1196 X, S 1251 N, S 364 P, S 549 N, S 549 R(A>C), S 5549 R(T>G), V 232 D, V 520 F/I, W 1089 X, W 1204 X, W 1282 X, Y 122 X

Выявленные гены рецессивных заболеваний Заболевание Число наблюдений 10 Частота носительства 1 : 15 1. Биотинидазная недостаточность 2. Несиндромальнная потеря слуха 6 1 : 25 3. Болезнь Тай-Сакса 4 1 : 35 4. Rh-null синдром 6 1 : 25 5. Болезнь фон Виллебранта 3 1 : 50 6. Наследственный сфероцитоз 4 1 : 35 7. Синдром Гурлера 3 1 : 50 8. 9. Дифицит корот. ацил Ко. А дегидрогеназ Болезни Гоше 2 2 1 : 75 10. Глутаровая ацидемии 1 типа 1 < 1 : 143 11. Поликистоз почек 1 < 1 : 143 12. Недостаточность 3 метилкротонил Ко. А кокарбоксилазы

Примеры носительства генов рецессивных заболеваний Пациент С. , 29 лет, женщина 1. Этилмалоновая ацидурия – 625 G>A в ACADS 2. Гемохроматоз - H 63 D в HFE 3. Недостаточность MTGFR – A 1298 C и C 677 T 4. Болезнь Сандхоффа - S 62 L в HEXB 5. Болезнь Тай-Сакса - ins 12+1 G>C в HEXA Пациент Б. , 35 лет, мужчина 1. Муковисцидоз - I 148 Tв CFTR 2. Галактоземия – N 314 D в GALT 3. Несиндромная наследственная потеря слуха типа DFNB 1 и DFNB 9 - 35 del. G GJB 2 4. Гемохроматоз - H 63 D в HFE 5. Недостаточность MTGFR - A 1298 C и A 1298 C 6. Болезнь Сандхоффа - S 62 L в HEXB

Примеры носительства генов рецессивных заболеваний Пациент М. , 41 год, мужчина 1. Семейная средизем. лихорадка – K 695 R в MEFV 2. Галактоземия – N 314 D в GALT 3. Несиндромная наследственная потеря слуха типа DFNB 1 и DFNB 9 - 35 del. G GJB 2 4. Болезнь Краббе - R 168 C в GALC 5. Недостаточность MTGFR - A 1298 C в MTGFR Пациент П. , 12 лет, мужчина 1. Недостаточность кортикостерон метил оксидазы - V 386 A в CYP 11 B 2 2. Этилмалоновая ацидурия - 625 G>A в ACADS 3. Семейная средиземноморская лихорадка - A 744 S в MEFV 4. Гемохроматоз - C 282 Y в HFE 5. Болезнь Краббе - R 168 C в GALC 6. Недостаточность MTGFR - C 677 T в MTGFR 7. Наследственный сфероцитоз - V 463 I в ANK 1

Примеры носительства генов рецессивных заболеваний Пациент Б. , 45 лет, мужчина 1. Этилмалоновая ацидурия - 2 копии 625 G>A в ACADS 2. Недостаточность MTGFR - 2 копии C 677 T 3. Муковисцидоз - I 148 T в CFTR 4. Церобросухожильный ксантоматоз - P 384 L в CYP 27 A 1 Пациент Р. , 41 год, женщина 1. Этилмалоновая ацидурия - 2 копии 625 G>A в ACADS 2. Галактоземия - N 314 D и L 218 L в GALT 3. Дефицит MTGFR - E 429 A + A 222 V + R 594 Q, 4. Несиндромная наследственная потеря слуха типа DFNB 1 и DFNB 9 - 35 del. G GJB 2

Риск развития полигенного (мультифакторного) заболевания 25 заболевания 161 генов 163 SNP

25 мультифакторных заболевания N Нозология 1. Возрастная макулярная дегенерация 14. Рак легкого 2. Болезнь Альцгеймера с поздним началом 15. Заболевания периферических артерий 3. Боковой амиотрофический склероз 16. Меланома 4. Бронхиальная астма 17. Рассеянный склероз 5. Мерцательная аритмия 18. Инфаркт миокарда 6. Рак молочной железы 19. Ожирение 7. Колоректальный рак 20. Остеоартрит 8. Ишемическая болезнь сердца 21. Псориаз 9. Сахарный диабет 1 типа 22. Рак предстательной железы 10. Сахарный диабет 2 типа 23. Ревматоидный артрит 11. Артериальная гипертензия 24. Системная красная волчанка 12. Хронический лимфоцитарный лейкоз 25. Язвенный колит 13. Эксфолиативная глаукома

Гены предрасположенности – это аллельные варианты (мутантные варианты) генов, которые совместимы с жизнью, но при определенных неблагоприятных условиях способствуют развитию того или иного заболевания.

Риск возникновения заболеваний Риск развития возрастной макулярной дегенерации Популяционный риск 12/100 (США). В России заболеваемость ВМД составляет более 15 на 1000 населения. Распространённость увеличивается с возрастом: 1, 6% - в возрасте 52– 64 лет, 11% - возрасте 65– 74 лет, 27, 9% - старше 75 лет. Преобладающий пол — женский.

Сочетание аллельных вариантов генов ARMS 2 and CFH и риск развития возрастной макулярной дегенерации (ВМД) при анализе 1119 случаев и 922 контролей. CFH Y 402 H контроли случаи OR (95% ДИ) ARMS 2 rs 10490924 TT TC CC GG 223 295 73 61 178 145 1 2. 03 7. 10 (1. 61, 2. 56) (5. 33, 9. 46) 103 149 36 84 225 196 2. 85 5. 79 20. 24 (2. 45, 3. 31) (4. 36, 7. 68) (14. 42, 28. 31) 19 21 3 46 105 79 8. 11 16. 46 57. 58 (6. 01, 10. 94) (11. 14, 24. 27) (37. 24, 89. 00) GT TT

Частота встречаемости аллельных вариантов (полиморфизмов) гена CFH (Y 402 H ) и риск развития возрастной макулярной дегенерации (ВМД) Когорта Фенотип и количество наблюдений Аллельные варианты CT/TT TT CT CC 214 327 CC /TT OR 95% ДИ 70 1. 76 (1. 35, 2. 28) 6. 43 (4. 58, 9. 01) 7. 37 (4. 72, 11. 50) 6. 72 (5. 14, 8. 79) Собственное Контроли (594) исследование ВМД (759) 137 Контроли (328) Второе исследование ВМД (361) Объединенная Контроли (922) когорта ВМД (1120) 368 288 141 148 46 62 149 2. 49 (1. 72, 3. 61) 355 475 116 1. 99 (1. 61, 2. 46) 199 530 437

Частота встречаемости аллельных вариантов (полиморфизмов) rs 10490924 гена ARMS 2 и риск развития возрастной макулярной дегенерации (ВМД) Hum. Mol. Genet. (1 November 2005) 14 (21): 3227 -3236; PMID: 16174643 Когорта Фенотип и количество наблюдений Контроли Собственное 594 исследование ВМД 759 Контроли 328 Второе исследование ВМД 361 Контроли 922 Объединен. ВМД ная когорта 1120 Аллельные варианты GG GT TT 388 179 GT относительно GG TT относительно GG OR 95% ДИ OR 95% ДИ 2. 82 (2. 23, 3. 58) 7. 61 (4. 90, 11. 82) 2. 48 (1. 78, 3. 47) 9. 54 (5. 35, 17. 03) 2. 69 (2. 22, 3. 27) 8. 21 (5. 79, 11. 65) 27 268 349 142 203 109 16 117 156 88 591 288 43 385 505 230

Наследственные опухоли Генеалогия Наполеона
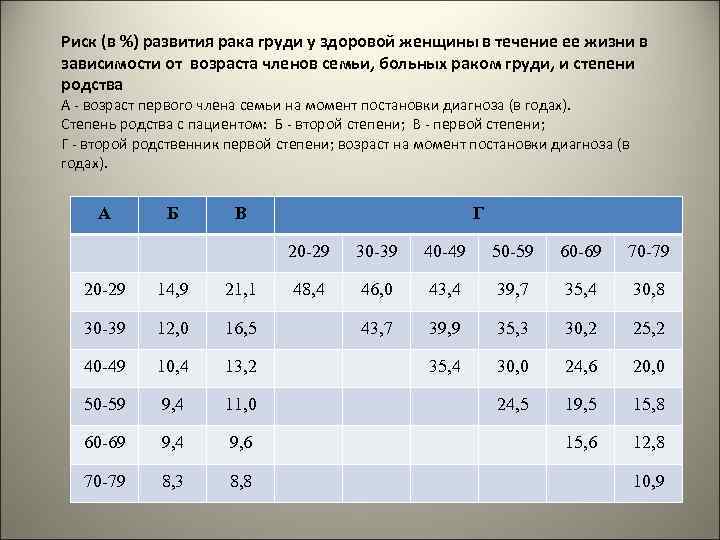
Риск (в %) развития рака груди у здоровой женщины в течение ее жизни в зависимости от возраста членов семьи, больных раком груди, и степени родства A - возраст первого члена семьи на момент постановки диагноза (в годах). Степень родства с пациентом: Б - второй степени; В - первой степени; Г - второй родственник первой степени; возраст на момент постановки диагноза (в годах). А Б В Г 20 -29 30 -39 40 -49 50 -59 60 -69 70 -79 48, 4 46, 0 43, 4 39, 7 35, 4 30, 8 43, 7 39, 9 35, 3 30, 2 25, 2 35, 4 30, 0 24, 6 20, 0 24, 5 19, 5 15, 8 15, 6 12, 8 20 -29 14, 9 21, 1 30 -39 12, 0 16, 5 40 -49 10, 4 13, 2 50 -59 9, 4 11, 0 60 -69 9, 4 9, 6 70 -79 8, 3 8, 8 10, 9

Встречаемость генетически детерминированных и спорадических случаев опухолей на примере рака молочной железы

Риск развития РМЖ Ген Название 1. CHEK 2 checkpoint homolog (S. pombe) Аллель, мутация 1100 del. C Источник ОР для гомо. 15122511 2. ESR 1 estrogen receptor 1 А 2. 7 4. 8 1, 59 3. fibroblast growth factor receptor 2 Г 1, 64 17529973 Межгенная точка (предполагаемый эффект - transcriptional regulation) Межгенная точка А 1, 24 19567422 Г 1. 21 18577746 6. FGFR 2 Intergen rs 13387042 Intergen rs 13281615 MRPS 30 mitochondrial ribosomal protein S 30 Г 1. 27 18438407 7. TNRC 9 Т 1. 44 17529974 8. AKAP 9 T 1. 27 18334708 9. LSP 1 trinucleotide repeat-containing gene 9 protein A kinase (PRKA) anchor protein (yotiao) 9 lymphocyte-specific protein 1 T 1. 25 21127985 10. MAP 3 K 1 PALB 2 mitogen-activated protein kinase 1 partner and localizer of BRCA 2 Ц 1, 22 2. 3 20809358 4. 5. 11. 1592 del. T 18172190 19219042 21285249

Объем исследований при оценке генетической предрасположенности развития РМЖ Ген CASP 8 CHEK 2 ESR 1 In_genic_2 q 35 In_genic_8 q 24 TNRC 9 MRPS 30 AKAP 9 LSP 1 MAP 3 K 1 Объем выборки 18, 290 cases and 22, 670 controls from 15 studies 12, 439 cases, 13, 253 control 10, 860 cases and 9, 065 controls from 10 studies meta-analyses of 26, 000 cases and 27, 000 control 3, 472 cases and 900 controls 4, 554 case and 17, 577 controls subjects 2270 case and 2280 control subjects 4, 554 case subjects and 17, 577 controls 6, 145 cases and 33, 016 controls 1110 case and 1131 controls и 9523 case and 13770 controls from 6 studies 21, 860 cases and 22, 578 controls 33, 920 cases and 35, 671 controls. 21, 860 cases and 22, 578 controls 26, 015 cases and 33, 962 controls PMID 17293864 19629679 15122511 18172190 19219042 17529974 18577746 17529974 18438407 18334708 17529967 21127985 17529967 20809358

Основные направления использования молекулярных методов в онкологии • ДНК-диагностику наследственных форм рака. • ДНК-диагностику спорадических форм рака. • Определение микрометастазов. • ДНК-диагностику биологических канцерогенов (HPV 16 и 18 типов, ВЭБ-инфекции, HBV и HCV, ретровирусы и т. п. ). • Доклиническую диагностику опухолей (определение онкогенов и мутаций супрессоров)). • Таргентная терапия

Суммарный (кумулятивный ) генетический риск при наличии нескольких негативных аллелей. Alan M. Pittman et al. (2008), метод GWAS, платформ Illumina 550 K аrray Изучены SNP: rs 6983267**, rs 16892766**, rs 10795668**, rs 3802842**, rs 4779584, rs 12953717. Обследовано : 2863 больных колоректальным раком 2818 здоровых лиц - контрольная группа Установлено: каждый SNP независимо увеличивает ОР возникновения заболевания; сочетание негативных аллелей увеличивает суммарный риск более значимо, чем просто сумма ОР каждого их аллелей; сочетание 7 маркеров увеличивает общий ОР более 5, 0.


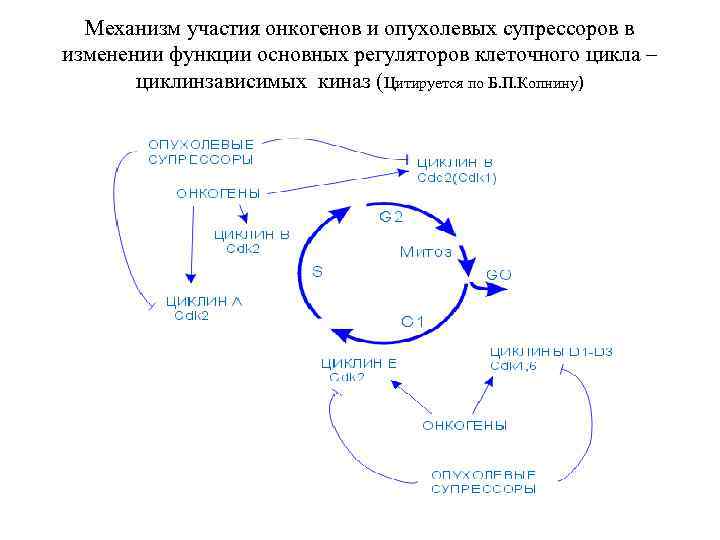
Механизм участия онкогенов и опухолевых супрессоров в изменении функции основных регуляторов клеточного цикла – циклинзависимых киназ (Цитируется по Б. П. Копнину)


Самостоятельные генетические риски при заболеваниях ассоциированные с СД N Нозология Гены 1. Ишемическая болезнь HNF 1 A, MRAS, MTHFD 1 L, CDH 13, SEZ 6 L, сердца SMAD 3, Intergenic rs 501120, 3008621, 1333049, 2943634, 383830, 17411031 2. Инфаркт миокарда CXCL 12, MIA 3, PCSK 9, PHACTR 1, SH 2 B 3, WDR 12, OR 13 G 1, PRR 4, Intergenic rs 646776, 9982601, 10757278 3. Ожирение FTO, MC 4 R, INSIG 2, PCSK 1 4. Заболевания периферических артерий CHRNA 3 5. Артериальная гипертензия BCAT 1, PRARGCIA

СЛАЙД № 64 Биохимические методы В НАЧАЛО НАЗАД ДАЛЕЕ В КОНЕЦ

СЛАЙД № 66 Неонатальный скрининг на некоторые НБО В США, Канаде и большинстве развитых стран новорожденным в первые несколько суток жизни проводят обследования на наследственные нарушения обмена веществ: врожденный гипотиреоз, фенилкетонурию, галактоземию, дефицит галактокиназы, болезнь кленового сиропа, гомоцистинурию и дефицит биотинидазы. Постановлением Правительства РФ от 31 декабря 2005 г. № 870 "Об обеспечении государственных и муниципальных учреждений здравоохранения в 2006 году за счет средств федерального бюджета диагностическими средствами и антиретровирусными препаратами в целях профилактики, выявления и лечения лиц, инфицированных вирусами иммунодефицита человека и гепатитов В и С, оборудованием и расходными материалами для неонатального скрининга”. Дополнительно к уже проводящемуся неонатальному скринингу на фенилкетонурию и гипотиреоз в программу с 2006 года введены скрининги на: • Адреногенитальный синдром; • Муковисцидоз (кистозный фиброз); В НАЧАЛО ДАЛЕЕ НАЗАД В КОНЕЦ • Галактоземию. Г 20 Г 21 Г 22 Г 23 Г 24

СЛАЙД № 67 Частота ложноположительных результатов при скрининге Harvey L. Levy and Simone Albers Аnnu. Rev. Genomics Hum. Genet. , 2000, 01: 139 -177 Нарушение Показатель Частота встречаемости Доля в % Врожденная гиперплазия надпочечников 17 оксипрогестерон Носительство 1: 100 Заболевание 1: 15000 0. 2 - 0. 5 Врожденный гипотиреоз Тироксин/ТТГ Заболевание 1: 2000 0. 04 - 0. 5 Галактоземия Галактоза/GALT* Заболевание 1: 62 000 Фенилкетонурия Фенилаланин Носительство 1: 70, Заболевание 1: 3000 0. 03 - 0. 1 Кистофиброз (муковисцидоз) IRT ** Носительство 1: 40, Заболевание 1: 2000 0. 2 - 1. 0 *GALT - галактозо-1 -фосфат уридилтрансфераза ** IRT - иммунореактивный трипсиноген В НАЧАЛО НАЗАД 0. 05 - 0. 7 ДАЛЕЕ В КОНЕЦ

Биохимические методы диагностики наследственных болезней обмена веществ (НБО) СЛАЙД № 65 К наследственным болезням обмена веществ (НБО) - моногенно наследующихся заболеваний (более 700 нозологических единиц), обусловленных мутациями генов, под контролем которых осуществляется синтез белков, которые выполняют различные функции в организме – ферментного катализа, структурные, транспортные. Суммарная частота довольно высока и составляет примерно 1: 1000. Маркерами НБО являются биохимические признаки, поэтому биохимические методы, включающие энзимодиагностику и количественное определение метаболитов, играют важнейшую роль в диагностике этих заболеваний. Диагностика НБО включает несколько этапов: 1. Выявление дефектного звена метаболического пути посредством анализа Г 17 (количественного, полуколичественного или качественного) соответствующих метаболитов; Г 18 2. Выявление дисфункции белка посредством оценки его количества и/или активности; Такая программа используется не только для решения научных проблем, касающихся изучения молекулярных механизмов патогенеза НБО и выявления гено-фенотипических Г 19 корреляций. Она необходима прежде всего для практической диагностики НБО. Верифицировать диагноз на уровне белка и/или мутантного гена необходимо как для проведения пренатальной диагностики, медико-генетического консультирования, так и в ряде случаев для назначения адекватной терапии. В НАЧАЛО НАЗАД ДАЛЕЕ В КОНЕЦ

ГИПЕРССЫЛКА № 17 I. Этап исследования метаболитов Оценка метаболитов в биологических жидкостях – необходимый этап диагностики аминоацидопатий, органических ацидурий, мукополисахаридозов, митохондриальных и пероксисомных болезней, дефектов метаболизма пуринов и пиримидинов и т. д. Для этих целей используются методы качественного химического анализа, спектрофотометрические методы количественной оценки соединений, а также различные виды хроматографии – тонкослойную хроматографию (ТСХ), высокоэффективную жидкостную хроматографию (ВЭЖХ), газовую хроматографию (ГХ), масс-спектрометрию (ХМС). Хроматографические методы анализа позволяют эффективно разделить сложные многокомпонентные смеси, к которым в том числе относится и биологический материал. Биологическим материалом для этих исследований обычно служит плазма или сыворотка крови и образцы мочи. При некоторых заболеваниях для постановки диагноза необходимо исследование цереброспинальной жидкости (например, некетотической гиперглицинемии). ВЫХОД ИЗ ГИПЕРССЫЛКИ

Качественные тесты с мочой Определяют избыточную концентрацию субстратов или их производных, накапливающихся при наследственных болезнях обмена. Цвет и запах: лейциноз, тирозинемия, изовалериановая ацидемия, ФКУ, алькаптонурия, цистинурия, 3 -гидрокси-3 -метилглутаровая ацидурия Тест Бенидикта: галактоземия, врождённая непереносимость фруктозы, алкаптонурия. Также положителен при синдроме Фанкони, диабете, лактазной недостаточности, приёме антибиотиков Тест с хлоридом железа: ФКУ, лейциноз, гиперглицинемия, алкаптонурия, тирозинемия, гистидинемия. Также положителен при циррозе, плеохромацитоме, гипербиллирубинемии, лактат ацидозе, кетоацидозе, меланоме Тест с динитрофенилгидразином (ДНФГ): ФКУ, лейциноз, гиперглицинемия, алкаптонурия, гликогенозы, лактат ацидозе Тест с п-нитроанилином: метилмалоновая ацидурия Сульфитный тест: недостаточность молибденового кофактора Тест на гомогентизиновую кислоту: алкаптонурия Тест с нитрозонафтолом: тирозинемия. Также положителен при фруктоземии и галактоземии Полуколичественные тесты с мочой Тест на пролин: пролинемия I и II, иминоглицинурия Тест с цианид-нитропруссидом: гомоцистинурия, цистинурия ЦПХ-тест: мукополисахаридозы

Методы ВЭЖХ ГИПЕРССЫЛКА № 17. 4. 1 Аминоацидопатии До середины 80 -х гг. анализ проводился с помощью аминокислотного анализатора, который до настоящего времени не утратил своего значения и является ни чем иным, как полностью автоматизированной ВЭЖХ с ионообменной колонкой. Для дифференциальной диагностики ФКУ методом ВЭЖХ определяется количество птеринов и их производных в моче. При классической форме ФКУ повышается уровень общих птеринов, но содержание биоптерина и тетрагидробиоптерина не отличается от нормальных значений. При недостаточности дегидроптеринредуктазы наблюдается резкое снижение или отсутствие тетрагидробиоптерина и увеличение концентрации биоптерина. В случае недостаточности биоптеринсинтетазы значительно снижается или отсутствует тетрагидробиоптерин и всегда полностью отсутствует биоптерин. Болезни пуринового и пиримидинового обмена ВЭЖХ является эффективным методом, позволяющим диагностировать этот класс наследственных болезней обмена. Так, например, при анализе плазмы, мочи и спиномозговой жидкости пациентов с недостаточностью дегидротиминдигидрогеназы наблюдается значительное повышение уровня урацила и тимина. Болезни углеводного обмена С помощью ВЭЖХ определяется количество моно- и дисахаридов в моче в виде соответствующих дансильных производных; варьируя при хроматографии состав подвижной фазы, добиваются хорошего разделения маннозы, галактозы и фруктозы. Эндокринопатии При диагностике гипотериоза анализируется концентрация тироидных гормонов с помощью ВЭЖХ. Определение количества 17 α-оксипрогестерона методом ВЭЖХ является эффективным методом диагностики ВГКН. ВЫХОД ИЗ ГИПЕРССЫЛКИ

ГИПЕРССЫЛКА № 17. 4. 2 Методы газовой хроматографии Одним из типичных примеров использования ГХ является диагностика пероксисомных болезней (ПБ). Для проведения хроматографического анализа искомые соединения превращаются в соответствующие метиловые или триметилсилиловые эфиры. Эти соединения и анализируются ГХ. В таблице приведён один из вариантов классификации ПБ и перечень диагностически значимых биохимических маркеров (ОДЦЖК, желчные кислоты, фитановая и пристановая кислоты, плазмалогены) для каждого заболевания. В ряде случаев также определяется уровень пипеколиновой кислоты (продукта катаболизма Lлизина в мозге), но повышение количества этого соединения наблюдается при заболеваниях, не относящихся к группе ПБ. Метод ХМС широко используется в диагностике органических ацидурий. Применяя этот хроматографический метод, можно количественно измерить более 100 различных соединений, экскретируемых с мочой. ВЫХОД ИЗ ГИПЕРССЫЛКИ

ГИПЕРССЫЛКА № 17. 4. 2. 1 Биохимические маркеры пероксисомных болезней ОДЦЖК Фитановая кислота Пипеколиновая кислота ДГХК, ТГХК Плазмалогены Синдром Цельвегера + + + Неонатальная адренолейкодистрофия + + + Х-сцепленная адренолейкодистрофия + - - Псевдо-неонатальная адренолейкодистрофия + - - Цельвегер-подобный синдром + - - + - Синдром псевдо-Цельвегера + - - + - Инфантильная форма болезни Рефсума + + + Гиперпипеколиновая ацидемия + + + - + Недостаточность бифункционального белка + - - + - Болезнь Рефсума - + - - - Ризомелическая точечная остеохондродисплазия - + - - + Неризомелический тип точечной хондродисплазии - + - - + Акаталазия - - - Первичная гипероксалурия, тип 1 - - - Ди- и тригидроксихолестанемия - -+ - Атипичная рибофлавинзависимая глутаровая ацидурия - - - Нозологическая форма ПБ ВЫХОД ИЗ ГИПЕРССЫЛКИ

ГИПЕРССЫЛКА № 17. 4. 3 Тандемная масс-спектрометрия • Принцип метода - оценка соотношения положительного и отрицательного заряда молекулы к ее массе. • ТМС - тандемная масс-спектрометрия – позволяет охарактеризовать структуру, молекулярную массу и провести количественную оценку 3000 соединений одновременно. При этом не требуется длительной подготовки проб для проведения анализа (как, например, для ГХ), а время исследования занимает несколько минут. • В мировой практике здравоохранения этот метод используют для проведения массового скрининга новорожденных на наследственные болезни обмена веществ (НБО). • Нозологические формы НБО, которые можно диагностировать с использованием ТМС, приведены в таблице. ВЫХОД ИЗ ГИПЕРССЫЛКИ

ГИПЕРССЫЛКА № 17. 4. 3. 1 Заболевания, диагностируемые с помощью тандемной массспектрометрии (ТМС) Нозологическая форма Частота Органические ацидурии Глутаровая ацидурия, тип 1 1: 30000 Глутаровая ацидурия, тип 2 ? Пропионовая ацидемия 1: 50000 Метилмалоновая ацидурия 1: 48000 Изовалериановая ацидурия 1: 50000 Аминоацидопатии Лейциноз 1: 185000 ФКУ 1: 8000 Тирозинемия, тип 1 1: 100000 Некетотическая гиперглицинемия 1: 55000 Цитрулинемия 1: 250000 Дефекты β-окисления Недостаточность короткоцепочечной ацил-Ко. А-дегидрогеназы ЖК ? Недостаточность среднецепочечной ацил-Ко. А-дегидрогеназы ЖК 1: 8000 Недостаточность очень длинноцепочечной ацил-Ко. А-дегидрогеназы ЖК ? Недостаточность длинноцепочечной 3 -гидроксиацил-Ко. А-дегидрогеназы ЖК ? Недостаточность 2, 4 -диеноил-Ко. А-редуктазы ? Недостаточность карнитинпальмитоилтрансферазы I, II ? ВЫХОД ИЗ ГИПЕРССЫЛКИ

НБО, диагностируемые с применением ГХ, ВЭЖХ и ТМС Класс НБО ГИПЕРССЫЛКА № 17. 4. 4 Определяемые метаболиты Хроматографический метод Аминокислотный анализатор, ВЭЖК Амипоацидопатии Аминокислоты, птеридины Митохондриальные болезни Лактат, пируват, 3 -гидрокси-бутират, ацетоацетат Органические ацидурии Органические кислоты Болезни пуринового и пиримидинового обмена Пурины, пиримидины, мочевая кислота ВЭЖК Болезни углеводного обмена Моно- и дисахариды ВЭЖК Лизосомные болезни Олигосахариды ВЭЖК Нарушения митохондриального βокисления Карнитин и его эфиры, разветвлённые и неразветвлённые дикарбоновые кислоты от С 6 до С 14 Пероксисомные болезни 0 ДЦЖК, фитановая кислота, желчные кислоты, плазмалогены, пипеколиновая кислота Болезни обмена металлов Ионы металлов, сульфатов, аминокислот ВЭЖК Наследственные болезни транспорта метаболитов Сиаловые кислоты, хлориды, сахара ВЭЖК Наследственные болезни ЖКТ Моно- и дисахариды ВЭЖК Болезни холестеринового обмена Холестерин и его производные, триацилглицериды Болезни обмена нейротрансмиттеров Катехоламины, аминокислоты ВЭЖК Болезни обмена гема и порфиринов Порфирины ВЭЖК Наследственные эндокринопатии Стероидные и тироидные гормоны ВЭЖК ВЫХОД ИЗ ГИПЕРССЫЛКИ ВЭЖК ГХ, ХМС, ВЭЖК ГХ, ХМС





Ten Most Common CFTR Mutations in Caucasians with Related Phenotypic Expression Mutation Relative Frequency Mutation Functional Class 1 ΔF 508 66. 0% II G 542 X 2. 4% I G 551 D 1. 6% III N 1303 Lys 1. 3% II W 1282 X 1. 2% I R 553 X 0. 7% I 621+1 G>T 0. 7% I 1717 -1 G>A 0. 6% I R 117 H 0. 3% IV Non-classic R 1162 X 0. 3% Not clear 4 Classic Phenotype 2 Classic 3

ФКУ - Характеризующаяся недостатком фермента, приводящим к блокированию гидроксилирования фенилаланина и превращения его в тирозин. Средняя частота встречаемости около 1 случая на 10 000 детей. наследуется по аутосомно-рецессивному типу, оба пола поражаются с одинаковой частотой. Средняя частота гетерозиготности по ФКУ составляет 1: 70. Ген ФАГ человека локализован на длинном плече 12 хромосомы в сегменте 12 q 22 - 12 q 24. 1, состав 13 экзонов, протяженностью 90000 пар оснований. Протяженность экзонов колеблется от 57 пар нуклеотидов (9 -ый экзон) до 892 нуклеотидов (13 -ый экзон). ( Lidsky A. S. , 1984 ; Lidsky A. S. , 1985, Di. Lella A. G. , 1986 ). В настоящее время в гене ФАГ человека зарегистрировано свыше 170 мутаций ( Scriver C. R. , 1995 ). Диагностика – определение фенилаланина в крови на 2 -5 день. • ВГТ Популяционная частота составляет 1: 3000 • Адрено-генитальный синдром. Врожденная гиперплазия надпочечников (Congenital Adrenal Hyperplasia - CAH) - аутосомно-рецессивное эндокринное заболевание с частотой 1: 15000. • • Кистозный фиброз (CF) - аутосомно-рецессивное заболевание с частотой от 1: 2000 до 1: 3000 Галактоземия Три генетически детерминированные ферментативных дефекта приводят к нарушению метаболизме галактозы: галактокиназы (GALK), галактозо-1 -фосфат-уридилтрансферазы (GALT), и уридин-дифосфат-галактозо-4 -эпимеразы. Классическая галактоземия, наиболее тяжелая форма нарушения метаболизма галактозы, вызывается дефицитом GALT, который ведет к накоплению галактозы и галактозо-1 -фосфатов. Ген GALT клонирован и хорошо изучен. Выявлено более 130 различных мутаций связанных с галактоземией. Наиболее часто встречающиеся мутации: Q 188 R примерно у 70% пациентов; Q 188 R, K 285 N, S 135 L, N 314 D, L 195 P, Y 209 C – 87, 5% -87. 5% мутантных аллелей у детей с галактоземией Средняя частота 1: 62 000 (Levy HL, Hammersen G. 1978).

Строение гена PHOX 2 B и типы мутаций при синдроме Ундины (Congenital Central Hypoventilation Syndrome)

Мутации гена PHOX 2 B и изменения активности регуляторного домена белка
Главная версия от 09_02_12.ppt