Лабораторная № 1 Правила работы и основные методы












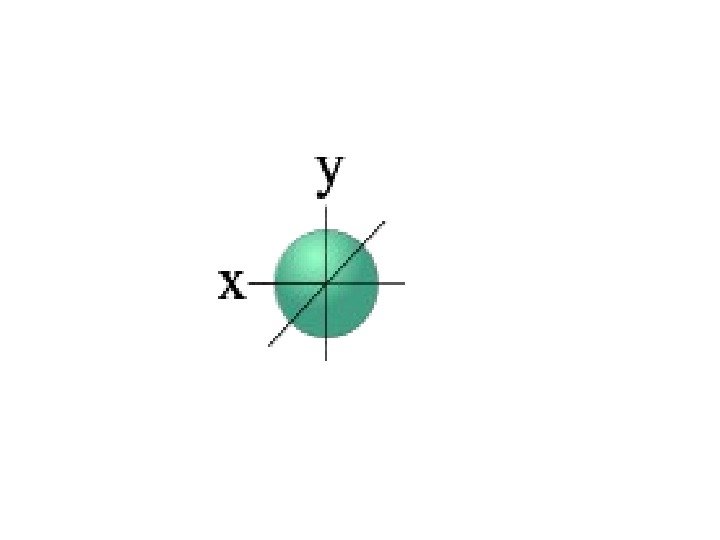

















lr_№1_pravila_raboty_v_laboratorii.ppt
- Размер: 201.0 Кб
- Автор:
- Количество слайдов: 31
Описание презентации Лабораторная № 1 Правила работы и основные методы по слайдам
 Лабораторная № 1 Правила работы и основные методы исследований в химической лаборатории
Лабораторная № 1 Правила работы и основные методы исследований в химической лаборатории
 Практическая часть Правила работы в химической лаборатории
Практическая часть Правила работы в химической лаборатории
 Цель • Сформировать представления о правилах и методах работы в химической лаборатории • Задачи – Научиться методам безопасной работы в лаборатории – Научиться пользоваться оборудованием химической лаборатории
Цель • Сформировать представления о правилах и методах работы в химической лаборатории • Задачи – Научиться методам безопасной работы в лаборатории – Научиться пользоваться оборудованием химической лаборатории
 • Работать в лаборатории необходимо в халате, защищая одежду и кожу от попадания и разъедания реактивами и обсемененности микроорганизмами. • Каждый должен работать на закрепленном за ним рабочем месте. Переход на другое место без разрешения преподавателя не допускается. • Рабочее место следует поддерживать в чистоте, не загромождать его посудой и побочными вещами. • Студентам запрещается работать в лаборатории без присутствия преподавателя или лаборанта, а также в неустановленное время без разрешения преподавателя. • До выполнения каждой лабораторной работы можно приступить только после получения инструктажа по технике безопасности и разрешения преподавателя. • Приступая к работе, необходимо: осознать методику работы, правила ее безопасного выполнения; проверить соответствие взятых веществ тем веществам, которые указаны в методике работы.
• Работать в лаборатории необходимо в халате, защищая одежду и кожу от попадания и разъедания реактивами и обсемененности микроорганизмами. • Каждый должен работать на закрепленном за ним рабочем месте. Переход на другое место без разрешения преподавателя не допускается. • Рабочее место следует поддерживать в чистоте, не загромождать его посудой и побочными вещами. • Студентам запрещается работать в лаборатории без присутствия преподавателя или лаборанта, а также в неустановленное время без разрешения преподавателя. • До выполнения каждой лабораторной работы можно приступить только после получения инструктажа по технике безопасности и разрешения преподавателя. • Приступая к работе, необходимо: осознать методику работы, правила ее безопасного выполнения; проверить соответствие взятых веществ тем веществам, которые указаны в методике работы.
 • Опыт необходимо проводить в точном соответствии с его описанием в методических указаниях, особенно придерживаться очередности добавления реактивов. • Для выполнения опыта пользоваться только чистой, сухой лабораторной посудой; для отмеривания каждого реактива нужно иметь мерную посуду (пипетки, бюретки, мензурку, мерный цилиндр или мерный стакан); не следует выливать избыток налитого в пробирку реактива обратно в емкость, чтобы не испортить реактив. • Если в ходе опыта требуется нагревание реакционной смеси, надо следовать предусмотренным методическим указаниям способа нагрева: на водяной бане, на электроплитке или на газовой горелке и др. Сильно летучие горючие вещества опасно нагревать на открытом огне. • Пролитые на пол и стол химические вещества обезвреживают и убирают под руководством лаборанта (преподавателя) в соответствии с правилами. • При работе в лаборатории следует соблюдать следующие требования: выполнять работу нужно аккуратно, добросовестно, внимательно, экономно, быть наблюдательным, рационально и правильно использовать время, отведенное для работы. • По окончании работы следует привести в порядок свое рабочее место: помыть посуду, протереть поверхность рабочего лабораторного стола, закрыть водопроводные краны, выключить электрические приборы.
• Опыт необходимо проводить в точном соответствии с его описанием в методических указаниях, особенно придерживаться очередности добавления реактивов. • Для выполнения опыта пользоваться только чистой, сухой лабораторной посудой; для отмеривания каждого реактива нужно иметь мерную посуду (пипетки, бюретки, мензурку, мерный цилиндр или мерный стакан); не следует выливать избыток налитого в пробирку реактива обратно в емкость, чтобы не испортить реактив. • Если в ходе опыта требуется нагревание реакционной смеси, надо следовать предусмотренным методическим указаниям способа нагрева: на водяной бане, на электроплитке или на газовой горелке и др. Сильно летучие горючие вещества опасно нагревать на открытом огне. • Пролитые на пол и стол химические вещества обезвреживают и убирают под руководством лаборанта (преподавателя) в соответствии с правилами. • При работе в лаборатории следует соблюдать следующие требования: выполнять работу нужно аккуратно, добросовестно, внимательно, экономно, быть наблюдательным, рационально и правильно использовать время, отведенное для работы. • По окончании работы следует привести в порядок свое рабочее место: помыть посуду, протереть поверхность рабочего лабораторного стола, закрыть водопроводные краны, выключить электрические приборы.
 • Правила техники безопасности в лаборатории при работе с кислотами и щелочами • Кислоты и щелочи в большинстве относятся к веществам повышенного класса опасности и способны вызвать химические ожоги и отравления. Поэтому необходимо внимательно следить за тем, чтобы реактивы не попадали на лицо, руки и одежду. • Не ходить по лаборатории с концентрированными кислотами и щелочами, а наливать их только в отведенном для этого месте. • Разливать концентрированную азотную, серную и соляную кислоты следует только при включенной вентиляции в вытяжном шкафу. • Запрещается набирать кислоты и щелочи в пипетку ртом. Для этого следует применять резиновую грушу и прочее оборудование для отбора проб. • Для приготовления растворов серной, азотной и других кислот необходимо их приливать к воде тонкой струей при непрерывном перемешивании, а не наоборот. Приливать воду в кислоту запрещается! • Растворять твердые щелочи следует путем медленного добавления их небольшими кусочками к воде при непрерывном перемешивании. Кусочки щелочи нужно брать только щипцами. • При смешивании веществ, которое сопровождается выделением тепла, необходимо пользоваться термостойким толстостенной стеклянной или фарфоровой посудой. • Разлитые кислоты или щелочи необходимо немедленно засыпать песком, нейтрализовать, и только после этого проводить уборку. • При попадании на кожу или одежду кислоты, надо смыть ее большим количеством воды, а затем 3 -5% раствором питьевой соды или разбавленным раствором аммиака. • При попадании на кожу или одежду щелочи, после смывания ее большим количеством воды, нужно провести обработку 2 -3% раствором борной, лимонной или уксусной кислотами. • Вещества, фильтры, бумагу, использованные при работе, следует выбрасывать в специальное ведро, концентрированные растворы кислот и щелочей также сливать в специальную посуду.
• Правила техники безопасности в лаборатории при работе с кислотами и щелочами • Кислоты и щелочи в большинстве относятся к веществам повышенного класса опасности и способны вызвать химические ожоги и отравления. Поэтому необходимо внимательно следить за тем, чтобы реактивы не попадали на лицо, руки и одежду. • Не ходить по лаборатории с концентрированными кислотами и щелочами, а наливать их только в отведенном для этого месте. • Разливать концентрированную азотную, серную и соляную кислоты следует только при включенной вентиляции в вытяжном шкафу. • Запрещается набирать кислоты и щелочи в пипетку ртом. Для этого следует применять резиновую грушу и прочее оборудование для отбора проб. • Для приготовления растворов серной, азотной и других кислот необходимо их приливать к воде тонкой струей при непрерывном перемешивании, а не наоборот. Приливать воду в кислоту запрещается! • Растворять твердые щелочи следует путем медленного добавления их небольшими кусочками к воде при непрерывном перемешивании. Кусочки щелочи нужно брать только щипцами. • При смешивании веществ, которое сопровождается выделением тепла, необходимо пользоваться термостойким толстостенной стеклянной или фарфоровой посудой. • Разлитые кислоты или щелочи необходимо немедленно засыпать песком, нейтрализовать, и только после этого проводить уборку. • При попадании на кожу или одежду кислоты, надо смыть ее большим количеством воды, а затем 3 -5% раствором питьевой соды или разбавленным раствором аммиака. • При попадании на кожу или одежду щелочи, после смывания ее большим количеством воды, нужно провести обработку 2 -3% раствором борной, лимонной или уксусной кислотами. • Вещества, фильтры, бумагу, использованные при работе, следует выбрасывать в специальное ведро, концентрированные растворы кислот и щелочей также сливать в специальную посуду.
 • Правила техники безопасности в лаборатории с легковоспламеняющимися и горючими жидкостями (ЛВЖ и ГЖ) • Все работы с ЛВЖ и ГЖ должны осуществляться в вытяжном шкафу при включенной вентиляции, отключенных газовых проводках и электронагревательных приборов. • Запрещается нагревать на водяных банях вещества, которые могут вступать между собой в реакцию, которая сопровождается взрывом или выделением паров и газов. • При случайном проливании ЛВЖ (сероуглерод, бензин, диэтиловый эфир и др. ), а также при потерях горючих газов необходимо немедленно отключить все источники открытого огня, электронагревательные приборы. • Сосуды, в которых проводились работы с ЛВЖ и ГЖ, после окончания исследований должны быть немедленно освобождены от оставшейся жидкости и промыты. • Опыты с ядовитыми веществами, которые имеют сильно выраженный запах, можно проводить только в вытяжном шкафу. • При тушении бензина, спирта, эфира, пользоваться песком, которым следует засыпать на вспыхнувшее пламя. • При распознавании газа по запаху, который выделяется, нюхать газ только на определенном расстоянии, направляя его струю движением руки от сосуда к себе.
• Правила техники безопасности в лаборатории с легковоспламеняющимися и горючими жидкостями (ЛВЖ и ГЖ) • Все работы с ЛВЖ и ГЖ должны осуществляться в вытяжном шкафу при включенной вентиляции, отключенных газовых проводках и электронагревательных приборов. • Запрещается нагревать на водяных банях вещества, которые могут вступать между собой в реакцию, которая сопровождается взрывом или выделением паров и газов. • При случайном проливании ЛВЖ (сероуглерод, бензин, диэтиловый эфир и др. ), а также при потерях горючих газов необходимо немедленно отключить все источники открытого огня, электронагревательные приборы. • Сосуды, в которых проводились работы с ЛВЖ и ГЖ, после окончания исследований должны быть немедленно освобождены от оставшейся жидкости и промыты. • Опыты с ядовитыми веществами, которые имеют сильно выраженный запах, можно проводить только в вытяжном шкафу. • При тушении бензина, спирта, эфира, пользоваться песком, которым следует засыпать на вспыхнувшее пламя. • При распознавании газа по запаху, который выделяется, нюхать газ только на определенном расстоянии, направляя его струю движением руки от сосуда к себе.
 Теоретическая часть
Теоретическая часть
 • Атом — это наименьшая частица химического элемента, сохраняющая все его химические свойства. • Атом состоит из – ядра, имеющего положительный электрический заряд – отрицательно заряженных электронов
• Атом — это наименьшая частица химического элемента, сохраняющая все его химические свойства. • Атом состоит из – ядра, имеющего положительный электрический заряд – отрицательно заряженных электронов
 • При химических реакциях ядра атомов остаются без изменений, изменяется лишь строение электронных оболочек вследствие перераспределения электронов между атомами. • Способностью атомов отдавать или присоединять электроны определяются его химические свойства.
• При химических реакциях ядра атомов остаются без изменений, изменяется лишь строение электронных оболочек вследствие перераспределения электронов между атомами. • Способностью атомов отдавать или присоединять электроны определяются его химические свойства.
 • Электрон имеет двойственную (корпускулярно-волновую) природу. Благодаря волновым свойствам электроны в атоме могут иметь только строго определенные значения энергии, которые зависят от расстояния до ядра. • Электроны, обладающие близкими значениями энергии образуют энергетический уровень. Он содержит строго определенное число электронов — максимально 2 n * n. • Энергетические уровни подразделяются на s -, p -, d — и f — подуровни; их число равно номеру уровня.
• Электрон имеет двойственную (корпускулярно-волновую) природу. Благодаря волновым свойствам электроны в атоме могут иметь только строго определенные значения энергии, которые зависят от расстояния до ядра. • Электроны, обладающие близкими значениями энергии образуют энергетический уровень. Он содержит строго определенное число электронов — максимально 2 n * n. • Энергетические уровни подразделяются на s -, p -, d — и f — подуровни; их число равно номеру уровня.


 Квантовые числа электронов Состояние каждого электрона в атоме обычно описывают с помощью четырех квантовых чисел: главного ( n ), орбитального ( l ), магнитного ( m ) и спинового ( s ). Первые три характеризуют движение электрона в пространстве, а четвертое — вокруг собственной оси. •
Квантовые числа электронов Состояние каждого электрона в атоме обычно описывают с помощью четырех квантовых чисел: главного ( n ), орбитального ( l ), магнитного ( m ) и спинового ( s ). Первые три характеризуют движение электрона в пространстве, а четвертое — вокруг собственной оси. •
 Главное квантовое число ( n ). • Определяет энергетический уровень электрона, удаленность уровня от ядра, размер электронного облака. Принимает целые значения ( n = 1, 2, 3. . . ) и соответствует номеру периода. Из периодической системы для любого элемента по номеру периода можно определить число энергетических уровней атома и какой энергетический уровень является внешним. • Пример. • Элемент кадмий Cd расположен в пятом периоде, значит n = 5. В его атоме электроны ра c пределены по пяти энергетическим уровням ( n = 1, n = 2, n = 3, n = 4, n = 5); внешним будет пятый уровень ( n = 5).
Главное квантовое число ( n ). • Определяет энергетический уровень электрона, удаленность уровня от ядра, размер электронного облака. Принимает целые значения ( n = 1, 2, 3. . . ) и соответствует номеру периода. Из периодической системы для любого элемента по номеру периода можно определить число энергетических уровней атома и какой энергетический уровень является внешним. • Пример. • Элемент кадмий Cd расположен в пятом периоде, значит n = 5. В его атоме электроны ра c пределены по пяти энергетическим уровням ( n = 1, n = 2, n = 3, n = 4, n = 5); внешним будет пятый уровень ( n = 5).
 Орбитальное квантовое число ( l ) • характеризует геометрическую форму орбитали. Принимает значение целых чисел от 0 до ( n — 1). Независимо от номера энергетического уровня, каждому значению орбитального квантового числа соответствует орбиталь особой формы. Набор орбиталей с одинаковыми значениями n называется энергетическим уровнем, c одинаковыми n и l — подуровнем. • • Для • l =0 s — подуровень, s — орбиталь – орбиталь сфера • l =1 p — подуровень, p — орбиталь – орбиталь гантель • l =2 d — подуровень, d — орбиталь – орбиталь сложной формы • f -подуровень, f -орбиталь – орбиталь еще более сложной формы •
Орбитальное квантовое число ( l ) • характеризует геометрическую форму орбитали. Принимает значение целых чисел от 0 до ( n — 1). Независимо от номера энергетического уровня, каждому значению орбитального квантового числа соответствует орбиталь особой формы. Набор орбиталей с одинаковыми значениями n называется энергетическим уровнем, c одинаковыми n и l — подуровнем. • • Для • l =0 s — подуровень, s — орбиталь – орбиталь сфера • l =1 p — подуровень, p — орбиталь – орбиталь гантель • l =2 d — подуровень, d — орбиталь – орбиталь сложной формы • f -подуровень, f -орбиталь – орбиталь еще более сложной формы •
 • На первом энергетическом уровне ( n = 1) орбитальное квантовое число l принимает единственное значение l = ( n — 1) = 0. Форма обитали — сферическая; на первом энергетическом только один подуровень — 1 s. Для второго энергетического уровня ( n = 2) орбитальное квантовое число может принимать два значения: l = 0, s — орбиталь — сфера большего размера, чем на первом энергетическом уровне; l = 1, p — орбиталь — гантель. Таким образом, на втором энергетическом уровне имеются два подуровня — 2 s и 2 p. Для третьего энергетического уровня ( n = 3) орбитальное квантовое число l принимает три значения: l = 0, s — орбиталь — сфера большего размера, чем на втором энергетическом уровне; l = 1, p — орбиталь — гантель большего размера, чем на втором энергетическом уровне; l = 2, d — орбиталь сложной формы. • Таким образом, на третьем энергетическом уровне могут быть три энергетических подуровня — 3 s , 3 p и 3 d. •
• На первом энергетическом уровне ( n = 1) орбитальное квантовое число l принимает единственное значение l = ( n — 1) = 0. Форма обитали — сферическая; на первом энергетическом только один подуровень — 1 s. Для второго энергетического уровня ( n = 2) орбитальное квантовое число может принимать два значения: l = 0, s — орбиталь — сфера большего размера, чем на первом энергетическом уровне; l = 1, p — орбиталь — гантель. Таким образом, на втором энергетическом уровне имеются два подуровня — 2 s и 2 p. Для третьего энергетического уровня ( n = 3) орбитальное квантовое число l принимает три значения: l = 0, s — орбиталь — сфера большего размера, чем на втором энергетическом уровне; l = 1, p — орбиталь — гантель большего размера, чем на втором энергетическом уровне; l = 2, d — орбиталь сложной формы. • Таким образом, на третьем энергетическом уровне могут быть три энергетических подуровня — 3 s , 3 p и 3 d. •
 • Магнитное квантовое число ( m ) характеризует положение электронной орбитали в пространстве и принимает целочисленные значения от — I до + I , включая 0. Это означает, что для каждой формы орбитали существует (2 l + 1) энергетически равноценных ориентации в пространстве. • Для s — орбитали ( l = 0) такое положение одно и соответствует m = 0. Сфера не может иметь разные ориентации в пространстве. • Для p — орбитали ( l = 1) — три равноценные ориентации в пространстве (2 l + 1 = 3): m = -1, 0, +1. • Для d — орбитали ( l = 2) — пять равноценных ориентаций в пространстве (2 l + 1 = 5): m = -2, -1, 0, +1, +2. • Таким образом, на s — подуровне — одна, на p — подуровне — три, на d — подуровне — пять, на f — подуровне — 7 орбиталей. •
• Магнитное квантовое число ( m ) характеризует положение электронной орбитали в пространстве и принимает целочисленные значения от — I до + I , включая 0. Это означает, что для каждой формы орбитали существует (2 l + 1) энергетически равноценных ориентации в пространстве. • Для s — орбитали ( l = 0) такое положение одно и соответствует m = 0. Сфера не может иметь разные ориентации в пространстве. • Для p — орбитали ( l = 1) — три равноценные ориентации в пространстве (2 l + 1 = 3): m = -1, 0, +1. • Для d — орбитали ( l = 2) — пять равноценных ориентаций в пространстве (2 l + 1 = 5): m = -2, -1, 0, +1, +2. • Таким образом, на s — подуровне — одна, на p — подуровне — три, на d — подуровне — пять, на f — подуровне — 7 орбиталей. •
 Спиновое квантовое число ( s ) • характеризует магнитный момент, возникающий при вращении электрона вокруг своей оси. Принимает только два значения +1/2 и – 1/2 соответствующие противоположным направлениям вращения.
Спиновое квантовое число ( s ) • характеризует магнитный момент, возникающий при вращении электрона вокруг своей оси. Принимает только два значения +1/2 и – 1/2 соответствующие противоположным направлениям вращения.
 • Принципы заполнения орбиталей • • 1. Принцип Паули. В атоме не может быть двух электронов, у которых значения всех квантовых чисел ( n , l , m , s ) были бы одинаковы, т. е. на каждой орбитали может находиться не более двух электронов ( c противоположными спинами). • • 2. Правило Клечковского (принцип наименьшей энергии). В основном состоянии каждый электрон располагается так, чтобы его энергия была минимальной. Чем меньше сумма ( n + l ), тем меньше энергия орбитали. При заданном значении ( n + l ) наименьшую энергию имеет орбиталь с меньшим n. Энергия орбиталей возрастает в ряду: • • 1 S < 2 s < 2 p < 3 s < 3 p < 4 s < 3 d < 4 p < 5 s < 4 d < 5 p < 6 s < 5 d » 4 f < 6 p < 7 s. • • 3. Правило Хунда. Атом в основном состоянии должен иметь максимально возможное число неспаренных электронов в пределах определенного подуровня.
• Принципы заполнения орбиталей • • 1. Принцип Паули. В атоме не может быть двух электронов, у которых значения всех квантовых чисел ( n , l , m , s ) были бы одинаковы, т. е. на каждой орбитали может находиться не более двух электронов ( c противоположными спинами). • • 2. Правило Клечковского (принцип наименьшей энергии). В основном состоянии каждый электрон располагается так, чтобы его энергия была минимальной. Чем меньше сумма ( n + l ), тем меньше энергия орбитали. При заданном значении ( n + l ) наименьшую энергию имеет орбиталь с меньшим n. Энергия орбиталей возрастает в ряду: • • 1 S < 2 s < 2 p < 3 s < 3 p < 4 s < 3 d < 4 p < 5 s < 4 d < 5 p < 6 s < 5 d » 4 f < 6 p < 7 s. • • 3. Правило Хунда. Атом в основном состоянии должен иметь максимально возможное число неспаренных электронов в пределах определенного подуровня.
 • Полная электронная формула элемента • • Запись, отражающая распределение электронов в атоме химического элемента по энергетическим уровням и подуровням, называется электронной конфигурацией этого атома. В основном (невозбужденном) состоянии атома все электроны удовлетворяют принципу минимальной энергии. Это значит, что сначала заполняются подуровни, для которых: • • 1) Главное квантовое число n минимально; • • 2) Внутри уровня сначала заполняется s — подуровень, затем p — и лишь затем d — ( l минимально); • • 3) Заполнение происходит так, чтобы ( n + l ) было минимально (правило Клечковского); • • 4) В пределах одного подуровня электроны располагаются таким образом, чтобы их суммарный спин был максимален, т. е. содержал наибольшее число неспаренных электронов (правило Хунда). • • 5) При заполнении электронных атомных орбиталей выполняется принцип Паули. Его следствием является, что энергетическому уровню с номером n может принадлежать не более чем 2 n 2 электронов, расположенных на n 2 подуровнях. •
• Полная электронная формула элемента • • Запись, отражающая распределение электронов в атоме химического элемента по энергетическим уровням и подуровням, называется электронной конфигурацией этого атома. В основном (невозбужденном) состоянии атома все электроны удовлетворяют принципу минимальной энергии. Это значит, что сначала заполняются подуровни, для которых: • • 1) Главное квантовое число n минимально; • • 2) Внутри уровня сначала заполняется s — подуровень, затем p — и лишь затем d — ( l минимально); • • 3) Заполнение происходит так, чтобы ( n + l ) было минимально (правило Клечковского); • • 4) В пределах одного подуровня электроны располагаются таким образом, чтобы их суммарный спин был максимален, т. е. содержал наибольшее число неспаренных электронов (правило Хунда). • • 5) При заполнении электронных атомных орбиталей выполняется принцип Паули. Его следствием является, что энергетическому уровню с номером n может принадлежать не более чем 2 n 2 электронов, расположенных на n 2 подуровнях. •
 Полная электронная формула элемента • • Пример. • Цезий (С s ) находится в 6 периоде, его 55 электронов (порядковый номер 55) распределены по 6 энергетическим уровням и их подуровням. C облюдая последовательность заполнения электронами орбиталей получим: • • 55 Cs 1 s 2 2 p 6 3 s 2 3 p 6 4 s 2 4 p 6 4 d 10 5 s 2 5 p 6 5 d 10 6 s 1 •
Полная электронная формула элемента • • Пример. • Цезий (С s ) находится в 6 периоде, его 55 электронов (порядковый номер 55) распределены по 6 энергетическим уровням и их подуровням. C облюдая последовательность заполнения электронами орбиталей получим: • • 55 Cs 1 s 2 2 p 6 3 s 2 3 p 6 4 s 2 4 p 6 4 d 10 5 s 2 5 p 6 5 d 10 6 s 1 •
 • Углерод в органических соединениях, как правило, четырехвалентен ; атомы его способны соединяться не только с другими атомами, но и друг с другом, образуя цепи; последние могут замыкаться с образованием циклов. Это свойство углерода и явление изомерии и обуславливают многообразие органических веществ.
• Углерод в органических соединениях, как правило, четырехвалентен ; атомы его способны соединяться не только с другими атомами, но и друг с другом, образуя цепи; последние могут замыкаться с образованием циклов. Это свойство углерода и явление изомерии и обуславливают многообразие органических веществ.
 Состояние валентных электронов в атоме углерода • электронная структура невозбужденного атома углерода может быть выражена формулой • 1 s 2 2 p 2, • во втором (внешнем) электронном слое у него два спаренных (с противоположными спинами) s — электрона и только два неспаренных p -электрона, которые могут участвовать в образовании ковалентных связей.
Состояние валентных электронов в атоме углерода • электронная структура невозбужденного атома углерода может быть выражена формулой • 1 s 2 2 p 2, • во втором (внешнем) электронном слое у него два спаренных (с противоположными спинами) s — электрона и только два неспаренных p -электрона, которые могут участвовать в образовании ковалентных связей.
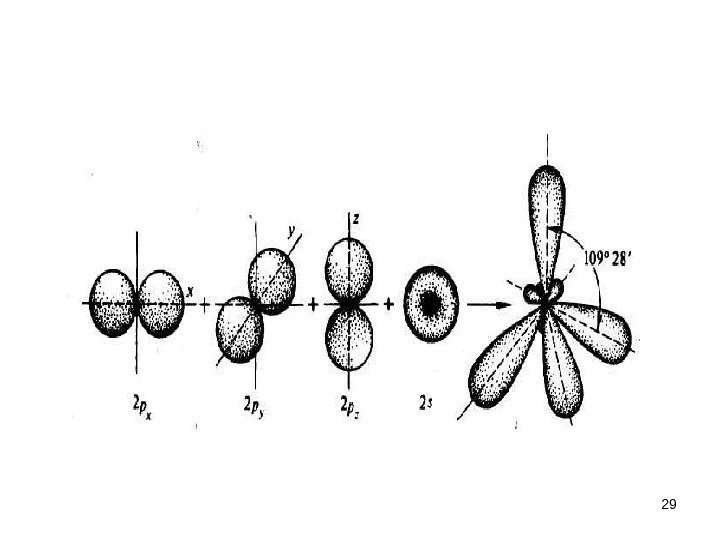
 • углерод должен был бы проявлять валентность, равную двум, но в большинстве своих соединений он четырехвалентен – образует четыре ковалентные связи. • Это объясняется тем, что при затрате некоторой энергии происходит «распаривание» 2 s — электронов: один из них переводится на свободную орбиту подуровня 2 p , и атом переходит в возбужденное состояние
• углерод должен был бы проявлять валентность, равную двум, но в большинстве своих соединений он четырехвалентен – образует четыре ковалентные связи. • Это объясняется тем, что при затрате некоторой энергии происходит «распаривание» 2 s — электронов: один из них переводится на свободную орбиту подуровня 2 p , и атом переходит в возбужденное состояние
 • у атома углерода, участвующего в образовании четырех ковалентных связей, во внешнем электронном слое, четыре валентных электрона. • Состояние их не одинаково. Один из них ( s — электрон), двигаясь вокруг ядра образует шаровое облако, подобное облаку электрона в атоме водорода ( s -состояние электрона).
• у атома углерода, участвующего в образовании четырех ковалентных связей, во внешнем электронном слое, четыре валентных электрона. • Состояние их не одинаково. Один из них ( s — электрон), двигаясь вокруг ядра образует шаровое облако, подобное облаку электрона в атоме водорода ( s -состояние электрона).
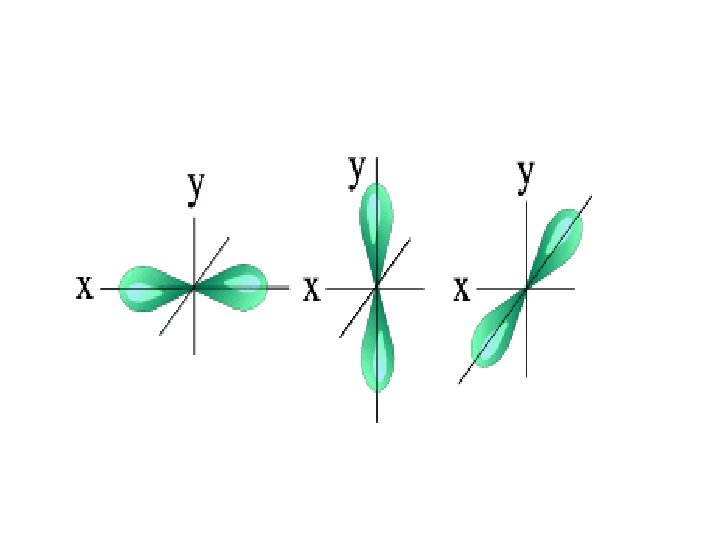
 • Облака трех других электронов ( p — электроны) имеют форму объемных восьмерок (гантелей) с «перетяжкой» в области ядра и ориентированных в трех взаимно перпендикулярных направлениях ( p — состояния электрона)
• Облака трех других электронов ( p — электроны) имеют форму объемных восьмерок (гантелей) с «перетяжкой» в области ядра и ориентированных в трех взаимно перпендикулярных направлениях ( p — состояния электрона)

 Химическая связь (Вопросы для самоподготовки) 1. Перечислите виды химической связи 2. Охарактеризуйте ковалентную связь по основным признакам 3. Охарактеризуйте ионную связь по основным признакам 4. Явление sp 3 , sp 2 , sp – гибридизации
Химическая связь (Вопросы для самоподготовки) 1. Перечислите виды химической связи 2. Охарактеризуйте ковалентную связь по основным признакам 3. Охарактеризуйте ионную связь по основным признакам 4. Явление sp 3 , sp 2 , sp – гибридизации
 Темы для сообщений 1. История органической химии 2. Определение структуры органических соединений. Инфракрасная спектроскопия и спектроскопия комбинационного рассеяния 3. Определение структуры органических соединений. Масс-спектроскопия
Темы для сообщений 1. История органической химии 2. Определение структуры органических соединений. Инфракрасная спектроскопия и спектроскопия комбинационного рассеяния 3. Определение структуры органических соединений. Масс-спектроскопия

