5e38c7c5c2de6e51bc81eeefb1af6c64.ppt
- Количество слайдов: 113
 Л. Л. ПЕРЧУК ТЕРМОДИНАМИКА МИНЕРАЛОВ
Л. Л. ПЕРЧУК ТЕРМОДИНАМИКА МИНЕРАЛОВ
 ТЕПЛОЕМКОСТЬ Если Т вещества с массой М повысилась на d T, то поглощенное им тепло равно d Q = mcd. T, (1) где mc - теплоемкость массы m при постоянстве P и V. Удельная теплоемкость определяется величинами m=1 г и T 2 -T 1 = 1 С. Средняя теплоемкость: (2) (3)
ТЕПЛОЕМКОСТЬ Если Т вещества с массой М повысилась на d T, то поглощенное им тепло равно d Q = mcd. T, (1) где mc - теплоемкость массы m при постоянстве P и V. Удельная теплоемкость определяется величинами m=1 г и T 2 -T 1 = 1 С. Средняя теплоемкость: (2) (3)
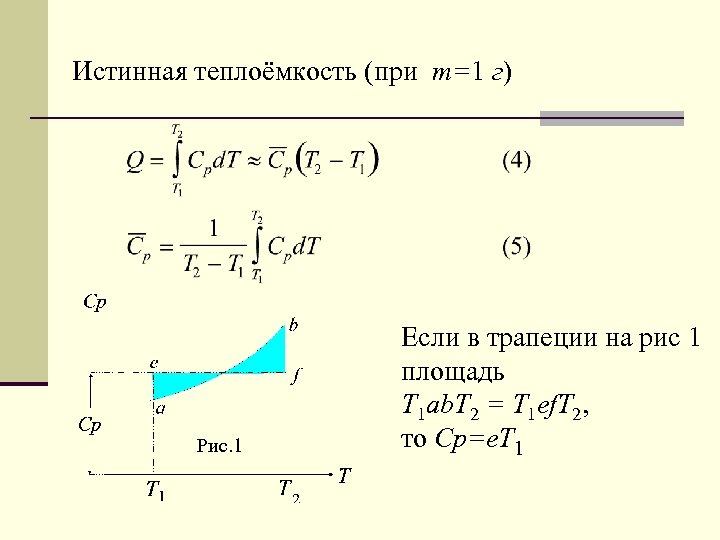 Истинная теплоёмкость (при m=1 г) Рис. 1 Если в трапеции на рис 1 площадь T 1 ab. T 2 = T 1 ef. T 2, то Ср=е. Т 1
Истинная теплоёмкость (при m=1 г) Рис. 1 Если в трапеции на рис 1 площадь T 1 ab. T 2 = T 1 ef. T 2, то Ср=е. Т 1
 Обычно теплоёмкость выражают через степенной ряд: Cp= a+b. T+c. T 2+. . . (6) ПРАВИЛО ДЮЛОНГА -ПТИ Для одноатомных твердых тел при 25 о. С: Cp = 6, 4; Cv= 6 кал/град Теплоемкость – экстенсивное свойство. Поэтому можно рассчитывать атомные теплоемкости соединений: Правило Дюлонга – Пти выполняется не всегда: С (алмаз) 1. 46 Be 4. 14 K 7. 07 Сs 7. 42
Обычно теплоёмкость выражают через степенной ряд: Cp= a+b. T+c. T 2+. . . (6) ПРАВИЛО ДЮЛОНГА -ПТИ Для одноатомных твердых тел при 25 о. С: Cp = 6, 4; Cv= 6 кал/град Теплоемкость – экстенсивное свойство. Поэтому можно рассчитывать атомные теплоемкости соединений: Правило Дюлонга – Пти выполняется не всегда: С (алмаз) 1. 46 Be 4. 14 K 7. 07 Сs 7. 42
 ПРАВИЛО БОЛЬЦМАНА где 3 – число степеней свободы атома в твердом теле, R=1, 987 кал/моль/град – газовая постоянная. В газах – три типа движений: (1) поступательное, (2) вращательное и (3)низкочастотные колебания. В твердых телах атомная теплоемкость связана в основном с низкочастотными колебаниями. Следовательно, возможен расчет СP на основе низкочастотных колебательных спектров. Пока методы такого расчета разработаны слабо. Эйнштейн первый применил квантовую идею Планка к расчету теплоемкостей "идеальных кристаллов":
ПРАВИЛО БОЛЬЦМАНА где 3 – число степеней свободы атома в твердом теле, R=1, 987 кал/моль/град – газовая постоянная. В газах – три типа движений: (1) поступательное, (2) вращательное и (3)низкочастотные колебания. В твердых телах атомная теплоемкость связана в основном с низкочастотными колебаниями. Следовательно, возможен расчет СP на основе низкочастотных колебательных спектров. Пока методы такого расчета разработаны слабо. Эйнштейн первый применил квантовую идею Планка к расчету теплоемкостей "идеальных кристаллов":
 где и где h - Планка, равная - 6. 605 10 -27' эрг. сек; k - константа Больцмана – 1. 38. 10 -16 эрг/град; – средняя частота (сек 1); QE - характеристическая температура Эйнштейна. Вместо средней частоты используют волновое число w (см-1), которое связано с и средней длиной волны уравнением В низкотемпературной области формула Эйнштейна не дает удовлетворительной сходимости с экспериментом.
где и где h - Планка, равная - 6. 605 10 -27' эрг. сек; k - константа Больцмана – 1. 38. 10 -16 эрг/град; – средняя частота (сек 1); QE - характеристическая температура Эйнштейна. Вместо средней частоты используют волновое число w (см-1), которое связано с и средней длиной волны уравнением В низкотемпературной области формула Эйнштейна не дает удовлетворительной сходимости с экспериментом.
 Дебай ее усовершенствовал. Он показал, что среднее значение низкотемпературных колебаний в трехмерном осцилляторе распределено неравномерно. В каждом линейном осцилляторе имеется свой спектр частот от 0 до некоторой максимальной величины, отличающейся от эйнштейновской множителем 4/3: vm = (4/3)vэйншт (11) Несколько слов об осциляторе. Оscillo - качаюсь (лат); oscillum - качание. Осциллятор – любая система, способная совершать колебания (механические, э/м и т. п. ). Чаще он одномерный. Если сила, возвращающая систему в положение равновесия, пропорциональна удалению от последнего, то осцилятор называется гармоническим. Будучи представлен самому себе, он совершает гармонические колебания.
Дебай ее усовершенствовал. Он показал, что среднее значение низкотемпературных колебаний в трехмерном осцилляторе распределено неравномерно. В каждом линейном осцилляторе имеется свой спектр частот от 0 до некоторой максимальной величины, отличающейся от эйнштейновской множителем 4/3: vm = (4/3)vэйншт (11) Несколько слов об осциляторе. Оscillo - качаюсь (лат); oscillum - качание. Осциллятор – любая система, способная совершать колебания (механические, э/м и т. п. ). Чаще он одномерный. Если сила, возвращающая систему в положение равновесия, пропорциональна удалению от последнего, то осцилятор называется гармоническим. Будучи представлен самому себе, он совершает гармонические колебания.
 Трехмерный осциллятор состоит из трех линейных, составляющие которых следующие: E =Eпот +Eкин =1/2 RT + 1/2 RT, где R = Nоk. Каждый атом можно рассматривать как 3 -х -мерный осциллятор: где qi – координата, т. е. смещение системы от равновесного состояния, p – количество движения и f коэффициент возвращающей силы. . КЛАССИЧЕСКИЙ ОСЦИЛЛЯТОР При смещении атома из положения равновесия на него действуют силы, стремящиеся его вернуть в это состояние. При небольших смещениях r возвращающую силу F принимают пропорциональной смещению
Трехмерный осциллятор состоит из трех линейных, составляющие которых следующие: E =Eпот +Eкин =1/2 RT + 1/2 RT, где R = Nоk. Каждый атом можно рассматривать как 3 -х -мерный осциллятор: где qi – координата, т. е. смещение системы от равновесного состояния, p – количество движения и f коэффициент возвращающей силы. . КЛАССИЧЕСКИЙ ОСЦИЛЛЯТОР При смещении атома из положения равновесия на него действуют силы, стремящиеся его вернуть в это состояние. При небольших смещениях r возвращающую силу F принимают пропорциональной смещению
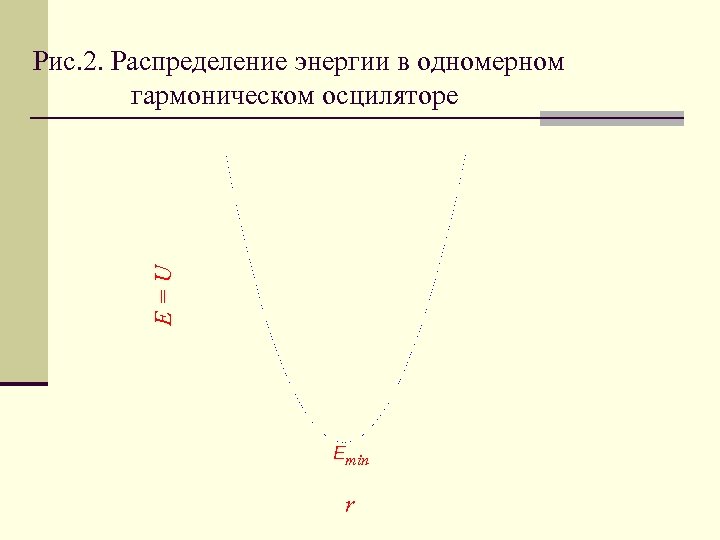 E=U Рис. 2. Распределение энергии в одномерном гармоническом осциляторе Emin r
E=U Рис. 2. Распределение энергии в одномерном гармоническом осциляторе Emin r
 При смещении атома из положения равновесия на него действуют силы, стремящиеся его вернуть в это состояние. При небольших смещениях r возвращающую силу F принимают пропорциональной смещению F(r) = - fr, Потенциальная энергия (Епот) квазиупругого вибратора Eпот =U = 1/2 fr 2 =1/2 fq 2 изменяется по параболическому закону. Это задача о параболической потенциальной яме для классической частицы, совершающей гармонические колебания в количестве r = A. cos(2 v ), где А – амплитуда, v – частота колебаний, – время. Кинетическая (Eкин) и потенциальная энергия составляют полную энергию осциллятора (вибратора), причем средние их значения равны между собой
При смещении атома из положения равновесия на него действуют силы, стремящиеся его вернуть в это состояние. При небольших смещениях r возвращающую силу F принимают пропорциональной смещению F(r) = - fr, Потенциальная энергия (Епот) квазиупругого вибратора Eпот =U = 1/2 fr 2 =1/2 fq 2 изменяется по параболическому закону. Это задача о параболической потенциальной яме для классической частицы, совершающей гармонические колебания в количестве r = A. cos(2 v ), где А – амплитуда, v – частота колебаний, – время. Кинетическая (Eкин) и потенциальная энергия составляют полную энергию осциллятора (вибратора), причем средние их значения равны между собой
 Но вернёмся к множителю Дебая. В области высоких значений температуры: CV=3 RD{T/Q) (12) Функции Дебая (D) табулированы во многих справочниках по физической химии и металлургии. Поправка Дебая позволила точнее описать экспериментальные данные в низкотемпературной области для кристаллов с однородной трехмерной структурой : CV = 233. 782 R(T/Q)3 (13) Для линейно полимеризованных структур: CV =43. 27(T/Q)2 (14) Для слоистых: CV =19. 64(T/Q) (15) Эмпирические формулы (14) и (15) получены В. В. Тарасовым.
Но вернёмся к множителю Дебая. В области высоких значений температуры: CV=3 RD{T/Q) (12) Функции Дебая (D) табулированы во многих справочниках по физической химии и металлургии. Поправка Дебая позволила точнее описать экспериментальные данные в низкотемпературной области для кристаллов с однородной трехмерной структурой : CV = 233. 782 R(T/Q)3 (13) Для линейно полимеризованных структур: CV =43. 27(T/Q)2 (14) Для слоистых: CV =19. 64(T/Q) (15) Эмпирические формулы (14) и (15) получены В. В. Тарасовым.
 Идея Мюллера Р Л Мюллер показал, что при 25 С в твердых телах происходит равное распределение термической энергии по степеням свободы при длине волны более 48 µm (w = 208 cм-1).
Идея Мюллера Р Л Мюллер показал, что при 25 С в твердых телах происходит равное распределение термической энергии по степеням свободы при длине волны более 48 µm (w = 208 cм-1).
 Тогда правило Дюлонга–Пти интерпретируется в такой форме: CV = n. R = 1. 987 n (16) где n – число низкочастотных степеней свободы: n = nо - (17) где no – общее число степеней свободы, – число замороженных низкочастотных колебаний, включенных в распределение термической энергии. Если вещество состоит из N атомов, то nо = 3 N (18) n =3 N – (19) Cледовательно, CV = 1. 987(3 N - ) (20) Cp = 1. 07 CV 2. 1(3 N - ) (21)
Тогда правило Дюлонга–Пти интерпретируется в такой форме: CV = n. R = 1. 987 n (16) где n – число низкочастотных степеней свободы: n = nо - (17) где no – общее число степеней свободы, – число замороженных низкочастотных колебаний, включенных в распределение термической энергии. Если вещество состоит из N атомов, то nо = 3 N (18) n =3 N – (19) Cледовательно, CV = 1. 987(3 N - ) (20) Cp = 1. 07 CV 2. 1(3 N - ) (21)
 Для идеального газа CP – CV = R Для реальных газов и твердых тел: (22) «Это типичные термодинамические уравнения, которые ничего не говорит об абсолютной величине всех входящих в него переменных, но показывает, как вычислить шестую, если известны остальные пять» (Э. А. Мелвин-Хьюз, Физическая химия. Т. 1. , М. : ИИЛ, 1962).
Для идеального газа CP – CV = R Для реальных газов и твердых тел: (22) «Это типичные термодинамические уравнения, которые ничего не говорит об абсолютной величине всех входящих в него переменных, но показывает, как вычислить шестую, если известны остальные пять» (Э. А. Мелвин-Хьюз, Физическая химия. Т. 1. , М. : ИИЛ, 1962).
 Эмпирические формулы CP = n. CV элементы галогениды сульфиды силикаты В общем случае: (26) n = 1. 051 n = 1. 038 n = 1. 021 n = 1. 016 (27) где Tm – температура плавления (градусы К). Идея Мюллера основана на модели кристалла с чисто металлическими или ионными связями. Это значит. . . , что мы должны перейти к рассмотрению проблемы химической связи.
Эмпирические формулы CP = n. CV элементы галогениды сульфиды силикаты В общем случае: (26) n = 1. 051 n = 1. 038 n = 1. 021 n = 1. 016 (27) где Tm – температура плавления (градусы К). Идея Мюллера основана на модели кристалла с чисто металлическими или ионными связями. Это значит. . . , что мы должны перейти к рассмотрению проблемы химической связи.
 ХИМЧЕСКАЯ СВЯЗЬ В твердых телах различается: ковалентная и ионная. Ковалентная связь возникает в результате обобщения электронных плотностей взаимодействующих атомов одного сорта, т. е. эта связь является универсальной. В молекулах, состоящих из атомов разного сорта электронное облако несимметрично и смещено к одному из ядер атомов. Такая связь имеет постоянный дипольный момент и является полярной. В предельном случае полярности возникает ионная связь – полное разделение электронных плотностей как результат взаимодействия атомов с разными зарядами. Рассмотрим некоторые простейшие схемы.
ХИМЧЕСКАЯ СВЯЗЬ В твердых телах различается: ковалентная и ионная. Ковалентная связь возникает в результате обобщения электронных плотностей взаимодействующих атомов одного сорта, т. е. эта связь является универсальной. В молекулах, состоящих из атомов разного сорта электронное облако несимметрично и смещено к одному из ядер атомов. Такая связь имеет постоянный дипольный момент и является полярной. В предельном случае полярности возникает ионная связь – полное разделение электронных плотностей как результат взаимодействия атомов с разными зарядами. Рассмотрим некоторые простейшие схемы.
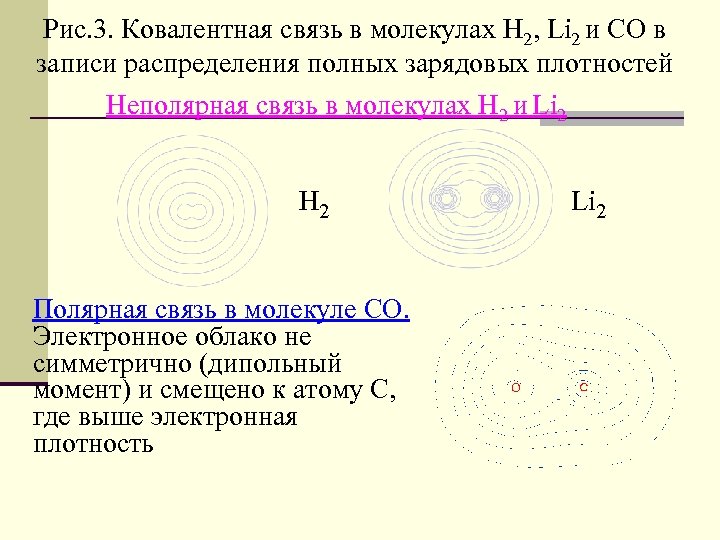 Рис. 3. Ковалентная связь в молекулах Н 2, Li 2 и СО в записи распределения полных зарядовых плотностей Неполярная связь в молекулах Н 2 и Li 2 H 2 Полярная связь в молекуле CO. Электронное облако не симметрично (дипольный момент) и смещено к атому С, где выше электронная плотность Li 2
Рис. 3. Ковалентная связь в молекулах Н 2, Li 2 и СО в записи распределения полных зарядовых плотностей Неполярная связь в молекулах Н 2 и Li 2 H 2 Полярная связь в молекуле CO. Электронное облако не симметрично (дипольный момент) и смещено к атому С, где выше электронная плотность Li 2
 Рис. 4. Распределение электронов в ионах щелочных металлов и галогенов Na+ K+ Rb+ Cs+ F- Cl- Br- I-
Рис. 4. Распределение электронов в ионах щелочных металлов и галогенов Na+ K+ Rb+ Cs+ F- Cl- Br- I-
 МЕТАЛЛИЧЕСКАЯ СВЯЗЬ Она имеет ту же природу, что и ковалентная и является ее разновидностью. Возникает она вследствие полной делокализации валентных электронов каждого атома. Т. е. ядра как бы погружены в электронное море. При этом возникают высокие координационные числа и происходит заметное увеличение полной энергии связи на один атом по сравнению с молекулой ( у Li. I на 39 ккал на атом и 13 ккал на молекулу). Когда химическая связь реализуется полностью (ионная или металлическая), отсутствуют замороженные степени свободы и формула Мюллера становится тождественной закону Дюлонга - Пти.
МЕТАЛЛИЧЕСКАЯ СВЯЗЬ Она имеет ту же природу, что и ковалентная и является ее разновидностью. Возникает она вследствие полной делокализации валентных электронов каждого атома. Т. е. ядра как бы погружены в электронное море. При этом возникают высокие координационные числа и происходит заметное увеличение полной энергии связи на один атом по сравнению с молекулой ( у Li. I на 39 ккал на атом и 13 ккал на молекулу). Когда химическая связь реализуется полностью (ионная или металлическая), отсутствуют замороженные степени свободы и формула Мюллера становится тождественной закону Дюлонга - Пти.
 CP 298 = 1. 07 R 3 N = 6. 37827 N (29) где N – число атомов в молекуле. Расчет по формуле (29) для йодидов дает CP 298, очень близкие по величине к экспериментальным данным: Li. I – 13. 0, Na. I – 12. 98, Cs. I – 12. 4 кал/град. По CP 298 можно судить о совершенстве характера химической связи. "Чистые" связи практически не встречаются. Обычно они промежуточные. Это обусловлено искажением плотностей электронных структур. Есть теория электроотрицательности атомов Л. Полинга. Электроотрицательность – сила притяжения электронов в ковалентной связи. Она может быть оценена количественно. Известно несколько шкал электроотрицательностей.
CP 298 = 1. 07 R 3 N = 6. 37827 N (29) где N – число атомов в молекуле. Расчет по формуле (29) для йодидов дает CP 298, очень близкие по величине к экспериментальным данным: Li. I – 13. 0, Na. I – 12. 98, Cs. I – 12. 4 кал/град. По CP 298 можно судить о совершенстве характера химической связи. "Чистые" связи практически не встречаются. Обычно они промежуточные. Это обусловлено искажением плотностей электронных структур. Есть теория электроотрицательности атомов Л. Полинга. Электроотрицательность – сила притяжения электронов в ковалентной связи. Она может быть оценена количественно. Известно несколько шкал электроотрицательностей.
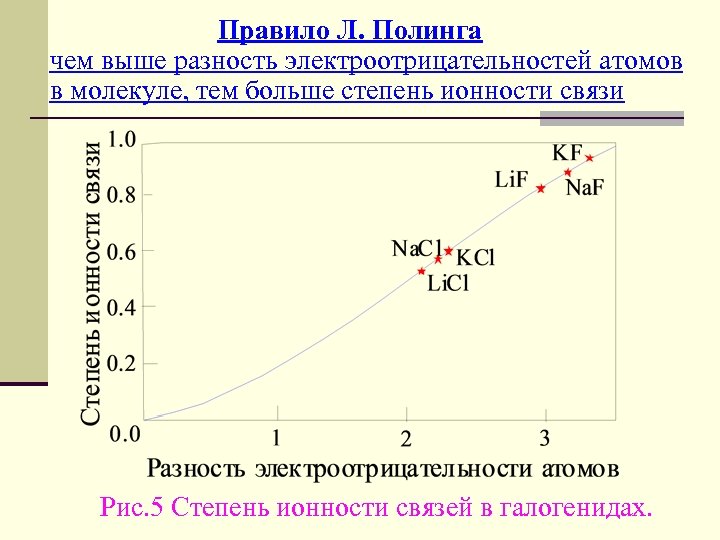 Правило Л. Полинга чем выше разность электроотрицательностей атомов в молекуле, тем больше степень ионности связи Рис. 5 Степень ионности связей в галогенидах.
Правило Л. Полинга чем выше разность электроотрицательностей атомов в молекуле, тем больше степень ионности связи Рис. 5 Степень ионности связей в галогенидах.
 Из правила Л. Полинга и формулы Мюллера следует: теплоемкость соединения тем выше, чем большая доля в нем ионной связи и чем меньшая доля ковалентной. Экспериментально найдена обратная связь между максимумами ИК – поглощения и усилением ионности связи, т. е. по Мюллеру – с возрастанием теплоемкости. Это значит, что теплоемкость, а следовательно и степень ионности связи и могут быть приближенно найдены из данных ИК –спектроскопии. На рис. 6 приведена такая связь для ортосиликатов.
Из правила Л. Полинга и формулы Мюллера следует: теплоемкость соединения тем выше, чем большая доля в нем ионной связи и чем меньшая доля ковалентной. Экспериментально найдена обратная связь между максимумами ИК – поглощения и усилением ионности связи, т. е. по Мюллеру – с возрастанием теплоемкости. Это значит, что теплоемкость, а следовательно и степень ионности связи и могут быть приближенно найдены из данных ИК –спектроскопии. На рис. 6 приведена такая связь для ортосиликатов.
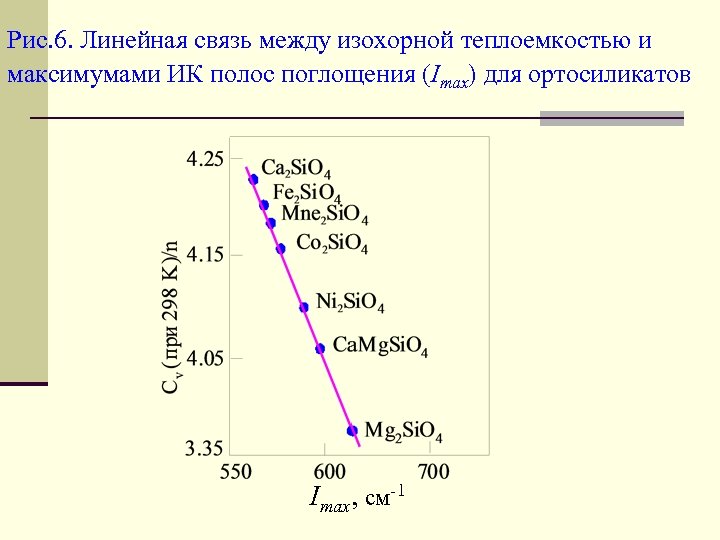 Рис. 6. Линейная связь между изохорной теплоемкостью и максимумами ИК полос поглощения (Imax) для ортосиликатов Imax, см-1
Рис. 6. Линейная связь между изохорной теплоемкостью и максимумами ИК полос поглощения (Imax) для ортосиликатов Imax, см-1
 В 20 -х годах прошлого столетия Брегг ввел представление об эффективных зарядах атомов в соединениях. Эффективный заряд – часть заряда, реализуемая на химическую связь. Остальная часть заряда заморожена, т. е. является потенциальной. Эффективный заряд можно рассчитывать, например, из данных рентгеновского анализа (В. С. Урусов, "Энергетическая кристаллохимия", М. : "Наука", 1975 г. ). На основе правила Мюллера можно утверждать, что CP 298 находится в прямой зависимости от степени ионности связи в кристалле и от величины эффективного заряда, gef. Чем выше gef , тем меньше в формуле Мюллера CP 298 = 2. 1(3 N – ) (30) Этим воспользовался А. А. Маракушев ("Очерки физикохимической петрологии", Т. I, М. : Наука, 1969 г). Он нашел такое выражение для теплоёмкости:
В 20 -х годах прошлого столетия Брегг ввел представление об эффективных зарядах атомов в соединениях. Эффективный заряд – часть заряда, реализуемая на химическую связь. Остальная часть заряда заморожена, т. е. является потенциальной. Эффективный заряд можно рассчитывать, например, из данных рентгеновского анализа (В. С. Урусов, "Энергетическая кристаллохимия", М. : "Наука", 1975 г. ). На основе правила Мюллера можно утверждать, что CP 298 находится в прямой зависимости от степени ионности связи в кристалле и от величины эффективного заряда, gef. Чем выше gef , тем меньше в формуле Мюллера CP 298 = 2. 1(3 N – ) (30) Этим воспользовался А. А. Маракушев ("Очерки физикохимической петрологии", Т. I, М. : Наука, 1969 г). Он нашел такое выражение для теплоёмкости:
 (31) Подставляем (30) в (31) и находим: (32) Рассмотрим Al 2 O 3, корунд, в котором N=5. Проверяем по формуле (27)
(31) Подставляем (30) в (31) и находим: (32) Рассмотрим Al 2 O 3, корунд, в котором N=5. Проверяем по формуле (27)
 Температура плавления корунда Tm = 2345 K. Теплоемкость – фундаментальное свойство веществ. Она хорошо согласуется со всеми физическими свойствами минералов. Так А. С. Поваренных установил правило: твердость минералов обратно пропорциональна степени ионности связи. Применяя правило Мюллера, можно постулировать: твердость минералов обратно пропорциональна их атомной теплоемкости.
Температура плавления корунда Tm = 2345 K. Теплоемкость – фундаментальное свойство веществ. Она хорошо согласуется со всеми физическими свойствами минералов. Так А. С. Поваренных установил правило: твердость минералов обратно пропорциональна степени ионности связи. Применяя правило Мюллера, можно постулировать: твердость минералов обратно пропорциональна их атомной теплоемкости.
 ЭНТРОПИЯ Энтропия (S) – приведенное количество тепла, отнесенное к абсолютной температуре. Изменение энтропии d. S для обратимого равновесного процесса равно: в соответствии с формулой (1): d. Q = CV d T Подставляем (34) в (33) и находим: (34) Энтропия - экстенсивная величина. Её относят к данной массе вещества (моль, атом, грамм, кг. и т. п. ).
ЭНТРОПИЯ Энтропия (S) – приведенное количество тепла, отнесенное к абсолютной температуре. Изменение энтропии d. S для обратимого равновесного процесса равно: в соответствии с формулой (1): d. Q = CV d T Подставляем (34) в (33) и находим: (34) Энтропия - экстенсивная величина. Её относят к данной массе вещества (моль, атом, грамм, кг. и т. п. ).
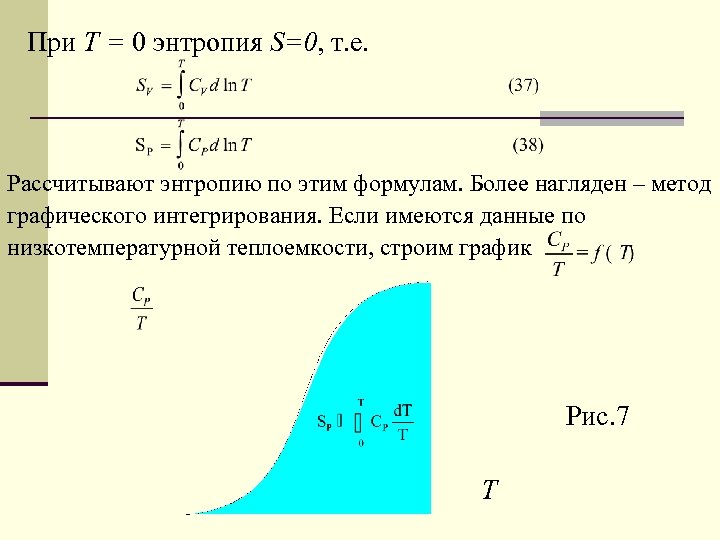 При T = 0 энтропия S=0, т. е. Рассчитывают энтропию по этим формулам. Более нагляден – метод графического интегрирования. Если имеются данные по низкотемпературной теплоемкости, строим график Рис. 7 T
При T = 0 энтропия S=0, т. е. Рассчитывают энтропию по этим формулам. Более нагляден – метод графического интегрирования. Если имеются данные по низкотемпературной теплоемкости, строим график Рис. 7 T
 В подавляющем большинстве фазовых переходов теплоемкость Cp (или CV) испытывает скачок, т. к. происходит разупорядочение структуры. При этом Ср разупорядоченного состояния кристалла выше, чем упорядоченного. Реже наоборот (Qz -Tr, плавление Si. О 2 и т. п. ). Однако возможны изоэнтропийные фазовые переходы. Они происходят без заметной перестройки структуры. Отсюда фазовые переходы первого и второго рода. Оба фазовых перехода сопровождаются скачком СР, но для перехода 1 го рода S > 0, Q 0 и V > 0, а в случае переходов 2 го рода S = 0, Q = 0 и V = 0. На рис. 8 показаны схемы изменения термодинамических характеристик при фазовых переходах первого и второго рода.
В подавляющем большинстве фазовых переходов теплоемкость Cp (или CV) испытывает скачок, т. к. происходит разупорядочение структуры. При этом Ср разупорядоченного состояния кристалла выше, чем упорядоченного. Реже наоборот (Qz -Tr, плавление Si. О 2 и т. п. ). Однако возможны изоэнтропийные фазовые переходы. Они происходят без заметной перестройки структуры. Отсюда фазовые переходы первого и второго рода. Оба фазовых перехода сопровождаются скачком СР, но для перехода 1 го рода S > 0, Q 0 и V > 0, а в случае переходов 2 го рода S = 0, Q = 0 и V = 0. На рис. 8 показаны схемы изменения термодинамических характеристик при фазовых переходах первого и второго рода.
 Рис. 8. ФАЗОВЫЕ ПЕРЕХОДЫ И ИХ ТЕРМОДИНАМИЧЕСКИЕ ХАРАКТЕРИСТИКИ Фазовый переход первого рода T 1 и T 2 – температуры фазовых перехода Фазовые переходы второго рода (изоэнтропийные)
Рис. 8. ФАЗОВЫЕ ПЕРЕХОДЫ И ИХ ТЕРМОДИНАМИЧЕСКИЕ ХАРАКТЕРИСТИКИ Фазовый переход первого рода T 1 и T 2 – температуры фазовых перехода Фазовые переходы второго рода (изоэнтропийные)
 По формулам (37) и (38) связь между энтропией и теплоемкостью прямая. Она закономерна для элементов и соединений, обладающих общностью химической природы. Для первых четырех групп элементов в периодической системе последовательно возрастают СV и СР: H - Li - Na - K - Rb - Cs Be - Mg - Ca - Sr - Ba B - Al - Ga - In - Tl C - Si - Ge - Sn – Pl Все эти закономерности вытекают из экстенсивности свойств энтропии и теплоемкости. С ростом атомного номера либо атомного веса SP и СР возрастают при T =const (сравнить с законом Дюлонга–Пти). В общем случае СР и SP возрастают с увеличением массы фаз.
По формулам (37) и (38) связь между энтропией и теплоемкостью прямая. Она закономерна для элементов и соединений, обладающих общностью химической природы. Для первых четырех групп элементов в периодической системе последовательно возрастают СV и СР: H - Li - Na - K - Rb - Cs Be - Mg - Ca - Sr - Ba B - Al - Ga - In - Tl C - Si - Ge - Sn – Pl Все эти закономерности вытекают из экстенсивности свойств энтропии и теплоемкости. С ростом атомного номера либо атомного веса SP и СР возрастают при T =const (сравнить с законом Дюлонга–Пти). В общем случае СР и SP возрастают с увеличением массы фаз.
 Отсюда, точнее из комплиментарности свойств Cp и SP вытекает правило: энтропия возрастает с увеличением степени ионности связей в солях одного типа (хлориды, фториды, метасиликаты, ортосиликаты). А. А. Маракушев (1969) нашел эмпирическую формулу: (39) где N -число атомов в формуле минералов, x и y эмпирические коэффициенты, значения которых табулированы.
Отсюда, точнее из комплиментарности свойств Cp и SP вытекает правило: энтропия возрастает с увеличением степени ионности связей в солях одного типа (хлориды, фториды, метасиликаты, ортосиликаты). А. А. Маракушев (1969) нашел эмпирическую формулу: (39) где N -число атомов в формуле минералов, x и y эмпирические коэффициенты, значения которых табулированы.
 ЭНТАЛЬПИЯ МИНЕРАЛОВ Энтальпия определяет теплоту реакции, необходимую для создания минерала из различных видов частиц (молекул, атомов, ионов). С теплоемкостью она связана уравнением (1). Энтальпия - характеристическая функция: (40) При постоянных Р и mi d. H=Td. S C учетом уже известного нам уравнения (36) (41) (42) d. H = CPd. T (43)
ЭНТАЛЬПИЯ МИНЕРАЛОВ Энтальпия определяет теплоту реакции, необходимую для создания минерала из различных видов частиц (молекул, атомов, ионов). С теплоемкостью она связана уравнением (1). Энтальпия - характеристическая функция: (40) При постоянных Р и mi d. H=Td. S C учетом уже известного нам уравнения (36) (41) (42) d. H = CPd. T (43)
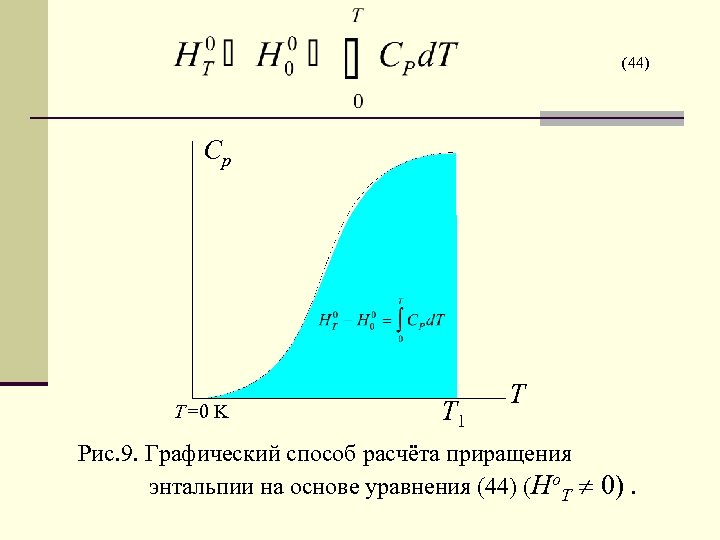 (44) Ср Т=0 K Т 1 Т Рис. 9. Графический способ расчёта приращения энтальпии на основе уравнения (44) (Ho. T 0).
(44) Ср Т=0 K Т 1 Т Рис. 9. Графический способ расчёта приращения энтальпии на основе уравнения (44) (Ho. T 0).
 При Т=0 K энтальпия минерала не равна нулю, т. е. (45) Ho. T 0 Тепловые колебания в решетке минимальны, кристалл максимально упорядочен вся энергия полностью затрачивается на химическую связь. Степень ионности связей минимальна, преобладают ковалентные связи. (46) С понижением T происходит упорядочение кристаллической и электронной структуры минералов. При T=4 K В металлах появляется сверхпроводимость. Следовательно, должны существенно преобладать ковалентные связи. Пока это гипотеза. Можно проверить на примере Li. F. Разложим его на атомы и на ионы по таким реакциям:
При Т=0 K энтальпия минерала не равна нулю, т. е. (45) Ho. T 0 Тепловые колебания в решетке минимальны, кристалл максимально упорядочен вся энергия полностью затрачивается на химическую связь. Степень ионности связей минимальна, преобладают ковалентные связи. (46) С понижением T происходит упорядочение кристаллической и электронной структуры минералов. При T=4 K В металлах появляется сверхпроводимость. Следовательно, должны существенно преобладать ковалентные связи. Пока это гипотеза. Можно проверить на примере Li. F. Разложим его на атомы и на ионы по таким реакциям:
 Li. F(тв) = Li+(газ) + F-(газ); Li. F(тв) = Li(газ) + F(газ) Первая из них, (47), должна характеризовать ионные, вторая ковалентные связи (48). Вычтем из (47) уравнение (48). В результате получаем обменное равновесие: Li+ (газ) + F-(газ) = Li (газ) +F(газ), для которого (47) (48) (49) Реакция резко смещена вправо, т. е. устойчив атомарный газ. Следовательно реакция (47) имеет предпочтение перед реакцией (48) и в Li. F в значительной мере преобладают ковалентные связи, если величиной определяется химическая связь в кристаллах.
Li. F(тв) = Li+(газ) + F-(газ); Li. F(тв) = Li(газ) + F(газ) Первая из них, (47), должна характеризовать ионные, вторая ковалентные связи (48). Вычтем из (47) уравнение (48). В результате получаем обменное равновесие: Li+ (газ) + F-(газ) = Li (газ) +F(газ), для которого (47) (48) (49) Реакция резко смещена вправо, т. е. устойчив атомарный газ. Следовательно реакция (47) имеет предпочтение перед реакцией (48) и в Li. F в значительной мере преобладают ковалентные связи, если величиной определяется химическая связь в кристаллах.
 Но каждое химическое соединение можно разложить на ионы по следующей схеме (при T = 0): 1. Na. F(тв) Na(тв)+1/2 F 2 (газ) атомизация = образование 2. F 2 (газ) F (газ)+F (газ) 3. Na(тв) Na (газ) 4. Na (газ) Na+ +e 5. F (газ) + e- F- электрону диссоциация сублимация ионизация сродство к U 0 = H 5 - H 4 - H 3 - H 2 + H 1 Эта величина считалась энергией кристаллической решетки. Однако вполне однозначно U 0 определяется реакцией 1. Это можно показать на примере Li. F, для котороого величина почти не зависит от T, хотя СР возрастает. Следовательно, величина определяет прочность химической связи, т. е. энергию
Но каждое химическое соединение можно разложить на ионы по следующей схеме (при T = 0): 1. Na. F(тв) Na(тв)+1/2 F 2 (газ) атомизация = образование 2. F 2 (газ) F (газ)+F (газ) 3. Na(тв) Na (газ) 4. Na (газ) Na+ +e 5. F (газ) + e- F- электрону диссоциация сублимация ионизация сродство к U 0 = H 5 - H 4 - H 3 - H 2 + H 1 Эта величина считалась энергией кристаллической решетки. Однако вполне однозначно U 0 определяется реакцией 1. Это можно показать на примере Li. F, для котороого величина почти не зависит от T, хотя СР возрастает. Следовательно, величина определяет прочность химической связи, т. е. энергию
 ккал/моль Рис. 10 ккал/моль Рассмотрим влияние температуры на энергию химической связи в минералах, на прочность этой связи и на ее характер. При Т = 0 K преобладает ковалентная связь. Гипотеза: с ростом температуры увеличивается степень ионности связи без существенного изменения ее прочности. Действительно, изменяется слабо, т. е. прочность химической связи остаётся почти постоянной.
ккал/моль Рис. 10 ккал/моль Рассмотрим влияние температуры на энергию химической связи в минералах, на прочность этой связи и на ее характер. При Т = 0 K преобладает ковалентная связь. Гипотеза: с ростом температуры увеличивается степень ионности связи без существенного изменения ее прочности. Действительно, изменяется слабо, т. е. прочность химической связи остаётся почти постоянной.
 Следовательно, должна существовать функция, которая бы описала характер перестройки электронной структуры кристалла и стремление его к разупорядочению. Такая энергия существует и носит название СВОБОДНАЯ ЭНЕРГИЯ ГИББСА (G) Она описывает понижение потенциальной энергии кристалла за счет увеличения тепловых колебаний атомов. Рост Т приводит к деформациям и разрывам в электронной плотности. Пусть ni - масса компонента i, µi - химический его потенциал. Согласно Гиббсу:
Следовательно, должна существовать функция, которая бы описала характер перестройки электронной структуры кристалла и стремление его к разупорядочению. Такая энергия существует и носит название СВОБОДНАЯ ЭНЕРГИЯ ГИББСА (G) Она описывает понижение потенциальной энергии кристалла за счет увеличения тепловых колебаний атомов. Рост Т приводит к деформациям и разрывам в электронной плотности. Пусть ni - масса компонента i, µi - химический его потенциал. Согласно Гиббсу:
 U = H - PV (52) где U - внутренняя энергия системы. G = H - TS (54) - уравнение Гиббса - Гельмгольца. G экстенсивный параметр, т. е. зависит от массы системы. При Р = 0 и Т = 0 G 00 = H 00 (55) При Т ≠ 0 G 0 T = H 0 T - T S 0 T (56) G 0 T - H 0 T = - TS 0 T (57) где:
U = H - PV (52) где U - внутренняя энергия системы. G = H - TS (54) - уравнение Гиббса - Гельмгольца. G экстенсивный параметр, т. е. зависит от массы системы. При Р = 0 и Т = 0 G 00 = H 00 (55) При Т ≠ 0 G 0 T = H 0 T - T S 0 T (56) G 0 T - H 0 T = - TS 0 T (57) где:
 В качестве стандартного состояния часто выбирают Т = 298 о. К. Тогда
В качестве стандартного состояния часто выбирают Т = 298 о. К. Тогда
 Уравнение Гиббса – Гельмгольца показывает, что возрастание Т снижает свободную энергию. Следовательно, химическая связь действительно изменяет свой характер (рис. 11).
Уравнение Гиббса – Гельмгольца показывает, что возрастание Т снижает свободную энергию. Следовательно, химическая связь действительно изменяет свой характер (рис. 11).
 Рис. 11
Рис. 11
 Выберем два состояния фазым – кристаллическое (cr) и расплавленное (liq) – и попробуем оценить изменение прочности и качества химической связи при росте температуры вплоть до фазового перехода cr liq. Если энтальпия отражает прочность и степень ионности связей (ion), то свободная энергия – их качество, т. е. эластичность (elast) или жесткость. В кристаллах связи ковалентные и жесткие, а в расплаве предельно ионные и эластичные. Следовательно, с переходом от первых ко вторым должная изменяться не только степень ионности связей (ŋion)
Выберем два состояния фазым – кристаллическое (cr) и расплавленное (liq) – и попробуем оценить изменение прочности и качества химической связи при росте температуры вплоть до фазового перехода cr liq. Если энтальпия отражает прочность и степень ионности связей (ion), то свободная энергия – их качество, т. е. эластичность (elast) или жесткость. В кристаллах связи ковалентные и жесткие, а в расплаве предельно ионные и эластичные. Следовательно, с переходом от первых ко вторым должная изменяться не только степень ионности связей (ŋion)
 но и степень их эластичности (ŋelasr): Степень ионности можно привести к степени ионности связи по Л. Полингу. В результате получим следующее выражение: где – степень ионности связи атомов в двухатомных молекулах солей, окислов сульфидов и т. п. при 298 К – вычисляется как функция электроотрицательностей. Соотношения всех этих рассмотренных характеристик химической связи приведены на рис. 12.
но и степень их эластичности (ŋelasr): Степень ионности можно привести к степени ионности связи по Л. Полингу. В результате получим следующее выражение: где – степень ионности связи атомов в двухатомных молекулах солей, окислов сульфидов и т. п. при 298 К – вычисляется как функция электроотрицательностей. Соотношения всех этих рассмотренных характеристик химической связи приведены на рис. 12.
 Рис. 12. Температурная зависимость степени ионности и степени эластичности связей в кристалле галита при давлении 1 атм.
Рис. 12. Температурная зависимость степени ионности и степени эластичности связей в кристалле галита при давлении 1 атм.
 Связь свободной энергии с константой химической реакции КР А + В + С = АВС ( 67 ) и µА + µB + µC = µАBC где µi – химический потенциал или парциальная молярная свободная энергия компонента i (в данном случае i = минерал) и тогда можно записать выражение связи константы КР химической реакции (67) с изменением свободной энергией Гиббса где – свободная энергия образования минерала i из элементов, а знак перед RTln. Kp укажет в какую сторону смещена реакция (67). В случае равновесия
Связь свободной энергии с константой химической реакции КР А + В + С = АВС ( 67 ) и µА + µB + µC = µАBC где µi – химический потенциал или парциальная молярная свободная энергия компонента i (в данном случае i = минерал) и тогда можно записать выражение связи константы КР химической реакции (67) с изменением свободной энергией Гиббса где – свободная энергия образования минерала i из элементов, а знак перед RTln. Kp укажет в какую сторону смещена реакция (67). В случае равновесия
 Величины свободной энергии образования минералов из элементов в различных изданиях обозначают по разному:
Величины свободной энергии образования минералов из элементов в различных изданиях обозначают по разному:
 если известна величина из (68) можно найти :
если известна величина из (68) можно найти :
 Через индекс Zo лучше обозначать потенциал Коржинского. Индекс F теперь почти не употребляется. Наиболее распространен индекс G. Следует помнить, что если в реакции типа (67) фазы А, В и С представлены элементами, то и где – cвободная энергия образования соединения АВС из элементов А, В и С.
Через индекс Zo лучше обозначать потенциал Коржинского. Индекс F теперь почти не употребляется. Наиболее распространен индекс G. Следует помнить, что если в реакции типа (67) фазы А, В и С представлены элементами, то и где – cвободная энергия образования соединения АВС из элементов А, В и С.
 Если не известно уравнение температурной зависимости теплоемкости, расчет свободной энергии образования минералов в высокотемпературной области можно производить по упрощенной формуле:
Если не известно уравнение температурной зависимости теплоемкости, расчет свободной энергии образования минералов в высокотемпературной области можно производить по упрощенной формуле:
 При расчете реакций в зависимости от Т и Р: где Vэ. я. – объем элементарной ячейки минерала, а Z – его координационное число.
При расчете реакций в зависимости от Т и Р: где Vэ. я. – объем элементарной ячейки минерала, а Z – его координационное число.
 Объемы элементарной ячейки (э. я. ) для различных сингоний Сингония , , a, b, c V(Å3) (упрощенные формулы) 90 о а b с Моноклинная 90 о, 90 о а b с Ромбическая Тетрагональная 90 о а b с а= b с abc a 2 c Кубическая 90 о а=b=с a 3 Триклинная Гексагональная 90 о, =120 о Тригональная 90 о, 90 о а=b с а=b=с=аrh -
Объемы элементарной ячейки (э. я. ) для различных сингоний Сингония , , a, b, c V(Å3) (упрощенные формулы) 90 о а b с Моноклинная 90 о, 90 о а b с Ромбическая Тетрагональная 90 о а b с а= b с abc a 2 c Кубическая 90 о а=b=с a 3 Триклинная Гексагональная 90 о, =120 о Тригональная 90 о, 90 о а=b с а=b=с=аrh -
 ГАЗЫ И ИХ СМЕСИ Идеальный газ i: Реальный газ i:
ГАЗЫ И ИХ СМЕСИ Идеальный газ i: Реальный газ i:
 где i фугитивность чистого газа i. Для идеального газа: i =Pi (87) Для реального i = i. Pi (88) где i - коэффициент фугитивности (летучести) Пусть Рist – давление в стандартном состоянии газа. Тогда: Рассмотрим методы расчета свойств реальных газов.
где i фугитивность чистого газа i. Для идеального газа: i =Pi (87) Для реального i = i. Pi (88) где i - коэффициент фугитивности (летучести) Пусть Рist – давление в стандартном состоянии газа. Тогда: Рассмотрим методы расчета свойств реальных газов.
 Почему методы расчета, а не экспериментальные данные? Ответ на этот вопрост: Петрологам необходимы данные при высоких Т-Р. Но вот здесь как раз долгое время существовала прореха: были хорошо изучены свойства газов при (1) высоких значениях давления, но при относительно низкой температуре, и при (2) низком давлении и высокой температуре (см. рис. ). Такое положение вещей было обусловлено необходимостью экспериментальных данных по свойствам газов и их смесей в приложении к решению технических задач (паровые котлы, ракетная техника, сжижение газов и т. п. )
Почему методы расчета, а не экспериментальные данные? Ответ на этот вопрост: Петрологам необходимы данные при высоких Т-Р. Но вот здесь как раз долгое время существовала прореха: были хорошо изучены свойства газов при (1) высоких значениях давления, но при относительно низкой температуре, и при (2) низком давлении и высокой температуре (см. рис. ). Такое положение вещей было обусловлено необходимостью экспериментальных данных по свойствам газов и их смесей в приложении к решению технических задач (паровые котлы, ракетная техника, сжижение газов и т. п. )
 1. Принцип соответственных состояний Приведенные параметры. Существует общая функциональная связь между приведенными параметрами любых газов, т. е. отношения данных T, P и V к значениям этих параметров в критических (кр) точках: Критическая точка определяется предельными значениями T и P, при которых исчезает разница между жидкостью и газом и возникает надкритический флюид. Однако и здесь не все так просто: в каждой из фаз сохраняются частички противоположной фазы. Посмотрите схематические диаграммы на рис. 13 и 14.
1. Принцип соответственных состояний Приведенные параметры. Существует общая функциональная связь между приведенными параметрами любых газов, т. е. отношения данных T, P и V к значениям этих параметров в критических (кр) точках: Критическая точка определяется предельными значениями T и P, при которых исчезает разница между жидкостью и газом и возникает надкритический флюид. Однако и здесь не все так просто: в каждой из фаз сохраняются частички противоположной фазы. Посмотрите схематические диаграммы на рис. 13 и 14.
 Рис. 13. Критическая точка в системе жидкость – пар
Рис. 13. Критическая точка в системе жидкость – пар
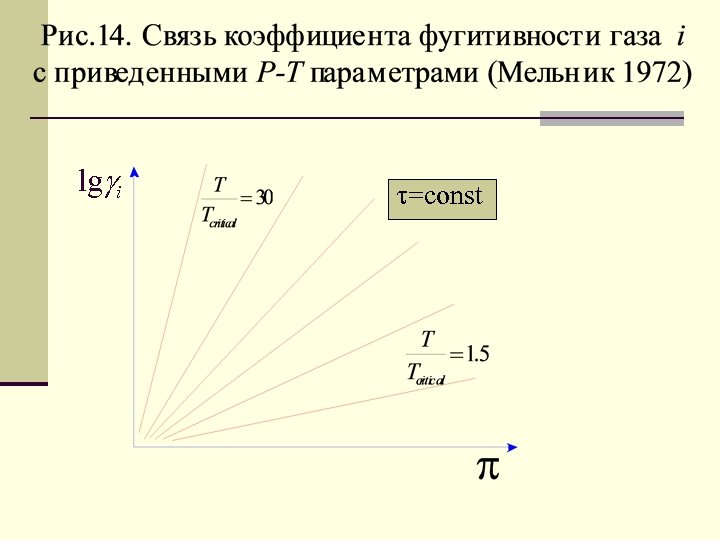 lg i =const
lg i =const
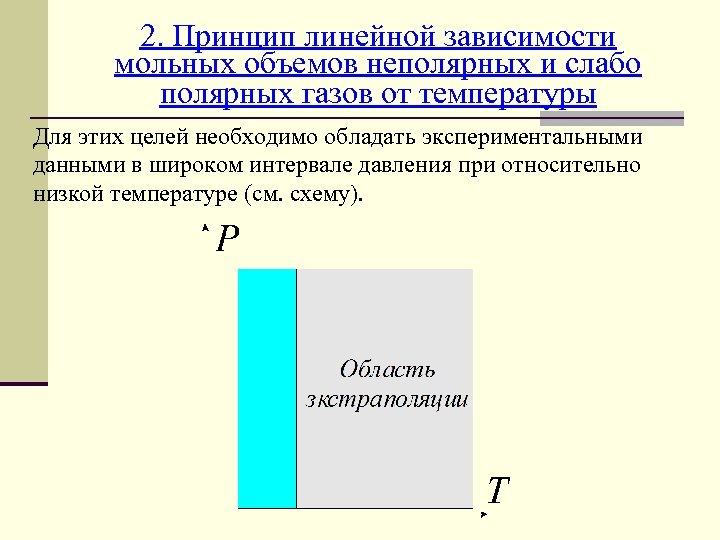 2. Принцип линейной зависимости мольных объемов неполярных и слабо полярных газов от температуры Для этих целей необходимо обладать экспериментальными данными в широком интервале давления при относительно низкой температуре (см. схему).
2. Принцип линейной зависимости мольных объемов неполярных и слабо полярных газов от температуры Для этих целей необходимо обладать экспериментальными данными в широком интервале давления при относительно низкой температуре (см. схему).
 СО 2
СО 2
 Для СО 2 из (85) и (86) можно получить выражение относительной молярной свободной энергии Гиббса Из (93) изотермическое выражение относительной молярной свободной энергии Гиббса для СО 2 имеет вид: где - приращение энергии Гиббса при Р=const с возрастанием Т. При P=1 атм эта величина определяется таким эмпирическим уравнением:
Для СО 2 из (85) и (86) можно получить выражение относительной молярной свободной энергии Гиббса Из (93) изотермическое выражение относительной молярной свободной энергии Гиббса для СО 2 имеет вид: где - приращение энергии Гиббса при Р=const с возрастанием Т. При P=1 атм эта величина определяется таким эмпирическим уравнением:
 Обычно табулируется, либо имеет аналитическое выражение. Но в основе так или иначе лежит сжимаемость CO 2 в широком интервале Т и Р: Полное описание термодинамических свойств СО 2 можно найти в справочнике В. М. Шмонова и К. И. Шмуловича (1975), основанном на собственных экспериментальных PVT данных, которые оказались практически идентичными расчетным (см. рис. 15 и 16, а также Мельник, 1978).
Обычно табулируется, либо имеет аналитическое выражение. Но в основе так или иначе лежит сжимаемость CO 2 в широком интервале Т и Р: Полное описание термодинамических свойств СО 2 можно найти в справочнике В. М. Шмонова и К. И. Шмуловича (1975), основанном на собственных экспериментальных PVT данных, которые оказались практически идентичными расчетным (см. рис. 15 и 16, а также Мельник, 1978).
 Рис. 15. Изобарическая линейная связь мольного объема СО 2 с температурой (Перчук, 1973; Перчук и Карпов, 1975; закрашена область исходных экспериментальных данных)
Рис. 15. Изобарическая линейная связь мольного объема СО 2 с температурой (Перчук, 1973; Перчук и Карпов, 1975; закрашена область исходных экспериментальных данных)
 Рис. 16. Изобары зависимости от температуры относительной молярной свободной энергии Гиббса для углекислоты, = =
Рис. 16. Изобары зависимости от температуры относительной молярной свободной энергии Гиббса для углекислоты, = =
 H 2 O
H 2 O
 Критическая точка для воды определена при Т =373. 46 о. С и Р = 221. 2 бар. Аномальные свойства воды известны достаточно широко. Однако мало кому известно, что Н 2 О кристаллизуется в восьми полиморфных модификациях (рис. 17 б), а до Р ~ 3000 бар мольный объем воды не связан линейно с температурой (рис. 18). Между тем приращение свободной энергии с температурой при 1 атм. , как и для СО 2, хорошо описывается «кубическим» уравнением Аналитическое выражение свободной энергии Гиббса для Н 2 О, выведенное из «первых принципов» квантовой физики (Gerya & Perchuk, 1997), широко используется для расчета реакций гидратациидегидратации минералов.
Критическая точка для воды определена при Т =373. 46 о. С и Р = 221. 2 бар. Аномальные свойства воды известны достаточно широко. Однако мало кому известно, что Н 2 О кристаллизуется в восьми полиморфных модификациях (рис. 17 б), а до Р ~ 3000 бар мольный объем воды не связан линейно с температурой (рис. 18). Между тем приращение свободной энергии с температурой при 1 атм. , как и для СО 2, хорошо описывается «кубическим» уравнением Аналитическое выражение свободной энергии Гиббса для Н 2 О, выведенное из «первых принципов» квантовой физики (Gerya & Perchuk, 1997), широко используется для расчета реакций гидратациидегидратации минералов.
 Рис. 17. Диаграммы состояния H 2 O а б
Рис. 17. Диаграммы состояния H 2 O а б
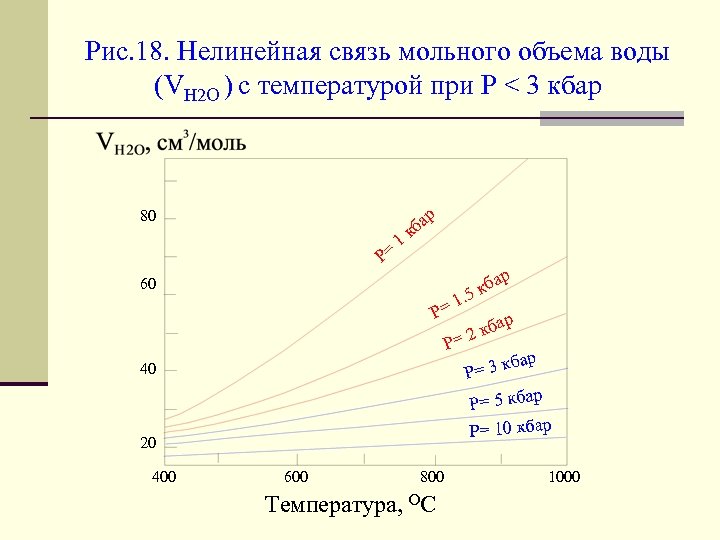 Рис. 18. Нелинейная связь мольного объема воды (VH 2 O ) c температурой при Р < 3 кбар р 80 Р= 1 а кб р 60 Р= 1 кба. 5 Р= 40 р кба Р= 3 Р= 5 кбар Р= 10 кбар 20 400 р а 2 кб 600 Температура, 800 ОС 1000
Рис. 18. Нелинейная связь мольного объема воды (VH 2 O ) c температурой при Р < 3 кбар р 80 Р= 1 а кб р 60 Р= 1 кба. 5 Р= 40 р кба Р= 3 Р= 5 кбар Р= 10 кбар 20 400 р а 2 кб 600 Температура, 800 ОС 1000
 Расчет реакций с участием флюида СО 2. Реакция карбонатизации волластонита Са. Si. O 3 + CO 2 = Ca. CО 3 + Si. O 2 (97) т. е. Wol +CO 2 = Cal + Qz В состоянии равновесия согласно условию (79) Если известны Р, Т и рассчитать значение , то из (98) легко :
Расчет реакций с участием флюида СО 2. Реакция карбонатизации волластонита Са. Si. O 3 + CO 2 = Ca. CО 3 + Si. O 2 (97) т. е. Wol +CO 2 = Cal + Qz В состоянии равновесия согласно условию (79) Если известны Р, Т и рассчитать значение , то из (98) легко :
 Если флюид состоит только из СО 2 , то определить из расчетной формулы (103) невозможно. Необходимо предварительно решить пропорцию: прямо Здесь два неизвестных и одно уравнение. Нужна еще одна реакция при тех же РS и Т. Давление можно предварительно определить, рассчитав диаграмму PST c изобарами PCO 2. Тогда задача решается тривиально.
Если флюид состоит только из СО 2 , то определить из расчетной формулы (103) невозможно. Необходимо предварительно решить пропорцию: прямо Здесь два неизвестных и одно уравнение. Нужна еще одна реакция при тех же РS и Т. Давление можно предварительно определить, рассчитав диаграмму PST c изобарами PCO 2. Тогда задача решается тривиально.
 Аналогичным образом решаются задачи по определению фугитивностей кислорода, воды и др. летучих компонентов. Необходимы лишь данные по свободным энергиям образования минералов из элементов и сжатым газам. Расчетом некоторых реакций гидратации-дегидратации с использованием известных баз данных вы займетесь на практических занятиях. Здесь же мы рассмотрим метод расчета f. О 2 в реакциях окисления металлов (Ме): к которым можно применить общую формулу
Аналогичным образом решаются задачи по определению фугитивностей кислорода, воды и др. летучих компонентов. Необходимы лишь данные по свободным энергиям образования минералов из элементов и сжатым газам. Расчетом некоторых реакций гидратации-дегидратации с использованием известных баз данных вы займетесь на практических занятиях. Здесь же мы рассмотрим метод расчета f. О 2 в реакциях окисления металлов (Ме): к которым можно применить общую формулу
 В качестве примера произведем расчет реакции окисления магнетита (Mag) c образованием гематита (Hem) 2 Fe 3 O 4 + 1/2 O 2 = 3 Fe 2 O 3 при Рs = 1 бар и Т = 800 К c использованием базы термодинамических данных (Powel & Holland, 1998):
В качестве примера произведем расчет реакции окисления магнетита (Mag) c образованием гематита (Hem) 2 Fe 3 O 4 + 1/2 O 2 = 3 Fe 2 O 3 при Рs = 1 бар и Т = 800 К c использованием базы термодинамических данных (Powel & Holland, 1998):
 ТЕРМОДИНАМИКА МИНЕРАЛОВ ПРЕМЕННОГО СОСТАВА Мольные доли n В бинарной смеси 1 и 2 Например, нефелин из рисчоррита Хибинского массива имеет такой состав:
ТЕРМОДИНАМИКА МИНЕРАЛОВ ПРЕМЕННОГО СОСТАВА Мольные доли n В бинарной смеси 1 и 2 Например, нефелин из рисчоррита Хибинского массива имеет такой состав:
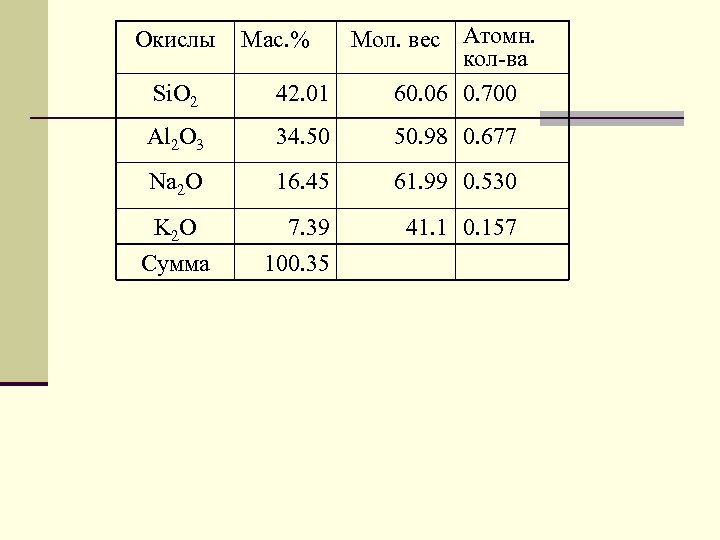 Si. O 2 Мол. вес Атомн. кол-ва 42. 01 60. 06 0. 700 Al 2 O 3 34. 50 50. 98 0. 677 Na 2 O 16. 45 61. 99 0. 530 K 2 O Сумма 7. 39 100. 35 41. 1 0. 157 Окислы Mac. %
Si. O 2 Мол. вес Атомн. кол-ва 42. 01 60. 06 0. 700 Al 2 O 3 34. 50 50. 98 0. 677 Na 2 O 16. 45 61. 99 0. 530 K 2 O Сумма 7. 39 100. 35 41. 1 0. 157 Окислы Mac. %
 В многокомпонентных смесях (твердых, жидких или газовых) Относительные термодинамические функции (функции смешения) Парциальные (Р и Т const) Фi m = Ф i - Фi 0 Интегральные (P и T const) Фm = Ф - Ф 0 (112) (113) Парциальный молярный объем смешения (или относительный молярный объем компонента i в минерале): Vim = Vi 0 (114)
В многокомпонентных смесях (твердых, жидких или газовых) Относительные термодинамические функции (функции смешения) Парциальные (Р и Т const) Фi m = Ф i - Фi 0 Интегральные (P и T const) Фm = Ф - Ф 0 (112) (113) Парциальный молярный объем смешения (или относительный молярный объем компонента i в минерале): Vim = Vi 0 (114)
 Он характеризует изменение полного объема раствора при смешении 1 моля чистого компонента i с бесконечно большим количеством раствора данного состава. Парциальная молярная энтропия смешения (или относительная парциальная молярная энтропия) Sim = Si - Si 0 (115) Парциальная молярная энтальпия смешения (или относительная парциальная молярная энтальпия). Нi m = Hi - Hi 0 (116) Парциальная молярная свободная энергия смешения (или относительная парциальная молярная свободная энергия)
Он характеризует изменение полного объема раствора при смешении 1 моля чистого компонента i с бесконечно большим количеством раствора данного состава. Парциальная молярная энтропия смешения (или относительная парциальная молярная энтропия) Sim = Si - Si 0 (115) Парциальная молярная энтальпия смешения (или относительная парциальная молярная энтальпия). Нi m = Hi - Hi 0 (116) Парциальная молярная свободная энергия смешения (или относительная парциальная молярная свободная энергия)
 Связь между парциальными величинами следует из уравнения (50) Уравнения Дюгема:
Связь между парциальными величинами следует из уравнения (50) Уравнения Дюгема:
 и запомним для дальнейших преобразований.
и запомним для дальнейших преобразований.
 Интегральные величины Они определяют разность между данной термодинамической величиной одного моля раствора и суммой соответствующих термодинамических величин чистых компонентов, слагающих данную смесь при постоянных Т и Р. Фm = Ф - (Х 1 Ф 10 + Х 2 Ф 20) (128) Интегральный молярный объем смешения (или относительный интегральный мольный объем) – изменение объема при образовании 1 моля раствора из Х 1 молей чистого компонента 1 и 1 -Х 1 чистого компонента 2. В соответствии со (128) записываем:
Интегральные величины Они определяют разность между данной термодинамической величиной одного моля раствора и суммой соответствующих термодинамических величин чистых компонентов, слагающих данную смесь при постоянных Т и Р. Фm = Ф - (Х 1 Ф 10 + Х 2 Ф 20) (128) Интегральный молярный объем смешения (или относительный интегральный мольный объем) – изменение объема при образовании 1 моля раствора из Х 1 молей чистого компонента 1 и 1 -Х 1 чистого компонента 2. В соответствии со (128) записываем:
 Интегральная молярная энтропия смешения (относительная интегральная молярная энтропия) – изменение при образовании одного моля раствора из Х 1 молей чистого компонента 1 и Х 2 молей компонента 2 при данных Т и Р: Интегральная молярная энтальпия смешения определяет теплоту, которую необходимо затратить при данных Т и Р для создания одного моля раствора из Х 1 молей чистого компонента 1 и Х 2 молей компонента 2:
Интегральная молярная энтропия смешения (относительная интегральная молярная энтропия) – изменение при образовании одного моля раствора из Х 1 молей чистого компонента 1 и Х 2 молей компонента 2 при данных Т и Р: Интегральная молярная энтальпия смешения определяет теплоту, которую необходимо затратить при данных Т и Р для создания одного моля раствора из Х 1 молей чистого компонента 1 и Х 2 молей компонента 2:
 Из уравнения Гиббса-Гельмгольца (50) вытекают соотношения, применимые как к парциальным, так и к интегральным величинам
Из уравнения Гиббса-Гельмгольца (50) вытекают соотношения, применимые как к парциальным, так и к интегральным величинам
 Идеальные растворы Идеальными называются растворы, для которых объем и энтальпия смешения равны нулю: Но остальные относительные функции при данных Т и Р зависят от состава фаз:
Идеальные растворы Идеальными называются растворы, для которых объем и энтальпия смешения равны нулю: Но остальные относительные функции при данных Т и Р зависят от состава фаз:
 Эти величины могут быть получены на основе статической термодинамики Sm Sпозиционная = кln. W (148) где к – константа Больцмана, W – вероятность, т. е. оптимальное число способов размещения атомов в кристаллической решетке:
Эти величины могут быть получены на основе статической термодинамики Sm Sпозиционная = кln. W (148) где к – константа Больцмана, W – вероятность, т. е. оптимальное число способов размещения атомов в кристаллической решетке:
 Так как раствор идеальный (Нm=0), то вероятность в (149) обозначает возможное число замен атомов одного сорта атомами другого сорта без изменения энергии кристаллической решетки. Далее используем так называемое правило Стирлинга: Ai! = exp(Ailn. Ai -Ai), (150) где Аi - общее число взаимозаменяемых атомов в одном моле раствора. В случае суммы его можно представить в таком виде:
Так как раствор идеальный (Нm=0), то вероятность в (149) обозначает возможное число замен атомов одного сорта атомами другого сорта без изменения энергии кристаллической решетки. Далее используем так называемое правило Стирлинга: Ai! = exp(Ailn. Ai -Ai), (150) где Аi - общее число взаимозаменяемых атомов в одном моле раствора. В случае суммы его можно представить в таком виде:
 Логарифмируем (149) и, используя (151), находим: где А 0 – число Авогадро, а R = к. A 0 (154) В (149) подставляем (152) и (154) и, учитывая (153), находим
Логарифмируем (149) и, используя (151), находим: где А 0 – число Авогадро, а R = к. A 0 (154) В (149) подставляем (152) и (154) и, учитывая (153), находим
 Уравнение (157) идентично уравнению (147). Энтропия – мера изменения свободной энергии от температуры. Следовательно уравнения (118) и (134) полностью распространяются на идеальные растворы. В соответствии с (137), (129) и (131) для идеальных растворов справедливы ур-я (138) и (139). Посмотрите диаграммы с концентрационными зависимостями и (Рис. 19) (отдельно для каждого значения Т дается.
Уравнение (157) идентично уравнению (147). Энтропия – мера изменения свободной энергии от температуры. Следовательно уравнения (118) и (134) полностью распространяются на идеальные растворы. В соответствии с (137), (129) и (131) для идеальных растворов справедливы ур-я (138) и (139). Посмотрите диаграммы с концентрационными зависимостями и (Рис. 19) (отдельно для каждого значения Т дается.
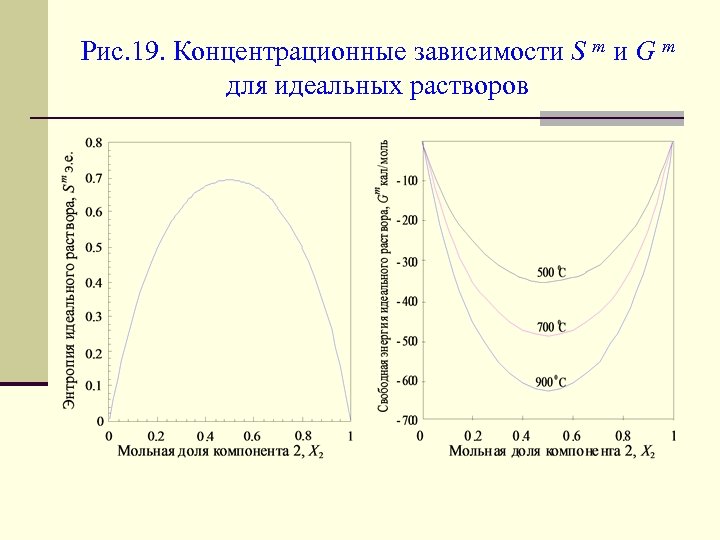 Рис. 19. Концентрационные зависимости S m и G m для идеальных растворов
Рис. 19. Концентрационные зависимости S m и G m для идеальных растворов
 Избыточные функции (Фе, Фiе) Они определяют степень отклонения данного реального раствора от идеального. И в соответствии со (137) V m = V e, V im = V ie (158) Hm = He , Hi m = Hi e (159) И далее: Sie = Sim(реальн) - Sim(идеальн) (160) Se = Sm(реальн) - Sm(идеальн) (161) Gie = Gim(реальн) - Gim(идеальн) (162) Ge = Gm (реальн) - Gm(идеальн) (163) Подставляем в (160) - (163) уравнения (142)-(145) и находим:
Избыточные функции (Фе, Фiе) Они определяют степень отклонения данного реального раствора от идеального. И в соответствии со (137) V m = V e, V im = V ie (158) Hm = He , Hi m = Hi e (159) И далее: Sie = Sim(реальн) - Sim(идеальн) (160) Se = Sm(реальн) - Sm(идеальн) (161) Gie = Gim(реальн) - Gim(идеальн) (162) Ge = Gm (реальн) - Gm(идеальн) (163) Подставляем в (160) - (163) уравнения (142)-(145) и находим:


 Рис. 20. Графическое представление избыточных функций (диагрпммы А и Б) и связь интегральной величины с парциальными через уравнение касательной (Б) А Б
Рис. 20. Графическое представление избыточных функций (диагрпммы А и Б) и связь интегральной величины с парциальными через уравнение касательной (Б) А Б
 Еще два уравнения связи парциальных функций с интегральными: Регулярные растворы Представление о них ввел Гильдебрандт, предложивший принять избыточную энтропию, равной нулю: Se = 0, Ge = Hm (180) Sie = 0, Gie = Him (181) Тогда
Еще два уравнения связи парциальных функций с интегральными: Регулярные растворы Представление о них ввел Гильдебрандт, предложивший принять избыточную энтропию, равной нулю: Se = 0, Ge = Hm (180) Sie = 0, Gie = Him (181) Тогда
 Для регулярных растворов характерна симметричная форма концентрационных зависимостей Ge и Ve. Избыточные парциальные молярные функции связаны между собой уравнениями Дюгема (см. также 120 - 127 и сравнить): X 1 d. V 1 e+X 2 d. V 2 e = 0 X 1 d. H 1 e+X 2 d. H 2 e = 0 (184) X 1 d. S 1 e+X 2 d. S 2 e = 0 (185) X 1 d. G 1 e+X 2 d. G 2 e = 0 или же : (183) (186)
Для регулярных растворов характерна симметричная форма концентрационных зависимостей Ge и Ve. Избыточные парциальные молярные функции связаны между собой уравнениями Дюгема (см. также 120 - 127 и сравнить): X 1 d. V 1 e+X 2 d. V 2 e = 0 X 1 d. H 1 e+X 2 d. H 2 e = 0 (184) X 1 d. S 1 e+X 2 d. S 2 e = 0 (185) X 1 d. G 1 e+X 2 d. G 2 e = 0 или же : (183) (186)
 Эти уравнения будут нами использованы в теории фазового соответствия.
Эти уравнения будут нами использованы в теории фазового соответствия.
 Влияние третьего компонента на термодинамические величины бинарного раствора Этот вопрос сложный, но очень важный. Необходимо запомнить, что каждое из приведенных выше уравнений справедливо и для тройных растворов, если (Х 1/Х 2)Т, Р = const или концентрация компонента 3 в этом растворе постоянна. Например: Вместе с тем существуют термодинамические модели, учитывающие взаимодействие всех компонентов в сложных растворах. Обычно они очень громоздкие, поэтому в уравнения термобарометров принято вводить эмпирические поправки на содержание третьего изоморфного компонента.
Влияние третьего компонента на термодинамические величины бинарного раствора Этот вопрос сложный, но очень важный. Необходимо запомнить, что каждое из приведенных выше уравнений справедливо и для тройных растворов, если (Х 1/Х 2)Т, Р = const или концентрация компонента 3 в этом растворе постоянна. Например: Вместе с тем существуют термодинамические модели, учитывающие взаимодействие всех компонентов в сложных растворах. Обычно они очень громоздкие, поэтому в уравнения термобарометров принято вводить эмпирические поправки на содержание третьего изоморфного компонента.
 Tермодинамическая активность где аi - активность компонента в растворе (смеси): В идеальной газовой смеси: аi = Pio= Xi. P (196)
Tермодинамическая активность где аi - активность компонента в растворе (смеси): В идеальной газовой смеси: аi = Pio= Xi. P (196)
 Эмпирические формулы для расчета избыточных термодинамических функций 1. Ряды Маргулеса для бинарных смесей при постоянных Т и Р
Эмпирические формулы для расчета избыточных термодинамических функций 1. Ряды Маргулеса для бинарных смесей при постоянных Т и Р
 В общем случае избыточные парциальные молярные величины при постоянных Т и Р зависят от состава фазы по формулам:
В общем случае избыточные парциальные молярные величины при постоянных Т и Р зависят от состава фазы по формулам:
 Уравнения (204) и (205) иногда называют рядами Гуггенхейма, хотя правильно было бы их называть рядами Маргулеса. В случае n=3 эти ряды имеют вид (для избыточных энергий): В простейшем случае, когда n = 3 концентрационную зависимость G 1 e или G 2 e можно выразить в виде обычного степенного ряда:
Уравнения (204) и (205) иногда называют рядами Гуггенхейма, хотя правильно было бы их называть рядами Маргулеса. В случае n=3 эти ряды имеют вид (для избыточных энергий): В простейшем случае, когда n = 3 концентрационную зависимость G 1 e или G 2 e можно выразить в виде обычного степенного ряда:
 По определению при Х 1 = 0 или Х 2 = 0 величины G 1 e и G 2 e обращаются в 0. Следовательно и AG 01 и AG 02 в рядах (209) и (210) равны нулю. Если продифференцировать (209) и (210) и подставить величины d. G 1 e и d. G 2 e в уравнение Дюгема: X 1 d. G 1 e + X 2 d. G 2 e = 0 (211) то можно выразить одни коэффициенты через другие. И тогда:
По определению при Х 1 = 0 или Х 2 = 0 величины G 1 e и G 2 e обращаются в 0. Следовательно и AG 01 и AG 02 в рядах (209) и (210) равны нулю. Если продифференцировать (209) и (210) и подставить величины d. G 1 e и d. G 2 e в уравнение Дюгема: X 1 d. G 1 e + X 2 d. G 2 e = 0 (211) то можно выразить одни коэффициенты через другие. И тогда:
 Уравнение (216) легко проверить, выразив его через парциальные величины (214) и (215) и учтя, что Х 1+Х 2=1, Расчеты по этим формулам можно проводить для некоторых Fe-Mg минералов (оливина, биотита, ортопироксена и т. п. ). Рассмотрим физический смысл коэффициентов в рядах. Согласно правилу Тейлора, любая функция может быть разложена в ряд по возрастающим
Уравнение (216) легко проверить, выразив его через парциальные величины (214) и (215) и учтя, что Х 1+Х 2=1, Расчеты по этим формулам можно проводить для некоторых Fe-Mg минералов (оливина, биотита, ортопироксена и т. п. ). Рассмотрим физический смысл коэффициентов в рядах. Согласно правилу Тейлора, любая функция может быть разложена в ряд по возрастающим
 Обозначим и получим ряды (209) и (210). В этом случае коэффициенты в (218) и (219) определяются следующими соотношениями:
Обозначим и получим ряды (209) и (210). В этом случае коэффициенты в (218) и (219) определяются следующими соотношениями:
 Расчет избыточных функций по кривым распада смесей Рассмотрим простейший случай равной растворимости компонентов на субсолидусе, т. е. его симметричность (рис. 21): Рис. 21
Расчет избыточных функций по кривым распада смесей Рассмотрим простейший случай равной растворимости компонентов на субсолидусе, т. е. его симметричность (рис. 21): Рис. 21
 Условие равновесия при Т 1: С использованием уравнений (117) и (193) находим: Так как фазы α и β образуют один ряд твердых растворов компонентов 1 и 2, то с учетом (222) уравнения (220) и (221) можно переписать так: где
Условие равновесия при Т 1: С использованием уравнений (117) и (193) находим: Так как фазы α и β образуют один ряд твердых растворов компонентов 1 и 2, то с учетом (222) уравнения (220) и (221) можно переписать так: где
 С учетом (214) и (215) эти уравнения переписываем в таком виде: Используя диаграмму с кривой распада (при каждой данной Т находим Х 1 =1 -Х 2 и Х 2 = 1 -Х 1 ), решаем эту систему уравнений 2 го порядка и находим коэффициенты А и А .
С учетом (214) и (215) эти уравнения переписываем в таком виде: Используя диаграмму с кривой распада (при каждой данной Т находим Х 1 =1 -Х 2 и Х 2 = 1 -Х 1 ), решаем эту систему уравнений 2 го порядка и находим коэффициенты А и А .
 Следовательно, нам известны концентрационные зависимости парциальных молярных энергий (избыточных) при данной Т 1. Например: Если твердый раствор близок к регулярному, величину А в уравнениях (214) и (215) можно найти по формуле: A = 2 RTкр (233) Она выводится просто. По определению:
Следовательно, нам известны концентрационные зависимости парциальных молярных энергий (избыточных) при данной Т 1. Например: Если твердый раствор близок к регулярному, величину А в уравнениях (214) и (215) можно найти по формуле: A = 2 RTкр (233) Она выводится просто. По определению:
 Дважды дифференцируем (234) по Х 1 и находим: При Х 1 = 0. 5 получаем уравнение (233).
Дважды дифференцируем (234) по Х 1 и находим: При Х 1 = 0. 5 получаем уравнение (233).
 Расчет избыточных функций по равновесиям минерал–водный раствор Пусть – твердый раствор компонентов 1 и 2, а водный раствор, близкий по свойствам к разбавленному. Изоморфные компоненты – общие для обоих растворов. 1 + 2 = 1 + 2 Условие бесконечной разбавленности дает: (239)
Расчет избыточных функций по равновесиям минерал–водный раствор Пусть – твердый раствор компонентов 1 и 2, а водный раствор, близкий по свойствам к разбавленному. Изоморфные компоненты – общие для обоих растворов. 1 + 2 = 1 + 2 Условие бесконечной разбавленности дает: (239)
 Используя уравнения (225) и (226), а также условие (239), находим: Вычтем из (240) уравнение (241): где Обозначим:
Используя уравнения (225) и (226), а также условие (239), находим: Вычтем из (240) уравнение (241): где Обозначим:
 Выражая находим: через и используя (245) и (247),
Выражая находим: через и используя (245) и (247),
 Аналогичным образом находим: Интегрирование этих значений можно произвести графически (рис. 22). ЖЕЛАЮ ВАМ УСПЕШНО СПРАВИТЬСЯ С ЭТИМ ЗАДАНИЕМ НА ПРАКТИЧЕСКИХ ЗАНЯТИЯХ!! Там же Вы пройдете метод расчета избыточных функций по пределам стабильности минералов переменного состава в присутствии газовой среды.
Аналогичным образом находим: Интегрирование этих значений можно произвести графически (рис. 22). ЖЕЛАЮ ВАМ УСПЕШНО СПРАВИТЬСЯ С ЭТИМ ЗАДАНИЕМ НА ПРАКТИЧЕСКИХ ЗАНЯТИЯХ!! Там же Вы пройдете метод расчета избыточных функций по пределам стабильности минералов переменного состава в присутствии газовой среды.
 Рис. 22. Графический расчет избыточных парциальных молярных свободных энергий Гиббса по ур-ям (245 а) и (246 а)
Рис. 22. Графический расчет избыточных парциальных молярных свободных энергий Гиббса по ур-ям (245 а) и (246 а)


