b11b73a96b82163c5c7e18a9d1530af6.ppt
- Количество слайдов: 70

“L’EVOLUZIONE E’ OGGI” 19 Settembre 2013 Ospedale “SS Antonio e Margherita”, Tortona Dabigatran: istruzioni pratiche d’uso i Dott. Sergio Agosti Cardiologo, Ospedale Novi Ligure (AL) www. docvadis. it/agostisergio@virgilio. it

Come comportarsi di fronte ad indicazione a PRADAXA…. .

A quali pazienti somministrare Dabigatran


RE-LY® – Criteri di inclusione 1. FA non valvolare documentata e 2. Almeno un fattore di rischio aggiuntivo per l’ictus: a. Storia di ictus pregresso, TIA, o embolia sistemica b. LVEF <40% c. Insufficienza cardiaca sintomatica, NYHA di Classe II o superiore d. Età ≥ 75 anni e. Età ≥ 65 anni e uno dei seguenti fattori di rischio aggiuntivi: diabete mellito, coronaropatia o ipertensione Ezekowitz MD, et al. Am Heart J 2009; 157: 805 -810. Dabigatran etexilato è in sviluppo clinico e non è approvato per l’uso in clinica per la prevenzione dell’ictus nei pazienti con fibrillazione atriale. Connolly SJ, et al. N Engl J Med 2009; 361: 1139 -1151.

Piano Terapeutico

Nuovi Anticoagulanti Orali (NAO): a quali pazienti? 1. Pz con difficoltà di accesso o adesione controlli 2. Pz con PT INR non adeguatamente controllato 3. Pazienti con elevato rischio ischemico 4. Politrattati per rischio interferenze 5. Nuovi pazienti che non vogliono intraprendere TAO 6. Pz in FA con pregressa emorragia cerebrale
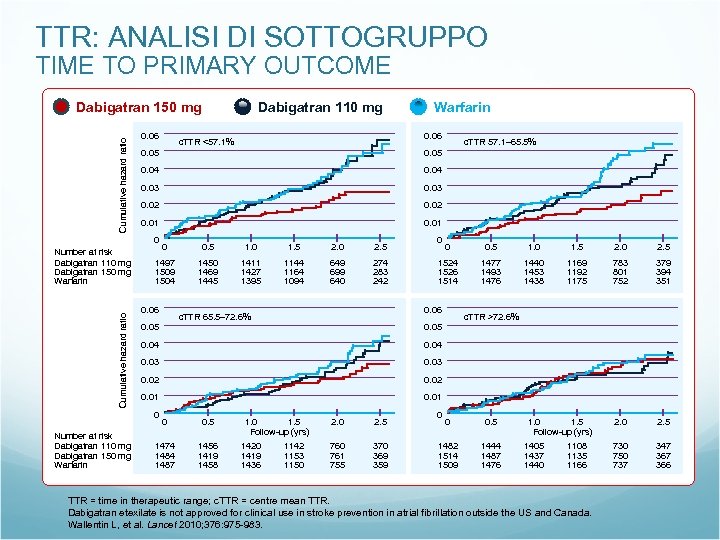
TTR: ANALISI DI SOTTOGRUPPO TIME TO PRIMARY OUTCOME Dabigatran 110 mg Cumulative hazard ratio Dabigatran 150 mg 0. 06 0. 04 0. 03 0. 02 0. 01 Cumulative hazard ratio c. TTR 57. 1– 65. 5% 0. 05 0. 01 0 0. 5 1. 0 1. 5 2. 0 2. 5 1497 1509 1504 1450 1469 1445 1411 1427 1395 1144 1164 1094 649 699 640 274 283 242 0. 06 0 0 0. 5 1. 0 1. 5 2. 0 2. 5 1524 1526 1514 1477 1493 1476 1440 1453 1438 1169 1192 1175 783 801 752 379 394 351 2. 0 2. 5 730 750 737 347 366 0. 06 c. TTR 65. 5– 72. 6% 0. 05 c. TTR >72. 6% 0. 05 0. 04 0. 03 0. 02 0. 01 0 Number at risk Dabigatran 110 mg Dabigatran 150 mg Warfarin 0. 06 c. TTR <57. 1% 0. 05 0 Number at risk Dabigatran 110 mg Dabigatran 150 mg Warfarin 0 0. 5 1474 1487 1456 1419 1458 1. 0 1. 5 Follow-up (yrs) 1420 1419 1436 1142 1153 1150 2. 5 760 761 755 370 369 359 0 0 0. 5 1482 1514 1509 1444 1487 1476 1. 0 1. 5 Follow-up (yrs) 1405 1437 1440 1108 1135 1166 TTR = time in therapeutic range; c. TTR = centre mean TTR. Dabigatran etexilate is not approved for clinical use in stroke prevention in atrial fibrillation outside the US and Canada. Wallentin L, et al. Lancet 2010; 376: 975 -983.
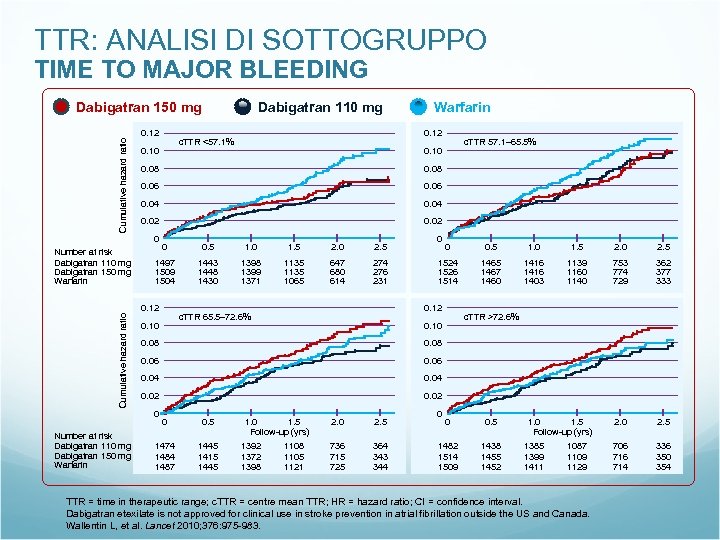
TTR: ANALISI DI SOTTOGRUPPO TIME TO MAJOR BLEEDING Dabigatran 110 mg Cumulative hazard ratio Dabigatran 150 mg 0. 12 0. 08 0. 06 0. 04 0. 02 0 0. 5 1. 0 1. 5 2. 0 2. 5 1497 1509 1504 1443 1448 1430 1398 1399 1371 1135 1065 647 680 614 276 231 Cumulative hazard ratio 0. 12 0 0 0. 5 1. 0 1. 5 2. 0 2. 5 1524 1526 1514 1465 1467 1460 1416 1403 1139 1160 1140 753 774 729 362 377 333 2. 0 2. 5 706 714 336 350 354 0. 12 c. TTR 65. 5– 72. 6% 0. 10 c. TTR >72. 6% 0. 10 0. 08 0. 06 0. 04 0. 02 0 Number at risk Dabigatran 110 mg Dabigatran 150 mg Warfarin c. TTR 57. 1– 65. 5% 0. 10 0. 08 0 Number at risk Dabigatran 110 mg Dabigatran 150 mg Warfarin 0. 12 c. TTR <57. 1% 0. 10 Warfarin 0 0. 5 1474 1487 1445 1415 1445 1. 0 1. 5 Follow-up (yrs) 1392 1372 1398 1105 1121 2. 0 2. 5 736 715 725 364 343 344 0 0 0. 5 1482 1514 1509 1438 1455 1452 1. 0 1. 5 Follow-up (yrs) 1385 1399 1411 1087 1109 1129 TTR = time in therapeutic range; c. TTR = centre mean TTR; HR = hazard ratio; CI = confidence interval. Dabigatran etexilate is not approved for clinical use in stroke prevention in atrial fibrillation outside the US and Canada. Wallentin L, et al. Lancet 2010; 376: 975 -983.

Come gestire lo switch
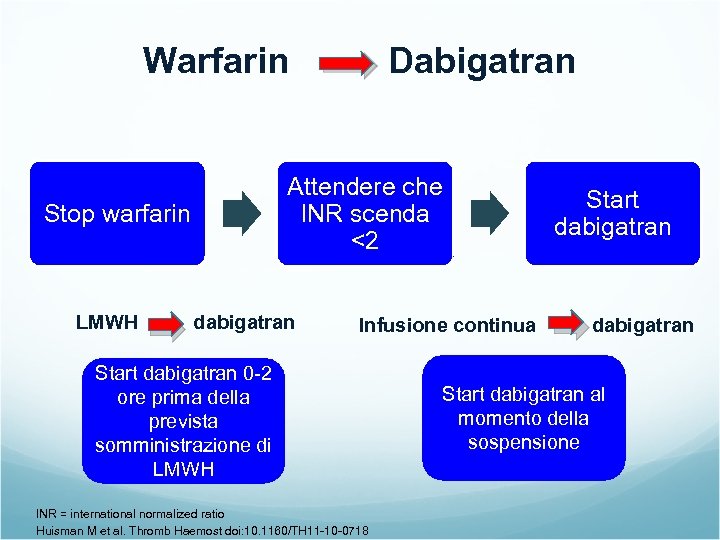
Warfarin Attendere che INR scenda <2 Stop warfarin LMWH Dabigatran dabigatran Infusione continua Start dabigatran 0 -2 ore prima della prevista somministrazione di LMWH INR = international normalized ratio Huisman M et al. Thromb Haemost doi: 10. 1160/TH 11 -10 -0718 Start dabigatran al momento della sospensione
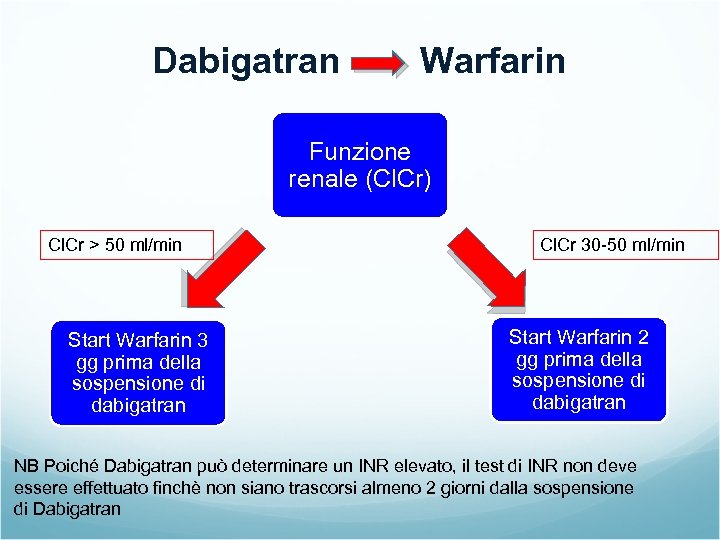
Dabigatran Warfarin Funzione renale (Cl. Cr) Cl. Cr > 50 ml/min Start Warfarin 3 gg prima della sospensione di dabigatran Cl. Cr 30 -50 ml/min Start Warfarin 2 gg prima della sospensione di dabigatran NB Poiché Dabigatran può determinare un INR elevato, il test di INR non deve essere effettuato finchè non siano trascorsi almeno 2 giorni dalla sospensione di Dabigatran

Nuovi Anticoagulanti Orali (NAO): a quali pazienti? 1. Pz con difficoltà di accesso o adesione controlli 2. Pz con PT INR non adeguatamente controllato 3. Pazienti con elevato rischio ischemico 4. Politrattati per rischio interferenze 5. Nuovi pazienti che non vogliono intraprendere TAO 6. Pz in FA con pregressa emorragia cerebrale
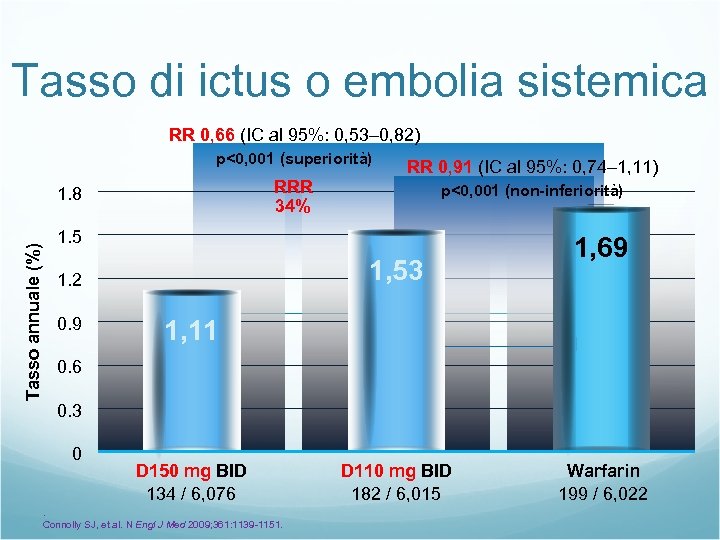
Tasso di ictus o embolia sistemica RR 0, 66 (IC al 95%: 0, 53– 0, 82) p<0, 001 (superiorità) RRR 34% Tasso annuale (%) 1. 8 RR 0, 91 (IC al 95%: 0, 74– 1, 11) p<0, 001 (non-inferiorità) 1. 5 1, 53 1. 2 0. 9 1, 69 1, 11 0. 6 0. 3 0 D 150 mg BID 134 / 6, 076 . Connolly SJ, et al. N Engl J Med 2009; 361: 1139 -1151. D 110 mg BID 182 / 6, 015 Warfarin 199 / 6, 022
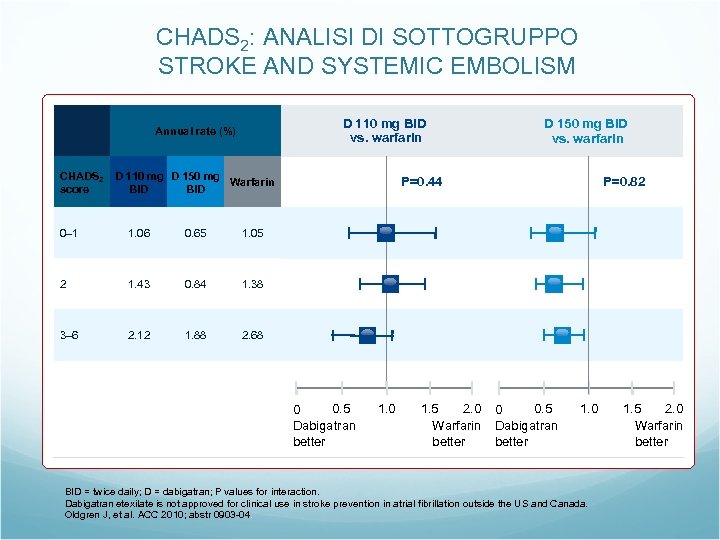
CHADS 2: ANALISI DI SOTTOGRUPPO STROKE AND SYSTEMIC EMBOLISM D 110 mg BID vs. warfarin Annual rate (%) CHADS 2 score D 110 mg D 150 mg Warfarin BID 0– 1 1. 06 0. 65 1. 43 0. 84 2. 12 1. 88 P=0. 82 1. 38 3– 6 P=0. 44 1. 05 2 D 150 mg BID vs. warfarin 2. 68 0. 5 0 Dabigatran better 1. 0 1. 5 2. 0 Warfarin better 0. 5 0 Dabigatran better 1. 0 BID = twice daily; D = dabigatran; P values for interaction. Dabigatran etexilate is not approved for clinical use in stroke prevention in atrial fibrillation outside the US and Canada. Oldgren J, et al. ACC 2010; abstr 0903 -04. 1. 5 2. 0 Warfarin better

Nuovi Anticoagulanti Orali (NAO): a quali pazienti? 1. Pz con difficoltà di accesso o adesione controlli 2. Pz con PT INR non adeguatamente controllato 3. Pazienti con elevato rischio ischemico 4. Politrattati per rischio interferenze 5. Nuovi pazienti che non vogliono intraprendere TAO 6. Pz in FA con pregressa emorragia cerebrale

Interazioni Warfarin-farmaci CYP 450
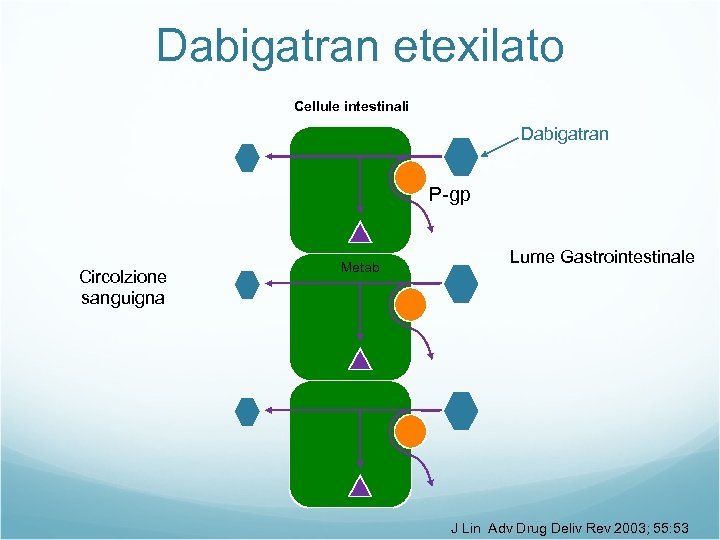
Dabigatran etexilato Cellule intestinali Dabigatran P-gp Circolzione sanguigna Metab Lume Gastrointestinale J Lin Adv Drug Deliv Rev 2003; 55: 53
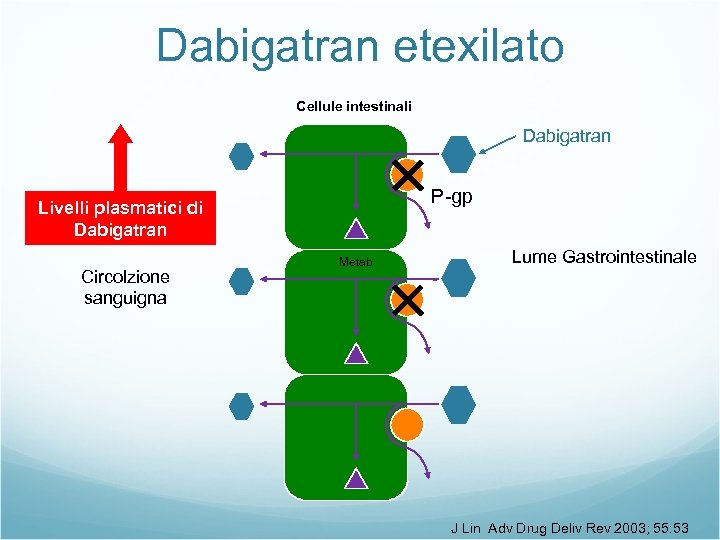
Dabigatran etexilato Cellule intestinali Dabigatran P-gp Livelli plasmatici di Dabigatran Circolzione sanguigna Metab Lume Gastrointestinale J Lin Adv Drug Deliv Rev 2003; 55: 53

Dabigatran etexilate e glicoproteine-P UTILIZZO CON CAUTELA Verapamil Amiodarone Chinidina Claritromicina (forte P-gp inibitore) DDI = drug–drug interaction; P-gp = P-glycoprotein Disclaimer: Dabigatran etexilate is now approved for clinical use in stroke prevention in atrial fibrillation in certain countries. Please check local prescribing information for further details. Dec 2011

Dabigatran etexilato CONTROINDICAZIONE • KETONAZOLO ev • CICLOSPORINA • TACROLIMUS • DRONEDARONE

Nuovi Anticoagulanti Orali (NAO): a quali pazienti? 1. Pz con difficoltà di accesso o adesione controlli 2. Pz con PT INR non adeguatamente controllato 3. Pazienti con elevato rischio ischemico 4. Politrattati per rischio interferenze 5. Nuovi pazienti che non vogliono intraprendere TAO 6. Pz in FA con pregressa emorragia cerebrale

Nuovi Anticoagulanti Orali (NAO): a quali pazienti? 1. Pz con difficoltà di accesso o adesione controlli 2. Pz con PT INR non adeguatamente controllato 3. Pazienti con elevato rischio ischemico 4. Politrattati per rischio interferenze 5. Nuovi pazienti che non vogliono intraprendere TAO 6. Pz in FA con pregressa emorragia cerebrale
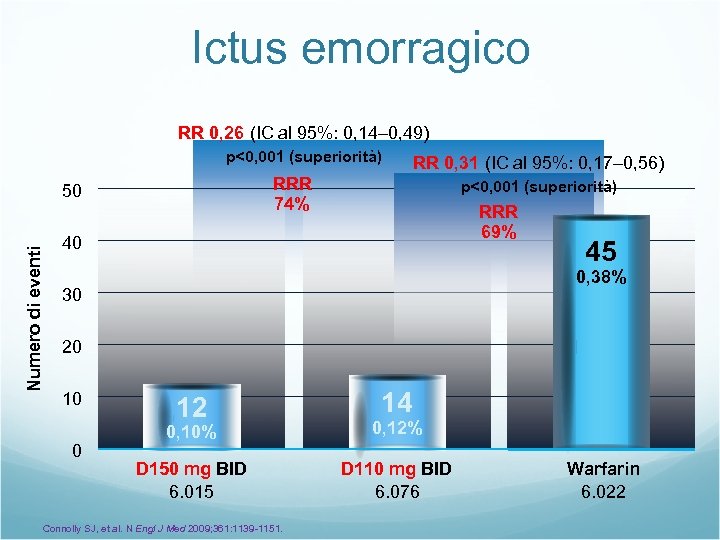
Ictus emorragico RR 0, 26 (IC al 95%: 0, 14– 0, 49) p<0, 001 (superiorità) RRR 74% 50 Numero di eventi RR 0, 31 (IC al 95%: 0, 17– 0, 56) p<0, 001 (superiorità) RRR 69% 40 45 0, 38% 30 20 10 0 12 14 0, 10% 0, 12% D 150 mg BID 6. 015 D 110 mg BID 6. 076 Connolly SJ, et al. N Engl J Med 2009; 361: 1139 -1151. Warfarin 6. 022
Ictus emorragico Proteine vitamina K dipendenti proteina Matrix GLA (o MGP) Emorragie cerebrali

Cosa dobbiamo fare di fronte ad un candidato a Dabigatran

Nuovi Anticoagulanti Orali (NAO) 1. Colloquio informativo 2. Controlli clinici 3. Gestione degli eventi intercorrenti

“Stressare” l’importanza della doppia somministrazione/die, durante i pasti
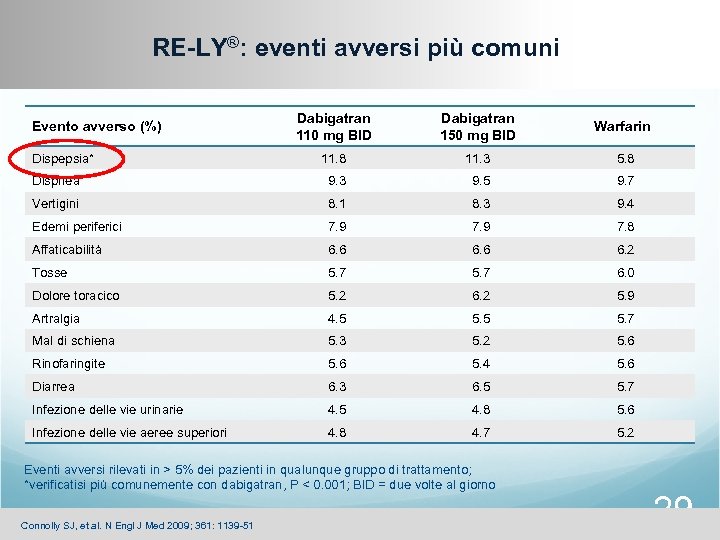
RE-LY®: eventi avversi più comuni Dabigatran 110 mg BID Dabigatran 150 mg BID Warfarin 11. 8 11. 3 5. 8 Dispnea 9. 3 9. 5 9. 7 Vertigini 8. 1 8. 3 9. 4 Edemi periferici 7. 9 7. 8 Affaticabilità 6. 6 6. 2 Tosse 5. 7 6. 0 Dolore toracico 5. 2 6. 2 5. 9 Artralgia 4. 5 5. 7 Mal di schiena 5. 3 5. 2 5. 6 Rinofaringite 5. 6 5. 4 5. 6 Diarrea 6. 3 6. 5 5. 7 Infezione delle vie urinarie 4. 5 4. 8 5. 6 Infezione delle vie aeree superiori 4. 8 4. 7 5. 2 Evento avverso (%) Dispepsia* Eventi avversi rilevati in > 5% dei pazienti in qualunque gruppo di trattamento; *verificatisi più comunemente con dabigatran, P < 0. 001; BID = due volte al giorno Connolly SJ, et al. N Engl J Med 2009; 361: 1139 -51 29

Come gestire la dispepsia How to manage dyspepsia All‘inizio della terapia spiegare al paziente la possibilità di avere dispepsia per ridurre il rischio di interruzione I sintomi sono spesso lievi; si presentano precocemente all‘inizio della terapia; spesso sono transitori Raccomandare di assume il farmaco a stomaco pieno o con un bel bicchiere d‘acqua Prendere in considerazione i PPI Huisman M et al. Thromb Haemost doi: 10. 1160/TH 11 -10 -0718
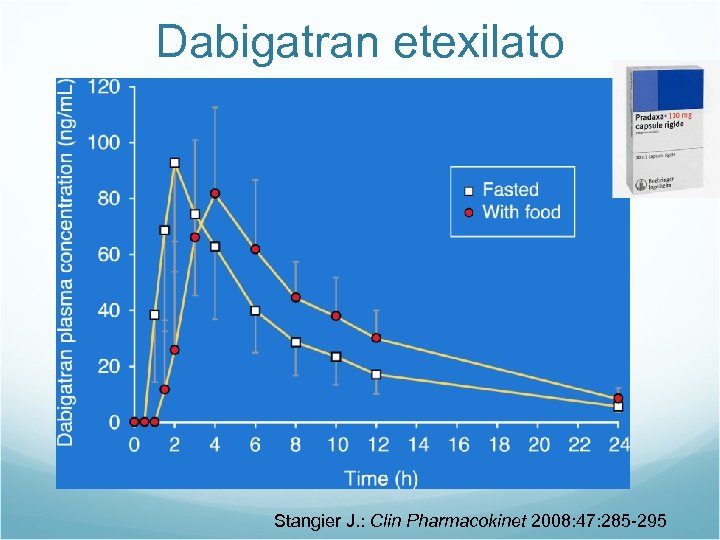
Dabigatran etexilato Stangier J. : Clin Pharmacokinet 2008: 47: 285 -295

RE-LY® – Sicurezza

Cosa fare in caso di dimenticanza

The 6 -hour rule Time since missed dose Recommendation <6 hours The patient should take the ‘missed’ dose >6 hours The patient should wait until their next scheduled dose

Conoscere la funzione renale del paziente (clearance creatinina)
Dabigatran etexilato Funzione renale prima di iniziare la terapia 80% di Dabigatran escreto per via renale

Dabigatran: valutazione della funzionalità renale del paziente prima di iniziare il trattamento La funzionalità renale deve essere valutata calcolando la Clearance della Creatinina* prima di iniziare il trattamento - Per escludere i pazienti con insufficienza renale severa (Cr. Cl <30 m. L/min) - Dabigatran 110 mg BID dovrebbe essere considerato in pazienti con insufficienza renale moderata (Cr. Cl 30– 50 m. L/min) associata ad un elevato rischio di sanguinamento *Stimata con la formula di Cockcroft–Gault http: //www. ema. europa. eu/docs/it_IT/document_library/EPAR_-_Product_Information/human/000829/WC 500041059. pdf

Formula di Cockcroft e Gault GFR (ml/min): Peso (Kg) x (140 – età) X 0. 85 (donne) Creatininemia (mg/dl) x 72 Funzione renale normale Insufficienza renale lieve Insufficienza renale moderato Insufficienza renale grave Insufficienza renale “terminale” > 90 ml/min 60 – 89 ml/min 30 - 59 ml/min 15 – 29 ml/min < 15 ml/min


Decidere la dose giusta
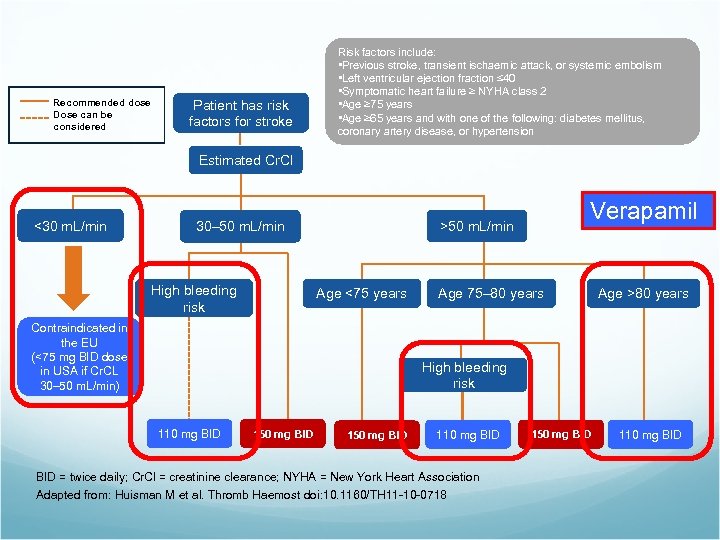
Recommended dose Dose can be considered Patient has risk factors for stroke Risk factors include: • Previous stroke, transient ischaemic attack, or systemic embolism • Left ventricular ejection fraction ≤ 40 • Symptomatic heart failure ≥ NYHA class 2 • Age ≥ 75 years • Age ≥ 65 years and with one of the following: diabetes mellitus, coronary artery disease, or hypertension Estimated Cr. Cl <30 m. L/min High bleeding risk Verapamil >50 m. L/min 30– 50 m. L/min Age <75 years Contraindicated in the EU (<75 mg BID dose in USA if Cr. CL 30– 50 m. L/min) Age 75– 80 years Age >80 years High bleeding risk 110 mg BID 150 mg BID 110 mg BID = twice daily; Cr. Cl = creatinine clearance; NYHA = New York Heart Association Adapted from: Huisman M et al. Thromb Haemost doi: 10. 1160/TH 11 -10 -0718 150 mg BID 110 mg BID

Nuovi Anticoagulanti Orali (NAO) 1. Colloquio informativo 2. Controlli clinici 3. Gestione degli eventi intercorrenti

Controlli clinici: QUANTI?

Global Registry on Long-Term Oral Antithrombotic Treatment in AF Patients • Collection of data on dabigatran in countries/regions and globally • Increase knowledge on AF patients, treatment patterns, and outcome events in a real-world setting • Involvement of up to 2200 physicians worldwide: GPs, cardiologists, neurologists, internists, geriatricians, etc – hospital based or private practice up to 56 000 patients 2200 sites up to 50 countries

Controlli clinici: COSA CHIEDERE? • Terapia concomitante • Diatesi emorragica • Compliance (BID)

Controlli clinici: Ci sono esami o controlli ematochimici da richiedere
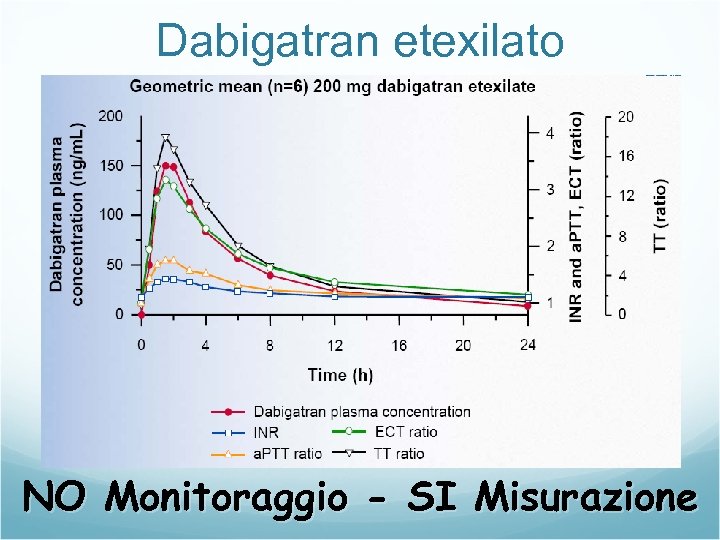
Dabigatran etexilato NO Monitoraggio - SI Misurazione
Dabigatran etexilato Funzione renale almeno una volta all’anno 80% di Dabigatran escreto per via renale
Nuovi Anticoagulanti Orali (NAO) 1. Colloquio informativo 2. Controlli clinici 3. Gestione degli eventi intercorrenti

Cardioversione
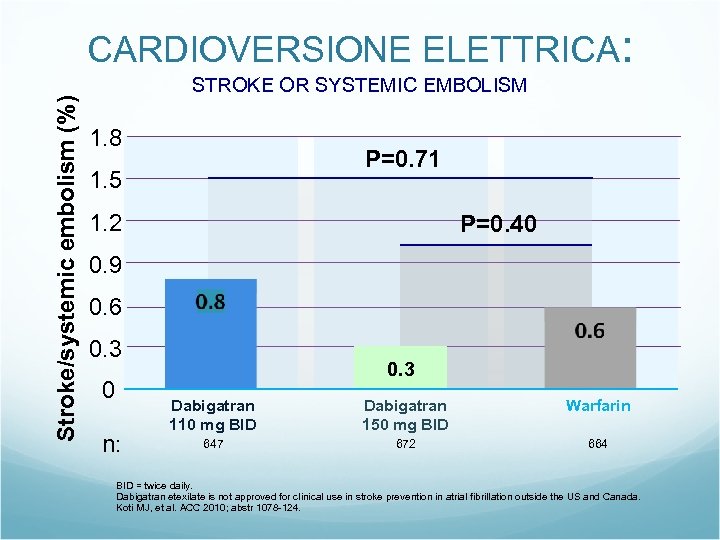
Stroke/systemic embolism (%) CARDIOVERSIONE ELETTRICA: STROKE OR SYSTEMIC EMBOLISM 1. 8 P=0. 71 1. 5 1. 2 P=0. 40 0. 9 0. 6 0. 3 0 n: 0. 3 Dabigatran 110 mg BID Dabigatran 150 mg BID Warfarin 647 672 664 BID = twice daily. Dabigatran etexilate is not approved for clinical use in stroke prevention in atrial fibrillation outside the US and Canada. Koti MJ, et al. ACC 2010; abstr 1078 -124.
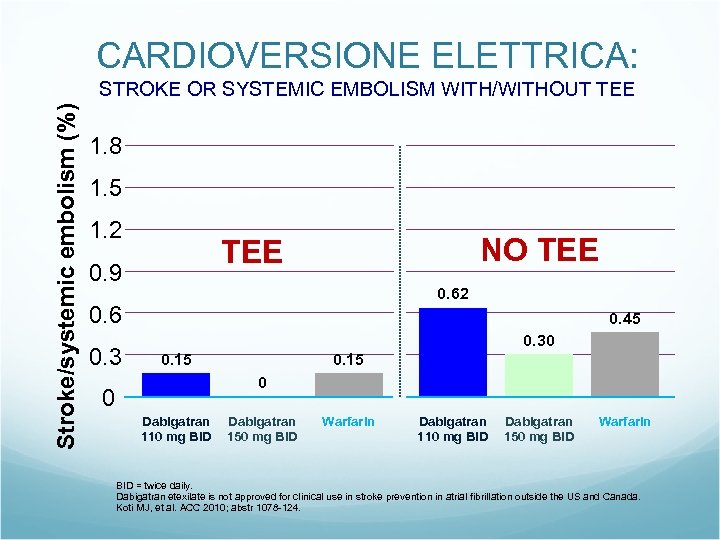
CARDIOVERSIONE ELETTRICA: Stroke/systemic embolism (%) STROKE OR SYSTEMIC EMBOLISM WITH/WITHOUT TEE 1. 8 1. 5 1. 2 NO TEE 0. 9 0. 62 0. 6 0. 3 0. 45 0. 30 0. 15 0 0 Dabigatran 110 mg BID Dabigatran 150 mg BID Warfarin BID = twice daily. Dabigatran etexilate is not approved for clinical use in stroke prevention in atrial fibrillation outside the US and Canada. Koti MJ, et al. ACC 2010; abstr 1078 -124.

Quale gestione in ambito chirurgico
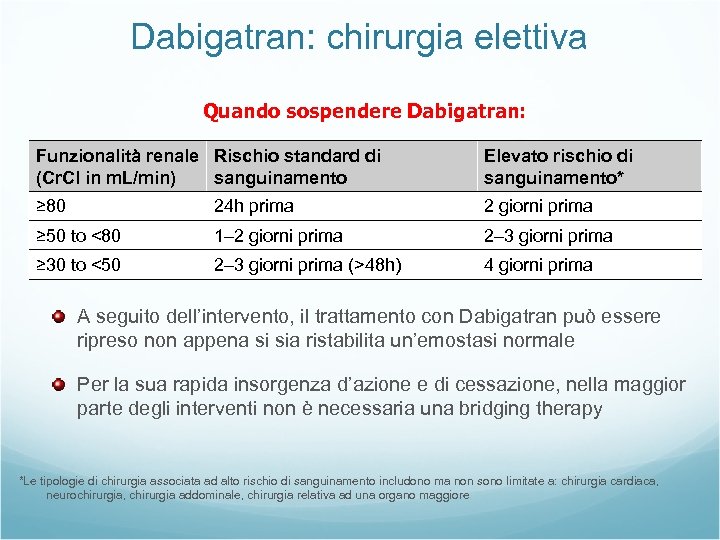
Dabigatran: chirurgia elettiva Quando sospendere Dabigatran: Funzionalità renale Rischio standard di (Cr. Cl in m. L/min) sanguinamento Elevato rischio di sanguinamento* ≥ 80 24 h prima 2 giorni prima ≥ 50 to <80 1– 2 giorni prima 2– 3 giorni prima ≥ 30 to <50 2– 3 giorni prima (>48 h) 4 giorni prima A seguito dell’intervento, il trattamento con Dabigatran può essere ripreso non appena si sia ristabilita un’emostasi normale Per la sua rapida insorgenza d’azione e di cessazione, nella maggior parte degli interventi non è necessaria una bridging therapy *Le tipologie di chirurgia associata ad alto rischio di sanguinamento includono ma non sono limitate a: chirurgia cardiaca, neurochirurgia, chirurgia addominale, chirurgia relativa ad una organo maggiore

Dabigatran: chirurgia d’urgenza In caso di chirurgia d’urgenza, dabigatran etexilato deve essere temporaneamente sospeso. L’intervento deve essere rimandato almeno per 12 ore dopo l’ultima dose assunta Se non è possibile rimandare, deve essere valutato il maggior rischio di sanguinamento rispetto all’urgenza dell’intervento stesso

Cosa fare in caso di complicanza emorragica
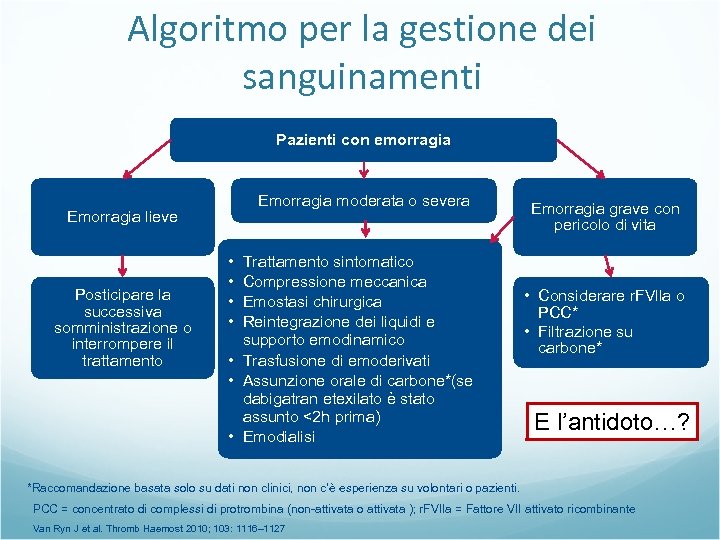
Algoritmo per la gestione dei sanguinamenti Pazienti con emorragia Emorragia moderata o severa Emorragia lieve Posticipare la successiva somministrazione o interrompere il trattamento • • Trattamento sintomatico Compressione meccanica Emostasi chirurgica Reintegrazione dei liquidi e supporto emodinamico • Trasfusione di emoderivati • Assunzione orale di carbone*(se dabigatran etexilato è stato assunto <2 h prima) • Emodialisi Emorragia grave con pericolo di vita • Considerare r. FVlla o PCC* • Filtrazione su carbone* E l’antidoto…? *Raccomandazione basata solo su dati non clinici, non c’è esperienza su volontari o pazienti. PCC = concentrato di complessi di protrombina (non-attivata o attivata ); r. FVIIa = Fattore VII attivato ricombinante Van Ryn J et al. Thromb Haemost 2010; 103: 1116– 1127

Esiste un antidoto?

• Anticorpo monoclonale contro il Dabigatran (DABI-FAB) • Ha conformazione simile alla trombina • Elevatissima affinità (350 vv vs trombina) • Non interagisce con l’attività coagulativa spontanea • Ha dimostrato una reversibilità potente ed immediata (1 minuto) dell’anticoagulazione da Dabigatran, in vivo sui ratti Blood. 2013 May 2; 121(18): 3554 -62.
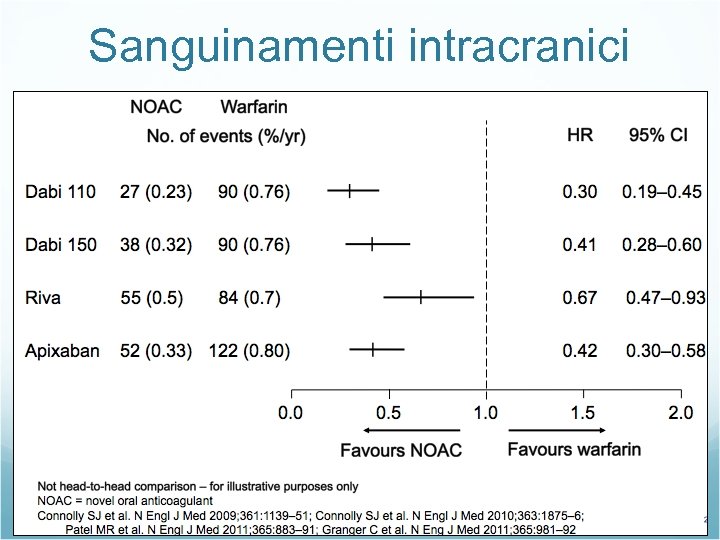
Sanguinamenti intracranici










GRAZIE PER L’ATTENZIONE
b11b73a96b82163c5c7e18a9d1530af6.ppt