FLA_Lektsia_5_2012.ppt
- Количество слайдов: 26

Л. № 5 АРЕНЫ (бензол и его производные) Общая характеристика. Ароматические углеводороды (арены) – соединения, содержащие в молекуле особую карбоциклическую группировку – бензольное кольцо. Простейший представитель аренов – бензол С 6 Н 6 (открыт М. Фарадеем в 1825 г. ). Первый вариант структуры бензола предложил А. Кекуле (1865 г. ).

Высокая ненасыщенность бензола должна была бы легко обнаруживаться по обесцвечиванию растворов брома и KMn. O 4. Однако оба эти теста на непредельность бензола отрицательны. – Устойчивость непредельных соединений к реакциям присоединения и окисления называется ароматичностью и объясняется специфичностью их электронной структуры.

Электронная структура бензола. Атомы углерода бензольного кольца находятся во втором валентном состоянии (sp 2), а все 12 атомов молекулы бензола располагаются в одной плоскости. Гибридные sp 2 – орбитали углерода ориентированы под углом 1200, а атомы углерода располагаются в вершинах правильного шестиугольника (рис. 15 а). Негибридные р-орбитали ориентированы перпендикулярно плоскости шестиугольника и, взаимно перекрываясь, образуют две сплошные области повышенной электронной плотности над и под плоскостью шестиугольника. Возникает единая для всех шести атомов углерода - электронная система (рис. 15 а), а между углеродами бензольного кольца одинаковые мезомерные связи, - промежуточные между одинарными и двойными, что подтверждается измерениями длин связей (от mesos – средний, промежуточный):
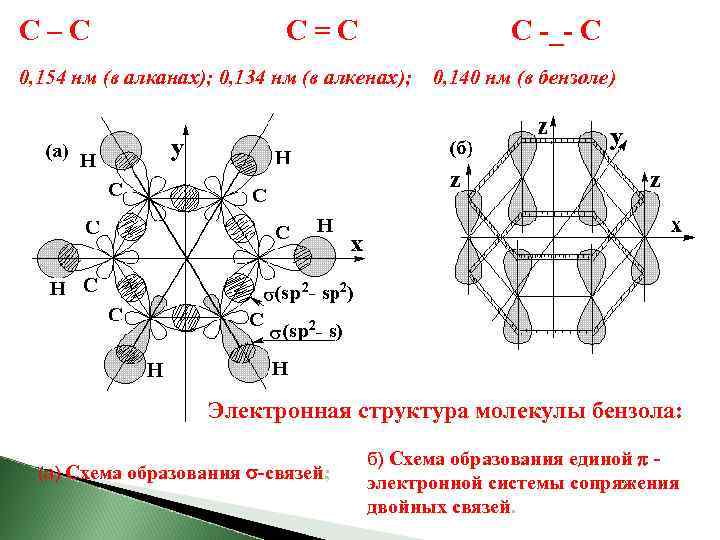
C–C C=C C -_- C 0, 154 нм (в алканах); 0, 134 нм (в алкенах); 0, 140 нм (в бензоле) Электронная структура молекулы бензола: (а) Схема образования -связей; б) Схема образования единой - электронной системы сопряжения двойных связей.

Равномерность распределения электронной плотности (эффект сопряжения) в молекуле бензола на структурной формуле изображается кольцом внутри шестиугольника.

Изомерия и номенклатура аренов. Гомологический ряд производных бензола имеет общую формулу Сn. H 2 n-6. (n 6). Гомологи бензола – результат замены в его молекуле атомов водорода на радикалы (алкилы). Источников изомерии аренов – три: а) количество и вид заместителей; б) различное положение заместителей в бензольном кольце; в) изомерия боковой цепи.

Номенклатура Для наименования аренов с несколькими радикалами в бензольном кольце его атомы углерода нумеруются от одного заместителя в сторону ближайшего другого (по или против часовой стрелки). Для наименования двузамещенных бензолов используются приставки орто-, мета- и пара-, соответственно для 1, 2 -; 1, 3 - и 1, 4 - положений заместителей (см. ниже ксилолы).
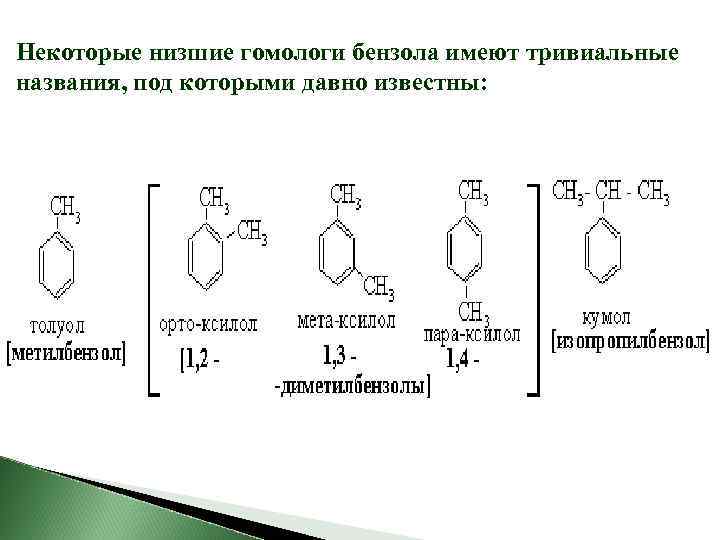
Некоторые низшие гомологи бензола имеют тривиальные названия, под которыми давно известны:
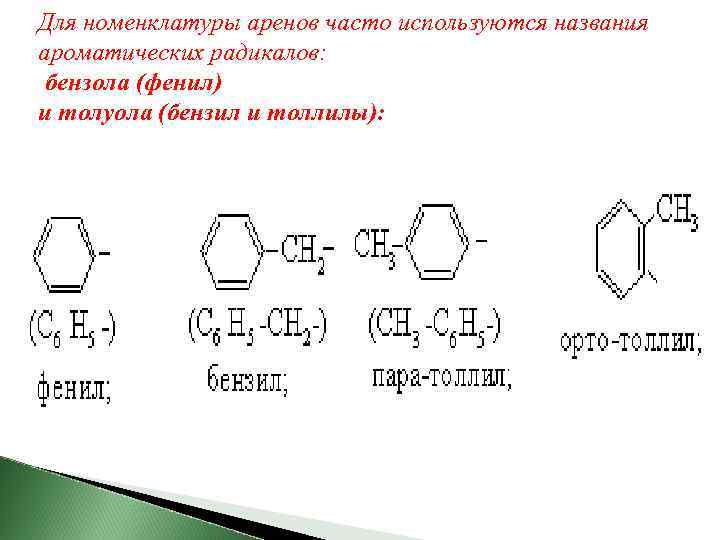
Для номенклатуры аренов часто используются названия ароматических радикалов: бензола (фенил) и толуола (бензил и толлилы):
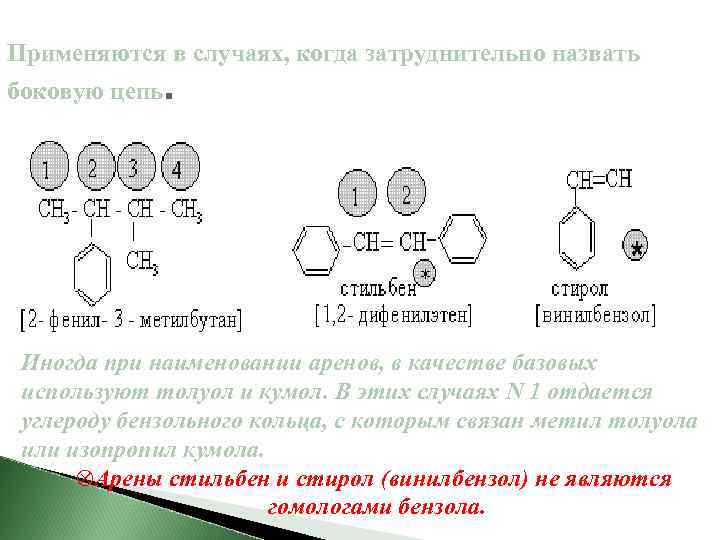
Применяются в случаях, когда затруднительно назвать боковую цепь. Иногда при наименовании аренов, в качестве базовых используют толуол и кумол. В этих случаях N 1 отдается углероду бензольного кольца, с которым связан метил толуола или изопропил кумола. Арены стильбен и стирол (винилбензол) не являются гомологами бензола.

Физические свойства аренов. Низшие арены – бензол, толуол, ксилолы, стирол – бесцветные легкоподвижные жидкости со слабыми запахами. Легче воды, с ней не смешиваются. Являются хорошими органическими растворителями. Огнеопасны. Горят сильно коптящим пламенем (углерода в бензоле 92, 3% (масс. )). Токсичны (ПДК=5 мг/м 3). Т. пл. от – 950 С для толуола до +13, 20 С для п-ксилола; Т. кип. от +800 до 1450 С.

Химические свойства аренов. Особенности химического поведения аренов обусловлены электронным строением бензольного кольца. Единая - электронная система определяет повышенную химическую устойчивость бензола и его гомологов к реакциям присоединения и окисления, но склонность их к реакциям замещения. Сам бензол - малоактивное вещество.
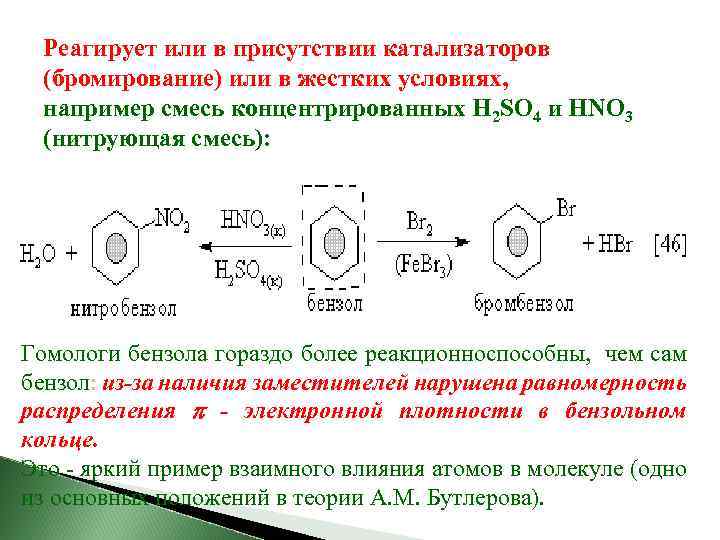
Реагирует или в присутствии катализаторов (бромирование) или в жестких условиях, например смесь концентрированных H 2 SO 4 и HNO 3 (нитрующая смесь): Гомологи бензола гораздо более реакционноспособны, чем сам бензол: из-за наличия заместителей нарушена равномерность распределения - электронной плотности в бензольном кольце. Это - яркий пример взаимного влияния атомов в молекуле (одно из основных положений в теории А. М. Бутлерова).
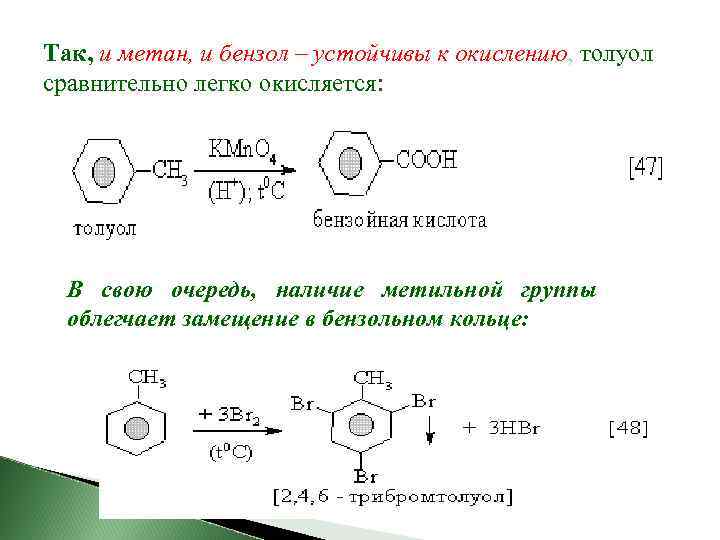
Так, и метан, и бензол – устойчивы к окислению, толуол сравнительно легко окисляется: В свою очередь, наличие метильной группы облегчает замещение в бензольном кольце:
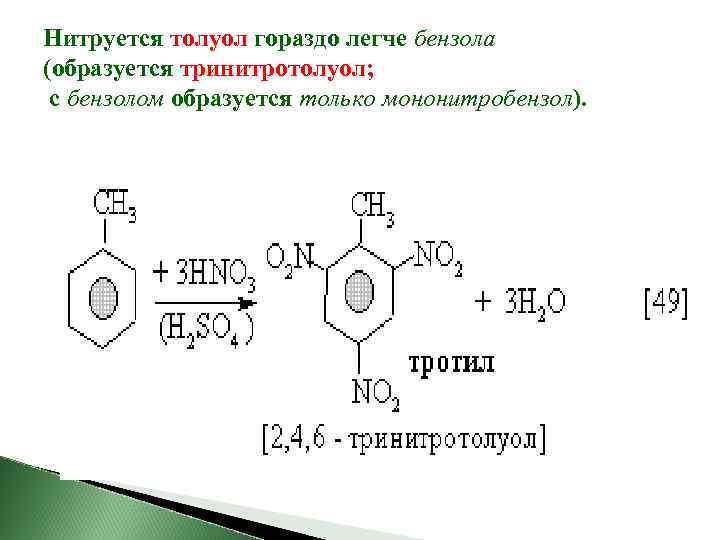
Нитруется толуол гораздо легче бензола (образуется тринитротолуол; с бензолом образуется только мононитробензол).
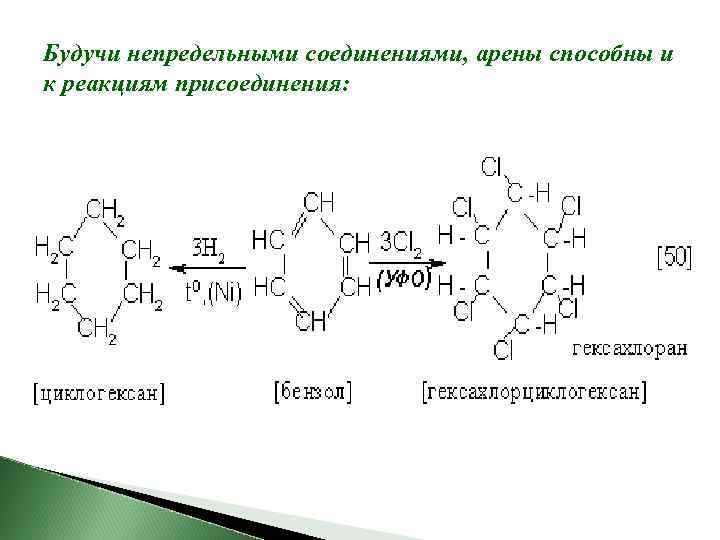
Будучи непредельными соединениями, арены способны и к реакциям присоединения:
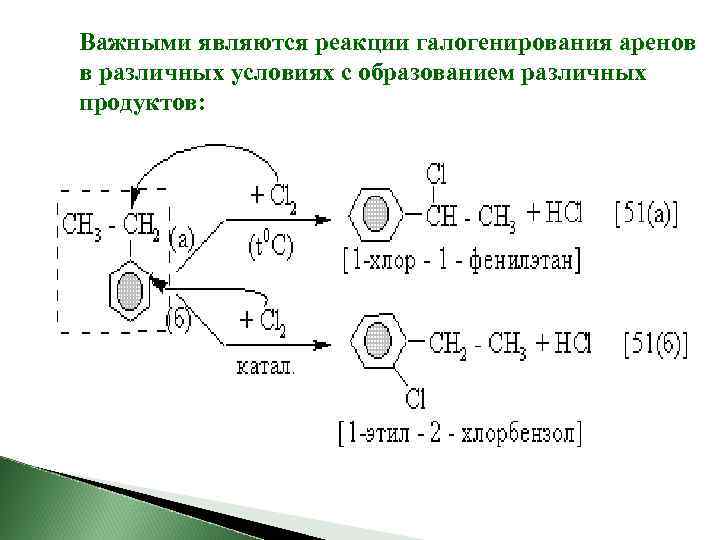
Важными являются реакции галогенирования аренов в различных условиях c образованием различных продуктов:

В присутствии катализатора (Al. Cl 3; Fe. Cl 3 и др. ) происходит замещение в бензольном кольце, а при нагреве (без катализатора) замещение в боковой цепи. При ультрафиолетовом облучении (УФО) идет реакция присоединения.

Получение аренов. Основными природными источниками ароматических углеводородов являются: нефть (до 50% в некоторых сортах) и антрацит (при его коксовании из 1 т угля получается до 12 кг аренов).
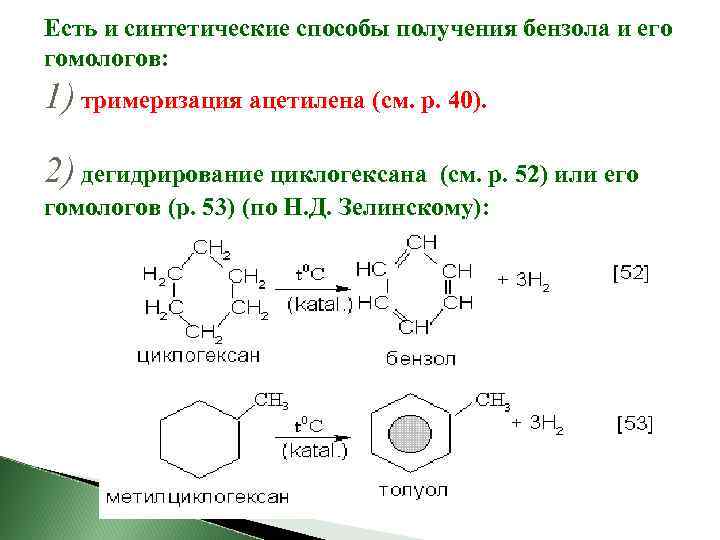
Есть и синтетические способы получения бензола и его гомологов: 1) тримеризация ацетилена (см. р. 40). 2) дегидрирование циклогексана (см. р. 52) или его гомологов (р. 53) (по Н. Д. Зелинскому):
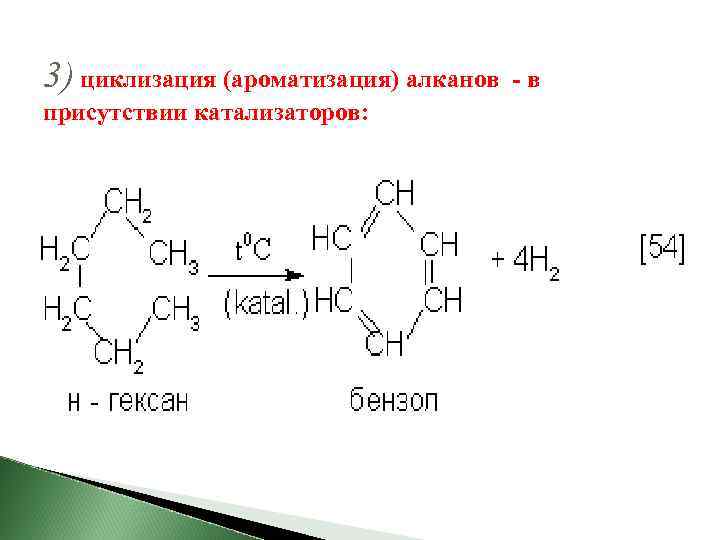
3) циклизация (ароматизация) алканов присутствии катализаторов: -в
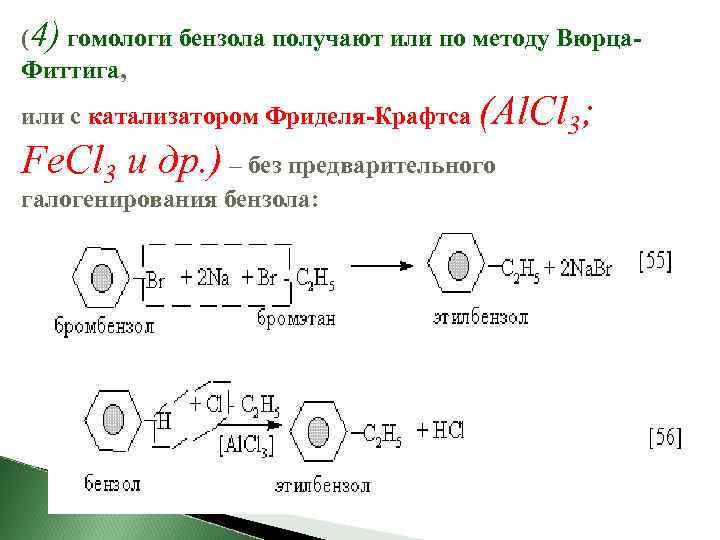
(4) гомологи бензола получают или по методу Вюрца. Фиттига, или с катализатором Фриделя-Крафтса (Al. Cl 3; Fe. Cl 3 и др. ) – без предварительного галогенирования бензола:
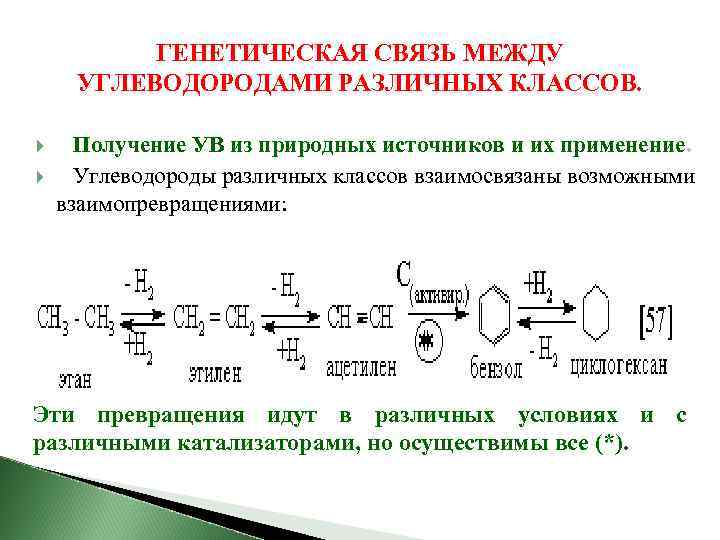
ГЕНЕТИЧЕСКАЯ СВЯЗЬ МЕЖДУ УГЛЕВОДОРОДАМИ РАЗЛИЧНЫХ КЛАССОВ. Получение УВ из природных источников и их применение. Углеводороды различных классов взаимосвязаны возможными взаимопревращениями: Эти превращения идут в различных условиях и с различными катализаторами, но осуществимы все (*).

Связаны различные углеводороды и едиными природными источниками, главными из которых являются природный газ, нефть и каменный уголь Природный газ ( от 75 до 99% СН 4) по теплотворной способности превосходит другие виды топлив ( уголь, торф, древесина, мазут и др. ). До 90% добываемого газа идет на нужды энергетики, а 10% - как сырьё химической промышленности.

Конверсией метана получают: (а) водород и сажу - чистый высокодисперсный углерод. Сажа используется как наполнитель при изготовлении автопокрышек; (б) ацетилен, из которого, в свою очередь, получают много ценных продуктов: - хлорвинил (СН 2=СНCl) и далее ПХВ (электороизоляция); - акрилонитрил (СН 2=СНCN) и далее ПАН (искусственное волокно); - винилацетат (СН 2=СНOOCCH 3) и далее ПВА (клей); - уксусный альдегид, который идет на получение этанола или уксусной кислоты. Используют ацетилен для резки и сварки металлов

Нефть – горючая маслообразная жидкость темно -коричневого цвета. Представляет собой смесь газообразных, жидких и твердых углеводородов (С 1 - С 50) как предельных, так и непредельных. В том числе. ароматических (содержание последних в некоторых сортах нефти достигает 50%). Кроме углеводородов, нефти содержат кислород , серу -, азот- и металлсодержащие вещества. *Превращение бензола в алифатические УВ может быть осуществлено после его гидрирования в циклогексан и крекинга последнего.
FLA_Lektsia_5_2012.ppt