Л19_Термо_2011.ppt
- Количество слайдов: 38
 Л 19 Скорости газовых молекул. Опыт Штерна. А – нагретая Pt нить, покрытая Ag; S 2 – диафрагма; S 1, S 3 – коаксиальные вращающиеся цилиндры При пропускании тока через Pt нить она разогревается до Т>Tпл Ag (962 С). S 1, S 2 и S 3 не вращаются, то пучок осаждается в виде узкой полоски D на S 3. При вращении системы с , изображение щели смещается в точку D . Δ s– расстояние между D и D ; Δt время пролета. Т нити в равнялась 1200 С, что соответствует vкв = 584 м/с. В эксперименте vкв = (560 640 м/с). Изображение щели D всегда размыто, т. е. , атомы Ag движутся с различными скоростями. 1
Л 19 Скорости газовых молекул. Опыт Штерна. А – нагретая Pt нить, покрытая Ag; S 2 – диафрагма; S 1, S 3 – коаксиальные вращающиеся цилиндры При пропускании тока через Pt нить она разогревается до Т>Tпл Ag (962 С). S 1, S 2 и S 3 не вращаются, то пучок осаждается в виде узкой полоски D на S 3. При вращении системы с , изображение щели смещается в точку D . Δ s– расстояние между D и D ; Δt время пролета. Т нити в равнялась 1200 С, что соответствует vкв = 584 м/с. В эксперименте vкв = (560 640 м/с). Изображение щели D всегда размыто, т. е. , атомы Ag движутся с различными скоростями. 1
 Таким образом, в этом опыте были не только измерены скорости газовых молекул, но и показано, что они имеют большой разброс по скоростям. Причина – в хаотичности теплового движения молекул. Ещё в XIX веке Дж. Максвелл утверждал, что молекулы, беспорядочно сталкиваясь друг с другом, как то «распределяются» по скоростям, причём вполне определённым образом. 2
Таким образом, в этом опыте были не только измерены скорости газовых молекул, но и показано, что они имеют большой разброс по скоростям. Причина – в хаотичности теплового движения молекул. Ещё в XIX веке Дж. Максвелл утверждал, что молекулы, беспорядочно сталкиваясь друг с другом, как то «распределяются» по скоростям, причём вполне определённым образом. 2
 Термодинамическая система Системой называется совокупность физических объектов исследования, заключенных в конечном объеме пространства. Границы системы могут быть: • как материальными, так и воображаемыми, • как неподвижными, так и движущимися, • как проницаемыми для вещества и энергии, так и непроницаемыми. Наиболее простой системой является идеальный газ Как правило, мы имеем дело с изолированными системами. Однако имеется взаимодействующих открытых систем. большой класс систем, с внешним окружением – 3
Термодинамическая система Системой называется совокупность физических объектов исследования, заключенных в конечном объеме пространства. Границы системы могут быть: • как материальными, так и воображаемыми, • как неподвижными, так и движущимися, • как проницаемыми для вещества и энергии, так и непроницаемыми. Наиболее простой системой является идеальный газ Как правило, мы имеем дело с изолированными системами. Однако имеется взаимодействующих открытых систем. большой класс систем, с внешним окружением – 3
 Закон сохранения энергии в открытых системах Пусть рассматриваемая система с энергией U имеет энтропию S, объем V и, будучи многокомпонентной, содержит частицы разного сорта в количествах N 1, N 2, N 3. . . , NК, так что ее состав может быть охарактеризован числом молей n 1=N 1/NA, …. n. K=NK/ NA, где К — число компонентов в системе, NA постоянная Авогадро. Эти величины в результате взаимодействия открытой системы с внешним окружением получают приращения d. S, d. V и dni. 4
Закон сохранения энергии в открытых системах Пусть рассматриваемая система с энергией U имеет энтропию S, объем V и, будучи многокомпонентной, содержит частицы разного сорта в количествах N 1, N 2, N 3. . . , NК, так что ее состав может быть охарактеризован числом молей n 1=N 1/NA, …. n. K=NK/ NA, где К — число компонентов в системе, NA постоянная Авогадро. Эти величины в результате взаимодействия открытой системы с внешним окружением получают приращения d. S, d. V и dni. 4
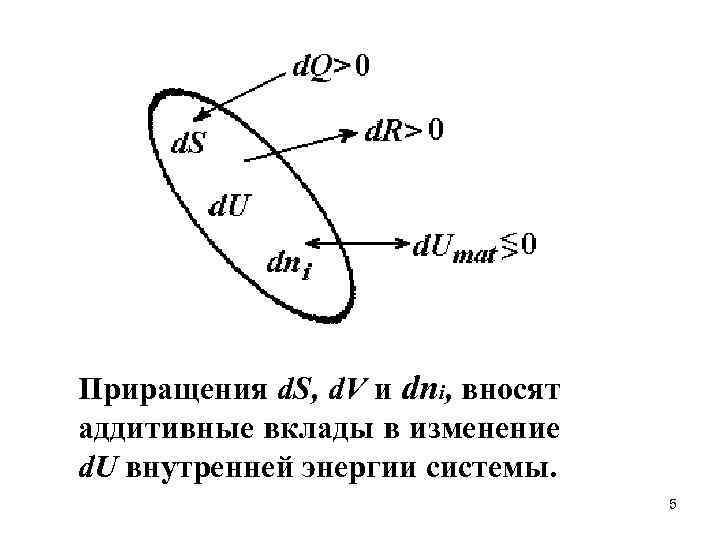 Приращения d. S, d. V и dni, вносят аддитивные вклады в изменение d. U внутренней энергии системы. 5
Приращения d. S, d. V и dni, вносят аддитивные вклады в изменение d. U внутренней энергии системы. 5
 Изменение внутренней энергии системы может происходить в результате протекания следующих процессов: • Обмена тепловой энергией d. Uтеп =d. Q (тепловой контакт) • Совершения механической работы d. Uмех =-d. R (механический контакт) • Обмен материальными частицами (материальный контакт) с изменением внутренней энергии на d. Uмат 6
Изменение внутренней энергии системы может происходить в результате протекания следующих процессов: • Обмена тепловой энергией d. Uтеп =d. Q (тепловой контакт) • Совершения механической работы d. Uмех =-d. R (механический контакт) • Обмен материальными частицами (материальный контакт) с изменением внутренней энергии на d. Uмат 6
 закон сохранения энергии для открытой системы может быть записан в дифференциальной форме Согласно, положительной теплотой (d. Q > 0) считается тепло, получаемое телом от посторонних источников, а положительной работой (d. R > 0) — работа, производимая телом над внешней средой; при этом первое дает положительный, а второе — отрицательный вклад в изменение внутренней энергии тела 7
закон сохранения энергии для открытой системы может быть записан в дифференциальной форме Согласно, положительной теплотой (d. Q > 0) считается тепло, получаемое телом от посторонних источников, а положительной работой (d. R > 0) — работа, производимая телом над внешней средой; при этом первое дает положительный, а второе — отрицательный вклад в изменение внутренней энергии тела 7
 Если отсутствует контакты, то механический и материальный механическая работа Изменение состава системы на величину dni вносит соответствующий вклад в величину d. Uмат , так что в общем случае коэффициент пропорциональности называется 8 химическим потенциалом частиц i-го сорта
Если отсутствует контакты, то механический и материальный механическая работа Изменение состава системы на величину dni вносит соответствующий вклад в величину d. Uмат , так что в общем случае коэффициент пропорциональности называется 8 химическим потенциалом частиц i-го сорта
 Таким образом, уравнение для первого закона термодинамики может быть записано в следующем виде Химический потенциал ( i), термодинамическая функция, применяемая при описании состояния систем с переменным числом частиц. В случае системы, состоящей из i компонентов, химический потенциал определяется как приращение внутренней энергии при добавлении к системе бесконечно малого количества молей i того компонента, отнесённое к этому количеству вещества, при постоянных объёме V, энтропии S и количествах молей каждого из остальных компонентов nj. 9
Таким образом, уравнение для первого закона термодинамики может быть записано в следующем виде Химический потенциал ( i), термодинамическая функция, применяемая при описании состояния систем с переменным числом частиц. В случае системы, состоящей из i компонентов, химический потенциал определяется как приращение внутренней энергии при добавлении к системе бесконечно малого количества молей i того компонента, отнесённое к этому количеству вещества, при постоянных объёме V, энтропии S и количествах молей каждого из остальных компонентов nj. 9
 Состояния системы Макроскопическое состояние. Принято говорить, что система находится в некотором макросостоянии, которое характеризуется давлением p, объемом V и температурой T термодинамическими параметрами данного макросостояния. Микроскопическое состояние. Полная информация о системе подразумевает знание 3 -х координат и 3 -х проекций скоростей всех частиц системы, то есть микроскопическое состояние системы характеризуется 6 N величинами в данный момент времени, где N число частиц системы. Так как в стационарном состоянии макросостояние не изменяется, но молекулы при этом постоянно движутся, меняя координаты и скорости, то данному макросостоянию системы отвечает огромное количество различных микросостояний! Статистический ансамбль систем - это множество одинаковых статистических систем, находящихся в одинаковом макросостоянии. 10
Состояния системы Макроскопическое состояние. Принято говорить, что система находится в некотором макросостоянии, которое характеризуется давлением p, объемом V и температурой T термодинамическими параметрами данного макросостояния. Микроскопическое состояние. Полная информация о системе подразумевает знание 3 -х координат и 3 -х проекций скоростей всех частиц системы, то есть микроскопическое состояние системы характеризуется 6 N величинами в данный момент времени, где N число частиц системы. Так как в стационарном состоянии макросостояние не изменяется, но молекулы при этом постоянно движутся, меняя координаты и скорости, то данному макросостоянию системы отвечает огромное количество различных микросостояний! Статистический ансамбль систем - это множество одинаковых статистических систем, находящихся в одинаковом макросостоянии. 10
 Фазовое пространство Поскольку значения координат и скоростей молекул могут принимать непрерывный ряд значений (в классической физике), может показаться, что каждому макросостоянию соответствуют бесконечное множество микросостояний. Как различать между собой микросостояния? В каком случае можно считать, что молекула перешла из одного микросостояния в другое? Классический случай. Каждая молекула реального газа занимает объем, в пределах которого другая молекула находиться не может. Т. о. , весь объем сосуда можно разделить на ячейки, объем V каждой из которых пропорционален d 3, где диаметр молекулы d ~ 10 10 м. Тогда, V ~10 30 м 3. Следовательно, в каждом кубическом метре объема имеется ~1030 ячеек. В газе (даже в реальном) занято молекулами лишь 0, 001% ячеек. Когда можно считать, что изменилось состояние при изменении скорости? На сколько должна измениться скорость? В рамках классической физики ответить на этот вопрос невозможно! 11
Фазовое пространство Поскольку значения координат и скоростей молекул могут принимать непрерывный ряд значений (в классической физике), может показаться, что каждому макросостоянию соответствуют бесконечное множество микросостояний. Как различать между собой микросостояния? В каком случае можно считать, что молекула перешла из одного микросостояния в другое? Классический случай. Каждая молекула реального газа занимает объем, в пределах которого другая молекула находиться не может. Т. о. , весь объем сосуда можно разделить на ячейки, объем V каждой из которых пропорционален d 3, где диаметр молекулы d ~ 10 10 м. Тогда, V ~10 30 м 3. Следовательно, в каждом кубическом метре объема имеется ~1030 ячеек. В газе (даже в реальном) занято молекулами лишь 0, 001% ячеек. Когда можно считать, что изменилось состояние при изменении скорости? На сколько должна измениться скорость? В рамках классической физики ответить на этот вопрос невозможно! 11
 Квантовая механика иначе определяет размер и количество ячеек. В природе (в соответствие с принципами квантовой механики) координаты и импульсы частиц не являются независимыми . В. Гейзенберг, учитывая волновые свойства микрочастиц, показал, что объект микромира невозможно одновременно с любой наперед заданной точностью характеризовать классически, то есть координатой и проекцией импульса на соответствующую ось. Соотношения неопределенностей: x неопределенность значений координаты; px неопределенность значений импульса. Тогда, объем элементарной ячейки фазового пространства одной молекулы: 12
Квантовая механика иначе определяет размер и количество ячеек. В природе (в соответствие с принципами квантовой механики) координаты и импульсы частиц не являются независимыми . В. Гейзенберг, учитывая волновые свойства микрочастиц, показал, что объект микромира невозможно одновременно с любой наперед заданной точностью характеризовать классически, то есть координатой и проекцией импульса на соответствующую ось. Соотношения неопределенностей: x неопределенность значений координаты; px неопределенность значений импульса. Тогда, объем элементарной ячейки фазового пространства одной молекулы: 12
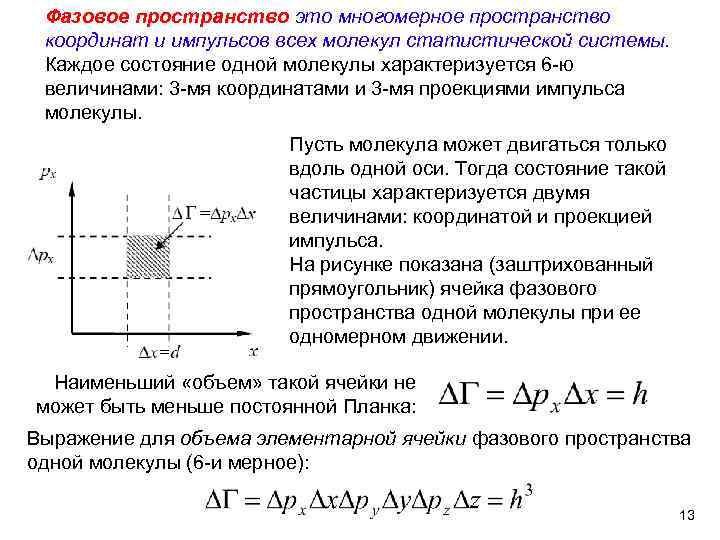 Фазовое пространство это многомерное пространство координат и импульсов всех молекул статистической системы. Каждое состояние одной молекулы характеризуется 6 ю величинами: 3 мя координатами и 3 мя проекциями импульса молекулы. Пусть молекула может двигаться только вдоль одной оси. Тогда состояние такой частицы характеризуется двумя величинами: координатой и проекцией импульса. На рисунке показана (заштрихованный прямоугольник) ячейка фазового пространства одной молекулы при ее одномерном движении. Наименьший «объем» такой ячейки не может быть меньше постоянной Планка: Выражение для объема элементарной ячейки фазового пространства одной молекулы (6 и мерное): 13
Фазовое пространство это многомерное пространство координат и импульсов всех молекул статистической системы. Каждое состояние одной молекулы характеризуется 6 ю величинами: 3 мя координатами и 3 мя проекциями импульса молекулы. Пусть молекула может двигаться только вдоль одной оси. Тогда состояние такой частицы характеризуется двумя величинами: координатой и проекцией импульса. На рисунке показана (заштрихованный прямоугольник) ячейка фазового пространства одной молекулы при ее одномерном движении. Наименьший «объем» такой ячейки не может быть меньше постоянной Планка: Выражение для объема элементарной ячейки фазового пространства одной молекулы (6 и мерное): 13
 Можно выделить объем элементарной ячейки : в подпространстве импульсов в подпространстве координат Тогда 6 и мерный объем элементарной ячейки фазового пространства можно записать в виде произведения объемов двух подпространств фазового пространства одной молекулы. Для статистической системы, содержащей N частиц, размерность фазового пространства 6 N, а это порядка 1026 «координат» (фазовых) на каждый кубометр реального газа! Термодинамической вероятностью (или статистическим весом) данного макросостояния называется величина Ga, равная количеству микросостояний, которым может быть реализовано данное макросостояние a. Очевидно, что G 0 > Ga. Отношение термодинамической вероятности Ga к полному количеству микросостояний, доступных системе, называется вероятностью данного макросостояния 14
Можно выделить объем элементарной ячейки : в подпространстве импульсов в подпространстве координат Тогда 6 и мерный объем элементарной ячейки фазового пространства можно записать в виде произведения объемов двух подпространств фазового пространства одной молекулы. Для статистической системы, содержащей N частиц, размерность фазового пространства 6 N, а это порядка 1026 «координат» (фазовых) на каждый кубометр реального газа! Термодинамической вероятностью (или статистическим весом) данного макросостояния называется величина Ga, равная количеству микросостояний, которым может быть реализовано данное макросостояние a. Очевидно, что G 0 > Ga. Отношение термодинамической вероятности Ga к полному количеству микросостояний, доступных системе, называется вероятностью данного макросостояния 14
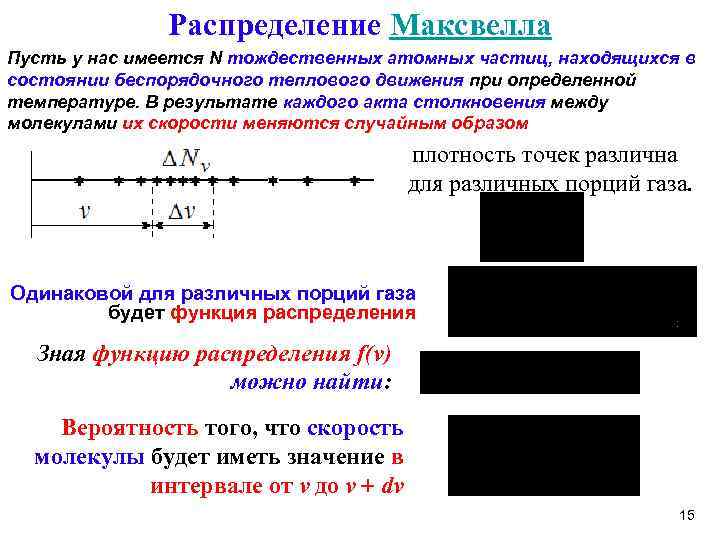 Распределение Максвелла Пусть у нас имеется N тождественных атомных частиц, находящихся в состоянии беспорядочного теплового движения при определенной температуре. В результате каждого акта столкновения между молекулами их скорости меняются случайным образом плотность точек различна для различных порций газа. Одинаковой для различных порций газа будет функция распределения Зная функцию распределения f(v) можно найти: Вероятность того, что скорость молекулы будет иметь значение в интервале от v до v dv 15
Распределение Максвелла Пусть у нас имеется N тождественных атомных частиц, находящихся в состоянии беспорядочного теплового движения при определенной температуре. В результате каждого акта столкновения между молекулами их скорости меняются случайным образом плотность точек различна для различных порций газа. Одинаковой для различных порций газа будет функция распределения Зная функцию распределения f(v) можно найти: Вероятность того, что скорость молекулы будет иметь значение в интервале от v до v dv 15
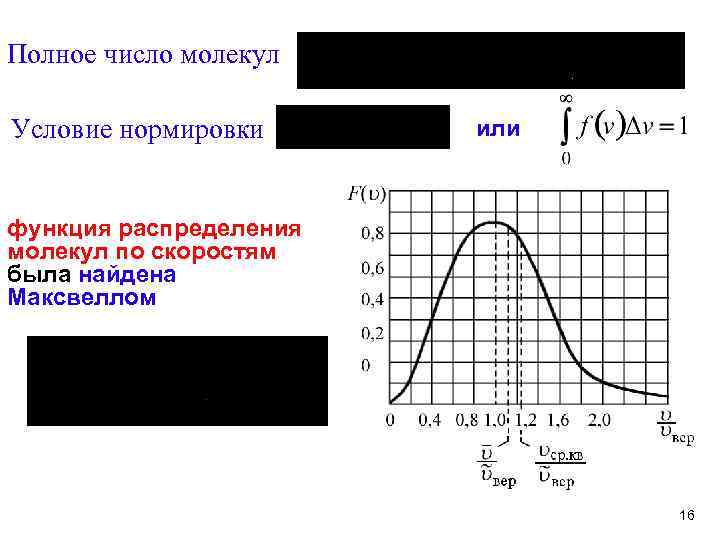 Полное число молекул Условие нормировки или функция распределения молекул по скоростям была найдена Максвеллом 16
Полное число молекул Условие нормировки или функция распределения молекул по скоростям была найдена Максвеллом 16
 Распределение Гиббса. Рассмотрим систему, которая может обмениваться с частицами, не входящими в эту систему (то есть с окружением), только энергией. Окружение термостат. Пусть такой системой является одна выбранная молекула, находящаяся в газе. Гиббс нашел формулу, позволяющую вычислить вероятность, с которой можно обнаружить выбранную систему, обладающую указанными выше свойствами, в некотором состоянии, то есть в некотором объеме d. Г фазового пространства: 17
Распределение Гиббса. Рассмотрим систему, которая может обмениваться с частицами, не входящими в эту систему (то есть с окружением), только энергией. Окружение термостат. Пусть такой системой является одна выбранная молекула, находящаяся в газе. Гиббс нашел формулу, позволяющую вычислить вероятность, с которой можно обнаружить выбранную систему, обладающую указанными выше свойствами, в некотором состоянии, то есть в некотором объеме d. Г фазового пространства: 17
 Распределение Гиббса: q - обобщенные координаты; р - обобщенные импульсы; W(q, р) - энергия системы, зависящая от обобщенных координат и импульсов; k = 1, 38 10 -23 Дж/К - постоянная Больцмана; Т - температура термостата; d. Г = d. Гq d. Гp - элемент объема фазового пространства. Эта формула, полученная Гиббсом, имеет столь же универсальное значение и так широко «работает» в природе, как и второй закон Ньютона, законы сохранения, уравнения Максвелла, уравнение Шредингера, распределение Гаусса. Заметим, что функцией распределения (плотностью вероятности) как и прежде, называется отношение вероятности обнаружения системы в некотором объеме к этому объему, только объем теперь не совсем обычный, а фазовый, то есть функцию распределения Гиббса можно записать как 18
Распределение Гиббса: q - обобщенные координаты; р - обобщенные импульсы; W(q, р) - энергия системы, зависящая от обобщенных координат и импульсов; k = 1, 38 10 -23 Дж/К - постоянная Больцмана; Т - температура термостата; d. Г = d. Гq d. Гp - элемент объема фазового пространства. Эта формула, полученная Гиббсом, имеет столь же универсальное значение и так широко «работает» в природе, как и второй закон Ньютона, законы сохранения, уравнения Максвелла, уравнение Шредингера, распределение Гаусса. Заметим, что функцией распределения (плотностью вероятности) как и прежде, называется отношение вероятности обнаружения системы в некотором объеме к этому объему, только объем теперь не совсем обычный, а фазовый, то есть функцию распределения Гиббса можно записать как 18
 Распределения Максвелла. Распределение Максвелла по векторам и компонентам скоростей. Выберем в качестве системы одну молекулу идеального газа. Пренебрегая внешними потенциальными полями, можно считать, что вся энергия системы это кинетическая энергия молекулы Тогда функция распределения Гиббса, записанная для подпространства скоростей для данной молекулы принимает вид Размерность фазового пространства одной молекулы равна 6. В каждой точке пространства молекула могла обладать любой скоростью, то есть координаты и импульсы молекулы являются независимыми переменными, независимыми случайными величинами. 19
Распределения Максвелла. Распределение Максвелла по векторам и компонентам скоростей. Выберем в качестве системы одну молекулу идеального газа. Пренебрегая внешними потенциальными полями, можно считать, что вся энергия системы это кинетическая энергия молекулы Тогда функция распределения Гиббса, записанная для подпространства скоростей для данной молекулы принимает вид Размерность фазового пространства одной молекулы равна 6. В каждой точке пространства молекула могла обладать любой скоростью, то есть координаты и импульсы молекулы являются независимыми переменными, независимыми случайными величинами. 19
 Тогда по теореме об умножении вероятностей независимых событий можно записать или константа C = Cq Cp, а фазовый объем равен d = d. V dp. Тогда, в силу независимости координат и импульсов, можно выделить отдельно распределение по координатам и распределение по импульсам и Так как импульс пропорционален скорости, то распределение по скоростям также пропорционально распределению по импульсам, то есть будет отличаться от распределения по импульсам только нормировочным множителем. 20
Тогда по теореме об умножении вероятностей независимых событий можно записать или константа C = Cq Cp, а фазовый объем равен d = d. V dp. Тогда, в силу независимости координат и импульсов, можно выделить отдельно распределение по координатам и распределение по импульсам и Так как импульс пропорционален скорости, то распределение по скоростям также пропорционально распределению по импульсам, то есть будет отличаться от распределения по импульсам только нормировочным множителем. 20
 Поэтому с учетом формулы кинетической энергии частицы может быть записана формула Очевидно, что она определяет вероятность обнаружить молекулу в фазовом объеме Применяя приведенные выше рассуждения для координат и импульсов теперь к проекциям скорости молекулы, получим что позволяет записать для каждой из проекций в силу их независимости и т. д. Это распределение, очевидно, показывает вероятность того, что проекция скорости будет лежать в интервале от vx до vx + dvx. Видно также, что вероятность иметь более высокие значения проек ции скорости достаточно быстро убывает, то есть молекула более охотно, с большей вероятностью, занимает состояния с более низкими значениями проекции скорости. 21
Поэтому с учетом формулы кинетической энергии частицы может быть записана формула Очевидно, что она определяет вероятность обнаружить молекулу в фазовом объеме Применяя приведенные выше рассуждения для координат и импульсов теперь к проекциям скорости молекулы, получим что позволяет записать для каждой из проекций в силу их независимости и т. д. Это распределение, очевидно, показывает вероятность того, что проекция скорости будет лежать в интервале от vx до vx + dvx. Видно также, что вероятность иметь более высокие значения проек ции скорости достаточно быстро убывает, то есть молекула более охотно, с большей вероятностью, занимает состояния с более низкими значениями проекции скорости. 21
 Чтобы окончательно записать функции распределения, осталось лишь их пронормировать: получим и две другие нормировочные постоянные будут иметь такое же значение Итак, распределение Максвелла по компонентам скорости имеет вид распределение Максвелла по векторам скоростей имеет вид 22
Чтобы окончательно записать функции распределения, осталось лишь их пронормировать: получим и две другие нормировочные постоянные будут иметь такое же значение Итак, распределение Максвелла по компонентам скорости имеет вид распределение Максвелла по векторам скоростей имеет вид 22
 Найти среднее значение и дисперсию полученных распределений. Распределение Максвелла по модулям скоростей. Найти вероятность того, что модуль скорости молекулы будет принадлежать интервалу от v до v + dv. В подпространстве скоростей элементом фазового объема является тонкий шаровой слой, центр которого совпадает с началом координат (именно в этом слое будут заканчиваться все векторы скорости почти одинаковой длины от v до v + dv и произвольного направления). Тогда удобно воспользоваться сферической системой координат, что позволит свести трехмерную задачу к одномерной, учитывая сферическую симметрию задачи. Объем шарового слоя Тогда распределение Гиббса примет вид: Нужно его пронормировать. 23
Найти среднее значение и дисперсию полученных распределений. Распределение Максвелла по модулям скоростей. Найти вероятность того, что модуль скорости молекулы будет принадлежать интервалу от v до v + dv. В подпространстве скоростей элементом фазового объема является тонкий шаровой слой, центр которого совпадает с началом координат (именно в этом слое будут заканчиваться все векторы скорости почти одинаковой длины от v до v + dv и произвольного направления). Тогда удобно воспользоваться сферической системой координат, что позволит свести трехмерную задачу к одномерной, учитывая сферическую симметрию задачи. Объем шарового слоя Тогда распределение Гиббса примет вид: Нужно его пронормировать. 23
 Учтем, что нижний предел интеграла равен нулю этот интеграл сводится к табличному, при вычислении которого удобно воспользоваться Г функцией И окончательно распределение Максвелла по скоростям принимает вид: 24
Учтем, что нижний предел интеграла равен нулю этот интеграл сводится к табличному, при вычислении которого удобно воспользоваться Г функцией И окончательно распределение Максвелла по скоростям принимает вид: 24
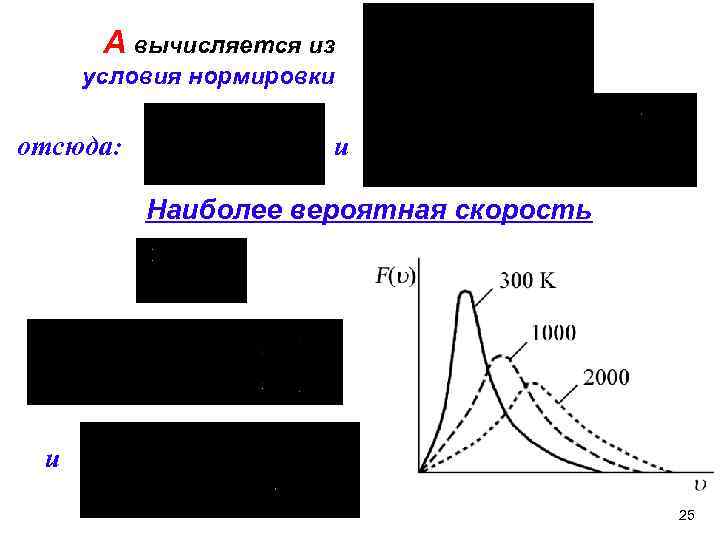 А вычисляется из условия нормировки отсюда: и Наиболее вероятная скорость и 25
А вычисляется из условия нормировки отсюда: и Наиболее вероятная скорость и 25
 Среднюю квадратичную скорость найдем используя соотношение Тогда – для одной молекулы. – для одного моля газа. 26
Среднюю квадратичную скорость найдем используя соотношение Тогда – для одной молекулы. – для одного моля газа. 26
 Средняя арифметическая скорость υср где nf( )d =dn – число молекул со скоростью от υ до υ+dυ. Если подставить сюда f(υ) и вычислить, то: Полезно знать, что 27
Средняя арифметическая скорость υср где nf( )d =dn – число молекул со скоростью от υ до υ+dυ. Если подставить сюда f(υ) и вычислить, то: Полезно знать, что 27
 Джеймс Клерк Максвелл James Clerk Maxwell (13. 06. 1831 – 05. 11. 1879) шотландский физик родился в Эдинбурге Наиболее известные работы основные законы электричества и магнетизма – уравнения Максвелла (1865) Распределение Максвелла в кинетической теории газов 28
Джеймс Клерк Максвелл James Clerk Maxwell (13. 06. 1831 – 05. 11. 1879) шотландский физик родился в Эдинбурге Наиболее известные работы основные законы электричества и магнетизма – уравнения Максвелла (1865) Распределение Максвелла в кинетической теории газов 28
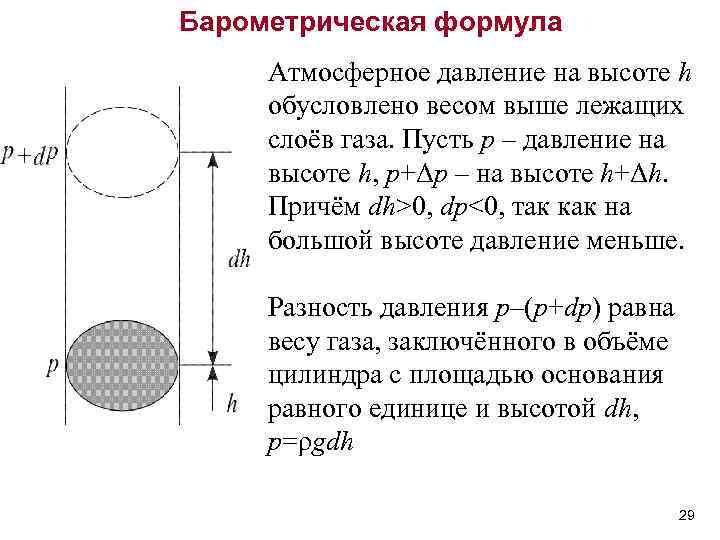 Барометрическая формула Атмосферное давление на высоте h обусловлено весом выше лежащих слоёв газа. Пусть p – давление на высоте h, p+Δp – на высоте h+Δh. Причём dh>0, dр<0, так как на большой высоте давление меньше. Разность давления p–(p+dp) равна весу газа, заключённого в объёме цилиндра с площадью основания равного единице и высотой dh, p=ρgdh 29
Барометрическая формула Атмосферное давление на высоте h обусловлено весом выше лежащих слоёв газа. Пусть p – давление на высоте h, p+Δp – на высоте h+Δh. Причём dh>0, dр<0, так как на большой высоте давление меньше. Разность давления p–(p+dp) равна весу газа, заключённого в объёме цилиндра с площадью основания равного единице и высотой dh, p=ρgdh 29
 p–(p+dp)=ρqdh, ρ плотность газа на высоте h, тогда где р0 – давление на высоте h=0. Это барометрическая формула. Из формулы следует, что р убывает с высотой тем быстрее, чем тяжелее газ (чем больше μ) и чем ниже температура. 30
p–(p+dp)=ρqdh, ρ плотность газа на высоте h, тогда где р0 – давление на высоте h=0. Это барометрическая формула. Из формулы следует, что р убывает с высотой тем быстрее, чем тяжелее газ (чем больше μ) и чем ниже температура. 30
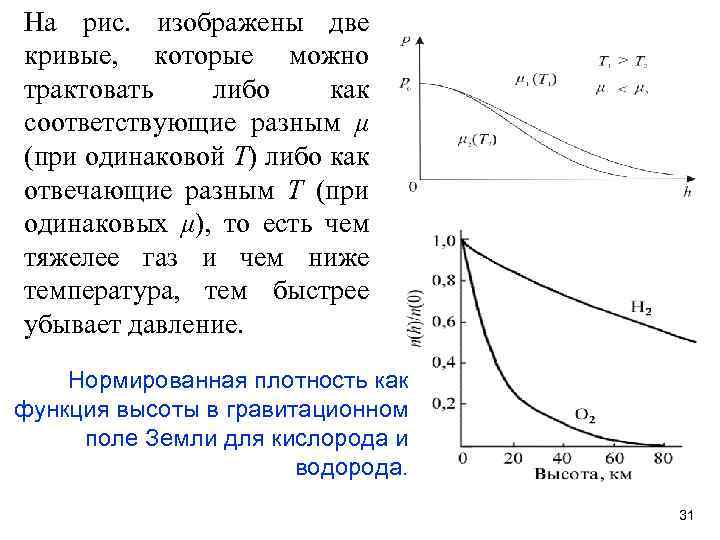 На рис. изображены две кривые, которые можно трактовать либо как соответствующие разным μ (при одинаковой Т) либо как отвечающие разным Т (при одинаковых μ), то есть чем тяжелее газ и чем ниже температура, тем быстрее убывает давление. Нормированная плотность как функция высоты в гравитационном поле Земли для кислорода и водорода. 31
На рис. изображены две кривые, которые можно трактовать либо как соответствующие разным μ (при одинаковой Т) либо как отвечающие разным Т (при одинаковых μ), то есть чем тяжелее газ и чем ниже температура, тем быстрее убывает давление. Нормированная плотность как функция высоты в гравитационном поле Земли для кислорода и водорода. 31
 Распределение Больцмана Известно р=nk. T – это основное уравнение МКТ заменим p и p 0 в барометрической формуле, получим где n 0 число молекул в единице объёма на высоте h=0, n – число молекул в единице объёма на высоте h. Так как μ=m. NА, R=NАk, то 32
Распределение Больцмана Известно р=nk. T – это основное уравнение МКТ заменим p и p 0 в барометрической формуле, получим где n 0 число молекул в единице объёма на высоте h=0, n – число молекул в единице объёма на высоте h. Так как μ=m. NА, R=NАk, то 32
 С уменьшением температуры число молекул на высотах, отличных от нуля убывает. При Т=0 тепловое движение прекращается, все молекулы расположились бы на земной поверхности. При высоких температурах, наоборот, молекулы оказываются распределёнными по высоте почти равномерно, а плотность молекул медленно убывает с высотой. Так как mgh – это потенциальная энергия, то на разных высотах Wn=mgh – различно. Следовательно функция характеризует распределение частиц по значениям потенциальной энергии: – функция распределения Больцмана. 33
С уменьшением температуры число молекул на высотах, отличных от нуля убывает. При Т=0 тепловое движение прекращается, все молекулы расположились бы на земной поверхности. При высоких температурах, наоборот, молекулы оказываются распределёнными по высоте почти равномерно, а плотность молекул медленно убывает с высотой. Так как mgh – это потенциальная энергия, то на разных высотах Wn=mgh – различно. Следовательно функция характеризует распределение частиц по значениям потенциальной энергии: – функция распределения Больцмана. 33
 Больцман (Ludwig Boltzmann) (20. 02. 1844 - 05. 11. 1906) немецкий физик родился в Вене (Vienna, Austria), умер в Триесте (Duino - near Trieste, Austria) 34
Больцман (Ludwig Boltzmann) (20. 02. 1844 - 05. 11. 1906) немецкий физик родился в Вене (Vienna, Austria), умер в Триесте (Duino - near Trieste, Austria) 34
 Больцман доказал, что соотношение справедливо не только в потенциальном поле сил гравитации, но и в любом потенциальном поле, для совокупности любых одинаковых частиц, находящихся в состоянии хаотического теплового движения. Опыт Перрена по экспериментальному определению числа Авогадро вес частицы с учетом силы Архимеда , 0 плотность вещества частицы и жидкости соответственно n 1 и n 2 число частиц в поле зрения микроскопа в двух слоях эмульсии x 1 и x 2 35
Больцман доказал, что соотношение справедливо не только в потенциальном поле сил гравитации, но и в любом потенциальном поле, для совокупности любых одинаковых частиц, находящихся в состоянии хаотического теплового движения. Опыт Перрена по экспериментальному определению числа Авогадро вес частицы с учетом силы Архимеда , 0 плотность вещества частицы и жидкости соответственно n 1 и n 2 число частиц в поле зрения микроскопа в двух слоях эмульсии x 1 и x 2 35
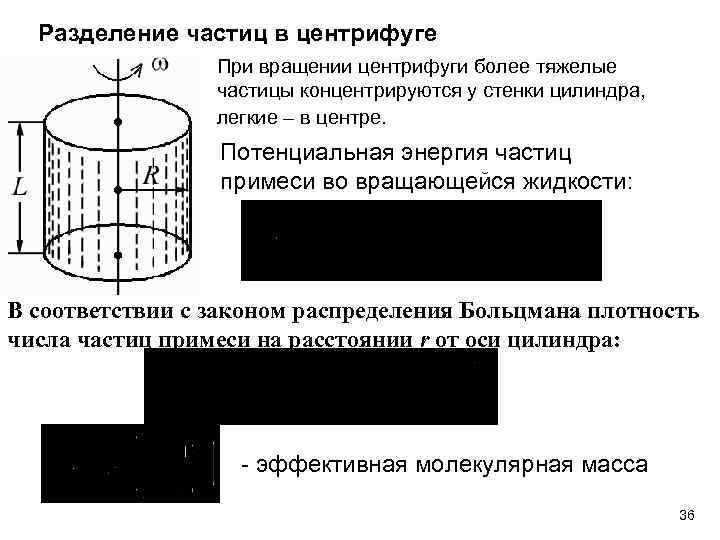 Разделение частиц в центрифуге При вращении центрифуги более тяжелые частицы концентрируются у стенки цилиндра, легкие – в центре. Потенциальная энергия частиц примеси во вращающейся жидкости: В соответствии с законом распределения Больцмана плотность числа частиц примеси на расстоянии r от оси цилиндра: эффективная молекулярная масса 36
Разделение частиц в центрифуге При вращении центрифуги более тяжелые частицы концентрируются у стенки цилиндра, легкие – в центре. Потенциальная энергия частиц примеси во вращающейся жидкости: В соответствии с законом распределения Больцмана плотность числа частиц примеси на расстоянии r от оси цилиндра: эффективная молекулярная масса 36
 Итак, Максвелл дал распределение частиц по значениям кинетической энергии, а Больцман – по значениям потенциальной энергии. Оба распределения можно объёдинить в один закон – распределение Максвелла–Больцмана. 37
Итак, Максвелл дал распределение частиц по значениям кинетической энергии, а Больцман – по значениям потенциальной энергии. Оба распределения можно объёдинить в один закон – распределение Максвелла–Больцмана. 37
 закон Максвелла–Больцмана, согласно которому, число молекул в единице объёма, скорости которых лежат в пределах от υ до υ+dυ равно если W – полная энергия W = Wп+Wк, где n 0 – число молекул в единице объёма в той точке, где Wп=0, и 38
закон Максвелла–Больцмана, согласно которому, число молекул в единице объёма, скорости которых лежат в пределах от υ до υ+dυ равно если W – полная энергия W = Wп+Wк, где n 0 – число молекул в единице объёма в той точке, где Wп=0, и 38


