Лекции по оптике для ИМ 3.ppt
- Количество слайдов: 35
 Квантовые свойства света
Квантовые свойства света
 Гипотеза квантов • 1900 г. Атомные осцилляторы излучают энергию не непрерывно, а определенными порциями – квантами, причем энергия кванта пропорциональна частоте колебаний: М. Планк (1858 – 1947), нем. ЛНП 1918 г.
Гипотеза квантов • 1900 г. Атомные осцилляторы излучают энергию не непрерывно, а определенными порциями – квантами, причем энергия кванта пропорциональна частоте колебаний: М. Планк (1858 – 1947), нем. ЛНП 1918 г.
 Фотоэффект – эффект возникновения электрических явлений при поглощении света веществом. Различают внешний, внутренний и вентильный фотоэффекты. Внешний фотоэффект – выход электронов через поверхность освещенного тела. Открыт Г. Герцем в 1887 г. , детально исследован А. Г. Столетовым в 1888 г.
Фотоэффект – эффект возникновения электрических явлений при поглощении света веществом. Различают внешний, внутренний и вентильный фотоэффекты. Внешний фотоэффект – выход электронов через поверхность освещенного тела. Открыт Г. Герцем в 1887 г. , детально исследован А. Г. Столетовым в 1888 г.
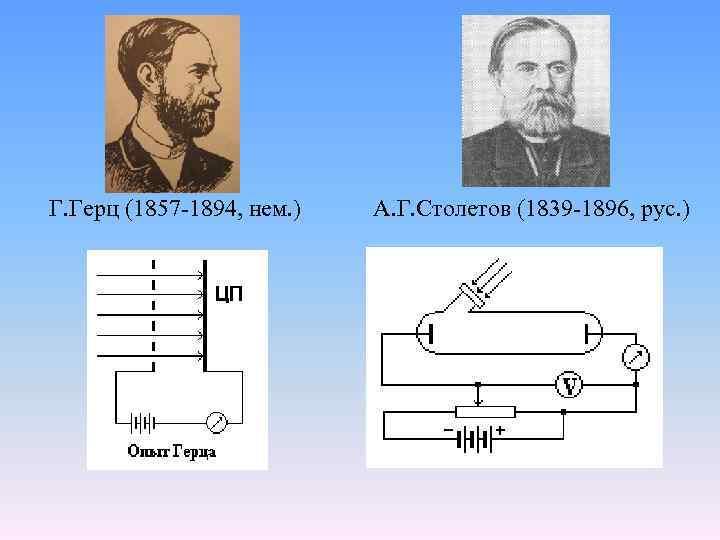 Г. Герц (1857 -1894, нем. ) А. Г. Столетов (1839 -1896, рус. )
Г. Герц (1857 -1894, нем. ) А. Г. Столетов (1839 -1896, рус. )
 Вольтамперная характеристика лампы • По величине силы тока насыщения можно определить количество электронов, вырываемых светом из катода за 1 секунду:
Вольтамперная характеристика лампы • По величине силы тока насыщения можно определить количество электронов, вырываемых светом из катода за 1 секунду:
 Вольтамперная характеристика лампы • По величине задерживающего напряжения может быть определена максимальная кинетическая энергия фотоэлектронов:
Вольтамперная характеристика лампы • По величине задерживающего напряжения может быть определена максимальная кинетическая энергия фотоэлектронов:
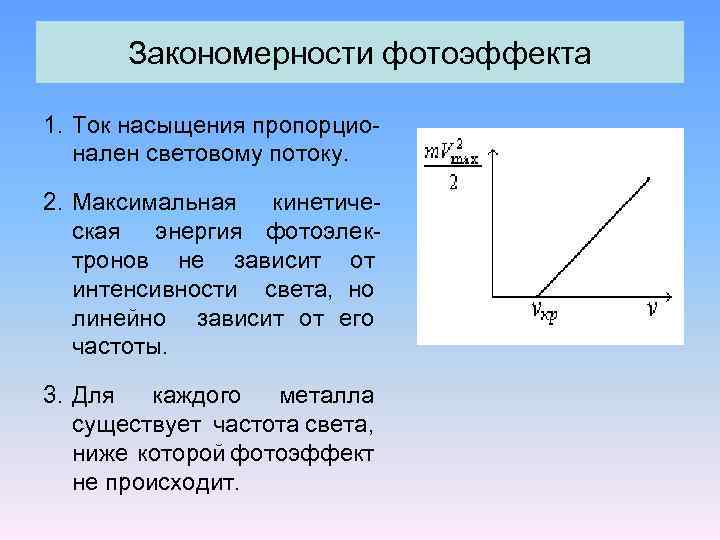 Закономерности фотоэффекта 1. Ток насыщения пропорционален световому потоку. 2. Максимальная кинетическая энергия фотоэлектронов не зависит от интенсивности света, но линейно зависит от его частоты. 3. Для каждого металла существует частота света, ниже которой фотоэффект не происходит.
Закономерности фотоэффекта 1. Ток насыщения пропорционален световому потоку. 2. Максимальная кинетическая энергия фотоэлектронов не зависит от интенсивности света, но линейно зависит от его частоты. 3. Для каждого металла существует частота света, ниже которой фотоэффект не происходит.
 Квантовая теория излучения • М. Планк, 1900 г. – гипотеза о квантовании процесса испускания и поглощения света атомом. (НП 1918 г. ) • А. Эйнштейн, 1905 г. – перенос гипотезы квантов на структуру излучения. (НП 1921 г. )
Квантовая теория излучения • М. Планк, 1900 г. – гипотеза о квантовании процесса испускания и поглощения света атомом. (НП 1918 г. ) • А. Эйнштейн, 1905 г. – перенос гипотезы квантов на структуру излучения. (НП 1921 г. )
 Квантовая теория излучения • А. Эйнштейн, 1905 г. . волновой вектор.
Квантовая теория излучения • А. Эйнштейн, 1905 г. . волновой вектор.
 Квантовая теория фотоэффекта • А. Эйнштейн, 1905 г.
Квантовая теория фотоэффекта • А. Эйнштейн, 1905 г.
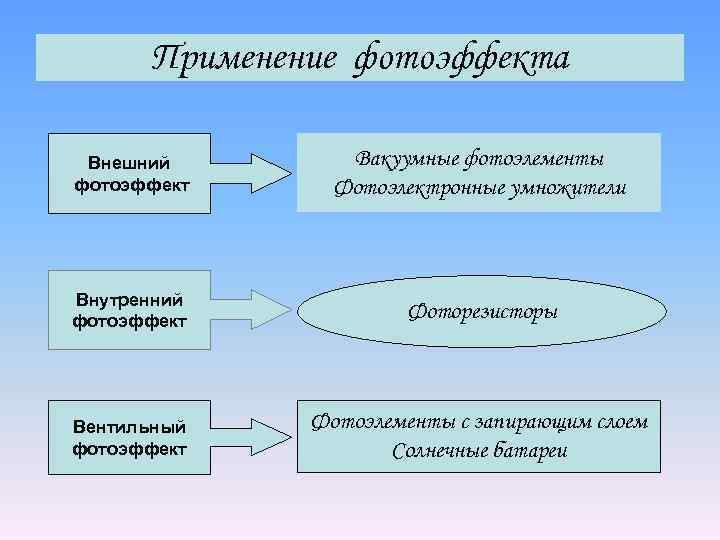 Применение фотоэффекта Внешний фотоэффект Вакуумные фотоэлементы Фотоэлектронные умножители Внутренний фотоэффект Фоторезисторы Вентильный фотоэффект Фотоэлементы с запирающим слоем Солнечные батареи
Применение фотоэффекта Внешний фотоэффект Вакуумные фотоэлементы Фотоэлектронные умножители Внутренний фотоэффект Фоторезисторы Вентильный фотоэффект Фотоэлементы с запирающим слоем Солнечные батареи
 Применение фотоэффекта Фотоумножитель Вентильный фотоэлемент
Применение фотоэффекта Фотоумножитель Вентильный фотоэлемент
 Давление света
Давление света
 • Гипотезу о существовании светового давления в начале 17 века высказал И. Кеплер на основе анализа формы кометных хвостов. И. Кеплер (нем. , 1571 -1630)
• Гипотезу о существовании светового давления в начале 17 века высказал И. Кеплер на основе анализа формы кометных хвостов. И. Кеплер (нем. , 1571 -1630)
 • В 1873 г. Дж. Максвелл рассчитал световое давление на основе электромагнитной теории: Дж. Максвелл (англ. , 1831 – 1879)
• В 1873 г. Дж. Максвелл рассчитал световое давление на основе электромагнитной теории: Дж. Максвелл (англ. , 1831 – 1879)
 Количественные оценки давления света Источник света Интенсивность света, Вт/м 2 Давление света, Па (при r=1) Солнце 1, 3· 103 10 -5 Обычные источники света Мощные импульсные лазеры до 105 10 -3 до 1015 107 Атмосферное давление РА = 105 Па.
Количественные оценки давления света Источник света Интенсивность света, Вт/м 2 Давление света, Па (при r=1) Солнце 1, 3· 103 10 -5 Обычные источники света Мощные импульсные лазеры до 105 10 -3 до 1015 107 Атмосферное давление РА = 105 Па.
 • П. Н. Лебедев в 1898 -99 г. экспериментально измерил световое давление и получил результаты, согласующиеся с теорией Максвелла. • У. Томсон: П. Н. Лебедев (рус. , 1866 – 1912) Известен как блестящий экспериментатор-виртуоз, автор исследований, выполненных скромными средствами на грани технических возможностей того времени, но поражающих глубокой интуицией и гениальностью. «Я всю жизнь воевал с Максвеллом, не признавая его светового давления, и вот… Лебедев заставил меня сдаться перед его опытами» .
• П. Н. Лебедев в 1898 -99 г. экспериментально измерил световое давление и получил результаты, согласующиеся с теорией Максвелла. • У. Томсон: П. Н. Лебедев (рус. , 1866 – 1912) Известен как блестящий экспериментатор-виртуоз, автор исследований, выполненных скромными средствами на грани технических возможностей того времени, но поражающих глубокой интуицией и гениальностью. «Я всю жизнь воевал с Максвеллом, не признавая его светового давления, и вот… Лебедев заставил меня сдаться перед его опытами» .
 Фотонная теория давления света • С точки зрения квантовой теории, давление света обусловлено тем, что каждый фотон при соударении с поверхностью тела передает ей импульс. • Если фотон поглощается, то он передает поверхности импульс p = hv/c. • При зеркальном отражении от поверхности в направлении нормали фотон передает поверхности импульс 2 p = 2 hv/c.
Фотонная теория давления света • С точки зрения квантовой теории, давление света обусловлено тем, что каждый фотон при соударении с поверхностью тела передает ей импульс. • Если фотон поглощается, то он передает поверхности импульс p = hv/c. • При зеркальном отражении от поверхности в направлении нормали фотон передает поверхности импульс 2 p = 2 hv/c.
 Световое давление: • определяет форму кометных хвостов; • препятствует гравитационному сжатию звезд; • влияет на движение космических аппаратов.
Световое давление: • определяет форму кометных хвостов; • препятствует гравитационному сжатию звезд; • влияет на движение космических аппаратов.
 Атом Резерфорда - Бора
Атом Резерфорда - Бора
 Истоки атомной физики • III век до н. э. – возникновение представлений об атомах как неделимых частицах веществ (Демокрит, Эпикур, Лукреций). • ХVIII век – доказательство реального существования атомов, молекул (М. В. Ломоносов, А. Лавуазье, Д. Дальтон). • 1869 г. – открытие Д. И. Менделеевым периодического закона для химических элементов.
Истоки атомной физики • III век до н. э. – возникновение представлений об атомах как неделимых частицах веществ (Демокрит, Эпикур, Лукреций). • ХVIII век – доказательство реального существования атомов, молекул (М. В. Ломоносов, А. Лавуазье, Д. Дальтон). • 1869 г. – открытие Д. И. Менделеевым периодического закона для химических элементов.
 • 1897 г. – открытие электрона (Дж. Томсон). • 1903 г. – построение первой модели атома, учитывающей существование электронов (Томсон, «Пудинг с изюмом» ). Томсон Джозеф Джон (1856 -1940, англ. ) ЛНП 1906 г.
• 1897 г. – открытие электрона (Дж. Томсон). • 1903 г. – построение первой модели атома, учитывающей существование электронов (Томсон, «Пудинг с изюмом» ). Томсон Джозеф Джон (1856 -1940, англ. ) ЛНП 1906 г.
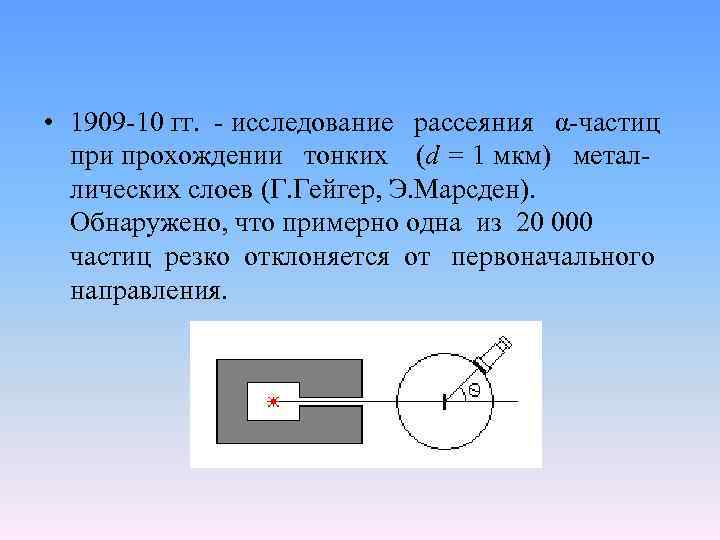 • 1909 -10 гг. - исследование рассеяния α-частиц при прохождении тонких (d = 1 мкм) металлических слоев (Г. Гейгер, Э. Марсден). Обнаружено, что примерно одна из 20 000 частиц резко отклоняется от первоначального направления.
• 1909 -10 гг. - исследование рассеяния α-частиц при прохождении тонких (d = 1 мкм) металлических слоев (Г. Гейгер, Э. Марсден). Обнаружено, что примерно одна из 20 000 частиц резко отклоняется от первоначального направления.
 • 1911 г. - Построение Резерфордом планетарной модели атома. • RA = 10 -10 м; RЯ = 10 -15 м. Э. Резерфорд (1871 -1937, англ. ) ЛНП 1908 г.
• 1911 г. - Построение Резерфордом планетарной модели атома. • RA = 10 -10 м; RЯ = 10 -15 м. Э. Резерфорд (1871 -1937, англ. ) ЛНП 1908 г.
 Трудности модели • Электрон в атоме движется ускоренно. С позиций классической электродинамики при таком движении электрон должен излучать. Расстояние от него до ядра должно непрерывно уменьшаться, а частота обращения (и частота излучения) должна непрерывно возрастать. За время порядка 10 -11 с электрон должен упасть на ядро. Т. о. , спектр излучения атома должен быть непрерывным, а атом – неустойчивым. Это противоречит действительности.
Трудности модели • Электрон в атоме движется ускоренно. С позиций классической электродинамики при таком движении электрон должен излучать. Расстояние от него до ядра должно непрерывно уменьшаться, а частота обращения (и частота излучения) должна непрерывно возрастать. За время порядка 10 -11 с электрон должен упасть на ядро. Т. о. , спектр излучения атома должен быть непрерывным, а атом – неустойчивым. Это противоречит действительности.
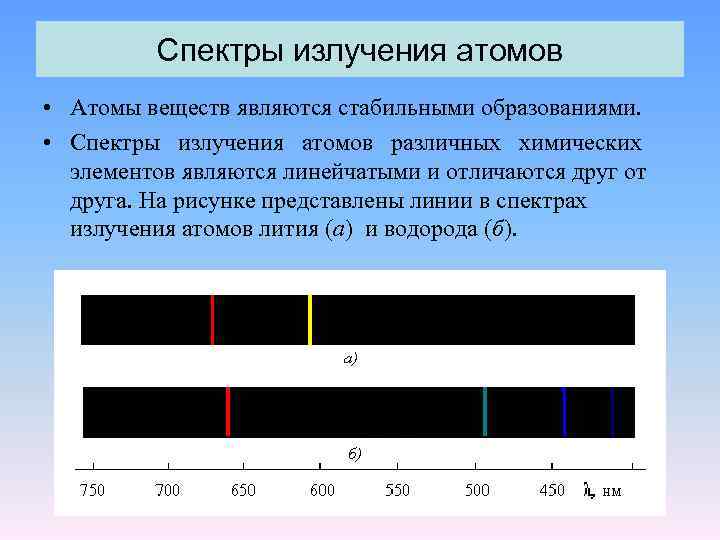 Спектры излучения атомов • Атомы веществ являются стабильными образованиями. • Спектры излучения атомов различных химических элементов являются линейчатыми и отличаются друг от друга. На рисунке представлены линии в спектрах излучения атомов лития (а) и водорода (б).
Спектры излучения атомов • Атомы веществ являются стабильными образованиями. • Спектры излучения атомов различных химических элементов являются линейчатыми и отличаются друг от друга. На рисунке представлены линии в спектрах излучения атомов лития (а) и водорода (б).
 Закономерности в спектре излучения атома водорода • В области видимого света спектральные линии излучения атома водорода подчиняются вполне определенной закономерности (Бальмер, 1885 г. ): Здесь R = 1, 1· 107 м-1 (постоянная Ридберга), m = 2, n = 3, 4, 5, 6. Спектральные линии при значениях n = 7, 8, 9… находятся в ультрафиолетовой области.
Закономерности в спектре излучения атома водорода • В области видимого света спектральные линии излучения атома водорода подчиняются вполне определенной закономерности (Бальмер, 1885 г. ): Здесь R = 1, 1· 107 м-1 (постоянная Ридберга), m = 2, n = 3, 4, 5, 6. Спектральные линии при значениях n = 7, 8, 9… находятся в ультрафиолетовой области.
 Закономерности в спектре излучения атома водорода • В области ультрафиолетового излучения наблюдается серия спектральных линий (открыта Лайманом в 1906 г. ), для которой при том же значении параметра R число m = 1, а n принимает значения 2, 3, 4… • Несколько серий спектральных линий наблюдаются в инфракрасной области излучения: серия Пашена – m = 3, n = 4, 5, 6… серия Брэкета – m = 4, n = 5, 6, 7… серия Пфунда – m = 5, n = 6, 7, 8…
Закономерности в спектре излучения атома водорода • В области ультрафиолетового излучения наблюдается серия спектральных линий (открыта Лайманом в 1906 г. ), для которой при том же значении параметра R число m = 1, а n принимает значения 2, 3, 4… • Несколько серий спектральных линий наблюдаются в инфракрасной области излучения: серия Пашена – m = 3, n = 4, 5, 6… серия Брэкета – m = 4, n = 5, 6, 7… серия Пфунда – m = 5, n = 6, 7, 8…
 Постулаты Бора • В атоме существуют стационарные состояния, находясь в которых он не излучает энергии. • В стационарных состояниях момент импульса электрона кратен постоянной Планка: n = 1, 2, 3… - квантовое число. • При переходе электрона с одной стационарной орбиты на другую излучается (поглощается) один фотон с энергией Н. Бор (1885 -1962, дат. ) ЛНП 1922 г.
Постулаты Бора • В атоме существуют стационарные состояния, находясь в которых он не излучает энергии. • В стационарных состояниях момент импульса электрона кратен постоянной Планка: n = 1, 2, 3… - квантовое число. • При переходе электрона с одной стационарной орбиты на другую излучается (поглощается) один фотон с энергией Н. Бор (1885 -1962, дат. ) ЛНП 1922 г.
 Теория атома водорода Н. Бора • В теории Бора расчет радиусов стационарных орбит и энергии атома водорода в этих состояниях проводится на основе использования двух уравнений – второго закона Ньютона и условия квантования электронных орбит:
Теория атома водорода Н. Бора • В теории Бора расчет радиусов стационарных орбит и энергии атома водорода в этих состояниях проводится на основе использования двух уравнений – второго закона Ньютона и условия квантования электронных орбит:
 • Исключив из этих уравнений скорость v, найдем формулу для радиуса стационарной орбиты электрона: Здесь r 1 – первый боровский радиус. r 1 = 0, 528· 10 -10 м = 5, 28 · 10 -2 нм.
• Исключив из этих уравнений скорость v, найдем формулу для радиуса стационарной орбиты электрона: Здесь r 1 – первый боровский радиус. r 1 = 0, 528· 10 -10 м = 5, 28 · 10 -2 нм.
 • Энергия атома Еn в стационарном состоянии равна, по модели Бора, сумме кинетической энергии электрона на стационарной орбите и потенциальной энергии взаимодействия электрона с ядром: Исключив из этого выражения скорость v с помощью уравнения, выражающего второй закон Ньютона, получим:
• Энергия атома Еn в стационарном состоянии равна, по модели Бора, сумме кинетической энергии электрона на стационарной орбите и потенциальной энергии взаимодействия электрона с ядром: Исключив из этого выражения скорость v с помощью уравнения, выражающего второй закон Ньютона, получим:
 • Подставив в выражение для энергии радиус стационарной орбиты, получим итоговую формулу для энергии стационарного состояния атома водорода:
• Подставив в выражение для энергии радиус стационарной орбиты, получим итоговую формулу для энергии стационарного состояния атома водорода:
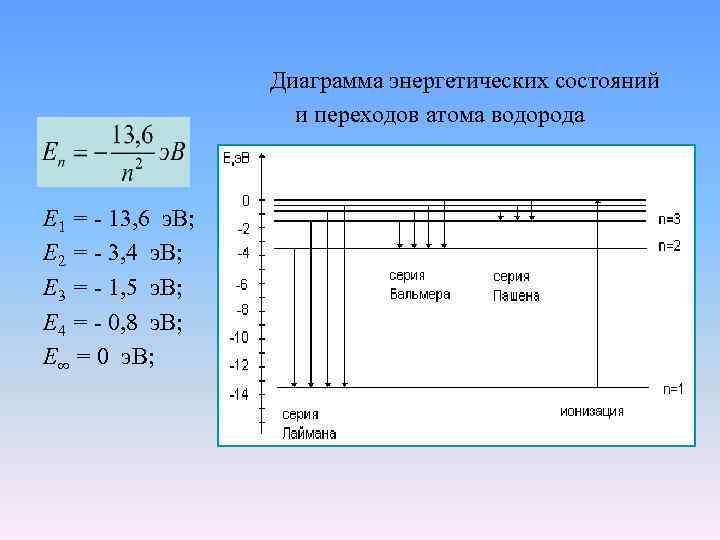 Диаграмма энергетических состояний и переходов атома водорода Е 1 = - 13, 6 э. В; Е 2 = - 3, 4 э. В; Е 3 = - 1, 5 э. В; Е 4 = - 0, 8 э. В; Е∞ = 0 э. В;
Диаграмма энергетических состояний и переходов атома водорода Е 1 = - 13, 6 э. В; Е 2 = - 3, 4 э. В; Е 3 = - 1, 5 э. В; Е 4 = - 0, 8 э. В; Е∞ = 0 э. В;
 Трудности теории Бора Теория Бора • внутренне противоречива; • не может объяснить спектры излучения атома гелия и более сложных атомов; • не дает никакого рецепта для вычисления интенсивности спектральных линий; • не может объяснить природу химических связей в молекулах.
Трудности теории Бора Теория Бора • внутренне противоречива; • не может объяснить спектры излучения атома гелия и более сложных атомов; • не дает никакого рецепта для вычисления интенсивности спектральных линий; • не может объяснить природу химических связей в молекулах.


