постулати Бора.ppt
- Количество слайдов: 16

Квантові постулати Н. Бора. Випромінювання та поглинання світла атомами. Атомні й молекулярні спектри. Спектральний аналіз та його застосування

В 1912 р. Бор декілька місяців працював в лабораторії Резерфорда. Він прийшов до висновку, що планетарна модель атома Резерфорда в основному є вірною. Але інтуїція підказувала йому, що для того щоб уникнути труднощів, з якими зіткнулися вчені під час застосування цієї моделі атома, в планетарну модель атома потрібно якимось чином включити квантову теорію, яка робила тоді перші кроки. Роботи Планка та Ейнштейна показали, що в нагрітих твердих тілах енергія електричних зарядів змінюється дискретними порціями під час переходу від одного дискретного стану до іншого, під час чого випускається квант випромінювання. Можливо, розмірковував Бор, що електрони в атомах також не можуть втрачати енергію безперервно, а повинні здійснювати при цьому квантові переходи. Працюючи над своєю теорією, Бор вже в наступному році сформулював свої постулати за які у 1922 році отримав Нобелівську премію з фізики

Нільс Бор (1885 – 1962) • 1913 рік – постулати Бора • 1922 рік – Нобелівська премія з фізики

Тема уроку. Квантові постулати Н. Бора. Випромінювання та поглинання світла атомами. Атомні й молекулярні спектри. Спектральний аналіз та його застосування Мета уроку. Розглянути сутність постулатів Бора, з'ясувати квантовий характер випромінювання та поглинання світла атомом та закономірності в лінійчастих спектрах; з'ясувати практичне застосування спектрального аналізу; навчитися застосовувати набуті знання під час розв'язування завдань різного рівня складності, розвивати логічне мислення, вміння робити висновки та узагальнення

План вивчення нової теми 1. Квантові постулати Бора 2. Випромінювання та поглинання світла атомами 3. Атомні та молекулярні спектри 4. Спектральний аналіз

Постулати Бора І постулат Атом може перебувати тільки в особливих стаціонарних (квантових) станах, кожному з яких відповідає певна енергія. В стаціонарному стані атом не випромінює електромагнітних хвиль ІІ постулат При переході атома з одного стаціонарного стану в інший випромінюється або поглинається квант електромагнітної енергії
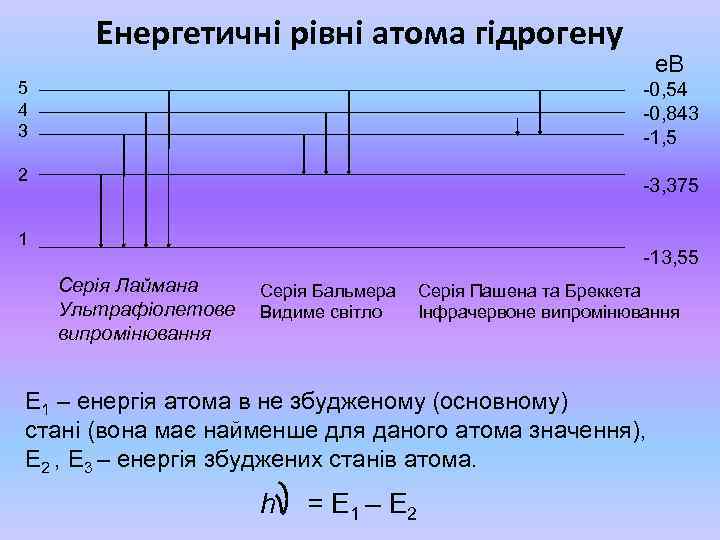
Енергетичні рівні атома гідрогену 5 4 3 е. В -0, 54 -0, 843 -1, 5 2 -3, 375 1 -13, 55 Серія Лаймана Серія Бальмера Ультрафіолетове Видиме світло випромінювання Серія Пашена та Бреккета Інфрачервоне випромінювання E 1 – енергія атома в не збудженому (основному) стані (вона має найменше для даного атома значення), E 2 , E 3 – енергія збуджених станів атома. h = E 1 – E 2

Неперервний (суцільний) спектр випромінювання Дають тіла, що перебувають у твердому або рідкому стані, які нагріті до високої температури

Лінійчастий спектр випромінювання Дають усі речовини в газоподібному атомарному (але не молекулярному) стані 2 – лінійчастий спектр випромінювання натрію 3 – лінійчастий спектр випромінювання гідрогену 4 – лінійчастий спектр випромінювання гелію

Смугасті спектри випромінювання Складається з окремих смуг, розділених певними проміжками Спектр вугільної дуги C 2 Спектр молекул йоду Дають молекули, що слабо зв'язані або не зв'язані між собою
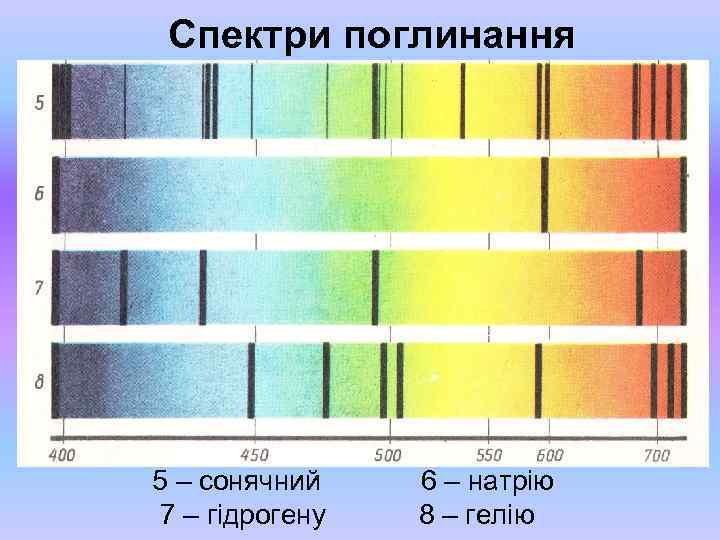
Спектри поглинання 5 – сонячний 7 – гідрогену 6 – натрію 8 – гелію

Спектральний аналіз – це метод вивчення хімічного складу (якісного та кількісного) речовини за спектром Особливість методу: 1) для аналізу достатньо речовини масою близько 10 -13 кг; 2) проводиться набагато швидше, ніж хімічний аналіз; 3) можна проводити без контакту з речовиною, яку вивчають – достатньо проаналізувати випромінювання речовини Спектри дають інформацію про: 1) температуру речовини; 2) тиск; 3) швидкість руху джерела; 4) магнітну індукцію Можна отримати інформацію про хімічний склад: 1) руд та мінералів; 2) у металургії; 3) у машинобудуванні; 4) в атомній індустрії; 5) сонця та зір; 6) складних органічних молекул
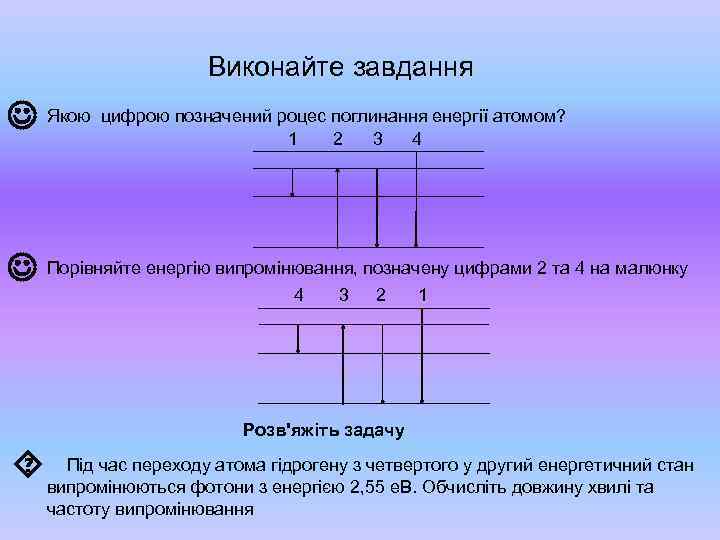
Виконайте завдання Якою цифрою позначений роцес поглинання енергії атомом? 1 2 3 4 Порівняйте енергію випромінювання, позначену цифрами 2 та 4 на малюнку 4 3 2 1 Розв'яжіть задачу Під час переходу атома з четвертого у другий енергетичний випромінюються фотони з гідрогену 2, 55 е. В. Обчисліть довжину хвилі та стан енергією частоту випромінювання

Тестове завдання 1. Постулат – це: а) пояснення; б) твердження; в) гіпотеза 2. Під час переходу електрона зі стаціонарного стану у збуджений, електрон: а) поглинає енергію; б) випромінює енергію; в) не випромінює та не поглинає енергію 3. Ультрафіолетове випромінювання описує серія: а) Лаймана; б) Бальмера; в) Пашена та Бреккета 4. Лінійчастий спектр випромінювання дають: а) молекули, що слабо зв’язані між собою; б) нагріті до високої температури тіла, що перебувають у твердому агрегатному стані; в) всі речовини, що перебувають в газоподібному атомарному стані 5. За допомогою спектроскопа дістали суцільний спектр. Що можна за цим спектром визначити: а) хімічний склад речовини; б) агрегатний стан речовини; в) температуру речовини

Підсумок 1. Розглянули сутність постулатів Бора 2. З'ясували квантовий характер випромінювання та поглинання світла атомом та закономірності в лінійчастих спектрах 3. 3'ясували практичне застосування спектрального аналізу 4. Навчилися застосовувати набуті знання під час розв'язування задач

Домашнє завдання Вивчіть § 77 -79, виконайте вправу 18 на с. 207, виконайте творчий експеримент “ Кухонна сіль може випромінювати світло ”
постулати Бора.ppt