Квантовая оптика.ppt
- Количество слайдов: 35
 Квантовая оптика
Квантовая оптика
 • Квантовой оптикой называют раздел оптики, занимающийся изучением явлений, в которых проявляются квантовые свойства света. • К таким явлениям относятся: тепловое излучение, фотоэффект, фотохимические процессы, вынужденное излучение (физика лазеров) и др.
• Квантовой оптикой называют раздел оптики, занимающийся изучением явлений, в которых проявляются квантовые свойства света. • К таким явлениям относятся: тепловое излучение, фотоэффект, фотохимические процессы, вынужденное излучение (физика лазеров) и др.
 Квантовые свойства света • Чтобы объяснить распределение энергии в спектре теплового излучения Планк допустил, что электромагнитные волны испускаются порциями (квантами). • Эйнштейн в 1905 г. пришел к выводу, что излучение не только испускается, но и распространяется и поглощается в виде квантов. Этот вывод позволил объяснить все экспериментальные факты (фотоэффект, эффект Комптона, и др. ), которые не могла объяснить классическая электродинамика, исходившая из волновых представлений о свойствах излучения.
Квантовые свойства света • Чтобы объяснить распределение энергии в спектре теплового излучения Планк допустил, что электромагнитные волны испускаются порциями (квантами). • Эйнштейн в 1905 г. пришел к выводу, что излучение не только испускается, но и распространяется и поглощается в виде квантов. Этот вывод позволил объяснить все экспериментальные факты (фотоэффект, эффект Комптона, и др. ), которые не могла объяснить классическая электродинамика, исходившая из волновых представлений о свойствах излучения.
 Макс Карл Эрнст Людвиг Планк (1858 – 1947) Альберт Эйнштейн (1879 -1955)
Макс Карл Эрнст Людвиг Планк (1858 – 1947) Альберт Эйнштейн (1879 -1955)
 • Таким образом, распространение света следует рассматривать не как непрерывный волновой процесс, а как поток локализованных в пространстве дискретных частиц, движущихся со скоростью с распространения света в вакууме. Впоследствии (в 1926 г. ) эти частицы получили название фотонов. Фотоны обладают всеми свойствами частицы (корпускулы).
• Таким образом, распространение света следует рассматривать не как непрерывный волновой процесс, а как поток локализованных в пространстве дискретных частиц, движущихся со скоростью с распространения света в вакууме. Впоследствии (в 1926 г. ) эти частицы получили название фотонов. Фотоны обладают всеми свойствами частицы (корпускулы).
 • Энергия фотона: E=h где h - постоянная Планка (6, 6 10 -34 Дж с) • Масса фотона: 2=h m=E/c 2 /c • Импульс фотона: p=E/c=h/λ
• Энергия фотона: E=h где h - постоянная Планка (6, 6 10 -34 Дж с) • Масса фотона: 2=h m=E/c 2 /c • Импульс фотона: p=E/c=h/λ
 Электронвольт (сокращённо э. В или e. V) — внесистемная единица измерения энергии, широко используемая в атомной и квантовой физике. Один электронвольт равен энергии, которая необходима для переноса электрона в электростатическом поле между точками с разницей потенциалов в 1 В. Так как работа при переносе заряда q равна q. U (где U — разность потенциалов), а заряд электрона составляет − 1, 6× 10− 19 Кл то 1 э. В = 1, 6× 10− 19 Дж.
Электронвольт (сокращённо э. В или e. V) — внесистемная единица измерения энергии, широко используемая в атомной и квантовой физике. Один электронвольт равен энергии, которая необходима для переноса электрона в электростатическом поле между точками с разницей потенциалов в 1 В. Так как работа при переносе заряда q равна q. U (где U — разность потенциалов), а заряд электрона составляет − 1, 6× 10− 19 Кл то 1 э. В = 1, 6× 10− 19 Дж.
 Спектроскопия
Спектроскопия
 СПЕКТРОСКОПИЯ (от лат. spectrum-образ, представление и греч. skopeo-смотрю) – раздел физики, изучающий спектры электромагнитного излучения. Спектры возникают при переходах между уровнями энергии в атомах, молекулах и образованных из них макроскопических системах.
СПЕКТРОСКОПИЯ (от лат. spectrum-образ, представление и греч. skopeo-смотрю) – раздел физики, изучающий спектры электромагнитного излучения. Спектры возникают при переходах между уровнями энергии в атомах, молекулах и образованных из них макроскопических системах.
 Различают спектры испускания (эмиссионные), поглощения (абсорбционные), отражения, рассеяния и люминесценции, которые изучают соответствующие виды спектроскопии.
Различают спектры испускания (эмиссионные), поглощения (абсорбционные), отражения, рассеяния и люминесценции, которые изучают соответствующие виды спектроскопии.
 В зависимости от природы объекта исследования выделяют атомную и молекулярную спектроскопию, а также спектроскопию вещества в конденсированном состоянии, включая спектроскопию кристаллов.
В зависимости от природы объекта исследования выделяют атомную и молекулярную спектроскопию, а также спектроскопию вещества в конденсированном состоянии, включая спектроскопию кристаллов.
 В соответствии с видами движения в молекуле молекулярную спектроскопию делят на: – электронную, – колебательную и – вращательную.
В соответствии с видами движения в молекуле молекулярную спектроскопию делят на: – электронную, – колебательную и – вращательную.
 Виды спектров • По характеру распределения значений физической величины спектры могут быть дискретными (линейчатыми), непрерывными (сплошными), а также представлять комбинацию (наложение) дискретных и непрерывных спектров.
Виды спектров • По характеру распределения значений физической величины спектры могут быть дискретными (линейчатыми), непрерывными (сплошными), а также представлять комбинацию (наложение) дискретных и непрерывных спектров.
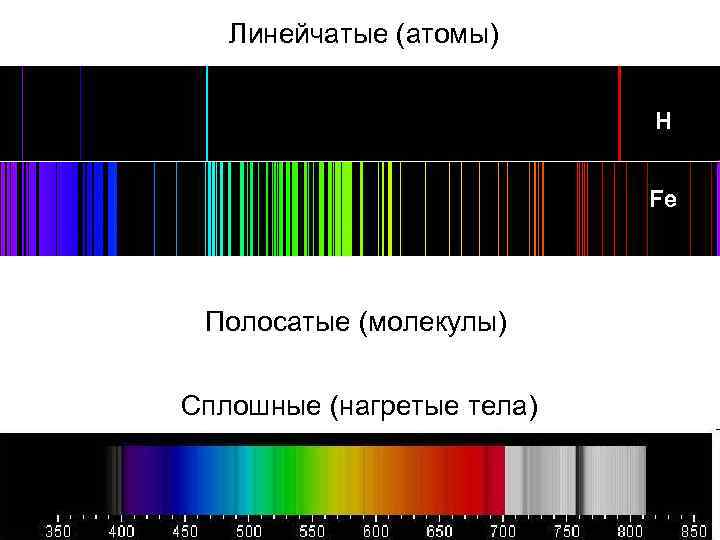 Линейчатые (атомы) H Fe Полосатые (молекулы) Сплошные (нагретые тела)
Линейчатые (атомы) H Fe Полосатые (молекулы) Сплошные (нагретые тела)
 Энергетические уровни • Когда электрон находится в связанном состоянии в атоме, он обладает потенциальной энергией, которая обратно пропорциональна его расстоянию от ядра. Эта энергия обычно измеряется в электронвольтах (э. В) и равна энергии, которую надо передать электрону, чтобы сделать его свободным (оторвать от атома). Согласно квантовомеханической модели атома связанный электрон может занимать только дискретный набор разрешённых энергетических уровней — состояний с определённой энергией. Наинизшее из разрешённых энергетических состояний называется основным, а все остальные — возбуждёнными.
Энергетические уровни • Когда электрон находится в связанном состоянии в атоме, он обладает потенциальной энергией, которая обратно пропорциональна его расстоянию от ядра. Эта энергия обычно измеряется в электронвольтах (э. В) и равна энергии, которую надо передать электрону, чтобы сделать его свободным (оторвать от атома). Согласно квантовомеханической модели атома связанный электрон может занимать только дискретный набор разрешённых энергетических уровней — состояний с определённой энергией. Наинизшее из разрешённых энергетических состояний называется основным, а все остальные — возбуждёнными.
 Визуализация орбиталей атома водорода
Визуализация орбиталей атома водорода
 • Для перехода электрона с одного энергетического уровня на другой нужно передать ему или отнять у него энергию. Это происходит путём соответственно поглощения или испускания фотона, причём энергия этого фотона равна абсолютной величине разности энергий начального и конечного уровней электрона. Энергия испущенного фотона пропорциональна его частоте, поэтому переходы между разными энергетическими уровнями проявляются в различных областях электромагнитного спектра. Каждый элемент имеет уникальный спектр испускания, который зависит от заряда ядра, заполнения электронных подоболочек, взаимодействия электронов, а также других факторов.
• Для перехода электрона с одного энергетического уровня на другой нужно передать ему или отнять у него энергию. Это происходит путём соответственно поглощения или испускания фотона, причём энергия этого фотона равна абсолютной величине разности энергий начального и конечного уровней электрона. Энергия испущенного фотона пропорциональна его частоте, поэтому переходы между разными энергетическими уровнями проявляются в различных областях электромагнитного спектра. Каждый элемент имеет уникальный спектр испускания, который зависит от заряда ядра, заполнения электронных подоболочек, взаимодействия электронов, а также других факторов.
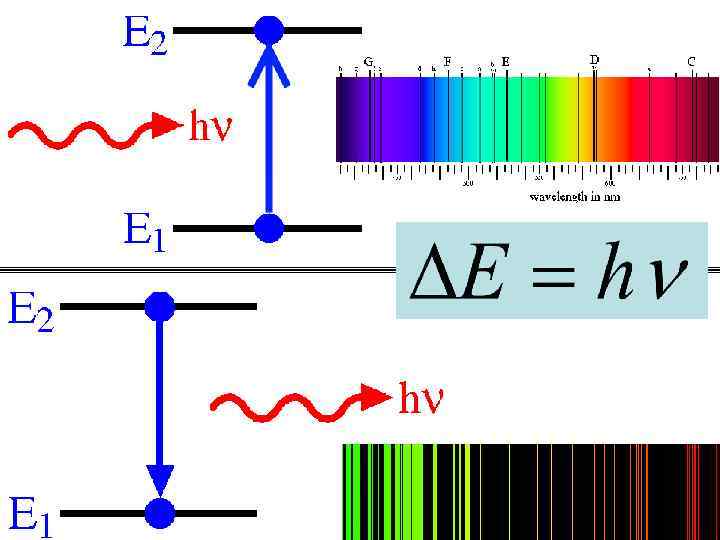
 • Когда излучение с непрерывным спектром проходит через вещество, некоторые фотоны поглощаются атомами или ионами, вызывая электронные переходы между энергетическим состояниями, разность энергий которых равна энергии поглощённого фотона. Затем эти возбуждённые электроны спонтанно переходят на уровень, лежащий ниже по энергии, снова испуская фотоны. Таким образом, вещество ведёт себя как фильтр, превращая исходный непрерывный спектр в спектр поглощения, в котором имеются серии тёмных полос. При наблюдении с тех углов, куда не направлено исходное излучение, можно заметить излучение с эмиссионным спектром, испускаемое атомами. Спектроскопические измерения энергии, амплитуды и ширины спектральных линий излучения позволяют определить вид излучающего вещества и физические условия в нём.
• Когда излучение с непрерывным спектром проходит через вещество, некоторые фотоны поглощаются атомами или ионами, вызывая электронные переходы между энергетическим состояниями, разность энергий которых равна энергии поглощённого фотона. Затем эти возбуждённые электроны спонтанно переходят на уровень, лежащий ниже по энергии, снова испуская фотоны. Таким образом, вещество ведёт себя как фильтр, превращая исходный непрерывный спектр в спектр поглощения, в котором имеются серии тёмных полос. При наблюдении с тех углов, куда не направлено исходное излучение, можно заметить излучение с эмиссионным спектром, испускаемое атомами. Спектроскопические измерения энергии, амплитуды и ширины спектральных линий излучения позволяют определить вид излучающего вещества и физические условия в нём.
 Нильс Хенрик Давид Бор (1885 -1962)
Нильс Хенрик Давид Бор (1885 -1962)
 Теория Бора водородоподобных атомов. Основана на двух постулатах Бора: • Существуют стационарные состояния атома, в которых он не излучает и не поглощает энергию. • Излучение и поглощение энергии атомом происходит при скачкообразном переходе из одного стационарного состояния в другое, при этом имеют место два соотношения:
Теория Бора водородоподобных атомов. Основана на двух постулатах Бора: • Существуют стационарные состояния атома, в которых он не излучает и не поглощает энергию. • Излучение и поглощение энергии атомом происходит при скачкообразном переходе из одного стационарного состояния в другое, при этом имеют место два соотношения:
 1. E = En 2 -En 1, где E - излучённая (поглощённая) энергия, n 1, n 2 номера квантовых состояний. 2. Правило квантования момента импульса: m r=nh/2 , n=1, 2, 3…
1. E = En 2 -En 1, где E - излучённая (поглощённая) энергия, n 1, n 2 номера квантовых состояний. 2. Правило квантования момента импульса: m r=nh/2 , n=1, 2, 3…
 • Далее исходя из соображений классической физики о круговом движении электрона вокруг неподвижного ядра по стационарной орбите под действием кулоновской силы притяжения, Бором были получены выражения для радиусов стационарных орбит и энергии электрона на этих орбитах: боровский радиус постоянная Ридберга
• Далее исходя из соображений классической физики о круговом движении электрона вокруг неподвижного ядра по стационарной орбите под действием кулоновской силы притяжения, Бором были получены выражения для радиусов стационарных орбит и энергии электрона на этих орбитах: боровский радиус постоянная Ридберга
 Достоинства теории Бора • Объяснила дискретность энергетических состояний водородоподобных атомов. • Теория Бора подошла к объяснению внутриатомных процессов с принципиально новых позиций, стала первой полуквантовой теорией атома. • Эвристическое значение теории Бора состоит в смелом предположении о существовании стационарных состояний и скачкообразных переходов между ними. Эти положения позднее были распространены и на другие микросистемы.
Достоинства теории Бора • Объяснила дискретность энергетических состояний водородоподобных атомов. • Теория Бора подошла к объяснению внутриатомных процессов с принципиально новых позиций, стала первой полуквантовой теорией атома. • Эвристическое значение теории Бора состоит в смелом предположении о существовании стационарных состояний и скачкообразных переходов между ними. Эти положения позднее были распространены и на другие микросистемы.
 Недостатки теории Бора • Не смогла объяснить интенсивность спектральных линий. • Справедлива только для водородоподобных атомов и не работает для атомов, следующих за ним в таблице Менделеева. • Теория Бора логически противоречива: не является ни классической, ни квантовой. В системе двух уравнений, лежащих в её основе, одно — уравнение движения электрона — классическое, другое — уравнение квантования орбит — квантовое.
Недостатки теории Бора • Не смогла объяснить интенсивность спектральных линий. • Справедлива только для водородоподобных атомов и не работает для атомов, следующих за ним в таблице Менделеева. • Теория Бора логически противоречива: не является ни классической, ни квантовой. В системе двух уравнений, лежащих в её основе, одно — уравнение движения электрона — классическое, другое — уравнение квантования орбит — квантовое.
 Спектральные серии водорода • Спектральные серии водорода — набор спектральных серий, составляющих спектр атома водорода. Поскольку водород наиболее простой атом, его спектральные серии наиболее изучены. Они хорошо подчиняются формуле Ридберга:
Спектральные серии водорода • Спектральные серии водорода — набор спектральных серий, составляющих спектр атома водорода. Поскольку водород наиболее простой атом, его спектральные серии наиболее изучены. Они хорошо подчиняются формуле Ридберга:
 Серия Название серии n → 1 n=3 (-1, 51 э. В) n → 2 Бальмера (H) n → 3 Пашена (P) n → 4 Брекета (B) n → 5 n=4 (-0, 85 э. В) Лаймана (Ly) Пфунда (Pf) n=2 (-3, 40 э. В) 656 нм 482 нм n=1 (-13, 6 э. В) 434 нм 410 нм
Серия Название серии n → 1 n=3 (-1, 51 э. В) n → 2 Бальмера (H) n → 3 Пашена (P) n → 4 Брекета (B) n → 5 n=4 (-0, 85 э. В) Лаймана (Ly) Пфунда (Pf) n=2 (-3, 40 э. В) 656 нм 482 нм n=1 (-13, 6 э. В) 434 нм 410 нм
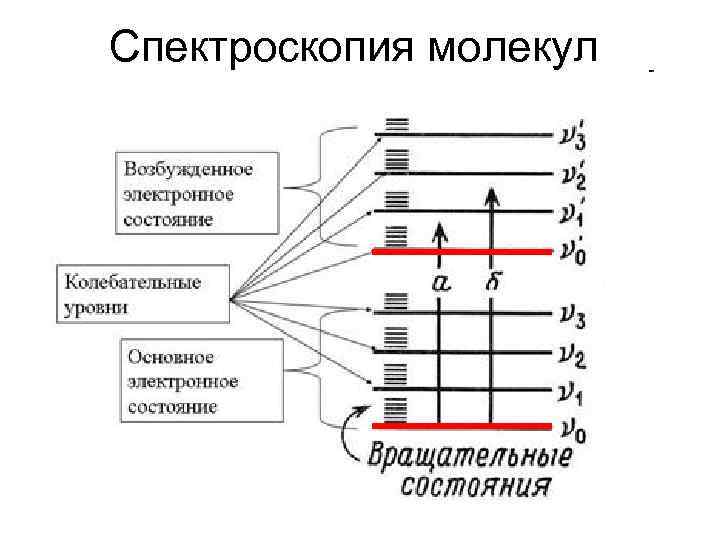 Спектроскопия молекул
Спектроскопия молекул
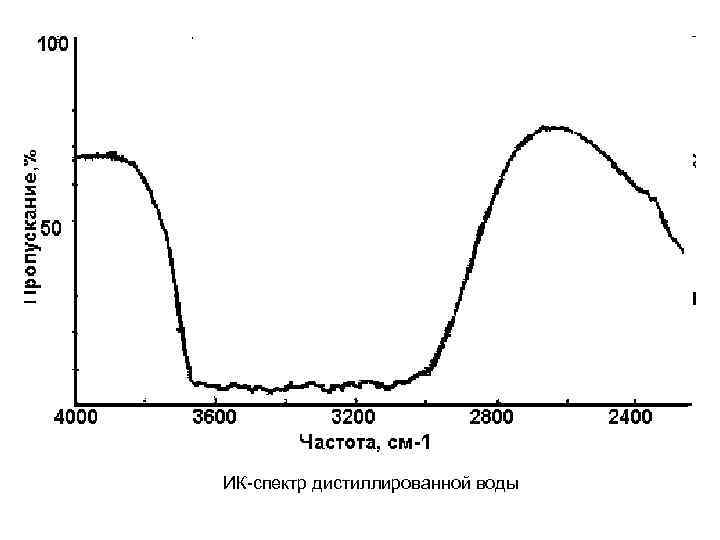 ИК-спектр дистиллированной воды
ИК-спектр дистиллированной воды
 • Спектроскоп (от спектр и греч. skopeo — смотрю) — оптический прибор для визуального наблюдения спектра излучения. Используется для быстрого качественного спектрального анализа веществ Разложение излучения в спектр осуществляется, например, оптической призмой.
• Спектроскоп (от спектр и греч. skopeo — смотрю) — оптический прибор для визуального наблюдения спектра излучения. Используется для быстрого качественного спектрального анализа веществ Разложение излучения в спектр осуществляется, например, оптической призмой.
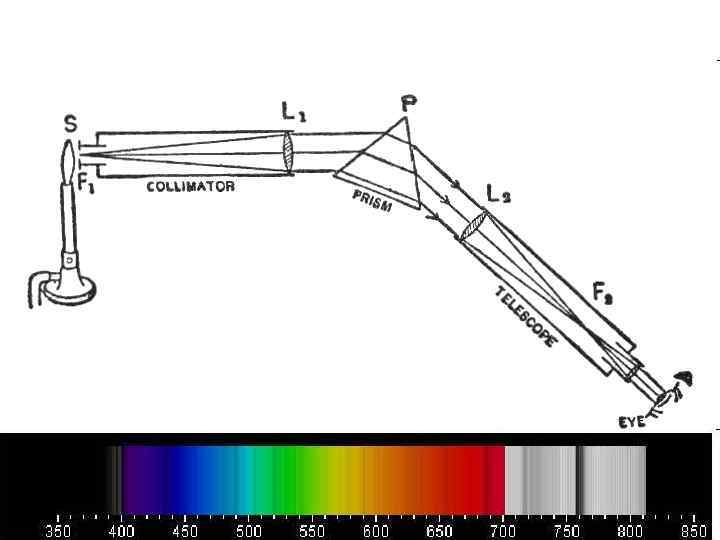
 • Спектрометр (лат. spectrum от лат. spectare — смотреть и метр от др. -греч. μέτρον — мера, измеритель) — оптический прибор, используемый в спектроскопических исследованиях для накопления спектра, его количественной обработки и последующего анализа с помощью различных аналитических методов. Обычно измеряемыми величинами являются интенсивность и энергия (длина волны, частота) излучения.
• Спектрометр (лат. spectrum от лат. spectare — смотреть и метр от др. -греч. μέτρον — мера, измеритель) — оптический прибор, используемый в спектроскопических исследованиях для накопления спектра, его количественной обработки и последующего анализа с помощью различных аналитических методов. Обычно измеряемыми величинами являются интенсивность и энергия (длина волны, частота) излучения.

 Цветовое зрение • В глазу человека содержатся два типа светочувствительных клеток (рецепторов): высокочувствительные палочки, отвечающие за сумеречное (ночное) зрение, и менее чувствительные колбочки, отвечающие за цветное зрение. • В сетчатке глаза человека есть три вида колбочек, максимум чувствительности которых приходится на красный, зелёный и синий участок спектра, то есть соответствует трем «основным» цветам. Они обеспечивают распознавание тысяч цветов и оттенков. Кривые спектральной чувствительности трёх видов колбочек частично перекрываются, что вызывает эффект метамерии. Очень сильный свет возбуждает все 3 типа рецепторов, и потому воспринимается, как излучение слепяще-белого цвета.
Цветовое зрение • В глазу человека содержатся два типа светочувствительных клеток (рецепторов): высокочувствительные палочки, отвечающие за сумеречное (ночное) зрение, и менее чувствительные колбочки, отвечающие за цветное зрение. • В сетчатке глаза человека есть три вида колбочек, максимум чувствительности которых приходится на красный, зелёный и синий участок спектра, то есть соответствует трем «основным» цветам. Они обеспечивают распознавание тысяч цветов и оттенков. Кривые спектральной чувствительности трёх видов колбочек частично перекрываются, что вызывает эффект метамерии. Очень сильный свет возбуждает все 3 типа рецепторов, и потому воспринимается, как излучение слепяще-белого цвета.
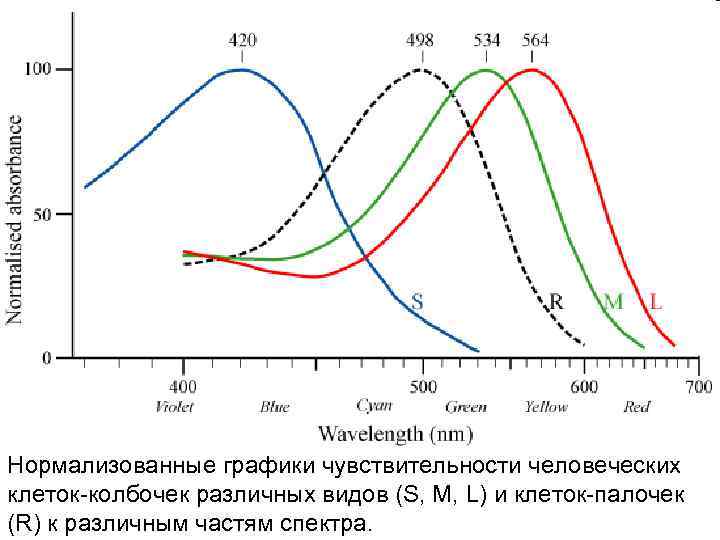 Нормализованные графики чувствительности человеческих клеток-колбочек различных видов (S, M, L) и клеток-палочек (R) к различным частям спектра.
Нормализованные графики чувствительности человеческих клеток-колбочек различных видов (S, M, L) и клеток-палочек (R) к различным частям спектра.


