Квантовая механика (2 часть) - 21.02.12.ppt
- Количество слайдов: 46
 Квантовая механика Раздел 7 Физика атомов и молекул Курс лекций по общей физики Доцент Петренко Л. Г. Кафедра общей и экспериментальной физики НТУ «ХПИ» Харьков - 2012 год
Квантовая механика Раздел 7 Физика атомов и молекул Курс лекций по общей физики Доцент Петренко Л. Г. Кафедра общей и экспериментальной физики НТУ «ХПИ» Харьков - 2012 год
 Раздел 7. ФИЗИКА АТОМОВ И МОЛЕКУЛ 7. 1. АТОМ 7. 1. 1. Объяснение устойчивости ядра с помощью соотношений неопределённостей Гейзенберга. Водородоподобные атомы и мезоатомы. Энергетические уровни. Правила квантования энергии и азимутального момента водородоподобных атомов. Главное, азимутальное и магнитное квантовые числа. Пространственное распределение электрона в атоме водорода. Сферически симметричные состояния электрона в атоме водорода. Классическая физика не могла объяснить стабильность атома. В соответствии с классическими представлениями электроны под воздействием кулоновского поля ядра должны были бы упасть на ядро. В соответствии с квантовыми представлениями чем меньше область локализации электрона, тем большей становится неопределённость его импульса и тем большую энергию нужно затратить, чтобы удержать электрон в этой области. Электрону энергетически не выгодно упасть на ядро.
Раздел 7. ФИЗИКА АТОМОВ И МОЛЕКУЛ 7. 1. АТОМ 7. 1. 1. Объяснение устойчивости ядра с помощью соотношений неопределённостей Гейзенберга. Водородоподобные атомы и мезоатомы. Энергетические уровни. Правила квантования энергии и азимутального момента водородоподобных атомов. Главное, азимутальное и магнитное квантовые числа. Пространственное распределение электрона в атоме водорода. Сферически симметричные состояния электрона в атоме водорода. Классическая физика не могла объяснить стабильность атома. В соответствии с классическими представлениями электроны под воздействием кулоновского поля ядра должны были бы упасть на ядро. В соответствии с квантовыми представлениями чем меньше область локализации электрона, тем большей становится неопределённость его импульса и тем большую энергию нужно затратить, чтобы удержать электрон в этой области. Электрону энергетически не выгодно упасть на ядро.
 Вдали от ядра электрон можно считать свободной частицей и описывать его плоской волной де Бройля, имеющей непрерывный энергетический спектр. Приблизившись к ядру, электрон попадает в его силовое поле (в потенциальную яму), его движение становится ограниченным, а энергетический спектр - дискретным. Это следует из решений уравнений Шрёдингера для частицы в одномерной бесконечно глубокой потенциальной яме и для квантового гармонического осциллятора (простые квантовые модели). Более близка к реальности модель водородоподобного атома -электрон находится в центрально симметричном поле ядра элемента с зарядовым числом Z (порядковым номером). Его потенциальная энергия равна:
Вдали от ядра электрон можно считать свободной частицей и описывать его плоской волной де Бройля, имеющей непрерывный энергетический спектр. Приблизившись к ядру, электрон попадает в его силовое поле (в потенциальную яму), его движение становится ограниченным, а энергетический спектр - дискретным. Это следует из решений уравнений Шрёдингера для частицы в одномерной бесконечно глубокой потенциальной яме и для квантового гармонического осциллятора (простые квантовые модели). Более близка к реальности модель водородоподобного атома -электрон находится в центрально симметричном поле ядра элемента с зарядовым числом Z (порядковым номером). Его потенциальная энергия равна:
 Графически эта функция представляет собой гиперболу. Таким образом, решается задача о нахождении электрона в потенциальной яме с гиперболическими краями. Состояние электрона в водородоподобном атоме описывается волновой функцией, удовлетворяющей стационарному уравнению Шрёдингера: Выполнение стандартных условий (конечность, однозначность, непрерывность) для волновой функции возможно только в двух случаях: 1) при любых положительных значениях энергии (W 0) – электрон удаляется от ядра на бесконечность; 2) при дискретных отрицательных значениях энергии (W 0): В этом случае электрон связан с ядром.
Графически эта функция представляет собой гиперболу. Таким образом, решается задача о нахождении электрона в потенциальной яме с гиперболическими краями. Состояние электрона в водородоподобном атоме описывается волновой функцией, удовлетворяющей стационарному уравнению Шрёдингера: Выполнение стандартных условий (конечность, однозначность, непрерывность) для волновой функции возможно только в двух случаях: 1) при любых положительных значениях энергии (W 0) – электрон удаляется от ядра на бесконечность; 2) при дискретных отрицательных значениях энергии (W 0): В этом случае электрон связан с ядром.
 Эта формула полностью соответствует формуле, полученной Н. Бором на основе его постулатов. Энергетический уровень с n=1 называется основным. На рисунке это самый нижний уровень. Для атома водорода: Все остальные энергетические уровни называются возбуждёнными: По мере роста n энергетические уровни сближаются. Таким образом, дискретность уровней, присущая квантовой механике, уменьшается, а характер поведения микрочастицы приближается к классическому. В этом проявляется принцип соответствия Бора. При n энергия Wn 0.
Эта формула полностью соответствует формуле, полученной Н. Бором на основе его постулатов. Энергетический уровень с n=1 называется основным. На рисунке это самый нижний уровень. Для атома водорода: Все остальные энергетические уровни называются возбуждёнными: По мере роста n энергетические уровни сближаются. Таким образом, дискретность уровней, присущая квантовой механике, уменьшается, а характер поведения микрочастицы приближается к классическому. В этом проявляется принцип соответствия Бора. При n энергия Wn 0.
 Если электрону, находящемуся в основном состоянии, передать энергию, равную W 1, он сможет оторваться от ядра, и атом ионизируется. Энергия ионизации атома водорода равна Wион= -W 1 =13, 55 э. В. Энергия ионизации других водородоподобных атомов равна: Wион = - W 1. Z 2 = 13, 55. Z 2 э. В. Из решения уравнения Шрёдингера следует, что момент импульса электрона, характеризующий его вращательное движение вокруг ядра, не может быть произвольным его модуль квантуется, т. е. может принимать только дискретный ряд значений Его ориентация в пространстве может быть только такой, при которой его проекция на некоторую ось Z имеет квантованные значения:
Если электрону, находящемуся в основном состоянии, передать энергию, равную W 1, он сможет оторваться от ядра, и атом ионизируется. Энергия ионизации атома водорода равна Wион= -W 1 =13, 55 э. В. Энергия ионизации других водородоподобных атомов равна: Wион = - W 1. Z 2 = 13, 55. Z 2 э. В. Из решения уравнения Шрёдингера следует, что момент импульса электрона, характеризующий его вращательное движение вокруг ядра, не может быть произвольным его модуль квантуется, т. е. может принимать только дискретный ряд значений Его ориентация в пространстве может быть только такой, при которой его проекция на некоторую ось Z имеет квантованные значения:
 Магнитный момент электрона и его проекция на ось Z тоже квантуются: - магнетон Бора. Таким образом, собственные функции уравнения Шрёдингера содержат три целочисленных параметра - n, l, m: = nlm. Параметр n называется главным квантовым числом и определяет энергетические уровни электрона в атоме. Параметр l называется орбитальным (азимутальным) квантовым числом и определяет модуль момента импульса электрона. Параметр m называется магнитным квантовым числом и определяет проекцию момента импульса на некоторое направление Z.
Магнитный момент электрона и его проекция на ось Z тоже квантуются: - магнетон Бора. Таким образом, собственные функции уравнения Шрёдингера содержат три целочисленных параметра - n, l, m: = nlm. Параметр n называется главным квантовым числом и определяет энергетические уровни электрона в атоме. Параметр l называется орбитальным (азимутальным) квантовым числом и определяет модуль момента импульса электрона. Параметр m называется магнитным квантовым числом и определяет проекцию момента импульса на некоторое направление Z.
 Энергия электрона зависит только от главного квантового числа n , но каждому собственному значению энергии Wn соответствует несколько собственных функций nlm , отличающиеся значениями l и m. Состояния с одинаковой энергией называются вырожденными, а количество таких состояний - кратностью вырождения: В атомной физике употребляется заимствованные из спектроскопии условные обозначения состояний электрона с различными значениями l:
Энергия электрона зависит только от главного квантового числа n , но каждому собственному значению энергии Wn соответствует несколько собственных функций nlm , отличающиеся значениями l и m. Состояния с одинаковой энергией называются вырожденными, а количество таких состояний - кратностью вырождения: В атомной физике употребляется заимствованные из спектроскопии условные обозначения состояний электрона с различными значениями l:
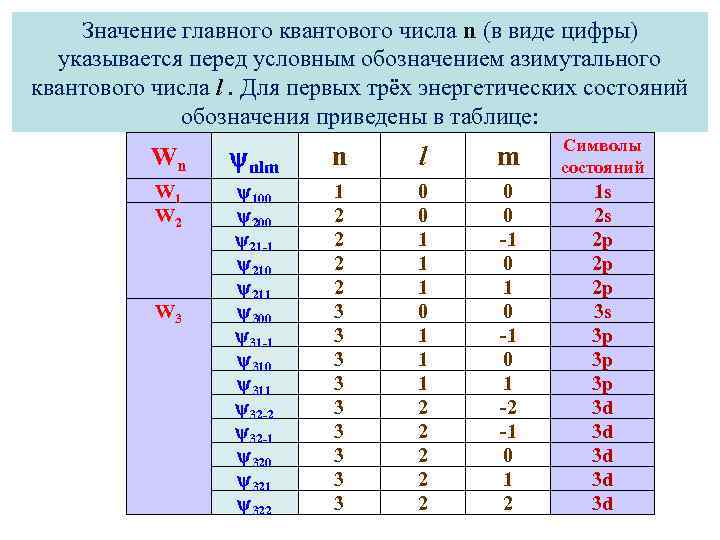 Значение главного квантового числа n (в виде цифры) указывается перед условным обозначением азимутального квантового числа l. Для первых трёх энергетических состояний обозначения приведены в таблице: Wn nlm n l m Символы состояний W 1 W 2 100 21 -1 210 211 300 31 -1 310 311 32 -2 32 -1 320 321 322 1 2 2 3 3 3 3 3 0 0 1 1 1 2 2 2 0 0 -1 0 1 -2 -1 0 1 2 1 s 2 s 2 p 2 p 2 p 3 s 3 p 3 p 3 p 3 d 3 d 3 d W 3
Значение главного квантового числа n (в виде цифры) указывается перед условным обозначением азимутального квантового числа l. Для первых трёх энергетических состояний обозначения приведены в таблице: Wn nlm n l m Символы состояний W 1 W 2 100 21 -1 210 211 300 31 -1 310 311 32 -2 32 -1 320 321 322 1 2 2 3 3 3 3 3 0 0 1 1 1 2 2 2 0 0 -1 0 1 -2 -1 0 1 2 1 s 2 s 2 p 2 p 2 p 3 s 3 p 3 p 3 p 3 d 3 d 3 d W 3
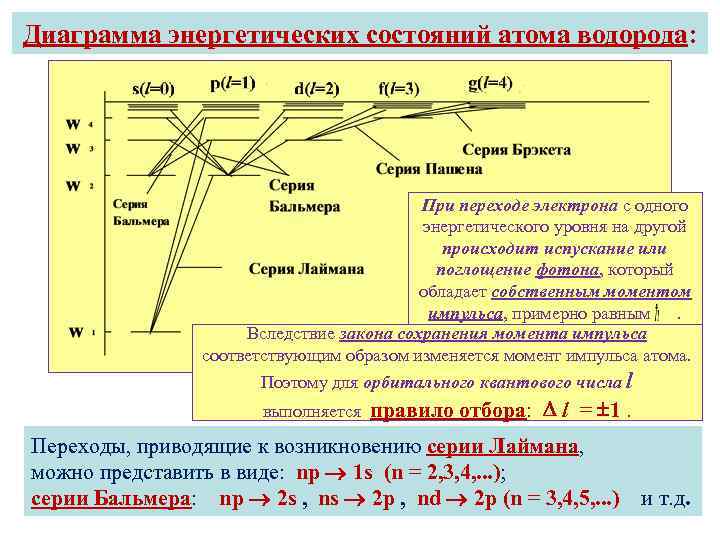 Диаграмма энергетических состояний атома водорода: При переходе электрона с одного энергетического уровня на другой происходит испускание или поглощение фотона, который обладает собственным моментом импульса, примерно равным. Вследствие закона сохранения момента импульса соответствующим образом изменяется момент импульса атома. Поэтому для орбитального квантового числа l выполняется правило отбора: l = 1. Переходы, приводящие к возникновению серии Лаймана, можно представить в виде: np 1 s (n = 2, 3, 4, . . . ); серии Бальмера: nр 2 s , ns 2 p , nd 2 p (n = 3, 4, 5, . . . ) и т. д.
Диаграмма энергетических состояний атома водорода: При переходе электрона с одного энергетического уровня на другой происходит испускание или поглощение фотона, который обладает собственным моментом импульса, примерно равным. Вследствие закона сохранения момента импульса соответствующим образом изменяется момент импульса атома. Поэтому для орбитального квантового числа l выполняется правило отбора: l = 1. Переходы, приводящие к возникновению серии Лаймана, можно представить в виде: np 1 s (n = 2, 3, 4, . . . ); серии Бальмера: nр 2 s , ns 2 p , nd 2 p (n = 3, 4, 5, . . . ) и т. д.
 Таким образом, в квантовой механике получено подтверждение выводов теории Бора для водородоподобного атома. Более того, в квантовой механике рассчитываются вероятности различных переходов электронов между уровнями и объясняется разная интенсивность линий в спектре излучения водорода. Полученная в результате решения уравнения Шрёдингера волновая функция может быть представлена в виде произведения радиальной функции Rnl(r) и угловой Ylm( , ): nlm(r, , ) = Rnl(r). Ylm( , ). Радиальная функция Rnl(r) зависит от потенциальной энергии. Угловая функция Ylm( , ) определяется моментом импульса электрона (квантовое число l ) и его проекции на ось Z (квантовое число m).
Таким образом, в квантовой механике получено подтверждение выводов теории Бора для водородоподобного атома. Более того, в квантовой механике рассчитываются вероятности различных переходов электронов между уровнями и объясняется разная интенсивность линий в спектре излучения водорода. Полученная в результате решения уравнения Шрёдингера волновая функция может быть представлена в виде произведения радиальной функции Rnl(r) и угловой Ylm( , ): nlm(r, , ) = Rnl(r). Ylm( , ). Радиальная функция Rnl(r) зависит от потенциальной энергии. Угловая функция Ylm( , ) определяется моментом импульса электрона (квантовое число l ) и его проекции на ось Z (квантовое число m).
 Для n-го состояния электрона в атоме плотность вероятности нахождения электрона в атоме достигает максимума при r, равном соответствующему боровскому радиусу rn. Однако и при r, не равном радиусам боровских орбит, плотность вероятности не равна нулю. Электрон при своём движении как бы «размазан» по всему объёму атома, образуя электронное облако, плотность которого определяет вероятность нахождения электрона в различных точках объёма атома. Квантовое число n характеризует размер, квантовое число l - форму электронного облака, а квантовое число m - ориентацию электронного облака в пространстве.
Для n-го состояния электрона в атоме плотность вероятности нахождения электрона в атоме достигает максимума при r, равном соответствующему боровскому радиусу rn. Однако и при r, не равном радиусам боровских орбит, плотность вероятности не равна нулю. Электрон при своём движении как бы «размазан» по всему объёму атома, образуя электронное облако, плотность которого определяет вероятность нахождения электрона в различных точках объёма атома. Квантовое число n характеризует размер, квантовое число l - форму электронного облака, а квантовое число m - ориентацию электронного облака в пространстве.
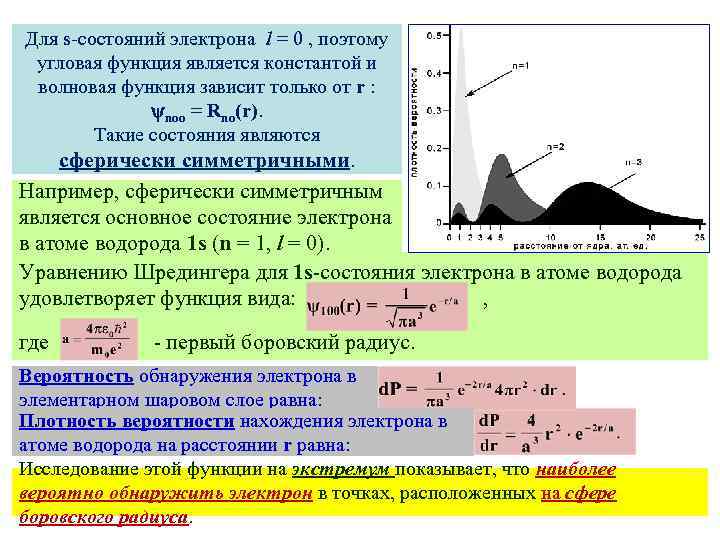 Для s-состояний электрона l = 0 , поэтому угловая функция является константой и волновая функция зависит только от r : noo = Rno(r). Такие состояния являются сферически симметричными. Например, сферически симметричным является основное состояние электрона в атоме водорода 1 s (n = 1, l = 0). Уравнению Шредингера для 1 s-состояния электрона в атоме водорода удовлетворяет функция вида: , где - первый боровский радиус. Вероятность обнаружения электрона в элементарном шаровом слое равна: Плотность вероятности нахождения электрона в атоме водорода на расстоянии r равна: Исследование этой функции на экстремум показывает, что наиболее вероятно обнаружить электрон в точках, расположенных на сфере боровского радиуса.
Для s-состояний электрона l = 0 , поэтому угловая функция является константой и волновая функция зависит только от r : noo = Rno(r). Такие состояния являются сферически симметричными. Например, сферически симметричным является основное состояние электрона в атоме водорода 1 s (n = 1, l = 0). Уравнению Шредингера для 1 s-состояния электрона в атоме водорода удовлетворяет функция вида: , где - первый боровский радиус. Вероятность обнаружения электрона в элементарном шаровом слое равна: Плотность вероятности нахождения электрона в атоме водорода на расстоянии r равна: Исследование этой функции на экстремум показывает, что наиболее вероятно обнаружить электрон в точках, расположенных на сфере боровского радиуса.
 7. 1. 2. Сложные атомы. Механический и магнитный моменты атомов. Эффект Зеемана. Спиновое квантовое число. Опыт Штерна и Герлаха. Типы связи электронов в атомах. В общем случае атомы представляют собой сложную многоэлектронную систему, в которой каждый электрон движется в поле, создаваемом как ядром, так и всеми другими электронами. Это поле не является кулоновским. Уравнение Шредингера можно представить в виде: i - номер электрона; N – количество электронов в атоме; W - полная энергия системы; me - масса электрона; - потенциальная энергия взаимодействия i-го электрона с ядром, находящимся от него на расстоянии ri , Ui - потенциальная энергия взаимодействия i-го электрона с остальными электронами. Такое сложное уравнение можно решить только приближёнными методами. Наиболее простым является решение для атома щелочного металла, у которого имеется только один валентный электрон, находящийся в усреднённом электрическом поле электронно-ядерного остова. Энергия других электронов в различных стационарных состояниях не меняется.
7. 1. 2. Сложные атомы. Механический и магнитный моменты атомов. Эффект Зеемана. Спиновое квантовое число. Опыт Штерна и Герлаха. Типы связи электронов в атомах. В общем случае атомы представляют собой сложную многоэлектронную систему, в которой каждый электрон движется в поле, создаваемом как ядром, так и всеми другими электронами. Это поле не является кулоновским. Уравнение Шредингера можно представить в виде: i - номер электрона; N – количество электронов в атоме; W - полная энергия системы; me - масса электрона; - потенциальная энергия взаимодействия i-го электрона с ядром, находящимся от него на расстоянии ri , Ui - потенциальная энергия взаимодействия i-го электрона с остальными электронами. Такое сложное уравнение можно решить только приближёнными методами. Наиболее простым является решение для атома щелочного металла, у которого имеется только один валентный электрон, находящийся в усреднённом электрическом поле электронно-ядерного остова. Энергия других электронов в различных стационарных состояниях не меняется.
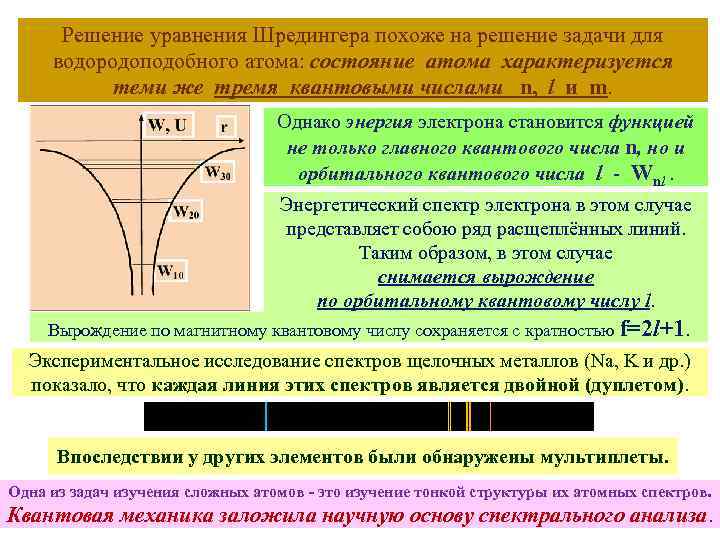 Решение уравнения Шредингера похоже на решение задачи для водородоподобного атома: состояние атома характеризуется теми же тремя квантовыми числами n, l и m. Однако энергия электрона становится функцией не только главного квантового числа n, но и орбитального квантового числа l - Wnl. Энергетический спектр электрона в этом случае представляет собою ряд расщеплённых линий. Таким образом, в этом случае снимается вырождение по орбитальному квантовому числу l. Вырождение по магнитному квантовому числу сохраняется с кратностью f=2 l+1. Экспериментальное исследование спектров щелочных металлов (Na, K и др. ) показало, что каждая линия этих спектров является двойной (дуплетом). Впоследствии у других элементов были обнаружены мультиплеты. Одна из задач изучения сложных атомов - это изучение тонкой структуры их атомных спектров. Квантовая механика заложила научную основу спектрального анализа.
Решение уравнения Шредингера похоже на решение задачи для водородоподобного атома: состояние атома характеризуется теми же тремя квантовыми числами n, l и m. Однако энергия электрона становится функцией не только главного квантового числа n, но и орбитального квантового числа l - Wnl. Энергетический спектр электрона в этом случае представляет собою ряд расщеплённых линий. Таким образом, в этом случае снимается вырождение по орбитальному квантовому числу l. Вырождение по магнитному квантовому числу сохраняется с кратностью f=2 l+1. Экспериментальное исследование спектров щелочных металлов (Na, K и др. ) показало, что каждая линия этих спектров является двойной (дуплетом). Впоследствии у других элементов были обнаружены мультиплеты. Одна из задач изучения сложных атомов - это изучение тонкой структуры их атомных спектров. Квантовая механика заложила научную основу спектрального анализа.
 В 1896 году П. Зееман экспериментально обнаружил расщепление спектральных линий атомов, помещённых в магнитное поле, что обусловлено расщеплением энергетических уровней атомов. Это явление получило название эффекта Зеемана. В магнитном поле атомы, обладающие магнитным моментом, приобретают дополнительную энергию. Таким образом, магнитное поле снимает вырождение по магнитному квантовому числу m. Для магнитного квантового числа m существует правило отбора m = 0, 1. При наблюдении излучения, распространяющегося перпендикулярно направлению магнитного поля, спектральная линия с частотой 0 расщепляется на три компоненты (триплет) с частотами: 0 ( -компонента), 0+ 0 и 0 - 0 ( -компоненты), причём Все три компоненты линейно поляризованы: -компонента вдоль направления магнитного поля, а -компоненты – перпендикулярно. При наблюдении излучения, распространяющегося параллельно направлению магнитного поля, спектральная линия с частотой 0 ( -компонента) исчезает, а -компоненты (с частотами 0 0) оказываются циркулярно поляризованными с противоположным направлением вращения. Этот эффект называется простым или нормальным эффектом Зеемана.
В 1896 году П. Зееман экспериментально обнаружил расщепление спектральных линий атомов, помещённых в магнитное поле, что обусловлено расщеплением энергетических уровней атомов. Это явление получило название эффекта Зеемана. В магнитном поле атомы, обладающие магнитным моментом, приобретают дополнительную энергию. Таким образом, магнитное поле снимает вырождение по магнитному квантовому числу m. Для магнитного квантового числа m существует правило отбора m = 0, 1. При наблюдении излучения, распространяющегося перпендикулярно направлению магнитного поля, спектральная линия с частотой 0 расщепляется на три компоненты (триплет) с частотами: 0 ( -компонента), 0+ 0 и 0 - 0 ( -компоненты), причём Все три компоненты линейно поляризованы: -компонента вдоль направления магнитного поля, а -компоненты – перпендикулярно. При наблюдении излучения, распространяющегося параллельно направлению магнитного поля, спектральная линия с частотой 0 ( -компонента) исчезает, а -компоненты (с частотами 0 0) оказываются циркулярно поляризованными с противоположным направлением вращения. Этот эффект называется простым или нормальным эффектом Зеемана.
 В слабых магнитных полях наблюдается сложный или аномальный эффект Зеемана – расщепление спектральных линий на множество - или -компонент. При увеличении напряжённости магнитного поля расщепление спектральных линий растёт и постепенно начинают сливаться компоненты мультиплетов соседних спектральных линий. В сильном магнитном поле аномальный эффект Зеемана переходит в нормальный – из всех компонент мультиплетов остаются три линии (для поперечного) или две линии (для продольного) магнитного поля. слабое поле сильное поле Нормальный эффект Зеемана был объяснён ещё в 1897 году Х. Лоренцем на основе классической электронной теории. Объяснение же аномального эффекта Зеемана стало возможным только в рамках квантовой теории после обнаружения у электрона собственного момента импульса (спина) и собственного магнитного момента.
В слабых магнитных полях наблюдается сложный или аномальный эффект Зеемана – расщепление спектральных линий на множество - или -компонент. При увеличении напряжённости магнитного поля расщепление спектральных линий растёт и постепенно начинают сливаться компоненты мультиплетов соседних спектральных линий. В сильном магнитном поле аномальный эффект Зеемана переходит в нормальный – из всех компонент мультиплетов остаются три линии (для поперечного) или две линии (для продольного) магнитного поля. слабое поле сильное поле Нормальный эффект Зеемана был объяснён ещё в 1897 году Х. Лоренцем на основе классической электронной теории. Объяснение же аномального эффекта Зеемана стало возможным только в рамках квантовой теории после обнаружения у электрона собственного момента импульса (спина) и собственного магнитного момента.
 Предположение о существовании у электронов собственного момента импульса , названного спином, и соответствующего ему собственного магнитного момента было высказано в 1925 году американскими физиками С. Гаудсмитом и Дж. Уленбеком при истолковании опытов немецких физиков-экспериментаторов О. Штерна и В. Герлаха. Целью опытов Штерна-Герлаха (1922 г. ) было измерение магнитного момента атомов серебра, у которых орбитальные механические и магнитные моменты равны соответствующим моментам валентных электронов (моменты электронов внутренних замкнутых оболочек скомпенсированы). Схема опыта В вакуумной колбе нагреваемый до высокой температуры серебряный катод испускает пучок атомов серебра. Диафрагма В вырезает узкий пучок атомов, который проходит через перпендикулярно направленное, сильное и неоднородное (на расстояниях порядка размеров атома) магнитное поле и попадает на экран. Если бы магнитные моменты атомов серебра имели любые ориентации в пространстве, то на экране наблюдалось бы непрерывное распределение атомов с большей плотностью в центре экрана. Опыт же дал неожиданный результат – на экране наблюдались две резкие полосы, что соответствовало только двум возможным ориентациям магнитного момента во внешнем поле.
Предположение о существовании у электронов собственного момента импульса , названного спином, и соответствующего ему собственного магнитного момента было высказано в 1925 году американскими физиками С. Гаудсмитом и Дж. Уленбеком при истолковании опытов немецких физиков-экспериментаторов О. Штерна и В. Герлаха. Целью опытов Штерна-Герлаха (1922 г. ) было измерение магнитного момента атомов серебра, у которых орбитальные механические и магнитные моменты равны соответствующим моментам валентных электронов (моменты электронов внутренних замкнутых оболочек скомпенсированы). Схема опыта В вакуумной колбе нагреваемый до высокой температуры серебряный катод испускает пучок атомов серебра. Диафрагма В вырезает узкий пучок атомов, который проходит через перпендикулярно направленное, сильное и неоднородное (на расстояниях порядка размеров атома) магнитное поле и попадает на экран. Если бы магнитные моменты атомов серебра имели любые ориентации в пространстве, то на экране наблюдалось бы непрерывное распределение атомов с большей плотностью в центре экрана. Опыт же дал неожиданный результат – на экране наблюдались две резкие полосы, что соответствовало только двум возможным ориентациям магнитного момента во внешнем поле.
 Опыт Штерна и Герлаха показал, что проекция магнитного момента атомов на направление магнитного поля квантуется. Экспериментальное значение магнитного момента оказалось равным магнетону Бора с точностью до 10%. Опыты проводились с атомами элементов первой группы таблицы Менделеева, у которых единственный валентный электрон находится в s-состоянии, в котором орбитальное квантовое число l = 0, а следовательно равны нулю орбитальные механический и магнитный моменты. Поэтому возник вопрос - какое квантование было обнаружено в этих опытах? С. Гаудсмит и Дж. Уленбек выдвинули гипотезу о существовании у электронов собственного момента импульса (спина) и собственного магнитного момента. Они дали спину наглядное истолкование – связали его с вращением электрона (заряженного шарика) вокруг своей оси. Однако расчёт показал, что при pms = Б линейная скорость точек на поверхности электрона (шарика) примерно равна 200 с, (с - скорость света в вакууме), что противоречит теории относительности. Поэтому от таких модельных представлений пришлось отказаться. Спин электрона и других элементарных частиц следует рассматривать как внутреннее свойство, присущее этим частицам, такое как, например, масса и заряд.
Опыт Штерна и Герлаха показал, что проекция магнитного момента атомов на направление магнитного поля квантуется. Экспериментальное значение магнитного момента оказалось равным магнетону Бора с точностью до 10%. Опыты проводились с атомами элементов первой группы таблицы Менделеева, у которых единственный валентный электрон находится в s-состоянии, в котором орбитальное квантовое число l = 0, а следовательно равны нулю орбитальные механический и магнитный моменты. Поэтому возник вопрос - какое квантование было обнаружено в этих опытах? С. Гаудсмит и Дж. Уленбек выдвинули гипотезу о существовании у электронов собственного момента импульса (спина) и собственного магнитного момента. Они дали спину наглядное истолкование – связали его с вращением электрона (заряженного шарика) вокруг своей оси. Однако расчёт показал, что при pms = Б линейная скорость точек на поверхности электрона (шарика) примерно равна 200 с, (с - скорость света в вакууме), что противоречит теории относительности. Поэтому от таких модельных представлений пришлось отказаться. Спин электрона и других элементарных частиц следует рассматривать как внутреннее свойство, присущее этим частицам, такое как, например, масса и заряд.
 Из общих выводов квантовой механики следует, что спин квантуется по закону: Вектор может иметь 2 s+1 ориентаций в магнитном поле. Из опытов Штерна и Герлаха следует, что для электронов их две, т. е. 2 s+1 = 2 и s = 1/2. Численное значение спина электрона равно: По аналогии с пространственным квантованием орбитального момента импульса квантуется и проекция спина на направление внешнего поля: где ms= 1/2 - магнитное спиновое число. Таким образом, проекция спина на направление поля может принимать только два значения: Из опытов Штерна и Герлаха следует, что Тогда, поскольку векторы и направлены вдоль одной прямой в противоположные стороны, то: где s - спиновое гиромагнитное отношение, которое вдвое превышает орбитальное гиромагнитное отношение. ,
Из общих выводов квантовой механики следует, что спин квантуется по закону: Вектор может иметь 2 s+1 ориентаций в магнитном поле. Из опытов Штерна и Герлаха следует, что для электронов их две, т. е. 2 s+1 = 2 и s = 1/2. Численное значение спина электрона равно: По аналогии с пространственным квантованием орбитального момента импульса квантуется и проекция спина на направление внешнего поля: где ms= 1/2 - магнитное спиновое число. Таким образом, проекция спина на направление поля может принимать только два значения: Из опытов Штерна и Герлаха следует, что Тогда, поскольку векторы и направлены вдоль одной прямой в противоположные стороны, то: где s - спиновое гиромагнитное отношение, которое вдвое превышает орбитальное гиромагнитное отношение. ,
 . Собственный магнитный момент электрона и его спин связаны соотношением: Модуль собственного магнитного момента квантуется по закону: а его проекция на ось Z может иметь два значения: Полный механический момент импульса электрона слагается из двух моментов: орбитального , обусловленного движением электрона в атоме, и собственного (спина), не связанного с движением электрона в пространстве. Его модуль равен: где j - квантовое число полного момента, j = l + s, …, l - s (l и s -орбитальное и спиновое квантовые числа соответственно). Проекция полного механического момента электрона на направление Z : где mj = -j, -j+1, -j+2, . . . , j-2, j-1, j. Полный магнитный момент электрона равен: где g- множитель Ланде или g-фактор (фактор магнитного расщепления), равный:
. Собственный магнитный момент электрона и его спин связаны соотношением: Модуль собственного магнитного момента квантуется по закону: а его проекция на ось Z может иметь два значения: Полный механический момент импульса электрона слагается из двух моментов: орбитального , обусловленного движением электрона в атоме, и собственного (спина), не связанного с движением электрона в пространстве. Его модуль равен: где j - квантовое число полного момента, j = l + s, …, l - s (l и s -орбитальное и спиновое квантовые числа соответственно). Проекция полного механического момента электрона на направление Z : где mj = -j, -j+1, -j+2, . . . , j-2, j-1, j. Полный магнитный момент электрона равен: где g- множитель Ланде или g-фактор (фактор магнитного расщепления), равный:
 Механический и магнитный моменты многоэлектронного атома слагаются из соответствующих моментов отдельных электронов. При этом возможны два случая: 1. LS-связь - орбитальные моменты отдельных электронов взаимодействуют друг с другом сильнее, чем со спинами , которые в свою очередь взаимодействуют друг с другом сильнее, чем с орбитальными моментами. Вследствие этого образуются результирующий орбитальный момент атома и результирующий спин атома , которые определяют суммарный момент атома = +. Такой тип связи встречается наиболее часто. 2. JJ-связь - каждая пара и взаимодействуют друг с другом сильнее, чем с другими и , вследствие чего образуются суммарные электронные моменты , которые затем уже объединяются в суммарный момент атома = +. Такой тип связи наблюдается у тяжёлых атомов.
Механический и магнитный моменты многоэлектронного атома слагаются из соответствующих моментов отдельных электронов. При этом возможны два случая: 1. LS-связь - орбитальные моменты отдельных электронов взаимодействуют друг с другом сильнее, чем со спинами , которые в свою очередь взаимодействуют друг с другом сильнее, чем с орбитальными моментами. Вследствие этого образуются результирующий орбитальный момент атома и результирующий спин атома , которые определяют суммарный момент атома = +. Такой тип связи встречается наиболее часто. 2. JJ-связь - каждая пара и взаимодействуют друг с другом сильнее, чем с другими и , вследствие чего образуются суммарные электронные моменты , которые затем уже объединяются в суммарный момент атома = +. Такой тип связи наблюдается у тяжёлых атомов.
 7. 1. 3. Принцип тождественности. Симметрия волновой функции. Фермионы и бозоны. Принцип Паули. Распределение электронов по состояниям. Квантовые частицы, имеющие одинаковую массу, заряд, спин, квантовые числа являются тождественными и никакими экспериментальными методами их невозможно отличить друг от друга. Это один из фундаментальных принципов квантовой механики – принцип тождественности или принцип неразличимости тождественных частиц. В отличие от квантовых классические частицы обладают индивидуальностью – их можно пронумеровать, проследить за их траекторией. Состояние квантовой частицы описывается волновой функцией, позволяющей вычислять плотность вероятности 2 нахождения микрочастицы в окрестности той или иной точки пространства – понятие траектории в квантовой механике не существует. Если волновые функции двух микрочастиц перекрываются, то они становятся совершенно неразличимыми.
7. 1. 3. Принцип тождественности. Симметрия волновой функции. Фермионы и бозоны. Принцип Паули. Распределение электронов по состояниям. Квантовые частицы, имеющие одинаковую массу, заряд, спин, квантовые числа являются тождественными и никакими экспериментальными методами их невозможно отличить друг от друга. Это один из фундаментальных принципов квантовой механики – принцип тождественности или принцип неразличимости тождественных частиц. В отличие от квантовых классические частицы обладают индивидуальностью – их можно пронумеровать, проследить за их траекторией. Состояние квантовой частицы описывается волновой функцией, позволяющей вычислять плотность вероятности 2 нахождения микрочастицы в окрестности той или иной точки пространства – понятие траектории в квантовой механике не существует. Если волновые функции двух микрочастиц перекрываются, то они становятся совершенно неразличимыми.
 Принцип неразличимости тождественных частиц математически выражается так: (х1, х2) 2 = (х2, х1) 2, где х1 и х2 - совокупность пространственных и спиновых координат первой и второй частиц соответственно. Из этого равенства следует: (х1, х2) = (х2, х1). Принцип неразличимости тождественных частиц приводит к определённому свойству симметрии волновой функции. Если при перемене частиц местами волновая функция не меняет знак, она называется симметричной, если меняет - то антисимметричной. Симметрия волновых функций определяется спином частиц. Частицы с нулевым или целым спиновым числом описываются симметричной волновой функцией и называются бозонами. Частицы с полуцелым спиновым квантовым числом (электроны, протоны, нейтроны) описываются антисимметричной волновой функцией и называются фермионами. Для сложных частиц всё определяется суммарным спиновым числом.
Принцип неразличимости тождественных частиц математически выражается так: (х1, х2) 2 = (х2, х1) 2, где х1 и х2 - совокупность пространственных и спиновых координат первой и второй частиц соответственно. Из этого равенства следует: (х1, х2) = (х2, х1). Принцип неразличимости тождественных частиц приводит к определённому свойству симметрии волновой функции. Если при перемене частиц местами волновая функция не меняет знак, она называется симметричной, если меняет - то антисимметричной. Симметрия волновых функций определяется спином частиц. Частицы с нулевым или целым спиновым числом описываются симметричной волновой функцией и называются бозонами. Частицы с полуцелым спиновым квантовым числом (электроны, протоны, нейтроны) описываются антисимметричной волновой функцией и называются фермионами. Для сложных частиц всё определяется суммарным спиновым числом.
 Частицы, имеющие одинаковый набор квантовых чисел, описываются симметричными волновыми функциями. Такие частицы являются бозонами. Бозоны стремятся к «объединению» , «притягиваются» друг к другу. Чем больше бозонов в данном состоянии, тем охотнее другие бозоны стремятся попасть в это состояние. Фермионы, входящие в одну систему, не могут находиться в одинаковых состояниях и иметь одинаковые наборы квантовых чисел. Это составляет содержание ещё одного из фундаментальных принципов квантовой механики - принципа Паули, сформулированного в 1925 году. Фермионы стремятся к «уединению» , «отталкиваются» друг от друга. Для системы электронов принцип Паули записывается так: Z 1(n, l, m, ms) = 0 или 1, где Z 1(n, l, m, ms) - число электронов, имеющих определённый набор квантовых чисел n, l, m, ms.
Частицы, имеющие одинаковый набор квантовых чисел, описываются симметричными волновыми функциями. Такие частицы являются бозонами. Бозоны стремятся к «объединению» , «притягиваются» друг к другу. Чем больше бозонов в данном состоянии, тем охотнее другие бозоны стремятся попасть в это состояние. Фермионы, входящие в одну систему, не могут находиться в одинаковых состояниях и иметь одинаковые наборы квантовых чисел. Это составляет содержание ещё одного из фундаментальных принципов квантовой механики - принципа Паули, сформулированного в 1925 году. Фермионы стремятся к «уединению» , «отталкиваются» друг от друга. Для системы электронов принцип Паули записывается так: Z 1(n, l, m, ms) = 0 или 1, где Z 1(n, l, m, ms) - число электронов, имеющих определённый набор квантовых чисел n, l, m, ms.
 Поскольку для электронов ms может принимать только два значения: 1/2, то максимальное число электронов, имеющих определённый набор квантовых чисел n, l, m равно: Z 2(n, l, m) = 2. Поскольку m = - l, -l+1, . . . 0, . . . l-1, l, то максимальное число электронов, имеющих определённый набор квантовых чисел n и l равно: Z 3(n, l) = 2(2 l+1). Поскольку l = 0, 1, 2, 3. . . n-1, то максимальное число электронов, имеющих квантовое число n равно: Обобщение полученных результатов приводится в таблице: Z 1(n, l, m, ms) Z 2(n, l, m) Z 3(n, l) Z(n) 1 2 2(2 l+1) 2 n 2
Поскольку для электронов ms может принимать только два значения: 1/2, то максимальное число электронов, имеющих определённый набор квантовых чисел n, l, m равно: Z 2(n, l, m) = 2. Поскольку m = - l, -l+1, . . . 0, . . . l-1, l, то максимальное число электронов, имеющих определённый набор квантовых чисел n и l равно: Z 3(n, l) = 2(2 l+1). Поскольку l = 0, 1, 2, 3. . . n-1, то максимальное число электронов, имеющих квантовое число n равно: Обобщение полученных результатов приводится в таблице: Z 1(n, l, m, ms) Z 2(n, l, m) Z 3(n, l) Z(n) 1 2 2(2 l+1) 2 n 2
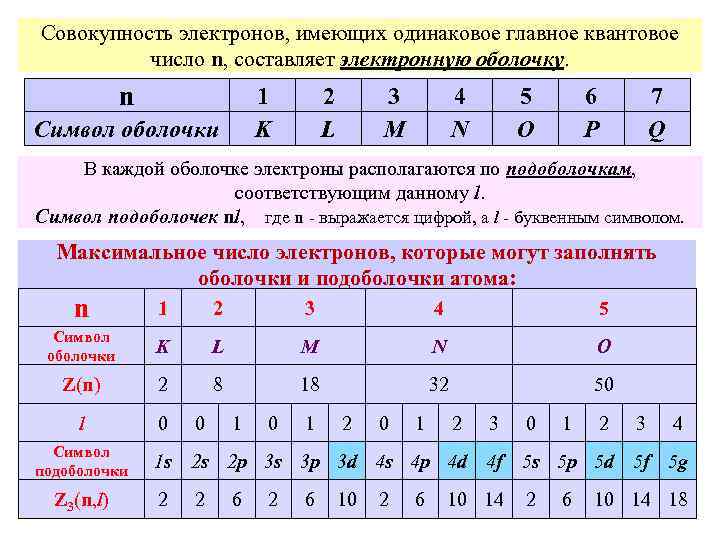 Совокупность электронов, имеющих одинаковое главное квантовое число n, составляет электронную оболочку. n 1 K Символ оболочки 2 L 3 M 4 N 5 O 6 P 7 Q В каждой оболочке электроны располагаются по подоболочкам, соответствующим данному l. Символ подоболочек nl, где n - выражается цифрой, а l - буквенным символом. Максимальное число электронов, которые могут заполнять оболочки и подоболочки атома: n 1 2 3 4 5 Символ оболочки K L M N O Z(n) 2 8 18 32 50 l 0 Символ подоболочки Z 3(n, l) 0 1 2 3 4 1 s 2 s 2 p 3 s 3 p 3 d 4 s 4 p 4 d 4 f 5 s 5 p 5 d 5 f 5 g 2 2 6 10 14 18
Совокупность электронов, имеющих одинаковое главное квантовое число n, составляет электронную оболочку. n 1 K Символ оболочки 2 L 3 M 4 N 5 O 6 P 7 Q В каждой оболочке электроны располагаются по подоболочкам, соответствующим данному l. Символ подоболочек nl, где n - выражается цифрой, а l - буквенным символом. Максимальное число электронов, которые могут заполнять оболочки и подоболочки атома: n 1 2 3 4 5 Символ оболочки K L M N O Z(n) 2 8 18 32 50 l 0 Символ подоболочки Z 3(n, l) 0 1 2 3 4 1 s 2 s 2 p 3 s 3 p 3 d 4 s 4 p 4 d 4 f 5 s 5 p 5 d 5 f 5 g 2 2 6 10 14 18
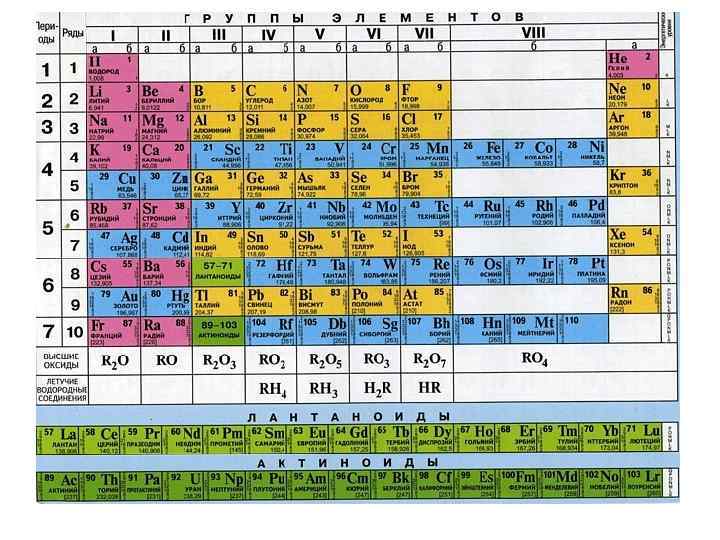
 7. 1. 4. Периодическая система элементов Д. И. Менделеева. Принцип Паули позволяет объяснить периодичность свойств атомов и принцип построения периодической системы элементов, составленной задолго до создания квантовой механики в 1869 году русским учёным Дмитрием Ивановичем Менделеевым. Периодическая система элементов является фундаментальным законом природы, на котором базируются современная химия, атомная и ядерная физика. Менделеев расположил известные в то время 64 химических элемента в порядке возрастания их атомных масс. Периодически через правильные промежутки - периоды элементы, оказавшиеся в таблице в одном вертикальном ряду - в группе, обнаруживают сходные физико-химические свойства. Но часть клеток оказалась незаполненной. В дальнейшем были открыты новые элементы, свойства некоторых из них были предсказаны Менделеевым. В настоящее время таблица полностью заполнена.
7. 1. 4. Периодическая система элементов Д. И. Менделеева. Принцип Паули позволяет объяснить периодичность свойств атомов и принцип построения периодической системы элементов, составленной задолго до создания квантовой механики в 1869 году русским учёным Дмитрием Ивановичем Менделеевым. Периодическая система элементов является фундаментальным законом природы, на котором базируются современная химия, атомная и ядерная физика. Менделеев расположил известные в то время 64 химических элемента в порядке возрастания их атомных масс. Периодически через правильные промежутки - периоды элементы, оказавшиеся в таблице в одном вертикальном ряду - в группе, обнаруживают сходные физико-химические свойства. Но часть клеток оказалась незаполненной. В дальнейшем были открыты новые элементы, свойства некоторых из них были предсказаны Менделеевым. В настоящее время таблица полностью заполнена.
 Теория периодической системы основана на законах квантовой механики. Основные принципы её таковы: 1) порядковый номер химического элемента равен числу элементарных положительных зарядов ядра; 2) состояние электронов в атоме определяется набором квантовых чисел n, l, m, ms ; 3) распределение электронов по состояниям удовлетворяет принципу минимума потенциальной энергии; 4) заполнение электронных энергетических состояний в атоме происходит в соответствии с принципом Паули; 5) химические и физические свойства элементов объясняются поведением внешних валентных электронов в атоме.
Теория периодической системы основана на законах квантовой механики. Основные принципы её таковы: 1) порядковый номер химического элемента равен числу элементарных положительных зарядов ядра; 2) состояние электронов в атоме определяется набором квантовых чисел n, l, m, ms ; 3) распределение электронов по состояниям удовлетворяет принципу минимума потенциальной энергии; 4) заполнение электронных энергетических состояний в атоме происходит в соответствии с принципом Паули; 5) химические и физические свойства элементов объясняются поведением внешних валентных электронов в атоме.
 Электроны, занимающие в атоме состояния с одинаковым n, образуют электронную оболочку (слой): K-, L-, M-. . . -оболочки. В каждой оболочке электроны располагаются по подоболочкам, соответствующим определённым квантовым числам l. Квантовые числа n и l задают электронную конфигурацию атома. Символическая формула электронной конфигурации : nl. Z (n - главное квантовое число, l - символическое обозначение орбитального квантового числа l, Z - количество электронов в атоме с данным набором значений n и l ). Например, электронная конфигурация алюминия (13 Al ) - 1 s 22 p 63 s 23 p 1. Периодическая система элементов отличается от идеальной - сначала заполняются состояния с наименьшей энергией, а затем большей. Энергетические уровни многоэлектронных атомов расщеплены, и у тяжёлых атомов некоторые энергетические уровни с большим n и малым l располагаются ниже, чем уровни с меньшим n и большим l. Поэтому имеются химические элементы, у которых происходит достройка последующих оболочек при недостроенной предыдущей. Такие элементы называются переходными.
Электроны, занимающие в атоме состояния с одинаковым n, образуют электронную оболочку (слой): K-, L-, M-. . . -оболочки. В каждой оболочке электроны располагаются по подоболочкам, соответствующим определённым квантовым числам l. Квантовые числа n и l задают электронную конфигурацию атома. Символическая формула электронной конфигурации : nl. Z (n - главное квантовое число, l - символическое обозначение орбитального квантового числа l, Z - количество электронов в атоме с данным набором значений n и l ). Например, электронная конфигурация алюминия (13 Al ) - 1 s 22 p 63 s 23 p 1. Периодическая система элементов отличается от идеальной - сначала заполняются состояния с наименьшей энергией, а затем большей. Энергетические уровни многоэлектронных атомов расщеплены, и у тяжёлых атомов некоторые энергетические уровни с большим n и малым l располагаются ниже, чем уровни с меньшим n и большим l. Поэтому имеются химические элементы, у которых происходит достройка последующих оболочек при недостроенной предыдущей. Такие элементы называются переходными.
 Атомы переходных элементов имеют незавершённые внутренние оболочки. Различают d-элементы, у которых происходит заполнение внутренних 3 d- , 4 d- , 5 d- , 6 d-подоболочек, и f-элементы, у которых заполняются внутренние 4 f-подоболочка (лантаноиды) и 5 f-подоболочка (актиноиды). К переходным элементам относятся: элементы от скандия 21 Sc до никеля 28 Ni; элементы от иттрия 39 Y до палладия 46 Pd; элементы от лантана 57 La до платины 78 Pt – группа лантаноидов; элементы от гафния 72 Hf до палладия 78 Pt; элементы от актиния 89 Ac до лоуренсия 103 Lr – группа актиноидов. элементы от резерфордия 104 Rf до ливермория 116 Lv.
Атомы переходных элементов имеют незавершённые внутренние оболочки. Различают d-элементы, у которых происходит заполнение внутренних 3 d- , 4 d- , 5 d- , 6 d-подоболочек, и f-элементы, у которых заполняются внутренние 4 f-подоболочка (лантаноиды) и 5 f-подоболочка (актиноиды). К переходным элементам относятся: элементы от скандия 21 Sc до никеля 28 Ni; элементы от иттрия 39 Y до палладия 46 Pd; элементы от лантана 57 La до платины 78 Pt – группа лантаноидов; элементы от гафния 72 Hf до палладия 78 Pt; элементы от актиния 89 Ac до лоуренсия 103 Lr – группа актиноидов. элементы от резерфордия 104 Rf до ливермория 116 Lv.
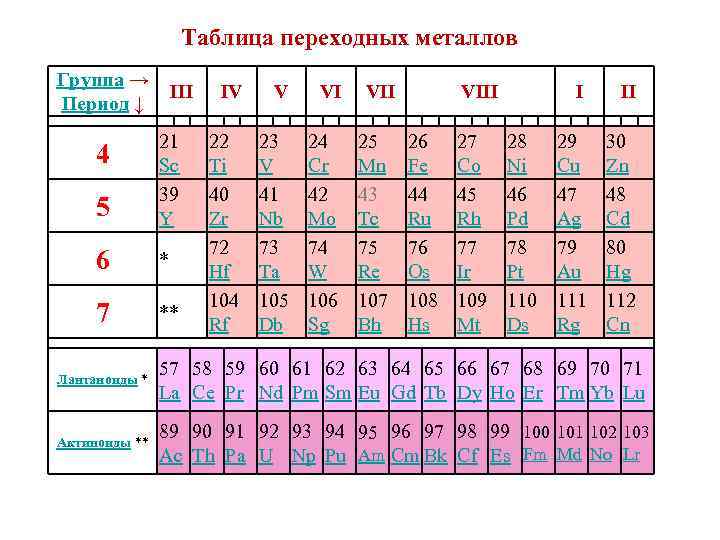 Таблица переходных металлов Группа → Период ↓ III 5 21 Sc 39 Y 6 * 7 ** 4 IV V VI 22 Ti 40 Zr 72 Hf 104 Rf 23 V 41 Nb 73 Ta 105 Db 24 Cr 42 Mo 74 W 106 Sg VII 25 Mn 43 Tc 75 Re 107 Bh VIII 26 Fe 44 Ru 76 Os 108 Hs 27 Co 45 Rh 77 Ir 109 Mt I 28 Ni 46 Pd 78 Pt 110 Ds II 29 Cu 47 Ag 79 Au 111 Rg 30 Zn 48 Cd 80 Hg 112 Cn Лантаноиды * 57 58 59 60 61 62 63 64 65 66 67 68 69 70 71 La Ce Pr Nd Pm Sm Eu Gd Tb Dy Ho Er Tm Yb Lu Актиноиды ** 89 90 91 92 93 94 95 96 97 98 99 100 101 102 103 Ac Th Pa U Np Pu Am Cm Bk Cf Es Fm Md No Lr
Таблица переходных металлов Группа → Период ↓ III 5 21 Sc 39 Y 6 * 7 ** 4 IV V VI 22 Ti 40 Zr 72 Hf 104 Rf 23 V 41 Nb 73 Ta 105 Db 24 Cr 42 Mo 74 W 106 Sg VII 25 Mn 43 Tc 75 Re 107 Bh VIII 26 Fe 44 Ru 76 Os 108 Hs 27 Co 45 Rh 77 Ir 109 Mt I 28 Ni 46 Pd 78 Pt 110 Ds II 29 Cu 47 Ag 79 Au 111 Rg 30 Zn 48 Cd 80 Hg 112 Cn Лантаноиды * 57 58 59 60 61 62 63 64 65 66 67 68 69 70 71 La Ce Pr Nd Pm Sm Eu Gd Tb Dy Ho Er Tm Yb Lu Актиноиды ** 89 90 91 92 93 94 95 96 97 98 99 100 101 102 103 Ac Th Pa U Np Pu Am Cm Bk Cf Es Fm Md No Lr
 Периодичность физико-химических свойств элементов объясняется повторяемостью электронной конфигурации во внешних s- и р-подоболочках (l=0 и l=1). Электроны, которые в оболочке с наибольшим n входят в состав s- и р-подоболочек, называются внешними или валентными электронами. Общее число электронов в s- и р-подоболочках равно 8. Столько же групп в таблице Менделеева. В химических реакциях атомы с числом валентных электронов меньшим 4 склонны отдавать свои валентные электроны, а атомы с числом валентных электронов большим 4 склонны присоединять электроны других атомов. Электроны в s- и р-подоболочках и определяют химические и оптические свойства атомов.
Периодичность физико-химических свойств элементов объясняется повторяемостью электронной конфигурации во внешних s- и р-подоболочках (l=0 и l=1). Электроны, которые в оболочке с наибольшим n входят в состав s- и р-подоболочек, называются внешними или валентными электронами. Общее число электронов в s- и р-подоболочках равно 8. Столько же групп в таблице Менделеева. В химических реакциях атомы с числом валентных электронов меньшим 4 склонны отдавать свои валентные электроны, а атомы с числом валентных электронов большим 4 склонны присоединять электроны других атомов. Электроны в s- и р-подоболочках и определяют химические и оптические свойства атомов.
 7. 2. МОЛЕКУЛА 7. 2. 1. Физическая природа химической связи. Ионный и ковалентный типы связи. Молекула водорода. Обменное взаимодействие. Мельчайшей частицей вещества, сохраняющей все его свойства, является молекула. Молекула состоит из одинаковых или различных атомов, соединённых между собой химическими связями. Устойчивость молекул и их свойства объясняются квантово-механическими закономерностями. Химические связи обусловлены взаимодействием внешних валентных электронов атомов из s- и р-подоболочек с максимальными для данных атомов главными квантовыми числами n. Существуют две основные формы химической связи: ионная (гетерополярная) и ковалентная (гомеополярная).
7. 2. МОЛЕКУЛА 7. 2. 1. Физическая природа химической связи. Ионный и ковалентный типы связи. Молекула водорода. Обменное взаимодействие. Мельчайшей частицей вещества, сохраняющей все его свойства, является молекула. Молекула состоит из одинаковых или различных атомов, соединённых между собой химическими связями. Устойчивость молекул и их свойства объясняются квантово-механическими закономерностями. Химические связи обусловлены взаимодействием внешних валентных электронов атомов из s- и р-подоболочек с максимальными для данных атомов главными квантовыми числами n. Существуют две основные формы химической связи: ионная (гетерополярная) и ковалентная (гомеополярная).
 Ионная связь. Теория ионной связи впервые была разработана М. Борном в 1918 году на примере молекул хлористого натрия (Na. Cl). Согласно этой теории электроны расположены в молекулах так, что у одного из ядер образуется их избыток, а около другого - недостаток. Благодаря переходу внешнего валентного электрона от одного атома к другому, образуется пара разноимённых ионов, взаимодействующих друг с другом электростатическими силами. С точки зрения квантовой механики при ионной связи образуется устойчивая электронная конфигурация s-p-подоболочек инертных элементов, обладающая наименьшей энергией. Ионным типом связи обладают соединения Na. Cl, KCl, Na. Br, Mg. O, Ca. O и др.
Ионная связь. Теория ионной связи впервые была разработана М. Борном в 1918 году на примере молекул хлористого натрия (Na. Cl). Согласно этой теории электроны расположены в молекулах так, что у одного из ядер образуется их избыток, а около другого - недостаток. Благодаря переходу внешнего валентного электрона от одного атома к другому, образуется пара разноимённых ионов, взаимодействующих друг с другом электростатическими силами. С точки зрения квантовой механики при ионной связи образуется устойчивая электронная конфигурация s-p-подоболочек инертных элементов, обладающая наименьшей энергией. Ионным типом связи обладают соединения Na. Cl, KCl, Na. Br, Mg. O, Ca. O и др.
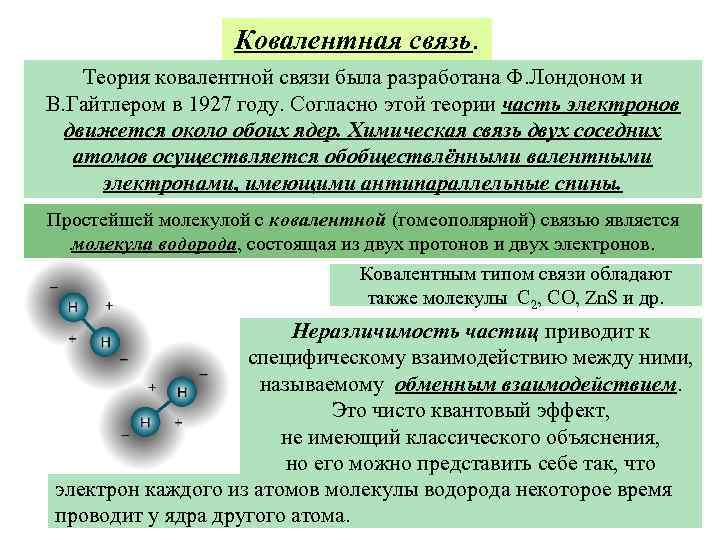 Ковалентная связь. Теория ковалентной связи была разработана Ф. Лондоном и В. Гайтлером в 1927 году. Согласно этой теории часть электронов движется около обоих ядер. Химическая связь двух соседних атомов осуществляется обобществлёнными валентными электронами, имеющими антипараллельные спины. Простейшей молекулой с ковалентной (гомеополярной) связью является молекула водорода, состоящая из двух протонов и двух электронов. Ковалентным типом связи обладают также молекулы С 2, CO, Zn. S и др. Неразличимость частиц приводит к специфическому взаимодействию между ними, называемому обменным взаимодействием. Это чисто квантовый эффект, не имеющий классического объяснения, но его можно представить себе так, что электрон каждого из атомов молекулы водорода некоторое время проводит у ядра другого атома.
Ковалентная связь. Теория ковалентной связи была разработана Ф. Лондоном и В. Гайтлером в 1927 году. Согласно этой теории часть электронов движется около обоих ядер. Химическая связь двух соседних атомов осуществляется обобществлёнными валентными электронами, имеющими антипараллельные спины. Простейшей молекулой с ковалентной (гомеополярной) связью является молекула водорода, состоящая из двух протонов и двух электронов. Ковалентным типом связи обладают также молекулы С 2, CO, Zn. S и др. Неразличимость частиц приводит к специфическому взаимодействию между ними, называемому обменным взаимодействием. Это чисто квантовый эффект, не имеющий классического объяснения, но его можно представить себе так, что электрон каждого из атомов молекулы водорода некоторое время проводит у ядра другого атома.
 Молекула водорода является квантовой системой и описывается уравнением Шрёдингера, учитывающим: а) движение электрона в молекуле, б) колебания атомов в молекуле, с) вращение молекулы. Решение такой задачи очень сложное. Обычно её решают отдельно для электронов и отдельно для ядер. Если, например, ядра считать неподвижными, то уравнение Шрёдингера принимает вид: где 1 и 2 - лапласианы, содержащие координаты одного и другого электронов, r 12 и R - расстояния между электронами и ядрами соответственно, r 1 е, r 2 е - модули радиусов-векторов первого и второго электронов, r 1 я, r 2 я -, первого и второго ядер. Решение этого уравнения получено методом Гайтлера-Лондона.
Молекула водорода является квантовой системой и описывается уравнением Шрёдингера, учитывающим: а) движение электрона в молекуле, б) колебания атомов в молекуле, с) вращение молекулы. Решение такой задачи очень сложное. Обычно её решают отдельно для электронов и отдельно для ядер. Если, например, ядра считать неподвижными, то уравнение Шрёдингера принимает вид: где 1 и 2 - лапласианы, содержащие координаты одного и другого электронов, r 12 и R - расстояния между электронами и ядрами соответственно, r 1 е, r 2 е - модули радиусов-векторов первого и второго электронов, r 1 я, r 2 я -, первого и второго ядер. Решение этого уравнения получено методом Гайтлера-Лондона.
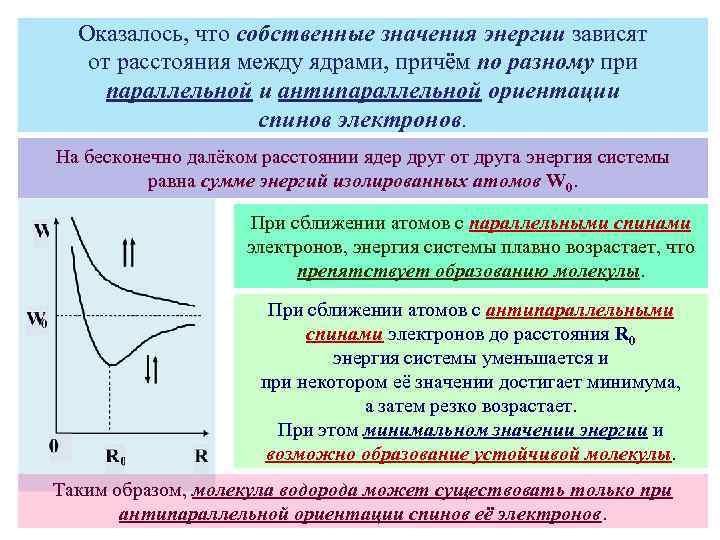 Оказалось, что собственные значения энергии зависят от расстояния между ядрами, причём по разному при параллельной и антипараллельной ориентации спинов электронов. На бесконечно далёком расстоянии ядер друг от друга энергия системы равна сумме энергий изолированных атомов W 0. При сближении атомов с параллельными спинами электронов, энергия системы плавно возрастает, что препятствует образованию молекулы. При сближении атомов с антипараллельными спинами электронов до расстояния R 0 энергия системы уменьшается и при некотором её значении достигает минимума, а затем резко возрастает. При этом минимальном значении энергии и возможно образование устойчивой молекулы. Таким образом, молекула водорода может существовать только при антипараллельной ориентации спинов её электронов.
Оказалось, что собственные значения энергии зависят от расстояния между ядрами, причём по разному при параллельной и антипараллельной ориентации спинов электронов. На бесконечно далёком расстоянии ядер друг от друга энергия системы равна сумме энергий изолированных атомов W 0. При сближении атомов с параллельными спинами электронов, энергия системы плавно возрастает, что препятствует образованию молекулы. При сближении атомов с антипараллельными спинами электронов до расстояния R 0 энергия системы уменьшается и при некотором её значении достигает минимума, а затем резко возрастает. При этом минимальном значении энергии и возможно образование устойчивой молекулы. Таким образом, молекула водорода может существовать только при антипараллельной ориентации спинов её электронов.
 7. 2. 2. Энергетическая структура молекул. Колебания и вращения двухатомной молекулы. Молекулярные спектры. Энергия изолированной молекулы W зависит от: 1) энергии движения электронов вокруг ядер We (электронная энергия), которая определяется электронной конфигурацией атомов, 2) энергии колебаний молекулы Wv (колебательная или вибрационная, энергия), при которых меняется расстояние между ядрами, 3) от энергии вращения ядер Wr (вращательная или ротационная энергия), при котором меняется ориентация молекулы в пространстве. Энергия квантового гармонического осциллятора квантуется: где v = 0, 1, 2, 3, . . . - колебательное квантовое число, для которого существует правило отбора v = 1, v - частота колебаний молекулы. Вращательная энергия молекулы, имеющей момент инерции I, частоту вращения r и квантованный момент импульса , также имеет квантованные значения: где J = 0, 1, 2, 3, . . . - вращательное квантовое число, для которого существует правило отбора J = 1.
7. 2. 2. Энергетическая структура молекул. Колебания и вращения двухатомной молекулы. Молекулярные спектры. Энергия изолированной молекулы W зависит от: 1) энергии движения электронов вокруг ядер We (электронная энергия), которая определяется электронной конфигурацией атомов, 2) энергии колебаний молекулы Wv (колебательная или вибрационная, энергия), при которых меняется расстояние между ядрами, 3) от энергии вращения ядер Wr (вращательная или ротационная энергия), при котором меняется ориентация молекулы в пространстве. Энергия квантового гармонического осциллятора квантуется: где v = 0, 1, 2, 3, . . . - колебательное квантовое число, для которого существует правило отбора v = 1, v - частота колебаний молекулы. Вращательная энергия молекулы, имеющей момент инерции I, частоту вращения r и квантованный момент импульса , также имеет квантованные значения: где J = 0, 1, 2, 3, . . . - вращательное квантовое число, для которого существует правило отбора J = 1.
 Таким образом, полная энергия молекулы равна: Вклад в полную энергию электронной, колебательной и вращательной её составляющих различный и примерно кратен отношениям: где me и mя - масса электрона и масса всех ядер молекулы соответственно. Поскольку me/mя 10 -5 10 -3, то We 1 10 э. В, W v 10 -2 10 -1 э. В, W r 10 -5 10 -3 э. В. то есть We W v W r. Электронная, колебательная и вращательная энергии молекулы квантуются и им соответствуют наборы дискретных энергетических уровней. Из теории и эксперимента следует, что расстояния между вращательными уровнями значительно меньше расстояния между колебательными уровнями, а расстояния между колебательными уровнями значительно меньше расстояния между электронными уровнями.
Таким образом, полная энергия молекулы равна: Вклад в полную энергию электронной, колебательной и вращательной её составляющих различный и примерно кратен отношениям: где me и mя - масса электрона и масса всех ядер молекулы соответственно. Поскольку me/mя 10 -5 10 -3, то We 1 10 э. В, W v 10 -2 10 -1 э. В, W r 10 -5 10 -3 э. В. то есть We W v W r. Электронная, колебательная и вращательная энергии молекулы квантуются и им соответствуют наборы дискретных энергетических уровней. Из теории и эксперимента следует, что расстояния между вращательными уровнями значительно меньше расстояния между колебательными уровнями, а расстояния между колебательными уровнями значительно меньше расстояния между электронными уровнями.
 Энергетические уровни двухатомной молекулы: При переходе с одного уровня на другой испускается или поглощается энергия Спектры излучения и поглощения молекул определяются структурой их энергетических уровней. Например, для вращательных спектров: В соответствии с правилом отбора J = 1. Тогда J 1 = J + 1 и J 2 = J. Спектр в этом случае имеет вид: Измеряя , можно определить момент инерции молекулы. Зная массу ядер, можно найти равновесное расстояние между ними в двухатомной молекуле.
Энергетические уровни двухатомной молекулы: При переходе с одного уровня на другой испускается или поглощается энергия Спектры излучения и поглощения молекул определяются структурой их энергетических уровней. Например, для вращательных спектров: В соответствии с правилом отбора J = 1. Тогда J 1 = J + 1 и J 2 = J. Спектр в этом случае имеет вид: Измеряя , можно определить момент инерции молекулы. Зная массу ядер, можно найти равновесное расстояние между ними в двухатомной молекуле.
 Спектр молекул довольно сложный. При разных типах переходов между энергетическими уровнями возникают различные типы молекулярных спектров - электронные, колебательные, вращательные, электронно-колебательные и колебательно вращательные. Типичные молекулярные спектры - полосатые, представляющие собой совокупность более или менее узких полос в ультрафиолетовой, видимой и инфракрасной областях. Спектр испускания молекул йода Чем больше атомов в молекуле, тем сложнее структура спектра. Колебательными и вращательными спектрами обладают только многоатомные молекулы. Электронно-колебательный молекулярный спектр Вращательное расщепление электронно-колебательной полосы
Спектр молекул довольно сложный. При разных типах переходов между энергетическими уровнями возникают различные типы молекулярных спектров - электронные, колебательные, вращательные, электронно-колебательные и колебательно вращательные. Типичные молекулярные спектры - полосатые, представляющие собой совокупность более или менее узких полос в ультрафиолетовой, видимой и инфракрасной областях. Спектр испускания молекул йода Чем больше атомов в молекуле, тем сложнее структура спектра. Колебательными и вращательными спектрами обладают только многоатомные молекулы. Электронно-колебательный молекулярный спектр Вращательное расщепление электронно-колебательной полосы
 Наличие колебательных и вращательных энергетических уровней молекул позволяет объяснить явление комбинационного рассеяния света, открытое в 1928 году советскими учёными Г. Е. Ландсбергом и Л. И. Мандельштамом, а также индийскими физиками Ч. Раманом и К. Кришнаном. Явление заключается в том, что монохроматический свет, падающий на вещество (газ, жидкость или прозрачный кристалл), рассеивается таким образом, что в его спектре, кроме основной спектральной линии, появляются новые. Частоты этих линий представляют собой суммы или разности частоты 0 падающего света и частот і собственных колебательных или вращательных переходов молекул рассеивающей среды. ( 0 - і) или фиолетовыми ( 0 + і) «спутниками» . Эти линии называются красными
Наличие колебательных и вращательных энергетических уровней молекул позволяет объяснить явление комбинационного рассеяния света, открытое в 1928 году советскими учёными Г. Е. Ландсбергом и Л. И. Мандельштамом, а также индийскими физиками Ч. Раманом и К. Кришнаном. Явление заключается в том, что монохроматический свет, падающий на вещество (газ, жидкость или прозрачный кристалл), рассеивается таким образом, что в его спектре, кроме основной спектральной линии, появляются новые. Частоты этих линий представляют собой суммы или разности частоты 0 падающего света и частот і собственных колебательных или вращательных переходов молекул рассеивающей среды. ( 0 - і) или фиолетовыми ( 0 + і) «спутниками» . Эти линии называются красными
 Согласно квантовой теории при поглощении света происходит неупругое столкновение фотонов с молекулами, при этом поглощается один фотон и испускается другой. Если энергия этих фотонов одинакова, то возникает основная линия. Если испускаемый фотон имеет меньшую энергию появляется красный спутник. Это означает, что происходит поглощение энергии, и молекула переходит в возбуждённое состояние. Если испускаемый фотон имеет большую энергию появляется фиолетовый спутник. Это означает, что происходит выделение энергии, и молекула переходит из возбуждённого состояния в нормальное. Изучая молекулярные спектры и спектры комбинационного рассеяния света, можно исследовать строение и свойства молекул. Эти методы используются в молекулярном спектральном анализе, в лазерной спектроскопии.
Согласно квантовой теории при поглощении света происходит неупругое столкновение фотонов с молекулами, при этом поглощается один фотон и испускается другой. Если энергия этих фотонов одинакова, то возникает основная линия. Если испускаемый фотон имеет меньшую энергию появляется красный спутник. Это означает, что происходит поглощение энергии, и молекула переходит в возбуждённое состояние. Если испускаемый фотон имеет большую энергию появляется фиолетовый спутник. Это означает, что происходит выделение энергии, и молекула переходит из возбуждённого состояния в нормальное. Изучая молекулярные спектры и спектры комбинационного рассеяния света, можно исследовать строение и свойства молекул. Эти методы используются в молекулярном спектральном анализе, в лазерной спектроскопии.
 Продолжение следует. . .
Продолжение следует. . .


