6ДЕ_квантовая и атомная физика.ppt
- Количество слайдов: 58
 КВАНТОВАЯ И АТОМНАЯ ФИЗИКА (6 дидактическая единица) Нельзя не знать
КВАНТОВАЯ И АТОМНАЯ ФИЗИКА (6 дидактическая единица) Нельзя не знать
 Нельзя не знать! 1. Спектр атома водорода (теория Бора) Постулаты Бора: ь Электроны в атоме могут находиться только в определенных стационарных состояниях, в которых электрон не излучает. ь При переходе электрона из одного стационарного состояния в другое атом излучает или поглощает порцию энергии E энергия электрона на m-ом и n-ом уровне ∞ – энергия излученного кванта при переходе с m-го уровня на n-ый. 4 3 Серия Пашена (ИК) 2 Серия Бальмера (видимый свет) – квант излучается – квант поглощается n=3 n=2 n=1 энергия радиус орбиты скорость электрона на n-ом уровне Серия Лаймана (УФ) 1 R = 2, 067· 1016 с− 1 – частота излученного кванта – постоянная Ридберга
Нельзя не знать! 1. Спектр атома водорода (теория Бора) Постулаты Бора: ь Электроны в атоме могут находиться только в определенных стационарных состояниях, в которых электрон не излучает. ь При переходе электрона из одного стационарного состояния в другое атом излучает или поглощает порцию энергии E энергия электрона на m-ом и n-ом уровне ∞ – энергия излученного кванта при переходе с m-го уровня на n-ый. 4 3 Серия Пашена (ИК) 2 Серия Бальмера (видимый свет) – квант излучается – квант поглощается n=3 n=2 n=1 энергия радиус орбиты скорость электрона на n-ом уровне Серия Лаймана (УФ) 1 R = 2, 067· 1016 с− 1 – частота излученного кванта – постоянная Ридберга
 Интернет-тесты n=1 Серия Лаймана hνmin=E 2 - E 1 =-3. 38 - (-13. 55) =10. 17 n=2 Серия Бальмера hνmax=E∞ - E 3 = 0 - (-3. 38) =3. 38 νmin/ νmax = 10. 17/3. 38 = 3
Интернет-тесты n=1 Серия Лаймана hνmin=E 2 - E 1 =-3. 38 - (-13. 55) =10. 17 n=2 Серия Бальмера hνmax=E∞ - E 3 = 0 - (-3. 38) =3. 38 νmin/ νmax = 10. 17/3. 38 = 3
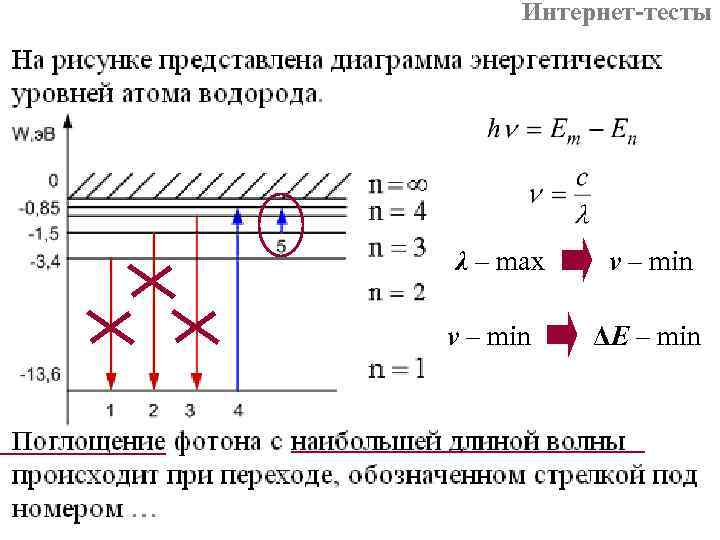 Интернет-тесты λ – max ν – min ΔE – min
Интернет-тесты λ – max ν – min ΔE – min

 Интернет-тесты Укажите, какому переходу соответствует: ь поглощение фотона с наибольшей длиной волны 5 ь поглощение фотона с наименьшей длиной волны 4 ь испускание фотона с наибольшей длиной волны 1 ь испускание фотона с наименьшей длиной волны 3 ь испускание фотона с максимальной энергией 3 ь испускание фотона с минимальной энергией 1
Интернет-тесты Укажите, какому переходу соответствует: ь поглощение фотона с наибольшей длиной волны 5 ь поглощение фотона с наименьшей длиной волны 4 ь испускание фотона с наибольшей длиной волны 1 ь испускание фотона с наименьшей длиной волны 3 ь испускание фотона с максимальной энергией 3 ь испускание фотона с минимальной энергией 1
 Интернет-тесты n=2 Серия Бальмера hν – min
Интернет-тесты n=2 Серия Бальмера hν – min
 Интернет-тесты n=1 Серия Лаймана
Интернет-тесты n=1 Серия Лаймана
 Интернет-тесты n=1 Серия Лаймана hν – min
Интернет-тесты n=1 Серия Лаймана hν – min
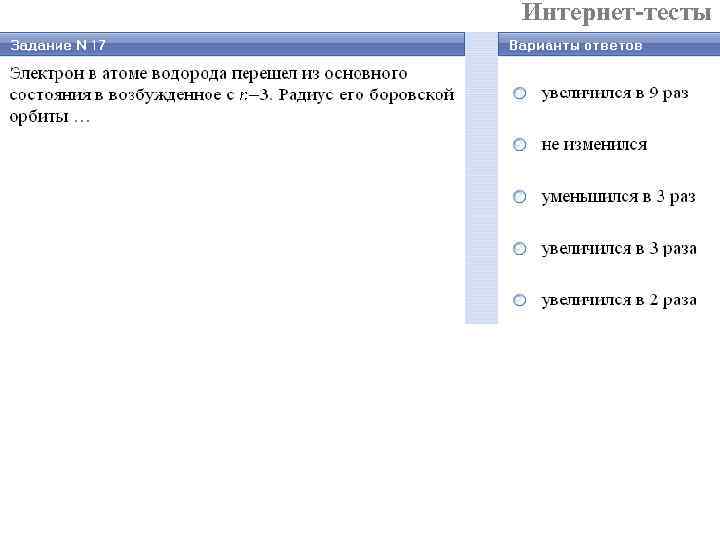 Интернет-тесты n 1=1 n 2=3
Интернет-тесты n 1=1 n 2=3
 2. Дуализм свойств микрочастиц – длина волны де Бройля Нельзя не знать! – импульс частицы h=6. 62· 10 -34 Дж·с– постоянная Планка чем меньше масса чатицы, тем более mv ↑ λ ↓ выражены её волновые свойствва Волновые и карпускулярные свойства одновременно не проявляются! – принцип неопределенности Гейзенберга Δx – неопределённость в определении координаты частицы Δpx – неопределённость в определении проекции импульса частицы – принцип неопределенности Гейзенберга ΔE – неопределённость энергии некоторого состояния системы Δt – промежуток времени, в течение которого это состояние существует
2. Дуализм свойств микрочастиц – длина волны де Бройля Нельзя не знать! – импульс частицы h=6. 62· 10 -34 Дж·с– постоянная Планка чем меньше масса чатицы, тем более mv ↑ λ ↓ выражены её волновые свойствва Волновые и карпускулярные свойства одновременно не проявляются! – принцип неопределенности Гейзенберга Δx – неопределённость в определении координаты частицы Δpx – неопределённость в определении проекции импульса частицы – принцип неопределенности Гейзенберга ΔE – неопределённость энергии некоторого состояния системы Δt – промежуток времени, в течение которого это состояние существует
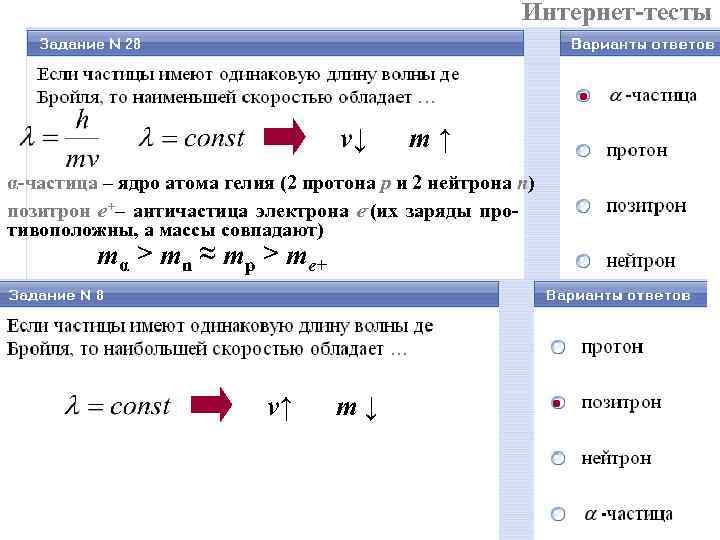 Интернет-тесты v↓ m↑ α-частица – ядро атома гелия (2 протона p и 2 нейтрона n) позитрон e+– античастица электрона e-(их заряды противоположны, а массы совпадают) mα > mn ≈ mp > me+ v↑ m↓
Интернет-тесты v↓ m↑ α-частица – ядро атома гелия (2 протона p и 2 нейтрона n) позитрон e+– античастица электрона e-(их заряды противоположны, а массы совпадают) mα > mn ≈ mp > me+ v↑ m↓
 Интернет-тесты m↓ mα > mn ≈ mp > me- m↑ λ↓ λ↑
Интернет-тесты m↓ mα > mn ≈ mp > me- m↑ λ↓ λ↑
 Интернет-тесты
Интернет-тесты
 Интернет-тесты λ n= λ α Если протон и нейтрон двигаются с одинаковыми скоростями, то отношения их длин волн де Бройля λp/λn равно… λ n= λ p 4 3
Интернет-тесты λ n= λ α Если протон и нейтрон двигаются с одинаковыми скоростями, то отношения их длин волн де Бройля λp/λn равно… λ n= λ p 4 3
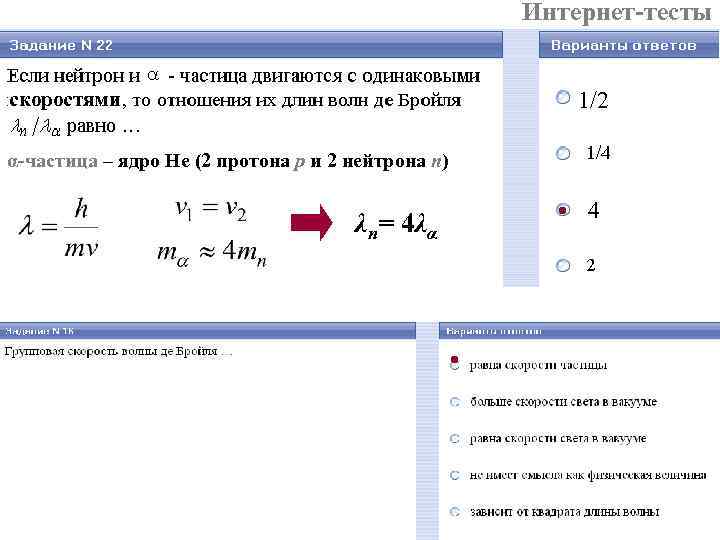 Интернет-тесты 1/2 скоростями α-частица – ядро He (2 протона p и 2 нейтрона n) λn= 4λα 4
Интернет-тесты 1/2 скоростями α-частица – ядро He (2 протона p и 2 нейтрона n) λn= 4λα 4
 Интернет-тесты
Интернет-тесты
 Интернет-тесты
Интернет-тесты
 3. Уравнение Шрёдингера Нельзя не знать! – общее уравнение Шрёдингера – мнимая единица – постоянная Планка – оператор Лапласа в одномерном случае: U(x, y, z, t)–потенциальная энергия частицы в силовом поле Ψ – волновая функция m – масса частицы – вероятность обнаружить частицу в объеме V
3. Уравнение Шрёдингера Нельзя не знать! – общее уравнение Шрёдингера – мнимая единица – постоянная Планка – оператор Лапласа в одномерном случае: U(x, y, z, t)–потенциальная энергия частицы в силовом поле Ψ – волновая функция m – масса частицы – вероятность обнаружить частицу в объеме V
 Нельзя не знать! – общее (временное) уравнение Шрёдингера – стационарное уравнение Шрёдингера E – полная энергия электрона в атоме. – стационарное уравнение Шрёдингера для водородоподобных атомов – стационарное уравнение Шрёдингера для гармонического осциллятора – стационарное уравнение Шрёдингера для частицы в одномерной потенциальной яме
Нельзя не знать! – общее (временное) уравнение Шрёдингера – стационарное уравнение Шрёдингера E – полная энергия электрона в атоме. – стационарное уравнение Шрёдингера для водородоподобных атомов – стационарное уравнение Шрёдингера для гармонического осциллятора – стационарное уравнение Шрёдингера для частицы в одномерной потенциальной яме
 Интернет-тесты
Интернет-тесты
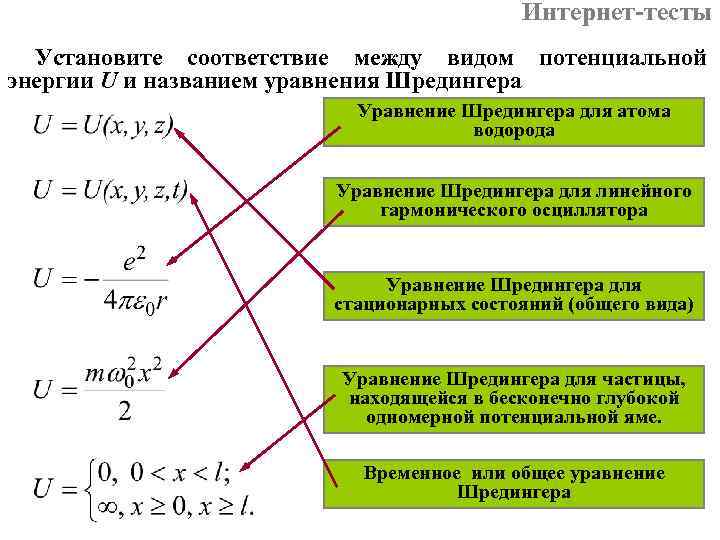 Интернет-тесты Установите соответствие между видом потенциальной энергии U и названием уравнения Шредингера Уравнение Шредингера для атома водорода Уравнение Шредингера для линейного гармонического осциллятора Уравнение Шредингера для стационарных состояний (общего вида) Уравнение Шредингера для частицы, находящейся в бесконечно глубокой одномерной потенциальной яме. Временное или общее уравнение Шредингера
Интернет-тесты Установите соответствие между видом потенциальной энергии U и названием уравнения Шредингера Уравнение Шредингера для атома водорода Уравнение Шредингера для линейного гармонического осциллятора Уравнение Шредингера для стационарных состояний (общего вида) Уравнение Шредингера для частицы, находящейся в бесконечно глубокой одномерной потенциальной яме. Временное или общее уравнение Шредингера
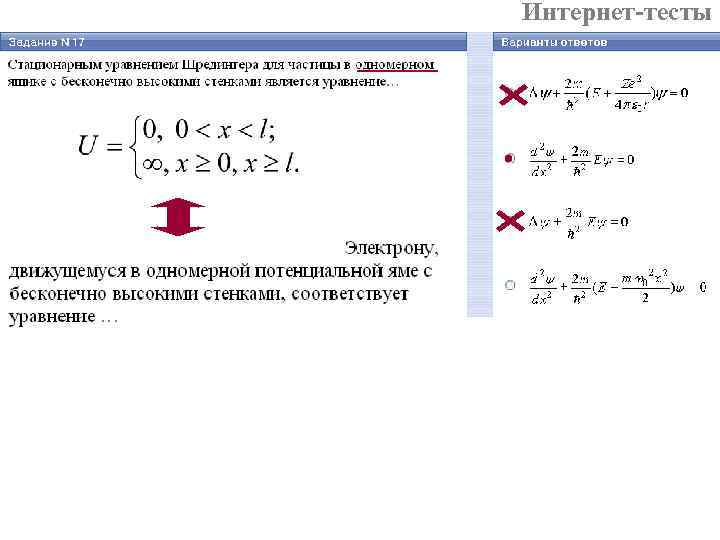 Интернет-тесты
Интернет-тесты
 Интернет-тесты для водорода Z=0
Интернет-тесты для водорода Z=0
 Интернет-тесты
Интернет-тесты
 Интернет-тесты
Интернет-тесты
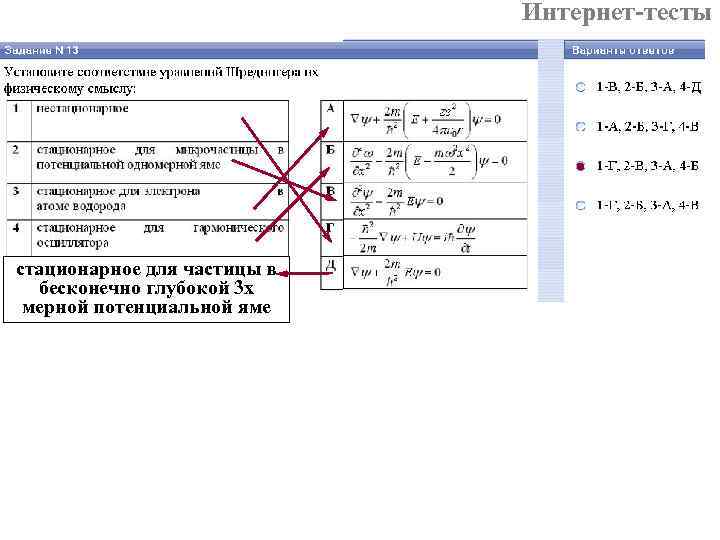 Интернет-тесты стационарное для частицы в ? бесконечно глубокой 3 х мерной потенциальной яме
Интернет-тесты стационарное для частицы в ? бесконечно глубокой 3 х мерной потенциальной яме
 Интернет-тесты U – не зависит от времени уравнение одномерное U =0
Интернет-тесты U – не зависит от времени уравнение одномерное U =0
 Интернет-тесты II U – не зависит от времени уравнение одномерное U =U 0
Интернет-тесты II U – не зависит от времени уравнение одномерное U =U 0
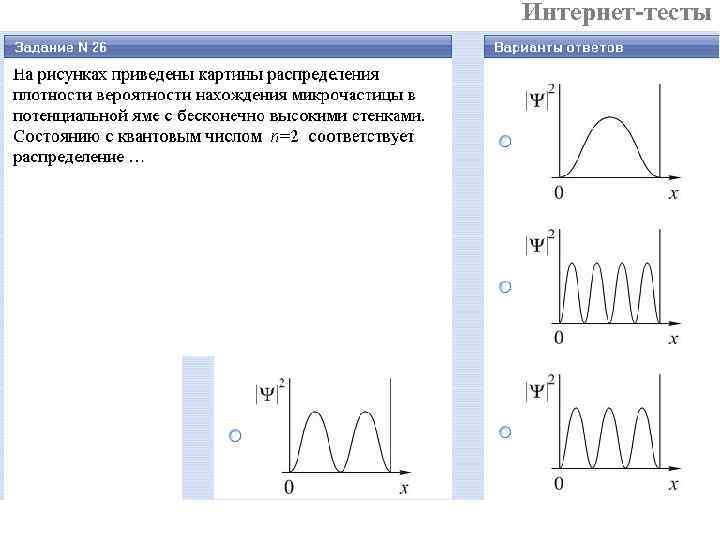
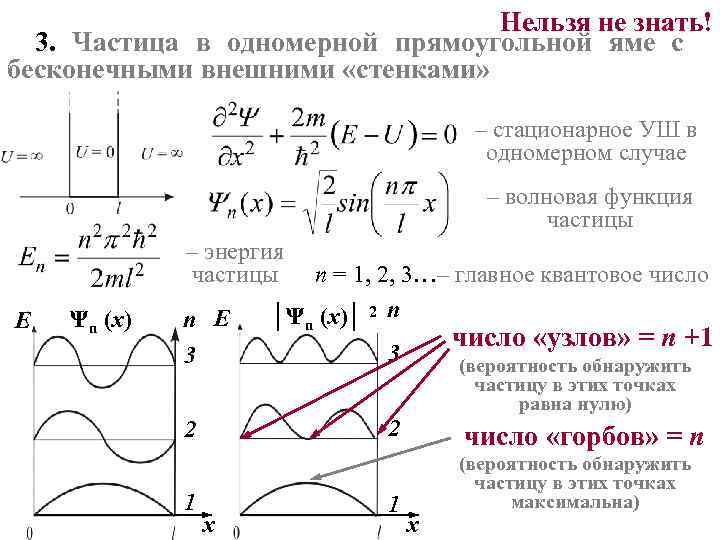 Нельзя не знать! 3. Частица в одномерной прямоугольной яме с бесконечными внешними «стенками» – стационарное УШ в одномерном случае – волновая функция частицы – энергия частицы E Ψn (x) n E 3 число «узлов» = n +1 3 (вероятность обнаружить частицу в этих точках равна нулю) 2 2 1 n = 1, 2, 3…– главное квантовое число │Ψn (x)│ 2 n x 1 число «горбов» = n x (вероятность обнаружить частицу в этих точках максимальна)
Нельзя не знать! 3. Частица в одномерной прямоугольной яме с бесконечными внешними «стенками» – стационарное УШ в одномерном случае – волновая функция частицы – энергия частицы E Ψn (x) n E 3 число «узлов» = n +1 3 (вероятность обнаружить частицу в этих точках равна нулю) 2 2 1 n = 1, 2, 3…– главное квантовое число │Ψn (x)│ 2 n x 1 число «горбов» = n x (вероятность обнаружить частицу в этих точках максимальна)
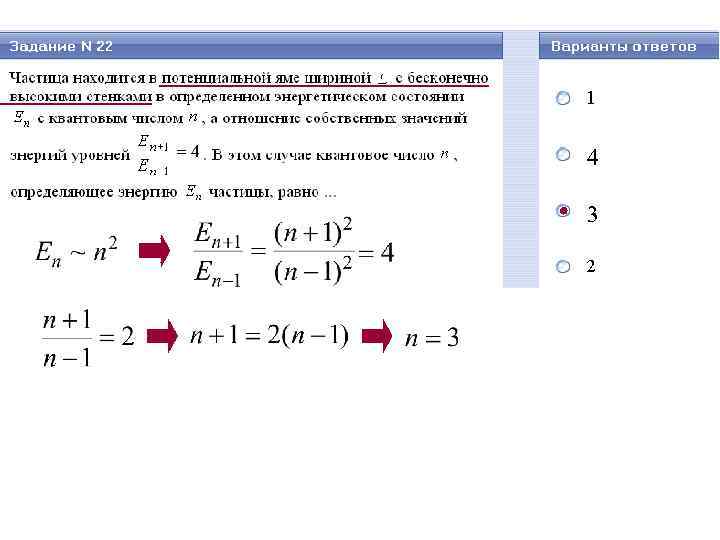 4 3
4 3
 4 3
4 3
 Интернет-тесты
Интернет-тесты
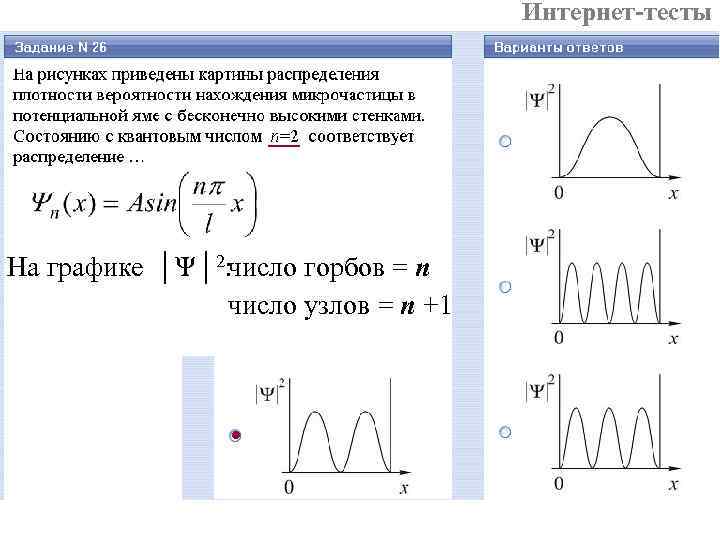 Интернет-тесты На графике │Ψ│2: число горбов = n число узлов = n +1
Интернет-тесты На графике │Ψ│2: число горбов = n число узлов = n +1
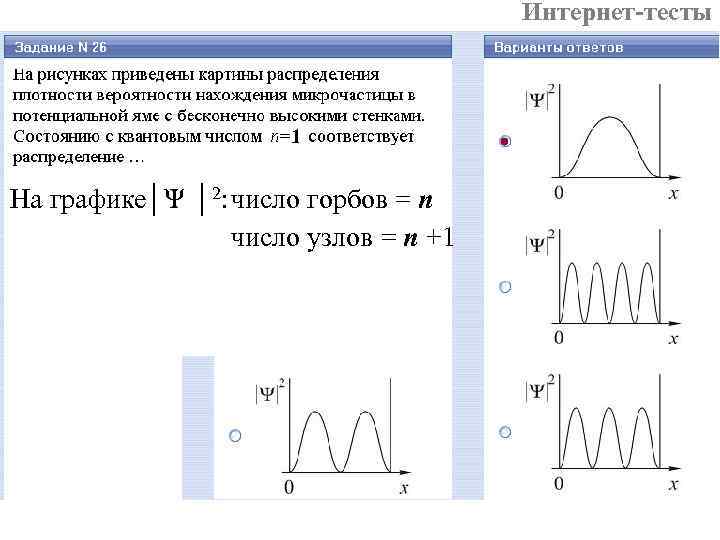 Интернет-тесты 1 На графике│Ψ │2: число горбов = n число узлов = n +1
Интернет-тесты 1 На графике│Ψ │2: число горбов = n число узлов = n +1
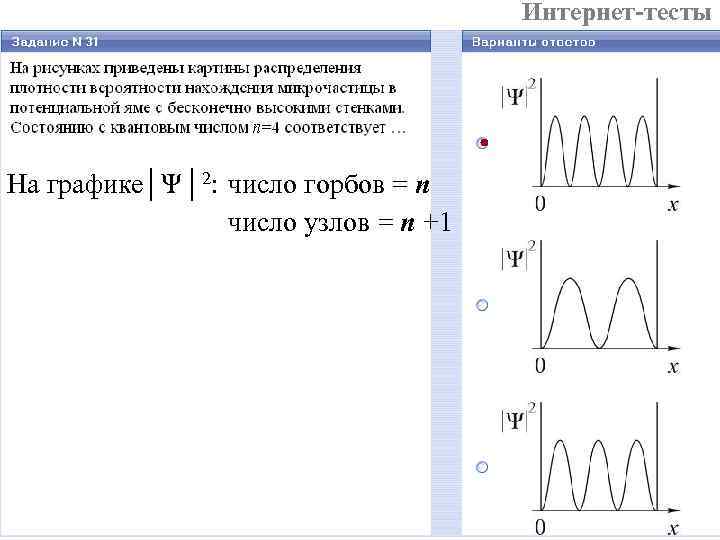 Интернет-тесты На графике│Ψ│2: число горбов = n число узлов = n +1
Интернет-тесты На графике│Ψ│2: число горбов = n число узлов = n +1
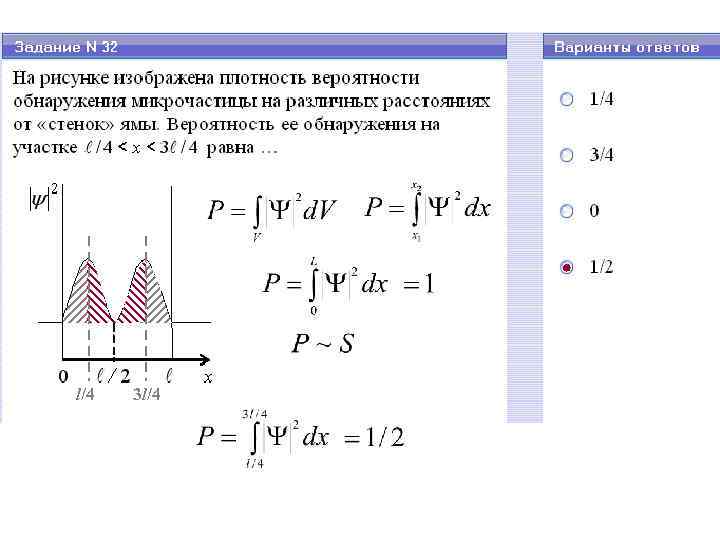 l/4 3 l/4
l/4 3 l/4
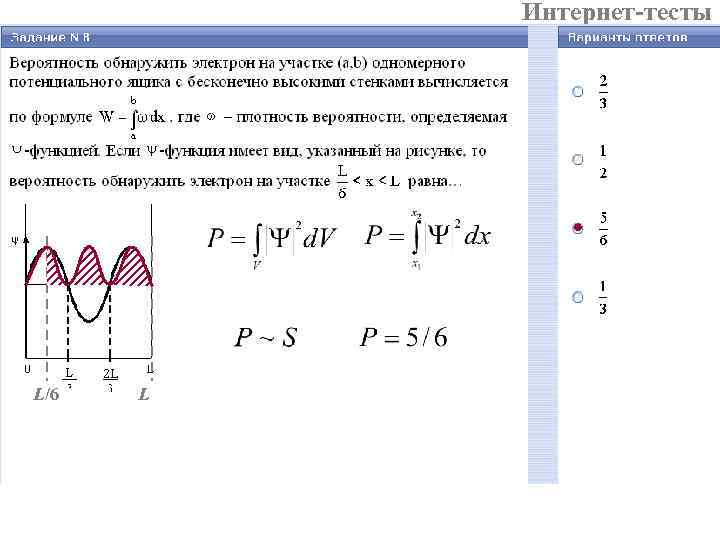 Интернет-тесты L/6 L
Интернет-тесты L/6 L
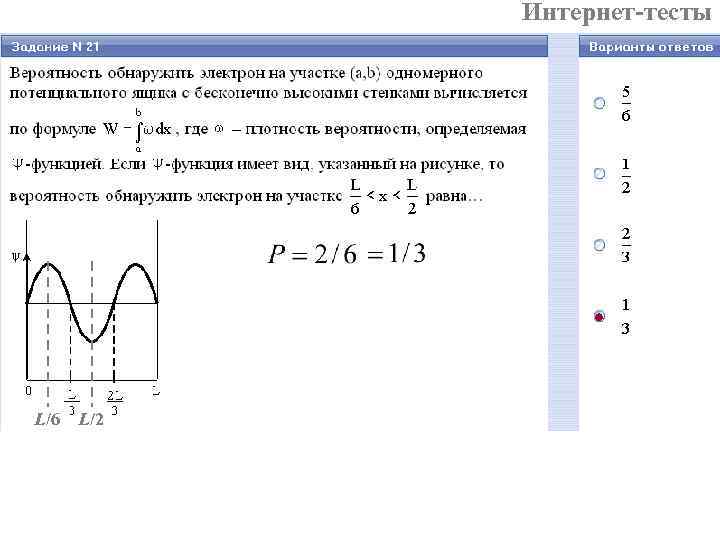 Интернет-тесты L/6 L/2
Интернет-тесты L/6 L/2
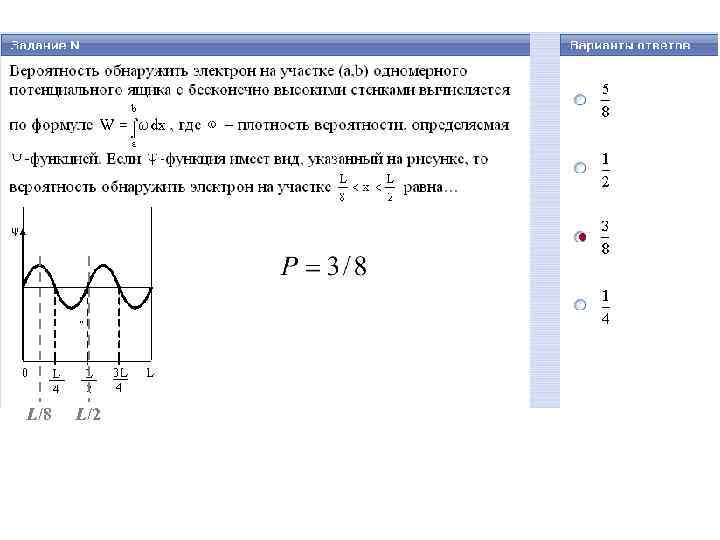 L/8 L/2
L/8 L/2
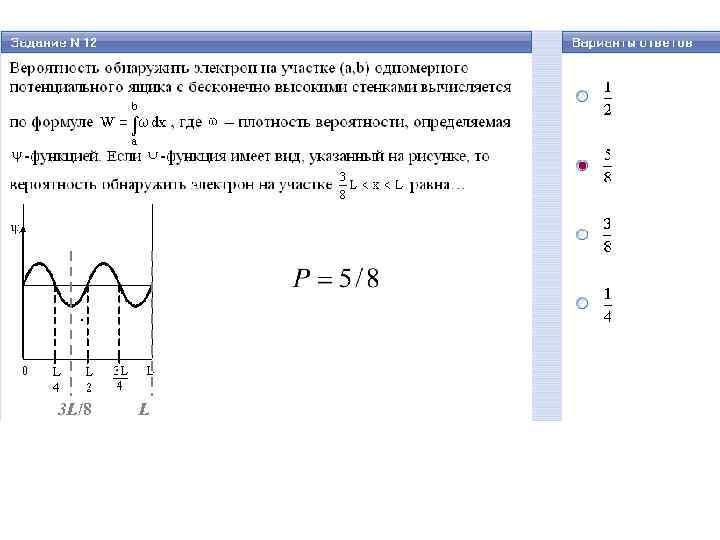 3 L/8 L
3 L/8 L
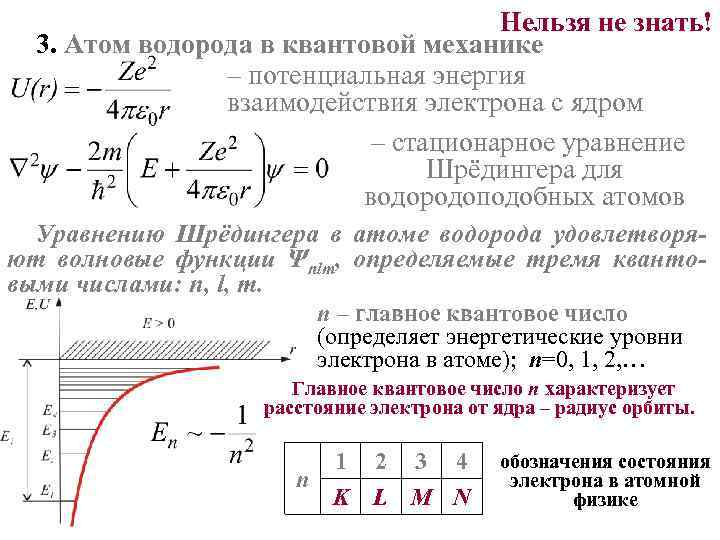 Нельзя не знать! 3. Атом водорода в квантовой механике – потенциальная энергия взаимодействия электрона с ядром – стационарное уравнение Шрёдингера для водородоподобных атомов Уравнению Шрёдингера в атоме водорода удовлетворяют волновые функции Ψnlm, определяемые тремя квантовыми числами: n, l, m. n – главное квантовое число (определяет энергетические уровни электрона в атоме); n=0, 1, 2, … Главное квантовое число n характеризует расстояние электрона от ядра – радиус орбиты. 1 n K 2 3 4 L M N обозначения состояния электрона в атомной физике
Нельзя не знать! 3. Атом водорода в квантовой механике – потенциальная энергия взаимодействия электрона с ядром – стационарное уравнение Шрёдингера для водородоподобных атомов Уравнению Шрёдингера в атоме водорода удовлетворяют волновые функции Ψnlm, определяемые тремя квантовыми числами: n, l, m. n – главное квантовое число (определяет энергетические уровни электрона в атоме); n=0, 1, 2, … Главное квантовое число n характеризует расстояние электрона от ядра – радиус орбиты. 1 n K 2 3 4 L M N обозначения состояния электрона в атомной физике
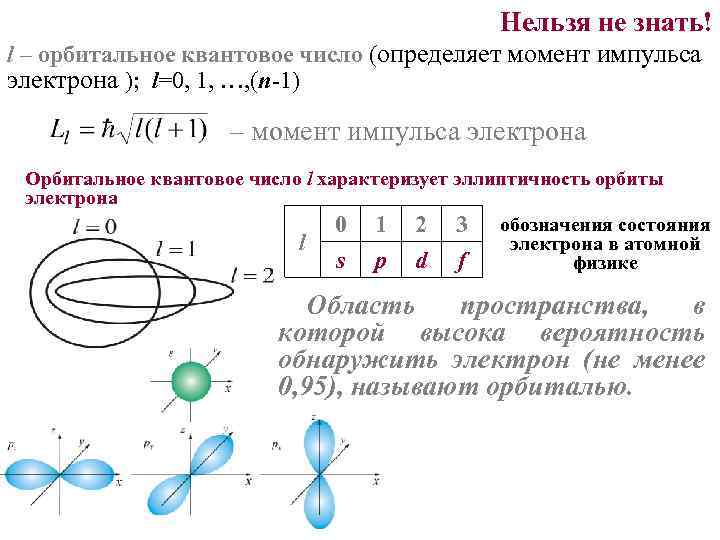 Нельзя не знать! l – орбитальное квантовое число (определяет момент импульса электрона ); l=0, 1, …, (n-1) – момент импульса электрона Орбитальное квантовое число l характеризует эллиптичность орбиты электрона 0 1 2 3 обозначения состояния l электрона в атомной s p d f физике Область пространства, в которой высока вероятность обнаружить электрон (не менее 0, 95), называют орбиталью.
Нельзя не знать! l – орбитальное квантовое число (определяет момент импульса электрона ); l=0, 1, …, (n-1) – момент импульса электрона Орбитальное квантовое число l характеризует эллиптичность орбиты электрона 0 1 2 3 обозначения состояния l электрона в атомной s p d f физике Область пространства, в которой высока вероятность обнаружить электрон (не менее 0, 95), называют орбиталью.
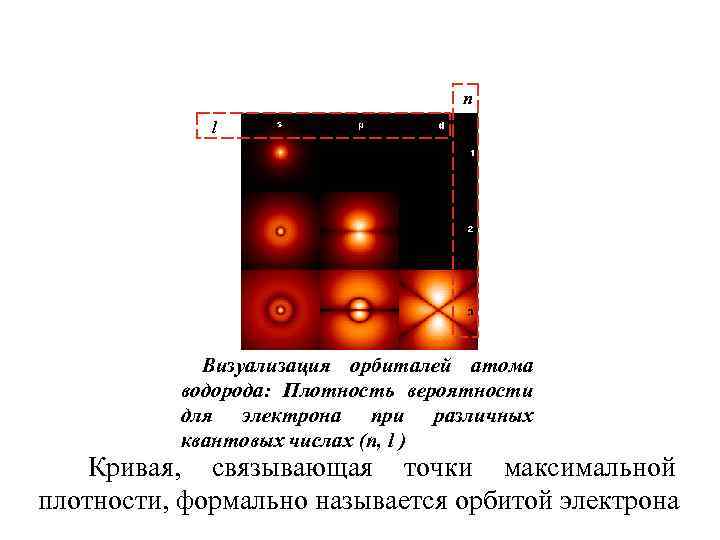 n l Визуализация орбиталей атома водорода: Плотность вероятности для электрона при различных квантовых числах (n, l ) Кривая, связывающая точки максимальной плотности, формально называется орбитой электрона
n l Визуализация орбиталей атома водорода: Плотность вероятности для электрона при различных квантовых числах (n, l ) Кривая, связывающая точки максимальной плотности, формально называется орбитой электрона
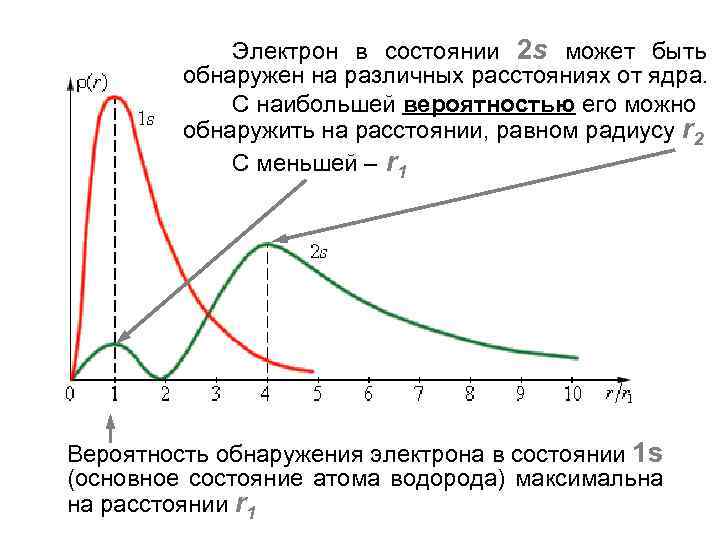 Электрон в состоянии 2 s может быть обнаружен на различных расстояниях от ядра. С наибольшей вероятностью его можно обнаружить на расстоянии, равном радиусу r 2 С меньшей – r 1 Вероятность обнаружения электрона в состоянии 1 s (основное состояние атома водорода) максимальна на расстоянии r 1
Электрон в состоянии 2 s может быть обнаружен на различных расстояниях от ядра. С наибольшей вероятностью его можно обнаружить на расстоянии, равном радиусу r 2 С меньшей – r 1 Вероятность обнаружения электрона в состоянии 1 s (основное состояние атома водорода) максимальна на расстоянии r 1
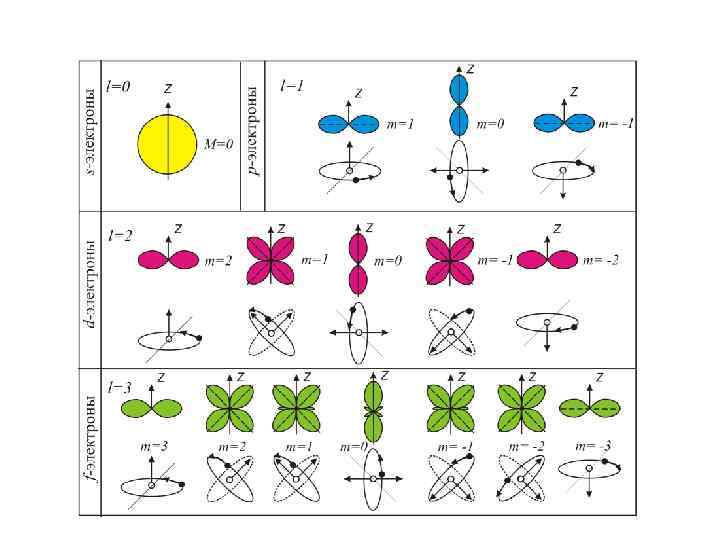
 Нельзя не знать! m – магнитное квантовое число (определяет проекцию момента импульса электрона на заданное направление); m=0, ± 1, ± 2, …, ±l – проекция момента импульса на направление внешнего поля Магнитное квантовое число m характеризует ориентацию электронного облака в пространстве Возможные ориентации вектора L в состояниях s, p, d.
Нельзя не знать! m – магнитное квантовое число (определяет проекцию момента импульса электрона на заданное направление); m=0, ± 1, ± 2, …, ±l – проекция момента импульса на направление внешнего поля Магнитное квантовое число m характеризует ориентацию электронного облака в пространстве Возможные ориентации вектора L в состояниях s, p, d.
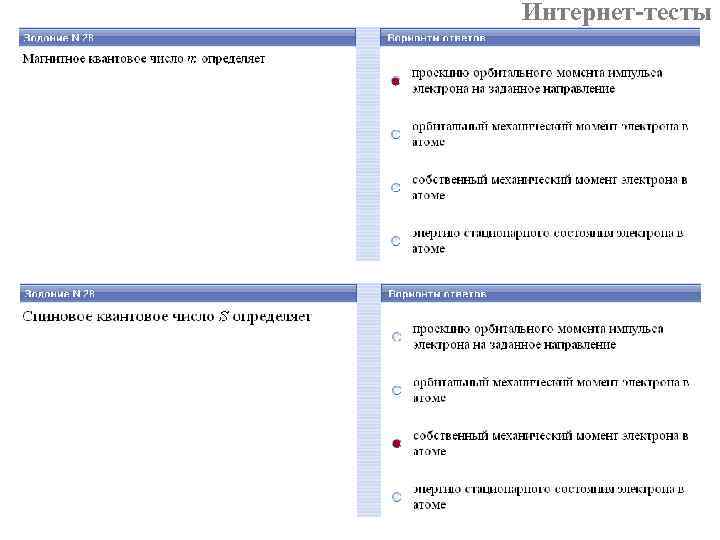
 Интернет-тесты спиновое квантовое число (спин)
Интернет-тесты спиновое квантовое число (спин)
 Интернет-тесты
Интернет-тесты
 Интернет-тесты На рисунке приведена одна из возможных ориентации момента импульса электрона в р состоянии. Какие еще значения может принимать проекция момента импульса на направление Z внешнего магнитного поля? • 2ћ Lz=ћm – проекция момента импульса электрона на • -2ћ направление внешнего магнитного поля m=0, ± 1, ± 2, …, ±l – магнитное квантовое число • - ћ • 0 На рисунке приведены некоторые из возможных ориентации момента импульса доя электронов в dсостоянии. Какие еще значения может принимать проекция момента импульса на направление Z внешнего магнитного поля? • 3ћ • -2ћ • - ћ
Интернет-тесты На рисунке приведена одна из возможных ориентации момента импульса электрона в р состоянии. Какие еще значения может принимать проекция момента импульса на направление Z внешнего магнитного поля? • 2ћ Lz=ћm – проекция момента импульса электрона на • -2ћ направление внешнего магнитного поля m=0, ± 1, ± 2, …, ±l – магнитное квантовое число • - ћ • 0 На рисунке приведены некоторые из возможных ориентации момента импульса доя электронов в dсостоянии. Какие еще значения может принимать проекция момента импульса на направление Z внешнего магнитного поля? • 3ћ • -2ћ • - ћ
 Интернет-тесты K-оболочка n=1 L-оболочка n=2 Первый n=1 и второй n=2 энергетические уровни полностью заполнены 8 10 18 Принцип Паули: в пределах одной квантовой системы в данном квантовом состоянии может находиться только один фермион. Состояние электрона в атоме определяется квантовыми числами: n, l, m, s. l=0, 1, …, (n-1) n=1 l=0 m=0 n=2 l=0 m=0 l=1 m=0 m=+1 m=-1 m=0, ± 1, ± 2, …, ±l s= ± 1/2 число s= ± 1/2 2 электрона электронов на s= ± 1/2 2 электрона n-ом уровне: Z(n)=2 n 2 s= ± 1/2 2 электрона Zобщ=2+2· 22 s= ± 1/2 2 электрона s= ± 1/2
Интернет-тесты K-оболочка n=1 L-оболочка n=2 Первый n=1 и второй n=2 энергетические уровни полностью заполнены 8 10 18 Принцип Паули: в пределах одной квантовой системы в данном квантовом состоянии может находиться только один фермион. Состояние электрона в атоме определяется квантовыми числами: n, l, m, s. l=0, 1, …, (n-1) n=1 l=0 m=0 n=2 l=0 m=0 l=1 m=0 m=+1 m=-1 m=0, ± 1, ± 2, …, ±l s= ± 1/2 число s= ± 1/2 2 электрона электронов на s= ± 1/2 2 электрона n-ом уровне: Z(n)=2 n 2 s= ± 1/2 2 электрона Zобщ=2+2· 22 s= ± 1/2 2 электрона s= ± 1/2
 Интернет-тесты главное квантовое число электронов 1 s 2 2 p 6 3 s 1 валентный электрон орбитальное квантовое число В стационарном состоянии электроны находятся на нижних энергетических уровнях. Валентный электрон находится на внешней оболочке атома. n=3 s l=0
Интернет-тесты главное квантовое число электронов 1 s 2 2 p 6 3 s 1 валентный электрон орбитальное квантовое число В стационарном состоянии электроны находятся на нижних энергетических уровнях. Валентный электрон находится на внешней оболочке атома. n=3 s l=0
 Интернет-тесты орбитальные квантовые числа l s: l=0 d: l=2 p: l=1 f: l=3 Правило отбора: Δl = ± 1 главные квантовые числа n
Интернет-тесты орбитальные квантовые числа l s: l=0 d: l=2 p: l=1 f: l=3 Правило отбора: Δl = ± 1 главные квантовые числа n
 Интернет-тесты s: l=0 d: l=2 p: l=1 f: l=3 Правило отбора: Δl = ± 1
Интернет-тесты s: l=0 d: l=2 p: l=1 f: l=3 Правило отбора: Δl = ± 1
 Интернет-тесты s: l=0 d: l=2 p: l=1 f: l=3 Правило отбора: Δl = ± 1
Интернет-тесты s: l=0 d: l=2 p: l=1 f: l=3 Правило отбора: Δl = ± 1

 Интернет-тесты k =0, 1, 2…
Интернет-тесты k =0, 1, 2…


