Квантовая Физика Сотников Д. 11 Б.ppt
- Количество слайдов: 21
 КВАНТОВАЯ ФИЗИКА Ква нтовая фи зика — раздел теоретической физики, в котором изучаются квантовомеханические и квантовополевые системы и законы их движения.
КВАНТОВАЯ ФИЗИКА Ква нтовая фи зика — раздел теоретической физики, в котором изучаются квантовомеханические и квантовополевые системы и законы их движения.
 Световые кванты Величайшая революция в физике совпала с началом 20 века. Попытки объяснить закономерности распределения энергии во время теплового (электромагнитного) излучения нагретого тела оказались несостоятельными (для них не подходили законы электромагнетизма Максвелла). Выход нашел немецкий физик Макс Планк (1858 -1947).
Световые кванты Величайшая революция в физике совпала с началом 20 века. Попытки объяснить закономерности распределения энергии во время теплового (электромагнитного) излучения нагретого тела оказались несостоятельными (для них не подходили законы электромагнетизма Максвелла). Выход нашел немецкий физик Макс Планк (1858 -1947).

 А. Эйнштейн дополнил гипотезу М. Планка: свет не только излучается отдельными порциями, но и поглощается тоже порциями (квантами), при чем порция света поглощается целиком. Электрон поглощает квант света и расходует энергию этого кванта на выход (1905 год).
А. Эйнштейн дополнил гипотезу М. Планка: свет не только излучается отдельными порциями, но и поглощается тоже порциями (квантами), при чем порция света поглощается целиком. Электрон поглощает квант света и расходует энергию этого кванта на выход (1905 год).
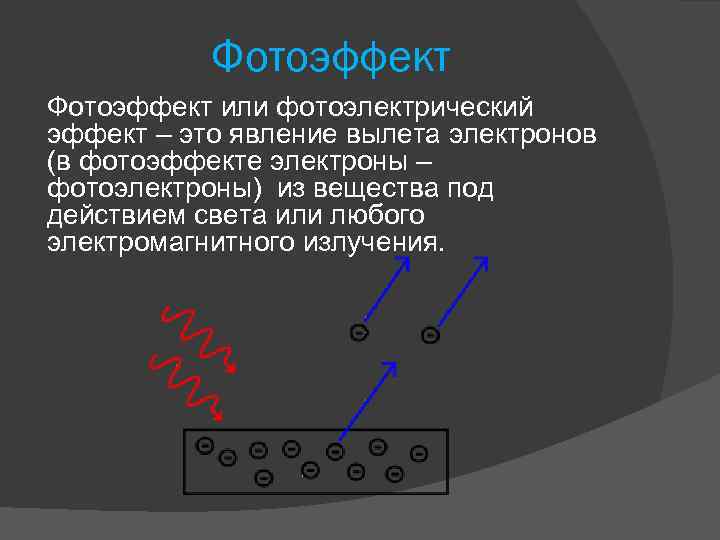 Фотоэффект или фотоэлектрический эффект – это явление вылета электронов (в фотоэффекте электроны – фотоэлектроны) из вещества под действием света или любого электромагнитного излучения.
Фотоэффект или фотоэлектрический эффект – это явление вылета электронов (в фотоэффекте электроны – фотоэлектроны) из вещества под действием света или любого электромагнитного излучения.
 Законы фотоэффекта
Законы фотоэффекта
 Основные формулы фотоэффекта
Основные формулы фотоэффекта

 Фотоны Фото н — элементарная частица, квант электромагнитного излучения (в узком смысле — света). Это безмассовая частица, способная существовать только двигаясь со скоростью света. Электрический заряд фотона также равен нулю.
Фотоны Фото н — элементарная частица, квант электромагнитного излучения (в узком смысле — света). Это безмассовая частица, способная существовать только двигаясь со скоростью света. Электрический заряд фотона также равен нулю.
 Фотоны Ф – образует инфракрасное излучение (величина фотона наименьшая) Ф Ф Ф Ф - образует ультрафиолетовое излучение (величина фотона набольшая)
Фотоны Ф – образует инфракрасное излучение (величина фотона наименьшая) Ф Ф Ф Ф - образует ультрафиолетовое излучение (величина фотона набольшая)
 Характеристики фотона
Характеристики фотона
 Свойство света, применимое к фотонам Свет обладает корпускулярно – волновым дуализмом (любой объект может проявлять как волновые, так и корпускулярные свойства): - при распространении свет ведет себя как волна - при излучении и поглощении свет ведет себя как поток частиц (фотонов или квантов)
Свойство света, применимое к фотонам Свет обладает корпускулярно – волновым дуализмом (любой объект может проявлять как волновые, так и корпускулярные свойства): - при распространении свет ведет себя как волна - при излучении и поглощении свет ведет себя как поток частиц (фотонов или квантов)
 Атомная физика Строение атома. Модель Томсона Не сразу ученые пришли к правильному представлению о строении атома. Первую модель атома предложил английский физик Дж. Томсон, открывшим электрон. Он предложил рассматривать атом как некоторое положительно заряженное тело с заключёнными внутри него электронами. Но это противоречило уже известным свойствам атома.
Атомная физика Строение атома. Модель Томсона Не сразу ученые пришли к правильному представлению о строении атома. Первую модель атома предложил английский физик Дж. Томсон, открывшим электрон. Он предложил рассматривать атом как некоторое положительно заряженное тело с заключёнными внутри него электронами. Но это противоречило уже известным свойствам атома.
 Атом в целом нейтрален, следовательно, основная масса атома приходится на его положительно заряженную часть. Для исследования распределения положительного заряда и массы внутри атома Эрнест Резерфорд предложил в 1906 году применить зондирование атома с помощью альфа-частиц.
Атом в целом нейтрален, следовательно, основная масса атома приходится на его положительно заряженную часть. Для исследования распределения положительного заряда и массы внутри атома Эрнест Резерфорд предложил в 1906 году применить зондирование атома с помощью альфа-частиц.
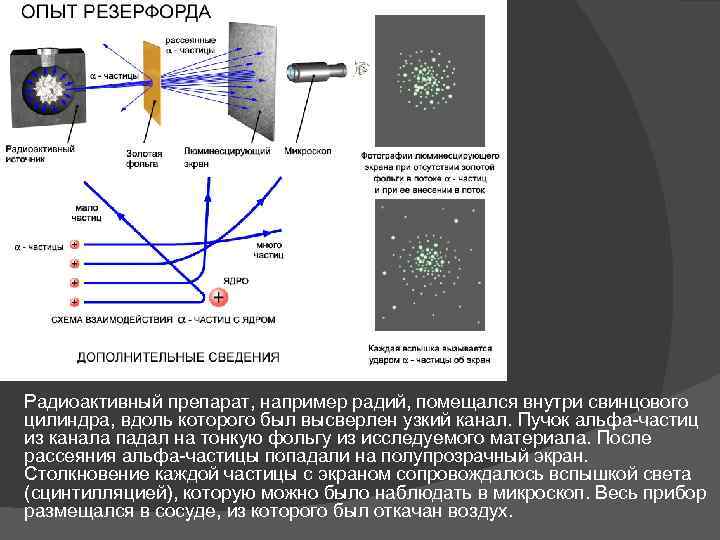 Радиоактивный препарат, например радий, помещался внутри свинцового цилиндра, вдоль которого был высверлен узкий канал. Пучок альфа-частиц из канала падал на тонкую фольгу из исследуемого материала. После рассеяния альфа-частицы попадали на полупрозрачный экран. Столкновение каждой частицы с экраном сопровождалось вспышкой света (сцинтилляцией), которую можно было наблюдать в микроскоп. Весь прибор размещался в сосуде, из которого был откачан воздух.
Радиоактивный препарат, например радий, помещался внутри свинцового цилиндра, вдоль которого был высверлен узкий канал. Пучок альфа-частиц из канала падал на тонкую фольгу из исследуемого материала. После рассеяния альфа-частицы попадали на полупрозрачный экран. Столкновение каждой частицы с экраном сопровождалось вспышкой света (сцинтилляцией), которую можно было наблюдать в микроскоп. Весь прибор размещался в сосуде, из которого был откачан воздух.
 Модифицируя экспериментальную установку, Резерфорд попытался обнаружить отклонение альфа-частиц на большие углы. Оказалось, что небольшое число альфа-частиц отклонилось на углы, большие 90 градусов. Это позволило понять, что частицы могли быть отброшены назад лишь в том случае, если положительный заряд атома и его масса сконцентрированы в очень малой области пространства. Так Резерфорд пришел к мысли о существовании атомного ядра.
Модифицируя экспериментальную установку, Резерфорд попытался обнаружить отклонение альфа-частиц на большие углы. Оказалось, что небольшое число альфа-частиц отклонилось на углы, большие 90 градусов. Это позволило понять, что частицы могли быть отброшены назад лишь в том случае, если положительный заряд атома и его масса сконцентрированы в очень малой области пространства. Так Резерфорд пришел к мысли о существовании атомного ядра.
 Планетарная модель атома В центре атома находится ядро. Вокруг ядра вращаются электроны: - ядро имеет положительный (+) заряд; - электроны имеют отрицательный (-) заряд; - заряд ядра равен заряду электронов (число протонов = число электронов); - масса атома сосредоточена в ядре; - заряд атома равен нулю
Планетарная модель атома В центре атома находится ядро. Вокруг ядра вращаются электроны: - ядро имеет положительный (+) заряд; - электроны имеют отрицательный (-) заряд; - заряд ядра равен заряду электронов (число протонов = число электронов); - масса атома сосредоточена в ядре; - заряд атома равен нулю
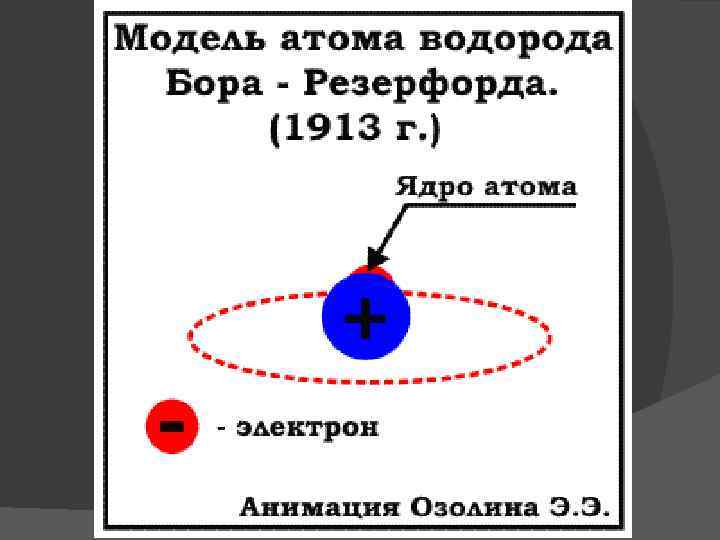
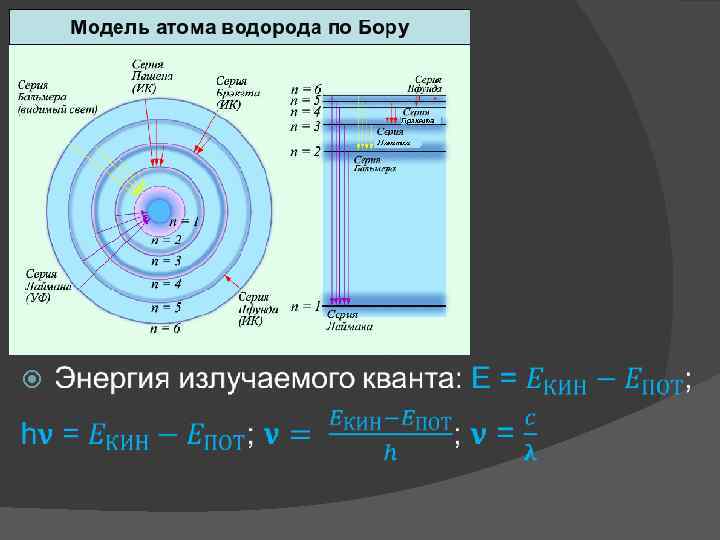
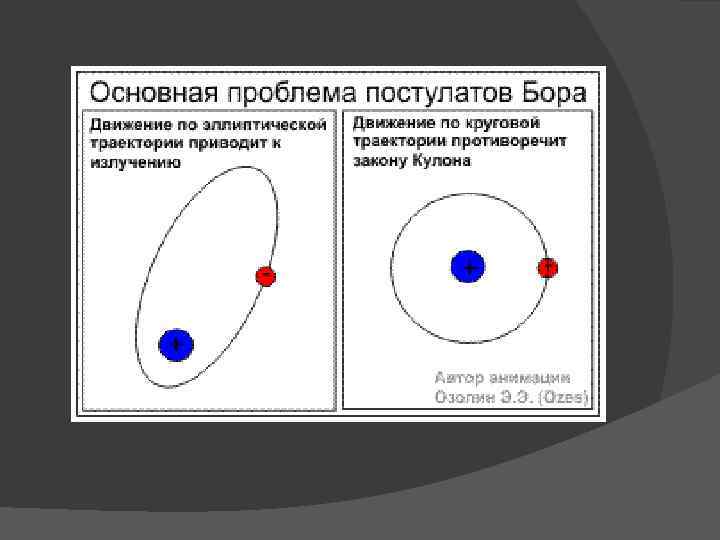
 Квантовые постулаты Бора Датский физик Бор Нильс сформулировал основные положения новой теории в виде постулатов: 1) Атомная система может находиться лишь в строго определенных стационарных состояниях, при этом атом не излучает и не поглощает энергию; 2) При переходе из одного стационарного состояния в другое атом излучает или поглощает один квант энергии
Квантовые постулаты Бора Датский физик Бор Нильс сформулировал основные положения новой теории в виде постулатов: 1) Атомная система может находиться лишь в строго определенных стационарных состояниях, при этом атом не излучает и не поглощает энергию; 2) При переходе из одного стационарного состояния в другое атом излучает или поглощает один квант энергии