Гальванический элемент.ppt
- Количество слайдов: 56

Курский государственный медицинский университет Кафедра общей химии Гальванический элемент © Лектор доцент кафедры общей химии к. х. н. Оксененко О. И.

План 1. Основные понятия. 2. Уравнение Нернста для расчета ЭДС гальванического элемента. 3. Классификация гальванических элементов. 4. Элемент Вестона. 5. Определение ЭДС компенсационным методом.

Гальванический элемент – это устройство, в котором энергия химической реакции превращается в электрическую.

История гальванических элементов Луиджи Гальвани (итальянский физиолог, профессор медицины Болонского университета) • в 1786 году открыл явление возникновения электрического тока при контакте разных металлов. • Гальвани обнаружил, что лапка мертвой лягушки прикосновении к ней металлическим предметом сокращается. • Наблюдения были истолкованы первооткрывателем как проявление «животного электричества» . http: //commons. wikimedia. org/wiki/File: Luigi_Galvani, _oil-painting. jpg? uselang=ru

Алеcсандро Вольта (итальянский физик и химик) • проделал серию опытов и пришел к выводу, что причиной сокращения мышц служит не «животное электричество» , а наличие цепи из разных проводников в жидкости. • В подтверждение А. Вольта заменил лапку лягушки электрометром и повторил все действия. В 1800 году А. Вольта впервые публично заявляет о своих открытиях на заседании Лондонского королевского общества, что проводник второго класса (жидкий) находится в середине и соприкасается с двумя проводниками первого класса из двух различных металлов. . . Вследствие этого возникает электрический ток того или иного направления. • http: //wiki. iteach. ru/images/d/d 2/Volta. jpg

• Алессандро Вольта создал первую «батарейку» – ванну, наполненную раствором соли, с погруженными в нее медным и цинковым электродами, • а впоследствии – и знаменитый «вольтов столб» – батарею из медных и цинковых дисков с картонными прокладками, пропитанными раствором соли или кислоты. Извещение об открытии произвело сенсацию не только в научном мире. Наполеон пригласил Вольта в Париж, лично присутствовал на демонстрации опыта, осыпал наградами и почестями. http: //upload. wikimedia. org/wikipedia/commons/2/20/Вольтов_столб_—_схема. png? uselang=ru

http: //musee-ampere. univ-lyon 1. fr/pile. jpg

• *Вы и сами можете легко сделать батарейку, подобную первому элементу Вольта, из обычного лимона. • Для этого просто воткните в лимон два гвоздя или шурупа – один стальной, а другой медный (латунь или другие металлы тоже подойдут). Ток такого элемента весьма мал, но напряжение вы сможете легко обнаружить обычным вольтметром.

Петров В. В. профессор Медико-Хирургической Академии Санкт-Петербурга • В 1803 году создал самый мощный в мире вольтов столб, составленный из 4 200 медных и цинковых кругов и развивающий напряжение до 2 500 вольт. • С помощью этого прибора ему удалось открыть такое важное явление, как электрическая дуга, применяемая в электросварке. • В Российской армии стал применяться электрический запал пороха и взрывчатки

http: //dic. academic. ru/pictures/brokgauz_efron/b 15_008 -0. jpg
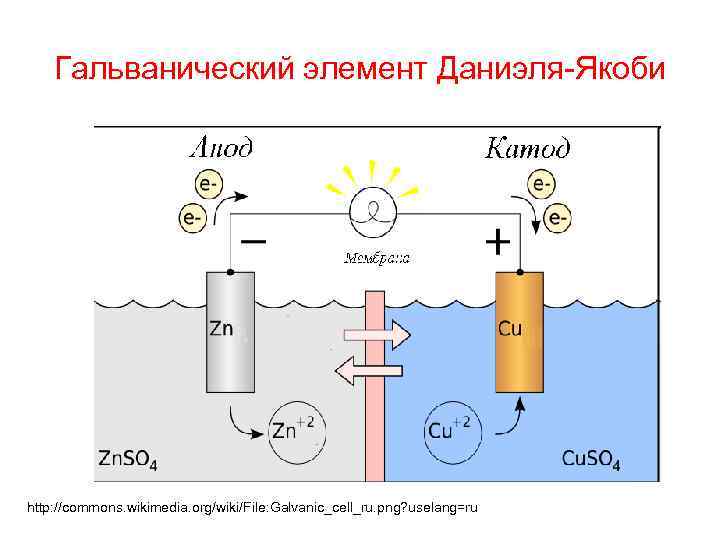
Гальванический элемент Даниэля-Якоби http: //commons. wikimedia. org/wiki/File: Galvanic_cell_ru. png? uselang=ru
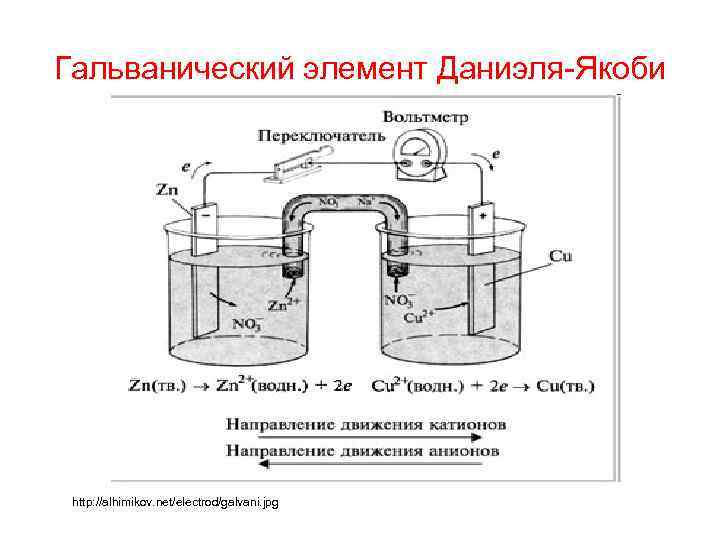
Гальванический элемент Даниэля-Якоби http: //alhimikov. net/electrod/galvani. jpg
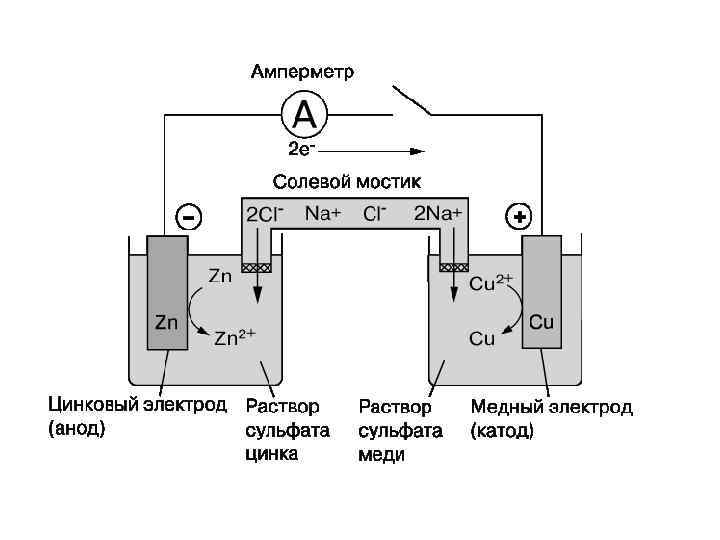
Гальванический элемент Даниэля-Якоби

• Гальванический элемент всегда записывают таким образом, чтобы • на левом электроде проходил процесс окисления, • а на правом — восстановление.

На аноде На катоде Анодом является элемент, имеющий меньший потенциал, а катодом – больший потенциал. Суммарный процесс:

Схема записи гальванического элемента

Диффузионный потенциал Скачок потенциала

Контактный потенциал

ЭДС гальванического элемента - разница электродных потенциалов (потенциал катода минус потенциал анода).

Уравнение Нернста для расчета ЭДС гальванического элемента (на примере элемента Даниэля-Якоби)

Пример расчета ЭДС

Реагенты, входящие в состав источника, расходуются в процессе его работы, и действие прекращается после расхода реагентов.

Классификация гальванических элементов I. По обратимости

1. Обратимые Условия: 1) обратимость химической реакции 2) равновесные условия работы элемента (то есть элемент должен давать бесконечно маленький ток. Для этого его ЭДС должна компенсироваться разницей потенциалов внешнего источника тока).

*Например, элемент Даниэля-Якоби. • Zn <=> Zn 2+ + 2 e окисление • Си 2+ + 2 е <=> Си восстановление 1. Если этот элемент замкнуть на внешний источник тока, ЭДС которого на бесконечно маленькую величину больше, чем ЭДС элемента Якоба-Даниэля, то в последнем будут проходить процессы, обратные тем, какие мы рассмотрели: на цинковом электроде будет выделяться цинк, а медный электрод будет растворяться. 2. Если же ЭДС внешнего элемента будет на бесконечно маленькую величину меньше, чем ЭДС элемента Якоба-Даниэля, то последний будет давать бесконечно маленький ток, то есть работать в равновесных (обратимых) условиях.

2. Необратимые Пример: элемент, в котором оба электрода погружены в раствор сульфата меди: Zn | Cu. SO 4 | Сu При приложении ЭДС, которая превышает ЭДС элемента, на левом электроде будет происходить выделение меди, а не цинка, то есть реакция, которая проходит в элементе, является необратимой.

II. По источнику энергии

1. Химический элемент Состоит из двух разных электродов. Источник электрической энергии химическая реакция, которая происходит в элементе. Например

2. Концентрационный ХЭ • Состоит из двух одинаковых электродов, погруженных в растворы с разными активностями • Источник электрической энергии - энергия переноса вещества из раствора с большей активностью в раствор с меньшей активностью.
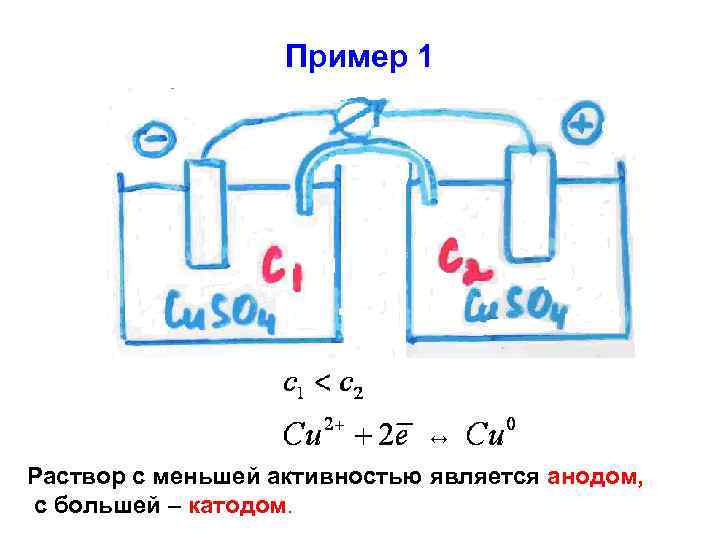
Пример 1 ↔ Раствор с меньшей активностью является анодом, с большей – катодом.

(продолжение)

Пример 2 Pt H 2 (р1) H+ H 2 (р2) Pt

III. По наличию непосредственного контакта между растворами

1. Цепь с переносом Электроды погружены в разные растворы, которые контактируют между собой, т. е. есть жидкостные границы. Примеры

2. Цепь без переноса Оба электрода погружены в один раствор, жидкостная граница отсутствует. Выравнивание активности потенциалопределяющих ионов идет за счет растворения на левом и выделения металла на правом электроде.
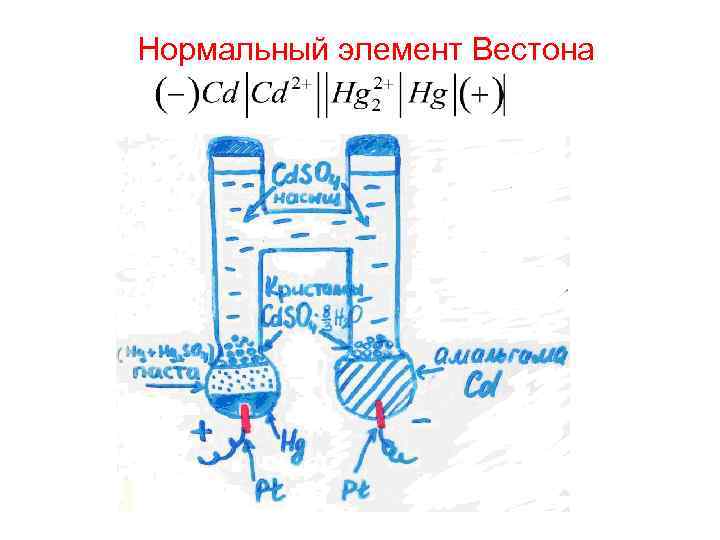
Нормальный элемент Вестона

При t=250 C Для других t 0, C:
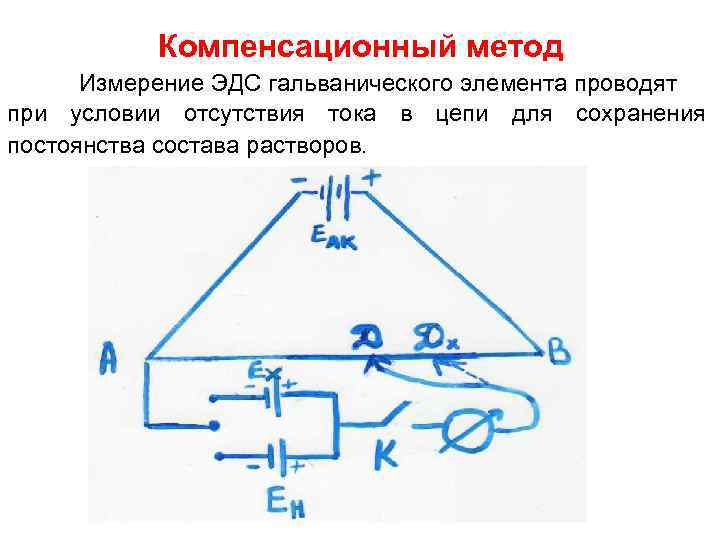
Компенсационный метод Измерение ЭДС гальванического элемента проводят при условии отсутствия тока в цепи для сохранения постоянства состава растворов.
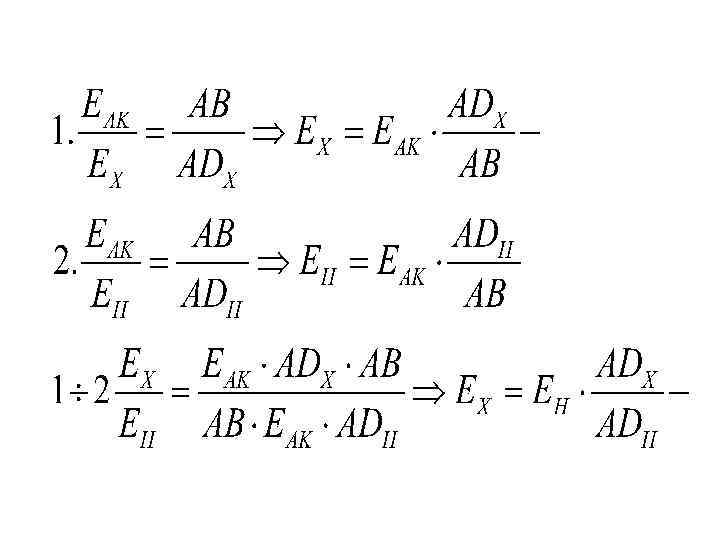

Сухие элементы не содержат раствора электролита. • Обычно именно их и называют словом «батарейка» . • Реакции, происходящие в них, необратимы, поэтому их нельзя перезарядить. Попытка зарядить батарейку может привести к порче батарейки и утечке щёлочи или других веществ, находящихся в батарейке. http: //diplomka. net/_pu/1/11627175. gif

Примеры Солевые элементы Лекланше (произвели настоящую революцию) • анод - цинковый электрод, • катод - электрод из смеси диоксида марганца с графитом (графит служит токоотводом). • Электролит - паста из раствора хлорида аммония с добавкой муки или крахмала в качестве загустителя. Мировое производство составляет больше 20 миллиардов штук в год, а их конструкция практически не изменилась за 120 лет с момента изобретения. http: //re. foto. radikal. ru/0709/05/e 57 a 57 f 67437. jpg

• Щелочные марганцево-цинковые элементы • Электролит - паста на основе гидроксида калия. • Преимущества: существенно большей ёмкостью, лучшей работой при низких температурах и при больших токах нагрузки. • Сейчас мировой спрос на эти элементы составляет больше 10 миллиардов штук в год. • Солевые и щелочные элементы широко применяются для питания радиоаппаратуры и различных электронных устройств.

Вторичные источники тока (аккумуляторы) • Реакции в них обратимы, поэтому они способны преобразовывать электрическую энергию в химическую, накапливая её (заряд), и выполнять обратное преобразование, отдавая электрическую энергию потребителю (разряд). Для распространённых аккумуляторов число циклов заряд-разряд обычно равно примерно 1000 и заметно зависит от условий эксплуатации. • • • Свинцовый (или кислотный). Электролит - 25 -30 % раствор серной кислоты. Электроды кислотного аккумулятора - свинцовые решетки, заполненные оксидом свинца, который при взаимодействии с электролитом превращается в Pb. SO 4. • • Щелочные аккумуляторы. Наибольшее применение получили никель-кадмиевые и никельметаллгидридные аккумуляторы, в которых электролитом служит KOH.

http: //commons. wikimedia. org/wiki/File: Ni. Cd_various. jpg? uselang=ru http: //fizika-solodova-em. narod. ru/7 a. gif http: //oldradio. onego. ru/IMAGES/TSIFR/batt_mal_b. jpg

Литий-полимерные и литий-ионные аккумуляторы широко используются в современной технике (мобильные телефоны, планшеты, ноутбуки). Характеризуются высокой ёмкостью и отсутствием эффекта памяти. http: //commons. wikimedia. org/wiki/File: Nokia_Battery. jpg? uselang=ru

Международный стандарт обозначений • • LR 20, LR 14, LR 6, LR 03, 6 F 22 описывается размер и форму батарейки, а также электрохимическую систему, на которой построен элемент. Буква "L", то перед вами щелочная батарейка, если "S" - то серебряно-цинковая, если "С" - то литиевая, если этой буквы нет - то солевая. " R" - обозначает цилиндрическую форму элемента, "F" - плоскую.

Электрохимические генераторы (топливные элементы) • - это элементы, в которых происходит превращение химической энергии в электрическую. Окислитель и восстановитель хранятся вне элемента, в процессе работы непрерывно и раздельно подаются к электродам. • В процессе работы топливного элемента электроды не расходуются. • Кислородно-водородный топливный элемент со щелочным электролитом • Восстановитель - водород (H 2), метанол (CH 3 OH), метан (CH 4) в жидком или газообразном состоянии. • Окислитель - кислород воздуха или чистый. • Энергоустановки применяются на космических кораблях, они обеспечивают энергией космический корабль и космонавтов.

О вреде использованных батареек

• Батарейки содержат различные тяжелые металлы, которые даже в небольших количествах могут причинить вред здоровью человека. Это цинк, марганец, кадмий, никель, ртуть и др. • После выбрасывания батарейки коррозируют (их металлическое покрытие разрушается), и тяжелые металлы попадают в почву и грунтовые воды. Из грунтовых вод эти металлы могут попасть в реки и озера или в артезианские воды, используемые для питьевого водоснабжения. Один из самых опасных металлов, ртуть, может попасть в организм человека как непосредственно из воды, так и при употреблении в пищу продуктов, приготовленных из отравленных растений или животных, поскольку этот металл имеет свойство накапливаться в тканях живых организмов. http: //900 igr. net/datai/fizika/Istochniki-elektricheskogo-toka/0010 -020 -Ustrojstvo-galvanicheskogo-elementa. jpg

• Одна пальчиковая батарейка, выброшенная в мусорное ведро, загрязняет тяжёлыми металлами около 20 квадратных метров земли, а в лесной зоне это территория обитания двух деревьев, двух кротов, одного ёжика и нескольких тысяч дождевых червей! • Каждая московская семья в год выбрасывает от 100 до 500 граммов и даже до килограмма использованных элементов питания. Суммарно в столице за год набирается около 2 -3 тысяч тонн батареек. http: //commons. wikimedia. org/wiki/File: Electric_batteries. jpg? uselang=ru


• Батарейки нужно перерабатывать на специальных заводах. • Проблема в том, что переработка стоит дороже, чем последующая продажа полученного сырья. • В Европе этим занимаются, и пункты приёма отработанных батареек встречаются на каждом шагу (можно, в общем, к ним везти. . ). Так собирает батарейки муниципалитет Лондона

Если пока нет контейнеров для сбора в России • В первую очередь, переходите, по возможности, на аккумуляторы – их выкидывать приходится гораздо реже. • Копить батарейки и ждать лучших времён, когда появятся пункты приёма… • Сдавать отработавшие аккумуляторы в редкие (но всё же существующие) пункты приёма для последующего захоронения. • Сейчас периодически проводятся акции, в ходе которых активисты собирают у населения батарейки, после чего сами сдают их.

Список литературы • 1. Физическая и коллоидная химия: Учебник/Под ред. Проф. А. П. Беляева. - М. : ГЭОТАР-Медиа, 2008. -704 с. • 2. Физическая химия. В 2 кн. Кн. 1/Под ред. К. С. Краснова - М: Высшая школа, 2001. -512 с.

Гальванический элемент.ppt